아산화질소
Nitrous oxide
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 | |
| 기타 이름 웃음가스, 달콤한 공기, 질소의 프로산화물, 저산화질소, 산화수소, 일산화수소 | |
| 식별자 | |
3D 모델(JSmol) | |
| 8137358 | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| ECHA 정보 카드 | 100.030.017 |
| E번호 | E942(광택제 등) |
| 2153410 | |
| 케그 | |
PubChem CID | |
| RTECS 번호 |
|
| 유니 | |
| UN 번호 | 1070(압축) 2201 (표준) |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 아니요 2 | |
| 몰 질량 | 44.013 g/g |
| 외모 | 무색 가스 |
| 밀도 | 1.977g/L(가스) |
| 녹는점 | -90.86°C(-131.55°F, 182.29K) |
| 비등점 | -88.48°C(-127.26°F, 184.67K) |
| 1.5g/L(15°C) | |
| 용해성 | 알코올, 에테르, 황산에 녹는 |
| 로그 P | 0.35 |
| 증기압 | 5150kPa(20°C) |
자화율(δ) | - 18.9 · 10−6 cm3 / 세로 |
굴절률(nD) | 1.000516(0°C, 101,325kPa) |
| 점성 | 14.90μPa/s[3] |
| 구조. | |
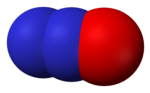
| 선형, C∞v | |
| 0.166 D | |
| 열화학 | |
표준 어금니 엔트로피 (S | 219.96 J/(K·mol) |
표준 엔탈피/ 형성 (δHf⦵298) | +82.05 kJ/mol |
| 약리학 | |
| N01AX13(WHO) | |
| 흡입 | |
| 약동학: | |
| 0.004% | |
| 5분 | |
| 호흡기 | |
| 위험 요소 | |
| GHS 라벨링: | |
   | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 안전 데이터 시트(SDS) | Ilo.org, ICSC 0067 |
| 관련 화합물 | |
| 산화질소 삼산화수소 이산화질소 사산화수소 오산화이질소 | |
관련 화합물 | 질산 암모늄 아지데 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
아산화질소(산화수소 또는 일산화수소)는 일반적으로 웃음 가스, 아질소 또는 [4]nos로 알려진 화학식 NO의
2 질소 산화물이다.상온에서 무색 불연성 가스이며, 약간 달콤한 향과 [5]맛이 납니다.높은 온도에서 아산화질소는 분자 산소와 유사한 강력한 산화제이다.
아산화질소는 마취 및 통증 감소 효과를 위해 특히 외과 및 [6]치과에서 상당한 의학적 용도를 가지고 있습니다.Humphry Davy가 만든 "웃음 가스"라는 속칭은 흡입 시 행복감을 느끼는 효과에서 유래했으며, 이는 해리성 마취제로 [6]레크리에이션을 이용하게 만들었다.그것은 세계보건기구의 필수 [7]의약품 목록에 있다.또한 로켓 추진제와 모터 경주에서 엔진의 출력을 높이기 위해 산화제로 사용됩니다.
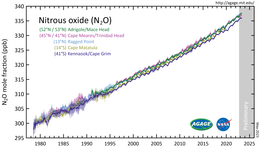
아산화질소의 대기 중 농도는 [8][9]2020년에 333ppb(ppb)에 도달하여 연간 약 1ppb의 속도로 증가하고 있다.그것은 성층권 오존의 주요 소거제이며, [10]CFC와 비슷한 영향을 미친다.2016년 말까지 10년간 NO 발생원 및 흡수원의 글로벌
2 회계에 따르면 연간 평균 배출량 17TgN/r(질소의 테라그램)의 약 40%가 인간 활동에서 비롯되었으며, 배출량 증가는 주로 신흥 [11][12]경제국 내 농업 및 산업 발생원의 확대에서 비롯되었다.세 번째로 중요한 장기수명 온실가스인 아산화질소는 [13][14]지구 온난화의 원인이 되기도 한다.
사용하다
로켓 모터
산화질소는 로켓 모터의 산화제로 사용해도 좋다.독성이 훨씬 적고, 상온에서의 안정성 때문에 보관도 쉽고 비행 시 비교적 안전하다는 점에서 다른 산화제에 비해 장점이 있습니다.부차적인 이점으로는 호흡 공기를 형성하기 위해 쉽게 분해될 수 있다.높은 밀도와 낮은 저장 압력(저온에서 유지되는 경우)으로 인해 저장된 고압 가스 [15]시스템과 높은 경쟁력을 갖출 수 있습니다.
1914년 미국 로켓의 선구자 로버트 고다드는 액체 연료 [16]로켓의 가능한 추진제로 아산화질소와 휘발유를 제안했다.아산화질소는 여러 하이브리드 로켓 설계에서 선택된 산화제입니다(액체 또는 기체 산화제와 고체 연료 사용).아산화질소와 수산기 종단 폴리부타디엔 연료의 조합은 SpaceShipOne 및 기타에 의해 사용되어 왔습니다.다양한 플라스틱을 연료로 하는 아마추어 로켓이나 고출력 로켓에도 사용되고 있습니다.
아산화질소는 모노로퍼제 로켓에도 사용될 수 있다.가열된 촉매가 존재할 경우 NO는
2 약 1,070°F(577°C)[17]의 온도에서 발열적으로 질소와 산소로 분해됩니다.열 방출이 크기 때문에 열 자기 분해가 우세해짐에 따라 촉매 작용이 빠르게 2차적으로 됩니다.진공 추진기에서, 이것은 180초나 되는 모노로플란트 고유 임펄스(Isp)를 제공할 수 있다.히드라진 추진기(사산화수소인 모노로프런트 또는 2프로프런트)에서 사용 가능한 I보다sp 현저히 적지만, 독성의 감소는 아산화질소를 조사할 가치가 있는 선택사항이 된다.
아산화질소는 309psi(21기압)[18]의 압력에서 약 600°C(1,112°F)에서 분쇄된다고 합니다.예를 들어, 600에서 필요한 점화 에너지는 6줄에 불과하지만
2, 130psi에서 NO는 2,500줄 점화 에너지 입력으로 [19][20]충분하지 않습니다.
내연기관
차량 경주에서 아산화질소(종종 "질소"라고 함)는 연소 중에 더 많은 산소를 공급하여 엔진이 더 많은 연료를 연소할 수 있도록 합니다.산소가 증가하면 연료 분사가 증가하여 엔진이 더 많은 엔진 출력을 낼 수 있습니다.이 가스는 저압/저온에서는 인화성이 없지만 화씨 약 570도(~300C)의 고온에서 분해되어 대기보다 더 많은 산소를 공급한다.그러므로, 그것은 종종 탈기가 더 쉬운 다른 연료와 섞인다.아산화질소는 강한 산화제로 과산화수소와 거의 동등하며 산소 가스보다 훨씬 강합니다.
아산화질소는 압축 액체로 저장됩니다. 흡기 매니폴드의 액체 아산화질소의 증발 및 팽창으로 인해 흡기 전하 온도가 크게 저하되어 더 많은 공기/연료 혼합물이 실린더로 유입됩니다.때로는 아산화질소가 흡기 매니폴드에(또는 그 전에) 주입되는 반면, 다른 시스템은 실린더(직접 포트 주입) 직전에 직접 주입되어 출력을 증가시킵니다.
이 기술은 제2차 세계대전 당시 GM-1 시스템을 탑재한 루프트바페 항공기에 의해 항공기 엔진의 출력을 높이기 위해 사용되었다.원래 Luftwaffe 표준 항공기에 우수한 고고도 성능을 제공하기 위한 것이었으나 기술적 고려로 인해 사용이 극도로 높은 고도로 제한되었다.따라서, 그것은 고고도 정찰기, 고속 폭격기, 고고도 요격기와 같은 전문 비행기에서만 사용되었다.그것은 때때로 또 다른 엔진 부스트 시스템인 MW 50을 장착한 Luftwaffe 항공기에서 발견될 수 있다. MW 50은 부스트 능력을 위해 메탄올을 사용한 항공 엔진의 물 주입 형태이다.
왕복 엔진에 아산화질소를 사용할 때 발생하는 주요 문제 중 하나는 엔진을 손상시키거나 파괴할 수 있는 충분한 출력을 생산할 수 있다는 것입니다.매우 큰 출력 증가가 가능하며, 엔진의 기계적 구조가 적절히 보강되지 않으면 이러한 작동 중에 엔진이 심각하게 손상되거나 파괴될 수 있습니다.가솔린 엔진의 아산화질소 증가에서는 "사전 점화"[21] 또는 "분리"("노크")를 방지하기 위해 적절한 작동 온도와 연료 레벨을 유지하는 것이 매우 중요합니다.아산화질소와 관련된 대부분의 문제는 전력 증가로 인한 기계적 결함에서 비롯된 것이 아닙니다.아산화질소는 실린더에 훨씬 더 밀도가 높은 전하를 허용하기 때문에 실린더 압력을 극적으로 증가시킵니다.압력 및 온도가 높아지면 피스톤 또는 밸브가 녹는 등의 문제가 발생할 수 있습니다.또한 피스톤 또는 헤드에 균열이 발생하거나 휘어지며 가열이 고르지 않아 사전 점화가 발생할 수 있습니다.
자동차용 액체 아산화질소는 의료용 아산화질소와 약간 다르다.소량의 이산화황(SO
2)을 첨가하여 약물 [22]남용을 방지한다.염기(예: 수산화나트륨)를 여러 번 세척하면 이를 제거할 수 있으며, 연소 중에 SO가 황산으로 추가로 산화되어
2 배출물이 [citation needed]더 깨끗해 질 때 관찰되는 부식 특성을 줄일 수 있습니다.
에어로졸 추진제
가스는 식품 첨가물(E 번호: E942)로, 특히 에어로졸 스프레이 추진제로 사용하도록 승인되었습니다.이러한 맥락에서 이것의 가장 일반적인 용도는 에어로졸 생크림 통과 조리용 스프레이입니다.
그 가스는 지방 화합물에 매우 잘 녹는다.에어로졸 생크림은 캔에서 나올 때까지 지방 크림에 녹여 기체가 되어 거품이 생긴다.이렇게 사용하면 액체의 4배 부피인 생크림을 만들 수 있는데 반해 크림에 공기를 넣어 휘저으면 2배 부피밖에 나지 않습니다.공기가 추진제로 사용되면 산소는 유지방의 석회화를 가속화하지만 아산화질소는 이러한 분해를 억제한다.탄산가스는 물에 산성이기 때문에 생크림에 사용할 수 없으며, 이는 크림을 응고시키고 셀저처럼 "반짝"하는 느낌을 줄 것이다.
하지만 아산화질소로 만든 생크림은 불안정해 30분에서 1시간 [23]안에 액체 상태로 돌아간다.따라서 바로 나오지 않는 음식을 꾸미는 방법은 적합하지 않다.
2016년 12월 동안 일부 제조업체는 8월 하순 플로리다의 에어 리퀴드 아산화질소 시설에서 발생한 폭발로 인해 미국에서 에어로졸 생크림이 부족하다고 보고했습니다.주요 시설이 오프라인인 상황에서, 이 회사는 부족 사태를 야기했고, 이로 인해 아산화질소의 공급을 식품 제조가 아닌 의료 고객으로 전환했습니다.통조림 생크림 사용이 보통 [24]최고조에 달하는 크리스마스와 휴가철에 이러한 부족 현상이 발생했다.
마찬가지로 레시틴(유화제)과 혼합된 다양한 종류의 기름으로 만들어진 쿠킹 스프레이는 아산화질소를 추진제로 사용할 수 있다.조리용 스프레이에 사용되는 다른 추진제로는 식품용 알코올과 프로판이 있습니다.
약
아산화질소는 [25]1844년부터 치과와 외과에서 마취제와 진통제로 사용되어 왔다.초기에는 고무 [26]천으로 만든 호흡 주머니로 구성된 간단한 흡입기를 통해 가스를 주입했다.오늘날, 가스는 마취 기화기와 의료용 인공호흡기를 통해 병원에서 투여되며, 2:1의 비율로 아산화질소를 정확히 투여하고 호흡에 영향을 미치는 흐름을 제공합니다.
아산화질소는 약한 일반 마취제이므로 일반적으로 일반 마취에서만 사용되는 것이 아니라 세보플루란이나 데스플루란과 같은 보다 강력한 일반 마취제의 운반 가스(산소와 혼합)로 사용됩니다.최소 폐포 농도는 105%이고 혈액/가스 분할 계수는 0.46이다.그러나 마취 시 아산화질소를 사용하면 수술 후 메스꺼움과 [27][28][29]구토의 위험이 증가할 수 있습니다.
치과의사들은 환자가 의식이 있을 때 흡입할
2 수 있는 NO/O
2 혼합물만 전달하는 더 단순한 기계를 사용한다.환자는 시술 내내 의식이 유지되고 [30]치과의사의 질문과 지시에 응답할 수 있는 충분한 정신 능력을 보유합니다.
아산화질소 흡입은 출산, 외상, 구강 수술 및 급성 관상동맥 증후군(심장 마비를 포함)과 관련된 통증을 완화하기 위해 자주 사용됩니다.분만 중에 사용하는 것은 출산 [31]여성들에게 안전하고 효과적인 원조인 것으로 나타났다.급성 관상동맥증후군에 대한 그것의 사용은 알려지지 않은 [32]이점이다.
영국과 캐나다에서 Entonox와 Nitronox는 구급대원(등록되지 않은 의사 포함)에 의해 빠르고 효과적인 진통 가스로 일반적으로 사용됩니다.
50% 아산화질소를 진통제로 투여하는 것이 상대적으로 쉽고 안전하다는 점을 고려할 때, 50% 아산화질소는 병원 전 환경에서 훈련을 받은 비전문 응급처치자가 사용할 수 있습니다.그 효과의 빠른 가역성은 [33]또한 진단을 막는 것을 방해할 것이다.
레크리에이션용


행복감 및/또는 약간의 환각을 일으키기 위한 목적으로 아산화질소의 오락적 흡입은 1799년 "웃는 가스 파티"[34]로 알려진 영국 상류층을 위한 현상으로 시작되었다.
19세기부터, 가스의 의료 및 요리 목적의 광범위한 가용성으로 인해 레크리에이션 사용이 전 세계로 크게 확대되었다.영국에서는 2014년 현재 거의 50만 명의 젊은이들이 나이트 스팟, 축제,[35] 파티에서 아산화질소를 사용하는 것으로 추정되고 있다.그 사용의 합법성은 나라마다, 심지어 일부 국가에서는 도시마다 크게 다르다.
그 약의 영국에 대한 광범위한 오락적 사용 그 웃음은 가스 블랙 시장에 언론인 매트 시어와 질소 산화물 통들 쉽게 온라인으로 가능하게 하는 것이지만, 병원 절도 사건일 것으로 예상된다는 hospitals,[36]에서 그것을 훔친 마약 거래자들을 만났다 안에는 2017년 부사장 다큐멘터리에 출연했었다.내선레어리 레어
런던 언론에 인용된 중요한 이슈는 아산화질소 캐니스터 쓰레기 처리의 영향이다. 이는 눈에 잘 띄고 [37]지역사회로부터 상당한 불만을 야기한다.
안전.
아산화질소의 주요 안전 위험은 아산화질소가 압축 액화가스, 질식 위험 및 해리성 마취제라는 사실에서 비롯된다.
아산화질소는 비교적 독성이 없지만, 숨을 들이마시거나 액체와 피부 또는 눈이 접촉하는 등 인간의 건강에 여러 가지 알려진 악영향을 미칩니다.
아산화질소는 외과의사, 치과의사, 간호사에게 중요한 직업상 위험요소이다.아산화질소는 인체에서 최소한으로 대사되기 때문에(0.004%의 비율로) 환자가 실내로 숨을 내쉴 때 효력을 유지하며, 실내 환기가 제대로 되지 않을 경우 의료진에게 음주 및 장기 노출 위험을 초래할 수 있습니다.아산화질소가 투여될 경우 폐가스 축적을 방지하기 위해 연속 흐름 외기 환기 시스템 또는
2 NO 스캐빈저 시스템이 사용됩니다.
국립산업안전보건원은 의료,[38] 치과 및 수의사들에게 마취 가스를 투여하는 동안 아산화질소에 대한 근로자들의 노출을 통제해야 한다고 권고한다.마취제를 [39]사용하지 않도록 권장 노출 한계(REL)를 25ppm(46mg/m3)로 설정했습니다.
정신적 및 육체적 장애
아산화질소에 노출되면 정신 능력, 시청각 능력 및 [40]손재주가 단기적으로 저하됩니다.이러한 영향은 유발된 공간적 및 시간적 방향 감각 상실과 결합되어 환경적 [41]위험으로부터 사용자에게 물리적 피해를 초래할 수 있다.
신경독성과 신경보호
다른 NMDA 수용체 길항제들과 마찬가지로, NO는 오랜 시간(수시간) 노출 시 [42][43][44][45]설치류에서 올니 병변의 형태로 신경독성을 발생시킨다고
2 제안되어 왔다.그러나 올니의 병변은 사람에게 발생하지 않으며 케타민과 같은 유사한 약물은 현재 급성 신경 [46][47]독성이 없는 것으로 여겨지고 있다.정상적인 상황에서는 NO가 빠르게 몸에서 배출되기 때문에
2 다른 NMDAR [48]길항제보다 신경독성이 낮다는 주장이 있다.실제로 설치류에서, 단기 피폭은 빠르게 회복 가능한 가벼운 부상만을 초래하고, 신경계 사망은 지속적이고 지속적인 [42]피폭 후에만 발생한다.또한 아산화질소는 저산소증으로 인해 장기간 노출되면 신경독성을 일으킬 수 있다.산소가 크림을 [50]썩게 만들기 때문에 산소를 포함하지 않는 생크림 충전기(휘펫 또는 "낭"[49]이라고도 함)와 같은 비의학적 제제의 경우 특히 그렇습니다.
중량(400g 이상 또는 200L 이하)독극물 통제 센터에 보고된 가스 없음) 또는 빈번한 사용자(예: 매일 또는 매주)의2 경우, 말초 신경 장애의 징후가 확인되었다. 즉, 운동실조증(게이트 이상) 또는 가장 예민한 감각(예: 따끔거림, 저림, 따끔거림, 따끔거림, 따끔거림)이 대부분이다.이것들은 신경학적 손상의 초기 신호로 간주되며 만성적인 [51]독성을 나타낸다.
또한 아산화질소는 비타민12 B의 양을 감소시킨다.이것은 사용자가 비타민12 B [52]결핍을 가지고 있는 경우 심각한 신경 독성을 일으킬 수 있습니다.
아산화질소는 부피 기준 75%로 설치류에서 중뇌동맥의 폐색에 의해 유발되는 허혈에 [48]의한 신경사멸을 감소시키고 신경세포배양에서의 NMDA에 의한2+ Ca 유입을 감소시켜 흥분독성에 관여하는 중요한 사건이다.
DNA손상
주변 아산화질소에 대한 직업적 노출은 DNA [53]합성의 중단으로 인한 DNA 손상과 관련이 있다.이 상관관계는 용량에[54][55] 의존하며 일상적인 오락적 사용으로 확대되는 것으로 보이지 않는다. 그러나 손상을 일으키는 데 필요한 노출의 지속 시간과 양을 확인하기 위해 추가 연구가 필요하다.
산소 부족
산소를 섞지 않고 순수한 아산화질소를 흡입하면 결국 산소부족으로 이어져 혈압 저하, 실신, 심장마비까지 일으킬 수 있다.가스통에 연결된 스트랩 온 마스크처럼 사용자가 지속적으로 많은 양을 흡입할 경우 이러한 현상이 발생할 수 있습니다.또한 사용자가 과도한 호흡 억제를 하거나 신선한 [56]공기 공급을 차단하는 다른 흡입 시스템을 사용하는 경우에도 발생할 수 있습니다.또 다른 위험은 가스 용기에서 직접 가스를 흡입할 경우 입술, 후두, 기관지에 동상 증상이 나타날 수 있다는 것이다.따라서 아산화질소는 콘돔이나 [57]풍선에서 흡입되는 경우가 많다.
비타민12 B 결핍증
아산화질소에 장기간 노출되면 비타민12 B가 결핍될 수 있다.그것은 산화에 의해 비타민12 B의 코발라민 형태를 불활성화시킨다.감각신경병증, 골수병증, 뇌병증을 포함한 비타민12 B 결핍 증상은 잠재의식 비타민12 B 결핍증 환자에게서 아산화질소 마취에 노출된 후 수일 또는 수주 내에 발생할 수 있다.
증상은 비타민12 B를 다량 섭취하면 치료되지만 회복이 더디고 [58]불완전할 수 있다.
비타민 B 수치가12 정상인 사람들은 노출이 반복되고 장기화되지 않는 한 아산화질소의 영향을 대수롭지 않게 만들기 위한 저장고가 있다.비타민12 B의 수치는 [59]아산화질소 마취를12 하기 전에 비타민 B 결핍의 위험 인자를 가진 사람들에게서 확인되어야 한다.
태아 발달
쥐를 대상으로 한 여러 실험 연구에 따르면 임신한 암컷이 아산화질소에 만성적으로 노출되면 발육 중인 [60][61][62]태아에게 악영향을 미칠 수 있다.
화학적/물리적 위험
실온(20°C[68°F])에서 포화 증기 압력은 50.525bar이며 임계 온도인 36.4°C(97.5°F)에서 72.45bar까지 상승합니다.따라서 압력 곡선은 [63]온도에 비정상적으로 민감합니다.
많은 강력한 산화제와 마찬가지로, 연료에 의한 부품의 오염은 "물 망치"와 같은 효과로 인해 소량의 아질소/연료 혼합물이 폭발하는 로켓 사고와 관련이 있습니다("디젤링"이라고도 합니다. 가스의 단열 압축으로 인한 가열은 분해 [64]온도에 도달할 수 있습니다.스테인리스강 및 알루미늄과 같은 일부 일반적인 건축 자재는 단열 [65]압축으로 인해 발화할 수 있는 오염 물질이 있기 때문에 아산화질소와 같은 강력한 산화제를 사용하는 연료로 작용할 수 있습니다.
배관에서의 아산화질소 분해가 대형 [18]탱크의 폭발로 이어진 사건도 있었다.
작용 메커니즘
의학에서 NO 작용의
2 약리학적 메커니즘은 완전히 알려져 있지 않다.그러나 광범위한 리간드 게이트 이온 채널을 직접 변조하는 것으로 나타났으며, 이는 많은 효과에서 중요한 역할을 할 수 있다.NMDAR 및 β-서브유닛2 함유 nACH 채널을 적당히 차단하고, AMPA, 카이네이트, GABAC 및3 5-HT 수용체를 약하게 억제하며, GABAA [66][67]및 글리신 수용체를 약간 강화한다.또한 2개의 포어 도메인K+
[68]채널을 활성화 하는 것으로 나타났습니다.NO는 꽤 많은 이온 채널에 영향을 미치지만
2, 마취, 환각 및 행복 효과는 NMDA 수용체 매개 전류 [66][69]억제를 통해 주로 또는 완전히 발생할 수 있다.이온 채널에 대한 영향 외에도 NO는
2 중추신경계의 일산화질소(NO)를 모방하는 작용을 할 수 있으며, 이는 진통제 및 [69]항불안제 특성과 관련이 있을 수 있다.아산화질소는 질소보다 30배에서 40배 더 용해된다.
아산화질소의 미각 이하 선량을 흡입하는 효과는 환경과 [70][71]개인차를 포함한 여러 요인에 따라 달라지는 것으로 알려져 왔다. 그러나 Jay([41]2008)는 그의 논의를 통해 아산화질소가 다음과 같은 상태와 감각을 유도하는 것으로 확실하게 알려져 있음을 시사한다.
- ★★★
- 상실
- 방향감퇴치
- 의 감도
또한 소수의 사용자는 통제되지 않는 발성과 근육 경련을 경험하게 됩니다.이러한 효과는 일반적으로 아산화질소 [41]발생원을 제거한 후 몇 분 후에 사라집니다.
랫드에서 NO는
2 도파민 방출을 유도하고 복부 피개 영역과 핵에서 도파민 작동성 뉴런을 활성화함으로써 중림비 보상 경로를 자극하며,[72][73][74][75] 아마도 시스템에 국재화된 NMDA 수용체의 길항작용을 통해 활성화된다.이 작용은 그것의 행복 효과와 관련이 있으며, 특히 그것의 진통 특성을 [72][73][74][75]증가시키는 것으로 보인다.
그러나 마우스에서 NO는
2 암페타민 유도 운반체 매개 도파민 방출을 핵암페타민 및 행동감작증에서 차단하고 코카인과 모르핀의 조건부 장소선호(CPP)를 폐지하며 그 [76][77]자체로 강화(또는 혐오) 효과를 발생시키지 않는다는 점은 주목할 만하다.랫드에서 NO의
2 CPP의 효과는 강화, 혐오, 변화 [78]없음으로 구성되어 있다.반면 [79]다람쥐원숭이에게는 양성강화제이며 [80]인간에게는 학대약으로 잘 알려져 있다.NO에 대한
2 이러한 불일치는 종의 변화나 방법론적 [77]차이를 반영할 수 있다.인간 임상 연구에서 NO는
2 높은 주관적 개인 [81][82]변동을 반영하여 쥐와 유사하게 혼합 반응을 생성하는 것으로 확인되었다.
불안행동시험에서 NO의
2 저용량은 효과적인 항불안제이며, 이러한 항불안 효과는 벤조디아제핀 수용체 길항제들에 의해 부분적으로 역전되기 때문에 GABAA 수용체의 활성 증대와 관련이 있다.이를 반영하듯, 벤조디아제핀의 항불안제 효과에 대한 내성이 발달한 동물은 [83]NO에 부분적으로
2 내성이 있다.실제로, 30
2% NO가 주어진 인간의 경우, 벤조디아제핀 수용체 길항제들은 [84]인간 임상 연구에서 "높다"고 느끼는 주관적인 보고를 감소시켰지만 정신 운동 성능을 변화시키지는 않았다.
NO의
2 진통 효과는 내인성 오피오이드 시스템과 하강성 노르아드레날린 시스템 사이의 상호작용과 관련이 있다.동물들에게 만성적으로 모르핀을 투여할 때, 그들은 그것의 진통 효과에 대한 내성을 발달시키고,[85] 이것은 또한 동물들을 NO의
2 진통 효과에 내성을 갖게 한다.행정과( 아니β-endorphin)또한 아산화 질소의antinociceptive 효과 블록 일부 내인성 opioids의 활동을 결합하는 항체의.는 내인성 opioids의 고장을 억제하는[86]마약은 또한 아산화 질소의antinociceptive 효과 potentiate.[86]몇몇 실험이 opioid 수용체 길항제 직접 침실에 지원을 보여 주었다.NO의
2 항노출 효과를 차단하지만 척수에 주사해도 효과가 없다.
간접 작용과는 별도로, 모르핀과 같은 아산화질소는 오피오이드 수용체 결합 [88][89]부위에서 결합함으로써 내인성 오피오이드 시스템과 직접 상호작용한다.
반대로 α-아드레노셉터2 길항제들은 척수에 직접 투여할 때는 NO의 통증
2 완화 효과를 차단하지만 [90]뇌에 직접 투여할 때는 그렇지 않다.실제로 노르에피네프린이 고갈된 α-아드레노셉터2B 녹아웃 마우스 또는 동물은 [91]NO의
2 항침습 효과에 거의 완전히 저항한다. 명백히 NO 유도성
2 오피오이드의 방출은 노르에피네프린을 척수로 방출하고 통증 신호를 [92]억제하는 뇌간 노르아드레날린 신경세포의 억제를 일으킨다.정확히 어떻게 NO가 내인성 오피오이드 펩타이드의 방출을 야기하는지는
2 여전히 불확실하다.
및
아산화질소는 희미하고 달콤한 냄새를 가진 무색 무독성 가스입니다.
아산화질소는 쌍극결합산소라디칼을 방출함으로써 연소를 지지하기 때문에 빛나는 부목을 재점화할 수 있다.
NO는
2 상온에서 불활성이며 반응이 거의 없습니다.온도가 올라가면 반응성이 높아집니다.예를 들어, 아산화질소는 460K(187°C)에서 NaNH와
2 반응하여 다음과 같은 NaN을 얻는다
3.
- 2
2 NaNH + NO
2 → NaN
3 + NaOH + NH
3
상기의 반응은 상업화학업계가 [93]기폭제로 사용하는 아지드화염을 생산하기 위해 채택한 방법이다.
★★★
이 가스는 영국의 자연철학자이자 화학자인 조셉 프리스틀리에 의해 1772년에 처음 합성되었는데, 그는 이것을 탈황성 아질소 [94]공기 또는 인화성 아질소 [95]공기라고 불렀다.프리스틀리는 자신의 [96]발견을 질산에 적신 철필링을 가열하여 "질소의 공기 감소"를 만드는 방법을 설명한 다양한 종류의 공기에 대한 실험과 관찰 (1775년)에서 발표했다.
★★★★★
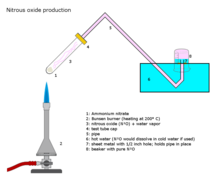
아산화질소의 첫 번째 중요한 사용은 토마스 베도스와 제임스 와트에 의해 가능해졌는데, 그는 의학적인 사용과 사실적인 공기 생산 (1794년)에 관한 책을 출판하기 위해 함께 일했다.이 책은 두 가지 이유로 중요했다.첫째, 제임스 와트는 "사실상의 공기"를 생산하는 새로운 기계와 가스를 흡입하는 새로운 "호흡 장치"를 발명했다.둘째, 이 책은 또한 결핵과 다른 폐질환이 "Factious Airs"[25]의 흡입으로 치료될 수 있다는 토마스 베도스의 새로운 의학 이론을 제시했다.

"Factious Airs"를 생산하기 위한 기계는 필요한 물질을 태우는 용광로, 생성된 가스가 나선형 파이프에서 통과되는 물('불순물'을 위한 용기), 그리고 마지막으로 생성된 가스 "공기"를 휴대용 에어백에 넣을 수 있는 가스계가 있는 가스 실린더(기밀 기름으로 만든 si)의 세 부분으로 구성되었습니다.lk) 호흡장치는 튜브와 마우스피스를 연결하는 휴대용 에어백 중 하나로 구성되었다.이 새로운 장비가 1794년까지 개발되고 생산되면서, 1798년 토마스 베도스가 핫웰스(브리스톨)에 "의료 공기에 의한 공압 질병 구제 기관"을 설립하면서 임상 시험을 [clarification needed]위한 길이 열렸다.건물 지하에서는 대형 기계가 젊은 험프리 데이비의 감독 하에 가스를 생산하고 있었는데, 데이비는 환자들이 [25]숨을 들이마실 수 있는 새로운 가스를 실험하도록 격려받았다.데이비의 첫 번째 중요한 업적은 아산화질소에 대한 조사였고 그의 결과를 책에 발표했다.연구, 화학 및 철학 (1800).이 출판물에서 데이비는 465페이지의 아산화질소의 진통제 효과와 556페이지의 [97]수술에 사용될 가능성에 주목하고 있다.데이비는 [98]아산화질소를 뜻하는 "웃는 가스"라는 이름을 만들었다.
데이비가 아산화질소를 흡입하면 의식이 있는 사람의 통증을 완화시킬 수 있다는 것을 발견했음에도 불구하고, 의사들이 마취에 아산화질소를 사용하려고 시도하기 전까지 44년이 더 흘렀다.주로 영국 상류층을 위해 마련된 "웃는 가스 파티"에서 아산화질소를 레크리에이션 약물로 사용한 것은 1799년부터 즉시 성공적이었습니다.가스의 효과는 일반적으로 사용자를 멍하고, 몽환적이고, 진정된 것처럼 보이게 하지만, 어떤 사람들은 또한 행복감에 빠져 낄낄대며 [99]종종 웃음을 터뜨린다.
미국의 초기 상업 제작자 중 한 명은 시인 에드거 앨런 포의 사촌인 조지 포로,[100] 그는 또한 가스를 액화시킨 최초의 사람이었다.
아산화질소가 환자의 치료에 마취약으로 처음 사용된 것은 1844년 [101]12월 11일 가드너 퀸시 콜튼과 존 맨키 릭스의 도움을 받아 치과 의사 호레이스 웰스가 치아 적출 시 통증에 둔감함을 보였을 때였다.그 후 몇 주 동안 웰스는 코네티컷주 하트포드에서 처음 12~15명의 아산화질소 환자를 치료했고, 그의 기록에 따르면 두 [102]사례에서만 실패했다.웰스가 1844년 12월 보스턴의 의학 협회에 보고한 이러한 설득력 있는 결과에도 불구하고, 이 새로운 방법은 다른 치과 의사들에 의해 즉시 채택되지 않았다.그 이유는 웰스가 1845년 1월 보스턴에서 열린 의학부와의 첫 공개 시연에서 부분적으로 성공하지 못했기 때문에 그의 동료들은 그 효과와 [103]안전성에 대해 의문을 품게 되었다.이 방법은 가드너 퀸시 콜튼이 뉴헤이븐과 [25]뉴욕에 막 설립한 모든 "콜튼 치과 협회" 클리닉에서 성공적으로 사용하기 시작한 1863년이 되어서야 널리 쓰이게 되었다.이후 3년 동안 콜튼과 그의 동료들은 25,000명 이상의 [26]환자에게 아산화질소를 성공적으로 투여했다.오늘날 아산화질소는 치과에서 국소마취제의 보조제로 사용되고 있다.
그러나 아산화질소는 병원 환경에서 큰 수술에 사용할 만큼 강한 마취제로는 발견되지 않았다.대신, 더 강하고 강력한 마취제인 디에틸 에테르는 1846년 10월에 클로로포름과 함께 사용되도록 입증되고 승인되었다.[25]그러나 1876년 조지프 토마스 클로버가 가스 에테르 흡입기를 발명했을 때 병원에서 아산화질소의 가벼운 흐름으로 모든 마취처리를 시작한 후 더 강한 에테르나 클로로포름으로 점차 마취를 증가시키는 것이 일반적인 관행이 되었다.클로버의 가스-에테르 흡입기는 환자에게 아산화질소와 에테르를 동시에 공급하도록 설계되었으며, 정확한 혼합물은 장치의 조작자에 의해 제어되었다.그것은 [26]1930년대까지 많은 병원에서 사용되었다.오늘날 병원에서는 보다 발전된 마취기를 사용하지만, 이 기계들은 여전히 클로버의 가스 에테르 흡입기로 시작된 것과 같은 원리를 사용하여 아산화질소로 마취를 시작하고, 더 강력한 마취기를 투여합니다.
콜튼의 아산화질소 대중화로 인해 평판이 좋지 않은 돌팔이들이 콜튼을 채택하게 되었고, 그들은 콜튼을 소비, 스크로풀라, 카타르 및 혈액, 인후 및 폐의 다른 질병에 대한 치료제로 홍보했다.아산화질소 치료제는 보스턴의 C. L. Blood와 Jerome Harris, [104][105]시카고의 Charles E. Barney와 같은 사람들에 의해 특허 의약품으로 투여되고 허가되었습니다.
.
아산화질소를 제조하는 다양한 방법에 대한 검토가 [106]발표되었습니다.
방법
아산화질소는 아산화질소와 [107]수증기로 분해되는 질산암모늄을[106] 약 250℃에서 세심하게 가열하여 산업 규모로 제조된다.
- NHNO
4
3 → 2
2 HO + NO
2
다양한 인산염의 첨가는 약간 낮은 온도에서 순도 가스의 형성에 유리하다.이 반응은 통제하기 어려울 수 있으며 [108]폭발을 일으킬 수 있습니다.
질산암모늄의 분해는 또한 가스를 준비하는 일반적인 실험실 방법이다.마찬가지로 질산나트륨과 [109]황산암모늄의 혼합물을 가열하여 얻을 수 있다.
- 2 NaNO
3 + (NH
4)2SO
4 → NaSO
2
4 + 2 NO
2 + 4 HO
2
또 다른 방법으로는 요소, 질산 및 [110]황산의 반응을 들 수 있다.
- 22 (NH)2 CO + 2 HNO
3 + HSO
2
4 → 2 NO
2 + 2 CO
2 + (NH4)2SO4 + 2 H
2O
이산화망간-비스무트 산화물 촉매에 의한 암모니아 직접 산화가 [111]보고되었다: cf.오스트발트 과정.
- 2 NH
3 + 2 O
2 → NO
2 + 3 HO
2
염화히드록실암모늄은 아질산나트륨과 반응하여 아산화질소를 생성한다.하이드록실아민 용액에 아질산염을 첨가하면 남은 부산물은 소금물뿐이다.그러나 히드록실아민 용액이 아질산염 용액에 첨가되면(질산염이 초과) 유독성 고산화질소도 생성된다.
- NHOHCl
3 + NaNO
2 → NO
2 + NaCl + 2
2 HO
SnCl
2 및 HCl로 HNO를 처리하는 방법도
3 입증되었습니다.
- 2
3 HNO + 8 HCl + 4 SnCl
2 → 5
2 HO + 4 SnCl
4 + NO
2
하이포나이트산은 pH 1~[112]3에서 25°C에서 16일의 반감기를 가진 물과 NO로2 분해된다.
- HNO222→HO2 + NO2
아산화질소는 지구 대기의 작은 구성 요소이며 행성 질소 순환의 활성 부분입니다.전 세계 현장에서 채취한 공기 샘플을 분석한 결과 2017년 [8]농도는 330ppb를 넘어섰다.연간 약 1ppb의 성장률 또한 최근 수십 [9]년 동안 가속화되었다.아산화질소의 대기 중 풍부도는 1750년 [114]기준치 약 270ppb에서 20% 이상 증가했다.NO의 중요한
2 대기 특성은 다음 표에 요약되어 있다.
| ★★★ | 치 |
|---|---|
| 오존 파괴 가능성(ODP) | 0.17[115] (CCLF3 = 1) |
| 지구온난화 가능성(GWP: 100년) | 265[116] (CO2 = 1) |
| 121년[116] |
2020년 10월 과학자들은 전지구
2 NO 발생원과 흡수원의 포괄적인 정량화를 발표했다.그들은 지난 40년 동안 인간에 의한 배출이 30% 증가했으며, 대기 농도 증가의 주요 원인이라고 보고했습니다.최근의 성장은 가장 높은 예상 배출 시나리오를 [11][14]초과했다.
2010년 기준으로 매년 약 2,950만 톤(질소 1,880만 톤 포함)의 NO가
2 대기 중으로 유입되고 있으며, 이 중 64%는 자연이고 36%는 인간 [117][118]활동에 의한 것으로 추정된다.
대기로 배출되는 NO의
2 대부분은 자연적, 인위적 공급원으로부터 토양과 [119]해양의 박테리아와 곰팡이를 탈질하는 것과 같은 미생물에 의해 생성된다.자연 식생 하의 토양은 아산화질소의 중요한 공급원으로 자연 발생 배출량의 60%를 차지한다.다른 자연 발생원에는 해양(35%)과 대기 화학 반응(5%)[117]이 포함된다.
2019년 연구에 따르면 해빙 영구 동토층 배출량은 이전에 [120]가정한 것보다 12배나 높은 것으로 나타났다.
인위 개변의 배출량의 주요 구성 요소 농업 토양과 가축 비료(42%), 유출과 앞당겨의 침출(25%), 바이오매스를 태우(10%), 화석 연료 연소와 산업 과정(10%), 다른 nitrogen-containing 대기 배출의 생물 분해(9%)과 인간 하수(5%)fertilised 있다.[121][122][123][124][125]농업은 토양 재배, 질소 비료 사용, 동물의 배설물 [126]처리를 통해 아산화질소 생산을 증가시킨다.이러한 활동은 자연적으로 발생하는 박테리아를 자극하여 더 많은 아산화질소를 생산한다.토양에서 방출되는 아산화질소는 시간과 [127]공간에 따라 현저하게 달라지기 때문에 측정하기가 어려울 수 있으며, 1년 중 대부분은 "핫 모멘트"[128][129] 및/또는 "핫 스팟"[130]으로 알려진 유리한 위치에서 발생할 수 있다.
산업용 배출 중 아질산과 아디핀산의 생산은 아산화질소 배출의 가장 큰 원천이다.아디핀산 방출은 특히 [121][131][132]시클로헥사논의 질화로부터 유도되는 니트롤산 중간체의 분해에서 발생한다.
아산화질소를 생성하는 자연적 과정은 질화 및 탈질소로 분류될 수 있다.구체적으로는 다음과 같습니다.
- 호기성 자기영양 질화, 암모니아(NH
3)에서 아질산염(NO−
2) 및 질산염(NO−
3)으로의 단계적 산화 - 혐기성 헤테로 영양소 탈질, NO에서 NO로의−
3−
2 단계적 환원, 일산화질소(NO), NO
2 및 궁극적으로는
2 N(산소 부족
2 상태에서 통성 혐기성 세균이 유기물질의 호흡에서 NO를 전자수용체로 사용하는 경우−
3) - 자가영양성 NH산화세균과
3 암모니아(NH
3)가 아질산염(NO−
2)으로 산화되는 경로에 의해 이루어지는 질화탈질소(NO), 질소분자질소
2
2(N)로 환원된다−
2. - 한 영양 호기성
이러한 과정은 광물 질소와 유기물의 가용성, 산도와 토양 유형, 그리고 토양 온도와 수분 함량과 같은 기후 관련 요인에 의해 영향을 받습니다.
가스의 대기로의 방출은 세포 내에서의 소비와 아산화질소 [133]환원효소에 의해 촉매작용에 의해 크게 제한됩니다.
에 영향
아산화질소는 온실가스로서 상당한 지구 온난화 잠재력을 가지고 있다.분자당 기준으로 100년 동안 고려했을 때, 아산화질소는 이산화탄소
2([116]CO)의 265배에 달하는 대기 중 열 차단 능력을 가지고 있습니다.그러나 낮은 농도(CO의 1/1
2,000 미만)로 인해 온실효과의 기여도는 이산화탄소의 1/3 미만이며 수증기와 [134]메탄에도 미치지 못한다.한편 대기 중 NO의
2 38% 이상이 인간 [121]활동의 결과이기 때문에 아산화질소의 제어는 온실가스 [135]배출 억제 노력의 일환으로 여겨진다.
노벨상 수상자인 폴 크루첸의 2008년 연구에 따르면 농업용 질산 비료에 기인하는 아산화질소 방출량은 심각하게 과소평가되고 있으며, 그 대부분은 환경보호국 [136]데이터에서 토양 및 해양 방출량이 될 것으로 추정된다.
아산화질소는 농사를 지으면 농사를 통해 대기로 방출되며, 농부가 질소 비료를 밭에 첨가하면 동물성 비료의 분해를 통해 배출된다.미국에서 방출되는 모든 아산화질소의 약 79%가 질소 수정에서 나온다.아산화질소는 화석연료의 연소 부산물로도 방출되지만 방출되는 양은 사용된 연료에 따라 달라진다.질소 비료의 합성에 사용되는 질산의 제조를 통해서도 배출된다.나일론과 다른 합성 의류 섬유들의 전구물질인 아디핀산의 생산도 아산화질소를 방출한다.인간에서 유래한 아산화질소의 총량은 약 40%이다.[137]
아산화질소는 또한 오존층을 얇게 만드는 데 관여되어 왔다.2009년 연구에 따르면 오존을
2 파괴하는 가장 중요한 배출물은 NO 배출이며 21세기 [10][138]내내 가장 큰 배출량을 유지할 것으로 예상된다.
미국에서 아산화질소의 소유는 연방법에 따라 합법적이며 DEA의 [139]권한 대상이 아니다.그러나 이는 식품의약품화장품법에 따라 식품의약국에 의해 규제되고 있으며, 인간의 소비를 목적으로 한 아산화질소의 판매 또는 유통을 금지하는 "브랜드 잘못" 조항에 따라 기소될 수 있다.많은 주들이 아산화질소의 보유, 판매, 유통을 규제하는 법을 가지고 있다.그러한 법은 보통 미성년자에 대한 유통을 금지하거나 특별한 허가 [citation needed]없이 판매될 수 있는 아산화질소의 양을 제한한다.예를 들어 캘리포니아 주에서는 레크리에이션 사용을 위한 소지는 금지되어 있으며 [140]경범죄로 간주됩니다.
2015년 8월, 영국 런던 램베스구 의회는 레크리에이션 목적의 약물 사용을 금지하여 위반자는 현장에서 1,000파운드 [141]이하의 벌금을 내야 한다.
뉴질랜드 보건부는 아산화질소는 처방약이며 처방전 없이 판매하거나 소지하는 것은 의약품법 [142]위반이라고 경고했다.이 진술은 의료용 이외의 모든 아산화질소 사용을 금지할 것으로 보이지만, 이는 레크리에이션용만 합법적으로 대상으로 한다는 것을 암시한다.
인도의 경우, 의료용 마취용으로 가스를 사용하는 경우, 벌크 실린더에서 더 작고 운반하기 쉬운 1,590리터 용량의[143] E형 탱크로 아산화질소를 이전하는 것은 합법적이다.
「」도 .
- ^ "[Nitrous oxide]". Degruyter.com. Retrieved 24 July 2022.
- ^ IUPAC 무기화학 용어 2005. PDF.
- ^ Takahashi, Mitsuo; Shibasaki-Kitakawa, Naomi; Yokoyama, Chiaki; Takahashi, Shinji (1996). "Viscosity of Gaseous Nitrous Oxide from 298.15 K to 398.15 K at Pressures up to 25 MPa". Journal of Chemical & Engineering Data. 41 (6): 1495–1498. doi:10.1021/je960060d. ISSN 0021-9568.
- ^ Tarendash, Albert S. (2001). Let's review: chemistry, the physical setting (3rd ed.). Barron's Educational Series. p. 44. ISBN 978-0-7641-1664-3.
- ^ PubChem. "Nitrous oxide". pubchem.ncbi.nlm.nih.gov. Retrieved 29 March 2022.
- ^ a b Quax, Marcel L. J.; Van Der Steenhoven, Timothy J.; Bronkhorst, Martinus W. G. A.; Emmink, Benjamin L. (July 2020). "Frostbite injury: An unknown risk when using nitrous oxide as a party drug". Acta Chirurgica Belgica. Taylor & Francis on behalf of the Royal Belgian Society for Surgery. 120 (1–4): 140–143. doi:10.1080/00015458.2020.1782160. ISSN 0001-5458. PMID 32543291. S2CID 219702849.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
{{cite book}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ a b "Nitrous Oxide (N2O) Mole Fraction" (PDF). Massachusettes Institute of Technology. Retrieved 15 February 2021.
- ^ a b "Trends in Atmospheric Nitrous Oxide". National Oceanic and Atmospheric Administration / Earth System Research Laboratories. Retrieved 15 February 2021.
- ^ a b Ravishankara, A. R.; Daniel, J. S.; Portmann, R. W. (2009). "Nitrous Oxide (N2O): The Dominant Ozone-Depleting Substance Emitted in the 21st Century". Science. 326 (5949): 123–5. Bibcode:2009Sci...326..123R. doi:10.1126/science.1176985. PMID 19713491. S2CID 2100618.
- ^ a b Tian, Hanqin; Xu, Rongting; Canadell, Josep G.; Thompson, Rona L.; Winiwarter, Wilfried; Suntharalingam, Parvadha; Davidson, Eric A.; Ciais, Philippe; Jackson, Robert B.; Janssens-Maenhout, Greet; et al. (October 2020). "A comprehensive quantification of global nitrous oxide sources and sinks". Nature. 586 (7828): 248–256. Bibcode:2020Natur.586..248T. doi:10.1038/s41586-020-2780-0. ISSN 1476-4687. PMID 33028999. S2CID 222217027. Archived from the original on 13 October 2020. Retrieved 9 November 2020.
- ^ Thompson, R. L., Lassaletta, L., Patra, P. K. et al. (2019). "Acceleration of global N2O emissions seen from two decades of atmospheric inversion". Nat. Clim. Change. 9 (12): 993–998. Bibcode:2019NatCC...9..993T. doi:10.1038/s41558-019-0613-7. S2CID 208302708.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ "Chapter 8". AR5 Climate Change 2013: The Physical Science Basis. pp. 677–678.
- ^ a b "Nitrous oxide emissions pose an increasing climate threat, study finds". phys.org. Retrieved 9 November 2020.
- ^ Berger, Bruno (5 October 2007). "Is nitrous oxide safe?" (PDF). Swiss Propulsion Laboratory. pp. 1–2.
...Self pressurizing (Vapor pressure at 20°C is ~50.1 bar...Nontoxic, low reactivity -> rel. safe handling (General safe ???)...Additional energy from decomposition (as a monopropellant: ISP of 170 s)...Specific impulse doesn't change much with O/F...[page 2] N2O is a monopropellant (as H2O2 or Hydrazine...)
- ^ 고다드, R. H. (1914) "로켓 장치" 미국 특허 1,103,503
- ^ 아산화질소 안전성우주 추진 그룹 (2012)
- ^ a b Munke, Konrad (2001년 7월 2일) 아산화질소 트레일러 파열, CGA 세미나 보고서, 2001년 10월 15-17일 미주리주 세인트루이스
- ^ "Scaled Composites Safety Guidelines for N
2O" (PDF). Scaled Composites. 17 June 2009. Archived from the original (PDF) on 12 July 2011. Retrieved 29 December 2013.For example, N2O flowing at 130 psi in an epoxy composite pipe would not react even with a 2500 J ignition energy input. At 600 psi, however, the required ignition energy was only 6 J.
- ^ FR-5904.프랫 앤 휘트니 항공기.
- ^ Cline, Allen W. (2000년 1월) "엔진 기본: 폭발 및 점화 전"입니다.컨택! 매거진
- ^ "Holley performance products, FAQ for Nitrous Oxide Systems". Holley. Retrieved 18 December 2013.
- ^ "Explora Science Nitrous use as a propellant and in cooking". Retrieved 19 February 2019.
- ^ Dewey, Caitlin (21 December 2016). "The real reason grocery stores are running out of whipped cream this Christmas". The Washington Post. Retrieved 22 December 2016.
- ^ a b c d e Sneader W (2005). Drug Discovery –A History. (Part 1: Legacy of the past, chapter 8: systematic medicine, pp. 74–87). John Wiley and Sons. ISBN 978-0-471-89980-8. Retrieved 21 April 2010.
- ^ a b c Miller AH (1941). "Technical Development of Gas Anesthesia". Anesthesiology. 2 (4): 398–409. doi:10.1097/00000542-194107000-00004. S2CID 71117361.
- ^ Divatia, Jigeeshu V.; Vaidya, Jayant S.; Badwe, Rajendra A.; Hawaldar, Rohini W. (1996). "Omission of Nitrous Oxide during Anesthesia Reduces the Incidence of Postoperative Nausea and Vomiting". Anesthesiology. 85 (5): 1055–1062. doi:10.1097/00000542-199611000-00014. PMID 8916823. S2CID 41549796.
- ^ Hartung, John (1996). "Twenty-Four of Twenty-Seven Studies Show a Greater Incidence of Emesis Associated with Nitrous Oxide than with Alternative Anesthetics". Anesthesia & Analgesia. 83 (1): 114–116. doi:10.1213/00000539-199607000-00020.
- ^ Tramèr, M.; Moore, A.; McQuay, H. (February 1996). "Omitting nitrous oxide in general anaesthesia: meta-analysis of intraoperative awareness and postoperative emesis in randomized controlled trials". British Journal of Anaesthesia. 76 (2): 186–193. doi:10.1093/bja/76.2.186. PMID 8777095.
- ^ Council on Clinical Affairs (2013). "Guideline on use of nitrous oxide for pediatric dental patients" (PDF). Reference Manual V37. 6: 206–210.
- ^ Copeland, Claudia. "Nitrous Oxide Analgesia for Childbirth". Pregnancy.org. Archived from the original on 25 May 2011.
- ^ O'Connor RE; Brady W; Brooks SC; Diercks, D.; Egan, J.; Ghaemmaghami, C.; Menon, V.; O'Neil, B. J.; et al. (2010). "Part 10: acute coronary syndromes: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care". Circulation. 122 (18 Suppl 3): S787–817. doi:10.1161/CIRCULATIONAHA.110.971028. PMID 20956226.
- ^ Faddy, S. C.; Garlick, S. R. (1 December 2005). "A systematic review of the safety of analgesia with 50% nitrous oxide: can lay responders use analgesic gases in the prehospital setting?". Emergency Medicine Journal. 22 (12): 901–908. doi:10.1136/emj.2004.020891. PMC 1726638. PMID 16299211.
- ^ Davy, Humphry (1800). Researches, chemical and philosophical : chiefly concerning nitrous oxide, or diphlogisticated nitrous air, and its respiration. Francis A. Countway Library of Medicine. London : printed for J. Johnson, St. Paul's Church-Yard, by Biggs and Cottle, Bristol.
- ^ "Warning over laughing gas misuse". The Guardian. London. Press Association. 9 August 2014. Retrieved 9 August 2014.
- ^ VICE (7 February 2017), Inside The Laughing Gas Black Market, archived from the original on 29 October 2021, retrieved 29 March 2019
- ^ "Recycling used laughing gas canisters for cash could help create a cleaner Britain". Metro. 10 July 2018. Retrieved 15 July 2019.
- ^ CDC.gov NIOSH 경고: 마취제 투여 중 아산화질소 노출 통제신시내티, 오호주: 미국 보건복지부, 공중보건부, 질병통제센터, 국립산업안전보건연구소, DHHS(NIOSH) 간행물 94-100호
- ^ "CDC – NIOSH Pocket Guide to Chemical Hazards – Nitrous oxide". www.cdc.gov. Retrieved 21 November 2015.
- ^ 권장 기준: 폐기물 마취 가스 및 증기에 대한 직업적 노출.미국 보건복지부, 질병통제센터, 국립산업안전보건연구소, DHW(NIOSH) 간행물 77B140호
- ^ a b c Jay M (1 September 2008). "Nitrous oxide: recreational use, regulation and harm reduction". Drugs and Alcohol Today. 8 (3): 22–25. doi:10.1108/17459265200800022.
- ^ a b Jevtovic-Todorovic V, Beals J, Benshoff N, Olney JW (2003). "Prolonged exposure to inhalational anesthetic nitrous oxide kills neurons in adult rat brain". Neuroscience. 122 (3): 609–16. doi:10.1016/j.neuroscience.2003.07.012. PMID 14622904. S2CID 9407096.
- ^ Nakao S, Nagata A, Masuzawa M, Miyamoto E, Yamada M, Nishizawa N, Shingu K (2003). "NMDA receptor antagonist neurotoxicity and psychotomimetic activity". Masui. The Japanese Journal of Anesthesiology (in Japanese). 52 (6): 594–602. PMID 12854473.
- ^ Jevtovic-Todorovic V, Benshoff N, Olney JW (2000). "Ketamine potentiates cerebrocortical damage induced by the common anaesthetic agent nitrous oxide in adult rats". British Journal of Pharmacology. 130 (7): 1692–8. doi:10.1038/sj.bjp.0703479. PMC 1572233. PMID 10928976.
- ^ Jevtovic-Todorovic V, Carter LB; Carter (2005). "The anesthetics nitrous oxide and ketamine are more neurotoxic to old than to young rat brain". Neurobiology of Aging. 26 (6): 947–56. doi:10.1016/j.neurobiolaging.2004.07.009. PMID 15718054. S2CID 25095727.
- ^ Slikker, W.; Zou, X.; Hotchkiss, C. E.; Divine, R. L.; Sadovova, N.; Twaddle, N. C.; Doerge, D. R.; Scallet, A. C.; Patterson, T. A.; Hanig, J. P.; Paule, M. G.; Wang, C. (2007). "Ketamine-Induced Neuronal Cell Death in the Perinatal Rhesus Monkey". Toxicological Sciences. 98 (1): 145–158. doi:10.1093/toxsci/kfm084. PMID 17426105.
- ^ Sun, Lin; Qi Li; Qing Li; Yuzhe Zhang; Dexiang Liu; Hong Jiang; Fang Pan; David T. Yew (November 2012). "Chronic ketamine exposure induces permanent impairment of brain functions in adolescent cynomolgus monkeys". Addiction Biology. 19 (2): 185–94. doi:10.1111/adb.12004. PMID 23145560. S2CID 23028521.
- ^ a b Abraini JH, David HN, Lemaire M (2005). "Potentially neuroprotective and therapeutic properties of nitrous oxide and xenon". Annals of the New York Academy of Sciences. 1053 (1): 289–300. Bibcode:2005NYASA1053..289A. doi:10.1111/j.1749-6632.2005.tb00036.x. PMID 16179534. S2CID 34160112.
- ^ De Vasconcellos, K.; Sneyd, J. R. (2013). "Nitrous oxide: Are we still in equipoise? A qualitative review of current controversies". British Journal of Anaesthesia. 111 (6): 877–85. doi:10.1093/bja/aet215. PMID 23801743.
- ^ Middleton, Ben (2012). Physics in anaesthesia. Banbury, Oxfordshire, UK: Scion Pub. Ltd. ISBN 978-1-904842-98-9.
- ^ van Riel, A.J.H.P. (2022). "Alarming increase in poisonings from recreational nitrous oxide use after a change in EU-legislation, inquiries to the Dutch Poisons Information Center". International Journal of Drug Policy. 100: 103519. doi:10.1016/j.drugpo.2021.103519. PMID 34753046.
- ^ Flippo, T. S.; Holder Jr, W. D. (1993). "Neurologic Degeneration Associated with Nitrous Oxide Anesthesia in Patients with Vitamin B12 Deficiency". Archives of Surgery. 128 (12): 1391–5. doi:10.1001/archsurg.1993.01420240099018. PMID 8250714.
- ^ Randhawa, G.; Bodenham, A. (1 March 2016). "The increasing recreational use of nitrous oxide: history revisited". British Journal of Anaesthesia. pp. 321–324. doi:10.1093/bja/aev297. PMID 26323292.
- ^ Wrońska-Nofer, Teresa; Nofer, Jerzy-Roch; Jajte, Jolanta; Dziubałtowska, Elżbieta; Szymczak, Wiesław; Krajewski, Wojciech; Wąsowicz, Wojciech; Rydzyński, Konrad (1 March 2012). "Oxidative DNA damage and oxidative stress in subjects occupationally exposed to nitrous oxide (N2O)". Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 731 (1): 58–63. doi:10.1016/j.mrfmmm.2011.10.010. PMID 22085808.
- ^ Wrońska-Nofer, Teresa; Palus, Jadwiga; Krajewski, Wojciech; Jajte, Jolanta; Kucharska, Małgorzata; Stetkiewicz, Jan; Wąsowicz, Wojciech; Rydzyński, Konrad (18 June 2009). "DNA damage induced by nitrous oxide: Study in medical personnel of operating rooms". Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 666 (1–2): 39–43. doi:10.1016/j.mrfmmm.2009.03.012. PMID 19439331.
- ^ 아산화질소의 위험.Just Say N2O
- ^ van Amsterdam, Jan; Nabben, Ton; van den Brink, Wim (22 October 2015). "Recreational nitrous oxide use: Prevalence and risks". Regulatory Toxicology and Pharmacology. 73 (3): 790–796. doi:10.1016/j.yrtph.2015.10.017. ISSN 1096-0295. PMID 26496821.
- ^ Giannini, A.J. (1999). Drug Abuse. Los Angeles: Health Information Press. ISBN 978-1-885987-11-2.
- ^ Conrad, Marcel (4 October 2006). "Pernicious Anemia". Retrieved 2 June 2008.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ Vieira, E.; Cleaton-Jones, P.; Austin, J.C.; Moyes, D.G.; Shaw, R. (1980). "Effects of low concentrations of nitrous oxide on rat fetuses". Anesthesia and Analgesia. 59 (3): 175–7. doi:10.1213/00000539-198003000-00002. PMID 7189346. S2CID 41966990.
- ^ Vieira, E. (1979). "Effect of the chronic administration of nitrous oxide 0.5% to gravid rats". British Journal of Anaesthesia. 51 (4): 283–7. doi:10.1093/bja/51.4.283. PMID 465253.
- ^ Vieira, E; Cleaton-Jones, P; Moyes, D. (1983). "Effects of low intermittent concentrations of nitrous oxide on the developing rat fetus". British Journal of Anaesthesia. 55 (1): 67–9. doi:10.1093/bja/55.1.67. PMID 6821624.
- ^ 아산화질소.공기 리퀴드 가스 백과사전.
- ^ "Vaseline triggered explosion of hybrid rocket". Ukrocketman.com.
- ^ "Safetygram 20: Nitrous Oxide" (PDF). Airproducts.com. Archived from the original (PDF) on 1 September 2006.
- ^ a b Yamakura T, Harris RA (2000). "Effects of gaseous anaesthetics nitrous oxide and xenon on ligand-gated ion channels. Comparison with isoflurane and ethanol". Anesthesiology. 93 (4): 1095–101. doi:10.1097/00000542-200010000-00034. PMID 11020766. S2CID 4684919.
- ^ Mennerick S, Jevtovic-Todorovic V, Todorovic SM, Shen W, Olney JW, Zorumski CF (1998). "Effect of nitrous oxide on excitatory and inhibitory synaptic transmission in hippocampal cultures". Journal of Neuroscience. 18 (23): 9716–26. doi:10.1523/JNEUROSCI.18-23-09716.1998. PMC 6793274. PMID 9822732.
- ^ Gruss M, Bushell TJ, Bright DP, Lieb WR, Mathie A, Franks NP (2004). "Two-pore-domain K+ channels are a novel target for the anesthetic gases xenon, nitrous oxide, and cyclopropane". Molecular Pharmacology. 65 (2): 443–52. doi:10.1124/mol.65.2.443. PMID 14742687. S2CID 7762447.
- ^ a b Emmanouil DE, Quock RM (2007). "Advances in Understanding the Actions of Nitrous Oxide". Anesthesia Progress. 54 (1): 9–18. doi:10.2344/0003-3006(2007)54[9:AIUTAO]2.0.CO;2. PMC 1821130. PMID 17352529.
- ^ Atkinson, Roland M.; Green, J. DeWayne; Chenoweth, Dennis E.; Atkinson, Judith Holmes (1 October 1979). "Subjective Effects of Nitrous Oxide: Cognitive, Emotional, Perceptual and Transcendental Experiences". Journal of Psychedelic Drugs. 11 (4): 317–330. doi:10.1080/02791072.1979.10471415. PMID 522172.
- ^ Walker, Diana J.; Zacny, James P. (1 September 2001). "Within- and between-subject variability in the reinforcing and subjective effects of nitrous oxide in healthy volunteers". Drug and Alcohol Dependence. 64 (1): 85–96. doi:10.1016/s0376-8716(00)00234-9. PMID 11470344.
- ^ a b Sakamoto S, Nakao S, Masuzawa M (2006). "The differential effects of nitrous oxide and xenon on extracellular dopamine levels in the rat nucleus accumbens: a microdialysis study". Anesthesia and Analgesia. 103 (6): 1459–63. CiteSeerX 10.1.1.317.6613. doi:10.1213/01.ane.0000247792.03959.f1. PMID 17122223. S2CID 1882085.
- ^ a b Benturquia N, Le Marec T, Scherrmann JM, Noble F (2008). "Effects of nitrous oxide on dopamine release in the rat nucleus accumbens and expectation of reward" (PDF). Neuroscience. 155 (2): 341–4. doi:10.1016/j.neuroscience.2008.05.015. PMID 18571333. S2CID 8180084.
- ^ a b Lichtigfeld FJ, Gillman MA (1996). "Role of dopamine mesolimbic system in opioid action of psychotropic analgesic nitrous oxide in alcohol and drug withdrawal". Clinical Neuropharmacology. 19 (3): 246–51. doi:10.1097/00002826-199619030-00006. PMID 8726543.
- ^ a b Koyanagi S, Himukashi S, Mukaida K, Shichino T, Fukuda K (2008). "Dopamine D2-like receptor in the nucleus accumbens is involved in the antinociceptive effect of nitrous oxide". Anesthesia and Analgesia. 106 (6): 1904–9. CiteSeerX 10.1.1.327.9838. doi:10.1213/ane.0b013e318172b15b. PMID 18499630. S2CID 9307391.
- ^ David HN, Ansseau M, Lemaire M, Abraini JH (2006). "Nitrous oxide and xenon prevent amphetamine-induced carrier-mediated dopamine release in a memantine-like fashion and protect against behavioral sensitization". Biological Psychiatry. 60 (1): 49–57. doi:10.1016/j.biopsych.2005.10.007. PMID 16427030. S2CID 23364066.
- ^ a b Benturquia N, Le Guen S, Canestrelli C (2007). "Specific blockade of morphine- and cocaine-induced reinforcing effects in conditioned place preference by nitrous oxide in mice". Neuroscience. 149 (3): 477–86. doi:10.1016/j.neuroscience.2007.08.003. PMID 17905521. S2CID 12414836.
- ^ Ramsay DS, Watson CH, Leroux BG, Prall CW, Kaiyala KJ (2003). "Conditioned place aversion and self-administration of nitrous oxide in rats". Pharmacology Biochemistry and Behavior. 74 (3): 623–33. doi:10.1016/S0091-3057(02)01048-1. PMID 12543228. S2CID 22910876.
- ^ Wood RW, Grubman J, Weiss B (1977). "Nitrous oxide self-administration by the squirrel monkey". The Journal of Pharmacology and Experimental Therapeutics. 202 (3): 491–9. PMID 408480.
- ^ Zacny JP, Galinkin JL (1999). "Psychotropic drugs used in anesthesia practice: abuse liability and epidemiology of abuse". Anesthesiology. 90 (1): 269–88. doi:10.1097/00000542-199901000-00033. PMID 9915336.
- ^ Dohrn CS, Lichtor JL, Coalson DW, Uitvlugt A, de Wit H, Zacny JP (1993). "Reinforcing effects of extended inhalation of nitrous oxide in humans". Drug and Alcohol Dependence. 31 (3): 265–80. doi:10.1016/0376-8716(93)90009-F. PMID 8462415.
- ^ Walker DJ, Zacny JP (2001). "Within- and between-subject variability in the reinforcing and subjective effects of nitrous oxide in healthy volunteers". Drug and Alcohol Dependence. 64 (1): 85–96. doi:10.1016/S0376-8716(00)00234-9. PMID 11470344.
- ^ Emmanouil DE, Johnson CH, Quock RM (1994). "Nitrous oxide anxiolytic effect in mice in the elevated plus maze: mediation by benzodiazepine receptors". Psychopharmacology. 115 (1–2): 167–72. doi:10.1007/BF02244768. PMID 7862891. S2CID 21652496.
- ^ Zacny JP, Yajnik S, Coalson D, Lichtor JL, Apfelbaum JL, Rupani G, Young C, Thapar P, Klafta J (1995). "Flumazenil may attenuate some subjective effects of nitrous oxide in humans: a preliminary report". Pharmacology Biochemistry and Behavior. 51 (4): 815–9. doi:10.1016/0091-3057(95)00039-Y. PMID 7675863. S2CID 39068081.
- ^ Berkowitz BA, Finck AD, Hynes MD, Ngai SH (1979). "Tolerance to nitrous oxide analgesia in rats and mice". Anesthesiology. 51 (4): 309–12. doi:10.1097/00000542-197910000-00006. PMID 484891. S2CID 26281498.
- ^ a b Branda EM, Ramza JT, Cahill FJ, Tseng LF, Quock RM (2000). "Role of brain dynorphin in nitrous oxide antinociception in mice". Pharmacology Biochemistry and Behavior. 65 (2): 217–21. doi:10.1016/S0091-3057(99)00202-6. PMID 10672972. S2CID 1978597.
- ^ Gillman M.A. [1986a]미니뷰:진통제 [하마취성] 아산화질소는 내인성 오피오이드 시스템과 상호작용한다 : 증거의 재검토.생명과학39: l209-l22l
- ^ (Daras, C., Cantrill, R. C., Gillman, M. A. [1983년]3[H]-나록손 치환: 오피오이드 작용제로서의 아산화질소의 증거.유럽 약리학 저널 89: 177-8.
- ^ 오리, C., 포드 라이스, F., 런던, E.D. [1989년]아산화질소와 할로탄이 기니피그 뇌의 뮤 수용체와 카파 오피오이드 수용체에 미치는 영향.마취과 70: 541-544).
- ^ Guo TZ, Davies MF, Kingery WS, Patterson AJ, Limbird LE, Maze M (1999). "Nitrous oxide produces antinociceptive response via alpha2B and/or alpha2C adrenoceptor subtypes in mice". Anesthesiology. 90 (2): 470–6. doi:10.1097/00000542-199902000-00022. PMID 9952154.
- ^ Sawamura S, Kingery WS, Davies MF, Agashe GS, Clark JD, Koblika BK, Hashimoto T, Maze M (2000). "Antinociceptive action of nitrous oxide is mediated by stimulation of noradrenergic neurons in the brainstem and activation of [alpha]2B adrenoceptors". J. Neurosci. 20 (24): 9242–51. doi:10.1523/JNEUROSCI.20-24-09242.2000. PMC 6773006. PMID 11125002.
- ^ Maze M, Fujinaga M (2000). "Recent advances in understanding the actions and toxicity of nitrous oxide". Anaesthesia. 55 (4): 311–4. doi:10.1046/j.1365-2044.2000.01463.x. PMID 10781114. S2CID 39823627.
- ^ Housecroft, Catherine E. & Sharpe, Alan G. (2008). "Chapter 15: The group 15 elements". Inorganic Chemistry (3rd ed.). Pearson. p. 464. ISBN 978-0-13-175553-6.
- ^ Keys, T.E. (1941). "The Development of Anesthesia". Anesthesiology. 2 (5): 552–574. Bibcode:1982AmSci..70..522D. doi:10.1097/00000542-194109000-00008. S2CID 73062366.
- ^ McEvoy, J. G. (6 March 2015). "Gases, God and the balance of nature: a commentary on Priestley (1772) 'Observations on different kinds of air'". Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences. 373 (2039): 20140229. Bibcode:2015RSPTA.37340229M. doi:10.1098/rsta.2014.0229. PMC 4360083. PMID 25750146.
- ^ Priestley J (1776). "Experiments and Observations on Different Kinds of Air". 2 (3).
{{cite journal}}: Cite journal requiresjournal=(help) - ^ Davy H (1800). Researches, chemical and philosophical –chiefly concerning nitrous oxide or dephlogisticated nitrous air, and its respiration. Printed for J. Johnson.
- ^ Hardman, Jonathan G. (2017). Oxford Textbook of Anaesthesia. Oxford University Press. p. 529. ISBN 9780199642045.
- ^ Brecher EM (1972). "Consumers Union Report on Licit and Illicit Drugs, Part VI – Inhalants and Solvents and Glue-Sniffing". Consumer Reports Magazine. Retrieved 18 December 2013.
- ^ "George Poe is Dead". Washington Post. 3 February 1914. Retrieved 29 December 2007.
- ^ Erving, H. W. (1933). "The Discoverer of Anæsthesia: Dr. Horace Wells of Hartford". The Yale Journal of Biology and Medicine. 5 (5): 421–430. PMC 2606479. PMID 21433572.
- ^ Wells H (1847). A history of the discovery, of the application of nitrous oxide gas, ether, and other vapours, to surgical operations. J. Gaylord Wells.
- ^ Desai SP, Desai MS, Pandav CS (2007). "The discovery of modern anaesthesia-contributions of Davy, Clarke, Long, Wells and Morton". Indian J Anaesth. 51 (6): 472–8.
- ^ "Alleged Forgery". The Inter Ocean. 28 September 1877. p. 8. Retrieved 26 October 2015.
- ^ "A Man of Ominous Name". The Inter Ocean. 19 February 1890. Retrieved 26 October 2015.
- ^ a b Parmon, V. N.; Panov, G. I.; Uriarte, A.; Noskov, A. S. (2005). "Nitrous oxide in oxidation chemistry and catalysis application and production". Catalysis Today. 100 (2005): 115–131. doi:10.1016/j.cattod.2004.12.012.
- ^ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
- ^ "Nitrous oxide plant". Sanghi Organization. Archived from the original on 27 November 2013. Retrieved 18 December 2013.
- ^ "Nitrogen Family". chemistry.tutorvista.com
- ^ "Preparation of Nitrous Oxide from Urea, Nitric Acid and Sulfuric Acid".
- ^ Suwa T, Matsushima A, Suziki Y, Namina Y (1961). "Manufacture of Nitrous Oxide by the Catalytic Oxidation of Ammonia". The Journal of the Society of Chemical Industry, Japan. 64 (11): 1879–1888. doi:10.1246/nikkashi1898.64.11_1879.
- ^ Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0-12-352651-5
- ^ "N
2O Budget". Global Carbon Project. Retrieved 9 November 2020. - ^ "Chapter 6". TAR Climate Change 2001: The Scientific Basis. p. 358.
- ^ Ravishankara, A. R.; Daniel, John S.; Portmann, Robert W. (27 August 2009), "Supporting Online Material for - Nitrous Oxide (N2O): The Dominant Ozone-Depleting Substance Emitted in the 21st Century" (PDF), Science, 326 (5949): 123–125, Bibcode:2009Sci...326..123R, doi:10.1126/science.1176985, PMID 19713491, S2CID 2100618
- ^ a b c "Chapter 8". AR5 Climate Change 2013: The Physical Science Basis. p. 731.
- ^ a b U.S. Environmental Protection Agency (2010), "Methane and Nitrous Oxide Emissions from Natural Sources". Report EPA 430-R-10-001.
- ^ "2011 U.S. Greenhouse Gas Inventory Report". U.S. Environmental Protection Agency. February 2011. Archived from the original on 25 March 2011. Retrieved 11 April 2011.
- ^ Sloss, Leslie L. (1992). Nitrogen Oxides Control Technology Fact Book. William Andrew. p. 6. ISBN 978-0-8155-1294-3.
- ^ McDermott-Murphy, Caitlin (6 June 2019). "No laughing matter". The Harvard Gazette. Retrieved 22 July 2019.
- ^ a b c K. L. Denman, G. Brasseur, et al. (2007), "Couplings Between Changes in the Climate System and Biogeochemistry". In Fourth Assessment Report of the Intergovernmental Panel on Climate Change, Cambridge University Press.
- ^ Steinfeld, H.; Gerber, P.; Wassenaar, T.; Castel, V.; Rosales, M. & de Haan, C. (2006). Livestock's long shadow: Environmental issues and options. Fao.org. Retrieved 2 February 2008.
- ^ "Overview of Greenhouse Gases: Nitrous Oxide". U.S. Environmental Protection Agency. 23 December 2015. Archived from the original on 12 August 2016. Retrieved 31 March 2016.
- ^ "Nitrous Oxide: Sources and Emissions". U.S. Environmental Protection Agency. 2006. Archived from the original on 16 January 2008. Retrieved 2 February 2008.
- ^ IPCC. 2013. Climate change: the physical basis (WG I, full report). p. 512.
- ^ Thompson, R. L.; Lassaletta, L.; Patra, P. K.; Wilson, C.; Wells, K. C.; Gressent, A.; Koffi, E. N.; Chipperfield, M. P.; Winiwarter, W.; Davidson, E. A.; Tian, H. (18 November 2019). "Acceleration of global N 2 O emissions seen from two decades of atmospheric inversion". Nature Climate Change. 9 (12): 993–998. Bibcode:2019NatCC...9..993T. doi:10.1038/s41558-019-0613-7. ISSN 1758-6798. S2CID 208302708.
- ^ Molodovskaya, Marina; Warland, Jon; Richards, Brian K.; Öberg, Gunilla; Steenhuis, Tammo S. (2011). "Nitrous Oxide from Heterogeneous Agricultural Landscapes: Source Contribution Analysis by Eddy Covariance and Chambers". Soil Science Society of America Journal. 75 (5): 1829. Bibcode:2011SSASJ..75.1829M. doi:10.2136/SSSAJ2010.0415.
- ^ Molodovskaya, M.; Singurindy, O.; Richards, B. K.; Warland, J. S.; Johnson, M.; Öberg, G.; Steenhuis, T. S. (2012). "Temporal variability of nitrous oxide from fertilized croplands: hot moment analysis". Soil Science Society of America Journal. 76 (5): 1728–1740. Bibcode:2012SSASJ..76.1728M. doi:10.2136/sssaj2012.0039. S2CID 54795634.
- ^ Singurindy, Olga; Molodovskaya, Marina; Richards, Brian K.; Steenhuis, Tammo S. (July 2009). "Nitrous oxide emission at low temperatures from manure-amended soils under corn (Zea mays L.)". Agriculture, Ecosystems & Environment. 132 (1–2): 74–81. doi:10.1016/j.agee.2009.03.001.
- ^ Mason, C.W.; Stoof, C.R.; Richards, B.K.; Das, S.; Goodale, C.L.; Steenhuis, T.S. (2017). "Hotspots of nitrous oxide emission in fertilized and unfertilized perennial grasses on wetness-prone marginal land in New York State". Soil Science Society of America Journal. 81 (3): 450–458. Bibcode:2017SSASJ..81..450M. doi:10.2136/sssaj2016.08.0249.
- ^ Reimer R. A.; Slaten C. S.; Seapan M.; Lower M. W.; Tomlinson P. E. (1994). "Abatement of N2O emissions produced in the adipic acid industry". Environmental Progress. 13 (2): 134–137. doi:10.1002/ep.670130217.
- ^ Shimizu, A.; Tanaka, K. & Fujimori, M. (2000). "Abatement of N2O emissions produced in the adipic acid industry". Chemosphere – Global Change Science. 2 (3–4): 425–434. Bibcode:2000ChGCS...2..425S. doi:10.1016/S1465-9972(00)00024-6.
- ^ Schneider, Lisa K.; Wüst, Anja; Pomowski, Anja; Zhang, Lin; Einsle, Oliver (2014). "Ch. 8 No Laughing Matter: The Unmaking of the Greenhouse Gas Dinitrogen Monoxide by Nitrous Oxide Reductase". In Kroneck, Peter M. H.; Sosa Torres, Martha E. (eds.). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. Vol. 14. Springer. pp. 177–210. doi:10.1007/978-94-017-9269-1_8. ISBN 978-94-017-9268-4. PMID 25416395.
- ^ US Environmental Protection Agency, "Climate Change Indicators: Atmospheric Concentrations of Greenhouse Gases" Web document, accessed on 2017-02-14
- ^ "4.1.1 Sources of Greenhouse Gases". IPCC TAR WG1 2001. Archived from the original on 29 October 2012. Retrieved 21 September 2012.
- ^ Crutzen, P. J.; Mosier, A. R.; Smith, K. A.; Winiwarter, W. (2008). "N2O release from agro-biofuel production negates global warming reduction by replacing fossil fuels". Atmospheric Chemistry and Physics. 8 (2): 389–395. Bibcode:2008ACP.....8..389C. doi:10.5194/acp-8-389-2008.
- ^ "Overview of Greenhouse Gases: Nitrous Oxide Emissions". United States Environmental Protection Agency. 6 October 2016. Retrieved 14 July 2019.
- ^ Grossman, Lisa (28 August 2009). "Laughing gas is biggest threat to ozone layer". New Scientist.
- ^ "US Nitrous Oxide Laws (alphabetically) Based on a search of online free legal databases. Conducted May 2002". Center for Cognitive Liberty and Ethics. Archived from the original on 24 January 2008. Retrieved 27 January 2008.
- ^ "CAL. PEN. CODE § 381b : California Code – Section 381b". Lp.findlaw.com.
- ^ "Lambeth Council bans laughing gas as recreational drug". BBC News. 17 August 2015. Retrieved 17 August 2015.
- ^ Anderton, Jim (26 June 2005). "Time's up for sham sales of laughing gas". Beehive.govt.nz. Archived from the original on 8 January 2015.
- ^ "Ohio Medical" (PDF). www.ohiomedical.com. Archived from the original (PDF) on 17 April 2016. Retrieved 20 September 2017.
External links
- Occupational Safety and Health Guideline for Nitrous Oxide
- Paul Crutzen Interview Freeview video of Paul Crutzen Nobel Laureate for his work on decomposition of ozone talking to Harry Kroto Nobel Laureate by the Vega Science Trust.
- National Pollutant Inventory – Oxide of nitrogen fact sheet
- National Institute for Occupational Safety and Health – Nitrous Oxide
- CDC – NIOSH Pocket Guide to Chemical Hazards – Nitrous Oxide
- Nitrous Oxide FAQ
- Erowid article on Nitrous Oxide
- Nitrous oxide fingered as monster ozone slayer, Science News
- Dental Fear Central article on the use of nitrous oxide in dentistry
- Altered States Database