피렌
Pyrene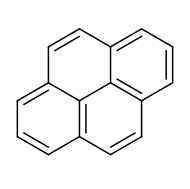 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 피렌[1] | |
| 기타 이름 벤조[디프]페난트렌 | |
| 식별자 | |
3D 모델(JSmol) | |
| 1307225 | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.004.481 |
| 84203 | |
| 케그 | |
PubChem CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C16H10 | |
| 몰 질량 | 202.256 g/120−1 |
| 외모 | 무색 고체 (많은 샘플에서 황색 불순물이 미량 수준에서 발견되는 경우가 많습니다.) |
| 밀도 | 1.271 g/mL |
| 녹는점 | 145 ~ 148 °C (293 ~298 °F, 418 ~421 K) |
| 비등점 | 404 °C (759 °F, 677 K) |
| 0.146mg/L | |
자화율(δ) | - 802.9·10cm−63/수직 |
| 위험 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 자극적인 |
| GHS [2]라벨링: | |
  | |
| 경고 | |
| H315, H319, H335, H410 | |
| P261, , , , , , , , , , , , , , | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 비고정적인 |
| 관련 화합물 | |
관련 PAH | 벤조피렌 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
피렌은 4개의 벤젠 고리로 구성된 다환 방향족 탄화수소(PAH)로, 결과적으로 평평한 방향족 시스템을 형성합니다.화학식은CH. 이 노란색 고체는 가장 작은 주변 용융 PAH(고리가 둘 이상의 면을 통해 융합된 PAH)입니다1610.피렌은 유기 [3]화합물의 불완전 연소 중에 형성된다.
발생 및 속성
피렌은 콜타르에서 처음 분리되었으며, 무게는 최대 2%까지 발생합니다.피렌은 주변용융 PAH로서 이성질체 플루오르안텐을 함유하는 5원환보다 공진안정성이 훨씬 높다.따라서 다양한 연소 조건에서 생산됩니다.예를 들어, 자동차는 약 1μg/[4]km를 생산한다.
반응
크롬산염에 의한 산화는 페리나프테논과 나프탈렌-1,4,5,8-테트라카르본산을 생성한다.피렌은 일련의 수소화 반응을 거치며 할로겐화, 디엘-알더 첨가 및 질화에 민감하며 선택성의 정도가 [4]다양합니다.브롬화는 3단계 [5]중 하나에서 발생합니다.
나트륨과 함께 환원하면 음이온이 생성된다.이 음이온으로부터 다양한 pi-arene 착체를 [6]제조할 수 있다.
광물리학
피렌 및 그 유도체는 예를 들어 피라닌 및 나프탈렌-1,4,5,8-테트라카르본산 등의 염료 및 염료 전구체를 제조하기 위해 상업적으로 사용된다.DCM 330nm의 선명한 대역 3개로 자외선-비스에 강한 흡광성을 갖췄다.방출은 흡수에 가깝지만 [7]375nm에서 이동합니다.신호의 형태는 용매에 따라 변화합니다.그 유도체는 또한 높은 양자 수율과 수명(에탄올 293K에서 각각 0.65 나노초, 410 나노초)을 가진 형광 분광학을 통한 귀중한 분자 프로브이다.피렌은 엑시머 성질이 [8]발견된 최초의 분자였다.이러한 엑시머는 450nm 전후로 나타난다.Theodor Förster는 [9]1954년에 이것을 보고했다.
적용들
피렌의 형광 방출 스펙트럼은 용매 극성에 매우 민감하기 때문에 피렌은 용매 환경을 결정하기 위한 탐침으로 사용되어 왔다.이는 들뜬 상태가 지면 상태와 다른 비평면 구조를 가지고 있기 때문입니다.일부 방출 대역은 영향을 받지 않지만 다른 대역은 용제와의 상호작용 강도에 따라 강도가 달라집니다.

피렌은 강력한 전자 공여 재료이며 에너지 변환 및 광수확 [7]용도에 사용할 수 있는 전자 공여-수용체 시스템을 만들기 위해 여러 재료와 결합할 수 있습니다.
안전 및 환경 요소
비록 벤조피렌만큼 문제가 있지는 않지만, 동물 연구에 따르면 피렌은 신장과 간에 독성이 있는 것으로 나타났다.현재 피렌이 물고기와 [11][12][13][14]조류에 있는 몇몇 살아있는 기능에 영향을 미치는 것으로 알려져 있다.
그것의 생분해는 철저하게 조사되었다.이 과정은 두 가지 CH=[15]CH 연결 각각에서 디히드록실화와 함께 시작됩니다.돼지를 대상으로 한 실험에서 소변 1-히드록시피렌은 [16]경구 투여 시 피렌의 대사물임을 알 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 206. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ GHS: PubChem
- ^ Figueira-Duarte, Teresa M.; Müllen, Klaus (2011). "Pyrene-Based Materials for Organic Electronics". Chemical Reviews. 111 (11): 7260–7314. doi:10.1021/cr100428a. PMID 21740071.
- ^ a b Senkan, Selim and Castaldi, Marco (2003) 울만의 산업화학 백과사전, Wiley-VCH, Weinheim.
- ^ Gumprecht, W. H. (1968). "3-Bromopyrene". Org. Synth. 48: 30. doi:10.15227/orgsyn.048.0030.
- ^ Kucera, Benjamin E.; Jilek, Robert E.; Brennessel, William W.; Ellis, John E. (2014). "Bis(pyrene)metal complexes of vanadium, niobium and titanium: Isolable homoleptic pyrene complexes of transition metals". Acta Crystallographica Section C: Structural Chemistry. 70 (8): 749–753. doi:10.1107/S2053229614015290. PMID 25093352.
- ^ a b Tagmatarchis, Nikos; Ewels, Christopher P.; Bittencourt, Carla; Arenal, Raul; Pelaez-Fernandez, Mario; Sayed-Ahmad-Baraza, Yuman; Canton-Vitoria, Ruben (2017-06-05). "Functionalization of MoS 2 with 1,2-dithiolanes: toward donor-acceptor nanohybrids for energy conversion". NPJ 2D Materials and Applications. 1 (1): 13. doi:10.1038/s41699-017-0012-8. ISSN 2397-7132.
- ^ Van Dyke, David A.; Pryor, Brian A.; Smith, Philip G.; Topp, Michael R. (May 1998). "Nanosecond Time-Resolved Fluorescence Spectroscopy in the Physical Chemistry Laboratory: Formation of the Pyrene Excimer in Solution". Journal of Chemical Education. 75 (5): 615. Bibcode:1998JChEd..75..615V. doi:10.1021/ed075p615.
- ^ Förster, Th.; Kasper, K. (June 1954). "Ein Konzentrationsumschlag der Fluoreszenz". Zeitschrift für Physikalische Chemie. 1 (5_6): 275–277. doi:10.1524/zpch.1954.1.5_6.275.
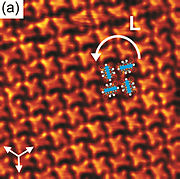
- ^ Pham, Tuan Anh; Song, Fei; Nguyen, Manh-Thuong; Stöhr, Meike (2014). "Self-assembly of pyrene derivatives on Au(111): Substituent effects on intermolecular interactions". Chem. Commun. 50 (91): 14089–92. doi:10.1039/C4CC02753A. PMID 24905327.
- ^ Oliveira, M.; Ribeiro, A.; Hylland, K.; Guilhermino, L. (2013). "Single and combined effects of microplastics and pyrene on juveniles (0+ group) of the common goby Pomatoschistus microps (Teleostei, Gobiidae)". Ecological Indicators. 34: 641–647. doi:10.1016/j.ecolind.2013.06.019.
- ^ Oliveira, M.; Gravato, C.; Guilhermino, L. (2012). "Acute toxic effects of pyrene on Pomatoschistus microps (Teleostei, Gobiidae): Mortality, biomarkers and swimming performance". Ecological Indicators. 19: 206–214. doi:10.1016/j.ecolind.2011.08.006.
- ^ Oliveira, M.; Ribeiro, A.; Guilhermino, L. (2012). "Effects of exposure to microplastics and PAHs on microalgae Rhodomonas baltica and Tetraselmis chuii". Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology. 163: S19–S20. doi:10.1016/j.cbpa.2012.05.062.
- ^ Oliveira, M.; Ribeiro, A.; Guilhermino, L. (2012). "Effects of short-term exposure to microplastics and pyrene on Pomatoschistus microps (Teleostei, Gobiidae)". Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology. 163: S20. doi:10.1016/j.cbpa.2012.05.063.
- ^ Seo, Jong-Su; Keum, Young-Soo; Li, Qing (2009). "Bacterial Degradation of Aromatic Compounds". International Journal of Environmental Research and Public Health. 6 (1): 278–309. doi:10.3390/ijerph6010278. PMC 2672333. PMID 19440284.
- ^ Keimig, S. D.; Kirby, K. W.; Morgan, D. P.; Keiser, J. E.; Hubert, T. D. (1983). "Identification of 1-hydroxypyrene as a major metabolite of pyrene in pig urine". Xenobiotica. 13 (7): 415–20. doi:10.3109/00498258309052279. PMID 6659544.
추가 정보
- Birks, J. B. (1969). Photophysics of Aromatic Molecules. London: Wiley.
- Valeur, B. (2002). Molecular Fluorescence: Principles and Applications. New York: Wiley-VCH.
- Birks, J. B. (1975). "Excimers". Reports on Progress in Physics. 38 (8): 903–974. Bibcode:1975RPPh...38..903B. doi:10.1088/0034-4885/38/8/001. ISSN 0034-4885.
- Fetzer, J. C. (2000). The Chemistry and Analysis of the Large Polycyclic Aromatic Hydrocarbons. New York: Wiley.