메타네티올
Methanethiol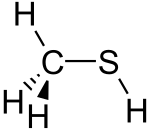 | |||
| | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 메타네티올 | |||
| 기타 이름 메틸메르캅탄 메르캅토메탄 메티올 티오메틸알코올/티오메타놀 메틸티올 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 3 DMet | |||
| 체비 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.000.748 | ||
| EC 번호 |
| ||
| 케그 | |||
PubChem CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 1064 | ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| CH3SH | |||
| 몰 질량 | 48.11g/120−1 | ||
| 외모 | 무색[1] 가스 | ||
| 냄새 | 썩은 양배추나 달걀과 같은 독특한 것 | ||
| 밀도 | 0.9g/mL(0°[1]C에서 액체) | ||
| 녹는점 | -123 °C (-189 °F, 150 K) | ||
| 비등점 | 5.95 °C (42.71 °F, 279.10 K) | ||
| 2% | |||
| 용해성 | 알코올, 에테르 | ||
| 증기압 | 1.7 atm (20°C)[1] | ||
| 산도(pKa) | ~10.4 | ||
| 위험 요소 | |||
| GHS 라벨링: | |||
   | |||
| 위험. | |||
| H220, H331, H410 | |||
| P210, , , , , , , , , , , | |||
| NFPA 704(파이어 다이아몬드) | |||
| 플래시 포인트 | -18 °C, 0 °F, 255[1] K | ||
| 폭발 한계 | 3.9%~21.[1]8% | ||
| 치사량 또는 농도(LD, LC): | |||
LD50(중간선량) | 60.67 mg/kg (표준)[2] | ||
LC50(중간 농도) | 3.3ppm (표준, 2시간) 675 ppm (rat, 4시간)[2] | ||
| NIOSH(미국 건강 노출 제한): | |||
PEL(허용) | C 10ppm (20mg/m3)[1] | ||
REL(권장) | C 0.5ppm (1mg/m3) [15분][1] | ||
IDLH(즉시 위험) | 150ppm[1] | ||
| 관련 화합물 | |||
관련 화합물 | 에단티올 | ||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
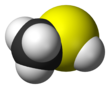
메틸메르캅탄(Methanethiol)은 화학식이
3 CHSH인 유기황 화합물이다.그것은 독특한 부패한 냄새를 가진 무색의 기체이다.그것은 식물 조직뿐만 아니라 동물(사람 포함)의 혈액, 뇌, 대변에서 발견되는 천연 물질이다.그것은 또한 일부 견과류와 치즈와 같은 특정 음식에서도 자연적으로 발생합니다.그것은 입냄새와 평탄한 냄새의 원인이 되는 화합물 중 하나이다.메타네티올은 가장 단순한 티올이며 때때로 MeSH로 약칭되기도 한다.인화성이 매우 높습니다.
구조 및 반응
그 분자는 메탄올처럼 탄소 원자에서 사면체이다.pK가a 10.4인 약한 산이지만 메탄올보다 약 10만 배 더 산성입니다.무색 소금은 다음과 같은 방법으로 얻을 수 있다.
- CHSH3 + CHUNa3 → CHSNA3 + CHOH3
티올레이트 음이온은 강한 친핵성 물질이다.
디메틸 이황화물로 산화될 수 있습니다.
- 2CHSH3 + [O] → CHSSCH33 + HO2
추가적인 산화는 이황화물을 냄새 없는 메탄술폰산 두 분자로 만든다.표백제는 이런 방식으로 메타네티올을 탈취한다.
발생.
메탄티오르(MeSH)는 펄프 공장에서 크래프트 펄프의 부산물로 방출됩니다.크래프트 펄핑에서 리그닌을 고알칼리성 매질에서 강구핵성 황화수소이온(HS−)에 의한 친핵성 공격에 의해 탈중합한다.그러나 부작용으로 HS는− 리그닌 중 메톡실기(OME)를 공격하여 탈메틸화하여 유리 페놀레이트기(PhO−)를 생성하고 MeSH를 방출한다.알칼리성으로 인해 MeSH는 쉽게 탈양성자(MeSNA)가 되며, 생성된 MeS− 이온도 강한 친핵성으로 황화디메틸과 더욱 반응한다.이 화합물은 액체에 남아 회수 보일러에서 연소되며, 여기서 황은 [3]황화나트륨으로 회수된다.
메탄티올은 습지의 부패하는 유기물에서 방출되며 특정 지역의 천연가스, 콜타르 및 일부 원유에 존재합니다.그것은 무와 같은 다양한 식물과 채소에서 발생합니다.
표면 해수에서 메타네티올은 알조 대사물 디메틸술포니오프로피온산(DMSP)의 1차 분해 생성물이다.해양세균은 황산염보다 훨씬 낮은 농도(약 0.3nM 대 28mM)로 바닷물에 존재함에도 불구하고 DMSP의 분해와 메타네티올의 혼입으로 단백질의 황 대부분을 얻는 것으로 보인다.산소가 있는 환경과 없는 환경 모두에서 박테리아는 메타네티올을 황화디메틸(DMS)로 변환할 수 있지만, 표면 바닷물에 있는 대부분의 DMS는 별도의 [citation needed]경로를 통해 생성됩니다.DMS와 메타네티올은 모두 일부 혐기성 토양에서 메타노제네시스 기질로 특정 미생물에 의해 사용될 수 있다.
메타네티올은 아스파라거스의 [4]신진대사의 부산물이다.아스파라거스를 먹은 후 소변에서 메타네티올이 생성되는 것은 한때 유전적 특성으로 여겨졌다.더 최근의 연구는 이 독특한 냄새는 사실 아스파라거스를 섭취한 후에 모든 사람에 의해 만들어 진다는 것을 암시하는 반면, 그것을 감지하는 능력 (메타네티올은 사실 "아스파라거스 오줌"의 많은 성분들 중 하나이다.)은 유전적인 [5]특성이다.소변 냄새의 변화를 일으키는 화학 성분은 아스파라거스를 [6]먹은 지 15분 만에 나타난다.
준비
메타네티올은 산화알루미늄 [7]촉매에서 메탄올과 황화수소 가스를 반응시켜 상업적으로 제조됩니다.
- CHOH3 + HS2 → CHSH3 + HO2
실용적이지 않지만 요오드화메틸과 티오요소의 [8]반응으로 제조할 수 있다.
사용하다
메타네티올은 주로 가금류와 동물성 [7]사료의 식성분으로 사용되는 필수 아미노산 메티오닌을 생산하는 데 사용된다.메타네티올은 또한 플라스틱 산업에서도 프리라디칼 중합[7] 촉진제 및 살충제 제조의 선구자로 사용됩니다.
이 화학물질은 메탄과 잘 섞이기 때문에 천연가스 산업에서도 악취제로 사용된다.혼합물의 특징적인 썩는 초목 냄새는 천연가스 소비자들에게 매우 사소한 [9]가스 누출의 징후로 널리 알려져 있습니다.
안전.
안전 데이터 시트(SDS)에는 메타네티올이 매우 강하고 역겨운 냄새를 가진 무색, 인화성 기체로 기재되어 있습니다.매우 높은 농도에서 그것은 매우 독성이 강하며 중추신경계에 영향을 미친다.그 침투하는 냄새는 위험한 농도에 대한 경고를 제공합니다.냄새 임계값은 1ppb로 [10]보고되었습니다.미국 OSHA 천장 한계는 10ppm으로 나열되어 있습니다.
사고
2001년에 25,000 US 갤런(95,000 L)의 폭발로 3명이 사망하고 9명이 [11]부상했습니다.
2014년 11월 15일 듀퐁의 라포르테 시설에서는 밀폐된 공간에서 메틸 메르캅탄의 치명적인 방출이 발생해 4명이 사망하고 1명이 부상했다.[12]
2022년 7월 14일 노스캐롤라이나주 샬롯에서 메타네티올이 우연히 방출되었다.부상자는 없었지만, 드문 날씨로 인해 냄새가 몇 시간 동안 지속되었다.많은 사람들은 천연가스 누출을 경험하고 있다고 믿었고, 이로 인해 많은 양의 긴급 전화가 걸려왔고 몇몇 지방 [13]관공서가 문을 닫았다.
레퍼런스
- ^ a b c d e f g h NIOSH Pocket Guide to Chemical Hazards. "#0425". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b "Methyl mercaptan". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ H. 식스타, 포타스트, A., Krotschek, A. W., 화학적 펄핑 공정펄프 핸드북, 식스타, H., Ed. Wiley-VCH Verlag GmbH & Co.:와인하임, 2006; 제1권, 페이지 169 (109-510)
- ^ Licher, Decker, Belin, Imbs, Montastruc, Giudicelli: "아스파라거스 이후 인간의 악취성 소변", 영국 임상약리학 저널, 1989년 5월
- ^ Lison M, Blondheim SH, Melmed RN (1980). "A polymorphism of the ability to smell urinary metabolites of asparagus". Br Med J. 281 (6256): 1676–8. doi:10.1136/bmj.281.6256.1676. PMC 1715705. PMID 7448566.
- ^ Skinny On: 디스커버리 채널이 웨이백머신에 아카이브된 2008-02-29
- ^ a b c Norell, John; Louthan, Rector P. (1988). "Thiols". Kirk-Othmer Concise Encyclopedia of Chemical Technology (3rd ed.). New York: John Wiley & Sons, Inc. pp. 946–963. ISBN 978-0471801047.
- ^ Reid, E. Emmet (1958). Organic Chemistry of Bivalent Sulfur. Vol. 1. New York: Chemical Publishing Company, Inc. pp. 32–33, 38.
- ^ SafeGase: 천연가스에 대해서:
- ^ Devos, M; F. Patte; J. Rouault; P. Lafort; L. J. Van Gemert (1990). Standardized Human Olfactory Thresholds. Oxford: IRL Press. p. 101. ISBN 0199631468.
- ^ "Deadly Explosion At Chemical Plant". www.cbsnews.com. Retrieved 2022-05-25.
- ^ "DuPont La Porte Facility Toxic Chemical Release CSB". www.csb.gov. Retrieved 2022-06-02.
- ^ Limehouse, Jonathan (2022-07-14). "What is the strong natural gas odor smell in Charlotte NC?". Charlotte Observer. Archived from the original on 2022-07-14. Retrieved 2022-07-14.