투호네
Thujone
| |||
 | |||
| 이름 | |||
|---|---|---|---|
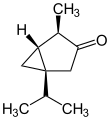
| IUPAC 이름 α: (1S, 4R, 5R)-4-메틸-1-(프로판-2-일)비시클로[3.1.0]헥산-3-온 β: (1S, 4S, 5R)-4-메틸-1-프로판-2-일비시클로[3.1.0]헥산-3-온 | |||
| 기타 이름 비시클로[3.1.0]헥산-3-온, 4-메틸-1-(1-메틸에틸)- [1S-(1α,4α,5α)]- α-투존 β-투존 투호네, 시스 3-Thujanone, (1S, 4R, 5R)-(-)- 투존 3-Thujanone, (-) l-Thujone; 4-메틸-1-(1-메틸에틸)비시클로[3.1.0]헥산-3-one-, (1S, 4R, 5R)- 3-Thujone; 시스-Tujone (Z)-Thujone (-)-투존; 비클로(3.1.0)헥산-3-온, 4-메틸-1-(1-메틸에틸)-(1S, 4R, 5R)- NSC 93742 1-이소프로필-4-메틸비시클로[3.1.0]아크산-3-온 | |||
| 식별자 | |||
| |||
3D 모델(JSmol) | |||
| 4660369 | |||
| 체비 | |||
| 첸블 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.013.096 | ||
| EC 번호 |
| ||
| 케그 | |||
PubChem CID | |||
| 유니 |
| ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| C10H16O | |||
| 몰 질량 | 152.237 g/g−1 | ||
| 밀도 | 0.92g/cm3(β-아크롬존), 0.16g/cm3(α-아크롬존) | ||
| 녹는점 | 25 °C 미만 | ||
| 비등점 | 203 °C (397 °F, 476 K) (alpha, beta-thujone) | ||
| 407 mg/L | |||
| 위험 요소 | |||
| GHS 라벨링: | |||
 | |||
| 경고 | |||
| H302 | |||
| P264, , , , , | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
투존(/θːuddʒoʊn/(![]() listen))[2]은 케톤 및 모노텔펜으로 주로 2가지 디아스테레오머(에피머) 형태인 α-투존 [3][4]및 +-β-투존이다.
listen))[2]은 케톤 및 모노텔펜으로 주로 2가지 디아스테레오머(에피머) 형태인 α-투존 [3][4]및 +-β-투존이다.
비록 그것은 압신테의 화학 화합물로 가장 잘 알려져 있지만, 소량의 존재로 인해 압신테의 자극제 및 정신 반응 효과의 원인이 될 것 같지는 않다.투존은 GABA에 대항제로 작용한다(알코올의 효과와는 반대).억제전달물질 GABA에 간섭함으로써 저용량으로 자극적이고 기분을 좋게 하는 효과를 전달할 수 있지만 GABA의 경쟁적 길항제로서 투존만 [5]경련으로 간주된다.그것은 또한 향수에 여러 에센셜 오일의 성분으로 사용된다.
자연발생적인 (-)α-튜존 및 (+)β-튜존 외에 (+)α-튜존 및 (-)β-튜존의 2가지 형태가 가능하다.2016년,[6] 그들은 자연에서도 살비아 오피셜리스에서 발견되었다.
원천
Thujone은 주로 1:2 비율의 이성질체의 혼합물로, 수목, 누트카 편백나무, 일부 유채나무, 쑥, 오레가노, 일반적인 현자나무, 탄시나무, 그리고 약쑥과 같은 많은 식물에서 발견됩니다.민트박쥐의 다양한 종에서도 발견된다.
생합성
투존의 생합성은 다른 모노텔펜의 합성과 유사하며, 디메틸알릴 피로인산(DMAPP)과 이소펜테닐 이인산(IPP)으로부터 제라닐 이인산([7]Geranyl Diphosphate)의 형성과 함께 시작되며, 제라닐 이인산합성효소에 의해 촉매된다.정량적 CNMR 스펙트럼 분석 결과 식물에서 투존을 형성하는 데 사용된 이소프렌 단위는 메틸에리톨 인산 경로(MEP)[8]에서 파생된 것으로 나타났다.
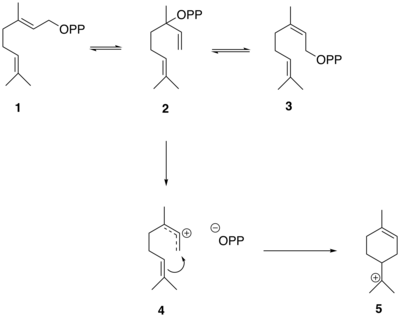
GPP로부터 사비넨에서 투잔 골격을 생성하는 반응은 GPP를 [7]기질로 하는 효소 사비넨 합성효소에 의해 매개된다.GPP(1)는 먼저 리날릴이인산(LPP)(2)과 네릴이인산(NPP)(3)으로 이성질화되며 LPP는 탈국재화알릴카티온이인산(4)을 우선적으로 형성한다.이온-쌍 중간체는 친전자성 첨가물을 순환시켜 α-terpinyl 3차 양이온(5)[7]을 생성한다.
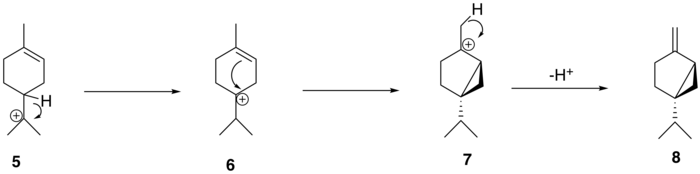
그런 다음 α-터피닐 양이온(5)은 바그너-메어웨인 재배열을 통해 1.2 수소화물 이동을 거치면서 테르피넨-4-일 양이온(6)을 형성한다.이 양이온은 양성자를 잃기 전에 투질 양이온 중간체(7)를 형성하기 위해 두 번째 환화를 거쳐 투질 양이온 전구체(+)-사비넨(8)을 형성한다.
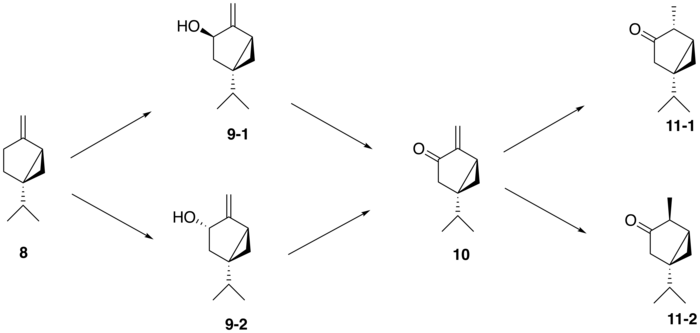
(+)-사비넨(8)으로부터 투존을 생성하기 위한 제안된 생합성 경로는 3단계 경로를 따른다: (+)-사비넨은 먼저 시토크롬 P450 효소에 의해 +)-사비놀(9-1,2)의 이성체로 산화되고, 이어서 탈수소효소를 통해 (+)-사비논(10)으로 변환된다.마지막으로 환원효소는 α-투존(11-1) 및 β-투존(11-2)[9]으로의 변환을 매개한다.(+)-사비놀 중간체의 이성질은 투존 생산 식물에 따라 다르다. 예를 들어, 서부 레드세다르(Thuja plicata)에서 투존은 (+)-트랜스-사비놀 중간체(9-1)에서만 파생되는 반면, 공통 정원 세이지(Salvia officinalis)에서는 (+)-sabol 중간체(+2-in)에서 형성된다.
약리학
분자 형태만을 살펴본 연구에 기초하여, 수년 동안 Thujone은 칸나비노이드 [11]수용체에 THC와 유사하게 작용하는 것으로 생각되었지만, 그 이후 이는 [12]거짓으로 판명되었다.투존은 GABAA 수용체[13] 길항제이며, 구체적으로는 GABAA 수용체 경쟁 길항제이다.GABA 수용체 활성화를 억제함으로써, 뉴런은 더 쉽게 발화할 수 있고, 이것은 근육 [14]경련과 경련을 일으킬 수 있다.GABAA 수용체와의 이러한 상호작용은 알파-투존에 [15]특이적이다.Thujone은 또한 5-HT3 [16][17]길항제이다.
마우스에서 두 이성질체 중 활성도가 높은 알파-투존의 중앙치사량(LD50)은 약 45mg/kg이며, 사망률은 30mg/kg에서 0%, 60mg/kg에서 100%이다.높은 용량에 노출된 쥐는 경련을 일으켜 1분 이내에 사망에 이르게 됩니다.30~45mg/kg의 쥐는 다리에 근육 경련을 일으켜 죽거나 회복될 때까지 전신 경련으로 진행된다.이러한 효과는 다른 GABA 길항제들과 일치한다.또한 알파-투존은 [14]생쥐의 간에서 빠르게 대사된다.디아제팜, 페노바르비탈 또는 1g/kg의 에탄올과 같은 GABA 양성 알로스테릭 조절제를 사용하여 전처리는 100mg/kg의 [citation needed]치사량을 방지합니다.
주의력 수행은 알코올에 저용량 및 고용량의 투존을 사용하여 테스트되었습니다.높은 선량은 주의력 수행에 단기적으로 부정적인 영향을 미쳤다.더 낮은 용량에서는 [18]눈에 띄는 효과가 나타나지 않았다.
투존은 뇌, 신장, 간 세포에 독성이 있다고 보고되고 있으며 너무 많은 양을 사용하면 경련을 일으킬[by whom?] 수 있다.나무수목과 같은 다른 투존 함유 식물들은 주로 면역계 자극[citation needed] 효과를 위해 한약재로 사용된다.이 식물의 에센셜 오일의 부작용에는 불안, 불면증, 경련 등이 있어 투존의 [5][19]중추신경계 효과를 확인할 수 있다.
압신테에서
투존은 압신테의 화합물로 가장 유명하다.과거에는 압신테가 최대 260~350mg/l의 [20]투혼을 함유하고 있는 것으로 생각되었지만, 최근 테스트에서는 이 추정치가 너무 높은 것으로 나타났다.2008년 가스 크로마토그래피-질량분석(GC-MS)을 사용하여 13개의 사전 반(1895–1910) 병을 조사한 결과, 이 병은 0.5~48.3mg/l 사이였으며 평균 25.4mg/l 2005년 연구에서는 1899년 고웜우드 조리법을 재현하고 GC-MS로 테스트한 결과 가장 높은 4.3mg/[23]l가 검출되었습니다.가스 크로마토그래피만으로는 다른 화합물이 간섭하여 겉으로 측정된 [24]양을 추가할 수 있으므로 이 용량에서 GC-MS 테스트는 중요하다.
역사
이 화합물은 19세기 중반 압신테가 유행한 후 발견되었다.알코올 중독을 연구한 발렌틴 매그넌 박사는 순수한 쑥기름을 동물들에게 실험한 결과 알코올의 영향과는 무관하게 발작을 일으키는 것을 발견했다.이를 근거로 약쑥기름이 소량 함유된 압신테는 일반 알코올보다 위험한 것으로 추정됐다.결국 이러한 반응의 원인으로 투존이 분리되었다.매그넌은 계속해서 250명의 알코올 중독자들을 연구했고 압신트를 마신 사람들은 발작과 환각을 겪었다고 언급했다.발작은 GABA 수용체와 상호작용하는 (+)-α-투존에 의해 발생하며,[15] 간질 활동을 일으킨다.현대의 증거에 비추어 볼 때, 이러한 결론은 의심스럽다. 왜냐하면 그것들은 다른 화합물과 [25]질병에 대한 부족한 이해에 기초하고 있고, 알코올과 압신트가 프랑스 [26]인종을 타락시키고 있다는 마그난의 믿음에 의해 흐려졌기 때문이다.
압신테가 금지되자 1970년대 영국 과학저널 네이처가 대마초에서 발견되는 1차 정신작용 물질인 테트라히드로카나비놀(THC)과 투존의 분자 형태를 비교한 논문을 발표하면서 뇌에도 같은 작용을 한다는 설이 제기되면서 연구가 중단됐다.아나비노이드[11][27]
최근에는 유럽 [28]이사회 지령 No. 88/388/EEC(1988)에 따라 위에서 설명한 연구가 실시되어 압신테에서 극소량의 투존만 검출되었다.
규정
유럽 연합
EU의 최대 tujone 레벨은 다음과 같습니다.[29][30]
- 세이지 및 비알코올 음료로 제조된 것을 제외한 아르테미시아 종으로 제조된 식품 0.5mg/kg
- 아르테미시아종으로 제조되지 않은 알코올 음료의 10mg/kg
- 25 mg/kg (세이지와 함께 준비된 식품)
- 아르테미시아종으로 제조된 알코올 음료의 35mg/kg
미국
미국에서는 음식에 순수한 투존을 첨가하는 것은 [31]허용되지 않는다.아르테미시아 종, 백삼나무, 참나무 이끼, 탄시 또는 실로우를 함유한 식품 또는 음료는 투존이 [32]없어야 하며, 이는 실제로 10mg/l 투존 [33]미만을 함유함을 의미한다.투존이 함유된 다른 허브는 제한이 없습니다.예를 들어, 세이지 오일과 세이지 오일(최대 50% 투존)은 식품의약국(FDA)의 일반적으로 안전한 물질([34]GRAS) 목록에 있습니다.
미국에서 판매되는 압신테는 아르테미시아가 [33]함유된 다른 음료에 적용되는 것과 동일한 기준에 따라 투존이 없어야 하므로 소량의 투존이 합법적으로 수입될 수 있다.
캐나다
캐나다에서 주류법은 주 정부의 영역이다.Alberta, Ontario 및 Nova Scotia는 [citation needed]10mg/kg Thujone, Quebec은 kg당 15mg, Manitoba는 l당 6-8mg Thujone, British Columbia는 Ontario와 동일한 수준을 준수합니다.그러나 서스캐처원과 퀘벡에서는 최대 1상자(보통 750ml 병 12개 또는 9L)를 구매하면 전 세계에서 구할 수 있는 모든 술을 살 수 있다.각 주류 게시판은 각 제품을 판매하기 전에 승인을 받아야 합니다.
α-투존의 화학 스펙트럼
1H NMR (500 MHz, CDCl3)
[ [ 3636 ] = 2.54 (dd, J = 18.8, 2.3, 1.1Hz, 1H, H-2), 2.21 (q, J = 7.2Hz, 1H, H-4), 2.07 (d, J = 18.8Hz, 1H, 1H, H-36'),, 1H, H-6').[35]
13C NMR(91MHz, CDCl3)
§ [140] = 221.7(C=O, C-3), 47.5(CH, C-4), 39.9(CH2, C-2), 33.1(CH, C-7), 29.8(C, C-1), 25.7(CH, C-5), 20.1(CH, C-9, C-8)
질량 분석
m/z: 81(100), 110(96.58), 109(59.88), 95(58.97), 67(57.37)[36]www.webbook.nist.gov 웹사이트에는 Thujone의 m/z 비율이 110(100), 81(~89), 95(~71); 67(~69), 109(~44)로 나열되어 있습니다.
적외선
cm−1: 3020, 2961, 1733, 1602, 1455, 1219, 1096, 1014.[37]
「 」를 참조해 주세요.
- 피오우누프카 – 압신테보다 투혼 함량이 높은 폴란드 알코올 제조물
레퍼런스
- ^ Richert, Clemens; Krupp, Felix; Frey, Wolfgang (2020). "Absolute Configuration of Small Molecules by Co‐Crystallization". Angew. Chem. Int. Ed. 59 (37): 15875–15879. doi:10.1002/anie.202004992. PMC 7540501. PMID 32441841.
- ^ 고대 그리스어 υα, tuj(a)에서 유래한 아세톤의 화학적 친척을 위한 삼나무 + - νη - -, - one, 여성 후견제
- ^ Perry NB, Anderson RE, Brennan NJ, Douglas MH, Heaney AJ, McGimpsey JA, Smallfield BM (1999). "Essential Oils from Dalmatian Sage (Salvia officinalis L.): Variations among Individuals, Plant Parts, Seasons, and Sites". J. Agric. Food Chem. 47 (5): 2048–2054. doi:10.1021/jf981170m. PMID 10552494.
- ^ Oppolzer W, Pimm A, Stammen B, Hume WE (1997). "Palladium-Catalysed Intramolecular Cyclisations of Olefinic Propargylic Carbonates and application to the diastereoselective synthesis of enantiomerically pure (−)-α-thujone". Helv. Chim. Acta. 80 (3): 623–639. doi:10.1002/hlca.19970800302.
- ^ a b Olsen, Richard W. (2000-04-25). "Absinthe and γ-aminobutyric acid receptors". Proceedings of the National Academy of Sciences of the United States of America. 97 (9): 4417–4418. Bibcode:2000PNAS...97.4417O. doi:10.1073/pnas.97.9.4417. ISSN 0027-8424. PMC 34311. PMID 10781032.
- ^ Williams, Jack D.; Yazarians, Jessica A.; Almeyda, Chelcie C.; Anderson, Kristin A.; Boyce, Gregory R. (23 May 2016). "Detection of the Previously Unobserved Stereoisomers of Thujone in the Essential Oil and Consumable Products of Sage (Salvia officinalis L.) Using Headspace Solid-Phase Microextraction–Gas Chromatography–Mass Spectrometry". Journal of Agricultural and Food Chemistry. 64 (21): 4319–4326. doi:10.1021/acs.jafc.6b01065. PMID 27181395.
- ^ a b c Dewick, Paul M (2009). Medicinal natural products: a biosynthetic approach (3rd ed.). John Wiley & Sons Ltd. pp. 195–197. ISBN 978-0-470-74167-2.
- ^ Umlauf, Dirk; Zapp, Josef (September 2004). "Biosynthesis of the irregular monoterpene artemisia ketone, the sesquiterpene germacrene D and other isoprenoids in Tanacetum vulgare L. (Asteraceae)". Phytochemistry. 65 (17): 2463–2470. doi:10.1016/j.phytochem.2004.08.019. PMID 15381410.
- ^ Foster, Adam J.; Hall, Dawn E. (Apr 2013). "Identification of Genes in Thuja plicata Foliar Terpenoid Defenses". Plant Physiology. 161 (4): 1993–2004. doi:10.1104/pp.112.206383. PMC 3613470. PMID 23388118.
- ^ Gesell, Andreas; Blaukopf, Markus (May 2015). "The Gymnosperm Cytochrome P450 CYP750B1 Catalyzes Stereospecific Monoterpene Hydroxylation of (+)-Sabinene in Thujone Biosynthesis in Western Redcedar". Plant Physiology. 168 (1): 94–106. doi:10.1104/pp.15.00315. PMC 4424034. PMID 25829465.
- ^ a b 콘라드 3세, 바르나비; (1988)압신테: 병 속의 역사크로니클 북스ISBN 0-8118-1650-8 페이지 152
- ^ Meschler JP, Howlett AC (March 1999). "Thujone exhibits low affinity for cannabinoid receptors but fails to evoke cannabimimetic responses". Pharmacol. Biochem. Behav. 62 (3): 473–80. doi:10.1016/S0091-3057(98)00195-6. PMID 10080239. S2CID 30865036.
- ^ Olsen RW (April 2000). "Absinthe and gamma-aminobutyric acid receptors". Proc. Natl. Acad. Sci. U.S.A. 97 (9): 4417–8. Bibcode:2000PNAS...97.4417O. doi:10.1073/pnas.97.9.4417. PMC 34311. PMID 10781032.
- ^ a b Höld KM, Sirisoma NS, Ikeda T, Narahashi T, Casida JE (April 2000). "Alpha-thujone (the active component of absinthe): gamma-aminobutyric acid type A receptor modulation and metabolic detoxification". Proc. Natl. Acad. Sci. U.S.A. 97 (8): 3826–31. Bibcode:2000PNAS...97.3826H. doi:10.1073/pnas.070042397. PMC 18101. PMID 10725394.
- ^ a b Höld, Karin M.; Sirisoma, Nilantha S.; Ikeda, Tomoko; Narahashi, Toshio; Casida, John E. (2000-04-11). "α-Thujone (the active component of absinthe): γ-Aminobutyric acid type A receptor modulation and metabolic detoxification". Proceedings of the National Academy of Sciences of the United States of America. 97 (8): 3826–3831. Bibcode:2000PNAS...97.3826H. doi:10.1073/pnas.070042397. ISSN 0027-8424. PMC 18101. PMID 10725394.
- ^ Deiml T, Haseneder R, Zieglgänsberger W, Rammes G, Eisensamer B, Rupprecht R, Hapfelmeier G (Feb 2004). "Alpha-thujone reduces 5-HT3 receptor activity by an effect on the agonist-reduced desensitization". Neuropharmacology. 46 (2): 192–201. doi:10.1016/j.neuropharm.2003.09.022. PMID 15002407. S2CID 54346490.
- ^ 식물 유래 천연물에 의한 이온성 GABA 수용체 조절
- ^ Dettling A, Grass H, Schuff A, Skopp G, Strohbeck-Kuehner P, Haffner HT (2004). "Absinthe: attention performance and mood under the influence of thujone". J. Stud. Alcohol. 65 (5): 573–81. doi:10.15288/jsa.2004.65.573. PMID 15536765.
- ^ Naser B, Bodinet C, Tegtmeier M, Lindequist U (Mar 2005). "Thuja occidentalis (Arbor vitae): A Review of its Pharmaceutical, Pharmacological and Clinical Properties". Evidence-Based Complementary and Alternative Medicine. 2 (1): 69–78. doi:10.1093/ecam/neh065. PMC 1062158. PMID 15841280.
- ^ 압신스주의: 현재 영향을 미치는 가상의 19세기 증후군, Padosch et al.2006년 10월 28일 취득.
- ^ 압신테 신화가 마침내 잠잠해지다
- ^ 투혼, 펜촌, 피노캄폰, 메탄올, 구리 및 안티몬 농도에 특화된 빈티지 프레반 압신테의 화학적 조성
- ^ 투혼 - 복근증 때문에?라첸마이어, 에메르트 외2006년 10월 28일 취득.
- ^ 2007-11-27 Wayback Machine, Emert et al.에 보관된 고체상 추출 및 가스 크로마토그래피를 사용하여 압신테에서 a/b-Thujone 및 관련 Terpenes의 측정.2006년 10월 28일 취득.
- ^ Lachenmeier, Dirk; Nathan-Maister, David; Breaux, Theodore; Luaute, Jean-Pierre; Emmert, Joachim (2010). "Absinthe, Absinthism and Thujone – New Insight into the Spirit's Impact on Public Health" (PDF). The Open Addiction Journal. 3: 32–38. doi:10.2174/1874941001003010032. Retrieved 6 July 2016.
- ^ 콘라드 3세, 바르나비; (1988)압신테: 병 속의 역사연대기 책.ISBN 0-8118-1650-8 페이지 101-105
- ^ Del Castillo J.; Anderson M.; Rubottom G.M. (1975). "Letters to Nature: Marijuana, absinthe and the central nervous system". Nature. 253 (5490): 365–366. doi:10.1038/253365a0. PMID 1110781. S2CID 4245058.
- ^ 유럽 이사회 지침 No. 88/388/EEC, 1988년 6월 22일
- ^ 2008년 12월 16일 유럽의회 및 이사회 규칙(EC) No 1334/2008, 유럽위원회.
- ^ 투존식품과학위원회(2003)의 의견 2006년 10월 28일 취득.
- ^ Laurie C. Dolan; Ray A. Matulka & George A. Burdock (2010). "Naturally Occurring Food Toxins". Toxins. 2 (9): 2289–2332. doi:10.3390/toxins2092289. PMC 3153292. PMID 22069686.
- ^ FDA 규정 21 CFR 172.510 – 인간 소비를 위한 식품에 직접 첨가할 수 있는 식품 첨가물.미국 식품의약국(2003년).2006년 10월 28일 취득.
- ^ a b 2007년 10월 17일 웨이백 머신에 2014-02-09년 보관된 미국 재무부 알코올 및 담배 세금 및 무역국 산업 회람 2007-5.2009년 5월 5일 취득
- ^ 일반적으로 안전한 것으로 인식되는 물질.2005-11-30 Wayback Machine Food and Drug Administration(2003)에 보관.2006년 10월 28일 취득.
- ^ a b Thamm, Irene; Richers, Johannes; Rychlik, Michael; Tiefenbacher, Konrad (2016). "A six-step total synthesis of α-thujone and d6-α-thujone, enabling facile access to isotopically labelled metabolites" (PDF). Chemical Communications. 52 (78): 11701–11703. doi:10.1039/c6cc05376a. ISSN 1359-7345. PMID 27709180.
- ^ Movafeghi, A.; Djozan, Dj.; Torbati, S. (2010-08-15). "Solid-phase microextraction of volatile organic compounds released from leaves and flowers of Artemisia fragrans, followed by GC and GC/MS analysis". Natural Product Research. 24 (13): 1235–1242. doi:10.1080/14786410903108951. ISSN 1478-6419. PMID 20645210. S2CID 2711713.
- ^ Lightner, David A.; Pak, Chwang Siek; Crist, B.Vincent; Rodgers, Stephen L.; Givens, John W. (January 1985). "The octant rule. XVI1. COnformation and circular dichroism of and 2-methylbicyclo[3.1.0]hexan-3-ones, thujone and isothujone". Tetrahedron. 41 (19): 4321–4330. doi:10.1016/s0040-4020(01)97203-5. ISSN 0040-4020.
추가 정보
- Lachenmeier DW, Nathan-Maister D, Breaux TA, Sohnius EM, Schoeberl K, Kuballa T (May 2008). "Chemical composition of vintage preban absinthe with special reference to thujone, fenchone, pinocamphone, methanol, copper, and antimony concentrations". J. Agric. Food Chem. 56 (9): 3073–81. doi:10.1021/jf703568f. PMID 18419128.
외부 링크
- Absinte는 Cern Courier의 Wayback Machine, 2008년 7월 8일 아카이브 완료 2012-03-19일
- 투존.정보 - 일부 상업 브랜드의 tujone, absinthe, absinthism 및 독립 tujone 등급에 대한 동료 리뷰 기사 데이터베이스.
- 투존의 흔들리는 역사 - 웜우드 소사이어티의 투존과 그 역사에 관한 기사.