글리신
Glycine
| |||
| |||
| |||
| 이름들 | |||
|---|---|---|---|
| IUPAC이름 글리신 | |||
| 계통 IUPAC명 아세트산[2] | |||
| 기타이름 2-아미노에탄올산 글리콜 당산 디카르바믹산 | |||
| 식별자 | |||
3D 모델(JSMO) | |||
| 약어 | Gly, G | ||
| ChEBI | |||
| 쳄블 | |||
| 켐스파이더 | |||
| 드럭뱅크 | |||
| ECHA 인포카드 | 100.000.248 | ||
| EC 번호 |
| ||
| 케그 | |||
펍켐 CID | |||
| 유니아이 | |||
CompTox 대시보드 (EPA) | |||
| |||
| 특성. | |||
| C2H5NO2 | |||
| 어금니 질량 | 75.067g·mol−1 | ||
| 외모 | 흰색실체 | ||
| 밀도 | 1.1607g/cm3[3] | ||
| 융점 | 233°C (451°F; 506K) (분해) | ||
| 249.9g/L(25°C)[4] | |||
| 용해도 | 피리딘에 용해되는 에탄올에 잘 녹지 않는 에테르에 불용성인 | ||
| 산도(pKa) | 2.34 (carbox), 9.6 (amino) | ||
| -40.3·10cm−63/mol | |||
| 약리학 | |||
| B05CX03(WHO) | |||
| 유해성 | |||
| 치사량 또는 농도(LD, LC): | |||
LD50(중앙선량) | 2600 mg/kg (mouse, 경구) | ||
| 부가자료페이지 | |||
| 글리신(자료페이지) | |||
별도의 언급이 없는 경우를 제외하고, 표준 상태(25 °C [77 °F], 100 kPa에서)의 재료에 대한 데이터가 제공됩니다. | |||
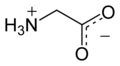
글리신(Glycine, 기호 Gly 또는 G; / ˈɡla ɪsi ːn/)은 단일 수소 원자를 곁사슬로 하는 아미노산입니다.화학식이 NH ‐CH ‐COOH인 가장 단순한 안정한 아미노산(카바믹산은 불안정)입니다.글리신은 단백질을 생성하는 아미노산 중 하나입니다.GG(GGU, GGC, GGA, GG)로 시작하는 모든 코돈에 의해 인코딩됩니다.글리신은 작은 R 그룹에 의해 발생하는 "유연성" 때문에 2차 단백질 구조에서 알파 나선의 형성에 필수적입니다.글리신은 억제적인 신경전달물질이기도 한데, 예를 들어 클로스트리디움 테타니 감염 시와 같이 척수 내에서 글리신의 방출을 방해하는 것은 억제되지 않은 근육 수축으로 인해 경련성 마비를 일으킬 수 있습니다.
이것은 유일한 카이랄 단백질 생성 아미노산입니다.단 하나의 수소 원자로 구성된 최소의 측쇄 때문에 친수성 또는 소수성 환경에 적합할 수 있습니다.
역사와 어원
글리신은 1820년 프랑스 화학자 앙리 브라노(Henri Braconnot)가 젤라틴을 황산과 함께 끓여 가수분해하면서 발견했습니다.[8]그는 처음에 그것을 "젤라틴의 설탕"이라고 불렀지만,[9][10] 프랑스의 화학자 장 밥티스트 부싱고는 1838년에 그것이 질소를 포함하고 있다는 것을 보여주었습니다.[11]1847년, 당시 독일 화학자 쥐스투스 폰 리빅의 제자였던 미국 과학자 에벤 노튼 호스포드가 "글리코콜"[12][13]이라는 이름을 제안했지만, 스웨덴 화학자 베르젤리우스는 1년 후에 더 간단한 현재의 이름을 제안했습니다.[14][15]이름은 그리스어 γλυκύς인 "스위트 테이스팅"("sweet tasting")에서 유래했습니다.1858년, 프랑스의 화학자 오귀스트 카아워는 글리신이 초산의 아민이라고 밝혀냈습니다.[17]
생산.
글리신은 가수분해된 단백질로부터 분리될 수 있지만, 이 경로는 화학적 합성에 의해 더 편리하게 제조될 수 있기 때문에 산업 생산에 사용되지 않습니다.[18]클로로아세트산과 암모니아를 혼합하여 글리신과 염화암모늄을 얻는 공정과 [19]미국과 일본의 주요 합성법인 [20]스트래커 아미노산 합성이 주요 공정입니다.[21]이런 방식으로 연간 약 15,000톤이 생산됩니다.[22]
글리신은 또한 EDTA 합성에서 불순물로 생성되며, 암모니아 동생성물의 반응으로부터 발생합니다.[23]
화학반응
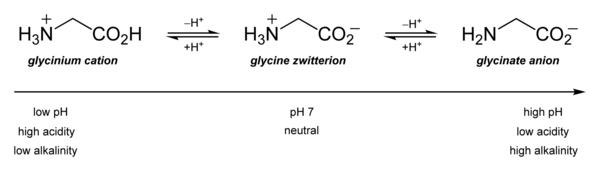
산-염기 특성이 가장 중요합니다.수용액에서 글리신은 양쪽성이다: pH = 2.4 이하에서는 글리시늄이라고 불리는 암모늄 양이온으로 전환됩니다.약 9.6 이상에서는 글리신산으로 전환됩니다.
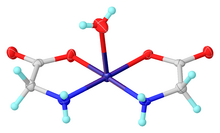
글리신은 아미노산 복합체를 형성하는 많은 금속 이온의 이중 리간드로서 기능합니다.전형적인 복합체는 Cu(글리시네이트),2 즉 Cu(HNCHCO222)이며,2 cis 및 trans 이성질체 둘 다에 존재합니다.
글리신은 산성 염화물과 함께 히푸르산과[24] 아세틸글리신과 같은 아미도카르복실산으로 전환됩니다.[25]아질산을 사용하면 글리콜산을 얻는다(반 슬라이크 결정).요오드화메틸을 사용하면 아민이 4차화되어 천연물인 트리메틸글리신이 생성됩니다.
- HNCHCOO + 3 CHI → (CH)NCHCOO + 3 HI
글리신은 글리실글리신의 형성을 시작으로 스스로 응축하여 펩타이드를 생성합니다.
- 2 HNCCHCOO → HNCCHCONCHCOO + HO
글리신 또는 글리실글리신의 열분해는 고리형 디아미드인 2,5-디케토피페라진을 제공합니다.
알코올과 함께 에스터를 형성합니다.그들은 종종 그들의 염산염, 예를 들어 글리신 메틸 에스터 염산염으로 분리됩니다.그렇지 않으면 유리 에스테르는 디케토피페라진으로 전환되는 경향이 있습니다.
2관능 분자로서 글리신은 많은 시약과 반응합니다.이것들은 N-중심 반응과 카르복실레이트-중심 반응으로 분류될 수 있습니다.
신진대사
생합성
글리신은 3-포스포글리세르산으로부터 유도되는 아미노산 세린으로부터 체내에서 생합성되기 때문에 인간의 식단에 필수적인 것은 아니지만, 보충제 판매자들이 만든 한 출판물은 글리신 생합성을 위한 대사 능력이 콜라겐 합성의 필요성을 충족시키지 못한다는 것을 보여주는 것 같습니다.[26]대부분의 생물체에서 세린 하이드록시메틸트랜스퍼레이스는 조인자 피리독살 인산을 통해 이러한 변형을 촉매합니다.[27]
대장균에서 글리신은 엽산을 표적으로 하는 항생제에 민감합니다.[28]
척추동물의 간에서 글리신 합성은 글리신 합성효소(glycine cleavage enzyme라고도 함)에 의해 촉매됩니다.이 변환은 쉽게 되돌릴 수 있습니다.[27]
글리신은 세린으로부터 합성되는 것 외에도 간과 신장의 장기간 대사를 통해 트레오닌, 콜린 또는 하이드록시프롤린으로부터도 유도될 수 있습니다.[29]
퇴화
글리신은 세 가지 경로를 통해 분해됩니다.동물과 식물에서 주요한 경로는 위에서 언급된 글리신 합성효소 경로의 반대입니다.이러한 맥락에서, 관련된 효소계는 보통 글리신 절단계(glyc.[27]
- 글리신 + 테트라하이드로폴산 + NAD ⇌ CO + NH + N,N-메틸렌 테트라하이드로폴산 + NADH + H
두 번째 경로에서 글리신은 두 단계로 분해됩니다.첫 번째 단계는 세린으로부터 글리신 생합성과 세린 하이드록시메틸트랜스퍼라제의 역반응입니다.세린은 세린 탈수효소에 의해 피루브산으로 전환됩니다.[27]
글리신은 세 번째 분해 경로에서 D-아미노산 산화효소에 의해 글리옥실레이트로 전환됩니다.글리옥실레이트는 간 젖산+ 탈수소효소에 의해 NAD 의존적 반응에서 옥살레이트로 산화됩니다.[27]
글리신의 반감기와 체내에서의 글리신의 제거는 용량에 따라 크게 다릅니다.[30]한 연구에서 반감기는 0.5시간에서 4.0시간 사이로 다양했습니다.[30]
생리기능
글리신의 주요 기능은 단백질의 전구체 역할을 한다는 것입니다.대부분의 단백질은 소량의 글리신만을 포함하는데, 주목할 만한 예외는 콜라겐인데, 히드록시프롤린과 함께 콜라겐의 나선 구조 형성에 주기적으로 반복되는 역할로 인해 약 35%의 글리신을 포함하고 있습니다.[27][31]유전자 코드에서 글리신은 GG로 시작하는 모든 코돈, 즉 GGU, GGC, GGA 및 GGG에 의해 코딩됩니다.
생합성 중간체로서
고등 진핵생물에서 포르피린의 핵심 전구체인 δ-아미노레불린산은 ALA 합성효소에 의해 글리신과 석시닐-CoA로부터 생합성됩니다.글리신은 모든 퓨린의 중심 CN2 소단위체를 제공합니다.[27]
신경전달물질로써
글리신은 중추신경계, 특히 척수, 뇌간, 망막에서 억제성 신경전달물질입니다.글리신 수용체가 활성화되면, 염화물은 이온성 수용체를 통해 뉴런으로 들어가 시냅스 후 전위(IPSP)를 억제합니다.스트리크닌은 이온성 글리신 수용체에 대한 강한 길항제인 반면 비쿠쿨린은 약한 길항제입니다.글리신은 글루타메이트와 함께 NMDA 수용체에 필요한 공동작용제입니다.척수에서 글리신의 억제 역할과는 대조적으로, 이러한 행동은 흥분성인 (NMDA) 글루타머테릭 수용체에서 촉진됩니다.[32]글리신의 LD는50 랫드(구강)에서 7930mg/kg이며,[33] 보통 과흥분에 의한 사망을 유발합니다.
사용하다
미국에서 글리신은 일반적으로 두 가지 등급으로 판매됩니다.미국 약사법("USP") 및 기술 등급.USP 등급 매출은 미국 글리신 시장의 약 80~85%를 차지합니다.예를 들어 정맥 주사의 경우 USP 기준 이상의 순도가 필요한 경우에는 보다 비싼 약학 등급의 글리신을 사용할 수 있습니다.USP 등급 기준을 충족할 수도 있고 충족하지 못할 수도 있는 기술 등급 글리신은 산업 응용 분야에서 사용하기 위해, 예를 들어 금속 복합화 및 마감 분야에서 에이전트로 더 낮은 가격에 판매됩니다.[34]
동물성 및 인간성 식품
글리신은 영양적인 가치 때문에 주사제를 제외하고는 음식에 널리 사용되지 않습니다.대신 음식 화학에서 글리신의 역할은 향료입니다.약간 달콤하고 사카린의 뒷맛에 반합니다.또한 금속 이온으로 복합화되어 있기 때문에 보존성도 가지고 있습니다.금속 글리시네이트 복합체(예: 구리(II) 글리시네이트는 동물 사료의 보충제로 사용됩니다.[22]
미국 식품의약국은 더 이상 글리신과 그 염을 일반적으로 인간 식품에 사용해도 안전하다고 인정하는 것으로 간주하지 않습니다.[36]
화공사
글리신은 다양한 화학 제품 합성의 중간생성물입니다.제초제 글리포세이트,[37] 이프로디온, 글리포신, 이미프로트린, 에글리나진 등의 제조에 사용됩니다.[22]티암페니콜과 같은 약의 중간체로 사용됩니다.[citation needed]
실험실 연구
글리신은 단백질 분석의 SDS-PAGE 방법에 사용되는 일부 용액의 중요한 성분입니다.전기영동 중 pH를 유지하고 시료 손상을 방지하는 완충제 역할을 합니다.글리신은 또한 SDS-PAGE 겔에서 관심있는 수많은 단백질의 탐색을 가능하게 하기 위해 웨스턴 블롯 막에서 단백질 표지 항체를 제거하는 데 사용됩니다.이를 통해 동일한 검체에서 더 많은 데이터를 추출할 수 있어 데이터의 신뢰성을 높이고 검체 처리량과 필요한 검체 수를 줄일 수 있습니다.이 프로세스를 스트리핑(stripping)이라고 합니다.
우주에서의 존재
글리신의 지구 밖 존재는 2009년에 확인되었는데, 이는 2004년 NASA의 우주선 스타더스트가 와일드 2 혜성에서 채취하여 지구로 돌아온 샘플들을 분석한 결과에 근거한 것입니다.글리신은 1970년 머치슨 운석에서 발견된 적이 있습니다.[38]우주 공간에서 글리신의 발견은 생명체의 "구성 요소"가 우주 전체에 널리 퍼져 있다고 주장하는 소위 "연판 페르미아"의 가설을 뒷받침했습니다.[39]2016년 로제타 우주선이 67P/추류모프-게라시멘코 혜성에서 글리신을 검출했다고 발표했습니다.[40]
성간매질에서 태양계 밖의 글리신의 검출은 논의되어 왔습니다.[41]2008년 막스 플랑크 전파천문연구소는 궁수자리 은하 중심 근처의 거대한 가스 구름인 거대 분자 하이마트에서 글리신 전구체(아미노아세토니트릴)의 스펙트럼선을 발견했습니다.[42]
진화
글리신은 초기 유전자 코드에 의해 정의될 것으로 제안됩니다.[43][44][45][46]예를 들어, 초기 유전자 코드의 프로토-펩타이드와 유사할 수 있는 낮은 복잡도 영역(단백질 내)은 글리신이 매우 풍부합니다.[46]
음식물에 존재
| 음식. | 백분율 내용을 무게로 (g/100g) |
|---|---|
| 간식, 돼지고기 껍질 | 11.04 |
| 참깨가루(저지방) | 3.43 |
| 음료, 단백질 분말(간장계) | 2.37 |
| 씨앗, 홍화씨앗 식사, 부분적으로 탈지됨 | 2.22 |
| 고기, 들소, 쇠고기 등 (각종 부위) | 1.5–2.0 |
| 젤라틴 디저트 | 1.96 |
| 씨앗, 호박, 호박씨알 | 1.82 |
| 터키, 모든 계층, 등, 고기, 가죽 | 1.79 |
| 닭고기, 구이기 또는 튀김, 고기 및 껍질 | 1.74 |
| 돼지고기, 갈은 것, 96% 기름기 / 4% 지방, 익힌 것, 부스러기 | 1.71 |
| 베이컨과 비프 스틱 | 1.64 |
| 땅콩 | 1.63 |
| 갑각류, 가시가재 | 1.59 |
| 향신료, 겨자씨, 갈은 것 | 1.59 |
| 살라미 | 1.55 |
| 견과류, 버터넛, 말린 것 | 1.51 |
| 생선, 연어, 핑크, 통조림, 배수된 고형물 | 1.42 |
| 아몬드 | 1.42 |
| 생선,고등어 | 0.93 |
| 바로 먹을 수 있는 시리얼, 그래놀라, 집에서 만든 | 0.81 |
| 부추, (구 모양과 아랫잎 부분) 동결건조 | 0.7 |
| 치즈, 파마산(및 기타), 갈은 것 | 0.56 |
| 콩, 녹색, 익힌, 삶아진, 물기를 뺀, 소금 없이 | 0.51 |
| 빵, 단백질(글루텐 포함) | 0.47 |
| 계란, 통, 익힌, 후라이드 | 0.47 |
| 콩, 흰색, 성숙한 씨앗, 요리, 삶음, 소금과 함께 | 0.38 |
| 렌틸콩, 성숙한 씨앗, 익히고 끓이고 소금과 함께 | 0.37 |
참고 항목
참고문헌
- ^ The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (11th ed.), Merck, 1989, ISBN 091191028X, 4386
- ^ pubchem.ncbi.nlm.nih.gov/compound/750#section=IUPAC-Name&fullscreen=true
- ^ 화학과 물리학 편람, CRC Press, 59판, 1978
- ^ "Solubilities and densities". Prowl.rockefeller.edu. Archived from the original on September 12, 2017. Retrieved November 13, 2013.
- ^ Dawson, R.M.C. 등, Data for Biochemical Research, Oxford, Clarendon Press, 1959
- ^ "Nomenclature and Symbolism for Amino Acids and Peptides". IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. Archived from the original on October 9, 2008. Retrieved March 5, 2018.
- ^ "Glycine Definition of glycine in English by Oxford Dictionaries". Archived from the original on January 29, 2018.
- ^ Plimmer, R.H.A. (1912) [1908]. Plimmer, R.H.A.; Hopkins, F.G. (eds.). The chemical composition of the proteins. Monographs on biochemistry. Vol. Part I. Analysis (2nd ed.). London: Longmans, Green and Co. p. 82. Retrieved January 18, 2010.
- ^ ; Braconnot, Henri (1820). "Sur la conversion des matières animales en nouvelles substances par le moyen de l'acide sulfurique" [On the conversion of animal materials into new substances by means of sulfuric acid]. Annales de Chimie et de Physique. 2nd series (in French). 13: 113–125. 114쪽 참조.
- ^ MacKenzie, Colin (1822). One Thousand Experiments in Chemistry: With Illustrations of Natural Phenomena; and Practical Observations on the Manufacturing and Chemical Processes at Present Pursued in the Successful Cultivation of the Useful Arts …. Sir R. Phillips and Company. p. 557.
- ^ Boussingault (1838). "Sur la composition du sucre de gélatine et de l'acide nitro-saccharique de Braconnot" [On the composition of sugar of gelatine and of nitro-glucaric acid of Braconnot]. Comptes Rendus (in French). 7: 493–495.
- ^ Horsford, E.N. (1847). "Glycocoll (gelatine sugar) and some of its products of decomposition". The American Journal of Science and Arts. 2nd series. 3: 369–381.
- ^ Ihde, Aaron J. (1970). The Development of Modern Chemistry. Courier Corporation. ISBN 9780486642352.
- ^ Berzelius, Jacob (1848). Jahres-Bericht über die Fortschritte der Chemie und Mineralogie (Annual Report on the Progress of Chemistry and Mineralogy). Vol. 47. Tübigen, (Germany): Laupp. p. 654. 654쪽: "Erhat dem Leimzuckerals Bases den Namen Glycocollgeben.… 글라이신젠난트베르덴(Glycingenanntwerden, und diesen Namenwerdeich anwenden)"이라고 썼습니다. (그는 당시 독일 화학자 쥐스투스 폰 리빅의 제자였던 미국 과학자 에벤 노튼 호스포드(Eben Norton Horsford)는 염기인 림주커(Leimzucker)에게 "글리코콜(glycocoll)"이라는 이름을 붙였습니다.이 이름은 화법적이지 않고 다른 기지의 이름과 충돌하는 결점이 있습니다.이것은 γλυχυς (달콤한)과 χολλα (동물 접착제)로 혼합되어 있습니다.이 유기농 베이스가 단 맛을 내는 유일한 [[유일]]이기 때문에, 그것은 훨씬 더 짧게 "글리신"이라고 명명될 수 있고, 저는 이 이름을 사용할 것입니다.)
- ^ Nye, Mary Jo (1999). Before Big Science: The Pursuit of Modern Chemistry and Physics, 1800-1940. Harvard University Press. ISBN 9780674063822.
- ^ "glycine". Oxford Dictionaries. Archived from the original on November 13, 2014. Retrieved December 6, 2015.
- ^ Cahours, A. (1858). "Recherches sur les acides amidés" [Investigations into aminated acids]. Comptes Rendus (in French). 46: 1044–1047.
- ^ Okafor, Nduka (March 9, 2016). Modern Industrial Microbiology and Biotechnology. CRC Press. ISBN 9781439843239.
- ^ Ingersoll, A. W.; Babcock, S. H. (1932). "Hippuric acid". Organic Syntheses. 12: 40.; Collective Volume, vol. 2, p. 328
- ^ Wiley (December 14, 2007). Kirk-Othmer Food and Feed Technology, 2 Volume Set. John Wiley & Sons. ISBN 9780470174487.
- ^ "Glycine Conference (prelim)". USITC. Archived from the original on February 22, 2012. Retrieved June 13, 2014.
{{cite web}}: CS1 maint : bot : 원본 URL 상태 알 수 없음 (링크) - ^ a b c Drauz, Karlheinz; Grayson, Ian; Kleemann, Axel; Krimmer, Hans-Peter; Leuchtenberger, Wolfgang & Weckbecker, Christoph (2007). "Amino Acids". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.
- ^ Hart, J. Roger (2005). "Ethylenediaminetetraacetic Acid and Related Chelating Agents". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a10_095.
- ^ Ingersoll, A. W.; Babcock, S. H. (1932). "Hippuric Acid". Org. Synth. 12: 40. doi:10.15227/orgsyn.012.0040.
- ^ Herbst, R. M.; Shemin, D. (1939). "Acetylglycine". Org. Synth. 19: 4. doi:10.15227/orgsyn.019.0004.
- ^ Meléndez-Hevia, E; De Paz-Lugo, P; Cornish-Bowden, A; Cárdenas, M. L. (December 2009). "A weak link in metabolism: the metabolic capacity for glycine biosynthesis does not satisfy the need for collagen synthesis". Journal of Biosciences. 34 (6): 853–72. doi:10.1007/s12038-009-0100-9. PMID 20093739. S2CID 2786988.
- ^ a b c d e f g Nelson, David L.; Cox, Michael M. (2005). Principles of Biochemistry (4th ed.). New York: W. H. Freeman. pp. 127, 675–77, 844, 854. ISBN 0-7167-4339-6.
- ^ Kwon, Yun Kyung; Higgins, Meytal B.; Rabinowitz, Joshua D. (2010). "Antifolate-Induced Depletion of Intracellular Glycine and Purines Inhibits Thymineless Death in E. Coli". ACS Chemical Biology. 5 (8): 787–795. doi:10.1021/cb100096f. PMC 2945287. PMID 20553049.
- ^ Wang, W.; Wu, Z.; Dai, Z.; Yang, Y.; Wang, J.; Wu, G. (2013). "Glycine metabolism in animals and humans: Implications for nutrition and health". Amino Acids. 45 (3): 463–77. doi:10.1007/s00726-013-1493-1. PMID 23615880. S2CID 7577607.
- ^ a b Hahn RG (1993). "Dose-dependent half-life of glycine". Urological Research. 21 (4): 289–291. doi:10.1007/BF00307714. PMID 8212419. S2CID 25138444.
- ^ Szpak, Paul (2011). "Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis". Journal of Archaeological Science. 38 (12): 3358–3372. doi:10.1016/j.jas.2011.07.022.
- ^ "Recent development in NMDA receptors". Chinese Medical Journal. 2000.
- ^ "Safety (MSDS) data for glycine". The Physical and Theoretical Chemistry Laboratory Oxford University. 2005. Archived from the original on October 20, 2007. Retrieved November 1, 2006.
- ^ "Glycine From Japan and Korea" (PDF). U.S. International Trade Commission. January 2008. Archived (PDF) from the original on June 6, 2010. Retrieved June 13, 2014.
- ^ Casari, B. M.; Mahmoudkhani, A. H.; Langer, V. (2004). "A Redetermination of cis-Aquabis(glycinato-κ2N,O)copper(II)". Acta Crystallogr. E. 60 (12): m1949–m1951. doi:10.1107/S1600536804030041.
- ^ "eCFR :: 21 CFR 170.50 -- Glycine (aminoacetic acid) in food for human consumption". ecfr.gov. Retrieved October 24, 2022.
- ^ Stahl, Shannon S.; Alsters, Paul L. (July 13, 2016). Liquid Phase Aerobic Oxidation Catalysis: Industrial Applications and Academic Perspectives. John Wiley & Sons. ISBN 9783527690152.
- ^ Kvenvolden, Keith A.; Lawless, James; Pering, Katherine; Peterson, Etta; Flores, Jose; Ponnamperuma, Cyril; Kaplan, Isaac R.; Moore, Carleton (1970). "Evidence for extraterrestrial amino-acids and hydrocarbons in the Murchison meteorite". Nature. 228 (5275): 923–926. Bibcode:1970Natur.228..923K. doi:10.1038/228923a0. PMID 5482102. S2CID 4147981.
- ^ "Building block of life found on comet - Thomson Reuters 2009". Reuters. August 18, 2009. Retrieved August 18, 2009.
- ^ European Space Agency (May 27, 2016). "Rosetta's comet contains ingredients for life". Retrieved June 5, 2016.
- ^ Snyder LE, Lovas FJ, Hollis JM, et al. (2005). "A rigorous attempt to verify interstellar glycine". Astrophys J. 619 (2): 914–930. arXiv:astro-ph/0410335. Bibcode:2005ApJ...619..914S. doi:10.1086/426677. S2CID 16286204.
- ^ Staff. "Organic Molecule, Amino Acid-Like, Found In Constellation Sagittarius 27 March 2008 - Science Daily". Retrieved September 16, 2008.
- ^ Trifonov, E.N (December 2000). "Consensus temporal order of amino acids and evolution of the triplet code". Gene. 261 (1): 139–151. doi:10.1016/S0378-1119(00)00476-5. PMID 11164045.
- ^ Higgs, Paul G.; Pudritz, Ralph E. (June 2009). "A Thermodynamic Basis for Prebiotic Amino Acid Synthesis and the Nature of the First Genetic Code". Astrobiology. 9 (5): 483–490. arXiv:0904.0402. Bibcode:2009AsBio...9..483H. doi:10.1089/ast.2008.0280. ISSN 1531-1074. PMID 19566427. S2CID 9039622.
- ^ Chaliotis, Anargyros; Vlastaridis, Panayotis; Mossialos, Dimitris; Ibba, Michael; Becker, Hubert D.; Stathopoulos, Constantinos; Amoutzias, Grigorios D. (February 17, 2017). "The complex evolutionary history of aminoacyl-tRNA synthetases". Nucleic Acids Research. 45 (3): 1059–1068. doi:10.1093/nar/gkw1182. ISSN 0305-1048. PMC 5388404. PMID 28180287.
- ^ a b Ntountoumi, Chrysa; Vlastaridis, Panayotis; Mossialos, Dimitris; Stathopoulos, Constantinos; Iliopoulos, Ioannis; Promponas, Vasilios; Oliver, Stephen G; Amoutzias, Grigoris D (November 4, 2019). "Low complexity regions in the proteins of prokaryotes perform important functional roles and are highly conserved". Nucleic Acids Research. 47 (19): 9998–10009. doi:10.1093/nar/gkz730. ISSN 0305-1048. PMC 6821194. PMID 31504783.
- ^ "National Nutrient Database for Standard Reference". U.S. Department of Agriculture. Archived from the original on March 3, 2015. Retrieved September 7, 2009.
{{cite journal}}:저널 요구사항 인용journal=(도움말)
추가열람
- Kuan YJ, Charnley SB, Huang HC, et al. (2003). "Interstellar glycine". Astrophys J. 593 (2): 848–867. Bibcode:2003ApJ...593..848K. doi:10.1086/375637.
- Nowak, Rachel. "Amino acid found in deep space - 18 July 2002 - New Scientist". Retrieved July 1, 2007.
외부 링크
- 글리신 MS 스펙트럼
- 글리신
- 글리신 절단계
- 글리신 치료법 - 조현병 치료의 새로운 방향?
- "Organic Molecule, Amino Acid-Like, Found In Constellation Sagittarius". ScienceDaily. March 27, 2008.
- Tsai, Guochuan E. (December 1, 2008). "A New Class of Antipsychotic Drugs: Enhancing Neurotransmission Mediated by NMDA Receptors". Psychiatric Times. 25 (14). Archived from the original on October 3, 2012. Retrieved January 23, 2009.
- ChemSub 온라인(글리신).
- 나사의 과학자들은 나사의 스타더스트 우주선에 의해 돌아온 와일드 2 혜성의 샘플에서 생명체의 기본 구성 요소인 글리신을 발견했습니다.