세린
Serine
| |||
| | |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 세린 | |||
| 기타 이름 2-아미노-3-히드록시프로판산 | |||
| 식별자 | |||
3D 모델(JSmol) |
| ||
| 체비 |
| ||
| 첸블 |
| ||
| 켐스파이더 | |||
| 드러그뱅크 |
| ||
| ECHA 정보 카드 | 100.000.250 | ||
| EC 번호 |
| ||
| |||
| 케그 | |||
PubChem CID | |||
| 유니 |
| ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 속성[2] | |||
| C3H7NO3 | |||
| 몰 질량 | 105.093 g/120−1 | ||
| 외모 | 흰 결정 또는 가루 | ||
| 밀도 | 1.603g/cm3(22°C) | ||
| 녹는점 | 246°C(475°F, 519K) 분해 | ||
| 용해성의 | |||
| 산도(pKa) | 2.21(디옥실), 9.15(디옥실)[1] | ||
| 보충 데이터 페이지 | |||
| Serine(데이터 페이지) | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
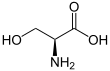
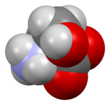
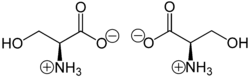
세린(Sembol Ser 또는 S)[3][4]은 단백질 생합성에 사용되는 α-아미노산이다.α-아미노기(생물학적 조건 하에서 양성자화+
3 -NH 형태), 카르복실기(생물학적 조건 하에서 탈양성자화 -COO 형태) 및 히드록시메틸기로 이루어진 측쇄를 함유하여 극성 아미노산으로 분류한다.그것은 정상적인 생리 상황에서 인체에서 합성될 수 있으며, 필수 아미노산이 아닙니다.코돈 UCU, UCC, UCA, UCG, AGU 및 AGC에 의해 부호화됩니다.
발생.
이 화합물은 자연적으로 발생하는 단백질 생성 아미노산 중 하나이다.L-스테레오 이성질체만이 단백질에서 자연적으로 나타난다.그것은 글리신을 포함한 다른 대사물로부터 체내에서 합성되기 때문에 인간의 식단에 필수적이지 않다.세린은 1865년 에밀 크레이머에 [5]의해 특히 풍부한 공급원인 실크 단백질로부터 처음 얻어졌다.이것의 이름은 비단인 세리쿰을 뜻하는 라틴어에서 유래되었다.세린의 건물은 [6]1902년에 세워졌다.단백질 중 L-serine 함량이 높은 식품원에는 달걀, 에다마메, 양고기, 간, 돼지고기, 연어, 정어리, 미역, [7][8]두부 등이 있다.
생합성
세린의 생합성은 포스포글리세린산 탈수소효소(EC 1.1.1.95)에 의해 3-포스포히드록시피루브산 및 NADH로 산화되면서 시작된다.포스포세린 트랜스아미나아제(EC2.6.1.52)에 의한 이 케톤의 환원아미네이션(트랜스아미네이션)은 3-포스페린(O-포스페린)을 생성하며, 포스포세린 포스파타아제(EC3.1.3)[9][10]에 의해 세린으로 가수분해된다.
대장균과 같은 박테리아에서 이러한 효소는 유전자 serA(EC 1.1.1.95), serC(EC 2.6.1.52) 및 serB(EC 3.1.3.3)[11]에 의해 암호화된다.
글리신 생합성:또한 세린히드록시메틸전달효소(SHMT=세린트랜스히드록시메틸라아제)는 L-세린에서 글리신으로의 가역변환(γ-알돌분해효소) 및 5,6,7,8-테트라히드로폴산염에서 5,10-메틸렌테트라히드로폴산(MTHF)(가수분해효소)[12]으로의 가역변환을 촉매한다.SHMT는 피리독살인산(PLP) 의존성 효소이다.글리신은 또한 글리신합성효소에 [9]의해 촉매되는 반응으로 CO4+ NH 및 mTHF로부터 형성될2, 수 있다.
합성 및 공업 생산
공업적으로 히드록시메틸전달효소에 [13]의해 촉매되는 글리신 및 메탄올로부터 L-세린을 제조한다.
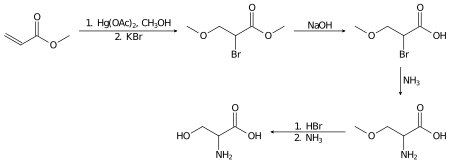
라세미크 세린은 몇 가지 [14]단계로 실험실에서 아크릴산메틸로부터 제조할 수 있습니다.
생물학적 기능
대사
세린은 퓨린과 피리미딘의 생합성에 관여한다는 점에서 신진대사에 중요하다.그것은 박테리아에서 트립토판뿐만 아니라 글리신, 시스테인을 포함한 여러 아미노산의 전구체이다.또한 스핑고리피드와 [citation needed]생합성에서 1탄소 조각의 주요 공여자인 엽산을 포함한 수많은 다른 대사물의 전구체이다.
시그널링
L-세린(그들의 에난티오머)의 세린 라세마아제에 의해 뉴런에서 합성된 D-세린은 NMDA 수용체를 공활성화함으로써 신경조절제 역할을 하며, NMDA 수용체가 글루탐산염에도 결합하면 개방될 수 있다.D-세린은 NMDA-글루탐산 수용체(NMDAR)의 글리신 부위(NR1)에서 강력한 작용제이다.수용체가 열리기 위해서는 글루탐산염과 글리신 또는 D-세린 중 하나가 결합되어야 하며, 또한 모공 차단제가 결합되어서는 안 된다(예2+2+:[15] Mg 또는 Zn).실제로 D-세린은 글리신 [16][17]자체보다 NMDAR의 글리신 부위에서 더 강력한 작용제이다.
D-세린은 비교적 최근까지 박테리아에만 존재하는 것으로 생각되었다; 그것은 D-아스파르트산염의 발견 직후 뇌에서 신호 분자로 존재하는, 자연적으로 사람에게 존재하는 것으로 발견된 두 번째 D 아미노산이었다.D 아미노산이 더 빨리 사람에게서 발견되었더라면, NMDA 수용체의 글리신 부위는 대신 D-세린 [18]부위로 명명되었을 것이다.중추신경계 외에도 D-세린은 연골,[19] 신장,[20] 말초 조직과 기관(예: 연골,[21] 신장, 말단)에서 신호 역할을 한다.
미각
퓨어 D-세린은 매우 희미한 곰팡이 향이 나는 오프 화이트 크리스털 파우더입니다.D-Serine은 중농도 및 [22]고농도에서 약간의 신맛을 더하여 달콤합니다.
임상적 의의
세린 결핍 장애는 아미노산 L-세린의 생합성에 있어 드문 결함이다.현재 세 가지 장애가 보고되었습니다.
- 3-포스포글리세린산탈수소효소결핍증
- 3-글루세린인산가수분해효소결핍증
- 포스포세린아미노전달효소결핍증
이러한 효소 결함은 선천성 소두증 및 심각한 정신운동 지체와 같은 심각한 신경학적 증상으로 이어지며, 또한 난치성 발작에 대한 3-포스포글리세린산탈수소효소 결핍증 환자에게도 나타난다.이러한 증상은 L-세린(때로는 글리신과 [23][24]결합)을 사용한 치료에 따라 다양한 정도로 반응합니다.치료에 대한 반응은 다양하며 장기적이고 기능적인 결과는 알려져 있지 않습니다.역학, 유전자형/표현형 상관관계 및 이러한 질환의 결과에 대한 이해를 개선하기 위한 기반을 제공하고, 진단 및 치료 전략을 평가하기 위해 비영리 신경전달물질에 대한 국제작업그룹(International Working Group on Neuro transmitters)이 환자 등록부를 구축했다. 관련 장애(iNTD).[25]
세린 생합성 장애 외에도, 세린 생합성 장애의 수송도 방해될 수 있다.한 가지 예는 경련성 사지마비증, 얇은 뇌량, 중성 아미노산 운반체 A의 기능에 영향을 미치는 돌연변이에 의해 야기되는 질병인 진행성 소두증이다.
치료용 연구
인간과 같은 척추동물이 [26]평생 동안 항상 최적의 양을 합성할 수 없기 때문에 L-세린의 비필수 아미노산 분류는 조건부로 간주되어 왔다.L-세린의 안전성은 근위축성 측삭경화증, ALS, 환자(ClinicalTrials.gov 식별자: NCT01835782)[27][28]를 대상으로 FDA가 승인한 인간 1상 임상시험에서 입증되었지만 ALS 증상에 대한 치료법은 아직 나타나지 않았다.2011년 메타 분석에서 보조 사르코신은 정신분열증의 [29]음성 및 전체 증상에 중간 크기의 효과인 것으로 밝혀졌다.또한 Lserserine이 [30]당뇨병에서 치료적 역할을 획득할 수 있다는 증거가 있다.
D-Serine은 [31]정신분열증의 잠재적 치료제로서 설치류에서 연구되고 있다.D-Serine은 또한 AD 환자의 [32]뇌척수액에서 상대적으로 높은 농도로 인해 조기 알츠하이머병(AD) 진단을 위한 잠재적 바이오마커로 묘사되어 왔다.
D-Serine은 청각 상실과 [33]이명 같은 감각성 청각 장애의 잠재적 치료제로 이론화되어 왔다.
「 」를 참조해 주세요.
- 이소세린
- 호모세린(이소트레오닌)
- 세린옥타머 클러스터
레퍼런스
- ^ 도슨, R.M.C. 등, 옥스퍼드, Clarendon Press, 1959년, Data for Phiothemical Research.
- ^ Weast RC, ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-512. ISBN 0-8493-0462-8.
- ^ "Nomenclature and Symbolism for Amino Acids and Peptides". IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. Archived from the original on 9 October 2008. Retrieved 5 March 2018.
- ^ 를 클릭합니다"Nomenclature and symbolism for amino acids and peptides (IUPAC-IUB Recommendations 1983)", Pure Appl. Chem., 56 (5): 595–624, 1984, doi:10.1351/pac198456050595.
- ^ "Ueber die Bestandtheile der Seide". Journal für praktische Chemie 96.
- ^ "Serine". The Columbia Encyclopedia 6th ed. encyclopedia.com. Retrieved 22 October 2012.
- ^ Brain Chemistry Labs 웹사이트
- ^ 자가 영양 데이터 웹 사이트
- ^ a b Stryer L (1988). Biochemistry (3rd ed.). New York: W.H. Freeman. p. 580. ISBN 978-0-7167-1843-7.
- ^ KEGG EC 3.1.3 등
- ^ 유니프로트: serB
- ^ Lehninger AL, Nelson DL, Cox MM (2000). Principles of Biochemistry (3rd ed.). New York: W. H. Freeman. ISBN 1-57259-153-6.
- ^ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker (2006). Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a02_057.pub2.
{{cite encyclopedia}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Carter HE, West HD (1940). "dl-Serine". Org. Synth. 20: 81. doi:10.15227/orgsyn.020.0081.
- ^ Liu Y, Hill RH, Arhem P, von Euler G (2001). "NMDA and glycine regulate the affinity of the Mg2+-block site in NR1-1a/NR2A NMDA receptor channels expressed in Xenopus oocytes". Life Sciences. 68 (16): 1817–26. doi:10.1016/S0024-3205(01)00975-4. PMID 11292060.
- ^ MacKay, Mary-Anne B.; Kravtsenyuk, Maryana; Thomas, Rejish; Mitchell, Nicholas D.; Dursun, Serdar M.; Baker, Glen B. (6 February 2019). "D-Serine: Potential Therapeutic Agent and/or Biomarker in Schizophrenia and Depression?". Frontiers in Psychiatry. 10: 25. doi:10.3389/fpsyt.2019.00025. ISSN 1664-0640. PMC 6372501. PMID 30787885.
D-Serine is more potent than glycine as a coagonist at the NMDA receptor, has a regional distribution in the brain that is similar to that of NMDA receptors and appears to be more closely associated with synaptic NMDA receptors than glycine (which is more closely associated with non-synaptic NMDA receptors).
- ^ Wolosker, Herman; Balu, Darrick T. (9 June 2020). "d-Serine as the gatekeeper of NMDA receptor activity: implications for the pharmacologic management of anxiety disorders". Translational Psychiatry. 10 (1): 184. doi:10.1038/s41398-020-00870-x. ISSN 2158-3188. PMC 7283225. PMID 32518273.
D-serine is functionally a more potent activator of synaptic NMDARs than glycine, and mounting evidence suggests that it serves as the major NMDAR co-agonist in limbic brain regions implicated in neuropsychiatric disorders.
- ^ Mothet JP, Parent AT, Wolosker H, Brady RO, Linden DJ, Ferris CD, Rogawski MA, Snyder SH (Apr 2000). "D-serine is an endogenous ligand for the glycine site of the N-methyl-D-aspartate receptor". Proceedings of the National Academy of Sciences of the United States of America. 97 (9): 4926–31. Bibcode:2000PNAS...97.4926M. doi:10.1073/pnas.97.9.4926. PMC 18334. PMID 10781100.
- ^ Takarada T, Hinoi E, Takahata Y, Yoneda Y (May 2008). "Serine racemase suppresses chondrogenic differentiation in cartilage in a Sox9-dependent manner". Journal of Cellular Physiology. 215 (2): 320–8. doi:10.1002/jcp.21310. PMID 17929246. S2CID 45669104.
- ^ Ma MC, Huang HS, Chen YS, Lee SH (Nov 2008). "Mechanosensitive N-methyl-D-aspartate receptors contribute to sensory activation in the rat renal pelvis". Hypertension. 52 (5): 938–44. doi:10.1161/HYPERTENSIONAHA.108.114116. PMID 18809793.
- ^ Ghasemi M, Rezania F, Lewin J, Moore KP, Mani AR (Jun 2010). "d-Serine modulates neurogenic relaxation in rat corpus cavernosum". Biochemical Pharmacology. 79 (12): 1791–6. doi:10.1016/j.bcp.2010.02.007. PMID 20170643.
- ^ Kawai M, Sekine-Hayakawa Y, Okiyama A, Ninomiya Y (Dec 2012). "Gustatory sensation of (L)- and (D)-amino acids in humans". Amino Acids. 43 (6): 2349–58. doi:10.1007/s00726-012-1315-x. PMID 22588481. S2CID 17671611.
- ^ de Koning TJ (April 2006). "Treatment with amino acids in serine deficiency disorders". Journal of Inherited Metabolic Disease. 29 (2): 347–351. doi:10.1007/s10545-006-0269-0. PMID 16763900. S2CID 25013468.
- ^ Tabatabaie L; Klomp LW; Berger R; de Koning TJ (March 2010). "L-serine synthesis in the central nervous system: a review on serine deficiency disorders". Mol Genet Metab. 99 (3): 256–262. doi:10.1016/j.ymgme.2009.10.012. PMID 19963421.
- ^ "Patient registry".
- ^ Metcalf, J. S.; Dunlop, R. A.; Powell, J. T.; Banack, S. A.; Cox, P. A. (2017). "L-Serine: a Naturally-Occurring Amino Acid with Therapeutic Potential". Neurotoxicity Research. 33 (1): 213–221. doi:10.1007/s12640-017-9814-x. ISSN 1029-8428. PMID 28929385. S2CID 20271849.
- ^ Dunlop RA, Cox PA, Banack SA, Rodgers KJ (2013). "The non-protein amino acid BMAA is misincorporated into human proteins in place of L-serine causing protein misfolding and aggregation". PLOS ONE. 8 (9): e75376. Bibcode:2013PLoSO...875376D. doi:10.1371/journal.pone.0075376. PMC 3783393. PMID 24086518.
- ^ Levine, Todd D.; Miller, Robert G.; Bradley, Walter G.; Moore, Dan H.; Saperstein, David S.; Flynn, Lynne E.; Katz, Jonathan S.; Forshew, Dallas A.; Metcalf, James S.; Banack, Sandra A.; Cox, Paul A. (2017-01-02). "Phase I clinical trial of safety of L-serine for ALS patients". Amyotrophic Lateral Sclerosis and Frontotemporal Degeneration. 18 (1–2): 107–111. doi:10.1080/21678421.2016.1221971. ISSN 2167-8421. PMID 27589995. S2CID 4584977.
- ^ Singh SP, Singh V (Oct 2011). "Meta-analysis of the efficacy of adjunctive NMDA receptor modulators in chronic schizophrenia". CNS Drugs. 25 (10): 859–85. doi:10.2165/11586650-000000000-00000. PMID 21936588. S2CID 207299820.
- ^ Holm, Laurits J.; Buschard, Karsten (2019). "L‐serine: a neglected amino acid with a potential therapeutic role in diabetes". APMIS. 127 (10): 655–659. doi:10.1111/apm.12987. ISSN 0903-4641. PMC 6851881. PMID 31344283.
- ^ Balu DT, Li Y, Puhl MD, Benneyworth MA, Basu AC, Takagi S, Bolshakov VY, Coyle JT (Jun 2013). "Multiple risk pathways for schizophrenia converge in serine racemase knockout mice, a mouse model of NMDA receptor hypofunction". Proceedings of the National Academy of Sciences of the United States of America. 110 (26): E2400-9. Bibcode:2013PNAS..110E2400B. doi:10.1073/pnas.1304308110. PMC 3696825. PMID 23729812.
- ^ Madeira C, Lourenco MV, Vargas-Lopes C, Suemoto CK, Brandão CO, Reis T, Leite RE, Laks J, Jacob-Filho W, Pasqualucci CA, Grinberg LT, Ferreira ST, Panizzutti R (May 5, 2015). "d-serine levels in Alzheimer's disease: implications for novel biomarker development". Translational Psychiatry. 5 (5): e561. doi:10.1038/tp.2015.52. PMC 4471283. PMID 25942042.
- ^ Wang, Jing; Serratrice, Nicolas; Lee, Cindy J.; François, Florence; Sweedler, Jonathan V.; Puel, Jean-Luc; Mothet, Jean-Pierre; Ruel, Jérôme (17 December 2021). "Physiopathological Relevance of D-Serine in the Mammalian Cochlea". Frontiers in Cellular Neuroscience. Frontiers Media SA. 15: 733004. doi:10.3389/fncel.2021.733004. ISSN 1662-5102. PMC 8718999. PMID 34975405.