바르비투레이트
Barbiturate
바르비투레이트는[a] 바르비투르산에서 화학적으로 파생된 우울증 약물의 한 종류입니다.[2] 그들은 의학적으로 불안제, 최면제, 항경련제로 사용될 때 효과적이지만 신체적, 심리적 중독 가능성뿐만 아니라 다른 가능한 부작용 중에서도 과다 복용 가능성이 있습니다. 항불안제 및 진정 효과로 오락적으로 사용되어 왔으며 따라서 이러한 사용과 관련된 위험으로 인해 대부분의 국가에서 통제되고 있습니다.
바르비투레이트는 주로 일상적인 의료 행위, 특히 불안 장애 및 불면증 치료에서 벤조디아제핀과 비벤조디아제핀("Z-drugs")으로 대체되었습니다. 이는 과다 복용 위험이 현저히 낮고 바르비투레이트 과다 복용에 대한 해독제가 없기 때문입니다. 그럼에도 불구하고, 바르비투레이트는 여전히 다양한 용도로 사용되고 있습니다. 전신마취, 뇌전증, 급성 편두통 또는 군집성 두통의 치료, 급성 긴장성 두통, 안락사, 사형, 조력자살.
사용하다
약
페노바르비탈과 같은 바르비투레이트는 오랫동안 불안제와 최면제로 사용되었습니다. 중간 작용 바르비투레이트는 잠드는 시간을 줄이고 총 수면 시간을 늘리고 REM 수면 시간을 줄입니다. 오늘날 이러한 목적으로 벤조디아제핀으로 대체된 것은 벤조디아제핀이 약물 과다복용 시 독성이 약하기 때문입니다.[4][5][6] 그러나 바르비투레이트는 여전히 항경련제(예: 페노바르비탈 및 프리미돈) 및 전신 마취제(예: 티오펜탈 나트륨)로 사용됩니다.
고용량의 바르비투레이트는 사망 시 의료 지원, 안락사 및 치명적인 주사에 의한 사형을 위해 근육 이완제와 함께 사용됩니다.[7][8] 바르비투레이트는 소동물 수의학에서 안락사제로 자주 사용됩니다.
취조
소듐 티오펜탈은 소듐 펜토탈이라는 이름으로 판매되는 초단작용 바르비투레이트입니다. 진정제와 불면증 치료에 사용되는 중간 작용 바르비투레이트인 "진실 혈청" 또는 나트륨 아미탈로 오인되는 경우가 많지만, 소위 나트륨 아미탈 "인터뷰"에서도 사용되었는데, 여기서 피조사자가 약물의 영향을 받은 상태에서 진실을 제공할 가능성이 더 높다고 잘못 생각됩니다.[9] 물에 녹였을 때 아미탈나트륨을 삼키거나 정맥주사로 투여할 수 있습니다. 이 약은 그 자체로 사람들에게 진실을 말하도록 강요하는 것이 아니라, 억제력을 감소시키고 창의적인 사고를 늦추는 것으로 생각되어 피험자들이 질문을 받을 때 허를 찔릴 가능성이 높아지고, 감정 폭발을 통해 피험자가 정보를 드러낼 가능성이 높아집니다. 거짓말은 진실을 말하는 것보다 다소 복잡하며, 특히 진정제-저혈압 약물의 영향을 받습니다.[10]
나트륨 티오펜탈에 의해 유발되는 기억력 손상 효과와 인지 장애는 피험자의 거짓말을 발명하고 기억하는 능력을 감소시키는 것으로 생각됩니다. 이러한 관행은 더 이상 법적으로 허용되지 않는 것으로 간주됩니다. 왜냐하면 이러한 심문을 받는 대상자들이 잘못된 기억을 형성하여 그러한 방법을 통해 얻은 모든 정보의 신뢰성에 의문을 제기할 수 있다는 결과 때문입니다. 그럼에도 불구하고, 특정한 상황에서 국방 및 법 집행 기관에서 고문 심문의 "인간적인" 대안으로 사용되는 것은 피조사자가 전술을 사용하는 국가 또는 기관의 안전에 중요한 정보를 가지고 있다고 판단되는 경우입니다.[11]
화학
1988년 6개의 상보적 수소 결합에 의한 인공 수용체 결합 바르비투레이트의 합성 및 결합 연구가 발표되었습니다.[12] 이 첫 번째 기사 이후로 물질과 분자 장치의 개념에서 약물로서의 효율성이 아니라 초분자 화학에 적용하기 위해 다양한 종류의 수용체뿐만 아니라 다양한 바르비투레이트와 시아누레이트가 설계되었습니다.
염기 화합물인 바르비투르산의 바람직한 IUPAC 명칭은 1,3-디아지난-2,4,6-트리오네입니다. 서로 다른 바르비투레이트는 기본 구조에서 서로 다른 치환기를 갖는데, 주로 고리의 5번 위치에 있습니다.[13] 현대 화학에서 바르비투레이트는 종종 크리스탈 익스플로러 프로그램으로 계산된 분자 간 상호 작용[1]을 보여주는 Hirshfeld 표면 표현에 의해 제시됩니다.

나트륨 바르비탈과 바르비탈은 또한 면역 전기영동 또는 고정 용액과 같은 생물학적 연구를 위한 pH 완충제로 사용되었습니다.[14][15]
분류
Barbiturate는 작업 기간에 따라 분류됩니다. 각 클래스의 예는 다음과 같습니다.[16]
- 초단파 연기(30분) : 티오펜톤, 메토헥시톤
- 단작용(2시간) : 헥소바비톤, 사이클로바비톤, 펜토바비톤, 세코바비톤
- 중간연기(3~6시간) : 모바비톤, 부타비톤
- 장시간 연기(6시간) : 페노바르비톤
적응증
바르비투레이트의 사용에 대한 표시는 다음과 같습니다.[17]
- 압류
- 신생아탈락증후군
- 불면증
- 불안.
- 마취유도
부작용

고령자와 임신한 여성에게 고려해야 할 특별한 위험이 있습니다. 사람이 나이가 들면, 신체는 바르비투레이트를 제거할 수 없게 됩니다. 그 결과 65세 이상의 사람들은 약물 의존과 우발적인 과다 복용을 포함한 바르비투레이트의 해로운 영향을 경험할 위험이 더 높습니다.[19] 임신 중 바르비투레이트를 복용하면 약물이 태반을 거쳐 태아에게 전달됩니다. 아기가 태어난 후에는 금단 증상이 나타나 호흡곤란을 겪을 수 있습니다. 또한, 바비투레이트를 복용하는 수유부는 모유를 통해 아기에게 약을 전달할 수 있습니다.[20] 바르비투레이트에 대한 드문 이상 반응은 스티븐스-주로 점막에 영향을 주는 존슨 증후군.
공통부작용
- 메스꺼움
- 저혈압
- 두통.
- 졸음
- 피부발진
심각한 부작용
- 혼란
- 코마
- 환각
- 실신
- 느린 호흡[21]
드문 부작용
관용과 의존성
정기적으로 사용하면 바르비투레이트의 효과에 대한 내성이 발달합니다. 연구에 따르면 바르비투레이트를 한 번만 투여해도 내성이 발생할 수 있습니다. 모든 GABAergic 약물과 마찬가지로 바르비투레이트 금단은 GABA 작용의 더 직접적인 메커니즘이 알코올 또는 벤조디아제핀보다 바르비투레이트 금단을 훨씬 더 심각하게 만들지만 섬망 트레멘스 및 벤조디아제핀 금단을 연상시키는 방식으로 발작과 같은 잠재적인 치명적인 영향을 생성합니다. 그것은 알려진 중독 물질 중 가장 위험한 금단 물질 중 하나로 여겨집니다. 벤조디아제핀과 유사하게, 더 긴 작용 바르비투레이트는 짧은 작용 및 초단 작용 바르비투레이트보다 덜 심각한 금단 증후군을 생성합니다. 금단 증상은 용량 의존적이며, 더 무거운 사용자는 저용량 중독자보다 더 큰 영향을 받습니다.
바르비투레이트 금단의 약리학적 치료는 종종 환자를 지속적으로 작용하는 벤조디아제핀(즉, 발륨)으로 전환한 다음 벤조디아제핀을 천천히 테이퍼링하는 확장 과정으로 구성됩니다. 바비투레이트에 대한 정신적 갈망은 경우에 따라 몇 달 또는 몇 년 동안 지속될 수 있으며 중독 전문가들은 상담/지원 그룹을 강력히 권장합니다. 환자는 높은 치사율과 비교적 갑작스러운 금단의 시작으로 인해 의사와 상의하지 않고 바비투레이트를 중단하는 작업을 시도해서는 안 됩니다. "콜드 칠면조"를 그만두려고 시도하면 흥분독성으로 인한 신경학적 손상, 경련 중 받는 심각한 신체적 손상, 심지어 그랑드말 발작 중 부정맥으로 인한 사망까지 발생할 수 있으며, 섬망 트레멘에 의한 사망과 유사합니다.[citation needed]
과다 복용
과다 복용의 일부 증상은 일반적으로 부진, 조정, 사고의 어려움, 말의 느림, 판단의 잘못, 졸음, 얕은 호흡, 비틀거림, 심할 경우 혼수 상태나 사망을 포함합니다. 바르비투레이트의 치사량은 내성에 따라 그리고 개인마다 크게 다릅니다. 치사량은 클래스 구성원 간에 매우 다양하며, 펜토바르비탈과 같은 초강력 바르비투레이트는 부탈비탈과 같은 저효능 바르비투레이트보다 상당히 낮은 용량으로 잠재적으로 치명적입니다. 의존성이 발현된 후 약물을 중단했을 때 위험하고 불쾌한 금단 증상이 나타날 수 있기 때문에 입원 환경에서도 내성 발생은 여전히 문제입니다. 바르비투레이트의 불안성 및 진정 효과에 대한 내성은 평활근, 호흡 및 심박수에 대한 효과에 대한 내성보다 더 빠르게 발생하는 경향이 있어 일반적으로 장기간 정신 의학적 사용에 적합하지 않습니다. 항경련 효과에 대한 내성은 생리학적 효과에 대한 내성과 더 상관관계가 있는 경향이 있지만, 이는 장기적인 뇌전증 치료를 위해 여전히 실행 가능한 옵션임을 의미합니다.
다른 중추신경계(중앙신경계) 억제제(예: 알코올, 아편, 벤조디아제핀)와 함께 과다 복용하는 바르비투레이트는 추가적인 중추신경계 및 호흡 억제제 효과로 인해 훨씬 더 위험합니다. 벤조디아제핀의 경우, 부가 효과를 가질 뿐만 아니라, 바르비투레이트는 벤조디아제핀 결합 부위의 결합 친화력을 증가시켜, 과장된 벤조디아제핀 효과를 초래합니다(ex. 벤조디아제핀이 채널 개방 빈도를 300% 증가시키고, 바르비투레이트가 채널 개방 지속 시간을 300% 증가시킨다면, 그러면 약물의 복합적인 효과는 채널의 전체 기능을 600%가 아닌 900% 증가시킵니다.
가장 오래 작용하는 바르비투레이트는 하루 또는 그 이상의 반감기를 가지며, 그 후 시스템에서 약물의 생체 축적을 초래합니다. 지속적으로 작용하는 바르비투레이트의 치료적, 오락적 효과는 약물보다 훨씬 빨리 사라집니다. 사용자가 약물의 혈장 결합 농도로부터 거의 또는 전혀 영향을 느끼지 않음에도 불구하고 반복 투여 후(치료제 또는 처방된 용량으로 복용한 경우에도) 약물이 혈중 독성 농도에 도달할 수 있도록 허용합니다. 약물의 효과가 끝난 후 알코올이나 다른 진정제를 섭취하는 사용자는 시스템이 제거되기 전에 다른 진정제로부터 매우 과장된 효과를 경험할 수 있으며, 이는 무력화되거나 심지어 치명적일 수 있습니다.
바르비투레이트는 많은 간 CYP 효소(특히 CYP2C9, CYP2C19 및 CYP3A4)를 유도하여 [22]많은 전구약물에서 과장된 효과를 초래하고 이러한 효소에 의해 비활성 대사산물로 대사되는 약물에서 감소된 효과를 초래합니다. 이는 CYP 효소에 의해 대사된 후 상당히 강력해지는 코데인, 트라마돌, 카리소프로돌과 같은 약물로 인해 치명적인 과다 복용을 초래할 수 있습니다. 클래스의 모든 알려진 구성원들이 관련된 효소 유도 능력을 가지고 있지만, 전반적으로 유도 정도와 각 특정 효소에 미치는 영향은 광범위하며, 페노바르비탈과 세코바르비탈은 가장 강력한 효소 유도제이고 부탈탈과 탈부탈은 클래스에서 가장 약한 효소 유도제 중 하나입니다.
바르비투르산 과다복용으로 스스로 목숨을 끊은 것으로 알려진 사람들로는 스테판 즈바이그, 찰스 보이어, 루안 링유, 달리다, 진느 데커스, 펠릭스 하우스도르프, 애비 호프만, 필리스 하이먼, C. P. 라마누잠, 조지 샌더스, 장 세버그, 뤼프 벨레즈와 헤븐스 게이트 컬트 회원들이 있습니다. 바르비투레이트 과다복용의 결과로 사망한 다른 사람들로는 피어 안젤리, 브라이언 엡스타인, 주디 갈랜드, 지미 헨드릭스, 마릴린 먼로, 잉거 스티븐스, 디나 워싱턴, 엘렌 윌킨슨, 앨런 윌슨이 있습니다. 어떤 경우에는 이것들도 자살로 추측되었습니다. 바르비투레이트와 다른 약물의 조합으로 사망한 사람들은 레이너 베르너 파스빈더, 도로시 킬갤런, 말콤 라우리, 에디 세지윅, 케네스 윌리엄스 등이 있습니다. 도로시 댄드리지는 약물 과다 복용이나 관련 없는 색전증으로 사망했습니다. 잉게보르 바흐만은 바르비투르산 금단의 결과로 사망했을 수도 있습니다(그녀는 화상으로 입원했고, 의사들은 그녀의 바르비투르산 중독을 인지하지 못했습니다).
금지사항
Barbiturate의 사용은 다음과 같은 조건에서 금지됩니다.
- 바리게이트 포르피리아 (바비투레이트에 의한 포르피리아 합성에 필요한 효소의 유도 때문)
- 천식 상태(바비투레이트로 인한 호흡 저하로 인한 것)[23]
작용기전
바르비투레이트는 양성 알로스테릭 조절제로 작용하고, 더 높은 용량에서는 GABAA 수용체의 작용제로 작용합니다.[24] GABA는 포유류 중추신경계(CNS)의 주요 억제 신경전달물질입니다. 바르비투레이트는 GABA 자체와 구별되고 또한 벤조디아제핀 결합 부위와도 구별되는 결합 부위인 [25]소단위 계면에 위치한 다수의 상동 막횡단 포켓에서 GABAA 수용체에 결합합니다. 벤조디아제핀과 마찬가지로 바르비투레이트는 이 수용체에서 GABA의 효과를 강화합니다. 이 GABAergic 효과 외에도 바르비투레이트는 이온성 글루타메이트 수용체의 하위 유형인 AMPA 및 카인산염 수용체도 차단합니다. 글루타메이트는 포유류 중추신경계의 주요 흥분성 신경전달물질입니다. 종합하면, 바르비투레이트가 억제 GABAA 수용체를 강화하고 흥분성 AMPA 수용체를 억제한다는 발견은 벤조디아제핀 및 퀴나졸리논과 같은 대체 GABA 강화제에 대한 이러한 제제의 우수한 CNS 억제 효과를 설명할 수 있습니다. 고농도에서는 P/Q형 전압 의존성 칼슘 채널에 대한 영향을 통해 글루타메이트와 같은 신경전달물질의 Ca 의존성2+ 방출을 억제합니다.[26] 바르비투레이트는 GABAA 수용체에서 염화 이온 채널 개방의 지속 시간을 증가시킴으로써 약리학적 효과를 생성합니다(약리학: 이것은 GABA)의 효능을 증가시키는 반면, 벤조디아제핀은 GABAA 수용체에서 염화 이온 채널의 개방 빈도를 증가시킵니다(약력학: 이것은 GABA)의 효능을 증가시킵니다. 과용 시 벤조디아제핀에 비해 바르비투레이트의 독성이 증가하는 이유는 염화 이온 채널의 직접적인 게이팅 또는 개방 때문입니다.[27][28]
또한, 바르비투레이트는 리간드-게이트 이온 채널의 전체 슈퍼패밀리에 결합하는 비교적 비선택적인 화합물이며, 그 중 GABAA 수용체 채널은 여러 대표자 중 하나에 불과합니다. 이온 채널의 이 Cys-loop 수용체 슈퍼패밀리는 뉴런 nACh 수용체 채널, 5-HT3 수용체 채널 및 글리신 수용체 채널을 포함합니다. 그러나 GABAA 수용체 전류는 바르비투레이트(및 기타 전신 마취제)에 의해 증가하는 반면 양이온 이온에 대해 주로 투과되는 리간드-게이트 이온 채널은 이러한 화합물에 의해 차단됩니다. 예를 들어, 신경 nAChR 채널은 티오펜탈 및 펜토바르비탈의 임상적으로 관련된 마취 농도에 의해 차단됩니다.[29] 이러한 발견은 (비GABA-ergic) 리간드-게이트 이온 채널, 예를 들어 신경 nAChR 채널이 바르비투레이트의 일부 (부작용) 효과를 매개한다는 것을 의미합니다.[30] 이것은 마취 농도에 사용될 때 고용량에서 바르비투레이트의 (경미한) 마취 효과를 담당하는 메커니즘입니다.
상호작용
바르비투레이트와의 약물 상호작용은 다음과 같습니다.[21]
- 술
- 오피오이드
- 벤조디아제핀
- 항응고제
- 항히스타민제
- atazanavir
- 피임약
- 보세프레비르
주의
다음을 사용하는 사람에게는 주의가 필요합니다.[21]
- 오피오이드 또는 벤조디아제핀과 같은 약물
- 술
다음 환자의 경우에도 주의가 필요합니다.
- 천식
- 신장 또는 간 문제
- 심장병
- 물질사용장애
- 우울증.
- 자살생각력
역사
바르비투르산은 1864년 11월 27일 독일의 화학자 아돌프 폰 바이어에 의해 처음 합성되었습니다. 이것은 요소를 디에틸 말로네이트로 응축함으로써 수행되었습니다. 그 물질이 어떻게 그 이름을 갖게 되었는지에 대해서는 여러 가지 이야기가 있습니다. 가장 유력한 이야기는 배이어와 그의 동료들이 그들의 발견을 축하하러 마을의 포병 수비대가 포병들의 수호성인인 성 바바라의 축제를 축하하고 있는 선술집에 갔다는 것입니다. 한 포병 장교가 바바라와 요소를 결합시켜 새로운 물질에 세례를 주었다고 합니다.[31] 또 다른 이야기는 Baeyer가 Barbara라는 이름의 뮌헨 여종업원의 소변에서 이 물질을 합성했다는 것입니다.[32] 그러나 1903년 바이엘에서 근무하는 두 명의 독일 과학자 에밀 피셔와 요제프 폰 메링이 개를 재우는 데 바르비탈이 매우 효과적이라는 것을 발견하기 전까지 의학적으로 가치 있는 물질은 발견되지 않았습니다. 바비탈은 그 후 베로날이라는 상호명으로 바이엘에 의해 시판되었습니다. 그가 아는 가장 평화로운 곳이 이탈리아의 도시 베로나였기 때문에 메링이 이 이름을 제안했다고 합니다.[31]
1950년대에 와서야 바르비투레이트의 행동 장애와 물리적 의존 가능성이 인정되었습니다.[33]
바르비투르산 자체는 중추신경계에 직접적인 영향을 미치지 않으며, 화학자들은 그로부터 약리활성 특성을 가진 2,500개 이상의 화합물을 유도했습니다. 바르비투레이트의 광범위한 등급은 발병 속도와 활동 기간에 따라 더 세분화되고 분류됩니다. 초단작용 바르비투레이트는 작용 기간이 매우 짧기 때문에 더 큰 조절이 가능하기 때문에 마취에 일반적으로 사용됩니다. 이러한 속성을 통해 의사는 응급 수술 상황에서 환자를 신속하게 "아래"에 넣을 수 있습니다. 또한 수술 중 합병증이 발생할 경우 의사는 환자를 마취에서 빨리 꺼낼 수 있습니다. 바르비투레이트의 중간 두 부류는 종종 "짧은/중간 연기"라는 제목으로 결합됩니다. 이 바르비투레이트는 마취 목적으로도 사용되며 때로는 불안이나 불면증을 위해 처방되기도 합니다. 그러나 바르비투레이트의 장기간 사용의 위험으로 인해 더 이상 일반적인 관행이 아닙니다. 수면을 위해 벤조디아제핀과 졸피뎀, 잘레플론, 에조피클론과 같은 Z-약물로 대체되었습니다. 바르비투레이트의 최종 등급은 지속 작용 바르비투레이트로 알려져 있습니다(가장 주목할 만한 것은 페노바르비탈로 반감기는 약 92시간입니다). 이 종류의 바르비투레이트는 거의 독점적으로 항경련제로 사용되지만 드물게 주간 진정제로 처방됩니다. 이 수업에서 바르비투레이트는 불면증에 사용되지 않습니다. 왜냐하면, 극도로 긴 반감기 때문에, 환자들은 잔류적인 "숙취" 효과로 잠에서 깨어나서 우울함을 느낄 것이기 때문입니다.
바르비투레이트는 대부분의 경우 유리산으로 사용되거나 나트륨, 칼슘, 칼륨, 마그네슘, 리튬 등의 염으로 사용될 수 있습니다. 바르비투르산의 코데인 및 디오니인계 염이 개발되었습니다. 1912년 바이엘은 루미날이라는 상품명으로 또 다른 바르비투르산 유도체인 페노바르비탈을 진정제-저혈압제로 소개했습니다.[34]
사회와 문화
법적 지위
제2차 세계 대전 동안 태평양 지역의 군인들은 일상적인 근무 조건의 더위와 습도에 대한 내성을 향상시키기 위해 "구프볼"을 받았습니다. Goofball은 혈압을 유지할 뿐만 아니라 호흡기에 대한 수요를 줄였습니다. 많은 군인들이 제대 전 몇 달간의 재활이 필요한 중독증을 가지고 돌아갔습니다. 이것은 의존성 문제를 증가시켰고, 종종 1950년대와 1960년대를 통해 알려지지 않은 환자에게 고용량을 처방하는 무관심한 의사들에 의해 악화되었습니다.[citation needed]
1950년대 후반과 1960년대에 바르비투르산 과다 복용과 의존성 문제에 대한 발표된 보고서가 증가하면서 의사들은 특히 가짜 요청에 대한 처방을 줄였습니다. 이것은 결국 통제 약물로서 바르비투레이트의 일정으로 이어졌습니다.
네덜란드에서 아편법은 목록 I에 있는 세코바르비탈을 제외하고 모든 바르비투레이트를 목록 II 약물로 분류하고 있습니다.
List II 의약품에는 의사가 List I 의약품과 동일하고 엄격한 지침에 따라 처방전을 작성해야 하는 소규모 그룹이 있습니다(처방서를 문자로 작성하고 환자 이름을 나열하며 이름과 이니셜, 주소를 포함해야 함). 처방전을 발급하는 허가된 처방전자의 도시 및 전화번호, 처방전이 발급되는 사람의 이름과 이니셜, 주소 및 도시). 그 약물 그룹 중에는 바르비투레이트 아모바르비탈, 부탈비탈, 사이클로바르비탈, 펜토바르비탈이 있습니다.
미국에서는 1970년의 통제 물질법에 따라 대부분의 바르비투르산을 통제 물질로 분류하고 있으며[update] 2023년 8월 현재도 그렇게 유지되고 있습니다. 바르비탈, 메틸페노바르비탈(메포바르비탈로도 알려져 있음) 및 페노바르비탈은 스케줄 IV 약물로 지정되었으며, "바비투르산 유도체의 임의의 양 또는 바르비투르산 유도체의 임의의 염을 포함하는 모든 물질"([35]다른 모든 바르비투르산)은 스케줄 III로 지정되었습니다. 원래 CSA에서는 스케줄 I, II 또는 V에 바르비투레이트가 배치되지 않았지만,[36] 아모바르비탈, 펜토바르비탈 및 세코바르비탈은 좌제 투여 형태가 아닌 한 스케줄 II 조절 물질입니다.[37]
1971년 비엔나에서 향정신성 물질에 관한 협약이 체결되었습니다. 암페타민, 바르비투레이트 및 기타 합성 물질을 규제하도록 설계된 조약의 제34판(2014년[update] 1월 25일 기준)은 세코바르비탈을 스케줄 II로, 아모바르비탈, 부탈, 사이클로바르비탈, 펜토바르비탈을 스케줄 III로, 알로바르비탈, 바르비탈, 부토바르비탈, 메포바르비탈, 페노바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부타바르비탈, 부 '그린 리스트'에 스케줄 IV로 바이닐 바이닐 바이닐탈이 있습니다.[38] 그러나 부탈탈, 카페인, 파라세타몰(아세트아미노펜) 등으로 구성된 복합제 피오리셋은 특별히 통제 물질 상태에서 면제되며, 파라세타몰 대신 아스피린을 함유하고 코데인 포스페이트를 함유할 수 있는 형제 피오리넷은 스케줄 III 약물로 남아 있습니다.
레크리에이션용
레크리에이션 사용자들은 바바리톤이 높으면 편안한 만족감과 행복감을 느낀다고 보고합니다. 신체적, 심리적 의존성 또한 반복적인 사용으로 발전할 수 있습니다.[39] 바르비투레이트의 만성 오남용은 심각한 질병과 관련이 있습니다. 한 연구에 따르면 진정제를 복용한 남성의 11%와 여성의 23%가 자살로 사망한다고 합니다.[40] 바르비투르산 중독의 다른 효과로는 졸음, 측면 및 수직 낭포, 언어 및 운동실조, 불안 감소 및 억제 상실이 있습니다. 바르비투레이트는 또한 디아제팜 및 클로나제팜과 같은 장기간 작용하는 벤조디아제핀과 유사한 방식으로 불법 약물 사용의 부작용 또는 금단 효과를 완화하기 위해 사용됩니다.[41][42] 종종 다물질 사용이 발생하며 바르비투레이트는 다른 사용 가능한 물질, 가장 일반적으로 알코올로 소비되거나 대체됩니다.
물질을 사용하는 사람들은 단작용과 중간작용의 바르비투레이트를 선호하는 경향이 있습니다.[43] 가장 많이 사용되는 것은 아모바르비탈(Amytal), 펜토바르비탈(Nembutal), 세코바르비탈(Secobarvital)입니다. 아모바르비탈과 세코바르비탈의 조합(투이날이라고 함)도 많이 사용됩니다. 단작용과 중간작용 바르비투레이트는 보통 진정제와 수면제로 처방됩니다. 이 알약들은 삼킨 지 15분에서 40분 후에 작용하기 시작하며, 그 효과는 5시간에서 6시간 동안 지속됩니다.
바비투레이트의 속어로는 바비, 바비, 파랑새, 인형, 월뱅거, 노랑, 다우너, 구더기, 수면자, '레드 & 블루스', 장난감 등이 있습니다.[44]
예
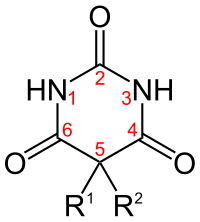
| 약칭 | R1 | R2 | IUPAC명 | 활동기간 |
|---|---|---|---|---|
| 알로바르비탈 | CH2CHCH2 | CH2CHCH2 | 5,5-diallylbarbiturate | 단막극 |
| 모바비탈[45] | CH2CH3 | (CH2)2CH(CH3)2 | 5-ethyl-5-isopentyl-barbiturate | 중급연기 |
| aprobarbital | CH2CHCH2 | CH(CH3)2 | 5-allyl-5-isopropyl-barbiturate | 중급연기 |
| 반년생의 | CH2CHCH2 | C6H5 | 5-allyl-5-phenyl-barbiturate | 중급연기 |
| 바비탈 | CH2CH3 | CH2CH3 | 5,5-diet메틸바르비투레이트 | 롱 액팅 |
| 발로바르비탈 | CH2CHCH2 | CH2CBrCH2 | 5-allyl-5-(2-bromo-allyl)-barbiturate | 단막극 |
| 펜토바르비탈[45] | CH2CH3 | CH CH3(CH2)2CH3 | 5-에틸-5-(1-메틸부틸)-바비투레이트 | 단막극 |
| 페노바르비탈[45] | CH2CH3 | C6H5 | 5-에틸-5-페닐바르비투레이트 | 롱 액팅 |
| 프리미돈 | CH2CH3 | C6H5 | 5-ethyl-5-phenyl-1,3-diazinane-4,6-dione (일반적인 바르비투레이트 구조의 2번 위치에 산소가 부족함) | 롱 액팅 |
| 제2탄두의[45] | CH2CHCH2 | CH3(CH2)2CH3 | 5-[(2R)-pentan-2-yl]-5-prop-2-enyl-barbiturate; 5-allyl-5-[(2R)-pentan-2-yl]-barbiturate | 단막극 |
| 티오펜탈의 | CH2CH3 | CH3(CH2)2CH3 | 5-에틸-5-(1-메틸부틸)-2-티오바르비투레이트 (#2 위치의 산소는 황으로 대체) | 초단발효 |
티오펜탈은 C=S 이중 결합으로 대체된 C=O 이중 결합 중 하나(옆 그림에서 탄소는 2로 표시됨)를 가진 바르비투레이트이며, R은 다음과 같습니다. CH23(에틸) 및 R3)는 CH(CH3)CH223(sec-펜틸)임. 티오펜탈은 미국에서 더 이상 사용할 수 없습니다.[46]
참고 항목
- 벤조디아제핀
- 향정신성
- Dille-Kopanyi 시약, Zwikker 시약 및 기타 바르비투레이트 스팟 테스트
설명주
참고문헌
- ^ 보, 버트, 스콧 골더. 2003. 2016년 4월 30일 Wayback Machine에 보관된 하버드 방언 조사. 케임브리지, MA: 하버드 대학교 언어학과.
- ^ Edward R. Garrett; Jacek T. Bojarski†; Gerald J. Yakatan (21 September 2006). "Kinetics of hydrolysis of barbituric acid derivatives". Journal of Pharmaceutical Sciences. 60 (8): 1145–54. doi:10.1002/jps.2600600807. PMID 5127086.
- ^ "DIGNITAS". Archived from the original on 9 October 2018. Retrieved 14 June 2011.
- ^ Whitlock FA (14 June 1975). "Suicide in Brisbane, 1956 to 1973: the drug-death epidemic". Med J Aust. 1 (24): 737–43. doi:10.5694/j.1326-5377.1975.tb111781.x. PMID 239307.
- ^ Johns MW (1975). "Sleep and hypnotic drugs". Drugs. 9 (6): 448–78. doi:10.2165/00003495-197509060-00004. PMID 238826. S2CID 38775294.
- ^ Jufe, GS (2007). "Nuevos hipnóticos: perspectivas desde la fisiología del sueño [New hypnotics: perspectives from sleep physiology]" (PDF). Vertex (Buenos Aires, Argentina) (in Spanish). 18 (74): 294–9. PMID 18265473.

- ^ "Administration and Compounding Of Euthanasic Agents". Archived from the original on 7 June 2008. Retrieved 15 July 2008.
- ^ Daniel Engber (3 May 2006). "Why do lethal injections have three drugs?". Slate Magazine. Archived from the original on 6 November 2018. Retrieved 15 July 2008.
- ^ Brown, David (20 November 2006). "Some Believe 'Truth Serums' Will Come Back". The Washington Post. Retrieved 26 July 2023.
- ^ "Neuroscience for Kids – Barbiturates". Archived from the original on 16 June 2008. Retrieved 2 June 2008.
- ^ Stocks, JT (1998). "Recovered memory therapy: a dubious practice technique". Social Work. 43 (5): 423–36. doi:10.1093/sw/43.5.423. PMID 9739631.
- ^ Chang, Suk Kyu.; Hamilton, Andrew D. (1988). "Molecular recognition of biologically interesting substrates: Synthesis of an artificial receptor for barbiturates employing six hydrogen bonds". Journal of the American Chemical Society. 110 (4): 1318–1319. doi:10.1021/ja00212a065.
- ^ "Barbiturates drug profile www.emcdda.europa.eu". www.emcdda.europa.eu. Retrieved 22 December 2021.
- ^ "Wolf D. Kuhlmann, "Buffer Solutions"" (PDF). 10 September 2006. Archived from the original (PDF) on 9 November 2016. Retrieved 28 July 2014.
- ^ Steven E. Ruzin (1999). Plant Microtechnique and Microscopy. Oxford University Press. Archived from the original on 3 June 2019. Retrieved 28 July 2014.
- ^ "JaypeeDigital Drugs Acting on Central Nervous System Sedative-Hypnotics, Alcohols, Antiepileptics and Antiparkinsonian Drugs". www.jaypeedigital.com. Retrieved 22 December 2021.
- ^ Skibiski, Jeanie; Abdijadid, Sara (2021), "Barbiturates", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30969553, retrieved 21 December 2021
- ^ Nutt, D; King, LA; Saulsbury, W; Blakemore, C (24 March 2007). "Development of a rational scale to assess the harm of drugs of potential misuse". Lancet. 369 (9566): 1047–53. doi:10.1016/s0140-6736(07)60464-4. PMID 17382831. S2CID 5903121.
- ^ WebMD. "Toxicity, Barbiturate". eMedicine. Archived from the original on 20 July 2008. Retrieved 15 July 2008.
- ^ Nau H; Kuhnz W; Egger HJ; Rating D; Helge H (November 1982). "Anticonvulsants during pregnancy and lactation. Transplacental, maternal and neonatal pharmacokinetics". Clin Pharmacokinet. 7 (6): 508–43. doi:10.2165/00003088-198207060-00003. PMID 6819105. S2CID 20617888.
- ^ a b c d "Barbiturates: Side Effects, Dosages, Treatment, Interactions, Warnings". RxList. Retrieved 22 December 2021.
- ^ "Livertox". Archived from the original on 2 July 2019. Retrieved 21 June 2019.
- ^ Skibiski, Jeanie; Abdijadid, Sara (2021), "Barbiturates", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30969553, retrieved 21 December 2021
- ^ Löscher, W.; Rogawski, M. A. (2012). "How theories evolved concerning the mechanism of action of barbiturates". Epilepsia. 53: 12–25. doi:10.1111/epi.12025. PMID 23205959. S2CID 4675696.
- ^ Chiara, D. C.; Jayakar, S. S.; Zhou, X.; Zhang, X.; Savechenkov, P. Y.; Bruzik, K. S.; Miller, K. W.; Cohen, J. B. (15 May 2013). "Specificity of Intersubunit General Anesthetic-binding Sites in the Transmembrane Domain of the Human α1β3γ2 γ-Aminobutyric Acid Type A (GABAA) Receptor". Journal of Biological Chemistry. 288 (27): 19343–19357. doi:10.1074/jbc.M113.479725. PMC 3707639. PMID 23677991.
- ^ Brunton, Laurence L.; Lazo, John S.; Parker, Keith L.; Goodman, Louis Sanford; Gilman, Alfred Goodman (2005). Goodman & Gilman's Pharmacological Basis of Therapeutics. McGraw-Hill. ISBN 978-0-07-142280-2.
- ^ Neil Harrison; Wallace B Mendelson; Harriet de Wit (2000). "Barbiturates". Neuropsychopharmacology. Retrieved 15 July 2008.
...Barbiturates therefore promote entry of GABA-activated channels into a long-lived open state, whereas [benzodiazepines] increase only the frequency of channel opening into the initial open state. These mechanistic studies reveal interesting details of the changes in channel gating caused by barbiturates but as yet have yielded no insights into the molecular sites of action. An additional interesting effect of barbiturates is direct gating of the channels, i.e., the barbiturates may open the channel even in the absence of GABA. This usually occurs at significantly higher concentrations than those that potentiate the actions of GABA; these concentrations also are generally higher than those required for clinically effective anesthesia.
- ^ Siegel, George J.; Bernard W. Agranoff; Stephen K. Fisher; R. Wayne Albers; Michael D. Uhler (1999) [1998]. "Part 2 Chapter 16". Basic Neurochemistry – Molecular, Cellular and Medical Aspects (Sixth ed.). Lippincott Williams and Wilkins. ISBN 978-0-397-51820-3. Retrieved 1 July 2008.
- ^ Weber, M; Motin, L; Gaul, S; Beker, F; Fink, RH; Adams, DJ (January 2005). "Intravenous anaesthetics inhibit nicotinic acetylcholine receptor-mediated currents and Ca2+ transients in rat intracardiac ganglion neurons". British Journal of Pharmacology. 144 (1): 98–107. doi:10.1038/sj.bjp.0705942. PMC 1575970. PMID 15644873.
- ^ Franks, NP; Lieb, WR (23 November 1998). "Which molecular targets are most relevant to general anaesthesia?". Toxicology Letters. 100–101: 1–8. doi:10.1016/S0378-4274(98)00158-1. PMID 10049127.
- ^ a b "Barbiturates". Archived from the original on 7 November 2007. Retrieved 31 October 2007.
- ^ 의학적 호기심. 영슨, 로버트 M. 런던: 로빈슨 출판사, 1997. 276쪽.
- ^ Galanter, Marc; Kleber, Herbert D. (1 July 2008). The American Psychiatric Publishing Textbook of Substance Abuse Treatment (4th ed.). United States of America: American Psychiatric Publishing Inc. p. 217. ISBN 978-1-58562-276-4.
- ^ Sneader, Walter (23 June 2005). Drug Discovery. John Wiley and Sons. p. 369. ISBN 978-0-471-89979-2.
- ^ Pub. L. 91-513, 1970년 10월 27일, 202(c) Sched. III(b)(1)
- ^ 21 U.S.C. § 812
- ^ 21 U.S.C. § §1308.12
- ^ "List of Psychotropic Substances under International Control ("Green List")" (PDF). International Narcotics Control Board. 25 January 2014. Archived from the original (PDF) on 24 September 2015. Retrieved 19 December 2013.
- ^ Schlatter J; Sitbon N; Saulnier JL (17 February 2001). "[Drugs and drug abusers]". Presse Med. 30 (6): 282–7. PMID 11252979.
- ^ Allgulander C, Ljungberg L, Fisher LD (May 1987). "Long-term prognosis in addiction on sedative and hypnotic drugs analyzed with the Cox regression model". Acta Psychiatr Scand. 75 (5): 521–31. doi:10.1111/j.1600-0447.1987.tb02828.x. PMID 3604738. S2CID 168126.
- ^ Emedicine Health. "Barbiturate Abuse". p. 1. Archived from the original on 2 August 2008. Retrieved 15 July 2008.
- ^ Faulkner TP; Hayden JH; Mehta CM; Olson DA; Comstock EG (1979). "Dose-response studies on tolerance to multiple doses of secobarbital and methaqualone in a polydrug abuse population". Clin Toxicol. 15 (1): 23–37. doi:10.3109/15563657908992476. PMID 498734.
- ^ Coupey SM (August 1997). "Barbiturates". Pediatr Rev. 18 (8): 260–4. doi:10.1542/pir.18-8-260. PMID 9255991.
- ^ Hamid H.; El-Mallakh RS; Vandeveir K (March 2005). "Substance Abuse: Medical and Slang Terminology". South Med J. 98 (3): 350–362. doi:10.1097/01.SMJ.0000153639.23135.6A. PMID 15813163. S2CID 29194849.
- ^ a b c d Smith, Roger; Bogusz, Maciej J (22 September 2011). "phenobarbital"+"secobarbital"+"amobarbital"+"r1"+"r2" Forensic Science (2 ed.). Elsevier. p. 245. ISBN 9780080554259. Retrieved 21 December 2013.
- ^ Skibiski, Jeanie; Abdijadid, Sara (2021), "Barbiturates", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30969553, retrieved 8 July 2021
외부 링크 및 추가 판독
- 이 페이지에서 사용되는 일부 공개 도메인 텍스트에 대한 미국 마약 집행국 소스.
- López-Muñoz, F.; Ucha-Udabe, R.; Alamo, C. (2005). "The history of barbiturates a century after their clinical introduction". Neuropsychiatric Disease and Treatment. 1 (4): 329–343. PMC 2424120. PMID 18568113.
- 국립 약물 남용 연구소: "10대를 위한 NIDA: 처방된 우울증 약"