디클로로메탄
Dichloromethane| | |||
 | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 디클로로메탄 | |||
| 기타 이름 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 첸블 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.000.763 | ||
| EC 번호 |
| ||
| 케그 | |||
PubChem CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 1593 | ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| CH2클론2 | |||
| 몰 질량 | 84.93 g/g−1/g | ||
| 외모 | 무색 액체 | ||
| 냄새 | 희미하고 클로로포름[4] 같은 | ||
| 밀도 | 1.3266g/cm3(20°C)[5] | ||
| 녹는점 | -96.7°C(-142.1°F, 176.5K) | ||
| 비등점 | 39.6°C(103.3°F, 312.8K) 720°C에서[6] 분해됩니다. 39.75°C(103.55°F, 312.90K) 760mmHg로[7] | ||
| 25.6g/L(15°C) 17.5g/L(25°C) 15.8g/L(30°C) 5.2 g/L (60 °C)[6] | |||
| 용해성 | 아세트산에틸, 알코올, 헥산, 벤젠, CCl4, 디에틸에테르, CHCl에서3 혼합 가능 | ||
| 로그 P | 1.19[8] | ||
| 증기압 | 0.13kPa(-70.5°C) 2 kPa (−40 °C) 19.3kPa(0°C) 57.3kPa(25°[9]C) 79.99kPa(35°[6]C) | ||
헨리의 법칙 상수(kH) | 3.25 L/atm/mol[7] | ||
자화율(δ) | - 46.6/10cm−63/수직선 | ||
굴절률(nD) | 1.4244 (20 °C)[7][10] | ||
| 점성 | 0.43cP(20°[7]C) 0.413 cP(25 °C) | ||
| 구조. | |||
| 1.6 D | |||
| 열화학 | |||
열용량 (C) | 102.3 J/(mol·K)[9] | ||
표준 어금니 엔트로피 (S | 174.5 J/(mol·K)[9] | ||
표준 엔탈피/ 형성 (δHf⦵298) | - 124.3 kJ/mol[9] | ||
표준 엔탈피/ 연소 (δHc⦵298) | -454.0 kJ/mol (표준 생성 [9]엔탈피로부터) | ||
| 위험 요소 | |||
| 산업안전보건(OHS/OSH): | |||
눈의 위험 | 자극성 | ||
| GHS [10]라벨링: | |||
  | |||
| 경고 | |||
| H315, , , , , , | |||
| P261, P281, P305+P351+P338 | |||
| NFPA 704(파이어 다이아몬드) | |||
| 플래시 포인트 | 없음, 그러나 100°C[11] 이상의 가연성 증기-공기 혼합물을 형성할 수 있음 | ||
| 556 °C (1,033 °F, 829 K) | |||
| 폭발 한계 | 13%~23%[4] | ||
| 치사량 또는 농도(LD, LC): | |||
LD50(중간선량) | 1.25g/kg (경구, 경구) 2 g/kg (경구,[6] 경구) | ||
LC50(중간 농도) | 24,929 장/분 (rat, 30 분) 14,400 ppm (표준, 7시간)[13] | ||
LCLo(최저 공개) | 5000ppm (피그, 2시간) 10,000ppm (표준, 7시간) 12,295ppm (고양이, 4.5시간) 14,108ppm (개, 7시간)[13] | ||
| NIOSH(미국 건강 노출 제한): | |||
PEL(허용) | 8시간 동안 25ppm(시간 가중 평균), 15분 동안 125ppm(STEL)[4][12] | ||
REL(권장) | Ca[4] | ||
IDLH(즉시 위험) | Ca [2300ppm][4] | ||
| 보충 데이터 페이지 | |||
| 디클로로메탄(데이터 페이지) | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
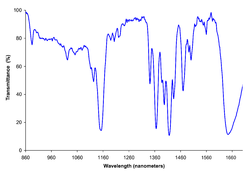
디클로로메탄(DCM 또는 염화메틸렌, 염화메틸렌[14], 중염화메틸렌)은 유기염소화합물로서 다음 식과 같다. CHCl22. 클로로포름과 같은 달콤한 냄새를 가진 무색 휘발성 액체로서 용매로서 널리 사용되고 있다.물과 혼합할 수는 없지만 극성이며 많은 유기 [15]용제와 혼합할 수 있습니다.
발생.
디클로로메탄의 천연 자원에는 해양 자원, 대조류, 습지, [16]화산이 포함된다.그러나 환경 내 디클로로메탄 대부분은 산업 [16]배출의 결과물이다.
생산.
DCM은 클로로메탄 또는 메탄 중 하나를 염소 가스로 400–500 °C에서 처리하여 생성된다.이러한 온도에서 메탄과 클로로메탄은 모두 일련의 반응을 거쳐 점차 더 많은 염소화 생성물을 생성한다.이 방법으로 1993년에는 [15]미국, 유럽, 일본에서 약 40만 톤이 생산되었다.
- CH4 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CHCl22 + HCl
- CHCl22 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCL4 + HCl
이러한 공정의 산출물은 부산물로 염화수소뿐만 아니라 클로로메탄, 디클로로메탄, 클로로포름 및 사염화탄소 혼합물이다.이 화합물들은 증류에 의해 분리된다.
DCM은 1839년 프랑스의 화학자 앙리 빅토르 레그노 (1810–1878)에 의해 처음 만들어졌으며,[17] 그는 햇빛에 노출된 클로로메탄과 염소의 혼합물로부터 분리시켰다.
사용하다
DCM의 휘발성과 광범위한 유기화합물을 용해할 수 있는 능력은 DCM을 많은 [15]화학공정에 유용한 용매로 만듭니다.식품 산업에서는 커피와 차를 탈카페인하고 홉이나 다른 [18][19]향신료의 추출물을 만드는 데 사용된다.그 휘발성으로 인해 에어로졸 스프레이 추진제 및 폴리우레탄 발포제로서 사용되었습니다.
수소 결합
염화메틸렌은 전자공여체에 수소를 결합할 수 있는 루이스산이다.경산으로 분류되며 ECW 모델에 포함됩니다.이는 기증자-수용체 결합에 대한 많은 열역학 연구에 사용되어 온 용제입니다.이러한 열역학 연구에서 염화메틸렌의 공여 수소 결합 보정이 [20][21]보고되었다.
특수한 용도
이 화합물의 낮은 끓는점은 화학 물질이 작은 온도 차이에서 기계적 에너지를 추출할 수 있는 열 엔진에서 작동할 수 있게 해줍니다.DCM 히트 엔진의 예는 드링킹 버드입니다.그 장난감은 [22]실온에서 작동한다.주크박스 디스플레이 및 홀리데이 버블 라이트의 유체로도 사용되며, 열원으로 램프 위에 컬러 버블 튜브가 있고 소량의 암염이 있어 열량과 상변화 용매의 핵생성 부위를 제공합니다.
DCM은 특정 플라스틱을 화학적으로 용접합니다.예를 들어, 전기 계량기의 케이스를 밀봉하는 데 사용됩니다.플라스틱 용접 접착제의 주요 부품으로 판매되는 이 제품은 모델 제작 애호가들이 플라스틱 부품을 함께 접합하기 위해 광범위하게 사용됩니다.그것은 보통 "디클로"라고 불립니다.
열 봉인된 의류 이송을 제거하는 데 의류 인쇄 산업에서 사용됩니다.
DCM은 토목 공학 재료 테스트 분야에서 사용됩니다. 구체적으로는 아스팔트 또는 마카담의 골재에서 바인더를 분리하여 [23]재료 테스트를 가능하게 하는 용매로서 역청 재료 테스트 중에 사용됩니다.
소의 해초 사료인 Asparagopsis taxiformis의 디클로로메탄 추출물이 메탄 배출량을 79%[24] 줄이는 것으로 나타났다.
페인트 스트리퍼의 주성분으로 사용되어 왔지만, 현재는 미국과 유럽연합에서 사용이 금지되어 있습니다.
독성
DCM은 단순한 클로로 탄화수소 중 독성이 가장 낮지만 건강에 심각한 위험을 가지고 있다.높은 휘발성으로 인해 급성 흡입 [25][26]위험이 있습니다.피부를 [4][27]통해서도 흡수될 수 있습니다.흡입을 통한 디클로로메탄에 대한 급성 과다 노출의 증상으로는 집중력 저하, 어지럼증, 피로, 메스꺼움, 두통, 저림, 약함, 상부 호흡기와 눈의 자극 등이 있습니다.더 심각한 결과로는 질식, 의식 상실, 혼수, [4][27]사망 등이 있습니다.
또한 DCM은 일산화탄소로 신체에 의해 대사되어 일산화탄소 [28]중독으로 이어질 수 있다.흡입에 의한 급성 피폭은 시신경[29] 장애와 [30]간염을 초래했다.피부 접촉이 길어지면 DCM이 피부의 지방 조직 일부를 녹여 피부 자극이나 화학적 [31]화상을 일으킬 수 있습니다.
실험실 [32]동물에서 폐, 간, 췌장암과 관련이 있기 때문에 발암성이 있을 수 있습니다.다른 동물 연구들은 유방암과 침샘암을 보여주었다.어느 수준이 [4][27]발암성일 수 있는지에 대한 연구는 아직 명확하지 않다.DCM은 태반을 가로지르지만 임신 중 DCM에 노출된 여성의 태아 독성은 [33]입증되지 않았다.동물 실험에서, 그것은 모성 독성이 있는 용량에서 페토독성이었지만 기형 유발 효과는 [32]나타나지 않았다.
기존 심장 문제가 있는 사람들에게서, DCM에 노출되면 비정상적인 심장 박동 및/또는 심장마비를 일으킬 수 있으며, 때로는 과다 [27]노출의 다른 증상 없이도 발생할 수 있습니다.기존 간, 신경계 또는 피부에 문제가 있는 사람은 [12]염화메틸렌에 노출된 후 악화될 수 있습니다.
규정
많은 국가에서 DCM이 함유된 제품에는 건강상의 위험을 경고하는 라벨이 부착되어 있어야 합니다.
2013년 2월 미국 산업안전보건국(OSHA)과 국립산업안전보건연구소는 2000년 이후 적어도 14명의 욕조 리피니셔가 DCM 노출로 사망했다고 경고했다.이 근로자들은 호흡 보호 장치가 불충분하거나 전혀 없는 상태에서 환기가 잘 되지 않는 욕실에서 혼자 일하고 있었으며,[12][27][34] DCM의 위험에 대한 교육은 받지 않았다. 그 이후로 OSHA는 DCM [35]표준을 발표했다.유럽연합에서는 2009년 유럽 의회가 소비자와 [36]많은 전문가들을 위한 페인트 스트리퍼에 DCM 사용을 금지하기로 의결했다.이 금지령은 2010년 [37]12월에 발효되었다.
유럽의 경우, SCOEL(Scientific Committee on Locational Exposure Limit Values, SCOEL)은 DCM에 100ppm의 직업상 피폭 한계(8시간 가중 평균)와 200ppm의 단기 피폭 한계(15분)[38]를 권고한다.
건강에 미치는 영향에 대한 우려로 인해 이러한 애플리케이션 [15][39]중 많은 부분에서 대안을 모색하고 있습니다.
미국 환경보호청(EPA)은 2019년 3월 15일 소비자용 페인트 제거기에서 염화메틸렌의 제조(수출입 포함)를 금지한다는 최종 규정을 180일 이내에 발표했지만 염화메틸렌이 많이 함유된 다른 제품에는 영향을 미치지 않는다.페인트 제거가 의도되지 않은 소비자 제품.
환경에 미치는 영향
오존
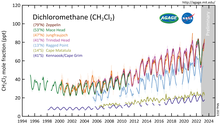
디클로로메탄은 몬트리올 [40]의정서에 의해 오존 파괴 물질로 분류되지 않는다.미국 대기청정법은 디클로로메탄을 오존 [41]감소제로 규제하지 않는다.최근 연구에 따르면 디클로로메탄과 다른 할로겐화 초단수명물질(VSLS)은 0.5년 미만의 짧은 대기 수명에도 불구하고 성층권으로 빠르게 이동하는 지역에서 방출될 경우 성층권 오존 파괴에 기여할 수 있다.[42] 디클로로메탄의 대기 중 함유량은 최근 몇 년 동안 증가하고 있다.
1998년부터 2016년까지 성층권을 통해 지상에서 중간 위도에서 측정된 오존 농도는 1.2 돕슨 [43]단위로 1% [44]미만으로 감소했다.이러한 감소의 이유는 불분명하지만, 한 가지 확인되지 않은 가설은 저층 [45]대기권에 디클로로메탄과 같은 단수명 물질이 존재한다는 것이다.
「 」를 참조해 주세요.
레퍼런스
- ^ 디클로로메탄
- ^ 프레온으로서의 디클로로메탄
- ^ 디클로로메탄(프리온)
- ^ a b c d e f g h NIOSH Pocket Guide to Chemical Hazards. "#0414". National Institute for Occupational Safety and Health (NIOSH).
- ^ Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 3.164. ISBN 1-4398-5511-0.
- ^ a b c d 디클로로메탄의 특성.chemister.ru
- ^ a b c d PubChem의 CID 6344
- ^ "Dichloromethane_msds".
- ^ a b c d e 린스트롬의 염화메틸렌, Peter J.; Mallard, William G. (ed.); NIST 화학 웹북, NIST 표준 참조 데이터베이스 번호 69, 국립 표준 기술 연구소, Gaithersburg (MD), http://webbook.nist.gov (2014-05-26)
- ^ a b 시그마-알드리치, 디클로로메탄2014년 5월 26일 취득.
- ^ "Real time measurement of dichloromethane containing mixtures" (PDF). Health & Safety Laboratory. Retrieved 5 August 2015.
- ^ a b c "Methylene Chloride Hazards for Bathtub Refinishers". OSHA-NIOSH Hazard Alert 2013-110. OSHA and NIOSH. Retrieved 22 January 2015.
- ^ a b "methylene chloride". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ 염화메틸렌
- ^ a b c d 로스버그, M. et al.(2006) Wiley-VCH, Weinheim의 Ulmann's Encyclopedia of Industrial Chemistry, Willy-VCH, Industrial Chemistry, Weinheim에 있는 "염화탄화수소"doi: 10.1002/14356007.a06_233.pub2.
- ^ a b Gribble, Gordon W. (2009). Naturally Occurring Organohalogen Compounds. Springer. ISBN 978-3211993248.
- ^ Regnault, V. (1839) "De l'action du chlore sur les les éthers hydrochloriques de l'alcool et de l'esprit de l'es points de la téorie des ethers" (에탄올과 메탄올의 염산 에테르 및 에테르에 대한 염소의 작용에 대한 염소의 작용)세컨드 파티. 클로어 수르 에테르 하이드로클로리케 드 레스프리트 드 보이(De l'action du Clore sur l'éther hydrochlorique de l'esprit de bois) (제2부).메탄올의 염산 에테르(즉, 클로로메탄)에 대한 염소 작용에 대해 377–380페이지.레그놀트는 디클로로메탄에게 에테르 하이드로클로리케 모노클로로레(단염화 염산 에테르)라는 이름을 붙여주었다.주의: Regnault는 디클로로메탄에 대한 경험식을 CHCl로244 제시했는데, 그 이유는 그 시기에 화학자들이 잘못된 원자 질량을 사용했기 때문이다.
독일어로 재인쇄:- Regnault, V. (1840). "Ueber die Einwirkung des Chlors auf die Chlorwasserstoffäther des Alkohols und Holzgeistes und über mehrere Punkte der Aethertheorie". Annalen der Chemie und Pharmacie. 33 (3): 310–334. doi:10.1002/jlac.18400330306. 페이지 328을 참조하십시오.
- Regnault, V. (1840). "Ueber die Wirkung des Chlors auf den Chlorwasserstoffäther des Alkohols und des Holzgeistes, so wie über mehrere Puncte der Aethertheorie". Journal für Praktische Chemie. 19: 193–218. doi:10.1002/prac.18400190134. 페이지 210을 참조하십시오.
- ^ Office of Environmental Health Hazard Assessment (September 2000). "Dichloromethane" (PDF). Public Health Goals for Chemicals in Drinking Water. California Environmental Protection Agency. Retrieved June 5, 2016.[영구 데드링크]
- ^ James2014-04-09T00:00:00+01:00, Emily. "Dichloromethane". Chemistry World.
- ^ Nozari, M. S.; Jensen, C. D.; Drago, R. S. (1973). "Eliminating solvation contributions to the enthalpy of adduct formation in weakly polar, acidic solvents". Journal of the American Chemical Society. 95 (10): 3162–3165. doi:10.1021/ja00791a015.
- ^ Drago, R. S.; Nusz, J. A..; Courtright, R. C. (1974). "Solvation contributions to enthalpies measured in methylene chloride". Journal of the American Chemical Society. 96 (7): 2082–2086. doi:10.1021/ja00814a016. 이 문서에서 사용하는 E&C 파라미터는 오래된 파라미터입니다.개선된 E&C 파라미터는 ECW 모델에 기재되어 있습니다.
- ^ Perelman, Yakov (1972) [1936]. Physics for Entertainment. Vol. 2. pp. 175–178. ISBN 978-1401309213. [1] [2]
- ^ Shell Bitumen (2003-09-25). The Shell Bitumen Handbook. ISBN 978-0-7277-3220-0.
- ^ Lorenna Machado, Marie Magnusson, Nicholas Paul, Nigel Tomkins (2016). "Identification of bioactives from the red seaweed Asparagopsis taxiformis that promote antimethanogenic activity in vitro". Journal of Applied Phycology. 28 (5): 3117–3126. doi:10.1007/s10811-016-0830-7.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Rioux JP, Myers RA (1988). "Methylene chloride poisoning: a paradigmatic review". J Emerg Med. 6 (3): 227–238. doi:10.1016/0736-4679(88)90330-7. PMID 3049777.
- ^ CDC (2012). "Fatal Exposure to Methylene Chloride Among Bathtub Refinishers — United States, 2000–2011". MMWR. 61 (7): 119–122. PMID 22357403.
- ^ a b c d e Hall, Ronald M. (4 February 2013). "Dangers of Bathtub Refinishing". National Institute for Occupational Safety and Health. Retrieved 21 January 2015.
- ^ Fagin J, Bradley J, Williams D (1980). "Carbon monoxide poisoning secondary to inhaling methylene chloride". Br Med J. 281 (6253): 1461. doi:10.1136/bmj.281.6253.1461. PMC 1714874. PMID 7437838.
- ^ Kobayashi A, Ando A, Tagami N, Kitagawa M, Kawai E, Akioka M, Arai E, Nakatani T, Nakano S, Matsui Y, Matsumura M (2008). "Severe optic neuropathy caused by dichloromethane inhalation". J Ocul Pharmacol and Ther. 24 (6): 607–612. doi:10.1089/jop.2007.0100. PMID 19049266.
- ^ Cordes DH, Brown WD, Quinn KM (1988). "Chemically induced hepatitis after inhaling organic solvents". West J Med. 148 (4): 458–460. PMC 1026148. PMID 3388849.
- ^ Wells GG, Waldron HA (1984). "Methylene chloride burns". Br J Ind Med. 41 (3): 420. doi:10.1136/oem.41.3.420. PMC 1009322. PMID 6743591.
- ^ a b USDHHS. "Toxicological Profile for Methylene Chloride" (PDF). Retrieved 2006-09-10.
- ^ Bell BP, Franks P, Hildreth N, Melius J (1991). "Methylene chloride exposure and birthweight in Monroe County, New York". Environ Res. 55 (1): 31–9. Bibcode:1991ER.....55...31B. doi:10.1016/S0013-9351(05)80138-0. PMID 1855488.
- ^ OSHA QuickTakes, 2013년 2월 1일
- ^ 염화메틸렌산업안전보건국osha.gov
- ^ "EU의 대부분의 DCM 페인트 스트리퍼 금지" FaintSquare News가 14년 5월 1일을 회수했습니다.
- ^ "COMMISSION REGULATION (EU) No 276/2010 (Official Journal of the European Union, L 86/7)". 2010-04-01. Retrieved 2012-02-07.
- ^ "SCOEL recommendations". 2011-04-22. Retrieved 2011-04-22.
- ^ "Summary of Regulations Controlling Air Emissions from Paint Stripping and Miscellaneous Surface Coating Operations" (PDF). U.S. Environmental Protection Agency – NESHAP 6H. 10 August 2016.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ United States Environmental Protection Agency (2015-07-17). "Ozone-Depleting Substances". Retrieved April 20, 2018.
- ^ United States Environmental Protection Agency (October 1995). "Questions and Answers on Ozone-Depleting Solvents and Their Substitutes". Retrieved April 20, 2018.
- ^ World Meteorological Organization, United Nations Environmental Program (15 April 2020). "Scientific Assessment of Ozone Depletion: 2018".
- ^ Reese, April (2018-02-09). "As polar ozone mends, UV shield closer to equator thins". Science. 359 (6376): 623. Bibcode:2018Sci...359..623R. doi:10.1126/science.359.6376.623. ISSN 0036-8075. PMID 29439223.
- ^ "Nasa Ozone Watch: Dobson Unit facts". ozonewatch.gsfc.nasa.gov. 3rd Paragraph: “The average amount of ozone in the atmosphere is roughly 300 Dobson Units,” (2.2 / 300 ≈ 0.73%). Archived from the original on 2011-10-14. Retrieved 2021-09-16.
- ^ Ball, W. T.; Alsing, J.; Mortlock, D. J.; Staehelin, J.; Haigh, J. D.; Peter, T.; Tummon, F.; Stübi, R.; Stenke, A. (2018-02-06). "Evidence for a continuous decline in lower stratospheric ozone offsetting ozone layer recovery" (PDF). Atmos. Chem. Phys. 18 (2): 1379–1394. Bibcode:2018ACP....18.1379B. doi:10.5194/acp-18-1379-2018. ISSN 1680-7324.
외부 링크
- 국제화학안전카드 0058
- NIOSH Pocket Guide to Chemical Hazards. "#0414". National Institute for Occupational Safety and Health (NIOSH).
- 국가 오염 물질 목록 – 디클로로메탄 팩트 시트
- 미국 독성학 프로그램 디클로로메탄
- IARC 요약 및 평가 제71권(1999년)
- 캐나다 환경보호법 우선순위 물질 목록 평가 보고서
- 유기 화합물 데이터베이스
- 지속 가능한 사용 및 업계 권장 사항