리마세미드
Remacemide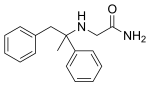 | |
| 임상 데이터 | |
|---|---|
| 상호 | 에코비아[1] |
| 기타 이름 | (±)-2-아미노-N-[1,2-di(페닐)프로판-2-일]아세트아미드 PR934-423 |
| 루트 행정부. | 입으로 |
| ATC 코드 |
|
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| 켐스파이더 | |
| 유니 | |
| CompTox 대시보드 (EPA ) | |
| 화학 및 물리 데이터 | |
| 공식 | C17H20N2O |
| 몰 질량 | 268.360 g/g−1/g |
| 3D 모델(JSmol) | |
| |
| |
| | |
리마세미드는 나트륨 채널 차단 특성을 [2]가진 저친화성 NMDA 길항제 역할을 하는 약물이다.급성 허혈성 뇌졸중,[3][4] 간질,[5] 헌팅턴병, 파킨슨병의 치료를 위해 연구되었다. 뇌전증
리마세미드는 발작 빈도에 약간의 효과만 있고 어지럼증을 유발하기 때문에, 리마세미드가 [6]간질에 효과적인 치료제가 될 것이라고 더 이상 믿지 않는다.뇌졸중, 헌팅턴병 또는 파킨슨병을 치료할 수 있는 리마미드의 잠재력에 대한 그러한 진술은 아직 이루어지지 않았지만, 리마미드는 더 이상 이러한 [citation needed]상태를 위해 개발되지 않고 있다.
리마세미드는 리마세미드 염산염, (±)-2-아미노-N-(1-메틸-1, 2-디페닐에틸)-아세트아미드 염산염 또는 FPL 12924로도 알려져 있다.AA.[7]
부작용
부작용의 결여
뇌전증에 대한 다른 많은 치료법과는 달리, 동물의 인지 성능에 대한 영향에 대한 증거는 [12][13][14][15][16]혼합되어 있지만, 리마세미드는 인간의 인지 성능이나[9][10][5] 운전 성능을[11] 손상시키지 않는 것으로 보인다.리마세미드는 [17]진정제가 아니에요
독성
마우스 신경손상 테스트를 위한 리마세미드의 중간 독성 선량은 5.6mg/[17]kg이다.추정 치사량은 생쥐에서 [17]약 927.3mg/kg이다.생쥐에서 28.1의 양호한 치료지수를 가지고 있다.[17]
약물 상호작용
레보도파
리마세미드는 레보도파(레보도파 치료 1시간 전 300mg의 리마세미드)의 흡수를 지연시키지만 전체 흡수는 지연시키지 않았다(레보도파 혈장 농도에 대한 곡선 아래 영역은 [18]변하지 않았다).
발프로산나트륨
리마세미드는 [19]간질 치료제인 발프로산나트륨과 상호작용하지 않는다.
카르바마제핀
라마세미드는 카바마제핀과 상호작용한다.리마세미드는 카바마제핀의 신진대사를 억제하는 반면, 카바마제핀은 리마세미드와 [20]FPL12495의 신진대사를 유도한다.
알코올
리마세미드염
리마세미드는 염산염 리마세미드로 가장 일반적으로 합성된다.그러나, 다른 리마세미드 소금과 그 결정에 대한 연구는 있었다. 다른 리마세미드 소금들은 맛이 더 좋거나 소아 현탁제제에 [21]더 적합한 용해성을 가질 수 있기 때문이다.
작용 메커니즘
리마세미드는 NMDA 수용체 [7]복합체의 이온 채널 부위에 약하고 비경쟁적으로 결합한다.리마세미드는 알로스테릭과 [22]채널 양쪽에서 결합합니다.그러나, 리마세미드는 NMDAR에 매우 약하게 결합하기 때문에, 흥분독성에 대한 리마세미드의 생체내 효과의 대부분은 더 강력한 데스글리신 유도체 FPL [7]12495로의 대사 변환에 의해 야기되는 것으로 생각된다.즉, 리마미드는 실제로 활성대사물 FPL 12495를 중추신경계에 [23]전달하는 프로드러그 역할을 할 수 있다.
Epilepsy
잘 검증되고 기술된 결석 유전자 모델 뇌전증에서, WAG/Rij 변종, 리마세미드 및 그 대사물 FPL 12495의 랫드는 스파이크/파동 방출 횟수에 대한 글루탐산염 길항제 공통 효과를 가진 것으로 밝혀졌다.EEG, 약물은 선량을 의존적으로 증가/파동 변화시킨다.그러나 다른 글루탐산염 길항제들과 달리 FPL12495는 스파이크파 방전의 [24]지속시간을 증가시켰다.
약동학
혈액-뇌 장벽
마취된 [25][26]동물의 일반적인 경동맥에 방사성 라벨 시험과 기준 물질을 주입하는 혈액-뇌 장벽을 통과하는 약물의 능력 측정값인 뇌흡수지수(BUI)는 51 ± 0.9 [23]SD이다.
에난티오머
리마세미드의 스테레오 이성질체는 쥐에게 경구 투여 시 최대 전기 충격 발작을 방지하는 데 있어 라세미 혼합물과 동일한 효력을 가지며, (+) 스테레오 이성질체는 덜 강력하다.[27]
대사물
FPL 12495
생체 내 리마세미드 효과의 대부분은 데스글리신 유도체 FPL 12495(±)[7]에 의해 발생하는 것으로 생각된다.FPL 12495(±)는 NMDAR에 [28]특이적이고 비경쟁적으로 결합한다.최대 전기 경련 충격에 대한 효과는 [7]리마미드보다 더 강력합니다.S 이성질체(FPL 12859)는 레이스믹 혼합물보다 훨씬 강력하지만 R 이성질체는 [7]레이스메이트보다 강력하지 않습니다.
FPL 12495는 ARL 12495라고도 불립니다.AA.[29][30][31]
기타 대사물
FPL 15053
FPL 15053은 리마세미드의 N-히드록시-데스글리시네이트이며, NMDAR에 대한 결합이 완만하고 테스트 마우스 및 [7]랫드에서 경련 및 사망률에 대한 영향이 완만하다.
FPL 14331 및 FPL 14465
FPL14331 및 FPL14465는 remacemide의 p-hydroxy-desglycinate로 i.p. 및 i.v.[7] 투여 후 최대 전기경련성 충격에 대해 어느 정도 효과를 나타낸다.
FPL 15455
FPL 15455는 리마세미드의 옥소아세트산 대사물이지만 생물학적 활성이 [7]입증되지 않았다.
FPL 14991 및 FPL 14981
FPL14991 및 FPL14981은 모두 리마세미드의 β-미드록시-데스글리신산염으로 [7]생쥐의 최대 전기경련충격에 대하여 적당한 유효성을 나타낸다.그러나 FPL 14981은 FPL 14991이 아닌 FPL 14981은 [7]생쥐에서 NMDLA 유도 경련 및 사망을 예방한다.
FPL 13592 및 FPL 15112
리마세미드의 히드록시-메틸 유도체(FPL 13592)와 데스글리신산(FPL 15112)은 정맥 투여 후에만 전기 충격으로 인한 경련을 방지하며, 데스글리신 유도체만 NMDAR에 [7]결합한다.
FPL 14467
FPL14467(p-dihydroxy-desglycine)은 생체내 불활성이며 NMDAR [7]결합에 약하다.
약역학
[3H]MK801의 50% 변위 값은 리마세미드의 경우 68μM, FPL 12495의 경우 0.48μM이었다.AA.[7]
역사
현황
Remacemide는 영국의 다국적 제약회사 AstraZeneca에 의해 가장 최근에 개발된 실험용 의약품이다.그러나, 2000년 이후, 그것의 진행에 대한 소식은 거의 없었다.몇 가지 소식통에 따르면 그 개발은 [32][33]중단되었다.
손바꾸기
리마세미드는 현재 없어진 영국 제약회사 피손스가 [34]개발 중인 마지막 약 중 하나였다.1995년 스웨덴의 제약회사 아스트라([35]Astra)에 의해 피슨의 연구 개발 사업과 함께 인수되었고, 1999년 영국 회사인 Zeneca(제네카)와 합병하여 AstraZeneca([36]제네카)를 설립하였다.2000년, AstraZeneca는 다른 [37]제약회사에 리마시드를 허가하는 것을 검토했지만, 그 이후로 리마시드에 대한 소식은 거의 없었다.Remacemide의 개발은 2001년 [33]7월에 중단되었을지도 모른다.
Fisons에 의한 발견 및 개발
1990년 Fisons의 연구진은 쥐와[17][27] [38]쥐에서 리마미드가 항경련제 역할을 한다는 것을 밝혀냈다. 글루탐산염 독성을 방지함으로써 리마미드가 신경보호제로서의 잠재력 때문에 헌팅턴병과[39] 파킨슨병의 [40]치료제로서도 곧 연구되고 있다.
아스트라
1995년 아스트라가 리마미드를 획득했을 때, 그것은 이미 항간질제로서[35] IIb상 임상 개발에 들어갔고 헌팅턴의 [39][41]치료제로서 1상 임상 개발에 들어갔습니다.
아스트라제네카
1998년, 아스트라가 제네카와의 합병을 발표했을 때, 리마세미드는 간질에 대한 3단계 실험과 파킨슨병에 대한 2단계 실험으로 진행되었고, 아스트라는 또한 신경성 통증 치료의 가능성을 조사하고 있었다.
합병 후 1999년, AstraZeneca는 신경 보호 효과를 위해 리마세미드를 조사하고 있으며, 2001년 헌팅턴병, 2003년 [43]파킨슨병과 간질에 대한 규제 제출을 계획했다고 보고했다.
레마세미드는 2000년 [1]3월 FDA에 의해 헌팅턴병 치료제로 지정됐다.
R&D 파이프라인에 대한 AstraZeneca의 보고서에서 Remacemide가 마지막으로 언급된 것은 2000년이었다. 이때 R&D 파이프라인은 헌팅턴병 치료의 remacemide 임상시험과 파킨슨병 치료의 remacemide 임상시험 중이었다.당시 FDA에 신약신청서(NDA)를 제출하고 CHMP에 시판허가신청서를 제출하는 것은 2001년 헌팅턴병,[37] 2003년 이후 파킨슨병 등으로 예상됐지만 아직 제출 소식은 없다.이 보고서에서는 또한 리마세미드가 "전략적 검토 중이며 면허 [37]활동의 잠재적 후보"라는 점에 주목했다(약물 면허에 관한 이 외부 기사 참조).
최신 뉴스
헌팅턴 연구 [44]그룹과 파킨슨 연구 [45]그룹에 따르면 진행 중인 리마세미드의 임상 실험은 없다.
유용성
리마세미드는 일반인이 이용할 수 없고 현재 임상시험이 진행 중이 아닌 실험용 의약품이다.Tocris [46]Bioscience의 조사 목적으로 AstraZeneca의 라이선스를 받아 이용할 수 있습니다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b FDA (2009-05-05). "Cumulative List of all Products that have received Orphan Designation" (excel document). FDA. Retrieved 28 April 2012.
- ^ Santangeli S, Sills GJ, Thompson GG, Brodie MJ (March 2002). "Na(+) channel effects of remacemide and desglycinyl-remacemide in rat cortical synaptosomes". European Journal of Pharmacology. 438 (1–2): 63–8. doi:10.1016/S0014-2999(02)01297-9. PMID 11906711.
- ^ Muir KW, Lees KR (September 1995). "Initial experience with remacemide hydrochloride in patients with acute ischemic stroke". Annals of the New York Academy of Sciences. 765 (1 Neuroprotecti): 322–3. Bibcode:1995NYASA.765..322M. doi:10.1111/j.1749-6632.1995.tb16602.x. PMID 7486631. S2CID 7573258.
- ^ Dyker AG, Lees KR (September 1999). "Remacemide hydrochloride: a double-blind, placebo-controlled, safety and tolerability study in patients with acute ischemic stroke". Stroke. 30 (9): 1796–801. doi:10.1161/01.STR.30.9.1796. PMID 10471426.
- ^ a b Wesnes KA, Edgar C, Dean AD, Wroe SJ (March 2009). "The cognitive and psychomotor effects of remacemide and carbamazepine in newly diagnosed epilepsy". Epilepsy & Behavior. 14 (3): 522–8. doi:10.1016/j.yebeh.2008.11.012. PMID 19111629. S2CID 6582499.
- ^ a b Leach JP, Marson AG, Hutton JL (2002). "Remacemide for drug-resistant localization related epilepsy". The Cochrane Database of Systematic Reviews (4): CD001900. doi:10.1002/14651858.CD001900. PMID 12519561.
- ^ a b c d e f g h i j k l m n Palmer GC, Murray RJ, Wilson TC, Eisman MS, Ray RK, Griffith RC, et al. (June 1992). "Biological profile of the metabolites and potential metabolites of the anticonvulsant remacemide". Epilepsy Research. 12 (1): 9–20. doi:10.1016/0920-1211(92)90086-9. PMID 1388119. S2CID 23097783.
- ^ a b "A multicenter randomized controlled trial of remacemide hydrochloride as monotherapy for PD. Parkinson Study Group". Neurology. 54 (8): 1583–8. April 2000. doi:10.1212/wnl.54.8.1583. PMID 10762497. S2CID 216064344.
- ^ Lockton J, Cole G, Hammersley M, Wesnes K (1998). "Cognitive function is unaffected by remacemide at therapeutic relevant single doses". J Psychopharmacol. 12 (A41).
- ^ Lockton JA, Wesnes KA, Yeates N, Rolan P, Diggory G (1998). "Remacemide does not affect cognitive function following multiple dosing". J Psychopharmacol. 12 (A41).
- ^ Ramaekers G, Lamers J, Verhey F, Muntjewerff D, Mobbs E, Sanders N, et al. (January 2002). "A comparative study of the effects of carbamazepine and the NMDA receptor antagonist remacemide on road tracking and car-following performance in actual traffic". Psychopharmacology. 159 (2): 203–10. doi:10.1007/s002130100898. PMID 11862350. S2CID 2774324.
- ^ Wright LK, Pearson EC, Hammond TG, Paule MG (May–Jun 2007). "Behavioral effects associated with chronic ketamine or remacemide exposure in rats". Neurotoxicology and Teratology. 29 (3): 348–59. doi:10.1016/j.ntt.2006.12.004. PMID 17291718.
- ^ Popke EJ, Allen RR, Pearson EC, Hammond TG, Paule MG (1 July 2001). "Differential effects of two NMDA receptor antagonists on cognitive-behavioral development in nonhuman primates I". Neurotoxicology and Teratology. 23 (4): 319–32. doi:10.1016/S0892-0362(01)00156-8. PMID 11485835.
- ^ Popke EJ, Allen RR, Pearson EC, Hammond TG, Paule MG (1 July 2001). "Differential effects of two NMDA receptor antagonists on cognitive--behavioral performance in young nonhuman primates II". Neurotoxicology and Teratology. 23 (4): 333–47. doi:10.1016/S0892-0362(01)00138-6. PMID 11485836.
- ^ Popke EJ, Patton R, Newport GD, Rushing LG, Fogle CM, Allen RR, et al. (1 March 2002). "Assessing the potential toxicity of MK-801 and remacemide: chronic exposure in juvenile rhesus monkeys". Neurotoxicology and Teratology. 24 (2): 193–207. doi:10.1016/S0892-0362(02)00206-4. PMID 11943507.
- ^ Paule MG, Fogle CM, Allen RR, Pearson EC, Hammond TG, Popke EJ (May 2003). "Chronic exposure to NMDA receptor and sodium channel blockers during development in monkeys and rats: long-term effects on cognitive function". Annals of the New York Academy of Sciences. 993 (1): 116–22, discussion 123–4. doi:10.1111/j.1749-6632.2003.tb07519.x. PMID 12853303. S2CID 19776727.
- ^ a b c d e Stagnitto ML, Palmer GC, Ordy JM, Griffith RC, Napier JJ, Becker CN, et al. (Sep–Oct 1990). "Preclinical profile of remacemide: a novel anticonvulsant effective against maximal electroshock seizures in mice". Epilepsy Research. 7 (1): 11–28. doi:10.1016/0920-1211(90)90050-6. PMID 1963406. S2CID 13657516.
- ^ "The impact of remacemide hydrochloride on levodopa concentrations in Parkinson's disease. Parkinson Study Group". Clinical Neuropharmacology. 22 (4): 220–5. Jul–Aug 1999. PMID 10442252.
- ^ Leach JP, Girvan J, Jamieson V, Jones T, Richens A, Brodie MJ (June 1997). "Lack of pharmacokinetic interaction between remacemide hydrochloride and sodium valproate in epileptic patients". Seizure. 6 (3): 179–84. doi:10.1016/S1059-1311(97)80003-9. PMID 9203245. S2CID 18469302.
- ^ Leach JP, Blacklaw J, Jamieson V, Jones T, Richens A, Brodie MJ (November 1996). "Mutual interaction between remacemide hydrochloride and carbamazepine: two drugs with active metabolites". Epilepsia. 37 (11): 1100–6. doi:10.1111/j.1528-1157.1996.tb01031.x. PMID 8917061. S2CID 23489355.
- ^ Lewis GR, Steele G, McBride L, Florence AJ, Kennedy AR, Shankland N, et al. (1 March 2005). "Hydrophobic vs. Hydrophilic: Ionic Competition in Remacemide Salt Structures". Crystal Growth & Design. 5 (2): 427–438. doi:10.1021/cg049836u.
- ^ Subramaniam S, Donevan SD, Rogawski MA (January 1996). "Block of the N-methyl-D-aspartate receptor by remacemide and its des-glycine metabolite". The Journal of Pharmacology and Experimental Therapeutics. 276 (1): 161–8. PMID 8558426.
- ^ a b Heyn H, McCarthy DJ, Curry SH, Eisman MS, Anders MW (May–Jun 1994). "Brain uptake and biotransformation of remacemide hydrochloride, a novel anticonvulsant". Drug Metabolism and Disposition. 22 (3): 443–6. PMID 8070322.
- ^ van Luijtelaar EL, Coenen AM (April 1995). "Effects of remacemide and its metabolite FPL 12495 on spike-wave discharges, electroencephalogram and behaviour in rats with absence epilepsy". Neuropharmacology. 34 (4): 419–25. doi:10.1016/0028-3908(95)00008-T. hdl:2066/28626. PMID 7566473. S2CID 12067526.
- ^ Hardebo JE, Nilsson B (October 1979). "Estimation of cerebral extraction of circulating compounds by the brain uptake index method: influence of circulation time, volume injection, and cerebral blood flow". Acta Physiologica Scandinavica. 107 (2): 153–9. doi:10.1111/j.1748-1716.1979.tb06455.x. PMID 525379.
- ^ Oldendorf WH, Pardridge WM, Braun LD, Crane PD (May 1982). "Measurement of cerebral glucose utilization using washout after carotid injection in the rat". Journal of Neurochemistry. 38 (5): 1413–8. doi:10.1111/j.1471-4159.1982.tb07920.x. PMID 7062059. S2CID 44670571.
- ^ a b Garske GE, Palmer GC, Napier JJ, Griffith RC, Freedman LR, Harris EW, et al. (September 1991). "Preclinical profile of the anticonvulsant remacemide and its enantiomers in the rat". Epilepsy Research. 9 (3): 161–74. doi:10.1016/0920-1211(91)90050-p. PMID 1660399. S2CID 40219442.
- ^ Hu RQ, Davies JA (December 1995). "The effect of the desglycinyl metabolite of remacemide on cortical wedges prepared from DBA/2 mice". European Journal of Pharmacology. 287 (3): 251–6. doi:10.1016/0014-2999(95)00500-5. PMID 8991798.
- ^ Norris SK, King AE (July 1997). "Electrophysiological effects of the anticonvulsant remacemide hydrochloride and its metabolite ARL 12495AA on rat CA1 hippocampal neurons in vitro". Neuropharmacology. 36 (7): 951–9. doi:10.1016/S0028-3908(97)00069-5. PMID 9257939. S2CID 20522408.
- ^ Leach JP, Sills GJ, Butler E, Forrest G, Thompson GG, Brodie MJ (July 1997). "Neurochemical actions of the desglycinyl metabolite of remacemide hydrochloride (ARL 12495AA) in mouse brain". British Journal of Pharmacology. 121 (5): 923–6. doi:10.1038/sj.bjp.0701219. PMC 1564774. PMID 9222548.
- ^ Norris SK, King AE (June 1997). "The stereo-isomers of the anticonvulsant ARL 12495AA limit sustained repetitive firing and modify action potential properties of rat hippocampal neurons in vitro". The Journal of Pharmacology and Experimental Therapeutics. 281 (3): 1191–8. PMID 9190853.
- ^ "remacemide () UKMi New Drugs Online Database". Retrieved 2 May 2012.
- ^ a b "remacemide AstraZeneca discontinued, Europe, USA, Canada (epilepsy)". R & D Focus Drug News. March 15, 2004. Archived from the original on May 18, 2013. Retrieved 2 May 2012.
- ^ "FISONS DISCONTINUES TIPREDANE DEV'T". the pharma letter. 12 April 1993. Retrieved 28 April 2012.
- ^ a b "Sweden's Astra Buys Most Of Fisons R&D Ops". the pharma letter. 27 March 1995. Retrieved 28 April 2012.
- ^ "AstraZeneca History". AstraZeneca. Retrieved 29 April 2012.
- ^ a b c "AstraZeneca R&D Pipeline: NCEs". AstraZeneca. 2000. Retrieved 28 April 2012.
- ^ Palmer GC, Harris EW, Napier JJ, Stagnitto ML, Garske GE, Griffith RC, Swinyard EA (1990). "Status of PR 934-423, a novel anticonvulsant targeted for generalized tonic/clonic seizures (new designation is FPL 12924AA)". Progress in Clinical and Biological Research. 361: 435–41. PMID 2290849.
- ^ a b Kieburtz K, Feigin A, McDermott M, Como P, Abwender D, Zimmerman C, et al. (May 1996). "A controlled trial of remacemide hydrochloride in Huntington's disease". Movement Disorders. 11 (3): 273–7. doi:10.1002/mds.870110310. PMID 8723144. S2CID 33908305.
- ^ Greenamyre JT, Eller RV, Zhang Z, Ovadia A, Kurlan R, Gash DM (June 1994). "Antiparkinsonian effects of remacemide hydrochloride, a glutamate antagonist, in rodent and primate models of Parkinson's disease". Annals of Neurology. 35 (6): 655–61. doi:10.1002/ana.410350605. PMID 8210221. S2CID 21875296.
- ^ "Completed Clinical Trials". Huntington Study Group. 2010. Archived from the original on 28 June 2012. Retrieved 29 April 2012.
- ^ "Astra 98 Annual Report" (PDF). Stellan Ståls Grafiska AB. Retrieved 28 April 2012.
- ^ Polinsky R. "AstraZeneca CNS". AstraZeneca. Retrieved 27 April 2012.
- ^ "Clinical Trials and Observational Studies in Progress". Huntington Study Group. 2010. Archived from the original on 18 May 2009. Retrieved 29 April 2012.
- ^ "Clinical Trials in Progress - Parkinson Study Group". Archived from the original on 11 September 2011. Retrieved 2 May 2012.
- ^ "Remacemide hydrochloride Cat. No. 1622". Tocris. Retrieved 29 April 2012.


