멜록시캄
Meloxicam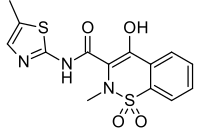 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | 모빅, 메타캄, 무베라, 안제소 등 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a601242년 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 입으로, 정맥주사로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 89%[4] |
| 단백질 결합 | 99.4%[4] |
| 신진대사 | 간(CYP2C9 및 3A4 매개)[4] |
| 제거 반감기 | 20시간[4] |
| 배설 | 소변과 소변은[4] 균등등하다. |
| 식별자 | |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| PDB 리간드 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.113.257 |
| 화학 및 물리적 데이터 | |
| 공식 | C14H13N3O4S2 |
| 어금질량 | 351.40 g·190−1 |
| 3D 모델(JSmol) | |
| | |
멜록시캠은 모빅이라는 상표명으로 판매되는 비스테로이드성 항염증제(NSAID)로 류머티스성 질환과 골관절염의 통증 및 염증을 치료하는 데 쓰인다.[5][6] 구강이나 정맥에 주사하여 쓴다.[6][7] 가능한 한 짧은 기간 동안 적은 용량으로 사용하는 것이 좋다.[6]
일반적인 부작용으로는 복통, 현기증, 붓기, 두통, 발진 등이 있다.[6] 심각한 부작용에는 심장병, 뇌졸중, 신장질환, 위궤양이 포함될 수 있다.[6] 임신 3개월째에는 사용을 권장하지 않는다.[6] 사이클록시겐제2(COX-2)를 차단하는 것보다 더 많이 차단한다(COX-1([6]COX-1) 화학 약품의 난독성 계열에 속하며, 피록시암과 밀접한 관련이 있다.[6]
멜록시캄은 1977년에 특허를 받았으며 2000년에 미국에서 의료용으로 승인되었다.[6][8] Boehringer Ingelheim에 의해 개발되었지만, 일반적인 약으로도 이용 가능하다.[6] 2019년에는 미국에서 2100만 개 이상의 처방전을 받아 31번째로 가장 많이 처방된 약이었다.[9][10] 정맥주사 멜록시암(Anjeso)은 2020년 2월 미국에서 의료용으로 승인되었다.[7]
역효과
멜록시암 사용은 위장 독성과 출혈, 두통, 발진, 그리고 매우 어둡거나 검은 대변(장출혈의 징후)을 일으킬 수 있다. 다른 NSAIDs와 마찬가지로, 이것의 사용은 심장마비나 뇌졸중과 같은 심혈관 질환의 위험 증가와 관련이 있다.[11] 그것은 디클로페낙,[12] 피록시캄,[13] 나프록센,[14] 그리고 아마도 COX-2 선택적이지 않은 모든 다른 NSAID들보다 위장 부작용을 적게 가지고 있다.[12] 멜록시캠은 트롬박산 A의 형성을 억제하지만 혈소판 기능을 방해할 수 있는 수준에서는 그렇게 하지 않는 것으로 보이지 않는다.[15][16]
최대 60일 기간의meloxicam 치료의 임의적인 통제된은 연구들이pooled 분석은 meloxicamthromboembolic 합병증의 NSAIDdiclofenac(대 0.8%0.2%씩)보다 통계적으로 상당히 낮은 번호였지만thromboembolic 행사와 piroxicam naproxen에 비슷한 발병율을 가진 관련된 것을 발견했다.[17]
미국 식품의약국(FDA)은 2020년 10월, 양수가 낮은 태아의 신장 질환 위험을 설명하기 위해 모든 비스테로이드성 항염증 약물에 대해 약물 라벨을 업데이트하도록 요구했다.[18][19] 그들은 임신 20주 혹은 그 이후에 임산부의 NSAIDs를 피하라고 권고한다.[18][19]
심혈관의
고혈압, 고콜레스테롤, 당뇨병을 앓고 있는 사람들은 심혈관 부작용의 위험이 있다. 심장병, 심장마비, 뇌졸중 가족력이 있는 사람들은 심각한 심혈관 부작용의 가능성이 매우 크기 때문에 그들의 치료 의사에게 말해야 한다.[20][21]
위장
NSAIDs는 출혈, 궤양, 위나 장의 천공 등을 포함한 심각한 위장 장애의 위험성을 유발하고 증가시키며, 이것은 치명적일 수 있다. 노인 환자들은 심각한 위장병에 걸릴 위험이 더 크다.[22]
입
미각 변태, 궤양성 구내염, 구강건조증 등의 위험이 높아져 수술이나 치과 시술 전 최소 4~6개의 반감기 사용을 보류하는 것이 좋다.[medical citation needed]
작용기전
멜록시탐은 아라키돈산을 프로스타글란딘 H로2 변환시키는 역할을 하는 효소인 사이클록시제나아제(COX)를 차단하는데, 이는 염증의 매개체인 프로스타글란딘 합성의 첫 단계다. 멜록시캠은 특히 낮은 치료 용량에서 COX-1에 대한 COX-2를 선택적으로 억제하는 것으로 나타났다.[4]
시뉴브럴 액의 멜록시캠 농도는 혈장 농도의 40%에서 50%까지 다양하다. 시노비탈 액의 자유분율은 플라즈마에 비해 시노비탈 액의 알부민 함량이 낮기 때문에 플라즈마보다 2.5배 높다. 이 침투의 의의는 알 수 없지만,[22] 동물 모델에서 관절염 치료에서 예외적으로 좋은 성과를 보인다는 점이 설명될 수 있다.[23]
약동학
흡수
멜록시암의 생물학적 이용가능성은 동등한 IV 볼러스 선량과 비교하여 구강 투여 시 감소한다. 고지방 아침식사 후 구강 멜록시암을 사용하면 평균 최고 약물의 수치가 약 22% 증가하지만, 제조사는 특정한 식사 권장 사항을 제시하지 않는다. 또한 제산제의 사용은 약동학적 상호작용을 나타내지 않는다.[2]
분배
멜록시암의 평균 유통량은 약 10L이다. 알부민에 주로 의존하는 단백질이 풍부하다.[16][24]
신진대사
멜록시암은 효소 CYP2C9와 CYP3A4(미네소)에 의해 4개의 비활성 대사물에 의해 간에서 광범위하게 대사된다. 과산화수소효소 활성은 나머지 두 대사물에 대한 책임이 있는 것으로 생각된다.[2][25]
배설
멜록시암은 주로 대사물의 형태로 배설되며 소변과 대변에서 동일한 범위 내에서 발생한다.[2] 변변치 않은 모약의 흔적이 소변과 대변에서 발견된다.[2] 평균 제거 반감기는 15~20시간이다.[2]
특정 모집단
노인학
75세 이상이나 출혈 위험과 관련된 약을 복용하는 경우를 포함하여 소화성 궤양 질환이나 위장 출혈 위험이 증가된 사람에게는 멜록시캠 사용을 권장하지 않는다.[26] 부작용은 용량에 의존하며 치료 기간과 관련이 있는 것으로 밝혀졌다.[26][2]
수의학용
멜록시엄은 개를 치료하기 위해 수의학에서 사용되지만,[27][28] 소와 외과 동물과 같은 다른 동물들에서도 사용이 금지되어 있는 것으로 보고 있다.[29][30]
가장 흔한 부작용으로는 위장 자극(항문, 설사, 궤양)이 있다.[27]
멜록시엄이 투여된 건강한 개들의 경우 권장 복용량에서 심혈관 시스템에 대한 수술 중 부작용은 보고되지 않았다.[31] 고양이에게 난독증을 투여하는 것은 수술 후 호흡수나 심박수에 영향을 미치지 않았다.[32]
동료가 검토한 한 저널 기사는 멜록시암을 포함한 NSAIDs를 위장 장애를 유발하고, 많은 용량에서 급성 신장 손상의 원인이 되며, 고양이에게 발작과 코마 같은 CNS 징후를 유발한다고 인용한다. 고양이는 NSAID에 대한 내성이 낮다고 덧붙인다.[33][34]
만성 신장질환이 있는 고양이에게 멜록시암을 투여했을 때 신장 배설 기능의 저하가 관찰되지 않았다. 멜록시암을 투여받은 고양이는 위약을 투여받은 고양이보다 단백뇨가 6개월이나 더 많았다. 만성 신장질환이 있는 고양이에게 멜록시엄을 주의 깊게 사용해야 한다는 결론이 나왔다.[35]
멜록시캄은 왕립 조류보호협회(RSPB)가 독수리의 죽음을 막기 위해 디클로페낙의 대안으로 조사를 받았다.[36]
약동학
개의 경우, 위로부터 멜록시암의 흡수는 음식물의 존재에 영향을 받지 않으며,[37] 멜록시암의 최고 농도(Cmax)는 투여 후 7~8시간 후에 혈액에서 발생한다.[37] 멜록시엄의 반감기는 개에서 대략 24시간이다.[37]
코알라(Phascolarctos cinereus)에서는 경구 투여 후 혈액에 흡수되는 멜록시캠이 거의 없다(즉, 생체이용성이 떨어진다).[38]
법적현황
미국
2003년 미국에서는 골관절염과 관련된 통증과 염증 관리를 위해 개에 사용하는 멜록시암의 구강(액체) 제형으로 멜록시암이 승인되었다.[39] 2005년 1월, 제품 인서트에는 "고양이에게는 사용하지 말라"[40]는 굵은 글씨로 경고가 추가되었다. 개에 사용할 수 있는 주입식 제형은 2003년 11월 미국 식품의약국(FDA)에 의해 승인되었다.[41]
2004년 10월, 고양이에게 사용하는 제형이 수술 전에만 사용되도록 승인되었다.[42] 이것은 주입 가능한 멜록시암으로, 1회 복용량만 표시되며, 2회 복용량을 투여하지 말라는 구체적이고 반복적인 경고가 있다.[43]
2005년 미국 식품의약국(FDA)은 라벨 외 사용을 위한 의약품 홍보가 포함된 홍보물에 대해 제조사에 위반 통지서를 보냈다.[44]
2020년 2월, 멜록시암 주사가 미국에서 사용되도록 승인되었다. FDA는 Baudax Bio에 안제소의 승인을 허가했다.[7][45]
유럽 연합
1990년대 초부터 이 제품이 출시된 유럽에서는 개의 급성 및 만성 통증 완화를 포함한 다른 항염증 혜택을 허가받고 있다.[citation needed] 2007년 6월, 고양이들의 고통의 장기적 완화를 위해 구술 버전의 멜록시캠이 허가되었다.[46] 멜록시암은 근골격계 질환과 관련된 통증을 완화하기 위해 말에도 사용이 허가되었다.[47]
멜록시캄은 1998년 1월 중앙집중화된 마케팅 허가를 통해 유럽연합 전체의 소에서 사용이 허가되었다.[48] 최초의 일반 멜록시컴 제품은 2006년에 승인되었다.[48]
다른 나라들
멜록시암은 2008년[update] 6월 현재 호주, 뉴질랜드, 캐나다에서 고양이 장기사용 등록이 되어 있다.[46]
참고 항목
참조
- ^ 임신 및 모유 수유 시 사용
- ^ Jump up to: a b c d e f g "Mobic- meloxicam tablet". DailyMed. Retrieved 15 May 2021.
- ^ "Anjeso- meloxicam injection". DailyMed. Retrieved 15 May 2021.
- ^ Jump up to: a b c d e f Noble S, Balfour JA (March 1996). "Meloxicam". Drugs. 51 (3): 424–30, discussion 431–32. doi:10.2165/00003495-199651030-00007. PMID 8882380.
- ^ British national formulary : BNF 76 (76 ed.). Pharmaceutical Press. 2018. pp. 1112–1113. ISBN 9780857113382.
- ^ Jump up to: a b c d e f g h i j "Meloxicam Monograph for Professionals". Drugs.com. AHFS. Archived from the original on 23 December 2018. Retrieved 23 December 2018.
- ^ Jump up to: a b c "Baudax Bio Announces FDA Approval of Anjeso for the Management of Moderate to Severe Pain". Baudax Bio, Inc. (Press release). 20 February 2020. Archived from the original on 21 February 2020. Retrieved 20 February 2020.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 519. ISBN 9783527607495. Archived from the original on 10 July 2020. Retrieved 30 June 2020.
- ^ "The Top 300 of 2019". ClinCalc. Retrieved 16 October 2021.
- ^ "Meloxicam - Drug Usage Statistics". ClinCalc. Retrieved 16 October 2021.
- ^ Stamm O, Latscha U, Janecek P, Campana A (January 1976). "Development of a special electrode for continuous subcutaneous pH measurement in the infant scalp". American Journal of Obstetrics and Gynecology. 124 (2): 193–5. doi:10.1016/S0002-9378(16)33297-5. PMID 2012.
- ^ Jump up to: a b Hawkey C, Kahan A, Steinbrück K, Alegre C, Baumelou E, Bégaud B, et al. (September 1998). "Gastrointestinal tolerability of meloxicam compared to diclofenac in osteoarthritis patients. International MELISSA Study Group. Meloxicam Large-scale International Study Safety Assessment". British Journal of Rheumatology. 37 (9): 937–45. doi:10.1093/rheumatology/37.9.937. PMID 9783757.
- ^ Dequeker J, Hawkey C, Kahan A, Steinbrück K, Alegre C, Baumelou E, et al. (September 1998). "Improvement in gastrointestinal tolerability of the selective cyclooxygenase (COX)-2 inhibitor, meloxicam, compared with piroxicam: results of the Safety and Efficacy Large-scale Evaluation of COX-inhibiting Therapies (SELECT) trial in osteoarthritis". British Journal of Rheumatology. 37 (9): 946–51. doi:10.1093/rheumatology/37.9.946. PMID 9783758.
- ^ Wojtulewski JA, Schattenkirchner M, Barceló P, Le Loët X, Bevis PJ, Bluhmki E, Distel M (April 1996). "A six-month double-blind trial to compare the efficacy and safety of meloxicam 7.5 mg daily and naproxen 750 mg daily in patients with rheumatoid arthritis". British Journal of Rheumatology. 35 Suppl 1: 22–8. doi:10.1093/rheumatology/35.suppl_1.22. PMID 8630632.
- ^ Zeidan, Anwar Z.; Al Sayed, Bashar; Bargaoui, Naceur; Djebbar, Mourad; Djennane, Malik; Donald, Royden; El Deeb, Khamis; Joudeh, Raed A.; Nabhan, Abdullah; Schug, Stephan A. (April 2013). "A Review of the Efficacy, Safety, and Cost-Effectiveness of COX-2 Inhibitors for Africa and the Middle East Region: COX-2 Inhibitors in Pain Management". Pain Practice. 13 (4): 316–331. doi:10.1111/j.1533-2500.2012.00591.x. PMID 22931375. S2CID 205715393. Retrieved 18 May 2021.
- ^ Jump up to: a b Gates, Brian J.; Nguyen, Trang T.; Setter, Stephen M.; Davies, Neal M. (1 October 2005). "Meloxicam: A reappraisal of pharmacokinetics, efficacy and safety". Expert Opinion on Pharmacotherapy. 6 (12): 2117–2140. doi:10.1517/14656566.6.12.2117. ISSN 1465-6566. PMID 16197363. S2CID 25512189. Retrieved 18 May 2021.
Meloxicam is extensively bound to plasma proteins (99.4%), primarily to albumin. Meloxicam has an apparent volume of distribution (Vd) 10 – 15 l in humans (0.1 – 0.2 l/kg) after oral administration and a mean volume of distribution at steady-state of 0.2 l/kg after intravenous administration."
"None of the meloxicam treatment groups demonstrated inhibition of platelet aggregation to either arachidonic acid (AC) or adenosine diphosphate (ADP). However, there were no significant changes in the platelet count, prothrombin and activated partial thromboplastin time in any of the meloxicam and indomethacin groups. Other crossover studies also confirmed that meloxicam 15 mg/day caused a major reduction of maximum thromboxane production, but no reduction in collagen- or AC-induced platelet aggregation. - ^ Singh G, Lanes S, Triadafilopoulos G (July 2004). "Risk of serious upper gastrointestinal and cardiovascular thromboembolic complications with meloxicam". The American Journal of Medicine. 117 (2): 100–6. doi:10.1016/j.amjmed.2004.03.012. PMID 15234645.
- ^ Jump up to: a b "FDA Warns that Using a Type of Pain and Fever Medication in Second Half of Pregnancy Could Lead to Complications". U.S. Food and Drug Administration (FDA) (Press release). 15 October 2020. Retrieved 15 October 2020.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ Jump up to: a b "NSAIDs may cause rare kidney problems in unborn babies". U.S. Food and Drug Administration. 21 July 2017. Retrieved 15 October 2020.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ "Meloxicam". MedlinePlus. Archived from the original on 29 November 2014. Retrieved 15 November 2014.
- ^ "Meloxicam". Drugs.com. Archived from the original on 16 November 2014. Retrieved 15 November 2014.
- ^ Jump up to: a b "Meloxicam official FDA information, side effects, and uses". Drugs.com. March 2010. Archived from the original on 16 March 2010. Retrieved 17 March 2010.
- ^ Engelhardt G, Homma D, Schlegel K, Utzmann R, Schnitzler C (October 1995). "Anti-inflammatory, analgesic, antipyretic and related properties of meloxicam, a new non-steroidal anti-inflammatory agent with favourable gastrointestinal tolerance". Inflammation Research. 44 (10): 423–33. doi:10.1007/BF01757699. PMID 8564518. S2CID 37937305.
- ^ Bekker, Alex; Kloepping, Carolyn; Collingwood, Shemille (2018). "Meloxicam in the management of post-operative pain: Narrative review". Journal of Anaesthesiology Clinical Pharmacology. 34 (4): 450–457. doi:10.4103/joacp.JOACP_133_18. ISSN 2231-2730. PMC 6360894. PMID 30774225.
- ^ "Meloxicam (Professional Patient Advice)". Drugs.com. Archived from the original on 6 August 2019. Retrieved 6 August 2019.
- ^ Jump up to: a b 2019 American Geriatrics Society Beers Criteria Update Expert Panel (April 2019). "American Geriatrics Society 2019 Updated AGS Beers Criteria® for Potentially Inappropriate Medication Use in Older Adults". Journal of the American Geriatrics Society. 67 (4): 674–694. doi:10.1111/jgs.15767. PMID 30693946. S2CID 59338182.
- ^ Jump up to: a b "Metacam- meloxicam suspension". DailyMed. Retrieved 15 May 2021.
- ^ "Metacam- meloxicam injection, solution". DailyMed. Retrieved 15 May 2021.
- ^ Off-label use discussed in: Arnold Plotnick MS, DVM, ACVIM, ABVP, Pain Management using Metacam Archived 14 July 2011 at the Wayback Machine, and Stein, Robert, Perioperative Pain Management Archived 18 April 2010 at the Wayback Machine Part IV, Looking Beyond Butorphanol, Sep 2006, Veterinary Anesthesia & Analgesia Support Group.
- ^ 토끼에 대한 오프라벨 사용 예는 마이애미 대학 생물학과의 웨이백 머신에서 2010년 6월 17일 보관된 토끼의 크렘펠, 다나, 힌드 림 파레시스 및 마비를 참조하십시오.
- ^ Boström IM, Nyman G, Hoppe A, Lord P (January 2006). "Effects of meloxicam on renal function in dogs with hypotension during anaesthesia". Veterinary Anaesthesia and Analgesia. 33 (1): 62–9. doi:10.1111/j.1467-2995.2005.00208.x. PMID 16412133.
- ^ Höglund OV, Dyall B, Gräsman V, Edner A, Olsson U, Höglund K (October 2018). "Effect of non-steroidal anti-inflammatory drugs on postoperative respiratory and heart rate in cats subjected to ovariohysterectomy". Journal of Feline Medicine and Surgery. 20 (10): 980–984. doi:10.1177/1098612X17742290. PMID 29165006. S2CID 30649716.
- ^ "Toxicology Brief: The 10 most common toxicoses in cats". Dvm360. 1 June 2006. Archived from the original on 29 August 2018. Retrieved 16 September 2018.
- ^ Merola V, Dunayer E (June 2006). "The 10 most common toxicoses in cats" (PDF). Veterinary Medicine: 340–342. Archived (PDF) from the original on 9 August 2019. Retrieved 9 August 2019.
- ^ KuKanich, Kate; George, Christopher; Roush, James K; Sharp, Sherry; Farace, Giosi; Yerramilli, Murthy; Peterson, Sarah; Grauer, Gregory F (29 June 2020). "Effects of low-dose meloxicam in cats with chronic kidney disease". Journal of Feline Medicine and Surgery. 23 (2): 138–148. doi:10.1177/1098612X20935750. PMID 32594827. S2CID 220256059.
- ^ Swan G, Naidoo V, Cuthbert R, Green RE, Pain DJ, Swarup D, et al. (March 2006). "Removing the threat of diclofenac to critically endangered Asian vultures". PLOS Biology. 4 (3): e66. doi:10.1371/journal.pbio.0040066. PMC 1351921. PMID 16435886.
- ^ Jump up to: a b c Khan SA, McLean MK (March 2012). "Toxicology of frequently encountered nonsteroidal anti-inflammatory drugs in dogs and cats". The Veterinary Clinics of North America. Small Animal Practice. 42 (2): 289–306, vi–vii. doi:10.1016/j.cvsm.2012.01.003. PMID 22381180.
- ^ Kimble B, Black LA, Li KM, Valtchev P, Gilchrist S, Gillett A, et al. (October 2013). "Pharmacokinetics of meloxicam in koalas (Phascolarctos cinereus) after intravenous, subcutaneous and oral administration". Journal of Veterinary Pharmacology and Therapeutics. 36 (5): 486–93. doi:10.1111/jvp.12038. PMID 23406022.
- ^ "NADA 141-213: New Animal Drug Application Approval (for Metacam (meloxicam) 0.5 mg/mL and 1.5 mg/mL Oral Suspension)" (PDF). Food and Drug Administration (FDA). 15 April 2003. Archived from the original (PDF) on 6 April 2017. Retrieved 24 July 2010.
- ^ "Client Information Sheet For Metacam (meloxicam) 1.5 mg/mL Oral Suspension" (PDF). Food and Drug Administration (FDA). January 2005. Archived from the original (PDF) on 15 November 2017.
Metacam is a prescription non-steroidal anti-inflammatory drug (NSAID) that is used to control pain and inflammation (soreness) due to osteoarthritis in dogs. Osteoarthritis (OA) is a painful condition caused by “wear and tear” of cartilage and other parts of the joints that may result in the following changes or signs in your dog: Limping or lameness, decreased activity or exercise (reluctance to stand, climb stairs, jump or run, or difficulty in performing these activities), stiffness or decreased movement of joints. Metacam is given to dogs by mouth. Do not use Metacam Oral Suspension in cats. Acute kidney injury and death have been associated with the use of meloxicam in cats.
- ^ "NADA 141-219: Metacam (meloxicam) 5 mg/mL Solution for Injection" (PDF). U.S. Food and Drug Administration (FDA). 12 November 2003. Archived from the original (PDF) on 15 November 2017. Retrieved 8 August 2019.
- ^ "Metacam 5 mg/mL Solution for Injection, Supplemental Approval" (PDF). U.S. Food and Drug Administration (FDA). 28 October 2004. Archived from the original (PDF) on 15 November 2017. Retrieved 8 August 2019.
- ^ 웹 사이트의 웨이백 머신에서 2011년 7월 2일 보관된 제조업체의 FAQ 및 고양이를 위한 임상 투여 지침을 참조하십시오. 2008년 9월 6일 웨이백 머신에 보관
- ^ "Notice of Violation" (PDF). U.S. Food and Drug Administration (FDA). 19 April 2005. Archived from the original (PDF) on 13 January 2017. Retrieved 8 August 2019.
- ^ "Anjeso (meloxicam) injection, for intravenous use" (PDF). U.S. Food and Drug Administration (FDA). February 2020. Archived (PDF) from the original on 22 February 2020. Retrieved 21 February 2020.
- ^ Jump up to: a b Gaschen FP, Schaer M, eds. (2016). "Recent NSAID developments". Clinical medicine of the dog and cat (3rd ed.). CRC Press. ISBN 9781482226065. Archived from the original on 1 September 2020. Retrieved 28 January 2020.
- ^ Maddison JE, Page SW, Church D, eds. (2008). "Meloxicam". Small animal clinical pharmacology (2nd ed.). Edinburgh: Saunders/Elsevier. pp. 301–302. ISBN 9780702028588.
- ^ Jump up to: a b Wright E (March 2007). "Generic and biosimilar medicinal products in the European Union" (PDF). Chemistry Today. 25 (2): 4–6. Archived (PDF) from the original on 28 January 2020. Retrieved 28 January 2020.
외부 링크
- "Meloxicam". Drug Information Portal. U.S. National Library of Medicine.


