콜린
Choline
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 2-히드록시-N,N,N-트리메틸탄-1-아미늄 | |
| 기타 이름 2-히드록시-N, N, N-트리메틸레타미늄 빌리뉴린 (2-히드록시에틸)트리메틸암모늄 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 1736748 | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| ECHA 정보 카드 | 100.000.487 |
| EC 번호 |
|
| 324597 | |
| 케그 | |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 채널514+ | |
| 몰 질량 | 104.17 g/g |
| 외모 | 점성 조해액(수산화콜린)[1] |
| 매우 용해성(수산화콜린)[1] | |
| 용해성 | 에탄올에 [1]녹는, 디에틸에테르 및 클로로포름([2]수산화콜린)에 녹지 않는 |
| 위험 요소 | |
| GHS 라벨링: | |
 | |
| 위험. | |
| H314 | |
| P260, , , , , , , , , | |
| NFPA 704(파이어 다이아몬드) | |
| 치사량 또는 농도(LD, LC): | |
LD50(중간선량) | 3~6g/kg, 쥐[1], 경구 |
| 안전 데이터 시트(SDS) | 4 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
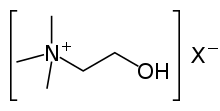
콜린은 인간과 다른 많은 [4]동물들에게 필수적인 영양소입니다.[3]콜린은 다양한 염분을 형성하는 양이온으로 발생한다(그림의− 식에서 X는 정의되지 않은 대항 [5]음이온이다).건강을 유지하기 위해, 그것은 콜린이나 포스파티딜콜린과 [4]같은 콜린 인지질로서 식단에서 얻어져야 한다.대부분의 다른 동물 종들뿐만 아니라 인간들도 콜린 드 노보를 만들지만, 일반적으로 생산량이 부족하다.콜린은 종종 비타민으로 분류되지 않고 아미노산과 같은 [2]신진대사를 하는 영양소로 분류된다.대부분의 동물에서 콜린 인지질은 세포막, 세포소기관막, 그리고 매우 저밀도 지방단백질에서 [4]필요한 구성요소이다.콜린은 신경전달물질인 아세틸콜린과 보편적인 메틸 공여물질인 S-아데노실메티오닌(SAM)을 생산하기 위해 필요하다.메틸화 시 SAM은 호모시스테인으로 변환된다.
증상적인 콜린 결핍은 사람에게서 드물게 비알코올성 지방간 질환과 근육 [4]손상을 일으킨다.콜린(7.5g/일 이상)의 과다 섭취는 [4][6]트리메틸아민으로 인해 저혈압, 발한, 설사 및 생선 같은 체취를 유발할 수 있습니다.콜린과 콜린 인지질의 풍부한 식이 공급원은 장기 고기, 계란 노른자, 유제품, 땅콩, 특정 콩, 견과류, 씨앗, 그리고 파스타와 쌀이 포함된 야채도 미국 식단의 [4][7]콜린 섭취에 기여한다.
화학
콜린은 수용성 4급 암모늄 [5][8]화합물 과입니다.콜린은 콜린 클래스의 모화합물로, 아미노 [9]기능에 3개의 메틸 치환기를 가진 에탄올아민으로 구성됩니다.수산화콜린은 콜린 염기로 알려져 있다.이것은 흡습성이기 때문에 트리메틸아민(TMA) 냄새가 나는 무색의 점성 수화 시럽으로 자주 볼 수 있습니다.콜린 수용액은 안정적이지만 에틸렌 글리콜, 폴리에틸렌 글리콜, [1]TMA로 서서히 분해된다.
염화콜린은 TMA를 [1]2-클로로에탄올로 처리하여 만들 수 있습니다.
- (CH3)3N + ClCHCHOH22 → (CH3)3NCHOH+22 · Cl–
2-클로로에탄올은 산화 에틸렌에서 생성될 수 있습니다.콜린은 역사적으로 레시틴의 [1]가수분해와 같은 자연 소스에서 생산되었다.
대사
생합성
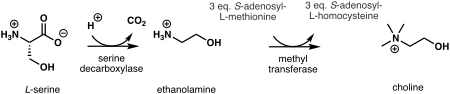
식물에서 콜린 데노보 생합성의 첫 번째 단계는 세린을 에탄올아민으로 탈탄산화시키는 것이며, 세린 탈탄산화효소에 [10]의해 촉매된다.에탄올아민으로부터의 콜린 합성은 세 가지 병렬 경로에서 발생할 수 있으며, 메틸전달효소에 의해 촉매되는 세 가지 연속 N-메틸화 단계는 유리염기,[11][12] 포스포염기 또는 포스파티딜기 [13]중 하나에 대해 수행된다.메틸기의 공급원은 S-아데노실-L-메티오닌이며,[14] 부생성물로 S-아데노실-L-호모시스테인이 생성된다.
인간과 대부분의 다른 동물에서 콜린의 데노보 합성은 포스파티딜레타놀라민 N-메틸전달효소([6]PEMT) 경로를 통해 이루어지지만, 생합성은 인간의 [15]요구 사항을 충족하기에 충분하지 않다.간 PEMT 경로에서 3-포스포글리세린산(3PG)은 인산기를 형성하는 아실-CoA로부터 2개의 아실기를 받는다.그것은 시티딘 삼인산과 반응하여 시티딘 이인산 디아실글리세롤을 형성한다.히드록실기는 세린과 반응하여 포스파티딜세린을 형성하고, 포스파티딜세린은 에탄올아민 및 포스파티딜에탄올아민(PE)으로 탈탄산화된다.PEMT 효소는 3개의 S-아데노실메티오닌(SAM) 공여자에서 포스파티딜타놀아민의 에탄올아민기로 3개의 메틸기를 이동하여 포스파티딜콜린 형태로 콜린을 형성한다.부산물로 [6]3개의 S-아데노실호모시스테인(SAH)을 형성한다.
콜린은 또한 분자를 포함한 더 복잡한 콜린으로부터 방출될 수 있다.예를 들어 포스파티딜콜린(PC)은 대부분의 세포 유형에서 콜린(Coline)으로 가수분해될 수 있다.콜린은 또한 CDP-콜린 경로, 세포질 콜린 키나아제(CK)가 ATP에서 포스포콜린(PCHOL)[2]으로 콜린을 인산화함으로써 생성될 수 있다.이것은 간과 신장과 같은 일부 세포 유형에서 발생한다.콜린인산시티딜전달효소(CPCT)는 시티딘3인산(CTP)에 의해 PC홀을 CDP-콜린(CDP-Coline)으로 변환한다.디아실글리세롤콜린포스포트랜스퍼라아제(CPT)[6]에 의해 CDP-콜린 및 디글리세라이드가 PC로 변환된다.
인간의 경우, 특정 PEMT 효소 돌연변이와 에스트로겐 결핍(종종 폐경으로 인한)은 콜린의 식이 수요를 증가시킨다.설치류에서 포스파티딜콜린의 70%는 PEMT 경로를 통해 형성되고 30%만이 CDP-콜린 [6]경로를 통해 형성된다.녹아웃 생쥐에서 PEMT 불활성화는 그들을 완전히 식이콜린에 [2]의존하게 만든다.
흡수.
사람의 경우 콜린 농도 구배 및 장세포막 전체의 전위에 의해 제어되는 촉진 확산에 의해 콜린은 SLC44A1(CTL1)막 단백질을 통해 장에서 흡수된다.SLC44A1은 콜린 운반 능력이 제한되어 있어 고농도에서는 일부가 흡수되지 않은 상태로 남아 있습니다.흡수된 콜린은 간문맥을 통해 장세포를 떠나 간을 지나 전신순환으로 들어간다.내장 미생물은 흡수되지 않은 콜린을 트리메틸아민으로 분해하고, 트리메틸아민은 간에서 산화되어 트리메틸아민 [6]N-옥시드로 분해합니다.
포스포콜린과 글리세로포스포콜린은 포스포리파아제(phospolipase)를 통해 가수분해돼 간문맥으로 들어간다.수용성 때문에 일부는 문맥으로 변하지 않고 빠져나간다.지용성 콜린 함유 화합물(포스파티딜콜린 및 스핑고미엘린)은 포스포리파아제(phospolipase)[6]에 의해 가수분해되거나 카이로미크론에 포함된 림프에 들어간다.
운송
인간에게서 콜린은 혈액 속의 자유 분자로 운반된다.콜린 함유 인지질 및 글리세로포스포콜린과 같은 다른 물질들은 혈중 리포단백질에서 운반된다.건강한 공복 성인의 혈장 콜린 수치는 l당 7-20 마이크로몰(μmol/l)이고 평균 10 μmol/l이다.수치는 조절되지만, 콜린 섭취와 결핍은 이러한 수치를 변화시킨다.콜린 섭취 후 약 3시간 동안 수치가 상승합니다.단식 성인의 혈장 내 포스파티딜콜린 수치는 1.5–2.5 mmol/l이다.그것의 섭취는 약 8-12시간 동안 유리콜린 수치를 증가시키지만, 포스파티딜콜린 수치에는 [6]큰 영향을 미치지 않는다.
콜린은 수용성 이온이기 때문에 운반체가 지용성 세포막을 통과해야 합니다.콜린 운반체에는 세 가지 유형이 [16]알려져 있습니다.
SLC5A7은 나트륨(Na+) 및 ATP 의존성 운반체이다.[16][6]그것들은 콜린에 대한 높은 결합 친화력을 가지고 있으며, 주로 뉴런으로 운반되며, 아세틸콜린 [6]생산과 간접적으로 관련이 있습니다.그들의 부족한 기능은 아세틸콜린 결핍을 통해 폐와 다른 근육에 유전적 약화를 일으킨다.녹아웃 생쥐의 경우, 그들의 기능 장애는 청색증과 [17]마비로 쉽게 사망에 이르게 된다.
CTL1은 콜린에 대해 적당한 친화력을 가지고 있으며 장, 간, 신장, 태반, 그리고 미토콘드리아를 포함한 거의 모든 조직에서 콜린을 운반한다.CTL1s는 포스파티딜콜린과 트리메틸글리신 [6]생산을 위한 콜린을 공급한다.CTL2는 특히 혀, 신장, 근육, 심장의 미토콘드리아에서 발생한다.그것들은 콜린에서 트리메틸글리신으로의 미토콘드리아 산화와 관련이 있다.CTL1s와 CTL2s는 아세틸콜린 생성과 관련이 없지만 혈액-뇌 장벽을 통해 콜린을 함께 운반한다.CTL2만 장벽의 뇌 쪽에서 발생합니다.그들은 또한 과도한 콜린을 뉴런에서 혈액으로 다시 제거한다.CTL1은 장벽의 혈액 쪽에서만 발생하지만 성상세포와 [16]뉴런의 막에서도 발생한다.
OCT1과 OCT2는 아세틸콜린 [6]생성과 관련이 없습니다.그들은 친화력이 낮은 콜린을 운반한다.OCT1은 주로 간과 신장에서 콜린을 운반하고 OCT2는 신장과 [16]뇌에서 운반한다.
보관소
콜린은 인지질로서 세포막과 세포기관에 저장되며, 포스파티딜콜린과 글리세로포스포스포콜린으로서 [6]세포 내부에 저장된다.
배설물
2~8g의 콜린 용량에서도 사람의 소변으로 소량의 콜린이 배설된다.배설은 신장 내에서 발생하는 운반체를 통해 발생합니다(수송 참조).트리메틸글리신은 간과 신장에서 디메틸글리신으로 탈메틸화된다(테트라히드로폴레이트는 메틸기 중 하나를 받는다).메틸글리신은 형성되거나 소변으로 배설되거나 글리신으로 [6]탈메틸화된다.
기능.
콜린과 그 유도체들은 인간과 다른 유기체에 많은 기능을 가지고 있다.가장 주목할 만한 기능은 콜린이 세포막을 형성하는 인지질, 신경전달물질 아세틸콜린, 그리고 삼투압조절기 트리메틸글리신(베타인)과 같은 다른 필수 세포 성분과 신호 전달 분자에 대한 합성 전구체 역할을 한다는 것입니다.트리메틸글리신은 차례로 [18][19]S-아데노실메티오닌의 생합성에 참여함으로써 메틸기의 공급원으로서의 역할을 한다.
인지질 전구체
콜린은 포스파티딜콜린과 스핑고미엘린과 같은 다른 인지질들로 변환됩니다.이것들은 모든 세포막과 대부분의 [2]세포소기관막에서 발견됩니다.포스파티딜콜린은 세포막의 구조적으로 중요한 부분이다.인간의 인지질의 40~50%는 포스파티딜콜린이다.[6]
콜린 인지질 또한 콜레스테롤과 함께 세포막에 지질 뗏목을 형성합니다.뗏목은 수용체 및 수용체 신호 전달 [2]효소의 중심이다.
포스파티딜콜린은 VLDL의 합성에 필요하다: 인지질의 70-95%는 인간의 [6]포스파티딜콜린이다.
콜린은 또한 대부분 포스파티딜콜린으로 구성된 혼합물인 폐계면활성제의 합성에 필요하다.계면활성제는 폐의 탄력성, 즉 폐 조직의 수축과 팽창 능력을 담당합니다.예를 들어 폐조직의 포스파티딜콜린 결핍은 급성호흡곤란증후군과 [20]관련이 있다.
포스파티딜콜린은 담즙으로 배설되어 그 속의 계면활성제로서 담즙산염과 함께 작용하여 지질 [2]흡수를 돕는다.
아세틸콜린 합성
콜린은 아세틸콜린을 생산하기 위해 필요하다.예를 들어,[6] 이것은 근육 수축, 기억력, 신경 발달에 필요한 역할을 하는 신경 전달 물질이다.그럼에도 불구하고, 인체에는 [2]다른 형태의 콜린에 비해 아세틸콜린이 거의 없다.뉴런은 또한 아세틸콜린을 [6]생산하기 위해 인지질 형태의 콜린을 세포막에 저장한다.
트리메틸글리신 소스
사람의 경우 콜린은 간 미토콘드리아에서 콜린산화효소에 의해 글리신 베타인 알데히드로 불가역적으로 산화된다.이것은 미토콘드리아 또는 사이토솔릭 베타인 알데히드 탈수소효소에 의해 트리메틸글리신으로 [6]산화된다.트리메틸글리신은 필요한 삼투압 조절기입니다.그것은 또한 호모시스테인을 메티오닌으로 메틸화하는 BHMT-효소 기질로 작용한다.S-아데노실메티오닌(SAM) 전구체입니다.SAM은 생물학적 메틸화 반응에서 일반적인 시약이다.예를 들어, 그것은 DNA의 구아니딘과 히스톤의 특정 리신을 메틸화한다.그래서 그것은 유전자 발현과 후생유전학적 조절의 일부이다.따라서 콜린 결핍은 혈중 [6]호모시스테인 수치를 높이고 SAM 수치를 감소시킨다.
식품의 함량
콜린은 특히 포스파티딜콜린과 같은 인지질의 형태로 음식에서 발생합니다.콜린은 비장기 고기, 곡물, 채소, 과일, 유제품에서 덜 발견되지만 장기 고기와 계란 노른자에서 가장 높다.식용유와 다른 식용유에는 총 콜린 [6]100g당 약 5mg이 들어 있습니다.미국에서 식품 라벨은 1일 550mg의 적정 섭취량을 기준으로 일일 가치(%DV)의 백분율로 나타낸다.하루 값의 100%는 음식 한 접시에 550mg의 [21]콜린이 함유되어 있다는 것을 의미한다.
인간의 모유에는 콜린이 풍부합니다.모유 수유는 아기에게 하루에 약 120mg의 콜린을 먹이는 것에 해당합니다.산모의 콜린 섭취량이 증가하면 모유의 콜린 함량이 증가하고 낮은 섭취량은 [6]감소한다.영아용 조제 분유는 충분한 콜린을 포함할 수도 있고 포함하지 않을 수도 있다.EU와 미국에서는 모든 영아용 조제 분유에 100kcal당 최소 7mg의 콜린을 의무적으로 첨가해야 한다.EU에서는 50mg/100kcal 이상의 수치는 [6][22]허용되지 않습니다.
트리메틸글리신은 콜린의 기능성 대사물이다.그것은 영양적으로는 콜린 대신이지만,[2] 일부만 대체한다.예를 [23]들어 많은 양의 트리메틸글리신은 밀겨(1,339mg/100g), 구운 밀 배아(1,240mg/100g), 시금치(600–645mg/100g)에서 발생한다.
| 고기 | 야채들 | ||
|---|---|---|---|
| 베이컨, 조리 | 124.89 | 콩, 스냅 | 13.46 |
| 쇠고기, 잘라낸 것, 익힌 것 | 78.15 | 비트루트 | 6.01 |
| 쇠고기 간, 프라이팬 | 418.22 | 브로콜리 | 40.06 |
| 닭고기, 로스팅, 껍질 포함 | 65.83 | 방울새싹 | 40.61 |
| 닭고기, 로스팅, 껍질 벗기기 | 78.74 | 양배추 | 15.45 |
| 닭간 | 290.03 | 당근 | 8.79 |
| 대구, 대서양 | 83.63 | 콜리플라워 | 39.10 |
| 다진 쇠고기, 75~85%의 기름기 없는 구운 고기 | 79.32–82.35 | 스위트콘, 옐로우 | 21.95 |
| 돼지등심 요리 | 102.76 | 오이 | 5.95 |
| 새우, 통조림 | 70.60 | 상추, 빙산 | 6.70 |
| 유제품(소) | 상추, 로메인 | 9.92 | |
| 버터, 소금에 절인 | 18.77 | 완두콩 | 27.51 |
| 치즈 | 16.50–27.21 | 사우어크라우트 | 10.39 |
| 코티지 치즈 | 18.42 | 시금치 | 22.08 |
| 우유, 통/슬림 | 14.29–16.40 | 고구마 | 13.11 |
| 사워크림 | 20.33 | 토마토 | 6.74 |
| 요구르트 플레인 | 15.20 | 애호박 | 9.36 |
| 곡류. | 과일들 | ||
| 귀리겨, 생 | 58.57 | 사과 | 3.44 |
| 귀리, 플레인 | 7.42 | 아보카도 | 14.18 |
| 쌀, 흰자 | 2.08 | 바나나 | 9.76 |
| 쌀, 갈색 | 9.22 | 블루베리 | 6.04 |
| 밀 겨 | 74.39 | 칸탈루페 | 7.58 |
| 밀배아, 구운 것 | 152.08 | 포도 | 7.53 |
| 다른이들 | 자몽 | 5.63 | |
| 빈, 네이비 | 26.93 | 오렌지 | 8.38 |
| 계란, 암탉 | 251.00 | 복숭아 | 6.10 |
| 올리브유 | 0.29 | 먹는 배 | 5.11 |
| 땅콩 | 52.47 | 가지치기 | 9.66 |
| 콩, 생 | 115.87 | 딸기 | 5.65 |
| 두부, 말랑말랑 | 27.37 | 수박 | 4.07 |
- ^ 특별히 언급하지 않는 한 음식은 날 것이다.함유량은 인지질을 포함한 유리콜린과 콜린의 대략적인 양이다.
일별 값
아래 표에는 새로운 일일 가치 및 새로운 영양 팩트 및 보충 팩트 [21]라벨을 반영하기 위해 업데이트된 콜린 소스가 포함되어 있습니다.이는 미국 농무부 농업연구국의 데이터를 반영한다.FoodData Central,[21] 2019년.
| 음식. | 1인분당 밀리그램(mg) | DV 비율* |
| 쇠고기 간, 프라이팬 프라이드, 3온스(85g) | 356 | 65 |
| 달걀, 완숙, 큰 달걀 1개 | 147 | 27 |
| 쇠고기 윗부분 둥근, 분리 가능한 살코기만, 조림, 3온스(85g) | 117 | 21 |
| 콩, 볶음,1⁄2컵 | 107 | 19 |
| 닭가슴살, 로스팅, 3온스(85g) | 72 | 13 |
| 쇠고기, 분쇄, 살코기 93%, 구이, 3온스(85g) | 72 | 13 |
| 대구, 대서양, 조리, 건열, 3온스(85g) | 71 | 13 |
| 버섯, 표고버섯, 익힌 것, 1/2컵 | 58 | 11 |
| 감자, 빨강, 구운 것, 살과 껍질, 큰 감자 1개 | 57 | 10 |
| 밀배아, 토스트, 1온스(28g) | 51 | 9 |
| 콩, 신장, 통조림, 1/2컵 | 45 | 8 |
| 퀴노아 요리 1컵 | 43 | 8 |
| 우유, 1% 지방, 1컵 | 43 | 8 |
| 요구르트, 바닐라, 무지방 1컵 | 38 | 7 |
| 방울양배추, 삶은 것, 1/2컵 | 32 | 6 |
| 브로콜리, 다진 것, 삶은 것, 물기를 뺀 것, 1/2컵 | 31 | 6 |
| 코티지 치즈 무지방 1컵 | 26 | 5 |
| 참치, 흰색, 물에 통조림, 고형물에서 물기를 뺀 것, 3온스(85g) | 25 | 5 |
| 땅콩, 드라이 로스팅, 1/4컵 | 24 | 4 |
| 콜리플라워, 1인치(2.5cm), 삶은 것, 물기를 뺀 것, 1⁄2컵 | 24 | 4 |
| 완두콩, 그린, 삶은 것, 1/2컵 | 24 | 4 |
| 해바라기씨, 기름구이, 1/4컵 | 19 | 3 |
| 밥, 갈색, 긴 알갱이, 익힌 것, 1개 | 19 | 3 |
| 빵, 피타, 통밀, 대형 1개(6+1⁄2인치 또는 직경 17cm) | 17 | 3 |
| 양배추, 삶은 것, 1/2컵 | 15 | 3 |
| 귤(만다린 오렌지), 섹션, 1~2컵 | 10 | 2 |
| 콩, 스냅, 생, 1/2컵 | 8 | 1 |
| 키위프루트, 생, 슬라이스 1/2컵 | 7 | 1 |
| 당근, 생, 다진 것, 1/2컵 | 6 | 1 |
| 사과, 생, 껍질째, 사등분 또는 다진 것, 1⁄2컵 | 2 | 0 |
DV = 일별 값입니다.미국 식품의약국(FDA)은 소비자들이 식품과 식이 보조제의 영양성분을 전체 식단의 맥락에서 비교할 수 있도록 돕기 위해 DVs를 개발했다.콜린 DV는 4세 이상 [citation needed]성인과 어린이의 경우 550mg입니다.FDA는 식품에 콜린이 첨가되지 않은 한 식품 라벨에 콜린 함량을 표시하도록 요구하지 않는다.DV의 20% 이상을 제공하는 음식은 영양소의 높은 공급원으로 간주되지만, DV의 낮은 비율을 제공하는 음식 또한 건강한 [21]식단에 기여합니다.
미국 농무부(USDA)의 식품 데이터 센터(FoodData Central)는 많은 식품의 영양소 함량을 나열하고 영양소 [21]함량별로 배열된 콜린을 포함한 식품의 포괄적인 목록을 제공합니다.
권장 식단
권장량은 1일 밀리그램(mg/일)입니다.유럽식품안전청(EFSA) 권고사항은 EU 국가들에 대한 일반적인 권고사항이다.EFSA는 섭취 [6]상한치를 설정하지 않았습니다.개별 EU 국가들은 보다 구체적인 권고사항을 가지고 있을 수 있다.National Academy of Medicine(NAM) 권장사항은 미국, [21]호주 및 [24]뉴질랜드에 적용됩니다.
| 나이 | EFSA 적정[6] 섭취량 | US NAM의 적절한[21] 섭취량 | US NAM 허용 상한 흡기[21] 레벨 |
|---|---|---|---|
| 영유아 | |||
| 0 ~ 6개월 | 미확립 | 125 | 미확립 |
| 7~12개월 | 160 | 150 | 미확립 |
| 1 ~ 3년 | 140 | 200 | 1,000 |
| 4 ~ 6년 | 170 | 250 | 1,000 |
| 7~8년 | 250 | 250 | 1,000 |
| 9~10년 | 250 | 375 | 1,000 |
| 11~13년 | 340 | 375 | 2,000 |
| 남성 | |||
| 14년 | 340 | 550 | 3,000 |
| 15~18년 | 400 | 550 | 3,000 |
| 19년 이상 | 400 | 550 | 3,500 |
| 여성 | |||
| 14년 | 340 | 400 | 3,000 |
| 15~18년 | 400 | 400 | 3,000 |
| 19 + y | 400 | 425 | 3,500 |
| 임신한 경우 | 480 | 450 | 3,500 (18년 이하의 경우 3,000) |
| 모유 수유인 경우 | 520 | 550 | 3,500 (18년 이하의 경우 3,000) |
모집단에서의 섭취량
2000년과 2011년 사이에 9개 EU 국가에서 수행된 12개 조사에 따르면 이들 국가의 성인의 콜린 섭취량은 하루 269-468mg으로 추정됐다.섭취량은 성인 여성이 269–444mg/일, 성인 남성이 332–468mg/일이었다.섭취량은 유아에서 하루 75–127mg, 1~3세에서는 151–210mg, 3-10세에서는 177–304mg, 10~18세에서는 244–373mg이었다.총 콜린 섭취 평균 추정치는 임산부 청소년의 경우 하루 336mg, 임산부의 [6]경우 하루 356mg이었다.
NHNES 2009-2012 조사에 기초한 연구는 일부 미국 하위 모집단에서 콜린 섭취량이 너무 낮다고 추정했다.이 기간 동안 섭취량은 2세 이상에서 315.2–318.8mg/d였다.2세 이상 어린이 중 남성의 15.6±0.8%, 여성의 6.1±0.6%만이 적정 섭취량(AI)을 초과했다.AI는 2~3세 62.9±3.1%, 4~8세 45.4±1.6%, 9~13세 9.0±1.0%, 14~18세 1.8±0.4%, 19세 이상 6.6±0.5%가 초과했다.어떤 하위 [25]집단에서도 상한 섭취량을 초과하지 않았다.
2013-2014년 미국 인구에 대한 NHNES 연구에 따르면, 2세에서 19세 사이의 콜린 섭취량은 하루에 256±3.8mg, 성인 20세 이상에서는 339±3.9mg이었다.섭취량은 남성 20 이상에서 402±6.1mg/d, 여성 20 [26]이상에서 278mg/d였다.
부족.
징후 및 증상
증상적인 콜린 결핍은 인간에게 드물다.대부분은 충분한 양의 음식을 섭취하고 제한된 양의 [2]음식을 생합성할 수 있다.증상적 결핍은 종종 특정 질병이나 다른 간접적인 원인에 의해 야기된다.심각한 결핍은 근육 손상과 간경화로 [27]발전할 수 있는 비알코올성 지방간 질환을 일으킨다.
인간 외에도 지방간은 다른 동물들의 콜린 결핍의 전형적인 징후이다.신장에서 출혈은 또한 몇몇 종에서 발생할 수 있다.이는 삼투압 [2]조절기 역할을 하는 콜린 유도 트리메틸글리신의 결핍으로 인한 것으로 추정된다.
원인과 메커니즘
에스트로겐 생산은 낮은 식단 콜린 섭취와 함께 개인에게 결핍을 유발하는 관련 요인이다.에스트로겐은 PEMT 효소를 생성하는 포스파티딜콜린을 활성화시킨다.폐경 전 여성은 여성의 에스트로겐 분비가 높기 때문에 남성보다 콜린에 대한 식이 요건이 낮다.에스트로겐 요법이 없다면 폐경 후 여성의 콜린 요구량은 남성과 비슷하다.콜린과 엽산 대사에 영향을 미치는 일부 단일 뉴클레오티드 다형성(유전자적 인자)도 관련이 있다.어떤 내장 미생물들은 또한 다른 것들보다 더 효율적으로 콜린을 분해하기 때문에 그것들도 관련이 [27]있다.
결핍 시 간에서 포스파티딜콜린의 가용성은 감소하며 이는 VLDL 형성에 필요하다.따라서 간에서 VLDL 매개 지방산 수송이 감소하여 [6]간에 지방이 축적됩니다.관찰된 간 손상을 설명하는 다른 동시 발생 메커니즘도 제안되었다.예를 들어 콜린 인지질 또한 미토콘드리아 막에 필요하다.이들의 가용성은 미토콘드리아 막이 적절한 전기화학적 구배를 유지하지 못하게 하는데, 이는 무엇보다도 β-산화를 통해 지방산을 분해하는 데 필요하다.그러므로 간 속의 지방대사는 [27]감소한다.
과잉 섭취
과도한 콜린 복용은 부작용을 일으킬 수 있다.예를 들어, 매일 8-20g의 콜린을 복용하면 저혈압, 메스꺼움, 설사 및 생선 같은 체취를 유발하는 것으로 밝혀졌다.냄새는 흡수되지 않은 콜린에서 나온 내장 미생물에 의해 형성된 트리메틸아민(TMA)[6] 때문이다.
간은 TMA를 트리메틸아민 N-옥사이드(TMAO)로 산화시킨다.체내 TMA와 TMAO의 높은 수치는 아테롬성 동맥경화와 사망률의 위험 증가와 관련이 있다.따라서 과도한 콜린 섭취는 내장 박테리아에 의해 TMA와 TMAO로 형성되는 카르니틴과 더불어 이러한 위험을 증가시키기 위해 가정되었다.그러나 콜린 섭취가 심혈관 [28]질환으로 인한 사망 위험을 증가시키는 것으로 나타나지는 않았다.TMA와 TMAO의 수치가 상승하는 것은 단지 사망률을 증가시키는 다른 근본적인 질병이나 유전적 요인의 증상일 뿐이다.그러한 요인은 TMA 및 TMAO 수준 관련 사망률을 관찰하는 특정 연구에서 적절하게 설명되지 않았을 수 있다.인과관계는 역방향 또는 교란 요인이 될 수 있으며 콜린 섭취량이 많아도 사람의 사망률을 증가시키지 않을 수 있다.예를 들어 신장 기능 장애는 심혈관 질환에 걸리기 쉽지만 TMA와 TMAO 배설을 [29]줄일 수도 있다.
건강에 미치는 영향
신경 튜브 폐쇄
일부 인간 연구는 신생아에서 [4]신경관 결손(NTD)의 위험을 크게 증가시키기 위해 모성 콜린 섭취량이 낮다는 것을 보여주었다.엽산 결핍도 NTD를 일으킨다.비타민12 B와 상호작용하는 콜린과 엽산은 메티오닌을 형성하기 위해 호모시스테인에 대한 메틸 공여체로 작용하며, 메티오닌은 [4]SAM을 형성할 수 있습니다.SAM은 포유류의 거의 모든 메틸화 반응의 기질이다.SAM을 통한 교란된 메틸화가 엽산과 NTD [30]사이의 관계에 원인이 될 수 있다고 제안되었다.이것은 [citation needed]콜린에도 적용될 수 있다.콜린 대사를 방해하는 특정 돌연변이는 신생아에서 NTD의 유병률을 증가시키지만 2015년 현재 [update][4]식이요법 콜린 결핍의 역할은 불분명하다.
심혈관 질환 및 암
콜린 결핍은 지방간을 유발하여 암과 심혈관 질환의 위험을 증가시킨다.콜린 결핍은 또한 DNA 메틸화에 관여하는 SAM 생성을 감소시킨다 – 이러한 감소는 발암에 기여할 수도 있다.그래서 결핍과 그 질병과의 연관성이 [6]연구되었다.그러나 자유 인구에 대한 관찰 연구는 낮은 콜린 섭취와 심혈관 질환 또는 대부분의 [4][6]암 사이의 연관성을 설득력 있게 보여주지 못했다.전립선암에 대한 연구는 [31][32]모순되어 왔다.
인지
높은 콜린 섭취와 인지 사이의 효과를 관찰한 연구는 인간 성인을 대상으로 수행되었으며,[4][33] 상반된 결과를 낳았다.인간의 유아와 어린이에 대한 유사한 연구는 모순되고 [4]제한적이다.
신생아 주기의 발달
이 섹션은 확인을 위해 추가 인용문이 필요합니다.(2016년 12월 (이 및 ) |
임신과 수유 모두 콜린에 대한 수요를 극적으로 증가시킨다.이러한 수요는 더 많은 콜린 드 노보를 생산하기 위해 에스트로겐 수치를 증가시킴으로써 PEMT의 상향 조절에 의해 충족될 수 있지만, PEMT의 활동이 증가했음에도 불구하고, 콜린에 대한 수요는 여전히 너무 높아서 일반적으로 체내 저장소가 고갈된다.이는 Pemt -/- 마우스(기능성 PEMT가 결여된 쥐)가 보조 [34]콜린을 공급하지 않으면 9-10일에 중단된다는 관찰로 대표된다.
임신과 수유 중에 모체의 콜린 저장소가 고갈되는 동안, 태반은 조직에 농도 구배에 반하여 콜린을 펌핑함으로써 콜린을 축적하고, 그 후 아세틸콜린과 같은 다양한 형태로 저장된다.양수의 콜린 농도는 모체의 [34]혈액보다 10배 더 높을 수 있다.
태아의 기능
콜린(Coline)은 세포막을 만드는 기질(신속한 태아와 모조직의 팽창), 1탄소 부분(DNA와 다른 기능의 메틸화를 위한 기질), 태아 및 태반 조직에서의 콜린 저장고, 그리고 리포단백질(지질 함유 단백질)의 증산을 위한 기질로서 임신 중에 높은 수요가 있다.'지방' 부분).[35][36][37]특히 콜린 섭취가 뇌에 미치는 영향에 관심이 있다.이것은 세포막을 만드는 재료로 콜린(특히 포스파티딜콜린을 만드는 데)을 사용하는 것에서 비롯됩니다.인간의 뇌 성장은 임신 3개월 동안 가장 빠르며 약 [38]5세까지 계속 빨라진다.이 기간 동안, 스핑고미엘린은 신경 [39]섬유를 미엘(절연)하는 데 사용되기 때문에 포스파티딜콜린(따라서 콜린)으로 만들어지기 때문에 수요가 높습니다.콜린은 또한 뇌 영역의 구조와 조직, 신경 생성, 골수 형성, 시냅스 형성에 영향을 줄 수 있는 신경 전달 물질인 아세틸콜린의 생산에 대한 수요도 있다.아세틸콜린은 태반에도 존재하며 세포 증식과 분화(세포수의 증가와 전용 세포 기능으로의 변화)와 분만을 조절하는데 도움을 [40][41]줄 수 있다.
뇌로의 콜린 흡수는 혈액-뇌 [42]장벽에 위치한 저선호도 전달체에 의해 제어된다.콜린이 풍부한 음식을 섭취한 후 콜린 농도가 급상승할 때 발생할 수 있는 동맥 혈장 콜린 농도가 14μmol/l 이상으로 증가할 때 수송이 발생한다.반대로 뉴런은 고선호도 전달체와 저선호도 전달체 모두에 의해 콜린을 획득한다.콜린은 막결합 포스파티딜콜린으로 저장되며 나중에 아세틸콜린 신경전달물질 합성에 사용될 수 있다.아세틸콜린은 필요에 따라 형성되고 시냅스를 가로질러 이동하며 다음 뉴런에 신호를 전달합니다.그 후 아세틸콜린에스테라아제에 의해 분해되고 유리콜린은 다시 [43]고친화도 트랜스포터에 의해 뉴런으로 흡수된다.
사용하다
염화콜린과 역산콜린은 식이 보조 식품에 사용된다.비타르트산염은 [2]흡습성이 낮기 때문에 더 자주 사용된다.특정 콜린 소금은 닭고기, 칠면조, 그리고 다른 동물 사료를 보충하기 위해 사용된다.일부 소금은 공업용 화학물질로도 사용됩니다. 예를 들어 포토 레지스트 [1]제거를 위한 포토 리소그래피에서 사용됩니다.콜린 테오필린산염과 콜린 살리실산염은 메타콜린과 카르바콜과 [45]같은 구조적 유사체뿐만 아니라 [1][44]의약품으로 사용된다.C-콜린과 같은 방사성 라벨이 부착된 콜린은 의료 [46]영상촬영에 사용된다.상업적으로 사용되는 다른 소금으로는 구연산트리콜린과 [1]중탄산콜린이 있다.
길항제 및 억제제
수백 개의 콜린 길항제 및 효소 억제제가 연구 목적으로 개발되었습니다.아미노메틸프로판올은 연구 도구로 사용된 최초의 것 중 하나이다.그것은 콜린과 트리메틸글리신 합성을 억제한다.그것은 콜린 결핍을 유발하여 설치류에서 지방간을 발생시킬 수 있다.디에탄올아민은 또 다른 화합물이지만 환경오염물질이기도 하다.N-시클로헥실콜린은 주로 뇌에서 콜린 흡수를 억제한다.헤미콜리늄-3은 보다 일반적인 억제제이지만 콜린 키나아제 또한 적당히 억제한다.보다 특이적인 콜린인산화효소 억제제 또한 개발되었다.트리메틸글리신 합성 억제제도 존재한다.카르복시부틸호모시스테인은 특정 BHMT [2]억제제의 예이다.
치매의 콜린 작동 가설은 약용 아세틸콜린에스테라아제 억제제뿐만 아니라 다양한 아세틸콜린 억제제까지 이끌어냈다.이러한 억제 연구 화학물질의 예로는 아세틸콜린의 가짜 신경전달물질 유사체인 트리에틸콜린, 호모콜린 및 콜린의 다른 많은 N-에틸 유도체를 들 수 있다.콜린 아세틸전달효소 억제제 또한 [2]개발되었다.
역사
검출
1849년, 아돌프 스트레이커는 돼지 [47][48]담즙으로부터 콜린을 분리한 최초의 사람이었다.1852년, L. Babo와 M.Hirschbrunn은 흰 겨자씨에서 콜린을 추출하여 [48]sinkaline이라고 이름 붙였다.1862년, 스트레이커는 돼지와 소의 담즙에 대한 실험을 반복했고, 그리스어로 담즙, 담즙을 뜻하는 콜린이라는 이름을 따서 처음으로 콜린을 불렀고 화학식 CHNO로513 [49][15]식별했다.1850년, 테오도르 니콜라스 고블리는 카르프의 뇌와 알에서 그가 1874년 포스파티딜콜린의 [50][51]혼합물이라는 것을 보여주며, 그가 그리스어로 계란 노른자 레키토스를 따서 레시틴이라고 이름 붙인 물질을 추출했다.
1865년, 오스카 리브레이치는 동물의 [52][15]뇌에서 "뉴린"을 분리했다.아세틸콜린과 리브레이크의 뉴린의 구조식은 1867년 아돌프 폰 바이어에 의해 [53][48]해결되었다.그해 말 뉴린과 싱칼린은 스트레이커의 콜린과 같은 물질로 밝혀졌다.따라서,[54][55][48] Bayer는 콜린의 구조를 최초로 해결했다.현재 뉴린으로 알려진 화합물은 [15]콜린과 관련이 없다.
영양소로서의 발견
1930년대 초, 찰스 베스트와 동료들은 특별한 식단을 하는 쥐와 당뇨병 개들의 지방간이 레시틴을 [15]먹임으로써 예방될 수 있다고 지적했고, 1932년 레시틴의 콜린이 이러한 예방 [56]효과에 전적으로 책임이 있다는 것을 증명했다.1998년, 미국 국립 의학 아카데미는 인간의 [57]식단에서 콜린에 대한 그들의 첫 번째 권장 사항을 보고했다.
레퍼런스
- ^ a b c d e f g h i j Kirk RE, et al. (2000). Kirk-Othmer encyclopedia of chemical technology. Vol. 6 (4th ed.). John Wiley & Sons. pp. 100–102. ISBN 9780471484943.
- ^ a b c d e f g h i j k l m n Rucker RB, Zempleni J, Suttie JW, McCormick DB (2007). Handbook of vitamins (4th ed.). Taylor & Francis. pp. 459–477. ISBN 9780849340222.
- ^ "Choline". Lexico Dictionaries. Retrieved 9 November 2019.
- ^ a b c d e f g h i j k l "Choline". Micronutrient Information Center, Linus Pauling Institute, Oregon State University. February 2015. Retrieved 11 November 2019.
- ^ a b "Choline". Human Metabolome Database. The Metabolomics Innovation Centre, University of Alberta, Edmonton, Canada. 17 August 2016. Retrieved 13 September 2016.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad "Dietary reference values for choline". EFSA Journal. 14 (8). 2016. doi:10.2903/j.efsa.2016.4484.
- ^ "Office of Dietary Supplements - Choline".
- ^ 브리태니커, 백과사전 편집장"콜린"브리태니커 백과사전, 2013년 12월 11일, https://www.britannica.com/science/choline.2022년 2월 17일에 접속.
- ^ 국립생명공학정보센터(2022).CID 305, 콜린에 대한 PubChem 화합물 요약.2022년 2월 17일 https://pubchem.ncbi.nlm.nih.gov/compound/Choline에서 취득.
- ^ Rontein D, Nishida I, Tashiro G, Yoshioka K, Wu WI, Voelker DR, Basset G, Hanson AD (September 2001). "Plants synthesize ethanolamine by direct decarboxylation of serine using a pyridoxal phosphate enzyme". The Journal of Biological Chemistry. 276 (38): 35523–9. doi:10.1074/jbc.M106038200. PMID 11461929.
- ^ Prud'homme MP, Moore TS (November 1992). "Phosphatidylcholine synthesis in castor bean endosperm : free bases as intermediates". Plant Physiology. 100 (3): 1527–35. doi:10.1104/pp.100.3.1527. PMC 1075815. PMID 16653153.
- ^ Nuccio ML, Ziemak MJ, Henry SA, Weretilnyk EA, Hanson AD (May 2000). "cDNA cloning of phosphoethanolamine N-methyltransferase from spinach by complementation in Schizosaccharomyces pombe and characterization of the recombinant enzyme". The Journal of Biological Chemistry. 275 (19): 14095–101. doi:10.1074/jbc.275.19.14095. PMID 10799484.
- ^ McNeil SD, Nuccio ML, Ziemak MJ, Hanson AD (August 2001). "Enhanced synthesis of choline and glycine betaine in transgenic tobacco plants that overexpress phosphoethanolamine N-methyltransferase". Proceedings of the National Academy of Sciences of the United States of America. 98 (17): 10001–5. Bibcode:2001PNAS...9810001M. doi:10.1073/pnas.171228998. PMC 55567. PMID 11481443.
- ^ "Superpathway of choline biosynthesis". BioCyc Database Collection: MetaCyc. SRI International.
- ^ a b c d e Zeisel SH (2012). "A brief history of choline". Annals of Nutrition & Metabolism. 61 (3): 254–8. doi:10.1159/000343120. PMC 4422379. PMID 23183298.
- ^ a b c d Inazu M (September 2019). "Functional Expression of Choline Transporters in the Blood-Brain Barrier". Nutrients. 11 (10): 2265. doi:10.3390/nu11102265. PMC 6835570. PMID 31547050.
- ^ Barwick KE, Wright J, Al-Turki S, McEntagart MM, Nair A, Chioza B, et al. (December 2012). "Defective presynaptic choline transport underlies hereditary motor neuropathy". American Journal of Human Genetics. 91 (6): 1103–7. doi:10.1016/j.ajhg.2012.09.019. PMC 3516609. PMID 23141292.
- ^ Glier MB, Green TJ, Devlin AM (January 2014). "Methyl nutrients, DNA methylation, and cardiovascular disease". Molecular Nutrition & Food Research. 58 (1): 172–82. doi:10.1002/mnfr.201200636. PMID 23661599.
- ^ Barak AJ, Beckenhauer HC, Junnila M, Tuma DJ (June 1993). "Dietary betaine promotes generation of hepatic S-adenosylmethionine and protects the liver from ethanol-induced fatty infiltration". Alcoholism, Clinical and Experimental Research. 17 (3): 552–5. doi:10.1111/j.1530-0277.1993.tb00798.x. PMID 8333583.
- ^ Dushianthan A, Cusack R, Grocott MP, Postle AD (June 2018). "Abnormal liver phosphatidylcholine synthesis revealed in patients with acute respiratory distress syndrome". Journal of Lipid Research. 59 (6): 1034–1045. doi:10.1194/jlr.P085050. PMC 5983399. PMID 29716960.
- ^ a b c d e f g h i "Choline". Office of Dietary Supplements (ODS) at the National Institutes of Health. Retrieved 19 May 2020.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "21 CFR 107.100: Infant formula; Nutrient requirements; Nutrient specifications; Choline content". Code of Federal Regulations, Title 21; Food and Drug Administration. 1 April 2019. Retrieved 24 October 2019.
- ^ a b Zeisel SH, Mar MH, Howe JC, Holden JM (May 2003). "Concentrations of choline-containing compounds and betaine in common foods". The Journal of Nutrition. 133 (5): 1302–7. doi:10.1093/jn/133.5.1302. PMID 12730414.
- ^ Choline (17 March 2014). "Choline". www.nrv.gov.au. Retrieved 22 October 2019.
- ^ Wallace TC, Fulgoni VL (2016). "Assessment of Total Choline Intakes in the United States". Journal of the American College of Nutrition. 35 (2): 108–12. doi:10.1080/07315724.2015.1080127. PMID 26886842. S2CID 24063121.
- ^ "What We Eat in America, NHANES 2013-2014" (PDF). Retrieved 24 October 2019.
- ^ a b c Corbin KD, Zeisel SH (March 2012). "Choline metabolism provides novel insights into nonalcoholic fatty liver disease and its progression". Current Opinion in Gastroenterology. 28 (2): 159–65. doi:10.1097/MOG.0b013e32834e7b4b. PMC 3601486. PMID 22134222.
- ^ DiNicolantonio JJ, McCarty M, OKeefe J (2019). "Association of moderately elevated trimethylamine N-oxide with cardiovascular risk: is TMAO serving as a marker for hepatic insulin resistance". Open Heart. 6 (1): e000890. doi:10.1136/openhrt-2018-000890. PMC 6443140. PMID 30997120.
- ^ Jia J, Dou P, Gao M, Kong X, Li C, Liu Z, Huang T (September 2019). "Assessment of Causal Direction Between Gut Microbiota-Dependent Metabolites and Cardiometabolic Health: A Bidirectional Mendelian Randomization Analysis". Diabetes. 68 (9): 1747–1755. doi:10.2337/db19-0153. PMID 31167879.
- ^ Imbard A, et al. (2013). "Neural tube defects, folic acid and methylation". International Journal of Environmental Research and Public Health. 10 (9): 4352–4389. doi:10.3390/ijerph10094352. PMC 3799525. PMID 24048206.
- ^ Richman EL, Kenfield SA, Stampfer MJ, Giovannucci EL, Zeisel SH, Willett WC, Chan JM (October 2012). "Choline intake and risk of lethal prostate cancer: incidence and survival". The American Journal of Clinical Nutrition. 96 (4): 855–63. doi:10.3945/ajcn.112.039784. PMC 3441112. PMID 22952174.
- ^ Han P, Bidulescu A, Barber JR, Zeisel SH, Joshu CE, Prizment AE, et al. (April 2019). "Dietary choline and betaine intakes and risk of total and lethal prostate cancer in the Atherosclerosis Risk in Communities (ARIC) Study". Cancer Causes & Control. 30 (4): 343–354. doi:10.1007/s10552-019-01148-4. PMC 6553878. PMID 30825046.
- ^ Wiedeman AM, Barr SI, Green TJ, Xu Z, Innis SM, Kitts DD (October 2018). "Dietary Choline Intake: Current State of Knowledge Across the Life Cycle". Nutrients. 10 (10): 1513. doi:10.3390/nu10101513. PMC 6213596. PMID 30332744.
- ^ a b Zeisel SH (2006). "Choline: critical role during fetal development and dietary requirements in adults". Annual Review of Nutrition. 26: 229–50. doi:10.1146/annurev.nutr.26.061505.111156. PMC 2441939. PMID 16848706.
- ^ Institute of Medicine, Food and Nutrition Board. Dietary reference intakes for Thiamine, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin and Choline. Washington, DC: National Academies Press. 1998.
- ^ Allen LH (2006). "Pregnancy and lactation". In Bowman BA, Russle RM (eds.). Present Knowledge in Nutrition. Washington DC: ILSI Press. pp. 529–543.
- ^ King JC (May 2000). "Physiology of pregnancy and nutrient metabolism". The American Journal of Clinical Nutrition. 71 (5 Suppl): 1218S–25S. doi:10.1093/ajcn/71.5.1218s. PMID 10799394.
- ^ Morgane PJ, Mokler DJ, Galler JR (June 2002). "Effects of prenatal protein malnutrition on the hippocampal formation". Neuroscience and Biobehavioral Reviews. 26 (4): 471–83. doi:10.1016/s0149-7634(02)00012-x. PMID 12204193. S2CID 7051841.
- ^ Oshida K, Shimizu T, Takase M, Tamura Y, Shimizu T, Yamashiro Y (April 2003). "Effects of dietary sphingomyelin on central nervous system myelination in developing rats". Pediatric Research. 53 (4): 589–93. doi:10.1203/01.pdr.0000054654.73826.ac. PMID 12612207.
- ^ Sastry BV (June 1997). "Human placental cholinergic system". Biochemical Pharmacology. 53 (11): 1577–86. doi:10.1016/s0006-2952(97)00017-8. PMID 9264309.
- ^ Sastry BV, Sadavongvivad C (March 1978). "Cholinergic systems in non-nervous tissues". Pharmacological Reviews. 30 (1): 65–132. PMID 377313.
- ^ Lockman PR, Allen DD (August 2002). "The transport of choline". Drug Development and Industrial Pharmacy. 28 (7): 749–71. doi:10.1081/DDC-120005622. PMID 12236062. S2CID 34402785.
- ^ Caudill MA (August 2010). "Pre- and postnatal health: evidence of increased choline needs". Journal of the American Dietetic Association. 110 (8): 1198–206. doi:10.1016/j.jada.2010.05.009. PMID 20656095.
- ^ Rutter P (2017). Community pharmacy: symptoms, diagnosis, and treatment (4th ed.). Elsevier. p. 156. ISBN 9780702069970.
- ^ Howe-Grant M, Kirk RE, Othmer DF, eds. (2000). "C2-Chlorocarbons to Combustion Technology". Kirk-Othmer encyclopedia of chemical technology. Vol. 6 (4th ed.). John Wiley & Sons. pp. 100–102. ISBN 9780471484943.
- ^ Guo Y, Wang L, Hu J, Feng D, Xu L (2018). "Diagnostic performance of choline PET/CT for the detection of bone metastasis in prostate cancer: A systematic review and meta-analysis". PLOS ONE. 13 (9): e0203400. Bibcode:2018PLoSO..1303400G. doi:10.1371/journal.pone.0203400. PMC 6128558. PMID 30192819.
- ^ Strecker A (1849). "Beobachtungen über die galle verschiedener thiere". Justus Liebigs Ann Chem (in German). 70 (2): 149–197. doi:10.1002/jlac.18490700203.
- ^ a b c d Sebrell WH, Harris RS, Alam SQ (1971). The vitamins. Vol. 3 (2nd ed.). Academic Press. pp. 4, 12. doi:10.1016/B978-0-12-633763-1.50007-5. ISBN 9780126337631.
- ^ Strecker A (1862). "Üeber einige neue bestandtheile der schweinegalle". Justus Liebigs Ann Chem (in German). 123 (3): 353–360. doi:10.1002/jlac.18621230310.
- ^ Gobley T (1874). "Sur la lécithine et la cérébrine". J Pharm Chim (in French). 19 (4): 346–354.
- ^ Sourkes TL (2004). "The discovery of lecithin, the first phospholipid" (PDF). Bull Hist Chem. 29 (1): 9–15. Archived (PDF) from the original on 13 April 2019.
- ^ Liebreich O (1865). "Üeber die chemische beschaffenheit der gehirnsubstanz". Justus Liebigs Ann Chem (in German). 134 (1): 29–44. doi:10.1002/jlac.18651340107.
- ^ Baeyer A (1867). "I. Üeber das neurin". Justus Liebigs Ann Chem (in German). 142 (3): 322–326. doi:10.1002/jlac.18671420311.
- ^ Dybkowsky W (1867). "Üeber die identität des cholins und des neurins" [On the identity of choline & neurin]. J Prakt Chem (in German). 100 (1): 153–164. doi:10.1002/prac.18671000126.
- ^ Claus A, Keesé C (1867). "Üeber neurin und sinkalin". J Prakt Chem (in German). 102 (1): 24–27. doi:10.1002/prac.18671020104.
- ^ Best CH, Hershey JM, Huntsman ME (May 1932). "The effect of lecithine on fat deposition in the liver of the normal rat". The Journal of Physiology. 75 (1): 56–66. doi:10.1113/jphysiol.1932.sp002875. PMC 1394511. PMID 16994301.
- ^ Institute of Medicine (US) Standing Committee on the scientific evaluation of dietary reference intakes and its panel on folate, other B. vitamins, and choline. National Academies Press (US). 1998. pp. xi, 402–413. ISBN 9780309064118.




