세륨(IV) 산화물
Cerium(IV) oxide | |
 | |
| 이름들 | |
|---|---|
| IUPAC이름 세륨(IV) 산화물 | |
| 기타이름 산화세릭, 세리아, 이산화세륨 | |
| 식별자 | |
| |
3D 모델(JSMO) | |
| ChEBI | |
| 켐스파이더 | |
| ECHA 인포카드 | 100.013.774 |
펍켐 CID | |
| 유니아이 |
|
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| CeO2 | |
| 어금니 질량 | 172.115 g/mol |
| 외모 | 흰색 또는 옅은 노란색 고체, 흡습성이 있는 |
| 밀도 | 7.215g/cm3 |
| 융점 | 2,400°C (4,350°F, 2,670K) |
| 비등점 | 3,500°C (6,330°F, 3,770K) |
| 불용성의 | |
| +26.0−6·10cm3/mol | |
| 구조. | |
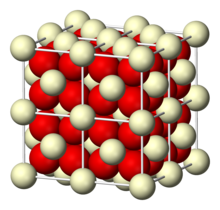
| 입방정계, cF12 (불소)[1] | |
| Fm3m, #225 | |
a = 5.41Å, b = 5.41Å, c = 5.41Å α = 90°,β = 90°,◦ = 90° | |
| Ce, 8, 큐빅 O, 4, 사면체 | |
| 유해성 | |
| NFPA 704 (파이어다이아몬드) | |
| 관련화합물 | |
관련화합물 | 세륨(III) 산화물 |
별도의 언급이 없는 경우를 제외하고, 표준 상태(25 °C [77 °F], 100 kPa에서)의 재료에 대한 데이터가 제공됩니다. | |
세륨(IV) 산화물은 희토류 금속 세륨의 산화물입니다.화학식 CeO의 옅은2 황백색 가루입니다.그것은 중요한 상업적 제품이며 광석으로부터 원소를 정제하는 중간체입니다.이 물질의 특징은 화학양론적이지 않은 산화물로 가역적으로 변환된다는 것입니다.
생산.
세륨은 산화물로 자연적으로 발생하며, 항상 다른 희토류 원소와 혼합되어 발생합니다.주요 광석과 모나자이트.수성 염기로 금속 이온을 추출한 후, Ce는 산화제를 첨가하고 pH를 조정함으로써 혼합물로부터 분리됩니다.이 단계는 CeO의2 낮은 용해도와 다른 희토류 원소가 [3]산화에 저항한다는 사실을 이용합니다.
산화세륨(IV)은 옥살산세륨 또는 수산화세륨의 하소에 의해 형성됩니다.
세륨은 또한 세륨(III) 산화물인 CeO를
2
3 형성하는데, CeO는 불안정하여 세륨()으로 산화됩니다.IV) [4]산화물
구조 및 결함 거동
산화세륨은 8좌표4+ Ce 및 4좌표2− O를 포함하는 공간군 Fm3m, #225인 플루오르사이트 구조를 채택합니다.고온에서는 산소를 방출하여 화학양론적이지 않은 음이온 결핍 형태를 제공하여 불소 [5]격자를 유지합니다.이 물질의 공식은(2−x) CeO이고 여기서 0 < x < 0.[6]28입니다.x의 값은 온도, 표면 종단, 산소 분압 모두에 따라 달라집니다.등식
광범위한 산소 분압(103–10−4 Pa)과 온도(1000–1900 °C)[7]에 걸쳐 평형 비화학양론 x를 예측하는 것으로 나타났습니다.
화학양론적이지 않은 형태는 파란색에서 검은색을 띠며 500°C [8]이상의 온도에서 이온 전도와 전자 전도를 모두 보여줍니다.
Ce3+
대 Ce의4+
비율을 비교하기 위해 X선 광전자 분광기를 사용하여 산소 공실의 수를 자주 측정합니다.
결함화학
세리아의 가장 안정적인 불소상에서는 산소의 분압이나 [9][10][11][12]물질의 응력 상태에 따라 여러 가지 결함을 보입니다.
우려되는 주요 결함은 산소 부족과 작은 폴라론(세륨 양이온 위에 국소화된 전자)입니다.산소결함의 농도가 증가하면 이온전도도가 증가하여 격자 내 산화물 음이온의 확산속도가 증가합니다.이러한 요소는 고체 산화물 연료 전지에서 고체 전해질로서의 응용에 유리한 성능을 제공합니다.도핑되지 않은 세륨과 도핑되지 않은 세륨은 또한 작은 폴라론을 형성하는 세륨 이온의 감소로 인해 낮은 산소 부분 압력에서 높은 전자 전도도를 나타냅니다.세리아 결정의 산소 원자는 평면에서 발생하기 때문에 이러한 음이온의 확산은 용이합니다.결함 농도가 증가함에 따라 확산 속도가 증가합니다.
말단 세리아 평면에 산소 빈자리가 있는 것은 흡착질 분자와의 세리아 상호작용의 에너지와 습윤성을 지배합니다.이러한 표면 상호작용을 제어하는 것은 촉매 [13]응용 분야에서 세리아를 활용하는 데 핵심적입니다.
자연발생
세륨(IV) 산화물은 광물 세리아나이트-([14][15]Ce)로 자연적으로 생성됩니다.그것은 4가 세륨 광물의 드문 예이며, 다른 예로는 스테틴다이트-(Ce)와 디르나사이트-(La)가 있습니다."-(Ce)" 접미사는 레빈슨 수식어로 알려져 있으며 [16]구조물의 특정 부위에서 어떤 요소가 지배적인지 보여주는 데 사용됩니다.희토류 원소(REE)를 함유하고 있는 광물의 이름에서 종종 발견됩니다.세리아나이트-(Ce)의 발생은 세리아나이트-(Ce)가 아닌 다른 광물의 구조에 적합한 세리아나이트-([17][14][15]Ce)와 쉽게 산화되는 세리아나이트-(Ce)가 3가를 유지하는 다른 RE로부터 분리되는 세륨 이상의 일부 예와 관련이 있습니다.
적용들
세륨은 크게 두 가지 용도를 가지고 있으며, 아래에 나열되어 있습니다.
세리아의 주된 산업적 응용은 연마, 특히 화학적-기계적 평탄화(CMP)[3]를 위한 것입니다.이러한 목적으로, 산화철과 지르코니아와 같은 이전에 사용되었던 많은 다른 산화물들을 대체했습니다.취미생활을 하는 사람들에게는 "옵티션스 루즈"[18][19] 라고도 합니다.
CeO는2 유리를 탈색하는 데 사용됩니다.녹색을 띤 철 불순물을 무색에 가까운 [3]산화철로 변환시켜 기능합니다.
기타 틈새 시장 및 신흥 애플리케이션
촉매작용
CeO는2 이종 촉매 분야에서 많은 관심을 끌었습니다.물과 가스의 이동 반응을 촉진합니다.일산화탄소를 산화시킵니다.환원된 유도체 Ce2O3는 [20][21][22][23]수소 방출과 함께 물을 감소시킵니다.
CeOx 물질의 상호가환성은 산화 촉매를 위한 세리아의 사용의 기본입니다.작지만 예시적인 한 가지 용도는 고온 세척 과정 중에 탄화수소 산화 촉매로서 자가 세척 오븐의 벽에 사용되는 것입니다.또 다른 소규모이지만 유명한 예는 가스 [24]맨틀에서 천연가스의 산화에 대한 그것의 역할입니다.

Ceria는 뚜렷한 표면 상호작용을 바탕으로 자동차 분야에서 촉매변환기의 센서로 더욱 활용되어 공기-배기 비율을 조절하여 NO 및 일산화탄소 [25]배출을 줄입니다x.
에너지 및 연료
세륨옥사이드의 이온 전도 및 전자 전도가 매우 크기 때문에 혼합 [26]전도체로 사용하기에 적합합니다.이와 같이, 산화 세륨은 산화 [27]지르코늄과 비교하여 고체 산화물 연료 전지(SOFC)의 관심 대상 물질입니다.
열화학적으로, 세륨(IV) 산화물-세륨(III) 산화물 사이클 또는 CeO2/CeO23 사이클은 수소 [28]제조를 위해 사용되어 온 2단계 물 분할 프로세스입니다.시스템 사이의 산소 부족을 활용하기 때문에 물 속의 세리아가 하이드록실([29]OH) 그룹을 형성할 수 있습니다.하이드록실 그룹은 산소가 산화됨에 따라 방출되어 청정 에너지의 원천이 될 수 있습니다.
광학
세륨 산화물은 적외선 필터, 촉매변환기의 산화종 및 백열 맨틀의[30] 이산화토륨 대체품으로 사용되었습니다.
용접
산화세륨은 가스 텅스텐 아크 용접을 위한 텅스텐 전극에 추가로 사용됩니다.순수 텅스텐 전극에 비해 전극 소모율을 줄이고 아크 시동 및 안정성을 용이하게 하는 장점이 있습니다.세리아 전극은 1987년 미국 시장에 처음 소개되었으며, AC, DC 전극 포지티브 및 DC 전극 네거티브에 유용합니다.
안전측면
세륨옥사이드 나노입자(nanoceria)는 항균 및 항산화 [31][32][33][34]활성이 조사되었습니다.
나노세리아는 더 낮은 광촉매 [35]활성을 갖기 때문에 자외선 차단제에서 산화아연과 이산화티타늄의 잠재적인 대체물입니다.
참고 항목
참고문헌
- ^ 프레이도트 파트나익.무기 화학물질 안내서.맥그로힐, 2002년 ISBN0-07-049439-8
- ^ E. A. 쿰머레와 G.Heger, "C-Ce2O3+γ, Ce7O12, 및 Ce11O20의 구조", Journal of Solid State Chemistry, vol. 147, no. 2, pp. 485–500, 1999
- ^ a b c Reinhardt, Klaus; Winkler, Herwig (2000). "Cerium Mischmetal, Cerium Alloys, and Cerium Compounds". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a06_139..
- ^ "Standard Thermodynamic Properties of Chemical Substances" (PDF). Archived from the original (PDF) on October 29, 2013.
- ^ 세륨옥사이드 표면의 DFT 연구 적용 표면 과학 2019 vol 478
- ^ 윌리엄 헤이스, A. M. 스톤햄 택배 도버 출판사, 2004.
- ^ Bulfin, B.; Lowe, A. J.; Keogh, K. A.; Murphy, B. E.; Lübben, O.; Krasnikov, S. A.; Shvets, I. V. (2013). "Analytical Model of CeO2 Oxidation and Reduction". The Journal of Physical Chemistry C. 117 (46): 24129–24137. doi:10.1021/jp406578z. hdl:2262/76279.
- ^ Ghillanyova, K.; Galusek, D. (2011). "Chapter 1: Ceramic oxides". In Riedel, Ralf; Chen, I-Wie (eds.). Ceramics Science and Technology, Materials and Properties, vol 2. John Wiley & Sons. ISBN 978-3-527-31156-9.
- ^ Munnings, C.; Badwal, S.P.S.; Fini, D. (2014). "Spontaneous stress-induced oxidation of Ce ions in Gd-doped ceria at room temperature". Ionics. 20 (8): 1117–1126. doi:10.1007/s11581-014-1079-2. S2CID 95469920.
- ^ Badwal, S.P.S.; Daniel Fini; Fabio Ciacchi; Christopher Munnings; Justin Kimpton; John Drennan (2013). "Structural and microstructural stability of ceria – gadolinia electrolyte exposed to reducing environments of high temperature fuel cells". J. Mater. Chem. A. 1 (36): 10768–10782. doi:10.1039/C3TA11752A.
- ^ Anandkumar, Mariappan; Bhattacharya, Saswata; Deshpande, Atul Suresh (2019-08-23). "Low temperature synthesis and characterization of single phase multi-component fluorite oxide nanoparticle sols". RSC Advances. 9 (46): 26825–26830. Bibcode:2019RSCAd...926825A. doi:10.1039/C9RA04636D. ISSN 2046-2069. PMC 9070433. PMID 35528557.
- ^ Pinto, Felipe M (2019). "Oxygen Defects and Surface Chemistry of Reducible Oxides". Frontiers in Materials. 6: 260. Bibcode:2019FrMat...6..260P. doi:10.3389/fmats.2019.00260. S2CID 204754299.
- ^ Fronzi, Marco; Assadi, M. Hussein N.; Hanaor, Dorian A.H. (2019). "Theoretical insights into the hydrophobicity of low index CeO2 surfaces" (PDF). Applied Surface Science. 478: 68–74. arXiv:1902.02662. Bibcode:2019ApSS..478...68F. doi:10.1016/j.apsusc.2019.01.208. S2CID 118895100.
- ^ a b "Cerianite-(Ce)". www.mindat.org. Retrieved 2020-11-12.
- ^ a b "List of Minerals". www.ima-mineralogy.org. 2011-03-21. Retrieved 2020-11-12.
- ^ Burke, Ernst (2008). "The use of suffixes in mineral names" (PDF). Elements. 4 (2): 96.
- ^ Pan, Yuanming; Stauffer, Mel R. (2000). "Cerium anomaly and Th/U fractionation in the 1.85 Ga Flin Flon Paleosol: Clues from REE- and U-rich accessory minerals and implications for paleoatmospheric reconstruction". American Mineralogist. 85 (7): 898–911. Bibcode:2000AmMin..85..898P. doi:10.2138/am-2000-0703. S2CID 41920305.
- ^ "Properties of Common Abrasives (Boston Museum of Fine Arts)" (PDF).
- ^ "Ceric oxide - CAMEO". cameo.mfa.org.
- ^ Ruosi Peng; et a. (2018). "Size effect of Pt nanoparticles on the catalytic oxidation of toluene over Pt/CeO2 catalysts". Applied Catalysis B: Environmental. 220.
- ^ Montini, Tiziano; Melchionna, Michele; Monai, Matteo; Fornasiero, Paolo (2016). "Fundamentals and Catalytic Applications of CeO2-Based Materials". Chemical Reviews. 116 (10): 5987–6041. doi:10.1021/acs.chemrev.5b00603. hdl:11368/2890051. PMID 27120134.
- ^ Paier, Joachim; Penschke, Christopher; Sauer, Joachim (2013). "Oxygen Defects and Surface Chemistry of Ceria: Quantum Chemical Studies Compared to Experiment". Chemical Reviews. 113 (6): 3949–3985. doi:10.1021/cr3004949. PMID 23651311.
- ^ Gorte, Raymond J. (2010). "Ceria in catalysis: From automotive applications to the water-gas shift reaction". AIChE Journal: NA. doi:10.1002/aic.12234.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Twigg, Martyn V. (2011). "Catalytic control of emissions from cars". Catalysis Today. 163: 33–41. doi:10.1016/j.cattod.2010.12.044.
- ^ "Mixed conductors". Max Planck institute for solid state research. Retrieved 16 September 2016.
- ^ Arachi, Y. (June 1999). "Electrical conductivity of the ZrO2–Ln2O3 (Ln=lanthanides) system". Solid State Ionics. 121 (1–4): 133–139. doi:10.1016/S0167-2738(98)00540-2.
- ^ "Hydrogen production from solar thermochemical water splitting cycles". SolarPACES. Archived from the original on August 30, 2009.
- ^ "New discoveries made on the role of Cerium Oxide in Hydrogen production". Ceric. 2018-07-01. Retrieved 2022-09-22.
- ^ "Cerium dioxide". DaNa. Archived from the original on 2013-03-02.
- ^ Rajeshkumar, S.; Naik, Poonam (2018). "Synthesis and biomedical applications of Cerium oxide nanoparticles – A Review". Biotechnology Reports. 17: 1–5. doi:10.1016/j.btre.2017.11.008. ISSN 2215-017X. PMC 5723353. PMID 29234605.
- ^ Karakoti, A. S.; Monteiro-Riviere, N. A.; Aggarwal, R.; Davis, J. P.; Narayan, R. J.; Self, W. T.; McGinnis, J.; Seal, S. (2008). "Nanoceria as antioxidant: synthesis and biomedical applications". JOM. 60 (3): 33–37. Bibcode:2008JOM....60c..33K. doi:10.1007/s11837-008-0029-8. PMC 2898180. PMID 20617106.
- ^ Rajeshkumar, S.; Naik, Poonam (2017-11-29). "Synthesis and biomedical applications of Cerium oxide nanoparticles – A Review". Biotechnology Reports. 17: 1–5. doi:10.1016/j.btre.2017.11.008. ISSN 2215-017X. PMC 5723353. PMID 29234605.
- ^ Hussain S, Al-Nsour F, Rice AB, Marshburn J, Yingling B, Ji Z, Zink JI, Walker NJ, Garantziotis S (2012). "Cerium dioxide nanoparticles induce apoptosis and autophagy in human peripheral blood monocytes". ACS Nano. 6 (7): 5820–9. doi:10.1021/nn302235u. PMC 4582414. PMID 22717232.
- ^ Zholobak, N.M.; Ivanov, V.K.; Shcherbakov, A.B.; Shaporev, A.S.; Polezhaeva, O.S.; Baranchikov, A.Ye.; Spivak, N.Ya.; Tretyakov, Yu.D. (2011). "UV-shielding property, photocatalytic activity and photocytotoxicity of ceria colloid solutions". Journal of Photochemistry and Photobiology B: Biology. 102 (1): 32–38. doi:10.1016/j.jphotobiol.2010.09.002. PMID 20926307.




