이산화 니오비움
Niobium dioxide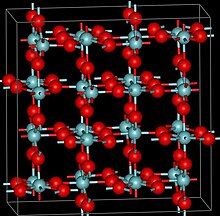 | |
| 이름 | |
|---|---|
| IUPAC 이름 니오비움(niobium)IV) 산화물, 이산화 니오비움 | |
| 기타 이름 니오비움(niobium)IV) 산화물, 이산화콜륨 | |
| 식별자 | |
3D 모델(JSmol) | |
| ECHA InfoCard | 100.031.632 |
| EC 번호 |
|
펍켐 CID | |
CompTox 대시보드 (EPA) | |
| 특성. | |
| NBO2 | |
| 어금질량 | 124.91 g/190 |
| 외관 | 푸르스름한 검은 고체 |
| 녹는점 | 1,915°C(3,479°F, 2,188K)[1] |
| 구조 | |
| 4각형, tI96 | |
| I41/a, 제88호 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
이산화 니오비움은 NbO라는2 공식을 가진 화학 화합물이다. NbO-NbO의1.942.09 구성범위를 가진 블루스-블랙 비스토리히메트릭 고체다.[1] 800–1350 °C에서 H로2 NbO를25 감소시킴으로써 준비할 수 있다.[1] 대안적인 방법은 1100 °C에서 Nb 분말을 사용한 NbO의25 반응이다.[2]
특성.
NbO의2 상온 형태는 Nb-Nb 거리가 짧은 4각형의 루틸레 같은 구조를 가지고 있어 Nb-Nb 본딩을 나타낸다.[3] 고온 형태도 짧은 Nb-Nb 거리를 가진 루타일 같은 구조를 가지고 있다.[4] 두 개의 고압 단계가 보고되었는데 하나는 루틸레와 같은 구조로, 하나는 Nb-Nb 거리가 짧고, 다른 하나는 배들리이트 관련 구조로 더 높은 압력을 가지고 있다.[5]
NbO는2 물에 용해되지 않으며 이산화탄소를 이산화탄소로, 아황산가스를 황으로 줄이는 강력한 환원제다.[1] 니오비움 금속의 생산을 위한 산업 공정에서 NbO는2 NbO의25 수소 저감에 의해 중간으로 생산된다.[6] NbO는2 이후 마그네슘 증기와 반응하여 니오비움 금속을 생산한다.[7]
참조
- ^ a b c d C. K. 굽타, A. K. 수리, S 굽타, K 굽타(1994), 니오비움의 추출물 금속, CRC 프레스, ISBN0-8493-6071-4
- ^ Pradyot Patnaik(2002) McGraw-Hill Professional ISBN 0-07-049439-8
- ^ 웰스 A.F. (1984) 구조 무기 화학 제5판 옥스퍼드 과학 간행물 ISBN 0-19-855370-6
- ^ Bolzan, A; Fong, Celesta; Kennedy, Brendan J.; Howard, Christopher J. (1994). "A Powder Neutron Diffraction Study of Semiconducting and Metallic Niobium Dioxide". Journal of Solid State Chemistry. 113 (1): 9–14. Bibcode:1994JSSCh.113....9B. doi:10.1006/jssc.1994.1334.
- ^ Haines, J.; Léger, J. M.; Pereira, A. S. (1999). "High-pressure structural phase transitions in semiconducting niobium dioxide". Physical Review B. 59 (21): 13650. Bibcode:1999PhRvB..5913650H. doi:10.1103/PhysRevB.59.13650. hdl:10183/198788.
- ^ 특허 EP1524252, 아산화 니오비움을 기반으로 한 시너티드 본체, 슈니터 C, Wötting G
- ^ 기체마그네슘, 미국 특허 6171363(2001), 셰히터 L.N., 트립 T.B., 라니 L.L. (H. C. 스타크, Inc.)에 의한 산화물 감소를 통한 탄탈룸/니오비움 금속가루 생산방법