메탄
Methane
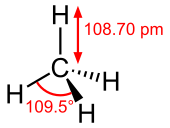 | |||
| | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 메탄[1] | |||
| 시스템 IUPAC 이름 카르반(권장하지[1] 않음) | |||
기타 이름
| |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 3 DMet | |||
| 1718732 | |||
| 체비 | |||
| 첸블 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.000.739 | ||
| EC 번호 |
| ||
| 59 | |||
| 케그 | |||
| 메쉬 | 메탄 | ||
PubChem CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 1971 | ||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| CH4 | |||
| 몰 질량 | 16.043 g/120−1 | ||
| 외모 | 무색 가스 | ||
| 냄새 | 무취 | ||
| 밀도 | |||
| 녹는점 | -182.456°C(-296.421°F, 90.694K)[3] | ||
| 비등점 | -161.5°C(-258.7°F, 111.6K)[3] | ||
| 임계점(T, P) | 190.56 K(-82.59 °C, -116.66 °F), 4.5992 메가파스칼(45.391 atm) | ||
| 22.7mg·L−1[4] | |||
| 용해도 | 에탄올, 디에틸에테르, 벤젠, 톨루엔, 메탄올, 아세톤에 용해되며 물에 불용성 | ||
| 로그 P | 1.09 | ||
헨리의 법칙 상수(kH) | 14 nmol·Pa−1·kg−1 | ||
| 복합 에시드 | 메타늄 | ||
| 복합 기지 | 메틸 음이온 | ||
자화율(δ) | - 17.4×10cm−63/수직−1[5] | ||
| 구조. | |||
| Td. | |||
| 사면체 | |||
| 0 D | |||
| 열화학[6] | |||
열용량 (C) | 35.7 J·(K·mol)−1 | ||
표준 어금니 엔트로피 (S | 186.3 J·(K·mol)−1 | ||
표준 엔탈피/ 형성 (δHf⦵298) | - 74.6 kJ/mol−1 | ||
깁스 자유 에너지 ( (Gf)) | - 50.5kJ/mol−1 | ||
표준 엔탈피/ 연소 (δHc⦵298) | -891 kJ/mol−1 | ||
| 위험[7] 요소 | |||
| GHS 라벨링: | |||
 | |||
| 위험. | |||
| H220 | |||
| P210 | |||
| NFPA 704(파이어 다이아몬드) | |||
| 플래시 포인트 | -188 °C (-306.4 °F, 85.1 K) | ||
| 537°C(999°F, 810K) | |||
| 폭발 한계 | 4.4–17% | ||
| 관련 화합물 | |||
관련 알칸 | |||
| 보충 데이터 페이지 | |||
| 메탄(데이터 페이지) | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
메탄(US: /mmθenn/MEH-thayn, 영국: /mimiːenn/ME-thayn)은 화학식이4 CH(1개의 탄소 원자가 4개의 수소 원자에 결합)인 화합물이다.14족 수소화물, 가장 단순한 알칸이며 천연가스의 주성분입니다.지구상에 메탄이 상대적으로 풍부하기 때문에 경제적으로 매력적인 연료이지만, 정상적인 온도와 압력 조건에서의 가스 상태 때문에 포획하고 저장하는 것은 기술적인 문제를 일으킨다.
자연적으로 발생하는 메탄은 지하와 해저 모두에서 발견되며 지질학적, 생물학적 과정에 의해 형성된다.가장 큰 메탄 저장고는 메탄 포접물의 형태로 해저에 있다.메탄이 표면과 대기에 도달하면, 그것은 대기 [9]메탄으로 알려져 있다.지구의 대기 중 메탄 농도는 1750년 이후 약 150% 증가했으며, 이는 수명이 길고 전 세계적으로 혼합된 모든 온실 [10]가스에서 발생하는 총 복사력의 20%를 차지한다.그것은 또한 화성을 포함한 다른 행성에서도 발견되었는데, 이것은 우주 생물학 연구에 [11]영향을 미친다.
특성 및 본딩
메탄은 4개의 동등한 C-H 결합을 가진 사면체 분자이다.그것의 전자 구조는 C와 H의 원자가 오비탈의 중첩으로 인한 4개의 결합 분자 오비탈에 의해 설명된다.가장 낮은 에너지 MO는 탄소의 2s 오비탈과 4개의 수소 원자의 1s 오비탈의 동상 조합이 겹친 결과이다.이 에너지 수준 위에는 탄소의 2p 궤도와 수소의 1s 궤도의 다양한 선형 조합이 겹치는 3중 축퇴된 MO 세트가 있다.결과적으로 발생하는 "3중 1중" 결합 방식은 광전자 스펙트럼 분석 측정과 일치한다.
메탄은 무취 가스이며 [12]무색인 것으로 보인다.특히 오버톤 대역으로 인해 스펙트럼의 빨간색 끝에서 가시광을 흡수하지만, 광로가 매우 긴 경우에만 효과가 나타난다.이것은 빛이 메탄을 포함한 대기를 통과하고 다시 [13]산란되기 때문에 천왕성과 해왕성이 파란색 또는 청록색을 띠게 하는 것입니다.
가정에서 천연가스의 친숙한 냄새는 안전 대책으로 보통 tert-butylthiol을 함유하는 혼합물을 첨가함으로써 달성된다.메탄은 [3]1기압에서 -161.5°C의 비등점을 가진다.기체로서는 표준 압력에서 공기 중 농도 범위(5.4~17%)에 걸쳐 인화성이 있습니다.
고체 메탄은 몇 가지 변형으로 존재한다.현재 [14]9개가 알려져 있다.메탄을 정상 압력으로 냉각시키면 메탄 I이 형성된다.이 물질은 입방정계(우주군 Fm3m)에서 결정화된다.수소 원자의 위치는 메탄 I에서 고정되지 않습니다. 즉, 메탄 분자가 자유롭게 회전할 수 있습니다.그러므로, 그것은 플라스틱 [15]결정이다.
화학 반응
메탄의 주요 화학반응은 연소, 증기로의 개질, 할로겐화이다.일반적으로 메탄 반응은 통제하기 어렵다.
선택적 산화
메탄에서 메탄올로의 부분 산화는 더 편리한 액체 연료로, 산소의 공급이 부족하더라도 반응이 일반적으로 이산화탄소와 물로 진행되기 때문에 어렵다.메탄 모노옥시게나아제 효소는 메탄으로부터 메탄올을 생성하지만 산업 규모의 [16]반응에는 사용할 수 없다.일부 균질 촉매 시스템과 이종 시스템이 개발되었지만 모두 상당한 단점이 있습니다.일반적으로 과산화로부터 보호되는 제품을 생성함으로써 작동합니다.예를 들어 Catalysta 시스템, 구리 제올라이트 및 알파 산소 활성 [17]부위를 안정화시키는 철 제올라이트가 있습니다.
한 그룹의 박테리아는 산소가 없을 때 산화제로 아질산염과 메탄 산화를 촉매하여 소위 [18]메탄 혐기성 산화를 일으킨다.
산염기 반응
다른 탄화수소와 마찬가지로 메탄은 극도로 약한 산이다.DMSO에서의 pK는a [19]56으로 추정됩니다.이것은 용액에서 탈양성자가 될 수 없지만, 복합 염기는 메틸리튬과 같은 형태로 알려져 있다.
메탄에서 파생된 다양한 양의 이온이 관찰되었으며, 대부분 저압 가스 혼합물에서 불안정한 종으로 나타났다.여기에는 메테늄 또는 메틸 양이온+
3 CH, 메탄 양이온+
4 CH 및 메탄늄 또는 양성자화된 메탄+
5 CH가 포함됩니다.이들 중 일부는 우주에서 발견되었다.메타늄은 또한 초산을 가진 메탄으로부터 희석된 용액으로 생산될 수 있다.CH나3+
7 CH와 같이2+
6 전하가 높은 양이온은 이론적으로 연구되어 [20]안정성이 있는 것으로 추측되고 있습니다.
C-H 결합의 강도에도 불구하고 메탄(및 기타 낮은 번호의 알칸)[21]에서 C-H 결합 활성화를 촉진하는 촉매에 대한 관심이 높다.
연소
메탄의 연소열은 55.5 MJ/[22]kg이다.메탄 연소는 다음과 같이 요약되는 다단계 반응이다.
피터스의 4단계 화학은 메탄 연소를 설명하는 체계적으로 감소된 4단계 화학이다.
메탄기 반응
적절한 조건 하에서 메탄은 할로겐 라디칼과 다음과 같이 반응합니다.
- X• + CH4 → HX + CH3•
- CH3• + X2 → CHX3 + X•
여기서 X는 할로겐이다: 불소(F), 염소(Cl), 브롬(Br) 또는 요오드(I).이 과정을 위한 이 메커니즘은 유리 래디칼 할로겐화라고 불립니다.이는 UV광 또는 다른 래디칼 이니시에이터(과산화물 등)가 할로겐 원자를 생성할 때 시작됩니다.할로겐 원자가 메탄 분자로부터 수소 원자를 추출해 할로겐화 수소 분자와 메틸 라디칼(CH•)을3 형성하는 2단계 연쇄 반응이 뒤따른다.메틸라디칼은 할로겐 분자와 반응하여 할로겐 분자를 형성하고,[23] 새로운 할로겐 원자를 부산물로 사용합니다.할로겐화 생성물에서도 비슷한 반응이 일어나 반응 조건과 할로겐 대 메탄 비율에 따라 수소 원자가 디할로메탄, 트리할로메탄, 궁극적으로는 테트라할로메탄 구조로 할로겐 원자에 의해 추가로 치환될 수 있다.
사용하다
메탄은 산업 화학 과정에 사용되며 냉장 액체(액화 천연 가스, LNG)로 운반될 수 있습니다.냉기체 밀도가 높아져 냉장 액체 용기의 누출이 처음에는 공기보다 더 무거운 반면, 주변 온도에서 가스는 공기보다 가볍습니다.가스 파이프라인은 많은 양의 천연가스를 분배하는데, 그 중 메탄이 주요 성분이다.
연료
메탄은 오븐, 가정, 온수기, 가마, 자동차,[24][25] 터빈 등의 연료로 사용된다.활성탄은 메탄을 저장하는 데 사용된다.정제된 액체 메탄은 BE-4 및 랩터 [27]엔진과 같이 액체 산소와 결합될 때 로켓 [26]연료로 사용됩니다.
천연가스의 주요 성분인 메탄은 가스터빈이나 증기발생기에서 연료로 연소시켜 발전하는 데 중요하다.다른 탄화수소 연료에 비해 메탄은 방출되는 열 단위당 이산화탄소를 적게 배출한다.약 891kJ/mol에서 메탄의 연소열은 다른 탄화수소보다 낮지만 분자량에 대한 연소열(891kJ/mol, 이 중 12.0g/mol은 탄소)의 비율을 보면 메탄은 가장 단순한 탄화수소인 557kJ보다 더 많은 열을 생성한다는 것을 알 수 있다.많은 도시에서 메탄은 가정 난방과 요리를 위해 가정으로 보내진다.이러한 맥락에서 그것은 보통 천연 가스라고 알려져 있는데, 이것은 입방 미터 당 39 메가 줄 또는 표준 입방 피트 당 1,000 BTU의 에너지 함유량을 가진 것으로 간주됩니다.액화천연가스(LNG)는 주로 메탄(CH4)을 액체 형태로 변환하여 저장 또는 운반이 용이합니다.
액체 로켓 연료로서 메탄은 작은 배기가스 분자를 생산하는 등유보다 유리하다.이렇게 하면 로켓 모터의 내부 부품에 그을음이 덜 쌓여서 부스터 재사용의 어려움을 줄일 수 있습니다.배기 가스의 낮은 분자량은 또한 추진에 사용할 수 있는 운동 에너지 형태의 열에너지의 비율을 증가시켜 로켓의 특정 임펄스를 증가시킵니다.액체 메탄은 또한 액체 산소(54–90 K)와 거의 양립할 수 있는 온도 범위(91–112 K)를 가지고 있다.
화학 원료
메탄가스가 대부분인 천연가스는 산업 규모로 수소가스를 생산하는데 사용된다.증기 메탄 개질(SMR) 또는 간단히 증기 개질이라고 알려진 증기 메탄 개질(SMR)은 상업용 벌크 수소 가스를 생산하는 표준 산업 방법입니다.전 세계에서 연간 5000만톤 이상(2013년)이 생산되고 있으며,[28] 주로 천연가스의 SMR에서 생산되고 있다.이 수소의 대부분은 석유 정제, 화학 물질 생산 및 식품 가공에 사용됩니다.매우 많은 양의 수소가 암모니아 산업 합성에 사용된다.
고온(700–1100°C)에서 금속 기반 촉매(니켈)가 있는 경우 증기는 메탄과 반응하여 "물 가스" 또는 "싱가스"로 알려진 CO와2 H의 혼합물을 생성합니다.
이 반응은 강한 흡열성(consumesconsumes性, δHr = 206 kJ/mol)이다.추가적인 수소는 물 가스 이동 반응을 통해 CO와 물의 반응에 의해 얻어진다.
- CO + HO2 co2 CO + H2
이 반응은 약한 발열성(발열, δHr = -41 kJ/mol)이다.
메탄올이 보다 전형적인 [29]전구체이긴 하지만 메탄올은 클로로메탄 생성 과정에서 자유방사성 염소화 처리되기도 한다.
수소는 메탄 열분해라고도 알려진 메탄의 직접 분해를 통해서도 생산될 수 있다.메탄 분해는 증기 메탄 개질과는 달리 직접적인 탄소 배출이 없기 때문에 저배출 수소 생산에 유망한 경로이다.수소 가스와 고체 탄소를 생성하기 위해 메탄의 결합을 끊으려면 1200°C 이상의 온도가 필요합니다.그러나 적절한 촉매를 사용하면 선택한 [30]촉매에 따라 반응 온도를 600°C~1000°C로 낮출 수 있습니다.반응식은 [31]아래 반응식과 같이 적당히 흡열된다.
시대
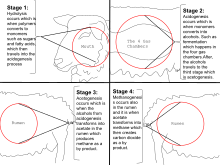
지질 경로
지질 메탄 생성의 두 가지 주요 경로는 (i)유기(열발생 또는 열발생)와 (ii)무기(비생물)[11]이다.열원성 메탄은 높은 온도와 깊은 퇴적층에서 유기물이 분해되면서 발생한다.퇴적 분지에 있는 대부분의 메탄은 열을 발생시킨다. 따라서, 열 발생 메탄은 천연 가스의 가장 중요한 원천이다.열 유발 메탄 성분은 일반적으로 (이전부터) 잔재로 간주됩니다.일반적으로 열원성 메탄(깊이)의 형성은 유기물 분해 또는 유기합성을 통해 발생할 수 있다.두 방법 모두 미생물(방법형성)을 포함할 수 있지만, 유기적으로도 발생할 수 있습니다.관련된 과정들은 또한 미생물이 있든 없든 메탄을 소비할 수 있다.
깊이에서 메탄의 더 중요한 원천은 비생물적이다.비생물학이란 메탄은 생물활동이 없는 무기화합물로부터 생성된다는 것을 의미합니다.매그마틱 과정이나 낮은 온도와 압력에서 발생하는 물-바위 반응을 통해, 예를 들어 독사화와 [32][33]같은.
생물 경로
지구의 메탄은 대부분 생물유전성이며, 고세균 영역의 일부 구성원에 의해서만 수행되는 것으로 알려진 혐기성 호흡의 한 형태인 메타노제네시스([34][35]methanogenesis)[36]에 의해 생성된다.메타노겐은 매립지와 다른 토양,[37] 반추동물,[38] 흰개미의 내장, 그리고 해저와 호수 바닥 아래에 있는 무독성 퇴적물을 차지한다.논은 또한 식물이 [39]자라는 동안 많은 양의 메탄을 발생시킨다.이 다단계 공정은 이러한 미생물에 의해 에너지로 사용됩니다.메타노제네시스 순반응은 다음과 같다.
- CO2 + 42 H→ CH4 + 2 HO2
이 과정의 마지막 단계는 메틸코엔자임M환원효소(MCR)[40]에 의해 촉매된다.

반추동물
소와 같은 반추동물은 메탄을 배출하는데, 이는 미국의 연간 대기 [41]중 메탄 배출량의 약 22%를 차지한다.한 연구에 따르면 일반적으로 가축 부문(주로 소, 닭, 돼지)은 인간에 의해 유발되는 [42]메탄의 37%를 생산한다.2013년 연구에서는 가축이 인간에 의한 메탄의 44%와 인간에 의한 온실가스 [43]배출의 약 15%를 차지한다고 추정했다.가축의 메탄 생산량을 줄이고, 치료나 식사 조절 [44][45]등 가스의 연소에너지를 [46]이용하기 위한 많은 노력이 진행되고 있다.
해저 퇴적물
침전물의 처음 몇 센티미터 안에 있는 호기성 미생물에 의해 산소가 제거되기 때문에 해저의 대부분은 무독성이다.산소가 풍부한 해저 아래에서 메타노겐은 다른 유기체에 의해 쓰이거나 [36]가스 하이드레이트에 갇힌 메탄을 생산한다.에너지를 위해 메탄을 이용하는 다른 유기체들은 메타노트로프 ('메탄 섭취')로 알려져 있으며, 깊은 곳에서 생성된 메탄이 거의 해수면에 [36]도달하지 않는 주된 이유이다.고세균과 박테리아 컨소시엄은 메탄의 혐기성 산화(AOM)를 통해 메탄을 산화시키는 것으로 밝혀졌으며, 이에 책임이 있는 유기체는 혐기성 메탄영양성 고세균(ANME)과 황산염 환원균(SRB)[47]이다.
산업 노선
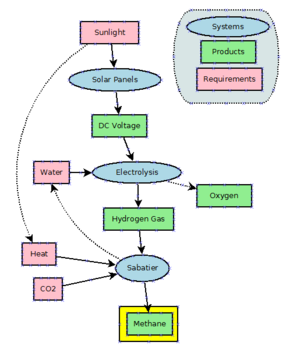
천연가스가 값싸게 풍부하기 때문에 산업적으로 메탄을 생산할 동기는 거의 없다.메탄은 사바티에 과정을 통해 이산화탄소를 수소화함으로써 생성될 수 있다.메탄은 또한 메탄보다 긴 사슬 분자를 생산하기 위해 대규모로 실행되는 피셔-트로프쉬 공정에서 일산화탄소의 수소화 작용의 부수적 산물이다.
대규모 석탄-메탄 가스화의 예로는 1984년 노스다코타 주 뷰라에서 중량, 회분 함량, 낮은 열량 및 스토어 중 자연 연소 성향으로 수송하기 어려운 자원인 저급 갈탄광의 풍부한 지역 자원을 개발하기 위한 방법으로 시작된 그레이트 플레인스 신연료 공장이 있다.분노와 수송.전 세계에는 유사한 공장이 다수 존재하지만, 이 공장들은 대부분 가솔린, 디젤 또는 다른 공정에 대한 공급 원료로 사용되는 긴 사슬 알칸의 생산을 목표로 하고 있습니다.
메탄에 대한 전력은 전기를 이용해 전기분해로 물에서 수소를 생산하고 사바티에 반응을 이용해 수소와 이산화탄소를 결합해 메탄을 생산하는 기술이다.2021년 현재 대부분 개발 중이며 대규모 사용은 아닙니다.이론적으로 이 프로세스는 변동성이 높은 풍력 터빈과 태양열 어레이에 의해 생성된 초과 및 비피크 전력의 완충재로 사용될 수 있다.그러나 현재 전력 에너지를 생산하기 위해 발전소(예: CCGT)에서 매우 많은 양의 천연가스가 사용되고 있기 때문에 효율의 손실은 허용되지 않는다.
실험실 합성
메탄은 메틸 리튬 또는 염화메틸 마그네슘과 같은 메틸 그리냐르 시약의 양성자로 생성될 수 있다.또한 무수 아세트산나트륨과 건조 수산화나트륨을 혼합하여 300°C 이상으로 가열할 수 있습니다([citation needed]부산물로 탄산나트륨을 사용).실제로, 표준 가스 공급 업체의 강철 가스 병으로 순수한 메탄 요구 사항을 쉽게 충족할 수 있습니다.
발생.
메탄은 1776년과 1778년 사이에 알레산드로 볼타에 의해 마조레 호수에서 나오는 습지 가스를 연구하던 중 발견되고 분리되었다.천연가스의 주요 성분으로 부피 기준 약 87%입니다.메탄의 주요 공급원은 천연 가스장으로 알려진 지질 퇴적물로부터의 추출이며, 석탄층 가스 추출은 주요 공급원이 됩니다. 석탄 퇴적물로부터 메탄을 추출하는 방법인 석탄층 메탄 추출은 탄층이 아닌 석탄층에서 메탄을 회수하는 방법인 반면, 강화된 석탄층 메탄 회수 방법은 탄층 메탄 추출을 참조하십시오.이것은 다른 탄화수소 연료와 관련이 있으며, 때로는 헬륨과 질소를 동반하기도 합니다.메탄은 유기물의 혐기성 붕괴에 의해 얕은 수준(저압)에서 생성되고 지구 표면 깊은 곳에서 메탄으로 재작업된다.일반적으로 천연가스를 발생시키는 퇴적물은 기름을 함유한 퇴적물보다 더 깊고 높은 온도로 매장된다.
메탄은 일반적으로 천연가스 형태로 파이프라인 또는 액화 형태로 LNG 운반선을 통해 대량으로 운반됩니다. 트럭으로 운반하는 나라는 거의 없습니다.
대기 메탄
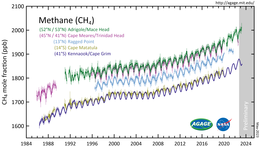
2010년 북극의 메탄 수치는 1850 nmol/mol로 측정되었다.이 수치는 지난 40만 년 동안 어느 때보다도 두 배 이상 높은 수치입니다.세계 대기의 역사적인 메탄 농도는 일반적으로 빙하기 동안 300에서 400nmol/mol 사이, 그리고 따뜻한 간빙기 동안 600에서 700nmol/mol 사이이다.지구의 바다는 북극 [48]메탄의 잠재적인 중요한 원천이다.
메탄은 지구온난화 잠재력이 100년 동안 34(잠재력2 1), 20년 [49][50]동안 72(잠재력 1) 온실가스이다.
지구의 대기 중 메탄 농도는 1750년 이후 약 150% 증가했으며, 이는 수명이 길고 전 세계적으로 혼합된 모든 온실 가스에서 발생하는 총 복사력의 20%를 차지한다.IPCC의 AR6에는 다음과 같이 기술되어 있다: "1750년 경부터 관측된 온실가스(GHG) 농도의 증가는 분명히 인간의 활동에 의해 야기된다.2011년(측정 AR5에 보도되)이후, 농도는 분위기가 증가하는데, 이산화 탄소(이산화 탄소)에 410ppm의 연간 평균에 도달하면서 계속해서, 메탄(CH4)에 1866년 ppb, 그리고 아산화 질소(아산화 질소)에 2019년에 332ppb.2019년에서(…), 대기 농도의 CO2가 적어도 2백만년( 높은 Jim의 그 어느 때보다 높았다.야레 속의 식용어nce)와 CH와2 NO의 농도가4 최소 800,000년 동안 어느 때보다도 높았다(매우 높은 신뢰도).1750년 이후 CO(47%)와4 CH(156%) 농도의 증가는22 지난 80만 년(매우 높은 신뢰도)[10]에 걸친 빙하기와 간빙기 사이의 자연 다년간의 변화(23%)를 훨씬 웃돌고 있다.
2015년부터 2019년까지 대기 중 메탄 수치가 급격히 상승한 것으로 [51][52]기록되었다.2020년 2월, 화석 연료 산업에서 방출되는 가스 및 방출량이 [53]상당히 과소평가되었을 수 있다는 보고가 있었다.
기후 변화는 자연 생태계에서 메탄 생산을 증가시켜 기후 변화 [36][54]피드백을 형성함으로써 대기 중 메탄 수치를 증가시킬 수 있다.메탄 배출량의 증가에 대한 또 다른 설명은 대기 [55]중 메탄을 제거하는 화학 반응이 느려지는 것일 수 있다.
쇄설물
메탄클라트레이트는 메탄의 단일 분자를 가두는 물 분자의 단단한 우리입니다.메탄 포접산염의 상당한 저장고는 고압(1 - 100 MPa, 낮은 끝은 낮은 온도 필요) 및 낮은 온도(< 15 °C, 상단 끝은 높은 [56]압력 필요)에 위치한 가스 포접산염 안정성 구역 내의 북극 영구 동토층과 해저 대륙 가장자리를 따라 발견되었다.메탄 포접은 생물학적 메탄, 열적 메탄 또는 둘의 혼합으로 형성될 수 있습니다.이 퇴적물들은 메탄 연료의 잠재적 원천일 [57][58]뿐만 아니라 지구 온난화의 잠재적 원인이기도 하다.가스 클래트레이트에 저장된 탄소의 전지구적 질량은 여전히 불확실하며, 12,500 Gt의 탄소, 500 Gt의 [59]탄소 정도로 추정되고 있다.추정치는 시간이 지남에 따라 감소했으며,[60] 가장 최근의 추정치는 약 1800 Gt입니다.이러한 불확실성의 대부분은 메탄 발생원과 흡수원의 지식 격차 그리고 전 세계적으로 메탄 포접물의 분포에 기인한다.예를 들어,[61] 메탄 공급원은 비교적 최근에 북극의 초저확산 능선에서 발견되었다.일부 기후 모델은 오늘날 해저에서 발생하는 메탄 배출 상태가 약 5550만 년 전 PETM(Palose-Eosene Thermal Maximum) 기간과 잠재적으로 유사하다고 제안하지만, 포접산염 해리에 의한 메탄이 현재 [60]대기에 도달했음을 나타내는 데이터는 없다.영구 동토층과 해저 메탄 포접물로부터의 북극 메탄 방출은 지구 온난화의 잠재적 결과이며 더 나아가서 원인이다; 이것은 포접물 총 [62][63][64][65]가설로 알려져 있다.2016년 자료에 따르면 북극 영구 동토층은 [66]예상보다 빨리 녹는다.
외계 메탄
성간 매질
메탄은 태양계의 많은 부분에 풍부하며, 잠재적으로 다른 태양계 물체의 표면에서 채취할 수 있다(특히 화성이나 타이탄에서[67] 발견된 지역 물질로부터 메탄 생산을 사용하여). 이는 귀환 [26][68]여행에 연료를 제공한다.
화성
메탄은 태양계의 모든 행성과 대부분의 큰 [citation needed]위성에서 검출되었다.화성을 제외하고, 그것은 비생물학적 [69][70]과정으로부터 온 것으로 여겨진다.

큐리오시티 탐사선은 화성 대기 중 메탄 수치의 계절적 변동을 기록했습니다.이러한 변동은 화성의 여름 말기에 0.[71][72][73][74][75][76][77][78]6ppm으로 최고조에 달했다.
메탄은 미래의 화성 임무에서 가능한 로켓 추진체로 제안되어 왔다. 그 이유는 부분적으로 현장 자원 [79]활용을 통해 화성에서 메탄을 합성할 수 있기 때문이다.사바티에 메탄화 반응의 적응은 혼합 촉매층 및 단일 원자로의 역수성 가스 이동과 함께 화성 지하 토양으로부터의 물과 화성 [67]대기 중의 이산화탄소를 이용하여 화성에서 이용 가능한 원료로부터 메탄을 생산하기 위해 사용될 수 있다.
메탄은 물, 이산화탄소, 그리고 [80]화성에서 흔한 것으로 알려진 미네랄 올리빈을 포함한 독사화라고[a] 불리는 비생물학적 과정에 의해 생성될 수 있다.
역사
1776년 11월, 메탄은 이탈리아와 스위스에 걸쳐 있는 마조레 호수의 늪에서 이탈리아 물리학자 알레산드로 볼타에 의해 과학적으로 처음 발견되었다.볼타는 벤자민 프랭클린이 쓴 "인화성 공기"[81]에 관한 논문을 읽고 나서 그 물질을 찾도록 영감을 받았습니다.볼타는 습지에서 분출되는 가스를 모아 1778년까지 순수한 [82]메탄가스를 분리했다.그는 또한 가스가 전기 [82]스파크로 점화될 수 있다는 것을 시연했다.
92명이 사망한 1812년 펠링 광산 참사 이후 험프리 데이비 경은 공포에 휩싸인 연소암은 사실상 [83]메탄이라는 사실을 밝혀냈다.
"메탄"이라는 이름은 1866년 독일의 화학자 아우구스트 빌헬름 [84][85]폰 호프만에 의해 만들어졌습니다.그 이름은 메탄올에서 유래되었다.
어원학
어원적으로 메탄이라는 단어는 알칸과에 속하는 물질을 나타내는 화학 접미사 "-ane"와 독일 메틸(1840) 또는 프랑스 메틸렌(영어 "메틸렌"에 해당하는)에서 직접 유래한 메틸이라는 단어에서 유래했다.1834년 장 밥티스트 뒤마와 외젠 페리고가 그리스어 '메티'(mead)와 '나무'를 뜻하는 '히레'(hyle)에서 유래했다.라디칼은 나무의 증류에 의해 처음 분리된 알코올인 메탄올에서 처음 검출되었기 때문에 이름을 따왔다.화학 접미사 -ane는 추상화를 나타내기 위해 적용되는 라틴 여성 접미사 -ina에서 유래한 좌표 화학 접미사 -ine에서 유래했다."-ane", "-ene", "-one" 등의 배위는 1866년 독일의 화학자 August Wilhelm von Hofmann (1818–1892)[86]에 의해 제안되었다.
약어
CH-C는4 메탄 덩어리에 포함된 탄소의 질량을 의미하며 메탄 덩어리는 항상 CH-C의4 [87][88]1.33배이다. CH-C는 메탄-탄소4 비율(질량 [89]기준 1.33배)을 의미하기도 한다.대기 중 메탄은 일반적으로 테라그램(Tg4 CH) 또는 수백만 미터톤(MMT4 CH) 단위로 측정되는데, 이는 같은 [90]것을 의미한다.나노몰(nmol, 10억분의 1 몰), 몰(mol), 킬로그램 및 그램과 같은 다른 표준 단위도 사용됩니다.
안전.
메탄은 무독성이지만 인화성이 매우 강하며 공기와 폭발성 혼합물을 형성할 수 있습니다.대부분의 사람들이 부작용 없이 21%에서 16%로 감소하는 것을 견딜 수 있기 때문에, 메탄은 또한 치환에 의해 산소 농도가 약 16% 이하로 감소하는 경우에도 질식제이다.질식 위험이 큰 메탄 농도는 가연성 또는 폭발성 혼합물의 5~15% 농도보다 훨씬 높다.메탄 오프 가스는 매립지 근처의 건물 내부에 침투하여 거주자를 상당한 수준의 메탄에 노출시킬 수 있습니다.일부 건물은 지하실 아래에 이 가스를 적극적으로 포집하여 건물 밖으로 배출할 수 있도록 특별히 설계된 회수 시스템을 갖추고 있습니다.
메탄가스 폭발은 많은 치명적인 광산 [91]재앙의 원인이 된다.메탄가스 폭발은 2010년 4월 5일 웨스트버지니아에서 [92]29명의 사망자를 낸 어퍼 빅 브랜치 탄광 참사의 원인이었다.제트 화재 참사로 결론난 과거의 우발적인 방출로 인해 천연가스 방출은 안전 공학 분야에서도 주요 관심사였다.[93][94]
「 」를 참조해 주세요.
설명 메모
인용문
- ^ a b "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. pp. 3–4. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
Methane is a retained name (see P-12.3) that is preferred to the systematic name ‘carbane’, a name never recommended to replace methane, but used to derive the names ‘carbene’ and ‘carbyne’ for the radicals H2C2• and HC3•, respectively.
- ^ "Gas Encyclopedia". Archived from the original on December 26, 2018. Retrieved November 7, 2013.
- ^ a b c d 헤인즈, 페이지 3.344
- ^ 헤인즈, 5.156페이지
- ^ 헤인즈, 페이지 3.578
- ^ 헤인즈, 5.26, 5.67페이지
- ^ "Safety Datasheet, Material Name: Methane" (PDF). USA: Metheson Tri-Gas Incorporated. December 4, 2009. Archived from the original (PDF) on June 4, 2012. Retrieved December 4, 2011.
- ^ NOAA Office of Response and Restoration, US GOV. "METHANE". noaa.gov. Archived from the original on January 9, 2019. Retrieved March 20, 2015.
- ^ Khalil, M. A. K. (1999). "Non-Co2 Greenhouse Gases in the Atmosphere". Annual Review of Energy and the Environment. 24: 645–661. doi:10.1146/annurev.energy.24.1.645.
- ^ a b "Climate Change 2021. The Physical Science Basis. Summary for Policymakers. Working Group I contribution to the WGI Sixth Assessment Report of the Intergovernmental Panel on Climate Change". IPCC. The Intergovernmental Panel on Climate Change. Archived from the original on August 22, 2021. Retrieved August 22, 2021.
- ^ a b Etiope, Giuseppe; Lollar, Barbara Sherwood (2013). "Abiotic Methane on Earth". Reviews of Geophysics. 51 (2): 276–299. Bibcode:2013RvGeo..51..276E. doi:10.1002/rog.20011. S2CID 56457317.
- ^ Hensher, David A.; Button, Kenneth J. (2003). Handbook of transport and the environment. Emerald Group Publishing. p. 168. ISBN 978-0-08-044103-0. Archived from the original on March 19, 2015. Retrieved February 22, 2016.
- ^ P.G.J Irwin; et al. (January 12, 2022). "Hazy Blue Worlds: A Holistic Aerosol Model for Uranus and Neptune, Including Dark Spots" (PDF). Journal of Geophysical Research: Planets. 127 (6). arXiv:2201.04516. doi:10.1029/2022JE007189. S2CID 245877540.
- ^ Bini, R.; Pratesi, G. (1997). "High-pressure infrared study of solid methane: Phase diagram up to 30 GPa". Physical Review B. 55 (22): 14800–14809. Bibcode:1997PhRvB..5514800B. doi:10.1103/physrevb.55.14800.
- ^ Wendelin Himmelheber. "Crystal structures". Archived from the original on February 12, 2020. Retrieved December 10, 2019.
- ^ Baik, Mu-Hyun; Newcomb, Martin; Friesner, Richard A.; Lippard, Stephen J. (2003). "Mechanistic Studies on the Hydroxylation of Methane by Methane Monooxygenase". Chemical Reviews. 103 (6): 2385–419. doi:10.1021/cr950244f. PMID 12797835.
- ^ Snyder, Benjamin E. R.; Bols, Max L.; Schoonheydt, Robert A.; Sels, Bert F.; Solomon, Edward I. (December 19, 2017). "Iron and Copper Active Sites in Zeolites and Their Correlation to Metalloenzymes". Chemical Reviews. 118 (5): 2718–2768. doi:10.1021/acs.chemrev.7b00344. PMID 29256242.
- ^ Reimann, Joachim; Jetten, Mike S.M.; Keltjens, Jan T. (2015). "Chapter 7 Metal Enzymes in "Impossible" Microorganisms Catalyzing the Anaerobic Oxidation of Ammonium and Methane". In Peter M.H. Kroneck and Martha E. Sosa Torres (ed.). Sustaining Life on Planet Earth: Metalloenzymes Mastering Dioxygen and Other Chewy Gases. Metal Ions in Life Sciences. Vol. 15. Springer. pp. 257–313. doi:10.1007/978-3-319-12415-5_7. ISBN 978-3-319-12414-8. PMID 25707470.
- ^ Bordwell, Frederick G. (1988). "Equilibrium acidities in dimethyl sulfoxide solution". Accounts of Chemical Research. 21 (12): 456–463. doi:10.1021/ar00156a004.
- ^ Rasul, G.; Surya Prakash, G.K.; Olah, G.A. (2011). "Comparative study of the hypercoordinate carbonium ions and their boron analogs: A challenge for spectroscopists". Chemical Physics Letters. 517 (1): 1–8. Bibcode:2011CPL...517....1R. doi:10.1016/j.cplett.2011.10.020.
- ^ Bernskoetter, W. H.; Schauer, C. K.; Goldberg, K. I.; Brookhart, M. (2009). "Characterization of a Rhodium(I) σ-Methane Complex in Solution". Science. 326 (5952): 553–556. Bibcode:2009Sci...326..553B. doi:10.1126/science.1177485. PMID 19900892. S2CID 5597392.
- ^ 일부 가연물의 에너지 함량(MJ/kg) 2014년 1월 9일 웨이백 기계에서 보관.사람.hofstra.edu 를 참조해 주세요.2014년 3월 30일 취득.
- ^ March, Jerry (1968). Advance Organic Chemistry: Reactions, Mechanisms and Structure. New York: McGraw-Hill Book Company. pp. 533–534.
- ^ "Lumber Company Locates Kilns at Landfill to Use Methane – Energy Manager Today". Energy Manager Today. September 23, 2015. Archived from the original on July 9, 2019. Retrieved March 11, 2016.
- ^ Cornell, Clayton B. (April 29, 2008). "Natural Gas Cars: CNG Fuel Almost Free in Some Parts of the Country". Archived from the original on January 20, 2019. Retrieved July 25, 2009.
Compressed natural gas is touted as the 'cleanest burning' alternative fuel available, since the simplicity of the methane molecule reduces tailpipe emissions of different pollutants by 35 to 97%. Not quite as dramatic is the reduction in net greenhouse-gas emissions, which is about the same as corn-grain ethanol at about a 20% reduction over gasoline
- ^ a b Thunnissen, Daniel P.; Guernsey, C. S.; Baker, R. S.; Miyake, R. N. (2004). "Advanced Space Storable Propellants for Outer Planet Exploration" (PDF). American Institute of Aeronautics and Astronautics (4–0799): 28. Archived from the original (PDF) on March 10, 2016.
- ^ "Blue Origin BE-4 Engine". Archived from the original on October 1, 2021. Retrieved June 14, 2019.
We chose LNG because it is highly efficient, low cost and widely available. Unlike kerosene, LNG can be used to self-pressurize its tank. Known as autogenous repressurization, this eliminates the need for costly and complex systems that draw on Earth’s scarce helium reserves. LNG also possesses clean combustion characteristics even at low throttle, simplifying engine reuse compared to kerosene fuels.
- ^ 수소 생산 전문가 패널 보고서: 수소 및 연료 전지 기술 자문 위원회 소위원회 2020년 2월 14일 웨이백 머신에 보관.미국 에너지부(2013년 5월).
- ^ 로스버그, M. et al.(2006) Wiley-VCH, Weinheim의 Ulmann's Encyclopedia of Industrial Chemistry, Willy-VCH, Industrial Chemistry, Weinheim에 있는 "염화탄화수소"doi: 10.1002/14356007.a06_233.pub2.
- ^ Lumbers, Brock (2022). "Mathematical modelling and simulation of the thermo-catalytic decomposition of methane for economically improved hydrogen production". International Journal of Hydrogen Energy. 47 (7): 4265–4283. doi:10.1016/j.ijhydene.2021.11.057. S2CID 244814932. Retrieved June 15, 2022.
- ^ Lumbers, Brock (2022). "Low-emission hydrogen production via the thermo-catalytic decomposition of methane for the decarbonisation of iron ore mines in Western Australia". International Journal of Hydrogen Energy. 47 (37): 16347–16361. doi:10.1016/j.ijhydene.2022.03.124. S2CID 248018294. Retrieved July 10, 2022.
- ^ Kietäväinen and Purkamo (2015). "The origin, source, and cycling of methane in deep crystalline rock biosphere". Front. Microbiol. 6: 725. doi:10.3389/fmicb.2015.00725. PMC 4505394. PMID 26236303.
- ^ Cramer and Franke (2005). "Indications for an active petroleum system in the Laptev Sea, NE Siberia". Journal of Petroleum Geology. 28 (4): 369–384. Bibcode:2005JPetG..28..369C. doi:10.1111/j.1747-5457.2005.tb00088.x. Archived from the original on October 1, 2021. Retrieved May 23, 2017.
- ^ Lessner, Daniel J. (2009년 12월) 메타노제네시스 생화학.수신자: eLS. John Wiley & Sons Ltd, Chichester.http://www.els.net 2011년 5월 13일 Wayback Machine에서 아카이브 완료
- ^ Thiel, Volker (2018), "Methane Carbon Cycling in the Past: Insights from Hydrocarbon and Lipid Biomarkers", in Wilkes, Heinz (ed.), Hydrocarbons, Oils and Lipids: Diversity, Origin, Chemistry and Fate, Handbook of Hydrocarbon and Lipid Microbiology, Springer International Publishing, pp. 1–30, doi:10.1007/978-3-319-54529-5_6-1, ISBN 9783319545295, S2CID 105761461
- ^ a b c d Dean, Joshua F.; Middelburg, Jack J.; Röckmann, Thomas; Aerts, Rien; Blauw, Luke G.; Egger, Matthias; Jetten, Mike S. M.; de Jong, Anniek E. E.; Meisel, Ove H. (2018). "Methane Feedbacks to the Global Climate System in a Warmer World". Reviews of Geophysics. 56 (1): 207–250. Bibcode:2018RvGeo..56..207D. doi:10.1002/2017RG000559. hdl:1874/366386.
- ^ Serrano-Silva, N.; Sarria-Guzman, Y.; Dendooven, L.; Luna-Guido, M. (2014). "Methanogenesis and methanotrophy in soil: a review". Pedosphere. 24 (3): 291–307. doi:10.1016/s1002-0160(14)60016-3.
- ^ Sirohi, S. K.; Pandey, Neha; Singh, B.; Puniya, A. K. (September 1, 2010). "Rumen methanogens: a review". Indian Journal of Microbiology. 50 (3): 253–262. doi:10.1007/s12088-010-0061-6. PMC 3450062. PMID 23100838.
- ^ IPCC. 기후 변화 2013: 2018년 10월 3일 Wayback Machine에서 보관된 물리 과학 기반입니다.유엔환경계획, 2013: Ch. 6, 페이지 507 IPCC.ch
- ^ Lyu, Zhe; Shao, Nana; Akinyemi, Taiwo; Whitman, William B. (2018). "Methanogenesis". Current Biology. 28 (13): R727–R732. doi:10.1016/j.cub.2018.05.021. PMID 29990451.
- ^ "Inventory of U.S. Greenhouse Gas Emissions and Sinks: 1990–2014". 2016. Archived from the original on April 12, 2019. Retrieved April 11, 2019.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말)[페이지 필요] - ^ FAO (2006). Livestock's Long Shadow–Environmental Issues and Options. Rome, Italy: Food and Agriculture Organization of the United Nations (FAO). Archived from the original on July 26, 2008. Retrieved October 27, 2009.
- ^ Gerber, P.J.; Steinfeld, H.; Henderson, B.; Mottet, A.; Opio, C.; Dijkman, J.; Falcucci, A. & Tempio, G. (2013). "Tackling Climate Change Through Livestock". Rome: Food and Agriculture Organization of the United Nations (FAO). Archived from the original on July 19, 2016. Retrieved July 15, 2016.
- ^ Roach, John (May 13, 2002). "New Zealand Tries to Cap Gaseous Sheep Burps". National Geographic. Archived from the original on June 4, 2011. Retrieved March 2, 2011.
- ^ Roque, Breanna M.; Venegas, Marielena; Kinley, Robert D.; Nys, Rocky de; Duarte, Toni L.; Yang, Xiang; Kebreab, Ermias (March 17, 2021). "Red seaweed (Asparagopsis taxiformis) supplementation reduces enteric methane by over 80 percent in beef steers". PLOS ONE. 16 (3): e0247820. Bibcode:2021PLoSO..1647820R. doi:10.1371/journal.pone.0247820. ISSN 1932-6203. PMC 7968649. PMID 33730064.
- ^ Silverman, Jacob (July 16, 2007). "Do cows pollute as much as cars?". HowStuffWorks.com. Archived from the original on November 4, 2012. Retrieved November 7, 2012.
- ^ Knittel, K.; Wegener, G.; Boetius, A. (2019), McGenity, Terry J. (ed.), "Anaerobic Methane Oxidizers", Microbial Communities Utilizing Hydrocarbons and Lipids: Members, Metagenomics and Ecophysiology, Handbook of Hydrocarbon and Lipid Microbiology, Springer International Publishing, pp. 1–21, doi:10.1007/978-3-319-60063-5_7-1, ISBN 9783319600635
- ^ "Study Finds Surprising Arctic Methane Emission Source". NASA. April 22, 2012. Archived from the original on August 4, 2014. Retrieved March 30, 2014.
- ^ IPCC 5차 평가 보고서, 표 8.7, 8장 8-58 2013년 11월 1일 Wayback Machine에서 아카이브(PDF; 8.0MB)
- ^ Shindell, D. T.; Faluvegi, G.; Koch, D. M.; Schmidt, G. A.; Unger, N.; Bauer, S. E. (2009). "Improved Attribution of Climate Forcing to Emissions". Science. 326 (5953): 716–718. Bibcode:2009Sci...326..716S. doi:10.1126/science.1174760. PMID 19900930. S2CID 30881469. Archived from the original on August 7, 2020. Retrieved August 25, 2020.
- ^ Nisbet, E.G. (February 5, 2019). "Very Strong Atmospheric Methane Growth in the 4 Years 2014–2017: Implications for the Paris Agreement". Global Biogeochemical Cycles. 33 (3): 318–342. Bibcode:2019GBioC..33..318N. doi:10.1029/2018GB006009.
- ^ McKie, Robin (February 2, 2017). "Sharp rise in methane levels threatens world climate targets". The Observer. ISSN 0029-7712. Archived from the original on July 30, 2019. Retrieved July 14, 2019.
- ^ 석유와 가스로부터의 Chelsea Harvey Methan 배출은 상당히 과소평가될 수 있다; 천연 자원으로부터의 메탄 추정치는 너무 높아서 인간 활동에 대한 부담을 옮기고 있다. 2020년 2월 24일 사이언티픽 아메리칸을 통한 웨이백 머신 E&E 뉴스에서 보관된 2020년 2월 21일
- ^ 데미안 캐링턴 (2020년 7월 21일)남극에서 발견된 해저 메탄 최초의 활발한 누출 2020년 7월 22일 웨이백 머신에 보관된
- ^ Ravilious, Kate (July 5, 2022). "Methane much more sensitive to global heating than previously thought – study". The Guardian. Retrieved July 5, 2022.
- ^ Bohrmann, Gerhard; Torres, Marta E. (2006), Schulz, Horst D.; Zabel, Matthias (eds.), "Gas Hydrates in Marine Sediments", Marine Geochemistry, Springer Berlin Heidelberg, pp. 481–512, doi:10.1007/3-540-32144-6_14, ISBN 9783540321446
- ^ 밀러, G.타일러(2007년).지구 유지: 통합 접근법.미국:Thomson Advantage Books, 페이지 160. ISBN 0534496725
- ^ Dean, J. F. (2018). "Methane feedbacks to the global climate system in a warmer world". Reviews of Geophysics. 56 (1): 207–250. Bibcode:2018RvGeo..56..207D. doi:10.1002/2017RG000559. hdl:1874/366386.
- ^ Boswell, Ray; Collett, Timothy S. (2011). "Current perspectives on gas hydrate resources". Energy Environ. Sci. 4 (4): 1206–1215. doi:10.1039/c0ee00203h.
- ^ a b Ruppel and Kessler (2017). "The interaction of climate change and methane hydrates". Reviews of Geophysics. 55 (1): 126–168. Bibcode:2017RvGeo..55..126R. doi:10.1002/2016RG000534. Archived from the original on February 7, 2020. Retrieved September 16, 2019.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ "New source of methane discovered in the Arctic Ocean". phys.org. May 1, 2015. Archived from the original on April 10, 2019. Retrieved April 10, 2019.
- ^ "Methane Releases From Arctic Shelf May Be Much Larger and Faster Than Anticipated" (Press release). National Science Foundation (NSF). March 10, 2010. Archived from the original on August 1, 2018. Retrieved April 6, 2018.
- ^ Connor, Steve (December 13, 2011). "Vast methane 'plumes' seen in Arctic ocean as sea ice retreats". The Independent. Archived from the original on December 25, 2011. Retrieved September 4, 2017.
- ^ "Arctic sea ice reaches lowest extent for the year and the satellite record" (Press release). The National Snow and Ice Data Center (NSIDC). September 19, 2012. Archived from the original on October 4, 2012. Retrieved October 7, 2012.
- ^ "Frontiers 2018/19: Emerging Issues of Environmental Concern". UN Environment. Archived from the original on March 6, 2019. Retrieved March 6, 2019.
- ^ Reuters (June 18, 2019). "Scientists shocked by Arctic permafrost thawing 70 years sooner than predicted". The Guardian. ISSN 0261-3077. Archived from the original on October 6, 2019. Retrieved July 14, 2019.
- ^ a b Zubrin, R. M.; Muscatello, A. C.; Berggren, M. (2013). "Integrated Mars in Situ Propellant Production System". Journal of Aerospace Engineering. 26: 43–56. doi:10.1061/(ASCE)AS.1943-5525.0000201.
- ^ "Methane Blast". NASA. May 4, 2007. Archived from the original on November 16, 2019. Retrieved July 7, 2012.
- ^ Chang, Kenneth (November 2, 2012). "Hope of Methane on Mars Fades". The New York Times. Archived from the original on June 8, 2019. Retrieved November 3, 2012.
- ^ Atreya, Sushil K.; Mahaffy, Paul R.; Wong, Ah-San (2007). "Methane and related trace species on Mars: origin, loss, implications for life, and habitability". Planetary and Space Science. 55 (3): 358–369. Bibcode:2007P&SS...55..358A. doi:10.1016/j.pss.2006.02.005. hdl:2027.42/151840.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Brown, Dwayne; Wendel, JoAnna; Steigerwald, Bill; Jones, Nancy; Good, Andrew (June 7, 2018). "Release 18-050 – NASA Finds Ancient Organic Material, Mysterious Methane on Mars". NASA. Archived from the original on June 7, 2018. Retrieved June 7, 2018.
- ^ NASA (June 7, 2018). "Ancient Organics Discovered on Mars – video (03:17)". NASA. Archived from the original on June 7, 2018. Retrieved June 7, 2018.
- ^ Wall, Mike (June 7, 2018). "Curiosity Rover Finds Ancient 'Building Blocks for Life' on Mars". Space.com. Archived from the original on June 7, 2018. Retrieved June 7, 2018.
- ^ Chang, Kenneth (June 7, 2018). "Life on Mars? Rover's Latest Discovery Puts It 'On the Table' – The identification of organic molecules in rocks on the red planet does not necessarily point to life there, past or present, but does indicate that some of the building blocks were present". The New York Times. Archived from the original on June 8, 2018. Retrieved June 8, 2018.
- ^ Voosen, Paul (June 7, 2018). "NASA rover hits organic pay dirt on Mars". Science. doi:10.1126/science.aau3992. S2CID 115442477.
- ^ ten Kate, Inge Loes (June 8, 2018). "Organic molecules on Mars". Science. 360 (6393): 1068–1069. Bibcode:2018Sci...360.1068T. doi:10.1126/science.aat2662. PMID 29880670. S2CID 46952468.
- ^ Webster, Christopher R.; et al. (June 8, 2018). "Background levels of methane in Mars' atmosphere show strong seasonal variations". Science. 360 (6393): 1093–1096. Bibcode:2018Sci...360.1093W. doi:10.1126/science.aaq0131. PMID 29880682.
- ^ Eigenbrode, Jennifer L.; et al. (June 8, 2018). "Organic matter preserved in 3-billion-year-old mudstones at Gale crater, Mars". Science. 360 (6393): 1096–1101. Bibcode:2018Sci...360.1096E. doi:10.1126/science.aas9185. PMID 29880683.
- ^ Richardson, Derek (September 27, 2016). "Elon Musk Shows Off Interplanetary Transport System". Spaceflight Insider. Archived from the original on October 1, 2016. Retrieved October 3, 2016.
- ^ Oze, C.; Sharma, M. (2005). "Have olivine, will gas: Serpentinization and the abiogenic production of methane on Mars". Geophysical Research Letters. 32 (10): L10203. Bibcode:2005GeoRL..3210203O. doi:10.1029/2005GL022691. S2CID 28981740.
- ^ 볼타, 알레산드로 (1777) 돈 알레산드로 볼타... Sul' Aria 인화성 Nativa Delle Paludi 2018년 11월 6일 Wayback Machine에 보관 [돈 알레산드로 볼타의 편지...이탈리아 밀라노, 주세페 마렐리.
- ^ a b Methane. BookRags. Archived from the original on March 3, 2016. Retrieved January 26, 2012.
- ^ Holland, John (1841). The history and description of fossil fuel, the collieries, and coal trade of Great Britain. London, Whittaker and Co. pp. 271–272. Retrieved May 16, 2021.
- ^ 57-58페이지의 각주를 참조한다Hofmann, A. W. (1866). "On the action of trichloride of phosphorus on the salts of the aromatic monoamines". Proceedings of the Royal Society of London. 15: 55–62. JSTOR 112588. Archived from the original on May 3, 2017. Retrieved June 14, 2016..
- ^ McBride, James Michael(1999) "단순 알칸의 계통명칭 개발"예일대학교 화학과(코네티컷주 뉴헤이븐).2012년 3월 16일 Wayback Machine에서 아카이브 완료
- ^ Harper, Douglas. "methane". Online Etymology Dictionary.
- ^ Jayasundara, Susantha (December 3, 2014). "Is there is any difference in expressing greenhouse gases as CH4Kg/ha and CH4-C Kg/ha?". ResearchGate. Archived from the original on October 1, 2021. Retrieved August 26, 2020.
- ^ "User's Guide For Estimating Carbon Dioxide, Methane, And Nitrous Oxide Emissions From Agriculture Using The State Inventory Tool" (PDF). US EPA. November 26, 2019. Archived (PDF) from the original on October 1, 2021. Retrieved August 26, 2020.
- ^ "What does CH4-C mean? – Definition of CH4-C – CH4-C stands for Methane-carbon ratio". acronymsandslang.com. Archived from the original on April 11, 2015. Retrieved August 26, 2020.
- ^ Office of Air and Radiation, US EPA (October 7, 1999). "U.S. Methane Emissions 1990–2020: Inventories, Projections, and Opportunities for Reductions (EPA 430-R-99-013)" (PDF). ourenergypolicy.org. Archived (PDF) from the original on October 26, 2020. Retrieved August 26, 2020.
- ^ Dozolme, Philippe. "Common Mining Accidents". About.com. Archived from the original on November 11, 2012. Retrieved November 7, 2012.
- ^ Messina, Lawrence & Bluestein, Greg (April 8, 2010). "Fed official: Still too soon for W.Va. mine rescue". News.yahoo.com. Archived from the original on April 8, 2010. Retrieved April 8, 2010.
- ^ OSMAN, Karim; GENIAUT, Baptiste; HERCHIN, Nicolas; BLANCHETIERE, Vincent (2015). "A review of damages observed after catastrophic events experienced in the mid-stream gas industry compared to consequences modelling tools" (PDF). Symposium Series. 160 (25). Retrieved July 1, 2022.
- ^ Casal, Joaquim; Gómez-Mares, Mercedes; Muñoz, Miguel; Palacios, Adriana (2012). "Jet Fires: a "Minor" Fire Hazard?" (PDF). Chemical Engineering Transactions. 26: 13–20. doi:10.3303/CET1226003. Retrieved July 1, 2022.
인용된 출처
- Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97th ed.). CRC Press. ISBN 9781498754293.
외부 링크
- 주기율표의 메탄 (노팅엄 대학교)
- 국제화학안전카드 0291
- 가스(메탄) 하이드레이트– 새로운 프런티어 – 미국 지질 조사
- Lunsford, Jack H. (2000). "Catalytic conversion of methane to more useful chemicals and fuels: A challenge for the 21st century". Catalysis Today. 63 (2–4): 165–174. doi:10.1016/S0920-5861(00)00456-9.
- CDC - 광업 메탄 제어 핸드북