케토베미돈
Ketobemidone그중에서도 케토간이라는 브랜드명으로 판매되는 케토베미돈은 강력한 합성 오피오이드 진통제다. 통증에 대한 효과는 모르핀과 동일한 범위에 있으며, 대사물인 노르케토베미돈에 의해 일부 NMDA 길항제 특성을 전달하기도 한다.[2] 이것은 다른 오피오이드에 잘 반응하지 않는 어떤 종류의 통증에 유용하게 만들 수도 있다.[2] 덴마크, 아이슬란드, 노르웨이, 스웨덴에서 판매되며 심한 통증에 사용된다.[3]
역사
케토베미돈은 제2차 세계대전 당시 회흐스트에 있는 I.G.파르벤인더스트리 연구실에서 아이슬렙과 동료들에 의해 처음으로 합성되었다.[4] 인간에 대한 최초의 연구는 1946년에 발표되었고,[5] 얼마 지나지 않아 임상 의학에 소개되었다. 1970년 통제 물질법이 공포되고 9628년의 ACSCN으로 부칙 I에 할당되었을 때 미국에서는 임상 용도로 사용되지 않았다. 2013년 현재 DEA에 의해 연간 제조 쿼터가 할당되지 않았다.[6]
화이저는 케토간과 케토락스라는 상표로 케토베미돈을 제조한다. 그것은 알약, 약, 주사액으로 이용 가능하다. 10 또는 25mg 케토베미돈을 함유한 일부 국가에서는 케토두르로 판매되는 지속적인 방출 제형이 존재한다.
약리학
이전 중독자들에 대한 실험은 그것이 꽤 중독성이 있으며 다른 오피오이드에 비해 많은 양을 섭취했을 때 전, 현재의 오피오이드 중독자들의 학대 잠재력이 증가했을 수 있다는 것을 보여주었다. 정부가 케토베미돈의 제조와 사용을 중단하도록 촉구하는 결의안의 초안을 마련하기 위한 노력이 처음 제안되었다.[7] 이 결과는 임상 관찰과 일치하지 않았으며, 1958년의 또 다른 연구에서는 모르핀보다 중독성이 강하지 않았다. 그 연구는 모르핀의 경우 행복감에 대한 선량은 진통제의 선량과 동일하지만 케토베미돈의 경우 진통 선량은 행복선량에 훨씬 못 미친다는 것을 알아챘다. 따라서 모르핀에 비하여도 케토베미돈은 유의미한 행복감을 유발하지 않고 훨씬 더 효과적일 수 있으며, 이것은 감독이나 자격을 갖춘 임상의에게 중독의 위험이 낮다. [8] 케토베미돈은 주로 스칸디나비아 국가에서 사용되며, 덴마크가 통계에서 1위를 차지했다.[9]
5-10mg의 구강 또는 5-7.5mg의 항문증은 정맥주사로 3~5시간 지속된다. 케토베미돈은 또한 진통증을 개선할 수 있는 스파스몰리틱으로 조제 시에도 사용할 수 있다.
신진대사
케토베미돈은 주로 페놀 하이드록실 그룹의 결합과 N-데메틸화에 의해 대사된다. 약 13-24%만이 정맥주사 후 변하지 않고 배설된다.[10]
화학
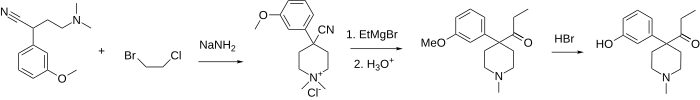
케토베미돈은 1-메틸-4-(3-히드록시페닐)-4-프로피오닐피페리딘이다. 보통 흰 가루인 염산염으로 사용할 수 있다. 알킬라팅(3-메톡시페닐)아세토나이트릴레와 bis(2-클로로에틸)메틸아민으로 합성되며, 에틸마그네슘브로마이드, 마지막으로 하이드로브롬산을 사용한 O-데메틸화(O-demethylation)로 합성된다.[11]
bis(2-cloroethyl)메틸아민의 강한 방부제 특성 때문에 케토베미돈(ketobemidone)을 얻기 위해 개발된 다른 루트가 많다. 아래에 표시된 경로는 2-클로로-N, N-디메틸레틸아민 또는 2-클로로-N-벤질-N-메틸레틸아민으로 동일한 (3-메톡시페닐)아세토나이트릴을 최초로 알킬리팅하는 경로를 나타낸다.[12] 다음, 아민 화합물 다시 한번, 따라서, 일반적인 4-(3-methoxyphenyl)-4-cyano-1-methyl-pyperidin에 thiophenol salt[13](N,N-dimethylammonium에)또는 촉매 hydrogenation[14](둘 다 화합물들을 위해서)를 사용하여 dequaternized 수 있는 4암모늄염을 습득하는 것은 피페리딘 링을 완성하느라고 혼합 1-bromo-2-chloroethane을 사용하여 alkylated 있다.e 후기는 에틸마그네슘 브로마이드와 에테르 갈라바지에 대한 그리냐드 반응 후 케토베미돈(ketobemidone은 에틸마그네슘 브로마이드와 에테르 갈라바지에 반응한다.
참고 항목
참조
- ^ https://www.ema.europa.eu/documents/psusa/ketobemidone-list-nationally-authorised-medicinal-products-psusa/0001807/202005_en.pdf
- ^ Jump up to: a b Ebert B, Thorkildsen C, Andersen S, Christrup LL, Hjeds H (September 1998). "Opioid analgesics as noncompetitive N-methyl-D-aspartate (NMDA) antagonists". Biochemical Pharmacology. 56 (5): 553–9. doi:10.1016/S0006-2952(98)00088-4. PMID 9783723.
- ^ Brayfield A, ed. (9 January 2017). "Ketobemidone Hydrochloride: Martindale: The Complete Drug Reference". MedicinesComplete. London, UK: Pharmaceutical Press. Retrieved 6 September 2017.
- ^ GB 특허 609763, "피페리딜 케톤 제조"는 1948-10-06년 발행되었으며, Ciba Ltd에 할당되었다.
- ^ 미국 특허권 2486796, Meischer, K.; Kaegi, H. Kaegi, "1-alkyl-4-hydroxypheryl-piperidil-4-ketones" 1949-11-01 발행
- ^ "DEA Diversion Control Division".
- ^ "Development of Synthetic Narcotic Drugs". Bulletin on Narcotic Drugs. 1956 (1): 11–14. 1956. Retrieved 2012-07-05.
- ^ Bondesson, U. (1982). Biological Fate of Ketobemidone in Man. Abstracts of Uppsala Dissertations from the Faculty of Pharmacy. 68. ISBN 978-91-554-1243-2.
- ^ "Statistical Information on Narcotic Drugs" (PDF). INCB. 2004. Archived from the original (PDF) on 2006-10-07. Retrieved 2006-09-07.
- ^ Bondesson U, Hartvig P, Danielsson B (1981). "Quantitative determination of the urinary excretion of ketobemidone and four of its metabolites after intravenous and oral administration in man". Drug Metabolism and Disposition. 9 (4): 376–80. PMID 6114838.
- ^ William Andrew Publishing (2013). "Cetobemidone" (excerpt). Pharmaceutical Manufacturing Encyclopedia. Elsevier. ISBN 9780815518563.
- ^ Avison AW, Morrison AL (1950). "303. Synthetic Analgesics. Part VI. The Synthesis of Ketobemidone". Journal of the Chemical Society (Resumed). 1950: 1469–1471. doi:10.1039/JR9500001469.
- ^ Shamma M, Deno NC, Remar JF (1966). "The selective demethylation of quaternary ammonium salts". Tetrahedron Letters. 7 (13): 1375–1379. doi:10.1016/s0040-4039(01)99725-4.
- ^ Kägi H, Miescher K (1949). "Über eine neue Synthese morphinähnlich wirkender 4-Phenylpiperidin-4-alkylketone und verwandter Verbindungen". Helvetica Chimica Acta. 32 (7): 2489–2507. doi:10.1002/hlca.19490320736.
외부 링크
- "Ketobemidone". Drug Information Portal. U.S. National Library of Medicine.