히드라조산
Hydrazoic acid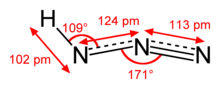 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 아지드화수소 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.029.059 |
| EC 번호 |
|
| 773 | |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| HN3 | |
| 몰 질량 | 43.03g/140 |
| 외모 | 무색의 휘발성이 높은 액체 |
| 밀도 | 1.09 g/cm3 |
| 녹는점 | - 80 °C (-112 °F, 193 K) |
| 비등점 | 37 °C (99 °F, 310 K) |
| 용해성이 높은 | |
| 용해성 | 알칼리, 알코올, 에테르에 녹는 |
| 산도(pKa) | 4.6 [1] |
| 켤레 기저 | 아지데 |
| 구조. | |
| 거의 선형의 | |
| 위험 요소 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 요소 | 고독성, 폭발성, 반응성 |
| GHS 라벨링: | |
   | |
| 위험. | |
| H200, H319, H335, H370 | |
| P201, , , , , , , , , , , , , , , ,, | |
| NFPA 704(파이어 다이아몬드) | |
| 관련 화합물 | |
기타 캐티온 | 아지드화나트륨 |
| 암모니아 히드라진 | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
수소 아지드 또는 [2]아조이미드로 알려진 히드라조산은 화학식이3 [3]HN인 화합물이다.실온과 압력에서 무색, 휘발성, 폭발성 액체입니다.이것은 질소와 수소의 화합물이며 따라서 피닉토겐 하이드라이드입니다.그것은 1890년 테오도르 커티우스에 [4]의해 처음 분리되었다.그 산은 용도가 적지만, 그것의 켤레 염기인 아지드 이온은 특수 공정에서 유용하다.
히드라조산은 다른 미네랄산과 마찬가지로 물에 녹는다.원액 히드라조산은 생성 δHfo(l, 298K) = +264 kJmol의−1 [6]표준 엔탈피로 위험한 폭발성을[5] 가진다.희석 시 기체 및 수용액(<10%)을 안전하게 조제할 수 있지만 즉시 사용해야 하며, 비등점이 낮기 때문에 히드라조산은 증발 및 응축 시 농축되어 폭발이 불가능한 희석용액이 용기 또는 원자로의 헤드스페이스에 [7]폭발이 가능한 물방울이 형성될 수 있다.[8]
생산.
그 산은 보통 아지드화 나트륨과 같은 아지드화 소금의 산성화에 의해 형성된다.일반적으로 물 속의 아지드화나트륨 용액은 아지드화염과 평형상태에서 미량의 하이드라조산을 포함하고 있지만, 보다 강한 산을 도입하면 용액에서 1차종을 하이드라조산으로 전환할 수 있다.순수산은 불쾌한 [2]냄새를 가진 극도로 폭발성이 높은 무색 액체로서 나중에 부분 증류를 통해 얻어질 수 있다.
- NaN3 + HCl → HN3 + NaCl
불용성 [9]황산바륨을 여과하여 아지드바륨용액을 희황산으로 처리하여 제조할 수도 있다.
원래는 수성 히드라진이 아질산과 반응하여 제조되었습니다.
- NH24 + HNO2 → HN3 + 22 HO
히드라지늄 양이온 [NH25]+의 경우 이 반응은 다음과 같이 기술됩니다.
- [+NH25] + HNO2 → HN3 + HO2 + [HO3]+
과산화수소, 염화니트로실, 트리클로로민 또는 질산과 같은 다른 산화제들도 히드라진으로부터 [10]히드라조산을 제조하기 위해 사용될 수 있다.
폐기 전 파괴
히드라조산은 아질산과 반응합니다.
- HN3 + HNO2 → NO2 + N2 + HO2
이 반응은 네 가지 다른 산화 상태의 [11]질소를 가진 화합물을 포함한다는 점에서 특이하다.
반응
히드라조산은 수용성이 낮은 납, 은 및 수은(I) 염을 형성하기 때문에 그 특성에서 할로겐산과 유사한 점이 있습니다.금속염은 모두 무수 형태로 결정화되어 가열 시 분해되어 순수한 [2]금속의 잔여물이 남습니다.약산(pKa = 4.75)이다.[6]그것의 중금속 소금은 폭발성이 있고 요오드화 알킬과 쉽게 상호작용합니다.무거운 알칼리 금속(리튬 제외) 또는 알칼리 토류 금속의 아지화물은 폭발성이 없지만 가열 시 보다 제어된 방식으로 분해되어 분광학적으로 순수한2 [12]N가스를 방출한다.히드라조산의 용액은 많은 금속(예: 아연, 철)을 수소의 방출과 아지드화물(이전에는 아조이미드 또는 히드라조이트라고도 함)이라고 불리는 염의 형성과 함께 용해시킨다.
히드라조산은 알데히드, 케톤 및 카르본산을 포함한 카르보닐 유도체와 반응하여 아민 또는 아미드를 생성하며 질소를 배출할 수 있다.이를 슈미트 반응 또는 슈미트 재배열이라고 합니다.
가장 강한 산에 용해되면 [HN2=N=N]+ 이온을 포함하는 폭발성 염류가 생성됩니다.[12] 예를 들어 다음과 같습니다.
- HN=N=N+H[SbCl6]→[HN2=N=N][+SbCl6]−
이온 [HN2=N=N]+은 디아조메탄 HC2=N+=N과− 등전자이다.
충격, 마찰, 스파크 등에 의해 유발되는 히드라조산의 분해는 질소와 수소를 생성한다.
- 23 HN → H2 + 32 N
히드라조산은 충분한 에너지에서 단분자 분해를 거친다.
- HN3 → NH + N2
가장 낮은 에너지 경로는 삼중항 상태로 NH를 생성하며, 스핀 금지 반응을 만든다.이것은 레이저 광분해 [13]연구를 통해 지상 전자 상태에서 특정한 양의 진동 에너지에 대해 속도가 결정된 몇 안 되는 반응 중 하나이다.또한 이러한 단분자 비율이 이론적으로 분석되었으며 실험 및 계산된 비율이 합리적인 [14]일치합니다.
독성
히드라조산은 휘발성이 강하고 독성이 강하다.그것은 톡 쏘는 냄새를 가지고 있고 수증기는 심한 두통을 일으킬 수 있다.이 화합물은 축적되지 않는 독으로 작용한다.
적용들
2-플루니트릴은 벤젠 용액에 과염소산마그네슘이 35 [15][16]°C에서 존재하는 상태에서 히드라조산3(HN)과 과염소산(HClO4) 혼합물로 플루푸르를 처리하여 양호한 수율로 제조되었다.
전체 기상 요오드 레이저(AGIL)는 히드라조산 가스와 염소를 혼합하여 들뜬 염화 질소를 생성합니다. 염화 질소는 요오드를 라제로 만드는 데 사용됩니다. 이렇게 하면 COIL 레이저의 액체 화학적 요구 사항을 피할 수 있습니다.
레퍼런스
- ^ 파트나이크 신부님무기 화학물질 매뉴얼.맥그로힐, 2002년 ISBN0-07-049439-8
- ^ a b c Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica. Vol. 3 (11th ed.). Cambridge University Press. pp. 82–83. 여기에는 동시대의 생산 프로세스에 대한 자세한 설명도 포함되어 있습니다.
- ^ Dictionary of Inorganic and Organometallic Compounds. Chapman & Hall.
- ^ Curtius, Theodor (1890). "Ueber Stickstoffwasserstoffsäure (Azoimid) N3H" [On hydrazoic acid (azoimide) N3H]. Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 3023–3033. doi:10.1002/cber.189002302232.
- ^ Furman, David; Dubnikova, Faina; van Duin, Adri C. T.; Zeiri, Yehuda; Kosloff, Ronnie (2016-03-10). "Reactive Force Field for Liquid Hydrazoic Acid with Applications to Detonation Chemistry". The Journal of Physical Chemistry C. 120 (9): 4744–4752. Bibcode:2016APS..MARH20013F. doi:10.1021/acs.jpcc.5b10812. ISSN 1932-7447.
- ^ a b Catherine E. Housecroft; Alan G. Sharpe (2008). "Chapter 15: The group 15 elements". Inorganic Chemistry, 3rd Edition. Pearson. p. 449. ISBN 978-0-13-175553-6.
- ^ 곤잘레스 보브스, F. et al Org프로세스 Res. Dev. 2012, 16, 2051-2057.
- ^ 트레이틀러, D.S. 등 조직프로세스 Res. Dev. 2017, 21, 460-467.
- ^ L. F. Audrieth, C. F. Gibbs 수소 아지드 수용액' 무기 합성 1939, vol. 1, 페이지 71-79.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 432. ISBN 978-0-08-037941-8.
- ^ 그린우드, 페이지 461-464.
- ^ a b Egon Wiberg; Nils Wiberg; Arnold Frederick Holleman (2001). "The Nitrogen Group". Inorganic chemistry. Academic Press. p. 625. ISBN 978-0-12-352651-9.
- ^ Foy, B.R.; Casassa, M.P.; Stephenson, J.C.; King, D.S. (1990). "Overtone-excited HN
3 (X1A') - Anharmonic resonance, homogeneous linewidths, and dissociation rates". Journal of Chemical Physics. 92: 2782–2789. doi:10.1063/1.457924. - ^ Besora, M.; Harvey, J.N. (2008). "Understanding the rate of spin-forbidden thermolysis of HN
3 and CH
3N
3". Journal of Chemical Physics. 129 (4): 044303. doi:10.1063/1.2953697. PMID 18681642. - ^ P. A. Pavlov; Kul'nevich, V. G. (1986). "Synthesis of 5-substituted furannitriles and their reaction with hydrazine". Khimiya Geterotsiklicheskikh Soedinenii. 2: 181–186.
- ^ B. Bandgar; Makone, S. (2006). "Organic reactions in water. Transformation of aldehydes to nitriles using NBS under mild conditions". Synthetic Communications. 36 (10): 1347–1352. doi:10.1080/00397910500522009. S2CID 98593006.
외부 링크
 Wikimedia Commons의 수소 아지드 관련 매체
Wikimedia Commons의 수소 아지드 관련 매체- OSHA: 히드라조산





