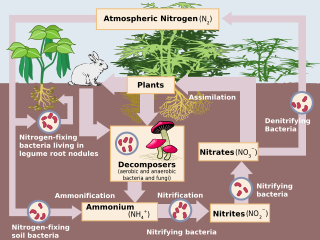
탈질
Denitrification탈질소는 질산염(NO3−)이 환원되어 일련의 중간 질소 산화물 생성물을 통해 최종적으로 분자 질소(N2)를 생성하는 미생물적으로 촉진되는 과정입니다.통성 혐기성 세균은 유기물 등의 전자공여체의 산화에 반응하여 질소산화 형태를 감소시키는 호흡의 일종으로서 탈질화를 실시한다.열역학적으로 대부분에서 최소로 유리한 순서대로 바람직한 질소 전자 수용체에는 질산염(NO3−), 아질산염(NO2−), 산화질소(NO), 산화질소(NO2)가2 포함되어 최종적으로 질소 사이클을 완료한다.탈질 미생물은 10% 미만의 매우 낮은 산소 농도와 에너지를 위한 유기 C를 필요로 합니다.탈질소는 NO를 제거하여3− 지하수로의 침수를 줄일 수 있으므로 질소 함량이 높은 하수나 동물 잔류물을 처리하는 데 전략적으로 사용될 수 있다.탈질 시 오존을 파괴하는 물질이자 지구 온난화에 상당한 영향을 미칠 수 있는 온실가스인 NO가 누출될2 수 있다.
이 과정은 주로 헤테로영양균(파라코커스 데니트리칸스 및 다양한 의사모나드 [1]등)에 의해 수행되지만, 자가영양 소실제(티오바실러스 데니트리칸스)[2]도 확인되었다.탈질제는 모든 주요 계통발생군에서 [3]나타난다.일반적으로 질산염이 N으로 완전히2 환원되는 과정에는 여러 종류의 박테리아가 관여하며, 환원 과정에서 [4]하나 이상의 효소 경로가 확인되었다.탈질 과정은 질산염 환원을 하는 유기체에 에너지를 제공할 뿐만 아니라, 일부 혐기성 섬모충류도 산소 호흡 [5]유기체에 미토콘드리아를 사용하는 것과 유사한 에너지를 얻기 위해 탈질성 엔도심비온을 사용할 수 있다.
질산염에서 [7][8]암모늄으로 직접 환원하는 과정도 nrf-gene을 가진 유기체에 대해 불임성 질산염에서 암모늄으로 환원하는 [6]과정으로 알려져 있다.이것은 질산염 감소의 수단으로서 대부분의 생태계에서 탈질소보다 덜 흔하다.탈질하는 미생물에 알려진 다른 유전자에는 [3]니르(니트라이트 환원효소)와 노스(산화질소 환원효소)가 포함된다.이러한 유전자를 가진 것으로 식별되는 유기체에는 알칼리게네스 페칼리스, 알칼리게네스 실로옥시단스, 많은 것이 프도모나스속, 브라디리조비움 자포니쿠스속 및 블라스토박터균이크리케타아제 등이 있다.[9]
개요
반반응
탈질화는 일반적으로 다음과 같은 반반응의 조합을 통해 진행되며, 효소는 괄호 안에 반응을 촉매한다.
- NO3− + 2 H+ + 2− e → NO
2− + HO2 (질산 환원효소) - NO
2− + 2 H+ + e− → NO + HO2 (니트라이트 환원효소) - 2 NO + 2 H+ + 2− e → NO
2 + HO2 (산화질소 환원효소) - NO
2 + 2 H+ + 2 e− → N
2 + HO2 (산화질소 환원효소)
전체 과정은 질산염(NO)이3− 완전히 디니트로겐(N2)으로 환원되는 순 균형 산화환원 반응으로 표현될 수 있습니다.
- 2 NO3− + 10− e + 12+ H → N2 + 6 HO2
탈질 조건
자연에서, 탈질소는 육상과 해양 [10]생태계에서 모두 일어날 수 있다.일반적으로 탈질소는 용해되어 자유롭게 사용 가능한 산소의 농도가 고갈되는 무독성 환경에서 발생합니다.이들 영역에서는 보다 에너지적으로 바람직한 전자수용체인 산소(O2) 대신 질산염(NO3−) 또는 아질산염(NO
2−)을 대체 말단 전자수용체로 사용할 수 있다.말단 전자수용체는 전자를 받아 반응에서 환원되는 화합물이다.무독성 환경의 예로는 토양,[11][12] 지하수, 습지, 저유소,[13] 환기가 잘 되지 않는 바다의 모서리 및 해저 퇴적물이 있습니다.
또한, 탈질소는 독성 환경에서도 발생할 수 있습니다.모래 해안 퇴적물의 [14]산소 농도 변동을 일으키는 조간대에서는 탈질제의 높은 활성이 관찰될 수 있다.예를 들어 파라코커스 데니트리칸스 균종은 산소와 무산소 양쪽 조건에서 동시에 탈질작용을 한다.산소를 노출하면 박테리아는 탈질 마지막 [15]단계를 촉매하는 효소인 아산화질소 환원효소를 이용할 수 있다.에어로빅 탈질제는 주로 프로테오박테리아문에 있는 그램 음성균이다.효소 NapAB, NirS, NirK 및 NosZ는 그람 음성 [16]박테리아에서 세포질 및 외막에 접한 넓은 공간인 주배강에 위치합니다.
탈질소는 토양 환경에서 동위원소 분획이라고 불리는 상태를 초래할 수 있다.두 개의 안정적인 질소 동위원소인 N과 N은 모두 침전물 프로파일에 있다.질소의 가벼운 동위원소 N은 탈질 중에 선호되며, 무거운 질소 동위원소 N은 잔류 물질에 남는다.이러한 선택성은 [17]N에 비해 바이오매스 내 N의 농도로 이어지며, N의 상대적 농도를 분석하여 탈질작용을 다른 공정과 구별한다.
폐수 처리에 사용
탈질법은 일반적으로 하수 및 도시 폐수에서 질소를 제거하기 위해 사용된다.또한[18] 과도한 농업용 또는 주거용 비료 [20]사용으로 인한 질산염 지하수 오염을 방지하기 위한 습지 및 강변지대에서[19] 중요한 과정이다.우드칩 바이오리액터는 2000년대부터 연구되어 왔으며 농업의 유출과[21] 심지어 [22]비료에서 질산염을 제거하는 데 효과적이다.
무산소 조건에서의 감소는 혐기성 암모늄 산화(아나목스)[23]라고 불리는 과정을 통해서도 발생할 수 있습니다.
- NH4+ + NO2− → N2 + 22 HO
일부 폐수처리공장에서는 메탄올, 에탄올, 아세테이트, 글리세린 또는 전매제품 등의 화합물을 폐수에 첨가하여 [24]탈질균을 위한 탄소 및 전자원을 제공한다.이러한 공학적 탈질 프로세스의 미생물 생태는 전자 공여자의 특성과 프로세스 작동 조건에 [25][26]의해 결정됩니다.탈질 공정은 산업용 [27]폐수 처리에도 사용된다.전기-생물화학반응기(EBR), 막생물반응기(MBR) 및 이동바닥생물반응기(MBR)를 포함한 많은 탈질 생물반응기 유형 및 설계는 산업 용도에 대해 상업적으로 이용 가능하다.
호기성 탈질제에 의해 수행되는 호기성 탈질소는 별도의 탱크의 필요성을 없애고 슬러지 수율을 낮출 수 있는 가능성을 제공할 수 있습니다.탈질 시 발생하는 알칼리성은 질화 [16]시 알칼리성 소비를 부분적으로 보상할 수 있기 때문에 덜 엄격한 알칼리성 요구사항이 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Carlson, C. A.; Ingraham, J. L. (1983). "Comparison of denitrification by Pseudomonas stutzeri, Pseudomonas aeruginosa, and Paracoccus denitrificans". Appl. Environ. Microbiol. 45 (4): 1247–1253. Bibcode:1983ApEnM..45.1247C. doi:10.1128/AEM.45.4.1247-1253.1983. PMC 242446. PMID 6407395.
- ^ Baalsrud, K.; Baalsrud, Kjellrun S. (1954). "Studies on Thiobacillus denitrificans". Archiv für Mikrobiologie. 20 (1): 34–62. doi:10.1007/BF00412265. PMID 13139524. S2CID 22428082.
- ^ a b Zumft, W G (1997). "Cell biology and molecular basis of denitrification". Microbiology and Molecular Biology Reviews. 61 (4): 533–616. doi:10.1128/mmbr.61.4.533-616.1997. PMC 232623. PMID 9409151.
- ^ Atlas, R.M., Barthas, R. 미생물 생태:기초와 응용 프로그램제3판벤자민 커밍스 출판사.ISBN 0-8053-0653-6
- ^ Graf, Jon S.; Schorn, Sina; Kitzinger, Katharina; Ahmerkamp, Soeren; Woehle, Christian; Huettel, Bruno; Schubert, Carsten J.; Kuypers, Marcel M. M.; Milucka, Jana (3 March 2021). "Anaerobic endosymbiont generates energy for ciliate host by denitrification". Nature. 591 (7850): 445–450. Bibcode:2021Natur.591..445G. doi:10.1038/s41586-021-03297-6. PMC 7969357. PMID 33658719.
- ^ An, S.; Gardner, WS (2002). "Dissimilatory nitrate reduction to ammonium (DNRA) as a nitrogen link, versus denitrification as a sink in a shallow estuary (Laguna Madre/Baffin Bay, Texas)". Marine Ecology Progress Series. 237: 41–50. Bibcode:2002MEPS..237...41A. doi:10.3354/meps237041.
- ^ Kuypers, MMM; Marchant, HK; Kartal, B (2011). "The Microbial Nitrogen-Cycling Network". Nature Reviews Microbiology. 1 (1): 1–14. doi:10.1038/nrmicro.2018.9. hdl:21.11116/0000-0003-B828-1. PMID 29398704. S2CID 3948918.
- ^ Spanning, R., Delgado, M. and Richardson, D. (2005). "The Nitrogen Cycle: Denitrification and its Relationship to N2 Fixation". Nitrogen Fixation: Origins, Applications, and Research Progress. pp. 277–342. doi:10.1007/1-4020-3544-6_13. ISBN 978-1-4020-3542-5.
It is possible to encounter DNRA when your source of carbon is a fermentable substrate, as glucose, so if you wanna avoid DNRA use a non fermentable substrate
{{cite book}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Liu, X.; Tiquia, S. M.; Holguin, G.; Wu, L.; Nold, S. C.; Devol, A. H.; Luo, K.; Palumbo, A. V.; Tiedje, J. M.; Zhou, J. (2003). "Molecular Diversity of Denitrifying Genes in Continental Margin Sediments within the Oxygen-Deficient Zone off the Pacific Coast of Mexico". Appl. Environ. Microbiol. 69 (6): 3549–3560. Bibcode:2003ApEnM..69.3549L. CiteSeerX 10.1.1.328.2951. doi:10.1128/aem.69.6.3549-3560.2003. PMC 161474. PMID 12788762.
- ^ Seitzinger, S.; Harrison, J. A.; Bohlke, J. K.; Bouwman, A. F.; Lowrance, R.; Peterson, B.; Tobias, C.; Drecht, G. V. (2006). "Denitrification Across Landscapes and Waterscapes: A Synthesis". Ecological Applications. 16 (6): 2064–2090. doi:10.1890/1051-0761(2006)016[2064:dalawa]2.0.co;2. hdl:1912/4707. PMID 17205890.
- ^ Scaglia, J.; Lensi, R.; Chalamet, A. (1985). "Relationship between photosynthesis and denitrification in planted soil". Plant and Soil. 84 (1): 37–43. doi:10.1007/BF02197865. S2CID 20602996.
- ^ Korom, Scott F. (1992). "Natural Denitrification in the Saturated Zone: A Review". Water Resources Research. 28 (6): 1657–1668. Bibcode:1992WRR....28.1657K. doi:10.1029/92WR00252.
- ^ Cornish Shartau, S. L.; Yurkiw, M.; Lin, S.; Grigoryan, A. A.; Lambo, A.; Park, H. S.; Lomans, B. P.; Van Der Biezen, E.; Jetten, M. S. M.; Voordouw, G. (2010). "Ammonium Concentrations in Produced Waters from a Mesothermic Oil Field Subjected to Nitrate Injection Decrease through Formation of Denitrifying Biomass and Anammox Activity". Applied and Environmental Microbiology. 76 (15): 4977–4987. Bibcode:2010ApEnM..76.4977C. doi:10.1128/AEM.00596-10. PMC 2916462. PMID 20562276.
- ^ Merchant; et al. (2017). "Denitrifying community in coastal sediments performs aerobic and anaerobic respiration simultaneously". The ISME Journal. 11 (8): 1799–1812. doi:10.1038/ismej.2017.51. PMC 5520038. PMID 28463234.
- ^ Qu; et al. (2016). "Transcriptional and metabolic regulation of denitrification in Paracoccus denitrificans allows low but significant activity of nitrous oxide reductase under oxic conditions". Environmental Microbiology. 18 (9): 2951–63. doi:10.1111/1462-2920.13128. PMID 26568281.
- ^ a b Ji, Bin; Yang, Kai; Zhu, Lei; Jiang, Yu; Wang, Hongyu; Zhou, Jun; Zhang, Huining (2015). "Aerobic denitrification: A review of important advances of the last 30 years". Biotechnology and Bioprocess Engineering. 20 (4): 643–651. doi:10.1007/s12257-015-0009-0. S2CID 85744076.
- ^ Dähnke K.; Thamdrup B. (2013). "Nitrogen isotope dynamics and fractionation during sedimentary denitrification in Boknis Eck, Baltic Sea". Biogeosciences. 10 (5): 3079–3088. Bibcode:2013BGeo...10.3079D. doi:10.5194/bg-10-3079-2013 – via Copernicus Publications.
- ^ Bachand, P. A. M.; Horne, A. J. (1999). "Denitrification in constructed free-water surface wetlands: II. Effects of vegetation and temperature". Ecological Engineering. 14 (1–2): 17–32. doi:10.1016/s0925-8574(99)00017-8.
- ^ Martin, T. L.; Kaushik, N. K.; Trevors, J. T.; Whiteley, H. R. (1999). "Review: Denitrification in temperate climate riparian zones". Water, Air, and Soil Pollution. 111: 171–186. Bibcode:1999WASP..111..171M. doi:10.1023/a:1005015400607. S2CID 96384737.
- ^ Mulvaney, R. L.; Khan, S. A.; Mulvaney, C. S. (1997). "Nitrogen fertilizers promote denitrification". Biology and Fertility of Soils. 24 (2): 211–220. doi:10.1007/s003740050233. S2CID 18518.
- ^ Ghane, E; Fausey, NR; Brown, LC (Jan 2015). "Modeling nitrate removal in a denitrification bed". Water Res. 71C: 294–305. doi:10.1016/j.watres.2014.10.039. PMID 25638338. (설명 필요)
- ^ Carney KN, Rodgers M; Lawlor, PG; Zhan, X (2013). "Treatment of separated piggery anaerobic digestate liquid using woodchip biofilters". Environ Technology. 34 (5–8): 663–70. doi:10.1080/09593330.2012.710408. PMID 23837316. S2CID 10397713. (설명 필요)
- ^ Dalsgaard, T.; Thamdrup, B.; Canfield, D. E. (2005). "Anaerobic ammonium oxidation (anammox) in the marine environment". Research in Microbiology. 156 (4): 457–464. doi:10.1016/j.resmic.2005.01.011. PMID 15862442.
- ^ Chen, K.-C.; Lin, Y.-F. (1993). "The relationship between denitrifying bacteria and methanogenic bacteria in a mixed culture system of acclimated sludges". Water Research. 27 (12): 1749–1759. doi:10.1016/0043-1354(93)90113-v.
- ^ Baytshtok, Vladimir; Lu, Huijie; Park, Hongkeun; Kim, Sungpyo; Yu, Ran; Chandran, Kartik (2009-04-15). "Impact of varying electron donors on the molecular microbial ecology and biokinetics of methylotrophic denitrifying bacteria". Biotechnology and Bioengineering. 102 (6): 1527–1536. doi:10.1002/bit.22213. PMID 19097144. S2CID 6445650.
- ^ Lu, Huijie; Chandran, Kartik; Stensel, David (November 2014). "Microbial ecology of denitrification in biological wastewater treatment". Water Research. 64: 237–254. doi:10.1016/j.watres.2014.06.042. PMID 25078442.
- ^ Constantin, H.; Fick, M. (1997). "Influence of C-sources on the denitrification rate of a high-nitrate concentrated industrial wastewater". Water Research. 31 (3): 583–589. doi:10.1016/s0043-1354(96)00268-0.