균질성
Homochirality호모치랄리티는 키랄리티 또는 손놀림의 균일성입니다.개체는 미러 이미지에 겹칠 수 없는 경우 키랄이 됩니다.예를 들어 인간의 왼손과 오른손은 서로 거울에 비친 이미지이지만 자신의 거울에 비친 이미지가 아니기 때문에 키랄입니다.생물학에서, 20개의 천연 아미노산 중 19개가 L-키랄인 반면, 설탕은 [1]D-키랄이다.균질성은 또한 모든 구성 요소가 동일한 에난티오머(원자 또는 분자의 오른손 또는 왼손 버전)인 특발성 물질을 언급할 수 있지만, 일부 원천은 이 용어의 사용을 막는다.
동질성에 목적이 있는지는 불분명하지만 정보 [2]저장의 한 형태로 보입니다.하나의 제안은 큰 조직화된 [3]분자의 형성에 있어서 엔트로피 장벽을 감소시킨다는 것입니다.아미노산이 라세미(항우체적으로 혼합된)[3] 아미노산보다 아미노산의 특발성 샘플에서 더 많은 양의 큰 골재를 형성한다는 것이 실험적으로 입증되었다.
동질성이 생전에 나타났는지 후에 나타났는지는 분명하지 않으며, 그 기원에 대한 많은 메커니즘이 [4]제안되어 왔다.이러한 모델들 중 일부는 세 가지 뚜렷한 단계를 제안합니다: 거울-대칭성 파괴는 미세한 반양성자 불균형을 만들고, 키랄성 증폭은 이 불균형을 기반으로 하며, 키랄성 전달은 분자 집합에서 다른 분자 집합으로 키랄성을 전달하는 것입니다.
생물학에서
아미노산은 펩타이드와 효소의 구성 요소인 반면, 당-펩타이드 사슬은 RNA와 DNA의 [5][6]중추이다.생물학적 유기체에서 아미노산은 거의 전적으로 왼손잡이 형태(L-아미노산)로 나타나고 설탕은 오른손잡이 형태(R-당류)[7][verification needed]로 나타난다.효소는 반응을 촉매하기 때문에 호르몬, 독소, 향기, 음식 [8]: 493–494 맛을 포함한 다양한 다른 화학 물질에 균질성을 부여합니다.글리신은 아키랄(예: 디메틸글리신) 또는 D 에난티오머 형태의 다른 비단백질 아미노산들과 마찬가지로 아키랄이다.
생물학적 유기체는 서로 다른 키랄성을 가진 분자를 쉽게 구별한다.이것은 냄새와 미각과 같은 생리적인 반응에 영향을 미칠 수 있다.에센셜 오일에서 발견되는 테르페노이드인 카르본은 L자 형태에서는 민트 냄새가 나고 [8]: 494 [verification needed]R자 형태에서는 캐러웨이 냄새가 난다.리모넨은 오른손잡이는 유자 맛이고 왼손잡이는 [9]: 168 송골송골 맛이에요.
균질성은 또한 약물에 대한 반응에도 영향을 미친다.탈리도마이드는 왼손잡이의 형태로 입덧을 치료하고 오른손잡이의 형태로 선천성 [9]: 168 기형을 일으킨다.불행히도 순수한 왼손잡이 버전을 투여하더라도 환자에서 [10]일부 버전은 오른손잡이 형식으로 변환할 수 있습니다.많은 약물이 라세미 혼합물(두 키랄리티의 동일한 양)과 특효약(한 키랄리티만 해당)으로 이용 가능하다.제조 공정에 따라서는 에난티오퍼러 형태가 입체 화학 [9]: 168 혼합물보다 생산 비용이 더 많이 들 수 있습니다.
키랄 기본 설정은 거시적 수준에서도 찾을 수 있습니다.달팽이 껍데기는 우회전 또는 좌회전 나선이 될 수 있지만, 어떤 형태든 특정 종에서 강하게 선호됩니다.식용 달팽이 포마티아는 2만 마리 중 1마리만 왼쪽 [11]: 61–62 나선형이다.식물의 감는 동작은 선호하는 키랄리티를 가질 수 있으며 소의 씹는 동작도 한 [12]방향으로 10% 초과합니다.
오리진스
대칭 파괴
생명 분자의 균질성의 기원에 대한 이론은 제안된 메커니즘에 따라 결정론적 또는 우연에 근거해 분류될 수 있다.만약 원인과 결과 사이에 관계가 있다면, 즉, 거울 대칭을 깨는 특정한 키랄장이나 영향이 있다면, 그 이론은 결정론적으로 분류된다. 그렇지 않으면 그것은 우연의 메커니즘에 기초한 이론으로 분류된다.[13]
생물 동질성의 기원의 다른 이론에 대한 다른 분류는 생명이 에난티오디스트리메이션 단계(생물학 이론) 이전에 나타났는지 또는 그 이후에 나타났는지에 따라 만들어질 수 있다.생물 이론은 동질성이 단순히 생명의 자연적 자기 증폭 과정의 결과라고 주장합니다 - 한 가지 키라리티를 선호하거나 다른 키라리티를 선호하는 생명의 형성은 우연히 우리가 관찰하는 키라리티와 함께 발생하거나, 생명의 모든 키라리티가 빠르게 발생하지만 재앙적인 사건과 s로 인해 발생했다고 합니다.trong 경쟁, 관찰되지 않은 다른 키랄 선호는 우세성과 '승리' [citation needed]키랄성 선택에서 대사성, 에난티오머적 농축에 의해 사라졌습니다.만약 그렇다면, 멸종된 키랄리티 사인의 잔해가 발견되어야 한다.이것이 사실이 아니기 때문에, 오늘날 생물 이론은 더 이상 뒷받침되지 않는다.
자연 자기 증폭 과정으로서의 키랄리티 컨센서스의 출현은 열역학 [14]제2법칙과도 관련이 있다.
결정론
결정론적 이론은 두 개의 하위 그룹으로 나눌 수 있다: 만약 초기 키랄 영향이 특정 공간 또는 시간 위치에서 발생한다면, 그 이론은 국지적 결정론적 것으로 분류된다; 키랄 선택이 일어난 시간에 키랄의 영향이 영구적이라면, 그것은보편적 결정론자로 분류됩니다.국부 결정론 이론과 우연 메커니즘에 기초한 이론의 분류 그룹은 중복될 수 있다.외부 키랄 영향이 결정론적 방법으로 초기 키랄 불균형을 발생시키더라도 외부 키랄 영향은 다른 곳에 엔antiomer 대응물이 있기 때문에 결과 신호는 랜덤할 수 있다.
결정론적 이론에서, 에난티오머 불균형은 외부 키랄장 또는 영향에 의해 생성되며, 생체 분자에 각인된 최종 신호는 그것 때문일 것이다.라세미 시동 소재로non-racemic 혼합물 생산을 위한 결정론적 메커니즘:전약 상호 작용이나 비대칭 환경(우주 rays[15]을 통해)그것들과 같은 원형으로 편광 빛, 석영 결정, 또는 지구의 회전, β-Radiolysis거나magnetochiral e.로 인한 같은 비대칭, 물리 법칙, 등이 포함된다.ffect.[16][17] 가장 일반적으로 받아들여지는 보편적 결정론은 전기 약 상호작용이다.설정되면 키랄리티가 [18]선택됩니다.
한 가지 가설은 머치슨 운석의 분자에 있어서의 에난티오머 불균형의 발견이 균질성의 외계의 기원을 지지한다는 것입니다: 에난티오머의 형성을 촉발할 수 있는 정렬된 성간 먼지 입자에 산란에서 유래한 원편광의 존재에 대한 증거가 있습니다.공간의 [11]: 123–124 키랄 물질 내에서 xaccess를 수행합니다.성간 자기장과 근성 자기장은 [19]이러한 방식으로 먼지 입자를 정렬할 수 있습니다.또 다른 추측(베스터-울브리히트 가설)은 베타 붕괴(패리티 위반 참조)와 같은 물리적 과정의 기본적인 키러리티가 생물학적으로 관련된 분자의 반감기를 약간 다르게 이끈다는 것을 시사한다.
우연론
우연 이론은 "절대 비대칭 합성, 즉 키랄 화학 시약이나 촉매의 개입 없이 아키랄 전구체로부터 에난티오머적으로 농축된 생성물의 형성은 통계적 근거만으로 사실상 불가피하다"[20]는 가정에 기초한다.
이항 분포에 의해 설명되는 거시적 특성으로 라세미 상태를 고려하십시오. 동전 던지기 실험은 두 개의 가능한 결과가 두 개의 에반티오머인 경우 좋은 비유입니다.각 베르누이 시행의 결과가 p (- ) \ = (1 - p )\ q (1 - p )\ display q (1 )\ display 로 발생하는 N{ N n개의 성공확률 다음 사용자로부터 제공됨:
(n , ) ( ) p ( - ) - \ p { } ( , N ) ={ N} { n } { } ( 1 - p )^{ N -n } 。
키랄리티의 N와 의N N2분자 N의 P 는 다음과 같습니다.
1(N /, N ) ( /) ( ) / 2 N ( \ P _ { / 2 n N ) ={ N} { / } \ ( \ { N } { N } } { N } } n 2 n 2 。
동전 던지기 실험과 마찬가지로, 이 경우 두 사건( L D이 하다고 가정합니다. p 1/ p=q 두 에난티오머의 양이 정확히 같은 총 몰수 제곱근에 반비례합니다. NN 라세미 화합물 1몰, 6. N 10에 대해 이 확률은 P/, 10가 레이스믹 상태를 찾을 확률은 매우 작기 때문에 무시할 수 있습니다.
이 시나리오에서는 효율적인 증폭 메커니즘을 통해 초기 확률적 역성 유전체 초과를 증폭할 필요가 있다.이 증폭 단계에서 가장 가능성이 높은 경로는 비대칭 자동 촉매에 의한 것입니다.자기촉매화학반응이란 반응 생성물 자체가 반응물인 것을 말한다. 즉, 반응 생성물 자체가 반응 촉매일 경우 화학반응이 자기촉매이다.비대칭 자기촉매에서 촉매는 키랄 분자이며, 이는 키랄 분자가 자체 생산을 촉매한다는 것을 의미합니다.편광에 의해 생성될 수 있는 초기 에난티오머 과잉은 보다 풍부한 에난티오머가 다른 에난티오머를 능가할 수 있도록 한다.
증폭
이론.
1953년 찰스 프랭크는 균질성이 [21][22]자기촉매의 결과라는 것을 증명하는 모델을 제안했다.그의 모델에서 키랄 분자의 L 및 D 에난티오머는 아키랄 분자 A로부터 자기 촉매적으로 생성된다.
그가 상호 반목이라고 부르는 반응을 통해 서로를 억압하는 동안
이 모델에서 라세미 상태는 아주 작은 에난티오머 과잉이 완전한 호모바이러스 상태로 증폭된다는 점에서 불안정합니다.이는 질량 작용의 법칙에서 반응 속도를 계산함으로써 알 수 있다.
는 자기촉매 반응 속도 상수, d는 상호 길항 반응 속도 상수, A 농도는 단순성을 위해 일정하게 유지한다.
의 해석용액은 [ /[ [ L / [ ] k ([ ]- [ ]) ( k t- ) ( [L] / [ / [ D ]、 { D ^ { } ) 입니다[ 0- []0 ){ ( [ 이 양수(및 그 반대)인 경우 / [{0} {0}의 비율은 지수보다 큰 속도로 증가합니다.모든 시작 조건은
] [ ] { { ] { }、[ [ ] 0 、 [ D ] = ( [D ] =) 。따라서 [ {_ { 및[ { [ {등 [L { [ 및[ {}은 불안정한 평형상태를 나타내며, 이는 상호 길항성을 나타내는 용어의 존재 여부에 따라 달라진다.
과잉를과 같이 정의함으로써
우리는 에난티오머 L과 D의 농도 변화율로부터 체인룰을 이용하여 에난티오머 과잉의 변화율을 계산할 수 있다.
이 방정식의 선형 안정성 분석 결과, 레이스믹 { ee이(가) 불안정합니다.집중 공간의 거의 모든 곳에서 시작하여 시스템은 균질 바이러스 상태로 발전합니다.
일반적으로 자기촉매만으로는 균질성을 얻을 수 없으며, 라세믹 혼합물의 불안정성을 위해 두 에난티오머 간의 상호 길항 관계가 존재해야 한다.그러나 최근의 연구에 따르면 호모치랄리티는 상호 길항 관계가 없는 상태에서 자가 촉매 작용으로 달성될 수 있지만 대칭 파괴의 기본 메커니즘은 다르다.[4][23]
실험
반응 시작 시 소량의 에난티오머 1개가 생성물로서 대량의 에난티오머 1개를 발생시키는 것을 증명하는 여러 실험들이 있다.예를 들어, Soai 반응은 자기 촉매입니다.[24][25]이미 존재하는 제품 에난티오머 중 하나에서 반응이 시작되면 제품은 동일한 에난티오머를 [26]더 많이 생산하기 위한 에난티오머 촉매로서 작용한다.0.2에 상당하는 1개의 에난티오머의 초기 존재는 제품의 최대 93%의 에난티오머 초과로 이어질 수 있습니다.
또 다른 연구는[27] 니트로소벤젠에 의한 프로피온알데히드의 프롤린 촉매 아미노산화에 관한 것이다.본 시스템에서는 촉매의 적은 에난티오머 과잉이 생성물의 큰 에난티오머 과잉으로 이어진다.
세린 옥타머[28][29] 클러스터도 경쟁 상대입니다.이러한 8개의 세린 분자의 클러스터는 특이한 호모치랄 선호로 질량 분석에서 나타나지만, 이러한 클러스터가 비이온화 조건 하에서 존재한다는 증거는 없으며 아미노산 위상 거동은 생체공학적으로 훨씬 [30]더 관련이 있다.류신의 10% Enantioenriched 샘플의 부분 승화가 승화에서 최대 82%의 농축으로 이어진다는 최근의 관찰은 아미노산의 Enantioenrich가 [31]우주에서 발생할 수 있음을 보여준다.부분 승화 과정은 온도 변화가 큰 유성의 표면에서 발생할 수 있다.이 발견은 2013년에 발사될 예정인 화성 유기물 검출기 개발에 영향을 미칠 수 있다. 화성 표면에서 정확히 미량의 아미노산을 승화 기술로 회수하는 것을 목표로 한다.
당류의 에난티오머 과잉의 높은 비대칭 증폭은 아미노산 촉매에 의한 탄수화물의[32] 비대칭 형성에도 존재한다.
한 고전적인 연구는 [33]실험실에서 일어나는 실험을 포함한다.물로부터 염소산나트륨이 결정화되도록 하고 편광계로 채취한 결정을 조사하면, 각 결정은 키랄로 판명되어 L형 또는 D형이다.일반적인 실험에서 수집된 L 결정의 양은 D 결정의 양과 같습니다(통계적 효과를 위해 보정됨).그러나 결정화 과정에서 염소산나트륨 용액을 교반하면 결정체는 배타적으로 L 또는 배타적으로 D가 된다.32개의 연속적인 결정화 실험에서 14개의 실험은 D-결정과 18개의 다른 L-결정들을 전달합니다.이 대칭 파괴에 대한 설명은 명확하지 않지만 핵 형성 과정에서 일어나는 자기 촉매 작용과 관련이 있다.
관련 실험에서 라세미 아미노산 유도체의 결정 현탁액은 에난티오머 쌍이 (동적인 운동 분해능과 비교하여)[34] 용액에서 평형을 이룰 수 있기 때문에 에난티오머 중 하나의 결정상을 100% 발생시킨다.
전송
일단 시스템에서 상당한 양의 유전체 농축이 생성되면, 전체 시스템을 통한 키랄리티 전이가 관례입니다.이 마지막 단계를 키랄 전송 단계라고 합니다.비대칭 합성에서의 많은 전략은 키랄 전달에 기초한다.특히 중요한 것은 예를 들어 만니히 반응에서 프롤린에 의한 유기 반응의 이른바 유기 촉매 반응이다.
키랄 비대칭의 전달을 위해 제안된 모델로는 중합,[35][36][37][38][39][40][43][44] 에피머화 또는 공중합이 있습니다.
라세미 아미노산의 광학 분해능
L-아미노산 간의 상관관계를 설명하는 이론은 존재하지 않는다.예를 들어 메틸기가 작은 알라닌과 벤질기가 큰 페닐알라닌을 예로 들면, 간단한 질문은 어떤 면에서 L-알라닌이 D-페닐알라닌보다 L-페닐알라닌과 더 닮고, 모든 L-아미노산이 선택되는 메커니즘이 무엇인가 하는 것이다.알라닌이 L이고 페닐알라닌이 D일 가능성이 있기 때문이다.
그것은 2004년 GDP는 자발적으로 재결정 동안 두 이성질체의 결정을 형성하고 과도한 라세미 D,L-asparagine(Asn), 아르기닌(아르지닌), 아스파라긴산(스파라 진산),glutamine(Gln), 히스티 딘(그의),leucine(레우), 메티오닌(메트로폴리탄 오페라), 페닐알라닌(페닐알라닌), ser과 같은 공존한다는 것 라세미 아미노산의 비대칭 결의안 유도 reported[45]다.ine(Ser), 발린(Val), 티로신(Tyr) 및 트립토판(Trp).이들 아미노산의 에난티오머 과잉 ee = 100 ×(L-D)/(L+D)는 유도제(Asn)의 과잉 ee = 100 ×(L-D)/(L+D)와 거의 선형적으로 상관되었다.12 D, L-아미노산(Ala, Asp, Arg, Glu, Gln, His, Leu, Met, Ser, Val, Pe, Tyr)과 초과 D, L-Asn의 혼합물을 재결정화 했을 때 우선적으로 Asn과 동일한 구성의 모든 아미노산이 [45]공결정화되었다.L- 또는 D-Asn 중 어느 쪽에서 농축이 이루어졌는지는 부수적이었으나, 일단 선택이 이루어지면 결정 형성의 열역학적 안정성 때문에 α-탄소에서 동일한 구성의 공존 아미노산이 우선적으로 관여하였다.최대 ee는 100%로 보고되었다.이러한 결과에 기초하여 광학활성분자의 도움 없이 단일 아미노산의 비대칭 합성이 발생하지 않더라도 라세미 아미노산의 혼합이 자발적이고 효과적인 광학분해능을 발생시키는 것이 제안된다.
라세미 아미노산으로부터 키랄리티의 형성을 실험적인 증거와 함께 합리적으로 설명한 최초의 연구입니다.
용어의 역사
이 용어는 켈빈이 1884년 그의 볼티모어 강의를 출판한 1904년에 도입되었습니다.켈빈은 두 분자 사이의 관계로서 호모치랄리티라는 용어를 사용했다. 즉, 두 분자가 같은 [32][46]키랄성을 가진다면 호모치랄리티이다.그러나 최근에는 호모치랄이 에난티오머릭 퓨어와 같은 의미로 사용되고 있다.이는 일부 저널(권장되지 [47]: 342 [48]않음)에서 허용되며, 그 의미는 저널의 이성질체 쌍에서 단일 광학 이성질체에 대한 프로세스 또는 시스템의 선호로 바뀐다.
「 」를 참조해 주세요.
- 키랄 라이프 개념 - 키랄 미러 버전의 생명체를 인공적으로 합성하는 것
- CIP 시스템
- 입체화학
- 파이퍼 효과
- 화학의 미해결 문제
레퍼런스
- ^ Nelson, Lehninger; et al. (2008). Lehninger Principles of Biochemistry. Macmillan. p. 474.
- ^ Carroll, James D. (March 2009). "A new definition of life". Chirality. 21 (3): 354–358. doi:10.1002/chir.20590. PMID 18571800.
- ^ a b Julian, Ryan R.; Myung, Sunnie; Clemmer, David E. (January 2005). "Do Homochiral Aggregates Have an Entropic Advantage?". The Journal of Physical Chemistry B. 109 (1): 440–444. doi:10.1021/jp046478x. PMID 16851034. S2CID 10599051.
- ^ a b Jafarpour, Farshid; Biancalani, Tommaso; Goldenfeld, Nigel (2017). "Noise-induced symmetry breaking far from equilibrium and the emergence of biological homochirality". Physical Review E. 95 (3): 032407. Bibcode:2017PhRvE..95c2407J. doi:10.1103/PhysRevE.95.032407. PMID 28415353.
- ^ Reusch, William. "Peptides & Proteins". Natural Products. Michigan State University. Retrieved 8 May 2018.
- ^ Lam, Eric (1997). "Nucleic acids and proteins". In Dey, P.M.; Harborne, J.B. (eds.). Plant Biochemistry. Burlington: Elsevier. p. 315. ISBN 9780080525723.
- ^ Zubay, Geoffrey (2000). Origins of Life: On Earth and in the Cosmos. Elsevier. p. 96. ISBN 9780080497617.
- ^ a b Seckbach, Joseph, ed. (2012). Genesis - in the beginning : precursors of life, chemical models and early biological evolution. Dordrecht: Springer. ISBN 9789400729407.
- ^ a b c Hazen, Robert M. (2007). Genesis : the scientific quest for life's origins. Washington, D.C.: Joseph Henry. ISBN 9780309103107.
- ^ Smith, Silas (July 2009). "Chiral Toxicology: It's the Same Thing... Only Different". Toxicological Sciences. 110 (1): 4–30. doi:10.1093/toxsci/kfp097. PMID 19414517.
- ^ a b Meierhenrich, Uwe (2008). Amino acids and the asymmetry of life caught in the act of formation. Berlin: Springer. ISBN 9783540768869.
- ^ Shaw, Andrew M. (2007). Astrochemistry From Astronomy to Astrobiology. Chichester: John Wiley & Sons. p. 247. ISBN 9780470091388.
- ^ 구이자로, A, 유스, M.생명의 분자 속 키랄리티의 기원(RSC Publishing, Cambridge, 2009), 제1호.
- ^ Jaakkola, S., Sharma, V. and Annila, A. (2008). "Cause of chirality consensus". Curr. Chem. Biol. 2 (2): 53–58. arXiv:0906.0254. doi:10.2174/187231308784220536. S2CID 8294807.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Globus, Noemie; Blandford, Roger D. (20 May 2020). "The Chiral Puzzle of Life". The Astrophysical Journal Letters. 895 (1): L11. arXiv:2002.12138. Bibcode:2020ApJ...895L..11G. doi:10.3847/2041-8213/ab8dc6. S2CID 211532577. Retrieved 3 July 2020.
- ^ Barron, L. D. (1986-09-01). "True and false chirality and absolute asymmetric synthesis". Journal of the American Chemical Society. 108 (18): 5539–5542. doi:10.1021/ja00278a029. ISSN 0002-7863.
- ^ Barron, L. D. (1981-08-20). "Optical activity and time reversal". Molecular Physics. 43 (6): 1395–1406. Bibcode:1981MolPh..43.1395B. doi:10.1080/00268978100102151. ISSN 0026-8976.
- ^ Clark, Stuart (July–August 1999). "Polarized Starlight and the Handedness of Life". American Scientist. 87 (4): 336. Bibcode:1999AmSci..87..336C. doi:10.1511/1999.4.336. ISSN 0003-0996.
- ^ Helman, Daniel S (6 July 2018). "Galactic Distribution of Chirality Sources of Organic Molecules". Acta Astronautica. 151: 595–602. arXiv:1612.06720. Bibcode:2018AcAau.151..595H. doi:10.1016/j.actaastro.2018.07.008. ISSN 0094-5765. S2CID 10024470.
- ^ Mislow, Kurt (2003). "Absolute Asymmetric Synthesis: A Commentary". Collection of Czechoslovak Chemical Communications. 68 (5): 849–864. doi:10.1135/cccc20030849. ISSN 1212-6950.
- ^ Frank, F.C. (1953). "On spontaneous asymmetric synthesis". Biochimica et Biophysica Acta. 11 (4): 459–463. doi:10.1016/0006-3002(53)90082-1. PMID 13105666.
- ^ Frank는 원본 논문에서 화학 반응 세트를 제안하지 않고 동적 방정식을 제안했으며, 여기서 두 가지 에난티오머의 농도는 각각 [n1]과 [n2]로 표시되었습니다.
- ^ Jafarpour, Farshid; Biancalani, Tommaso; Goldenfeld, Nigel (2015). "Noise-induced mechanism for biological homochirality of early life self-replicators". Physical Review Letters. 115 (15): 158101. arXiv:1507.00044. Bibcode:2015PhRvL.115o8101J. doi:10.1103/PhysRevLett.115.158101. PMID 26550754. S2CID 9775791.
- ^ Shibata, Takanori; Morioka, Hiroshi; Hayase, Tadakatsu; et al. (17 January 1996). "Highly Enantioselective Catalytic Asymmetric Automultiplication of Chiral Pyrimidyl Alcohol". Journal of the American Chemical Society. 118 (2): 471–472. doi:10.1021/ja953066g. ISSN 0002-7863.
- ^ Soai, Kenso; Sato, Itaru; Shibata, Takanori (2001). "Asymmetric autocatalysis and the origin of chiral homogeneity in organic compounds". The Chemical Record. 1 (4): 321–332. doi:10.1002/tcr.1017. ISSN 1528-0691. PMID 11893072.
- ^ Takanori Shibata; Hiroshi Morioka; Tadakatsu Hayase; Kaori Choji; Kenso Soai (1996). "Highly Enantioselective Catalytic Asymmetric Automultiplication of Chiral Pyrimidyl Alcohol". J. Am. Chem. Soc. 118 (2): 471–472. doi:10.1021/ja953066g.
- ^ Suju P. Mathew, Hiroshi Iwamura and Donna G. Blackmond (21 June 2004). "Amplification of Enantiomeric Excess in a Proline-Mediated Reaction". Angewandte Chemie International Edition. 43 (25): 3317–3321. doi:10.1002/anie.200453997. PMID 15213963.
- ^ Cooks, R. G., Zhang, D., Koch, K. J. (2001). "Chiroselective Self-Directed Octamerization of Serine: Implications for Homochirogenesis". Anal. Chem. 73 (15): 3646–3655. doi:10.1021/ac010284l. PMID 11510829. S2CID 27891319.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Nanita, S., Cooks, R. G. (2006). "Serine Octamers: Cluster Formation, Reactions, and Implications for Biomolecule Homochirality". Angew. Chem. Int. Ed. 45 (4): 554–569. doi:10.1002/anie.200501328. PMID 16404754.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Donna G. Blackmond; Martin Klussmann (2007). "Spoilt for choice: assessing phase behaviour models for the evolution of homochirality". Chem. Commun. (39): 3990–3996. doi:10.1039/b709314b. PMID 17912393.
- ^ Stephen P. Fletcher; Richard B. C. Jagt; Ben L. Feringa (2007). "An astrophysically relevant mechanism for amino acid enantiomer enrichment". Chem. Commun. 2007 (25): 2578–2580. doi:10.1039/b702882b. PMID 17579743.
- ^ a b Armando Córdova; Magnus Engqvist; Ismail Ibrahem; Jesús Casas; Henrik Sundén (2005). "Plausible origins of homochirality in the amino acid catalyzed neogenesis of carbohydrates". Chem. Commun. 15 (15): 2047–2049. doi:10.1039/b500589b. PMID 15834501.
- ^ Kondepudi, D. K., Kaufman, R. J. & Singh, N. (1990). "Chiral Symmetry Breaking in Sodium Chlorate Crystallization". Science. 250 (4983): 975–976. Bibcode:1990Sci...250..975K. doi:10.1126/science.250.4983.975. PMID 17746924. S2CID 41866132.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Noorduin, Wim L.; Izumi, Toshiko; Millemaggi, Alessia; Leeman, Michel; Meekes, Hugo; Van Enckevort, Willem J. P.; Kellogg, Richard M.; Kaptein, Bernard; Vlieg, Elias; Blackmond, Donna G. (January 2008). "Emergence of a Single Solid Chiral State from a Nearly Racemic Amino Acid Derivative" (PDF). Journal of the American Chemical Society. 130 (4): 1158–1159. doi:10.1021/ja7106349. PMID 18173274.
- ^ Sandars, P. G. H. (2003). "A toy model for the generation of homochirality during polymerization". Origins of Life and Evolution of the Biosphere. 33 (6): 575–587. Bibcode:2003OLEB...33..575S. doi:10.1023/a:1025705401769. ISSN 0169-6149. PMID 14601927. S2CID 25241450.
- ^ Brandenburg, Axel; Multamäki, Tuomas (July 2004). "How long can left and right handed life forms coexist?". International Journal of Astrobiology. 3 (3): 209–219. arXiv:q-bio/0407008. Bibcode:2004IJAsB...3..209B. doi:10.1017/s1473550404001983. ISSN 1473-5504. S2CID 16991953.
- ^ Brandenburg, A.; Andersen, A. C.; Höfner, S.; Nilsson, M. (June 2005). "Homochiral Growth Through Enantiomeric Cross-Inhibition". Origins of Life and Evolution of Biospheres. 35 (3): 225–241. arXiv:q-bio/0401036. Bibcode:2005OLEB...35..225B. doi:10.1007/s11084-005-0656-9. ISSN 0169-6149. PMID 16228640. S2CID 16833396.
- ^ Wattis, Jonathan A. D.; Coveney, Peter V. (June 2005). "Symmetry-breaking in Chiral Polymerisation". Origins of Life and Evolution of Biospheres. 35 (3): 243–273. arXiv:physics/0402091. Bibcode:2005OLEB...35..243W. doi:10.1007/s11084-005-0658-7. ISSN 0169-6149. PMID 16228641. S2CID 12451904.
- ^ Saito, Yukio; Hyuga, Hiroyuki (2005-05-15). "Chirality Selection in Open Flow Systems and in Polymerization". Journal of the Physical Society of Japan. 74 (5): 1629–1635. arXiv:physics/0503057. Bibcode:2005JPSJ...74.1629S. doi:10.1143/jpsj.74.1629. ISSN 0031-9015. S2CID 18419335.
- ^ Blanco, Celia; Hochberg, David (2011). "Chiral polymerization: symmetry breaking and entropy production in closed systems". Phys. Chem. Chem. Phys. 13 (3): 839–849. arXiv:1104.2225. Bibcode:2011PCCP...13..839B. doi:10.1039/c0cp00992j. ISSN 1463-9076. PMID 21057681. S2CID 516456.
- ^ Plasson, R.; Bersini, H.; Commeyras, A. (2004-11-17). "Recycling Frank: Spontaneous emergence of homochirality in noncatalytic systems". Proceedings of the National Academy of Sciences. 101 (48): 16733–16738. Bibcode:2004PNAS..10116733P. doi:10.1073/pnas.0405293101. ISSN 0027-8424. PMC 534711. PMID 15548617.
- ^ Stich, Michael; Blanco, Celia; Hochberg, David (2013). "Chiral and chemical oscillations in a simple dimerization model". Phys. Chem. Chem. Phys. 15 (1): 255–261. arXiv:1210.1872. Bibcode:2013PCCP...15..255S. doi:10.1039/c2cp42620j. ISSN 1463-9076. PMID 23064600. S2CID 2655068.
- ^ Wattis, Jonathan A. D.; Coveney, Peter V. (August 2007). "Sequence Selection during Copolymerization". The Journal of Physical Chemistry B. 111 (32): 9546–9562. doi:10.1021/jp071767h. ISSN 1520-6106. PMID 17658787.
- ^ Blanco, Celia; Hochberg, David (2012). "Homochiral oligopeptides by chiral amplification: interpretation of experimental data with a copolymerization model". Physical Chemistry Chemical Physics. 14 (7): 2301–11. arXiv:1202.2268. Bibcode:2012PCCP...14.2301B. doi:10.1039/c2cp22813k. ISSN 1463-9076. PMID 22237639. S2CID 16960638.
- ^ a b S. Kojo; H. Uchino; M. Yoshimura; K. Tanaka (2004). "Racemic D,L-asparagine causes enantiomeric excess of other coexisting racemic D,L-amino acids during recrystallization: a hypothesis accounting for the origin of L-amino acids in the biosphere". Chem. Comm. (19): 2146–2147. doi:10.1039/b409941a. PMID 15467844.
- ^ Morris, David G. (2001). Stereochemistry. Cambridge: Royal Society of Chemistry. p. 30. ISBN 978-1-84755-194-8.
- ^ Anslyn, Eric V.; Dougherty, Dennis A. (2006). Modern physical organic chemistry. Sausalito, Calif.: University Science Books. ISBN 9781891389313.
- ^ 다만, 메세지는 혼란스러울 수 있습니다.모스에서, G.P.(11996년 1월)."입체 화학의 기본 용어(가장 추천 1996년)"(PDF).순수·응용 화학. 68(12):2193–2222. doi:10.1351/pac199668122193.S2CID 98272391.5월 7일 2018년. Retrieved, Enantiomerically Pure/Enantiopure를 위한 진입;그러나 Homochiral를 위한 진입"enantiomerically pure/enantiopure을 참조하십시오." 말한다"homochiral의 동의어로 사용 강력하게 낙심하고 있" 말한다.
추가 정보
- Bailey, Jeremy (28 August 1998). "Stellar Circular Polarization and Biomolecular Homochirality". ScienceWeek. Archived from the original on 30 November 2010. Retrieved 5 May 2018.
- Ball, Philip (24 April 2009). "A circular argument?". Nature. doi:10.1038/news.2009.390.
- Brazil, Rachel (26 October 2015). "The origin of homochirality". Chemistry World. Retrieved 10 August 2018.
- Blackmond, Donna G.; Miller, Rom (21 June 2004). "How left-handed amino acids got ahead: a demonstration of the evolution of biological homochirality in the lab". www.imperial.ac.uk (Press release). Imperial College London. Retrieved 5 May 2018.
- Guijarro, Albert; Yus, Miguel (2008). The origin of chirality in the molecules of life : a revision from awareness to the current theories and perspectives of this unsolved problem. Cambridge, UK: Royal Society of Chemistry. ISBN 9780854041565.
- Hegstrom, Roger A.; Kondepudi, Dilip K. (1990). "The Handedness of the Universe". Scientific American. 262 (1): 108–115. Bibcode:1990SciAm.262a.108H. doi:10.1038/scientificamerican0190-108. JSTOR 24996649.
- Jafarpour, Farshid; Biancalani, Tommaso; Goldenfeld, Nigel (10 March 2017). "Noise-induced symmetry breaking far from equilibrium and the emergence of biological homochirality" (PDF). Physical Review E. 95 (3): 032407. Bibcode:2017PhRvE..95c2407J. doi:10.1103/PhysRevE.95.032407. PMID 28415353.
- Nansheng, Zhao (1999). "The role of homochirality in evolution". In Zucchi, C.; Caglioti, L.; Pályi, G. (eds.). Advances in BioChirality. Burlington: Elsevier. pp. 105–114. doi:10.1016/B978-008043404-9/50008-5. ISBN 9780080526621.
- Rouhi, A. Maureen (17 June 2004). "On the Genesis of Homochirality". Chemical & Engineering News. American Chemical Society. Retrieved 5 May 2018.
- Sedbrook, Danielle (28 July 2016). "Must the Molecules of Life Always be Left-Handed or Right-Handed?". Smithsonian. Retrieved 10 August 2018.
외부 링크
- 관찰은 균질성 이론을 뒷받침한다.Photonics Technology World 1998년 11월
- 균질성의 기원.노르디타 스톡홀름에서의 회의, 2008년 2월.








 대해 이 확률은 P
대해 이 확률은 P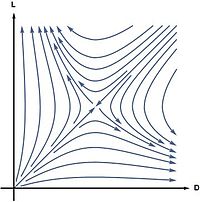


![{\displaystyle {\begin{aligned}{\frac {d[{\ce {L}}]}{dt}}&=k_{a}[{\ce {A}}][{\ce {L}}]-k_{d}{\ce {[L][D]}}\\{\frac {d[{\ce {D}}]}{dt}}&=k_{a}[{\ce {A}}][{\ce {D}}]-k_{d}{\ce {[L][D]}},\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2a8ae3fd5c4a5872bb86ef9127bd98381f5f9e12)
 자기촉매 반응 속도 상수,
자기촉매 반응 속도 상수,  상호 길항 반응 속도 상수, A 농도는 단순성을 위해 일정하게 유지한다.
상호 길항 반응 속도 상수, A 농도는 단순성을 위해 일정하게 유지한다. ![{\displaystyle ([L]_{0}-[D]_{0})}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eceec5368fc7f05776d490c8869673a326de49c7) 양수(및 그 반대)인 경우
양수(및 그 반대)인 경우 ![{\displaystyle [L]/[D]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/439fcfce6c97c70ea345dfd7b0a0cee0ffa0d5e5) 비율은 지수보다 큰 속도로 증가합니다.모든 시작 조건은
비율은 지수보다 큰 속도로 증가합니다.모든 시작 조건은![{\displaystyle [L]_{0}=[D]_{0}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/262f2ce1c587c2819c25d4f1a53c93a2ed8d08d0)
![{\displaystyle [L]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9432e9d1e600524a670e05b340c3bfe310cf12b8)
![{\displaystyle [D]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b1137d39625389c56402174e74b6a8de3da18864)
![{\displaystyle [L]_{0}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/db821cb086b0448d2c4d4db2bc348d6a1e7ec81b)
![{\displaystyle [D]_{0}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9bb94024805d4f35f68e5b277483c654c315d934)
![[L]](https://wikimedia.org/api/rest_v1/media/math/render/svg/c1eba88cad4b17de726ed2c779b29eecdf5819a2)
![[D]](https://wikimedia.org/api/rest_v1/media/math/render/svg/1c4bcb25d77a0de74082c849178200b8cf1340b4)
 같이 정의함으로써
같이 정의함으로써![{\displaystyle ee={\frac {[{\ce {D}}]-[{\ce {L}}]}{[{\ce {D}}]+[{\ce {L}}]}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d7dee4e2fd16d609fd4442e804a26cf421c6ab27)
![{\displaystyle {\frac {d(ee)}{dt}}=\left({\frac {2k_{d}{\ce {[L][D]}}}{[{\ce {D}}]+[{\ce {L}}]}}\right)ee.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3471e4bec966fec2b85a90def8c59c45db0076fb)
 (가) 불안정합니다.집중 공간의 거의
(가) 불안정합니다.집중 공간의 거의 




