히단토인
Hydantoin| | |||
| 이름 | |||
|---|---|---|---|
| 선호 IUPAC 이름 이미다졸리딘-2,4-디오네 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 켐벨 | |||
| 켐스파이더 | |||
| ECHA InfoCard | 100.006.650 | ||
| 케그 | |||
펍켐 CID | |||
| 유니 | |||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| C3H4N2O2 | |||
| 어금질량 | 100.077 g·migration−1 | ||
| 녹는점 | 220 °C(428 °F, 493 K) | ||
| 39.7 g/L (100 °C) | |||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
히단토인 또는 글리콜리루라는 CHC2(O)NHC(O)라는 공식을 가진 헤테로사이클릭 유기 화합물이다.NH. 글리콜산과 요소 반응에서 발생하는 무색 고체다.그것은 이미다졸리딘의 산화된 파생물이다.보다 일반적인 의미에서 하이드란토인은 모체와 같은 고리 구조를 가진 집단과 화합물의 종류를 지칭할 수 있다.예를 들어 페니토인(아래 참조)은 하이드란토인 분자의 5번 탄소로 대체된 2개의 페닐 그룹을 가지고 있다.[1]
합성
히단토인은 1861년 요산에 대한 연구 과정에서 아돌프 폰 배이어에 의해 처음으로 고립되었다.그는 알란토인의 수소화에 의해 그것을 얻었고, 그래서 이름이 붙여졌다.
프리드리히 우레흐는 1873년 알라닌 황산염과 시안산칼륨으로부터 5-메틸히단토인을 합성했는데, 현재 우레치 하단토인 합성이라고 알려져 있다.[2]이 방법은 알킬과 아릴시아네이트를 이용한 현대적인 경로와 매우 유사하다.5,5-디메틸 화합물은 아세톤 시아노 무수신(우레흐: 시아노 무수신 반응 참조)과 탄산암모늄에서도 얻을 수 있다.[3]이 반응 타입은 부셰러-베르크스 반응이라고 한다.[4][5]
히단토인은 알란토인을 하이드로다이오드산으로 가열하거나 "알코올성 암모니아로 브로마세틸 요소"를 가열하여 합성할 수도 있다.[6]하이드란토인의 순환구조는 도로시 한 1913년에 의해 확인되었다.[7]
실용적으로 중요한 것은 탄산암모늄을 함유한 시아노 무수인의 응결로 하이드란토를 얻는 것이다.우레흐의 작업을 따르는 또 다른 유용한 경로는 시안산염과 이소시아네이트로 아미노산이 응결되는 것을 포함한다.
사용 및 발생
제약
하이드란토인 그룹은 몇몇 의학적으로 중요한 화합물에서 찾을 수 있다.의약품에서, 하이드란토인 유도체는 항경련제의 종류를 형성한다;[8] 페니토인과 포스페니토인은 모두 하이드란토인 모이에티를 포함하고 있고 둘 다 발작장애의 치료에서 항경련제로 사용된다.하이드란토인 유도체 단트롤렌은 악성고열증, 신경성 악성증후군, 가소성, 엑스터시 도취 등을 치료하는 근육 이완제로 쓰인다.로피토인은 부정맥 하이드란틴의 예다.
살충제
하이드란토인 유도체 이미프로트린은 피레로이드 살충제다.Iprodione은 하이드란토인 그룹이 함유된 인기 있는 살균제다.[9]
3-(3,5-디클로로페닐)-히단토인은 S-7250의 비밀 특수 코드를 가지고 있다.
아미노산 합성
하이드란토의 가수 분해는 아미노산을 제공한다.
- RCHC(O)NHC(O)NH + HO2 → RCHC(NH2)COH2 + NH3
히단토인 자체는 뜨겁고 묽은 염산과 반응하여 글리신을 준다.메티오닌은 메티온에서 얻은 하이드란토를 통해 산업적으로 생산된다.[9]
메틸화
하이드란토의 메틸레이션은 다양한 파생상품을 산출한다.디메틸하이드란토인(DMH)은 하이드란토인의 디메틸파생물을 지칭할 수 있지만, 특히 5,5-디메틸하이드란토인을 지칭한다.[11]
할로겐화
일부 N-할로겐화 된 하이드란토인의 파생상품은 소독제/소독제 또는 바이오시드 제품에서 염소화 또는 브롬화제로 사용된다.N-할로겐화 3대 파생상품은 디클로로디메틸하이드란토인(DCDMH), 브로모클로로디메틸하이드란토인(BCDMH), 디브로모디메틸하이드란토인(DBDMH)이다.혼합 에틸-메틸 아날로그, 1,3-디클로로-5-에틸-메틸리미다졸리딘-2,4-디오네(브로모클로로에틸메틸하이드란토인)도 위와 혼합하여 사용한다.

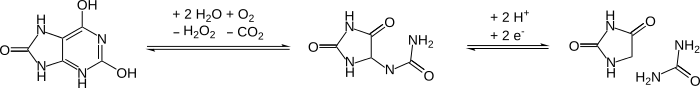
세포사후 하이드란토인으로의 DNA 산화
DNA에 들어있는 시토신과 티민 염기의 높은 비율은 유기체가 죽은 후 시간이 지남에 따라 하이드란토로 산화된다.그러한 수정은 DNA 중합체를 차단하여 PCR이 작동하지 못하게 한다.이런 손상은 고대 DNA 샘플을 다룰 때 문제가 된다.[12]
참조
- ^ Ware, Elinor (1950). "The Chemistry of the Hydantoins". Chem. Rev. 46 (3): 403–470. doi:10.1021/cr60145a001. PMID 24537833.
- ^ Urech, Friedrich (1873). "Ueber Lacturaminsäure und Lactylharnstoff". Liebigs Ann. (in German). 165 (1): 99–103. doi:10.1002/jlac.18731650110.
- ^ Wagner, E. C.; Baizer, Manuel (1940). "5,5-Dimethylhydantoin". Organic Syntheses. 20: 42. doi:10.15227/orgsyn.020.0042.; Collective Volume, vol. 3, p. 323
- ^ Bucherer, H. T.; Steiner, W. (1934). "J. Prakt. Chem." (in German). 140: 291.
{{cite journal}}:Cite 저널은 필요로 한다.journal=(도움말) - ^ 버그, 게르. 팻. 566,094 (1929) [C. A, 27, 1001 (1933년)]
- ^ Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica. Vol. 14 (11th ed.). Cambridge University Press. pp. 29–30.
- ^ Oakes, Elizabeth H. (2007). Encyclopedia of World Scientists. Facts on File. p. 298. ISBN 9780816061587.
- ^ "Hydantoin anticonvulsants". drugs.com.
- ^ a b Drauz, Karlheinz; Grayson, Ian; Kleemann, Axel; Krimmer, Hans-Peter; Leuchtenberger, Wolfgang; Weckbecker, Christoph (2007). "Amino Acids". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a02_057.pub2. ISBN 978-3527306732.
- ^ "5,5-Dimethylhydantoin (DMH) a Highly Effective, Halogen Stabilizer for Wet End Applications, PaperCo".
- ^ "5,5-Dimethylhydantoin".
- ^ Hofreiter, Michael; Serre, David; Poinar, Hendrik N.; Kuch, Melanie; Pääbo, Svante (2001). "Ancient DNA". Nature Reviews Genetics. 2 (5): 353–359. doi:10.1038/35072071. PMID 11331901. S2CID 205016024.
외부 링크
| 무료 사전인 위키트리노리에서 디메틸하이드란토를 찾아보자. |
- 아자르 DB: 하이드란토인
- 히단토인 인 더 케미IDplus 데이터베이스
- [1] 1926년 독일어 번역본 하인리히 빌츠와 칼 슬롯타의 하이드란토인 작성에 관한 독일어 리뷰 기사