비가바트린
Vigabatrin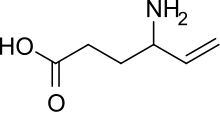 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | 사브릴, 비가드론 |
| 기타 이름 | γ-비닐-GABa |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a610016 |
| 임신 , 카테고리 |
|
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 80–90% |
| 단백질 결합 | 0% |
| 신진대사 | 대사되지 않은 |
| 제거 반감기 | 성인은 5~8시간, 노인은 12~13시간. |
| 배설 | 레날 |
| 식별자 | |
| |
| CAS 번호 |
|
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.165.122 |
| 화학 및 물리적 데이터 | |
| 공식 | C6H11NO2 |
| 어금질량 | 129.1987 g·190−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 171 ~ 177 °C(340 ~ 351 °F) |
| |
| |
| (iii) | |
브랜드명 Sabril인 Vigabatrin은 간질 치료에 사용되는 약물이다. 그것은 2019년에 일반 의약품으로 사용 가능하게 되었다.[1]
γ아미노부틸산(GABA)의 분해를 억제하여 작용한다. γ-비닐-GABA로도 알려져 있으며, GABA의 구조적 아날로그지만 GABA 수용체와 결합하지는 않는다.[2]
의학적 용법
뇌전증
캐나다에서 비가바트린은 치료 내성 간질, 복합적인 부분 발작, 2차 일반화된 발작, 웨스트 신드롬의 유아용 경련에서의 일요법 사용에 (다른 약과 함께) 보조 치료제로 사용되도록 승인된다.[2]
2003년 현재 멕시코에서 비가바트린은 재래식 요법(부제요법 또는 일요법)에 의해 만족스럽게 통제되지 않는 간질 치료나 최근 다른 요원을 시도하지 않은 진단된 환자(일요법)에서 승인되고 있다.[3]
비가바트린은 또한 2차 일반화된 토닉-클론 발작, 부분 발작, 그리고 서부 증후군으로 인한 유아용 경련에서 단일요법을 사용하는 데에도 사용된다.[3]
2009년 8월 21일, 룬드벡은 미국 식품의약국이 비가바트린에 대해 두 번의 신약 응용 승인을 허가했다고 발표했다. 이 약은 잠재적 편익이 시력 손실의 잠재적 위험보다 큰 소아성 경련을 가진 생후 1개월에서 2세까지의 소아환자에 대한 단일요법, 그리고 여러 가지 대체 트레아에 불충분하게 반응한 내화성 복합 부분 발작(CPS)을 가진 성인환자에 대한 보조(애드온)요법으로 표시된다.잠재적 편익이 시력 손실의 위험보다 더 큰 것으로 나타났다.[4]
1994년 푸흐트와 브란트너인탈러는 비가바트린이 발프로이트 나트륨으로 결과가 좋지 않은 레녹스-가스토 증후군을 가진 어린이의 85%에서 발작을 50-100% 감소시켰다고 보고했다.[5]
다른이들
Vigabatrin은 건강한 자원 봉사자들에게서 코티솔과 ACTH 수치 상승 외에도 공황 장애로 인한 첼시스토키닌 증상들을 감소시켰다.[6]
비가바트린은 선천적으로 지적장애, 저혈압, 발작, 언어장애, 아탁시아 등을 유발하는 GABA 신진대사 결함인 숙신성 세미알데히드 탈수소효소 결핍증(SSADHD)에서도 발작을 치료하는 데에도 쓰인다. 비가바트린은 GABA 트랜스미나제 억제를 통해 GHB 수치를 낮추는 데 도움을 준다. 그러나, 이것은 뇌에만 있다; 그것은 말초 GABA transaminase에 영향을 주지 않는다. 그래서 GHB는 계속해서 쌓이고 결국 뇌에 도달한다.[7]
역효과
중추신경계
Sleepiness (12.5%), headache (3.8%), dizziness (3.8%), nervousness (2.7%), depression (2.5%), memory disturbances (2.3%), diplopia (2.2%), aggression (2.0%), ataxia (1.9%), vertigo (1.9%), hyperactivity (1.8%), vision loss (1.6%) (See below), confusion (1.4%), insomnia (1.3%), impaired concentration (1.2%), personality issues (1.1%).[2] 전체 아동 299명 중 33명(11%)이 과잉행동하게 됐다.[2]
비가바트린 치료 과정에서 정신병이 생기는 환자도 있는데,[8] 이는 어린이보다 어른에게 더 흔하다.[9] 이것은 정신병력이 없는 환자들에게도 일어날 수 있다.[10] 그 밖에 드물게 나타나는 CNS 부작용으로는 불안감, 정서적 무감각, 자극성, 떨림, 비정상적인 걸음걸이, 언어장애 등이 있다.[2]
위장
복통(1.6%), 변비(1.4%), 구토(1.4%), 메스꺼움(1.4%) 등이 뒤를 이었다. 난독증과 식욕 증가는 임상시험 대상자의 1% 미만에서 발생했다.[2]
몸 전체로
피로(9.2%), 체중 증가(5.0%), 아스테니아(1.1%)[2] 등이었다.
테라토젠시티
토끼를 대상으로 한 기형학 연구에서는 하루 150mg/kg의 복용량이 새끼 2%에서 구개열을 일으키고 하루 200mg/kg의 복용량이 9%[2]에 이르는 것으로 나타났다. 2001년 3월에 발표된 연구에 따르면 이는 메티오닌 수치가 감소했기 때문일 수 있다.[11] 2005년, 연구는 대학 카타니아에서 행해진 물 미로와 개방 경작 작업의 가난한 공연을 펼쳤습니다,750-mg 그룹에서 쥐 체중 미달로 태어날 때는 쥐들 엄마가 주고 통제 집단까지 잡지 못 했고 1000mg그룹에서 쥐 임신. 살아남지 못해250–1000 mg/kg/day 소비됬다며 출판되었다.[12]
현재까지 인간에게는 통제된 기형학 데이터가 없다.
감각
2003년에 25명의 환자를 대상으로 한 소급 연구에서 프리젠과 말그그렌에 의해 비가바트린이 망막신경섬유층의 되돌릴 수 없는 확산 위축을 유발하는 것으로 나타났다.[13] 이것은 망막의 외측 영역(황반, 또는 중심 영역과는 반대로)에 가장 큰 영향을 미친다.[14] 영국에서 톰 에케와 다른 사람들에 의해 시각적 필드 결함은 일찍이 1997년에 보고되었다. 코마티쉬 등을 포함한 일부 저자들은 시각장 손실과 전기생리학적 변화가 Vigabatrin 사용자의 최대 50%에서 입증될 수 있다고 믿는다.
비가바트린의 망막 독성은 타우린 고갈에 기인할 수 있다.[15]
안전성 문제로 인해, Vigabatrin REMS 프로그램은 FDA가 이 약물을 시작하기 전에 정보에 입각한 결정을 보장하고 적절한 사용을 보장하도록 요구된다.[16]
상호작용
2002년에 발표된 한 연구는 비가바트린이 카바마제핀의 혈장 간극의 통계적으로 유의한 증가를 유발한다는 것을 발견했다.[17]
1984년, 웨일즈 대학의 DRS 림머와 리첸스는 페니토인을 투여한 비가바트린을 투여하면 치료 저항성 간질 환자가 혈청 페니토인 농도를 낮춘다고 보고했다.[18] 5년 후, 같은 두 과학자들은 5주 이내에 23%의 페니토인 농도가 감소했다고 보고했는데, 이는 이러한 상호작용의 메커니즘을 해명하려는 시도가 실패했음을 설명하는 논문이었다.[19]
약리학
비가바트린은 GABA의 카타볼리즘을 담당하는 효소인 감마-아미노부티릭산아미노트란스페라제(GABA-AT)의 되돌릴 수 없는 메커니즘 기반 억제제다. GABA-AT의 억제는 뇌의 GABA 수준을 증가시킨다.[2][20] Vigabatrin은 인종 화합물로, 그 [S]-enantomer는 약리학적으로 활발하다.[21],[22]
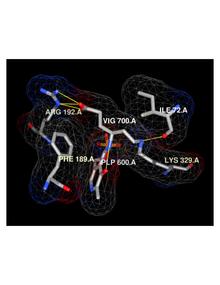
약동학
대부분의 약물에서, 반감기 제거는 투약 일정과 꾸준한 상태 농도에 도달하는데 필요한 시간의 유용한 예측 변수다. 그러나 비가바트린의 경우 생물학적 활동의 반감기가 제거 반감기보다 훨씬 긴 것으로 밝혀졌다.[24]
Vigabatrin의 경우, 연구자들이 응답자의 혈청 농도 수준과 비응답자의 혈청 농도 수준 간에 차이가 없음을 발견했기 때문에 목표 농도의 범위가 없다.[25] 대신에, 작용 지속시간은 GABA-T 재합성률의 더 많은 함수로 여겨지고 있다; GABA-T의 수준은 보통 약을 중단한 후 6일이 될 때까지 정상 상태로 돌아가지 않는다.[22]
역사
비가바트린은 1980년대에 간질 발작을 막기 위해 뇌의 GABA 농도를 높이겠다는 구체적인 목표를 가지고 개발되었다. 이를 위해 이 약은 GABA 기질을 저하시키는 GABA 트랜스미나제를 불가역적으로 억제하도록 설계됐다. 1989년 영국에서 치료 허가를 받았으나 미국 식품의약국(FDA)의 비가바트린 허가사용은 2009년 이전까지 미국에서 두 차례나 지연됐다. 1983년 동물실험에서 자궁내 부종이 발생하여 연기되었으나 인체실험에서 그 영향이 뚜렷하지 않아 약물 설계가 계속되었다. 1997년 인간의 말초적 시각장 결함과 연관돼 재판이 잠정 중단됐다.[26]
사회와 문화
브랜드 이름
비가바트린은 캐나다,[27] 멕시코,[3] 영국에서 사브릴로 팔리고 있다.[28] 덴마크의 상표명은 Sabrilex이다. Sabril은 2009년 8월 21일 미국에서 승인을 받았으며, 2009년 3월 미국 스폰서인 Charliams Pharmetic을 인수한 Lundbeck Inc.에 의해 미국에서 시판되고 있다.
일반 등가물
2019년 1월 16일, 식품의약품안전청은 미국 최초의 일반판 세이브릴(비가바트린)을 승인했다.[29]
참조
- ^ "Press Announcements - FDA approves first generic version of Sabril to help treat seizures in adults and pediatric patients with epilepsy". www.fda.gov. Retrieved 21 January 2019.
- ^ a b c d e f g h i 롱, 필립 W. "비가바트린." 2006년 4월 23일 웨이백 머신 인터넷 정신 건강. 1995-2003년.
- ^ a b c DEF 멕시코: Sabril은 2005년 9월 14일 웨이백 머신 Diccionario de Especialdades Farmaceuticas에 보관했다. 에디시온 49, 2003.
- ^ Bresnahan, Rebecca; Gianatsi, Myrsini; Maguire, Melissa J.; Tudur Smith, Catrin; Marson, Anthony G. (July 30, 2020). "Vigabatrin add-on therapy for drug-resistant focal epilepsy". The Cochrane Database of Systematic Reviews. 2020 (7): CD007302. doi:10.1002/14651858.CD007302.pub3. ISSN 1469-493X. PMC 8211760. PMID 32730657.
- ^ Feucht M, Brantner-Inthaler S (1994). "Gamma-vinyl-GABA (vigabatrin) in the therapy of Lennox-Gastaut syndrome: an open study". Epilepsia. 35 (5): 993–8. doi:10.1111/j.1528-1157.1994.tb02544.x. PMID 7925171. S2CID 24204172.
- ^ Zwanzger P, Baghai TC, Schuele C, Strohle A, Padberg F, Kathmann N, Schwarz M, Moller HJ, Rupprecht R (2001). "Vigabatrin decreases cholecystokinin-tetrapeptide (CCK-4) induced panic in healthy volunteers". Neuropsychopharmacology. 25 (5): 699–703. doi:10.1016/S0893-133X(01)00266-4. PMID 11682253.
- ^ Pearl, Phillip L; Robbins, Emily; Capp, Philip K; Gasior, Maciej; Gibson, K Michael (May 5, 2004). "Succinic Semialdehyde Dehydrogenase Deficiency". GeneReviews. Seattle, Washington: University of Washington. Retrieved September 6, 2010.
- ^ Sander JW, Hart YM (1990). "Vigabatrin and behaviour disturbance". Lancet. 335 (8680): 57. doi:10.1016/0140-6736(90)90190-G. PMID 1967367. S2CID 34456538.
- ^ Chiaretti A, Castorina M, Tortorolo L, Piastra M, Polidori G (1994). "[Acute psychosis and vigabatrin in childhood]". La Pediatria Medica e Chirurgica : Medical and Surgical Pediatrics (in Italian). 16 (5): 489–90. PMID 7885961.
- ^ Sander JW, Hart YM, Trimble MR, Shorvon SD (1991). "Vigabatrin and psychosis". Journal of Neurology, Neurosurgery, and Psychiatry. 54 (5): 435–9. doi:10.1136/jnnp.54.5.435. PMC 488544. PMID 1865207.
- ^ Abdulrazzaq YM, Padmanabhan R, Bastaki SM, Ibrahim A, Bener A (2001). "Placental transfer of vigabatrin (gamma-vinyl GABA) and its effect on concentration of amino acids in the embryo of TO mice". Teratology. 63 (3): 127–33. doi:10.1002/tera.1023. PMID 11283969.
- ^ Lombardo SA, Leanza G, Meli C, Lombardo ME, Mazzone L, Vincenti I, Cioni M (2005). "Maternal exposure to the antiepileptic drug vigabatrin affects postnatal development in the rat" (PDF). Neurological Sciences. 26 (2): 89–94. doi:10.1007/s10072-005-0441-6. hdl:2108/194069. PMID 15995825. S2CID 25257244.
- ^ Frisén L, Malmgren K (2003). "Characterization of vigabatrin-associated optic atrophy". Acta Ophthalmologica Scandinavica. 81 (5): 466–73. doi:10.1034/j.1600-0420.2003.00125.x. PMID 14510793.
- ^ Buncic JR, Westall CA, Panton CM, Munn JR, MacKeen LD, Logan WJ (2004). "Characteristic retinal atrophy with secondary "inverse" optic atrophy identifies vigabatrin toxicity in children". Ophthalmology. 111 (10): 1935–42. doi:10.1016/j.ophtha.2004.03.036. PMC 3880364. PMID 15465561.
- ^ Gaucher D; Arnault E; Husson Z; et al. (November 2012). "Taurine deficiency damages retinal neurones: cone photoreceptors and retinal ganglion cells". Amino Acids. 43 (5): 1979–1993. doi:10.1007/s00726-012-1273-3. PMC 3472058. PMID 22476345.
- ^ "SABRIL® (vigabatrin) tablets, for oral use SABRIL® (vigabatrin) powder for oral..." Sabril.net. Retrieved 2019-05-31.
- ^ Sanchez-Alcaraz, Agustín; Quintana MB; Lopez E; Rodriguez I; Llopis P (2002). "Effect of vigabatrin on the pharmacokinetics of carbamazepine". Journal of Clinical Pharmacy and Therapeutics. 27 (6): 427–30. doi:10.1046/j.1365-2710.2002.00441.x. PMID 12472982. S2CID 29986581.
- ^ Rimmer EM, Richens A (1984). "Double-blind study of gamma-vinyl GABA in patients with refractory epilepsy". Lancet. 1 (8370): 189–90. doi:10.1016/S0140-6736(84)92112-3. PMID 6141335. S2CID 54336689.
- ^ Rimmer EM, Richens A (1989). "Interaction between vigabatrin and phenytoin". British Journal of Clinical Pharmacology. 27 (Suppl 1): 27S–33S. doi:10.1111/j.1365-2125.1989.tb03458.x. PMC 1379676. PMID 2757906.
- ^ Rogawski MA, Löscher W (2004). "The neurobiology of antiepileptic drugs". Nat Rev Neurosci. 5 (7): 553–564. doi:10.1038/nrn1430. PMID 15208697. S2CID 2201038.
- ^ Sheean, G.; Schramm T; Anderson DS; Eadie MJ. (1992). "Vigabatrin--plasma enantiomer concentrations and clinical effects". Clinical and Experimental Neurology. 29: 107–16. PMID 1343855.
- ^ a b Gram L, Larsson OM, Johnsen A, Schousboe A (1989). "Experimental studies of the influence of vigabatrin on the GABA system". British Journal of Clinical Pharmacology. 27 (Suppl 1): 13S–17S. doi:10.1111/j.1365-2125.1989.tb03455.x. PMC 1379673. PMID 2757904.
- ^ Storici Paola; De Biase D; Bossa F; Bruno S; Mozzarelli A; Peneff C; Silverman R; Schirmer T. (2003). "Structures of γ-Aminobutyric Acid (GABA) Aminotransferase, a Pyridoxal 5'-Phosphate, and [2Fe-2S] Cluster-containing Enzyme, Complexed with γ-Ethynyl-GABA and with the Antiepilepsy Drug Vigabatrin". The Journal of Biological Chemistry. 279 (1): 363–73. doi:10.1074/jbc.M305884200. PMID 14534310.
- ^ Browne TR (1998). "Pharmacokinetics of antiepileptic drugs". Neurology. 51 (5 suppl 4): S2–7. doi:10.1212/wnl.51.5_suppl_4.s2. PMID 9818917. S2CID 39231047.
- ^ Lindberger M, Luhr O, Johannessen SI, Larsson S, Tomson T (2003). "Serum concentrations and effects of gabapentin and vigabatrin: observations from a dose titration study". Therapeutic Drug Monitoring. 25 (4): 457–62. doi:10.1097/00007691-200308000-00007. PMID 12883229. S2CID 35834401.
- ^ Ben-Menachem E. (2011). "Mechanism of Action of vigabatrin: correcting misperceptions". Acta Neurologica Scandinavica. 124 (192): 5–15. doi:10.1111/j.1600-0404.2011.01596.x. PMID 22061176. S2CID 25347559.
- ^ drugs.com Vigabatrin 마약 정보
- ^ 간질 치료 - 비가바트린 노퍽과 와베니 정신건강 파트너십 NHS 트러스트
- ^ "FDA approves first generic version of Sabril to help treat seizures in adults and pediatric patients with epilepsy". U.S. Food and Drug Administration (Press release). 2019-09-11.
외부 링크
- "Vigabatrin". Drug Information Portal. U.S. National Library of Medicine.


