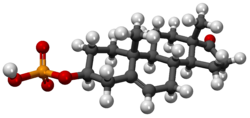
데히드로에피안드로스테론 황산염
Dehydroepiandrosterone sulfate | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 (3aS,3bR,7S,9aR,9bS,11aS)-9a,11a-디메틸-1-옥소-2,3,3a,3b,4,7,8,9a,9b,10,11a-테트라데카히드로-1H펜타[시클렌타] | |
| 기타 이름 안드로스테놀론 황산염, 프라스테론 황산염, 안드로스테-5-en-3β-ol-17-one 3β-황산염 | |
| 식별자 | |
3D 모델(JSmol) | |
| 약어 | DHEA 황산염, DHEA-S, DHEAS |
| 켐스파이더 | |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| 쵸스19285 | |
| 몰 질량 | 368.49 g/g |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
디하이드로에피안드로스테론 황산염은 DHEA 황산염 또는 DHEA-S로 약칭되며 안드로스테놀론 황산염으로도 알려져 있으며 부신 [1]피질에 의해 생성되는 내인성 안드로스테인 스테로이드이다.그것은 3β-황산에스테르이며, 데히드로에피안드로스테론(DHEA)의 대사물이며 DHEA보다 [2]훨씬 더 높은 상대 농도로 순환한다.스테로이드는 호르몬 불활성이고 대신 중요한 신경스테로이드와 신경트로핀이다.[2]
생물학적 활동
신경스테로이드 활성
다른 복합 스테로이드와 유사하게, DHEA-S는 호르몬 활성이 결여되어 스테로이드 호르몬 [3][4]수용체에 대한 친화력이 결여되어 있다.그러나 DHEA-S는 신경스테로이드 및 [2]신경트로핀으로서의 활성을 유지한다.이는 NMDA 수용체의 양성 알로스테릭 조절제(50nM–1μM), GABAA 수용체와 글리신 수용체의 음성 알로스테릭 조절제, 시그마-1 수용체의 약작용제(Kd > 50μM)[2][5]로 작용한다.또한 DHEA-S는 높은 친화력(약 5nM)[2][6][7][8]으로 TrkA와 p75NTR(신경성장인자(NGF) 및 뇌유래 신경영양인자(BDNF)와 같은 신경트로핀 수용체)에 직접 결합하고 활성화하는 것으로 밝혀졌다.
호르몬 활성
DHEA-S 자체는 호르몬 불활성이지만, DHEA로 [9]다시 전환될 수 있고, DHEA는 약한 안드로겐과 에스트로겐으로 전환될 수 있으며, 테스토스테론, 디히드로테스토스테론(DHT)과 [2][1][10]같은 보다 강력한 안드로겐으로 전환될 수 있다고 생각되어 왔다.이와 같이 DHEA-S는 안드로겐 및 에스트로겐 [2][1][10]효과의 가능성을 가진 프로호르몬이라고 생각되어 왔다.그러나 2005년 연구에 따르면 DHEA는 DHEA-S로 전환될 수 있지만 DHEA-S가 DHEA로 [11]전환된다는 증거는 발견되지 않았다.
기타 액티비티
DHEA-S는 또한 TRPV1 및 TRPC5 과도 수용체 전위 채널을 억제하고 P2X [5]수용체를 억제하는 것으로 밝혀졌다.
생화학
생합성
DHEA 및 DHEA-S는 부신피질자극호르몬(ACTH)[1]의 제어 하에 부신피질의 망상영역에서 생성된다.DHEA는 콜레스테롤 측쇄개열효소(CYP11A1, P450scc) 및 17α-히드록실화효소/17,20-리아제(CYP17A1)를 통해 콜레스테롤로부터 합성되며,[13] 중간체로는 프레그놀론 및 17α-히드록시 프레그네놀론을 포함한다.다음으로 DHEA를 C3β 위치에서 술포트랜스퍼라아제 SULT2A1을 통해 황산화하여 DHEA-S를 형성하고, 또한 그보다 적은 범위로 SULT1E1을 [13][14][15]형성한다.DHEA는 대부분 부신피질에서 유래하지만 생식선(10%)[16]에서 덜 분비되는 반면, DHEA-S는 거의 전적으로 부신피질에서 생성되고 분비되며, 95-100%는 여성의 [1][17][18]부신피질에서 유래한다.DHEA-S의 약 10~15mg은 젊은 [19]성인의 부신 피질에 의해 하루에 분비된다.
분배
알부민에 약하게 결합되어 있는 DHEA와 달리, DHEA-S는 알부민에 강하게 결합되어 있으며(즉, 매우 높은 친화력을 가지고), 이것이 비교 말기 [20][21]반감기가 훨씬 긴 이유이다.DHEA와 대조적으로 DHEA-S는 성호르몬 결합 글로불린(SHBG)[22]에 전혀 결합하지 않는다.
DHEA는 혈액-뇌 장벽을 쉽게 넘어 중추신경계로 [23]들어가는 반면, DHEA-S는 혈액-뇌 [24]장벽을 제대로 넘지 못한다.
대사
DHEA-S는 스테로이드 술파타아제(STS)[9]를 통해 DHEA로 다시 전환될 수 있다.폐경전 여성들의 경우, 순환의 테스토 스테론의 40%에서 75%DHEA-S의 말초 신진대사에서 폐경기 여성들의, 난포 호르몬의 90%, 주로 에스트론, DHEA-S.[2]의 말초 신진대사의 연구에서 estro의 임신한 증가성이 점쳐 수준 여성의 외생 DHEA-S의 행정부를 발견했다 나온 것을 도출한다.ne그리고 에스트라디올.[25]DHEA-S는 전립선암의 테스토스테론, 디히드로테스토스테론과 같은 강력한 안드로겐의 보고 역할을 하며, 이는 [26]이 암의 성장을 부채질한다.
DHEA-S의 소거 반감기는 710시간으로 소거 반감기가 1530분에 [21]불과한 DHEA보다 훨씬 길다.
소거
레벨

DHEA와 DHEA-S는 [29]체내에서 가장 많은 순환 스테로이드이다.DHEA-S의 혈장 수치는 DHEA의 100배 이상, 코티솔의 5~10배, 테스토스테론의 100~500배, 에스트라디올의 [30][3]1000~1만배다.
DHEA와 DHEA-S의 수치는 [2][1]일생 동안 다양하다.그들은 약 6~8세의 아드레날린까지 소아기 동안 낮게 유지되며, 그 시점에서 현저하게 [31]증가하며, 결국 약 20~30세에 [2][1]정점에 도달한다.생후 3년차부터 DHEA와 DHEA-S 수치는 점차 [29]감소한다.70세까지는 DHEA와 DHEA-S의 수치가 젊은 층보다 20~30% 낮고, 80세 이상에서는 DHEA와 DHEA-S의 수치가 젊은 [29]층보다 80~90% 낮아질 수 있다.
DHEA-S 수치는 [2][29]여성보다 남성에서 더 높다.
기준 범위
여성의[32] DHEA-S 기준 범위| 태닝 단계 및 평균 연령 | 하한 | 상한 | 구성 단위 | |
|---|---|---|---|---|
| 태너 1단계 | 14일 이상 | 16 | 96 | μg/dL |
| 태너 2기 | 10.5년 | 22 | 184 | |
| 태너 3기 | 11.6년 | 15 미만 | 296 | |
| 태너 4기 | 12.3년 | 17 | 343 | |
| 태너 5단계 | 14.5년 | 44 | 332 | |
| 18~29세 | 44 | 332 | ||
| 30~39세 | 31 | 228 | ||
| 40~49세 | 18 | 244 | ||
| 50~59년 | 15 미만 | 200 | ||
| > 또는 =60년 | 15 미만 | 157 | ||
| 태닝 단계 및 평균 연령 | 하한 | 상한 | 구성 단위 | |
|---|---|---|---|---|
| 태너 1단계 | 14일 이상 | 15 미만 | 120 | μg/dL |
| 태너 2기 | 11.5년 | 15 미만 | 333 | |
| 태너 3기 | 13.6년 | 15 미만 | 312 | |
| 태너 4기 | 15.1년 | 29 | 412 | |
| 태너 5단계 | 18.0년 | 89 | 457 | |
| 18~29세 | 89 | 457 | ||
| 30~39세 | 65 | 334 | ||
| 40~49세 | 48 | 244 | ||
| 50~59년 | 35 | 179 | ||
| > 또는 =60년 | 25 | 131 | ||
의료용
부족.
내분비학회는 DHEA-S의 역할이 지금까지 [33]수행된 연구에서 명확하지 않기 때문에 건강한 여성과 부신기능부전 환자 모두에게 DHEA-S의 치료적 사용을 금지할 것을 권고한다.DHEA-S 및 기타 안드로겐의 일상적 사용은 저안드로겐증, 부신기능저하, 난소수술, 글루코콜티코이드 사용 또는 낮은 안드로겐 수치와 관련된 기타 질환으로 인해 안드로겐 수치가 낮은 여성의 치료에서 권장되지 않는다. 이는 징후 및 증상 개선을 뒷받침하는 데이터가 제한적이기 때문이다.위험성에 [33]대한 장기 연구 없이 치료를 받은 점막입니다.
DHEA-S의 연령 관련 하락이 갱년기 증상 및 성욕 감소와 관련이 있을 수 있는 다른 노년 여성에서 DHEA-S 보충제는 현재 [34]결과를 개선한다고 말할 수 없다.
출산
나트륨염, 프라스테론황산나트륨, DHEA-S는 일본에서 [35][36][37][38][39][40][41]출산 시 자궁경부 숙성 및 자궁경부 확장 부전 치료제로 사용된다.
진단 용도
1890μM 또는 700~800μg/dL 이상의 DHEA-S 수치는 DHEA-S가 부신에서[42][43] 생성되고 [44]뇌에서도 합성되기 때문에 부신 기능 장애를 시사한다.따라서 DHEA-S의 존재는 과도한 안드로겐의 난소 또는 고환 기원을 배제하기 위해 사용된다.
다모증을 가진 여성들은 보통 DHEA-S [45]수치가 약간 상승한다.다낭성 난소 증후군의 일반적인 원인으로는 난소 기능 장애(다낭성 난소 증후군)와 부신 기능 장애(공부신 과형성, 쿠싱 증후군, 안드로겐 분비 종양)가 있다. 이러한 사례의 90%는 PCOS에 의해 발생하거나 선천적으로 [45]특발성이다.그러나 DHEA-S 수치(700μg/dL 이상)가 심각하게 증가하면 추가적인 작업이 필요하며 양성 또는 악성 부신 [45]변화에서 거의 기인한다.
화학
DHEA-S는 Androst-5-en-3β-ol-17-One 3β-황산염이라고도 하며, DHEA의 C3β 황산 에스테르 및 안드로스테인 스테로이드이다.
레퍼런스
- ^ a b c d e f g Risto Erkkola (2006). The Menopause. Elsevier. pp. 5–. ISBN 978-0-444-51830-9.
- ^ a b c d e f g h i j k Prough RA, Clark BJ, Klinge CM (2016). "Novel mechanisms for DHEA action". J. Mol. Endocrinol. 56 (3): R139–55. doi:10.1530/JME-16-0013. PMID 26908835.
- ^ a b Walter K.H. Krause (30 November 2008). Cutaneous Manifestations of Endocrine Diseases. Springer Science & Business Media. pp. 79–. ISBN 978-3-540-88367-8.
Plasma DHEA-S levels in adult men and women are 100-500 times higher than those of testosterone and 1000-10000 times higher than those of estradiol.
- ^ Mo Q, Lu SF, Simon NG (2006). "Dehydroepiandrosterone and its metabolites: differential effects on androgen receptor trafficking and transcriptional activity". J. Steroid Biochem. Mol. Biol. 99 (1): 50–8. doi:10.1016/j.jsbmb.2005.11.011. PMID 16524719. S2CID 30489004.
- ^ a b Steven R. King (9 November 2012). Neurosteroids and the Nervous System. Springer Science & Business Media. pp. 1, 12. ISBN 978-1-4614-5559-2.
- ^ Lazaridis I, Charalampopoulos I, Alexaki VI, Avlonitis N, Pediaditakis I, Efstathopoulos P, Calogeropoulou T, Castanas E, Gravanis A (2011). "Neurosteroid dehydroepiandrosterone interacts with nerve growth factor (NGF) receptors, preventing neuronal apoptosis". PLOS Biol. 9 (4): e1001051. doi:10.1371/journal.pbio.1001051. PMC 3082517. PMID 21541365.
- ^ Pediaditakis I, Iliopoulos I, Theologidis I, Delivanoglou N, Margioris AN, Charalampopoulos I, Gravanis A (2015). "Dehydroepiandrosterone: an ancestral ligand of neurotrophin receptors". Endocrinology. 156 (1): 16–23. doi:10.1210/en.2014-1596. PMID 25330101.
- ^ Gravanis A, Calogeropoulou T, Panoutsakopoulou V, Thermos K, Neophytou C, Charalampopoulos I (2012). "Neurosteroids and microneurotrophins signal through NGF receptors to induce prosurvival signaling in neuronal cells". Sci Signal. 5 (246): pt8. doi:10.1126/scisignal.2003387. PMID 23074265. S2CID 26914550.
- ^ a b Robert Morfin (2 September 2003). DHEA and the Brain. CRC Press. pp. 28–. ISBN 978-0-203-30121-0.
- ^ a b Marc A. Fritz; Leon Speroff (28 March 2012). Clinical Gynecologic Endocrinology and Infertility. Lippincott Williams & Wilkins. pp. 545–. ISBN 978-1-4511-4847-3.
- ^ Hammer F, Subtil S, Lux P, Maser-Gluth C, Stewart PM, Allolio B, Arlt W (2005). "No evidence for hepatic conversion of dehydroepiandrosterone (DHEA) sulfate to DHEA: in vivo and in vitro studies". J. Clin. Endocrinol. Metab. 90 (6): 3600–5. doi:10.1210/jc.2004-2386. PMID 15755854.
- ^ Häggström, Mikael; Richfield, David (2014). "Diagram of the pathways of human steroidogenesis". WikiJournal of Medicine. 1 (1). doi:10.15347/wjm/2014.005. ISSN 2002-4436.
- ^ a b Rainey WE, Nakamura Y (February 2008). "Regulation of the adrenal androgen biosynthesis". J. Steroid Biochem. Mol. Biol. 108 (3–5): 281–86. doi:10.1016/j.jsbmb.2007.09.015. PMC 2699571. PMID 17945481.
- ^ Mueller JW, Gilligan LC, Idkowiak J, Arlt W, Foster PA (2015). "The Regulation of Steroid Action by Sulfation and Desulfation". Endocr. Rev. 36 (5): 526–63. doi:10.1210/er.2015-1036. PMC 4591525. PMID 26213785.
- ^ Lawrence H Lash (2005). Drug Metabolism and Transport: Molecular Methods and Mechanisms. Springer Science & Business Media. pp. 353–. ISBN 978-1-59259-832-8.
- ^ Wolf-Bernhard Schill; Frank H. Comhaire; Timothy B. Hargreave (26 August 2006). Andrology for the Clinician. Springer Science & Business Media. pp. 243–. ISBN 978-3-540-33713-3.
- ^ Gretchen M. Lentz; Rogerio A. Lobo; David M. Gershenson; Vern L. Katz (2012). Comprehensive Gynecology. Elsevier Health Sciences. pp. 850–. ISBN 978-0-323-06986-1.
- ^ Dimitrios A. Linos; Jon A. van Heerden (5 December 2005). Adrenal Glands: Diagnostic Aspects and Surgical Therapy. Springer Science & Business Media. pp. 161–. ISBN 978-3-540-26861-1.
- ^ G.A.W. Rook; S. Lightman (6 December 2012). Steroid Hormones and the T-Cell Cytokine Profile. Springer Science & Business Media. pp. 205–. ISBN 978-1-4471-0931-0.
- ^ Kenneth L. Becker (2001). Principles and Practice of Endocrinology and Metabolism. Lippincott Williams & Wilkins. pp. 712–. ISBN 978-0-7817-1750-2.
- ^ a b Bruce Alan White; Susan P. Porterfield (2013). Endocrine and Reproductive Physiology, Mosby Physiology Monograph Series (with Student Consult Online Access),4: Endocrine and Reproductive Physiology. Elsevier Health Sciences. pp. 164–. ISBN 978-0-323-08704-9.
- ^ Paul M. Coates; M. Coates Paul; Marc Blackman; Marc R. Blackman, Gordon M. Cragg, Mark Levine, Jeffrey D. White, Joel Moss, Mark A. Levine (29 December 2004). Encyclopedia of Dietary Supplements (Print). CRC Press. pp. 170–. ISBN 978-0-8247-5504-1.
{{cite book}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Joseph E. Pizzorno (2013). Textbook of Natural Medicine. Elsevier Health Sciences. pp. 711–. ISBN 978-1-4377-2333-5.
- ^ Samuel S. C. Yen; Robert B. Jaffe; Robert L. Barbieri (January 1999). Reproductive Endocrinology: Physiology, Pathophysiology, and Clinical Management. Saunders. p. 40. ISBN 978-0-7216-6897-0.
Thus, the formation of DHEA-S occurs directly in the brain, particularly because DHEA-S does not cross the blood-brain barrier [...]
- ^ Nguyen AD, Conley AJ (2008). "Adrenal androgens in humans and nonhuman primates: production, zonation and regulation". Endocr Dev. Endocrine Development. 13: 33–54. doi:10.1159/000134765. ISBN 978-3-8055-8580-4. PMID 18493132.
- ^ Penning TM (2018). "Dehydroepiandrosterone (DHEA)-SO4 Depot and Castration-Resistant Prostate Cancer". Vitam. Horm. Vitamins and Hormones. 108: 309–331. doi:10.1016/bs.vh.2018.01.007. ISBN 9780128143612. PMC 6226251. PMID 30029732.
- ^ S.S. Nussey; S.A. Whitehead (8 April 2013). Endocrinology: An Integrated Approach. CRC Press. pp. 158–. ISBN 978-0-203-45043-7.
- ^ Mark A. Sperling (10 April 2014). Pediatric Endocrinology E-Book. Elsevier Health Sciences. pp. 485–. ISBN 978-1-4557-5973-6.
- ^ a b c d Philip E. Harris; Pierre-Marc G. Bouloux (24 March 2014). Endocrinology in Clinical Practice, Second Edition. CRC Press. pp. 521–. ISBN 978-1-84184-952-2.
- ^ Abraham Weizman (1 February 2008). Neuroactive Steroids in Brain Function, Behavior and Neuropsychiatric Disorders: Novel Strategies for Research and Treatment. Springer Science & Business Media. pp. 261–. ISBN 978-1-4020-6854-6.
- ^ Douglas T. Carrell; C. Matthew Peterson (23 March 2010). Reproductive Endocrinology and Infertility: Integrating Modern Clinical and Laboratory Practice. Springer Science & Business Media. pp. 158–. ISBN 978-1-4419-1436-1.
- ^ a b 디하이드로에피안드로스테론 황산염(DHEA-S), 2018-03-14 Mayo 의학교육연구재단 웨이백머신에 보관된 세럼.2012년 7월 취득
- ^ a b Wierman, Margaret E.; Arlt, Wiebke; Basson, Rosemary; Davis, Susan R.; Miller, Karen K.; Murad, Mohammad H.; Rosner, William; Santoro, Nanette (2014). "Androgen Therapy in Women: A Reappraisal: An Endocrine Society Clinical Practice Guideline". The Journal of Clinical Endocrinology & Metabolism. 99 (10): 3489–510. doi:10.1210/jc.2014-2260. PMID 25279570.
- ^ Elraiyah, Tarig; Sonbol, Mohamad Bassam; Wang, Zhen; Khairalseed, Tagwa; Asi, Noor; Undavalli, Chaitanya; Nabhan, Mohammad; Altayar, Osama; Prokop, Larry; Montori, Victor M.; Murad, Mohammad Hassan (2014). "The Benefits and Harms of Systemic Dehydroepiandrosterone (DHEA) in Postmenopausal Women With Normal Adrenal Function: A Systematic Review and Meta-analysis". The Journal of Clinical Endocrinology & Metabolism. 99 (10): 3536–42. doi:10.1210/jc.2014-2261. PMC 5393492. PMID 25279571.
- ^ J. Elks (14 November 2014). The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. Springer. pp. 641–. ISBN 978-1-4757-2085-3.
- ^ John W. Blunt; Murray H. G. Munro (19 September 2007). Dictionary of Marine Natural Products with CD-ROM. CRC Press. pp. 1075–. ISBN 978-0-8493-8217-8.
- ^ A. Kleemann; J. Engel; B. Kutscher; D. Reichert (14 May 2014). Pharmaceutical Substances, 5th Edition, 2009: Syntheses, Patents and Applications of the most relevant APIs. Thieme. pp. 2441–2442. ISBN 978-3-13-179525-0.
- ^ Martin Negwer; Hans-Georg Scharnow (2001). Organic-chemical drugs and their synonyms: (an international survey). Wiley-VCH. p. 1831. ISBN 978-3-527-30247-5.
3β-Hydroxyandrost-5-en-17-one hydrogen sulfate = (3β)-3-(Sulfooxy)androst-5-en-17-one. R: Sodium salt (1099-87-2). S: Astenile, Dehydroepiandrosterone sulfate sodium, DHA-S, DHEAS, KYH 3102, Mylis, PB 005, Prasterone sodium sulfate, Teloin
- ^ Jianqiu Y (1992). "Clinical Application of Prasterone Sodium Sulfate". Chinese Journal of New Drugs. 5: 015.
- ^ Sakaguchi M, Sakai T, Adachi Y, Kawashima T, Awata N (1992). "The biological fate of sodium prasterone sulfate after vaginal administration. I. Absorption and excretion in rats". J. Pharmacobio-Dyn. 15 (2): 67–73. doi:10.1248/bpb1978.15.67. PMID 1403604.
- ^ Sakai, Takanori; Sakaguchi, Minoru; Adachi, Yoshiko; Kawashima, Tsuneo; Awata, Norio (1992). "The Biological Fate of Sodium Prasterone Sulfate after Vaginal Administration II: Distribution after Single and Multiple Administration to Pregnant Rats". 薬物動態. 7 (1): 87–101. doi:10.2133/dmpk.7.87.
- ^ Somani N, Harrison S, Bergfeld WF (2008). "The clinical evaluation of hirsutism". Dermatologic Therapy. 21 (5): 376–91. doi:10.1111/j.1529-8019.2008.00219.x. PMID 18844715. S2CID 34029116.
- ^ "Polycystic Ovarian Syndrome Workup". eMedicine. 25 October 2011. Retrieved 19 November 2011.
- ^ Vaudry, H.; Do Rego, J. L.; Burel, D.; Luu-The, V.; Pelletier, G.; Vaudry, D.; Tsutsui, K. (2011). "Neurosteroid Biosynthesis in the Brain of Amphibians". Frontiers in Endocrinology. 2: 79. doi:10.3389/fendo.2011.00079. PMC 3355965. PMID 22649387.
- ^ a b c Sachdeva, Silonie (2010). "Hirsutism: Evaluation and Treatment". Indian Journal of Dermatology. 55. 1 (1): 3–7. doi:10.4103/0019-5154.60342. PMC 2856356. PMID 20418968.

