비티오놀
Bithionol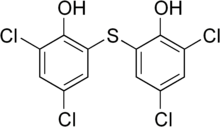 | |
 | |
| 임상자료 | |
|---|---|
| 기타 이름 | 2,4-dichloro- 6-(3,5-dichloro- 2-hydroxyphenyl)sulfanylphenol |
| ATC 코드 | |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.002.333 |
| 화학 및 물리적 데이터 | |
| 공식 | C12H6CL4O2S |
| 어금질량 | 356.04 g·1904−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 188°C(370°F) |
| |
| |
| | |
비티오놀은 항균성, 무염성, 조류독감이다.말에서[1] 아노플로체팔라 퍼포리아타(타입충)와 파시올라 간낭(간두엽)을 치료하는 데 쓰인다.
작용기전
비티오놀은 아데노신 삼인산염(ATP)을 순환 아데노신 모노인산염(cAMP)에 대한 카탈루션에 중요한 세포내 효소인 [2]용해성 아데닐리엘 사이클라아제의 강력한 억제제인 것으로 밝혀졌다.용해성 아데닐 시클라아제는 중탄산염에 의해 독특하게 활성화된다.이 효소에 의해 형성된 cAMP는 정자의 정전, 눈의 압력 조절, 산기 조절, 아스트로시테/네우론 통신과 관련이 있다.
용해성 아데닐 시클라아제의 이소머 특이 억제제인 오르가노클로로핀 헥사클로로페인과 관련이 있다.비티오놀에는 두 개의 방향족 고리가 있고 그 사이에 유황 원자가 접합되어 있으며 페닐 그룹에 여러 개의 염소 이온과 히드록실 그룹이 부착되어 있다.이 기능 그룹들은 소수성, 이온성, 극성 상호작용이 가능하다.
이러한 분자간 상호작용은 수용성 아데닐 시클라아제의 중탄산염 결합 부지에 비티오놀의 결합을 효과적으로 담당하여 일반적인 중탄산염 기질과의 경쟁적 억제를 유발한다.중탄산염 결합 부위 내 아르기닌 176의 사이드 체인은 비티오놀 분자의 방향성 링과 유의하게 상호작용한다.이 불가항력적이고 순응적인 변화는 수용성 아데닐 시클라아제의 활성 부위가 그것을 cAMP로 변환하기 위해 ATP를 적절하게 결합하는 능력을 방해한다. 아르기닌 176은 보통 활성 부위에서 ATP 및 다른 촉매 이온과 상호작용하므로, 그것이 정상 위치에서 비티오놀 억제제와 상호 작용하기 위해 돌리면 더 이상 F가 아니다.ATP를 활성 사이트에 바인딩된 상태로 유지하는 방법.
또 다른 형태의 억제에서 비티오놀은 단순한 중탄산나트륨보다 훨씬 큰 분자여서 수용성 아데닐 사이클라아제의 작은 채널을 통해 도달하고 ATP의 결합을 방해할 정도로 크기가 커 cAMP로의 전환을 방해한다.
중탄산염 결합 부위에서 비티오놀에 의한 수용성 아데닐 시클라아제의 이러한 억제는 혼합 억제 그래프를 통해 입증된다. 여기서 고농도의 비티오놀은 낮은 Vmax와 더 큰 Km를 갖는다.이는 빗티오놀의 농도가 높을 때 반응 속도가 감소하고 기판 사이의 친화력이 감소하는 것으로 해석된다.
그러나 임상적으로 관련된 수준에서 수용성 아데닐 시클라아제를 억제해야 하는 비티오놀의 농도 또한 생체내 세포독성이다.따라서 수용성 아데닐 사이클라아제를 억제하여 세포 내 cAMP 축적을 감소시키는 데 필요한 치료약으로 사용할 수 없다.그러나, 그것은 결국 용해성 아데닐 시클라아제의 중탄산염 결합 부지를 겨냥할 수 있는 화합물을 찾는 것을 조명한다.비티오놀은 대부분 알로스테릭 메커니즘을 통해 중탄산염 결합 부위를 통해 작용하는 것으로 알려진 최초의 수용성 아데닐 시클라아제 억제제다.
안전 및 규정
LD50(도덕, 마우스)은 2100mg/kg이다.[3]
비티오놀은 미국 FDA가 사진 감식 효과를 이유로 금지하기 전까지 비누와 화장품에 사용됐다.이 화합물은 광촉매 감작성을 유발하는 것으로 알려져 있다.[4]
참조
- ^ Sanada Y, Senba H, Mochizuki R, Arakaki H, Gotoh T, Fukumoto S, Nagahata H (2009). "Evaluation of Marked Rise in Fecal Egg Output after Bithionol Administration to Horse and its Application as a Diagnostic Marker for Equine Anoplocephala perfoliata Infection" (pdf). Journal of Veterinary Medical Science. 71 (5): 617–620. doi:10.1292/jvms.71.617. PMID 19498288.
- ^ Kleinboelting, S.; Ramos-Espiritu, L.; Buck, H.; Colis, L; Heuvel, J.V.; Glickman, J.F.; Levin, L.R.; Buck, J.; Steegborn, C. (2016). "Bithionol Potently Inhibits Human Soluble Adenylyl Cyclase through Binding to the Allosteric Activator Site". Journal of Biological Chemistry. 291 (18): 9776–9784. doi:10.1074/jbc.M115.708255. PMC 4850313. PMID 26961873.
- ^ Helmut Fiege; Heinz-Werner Voges; Toshikazu Hamamoto; Sumio Umemura; Tadao Iwata; Hisaya Miki; Yasuhiro Fujita; Hans-Josef Buysch; Dorothea Garbe (2007). "Phenol Derivatives". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_313.
- ^ Morton, I.K.; Hall, J.M. (1999). Concise Dictionary of Pharmacological Agents. doi:10.1007/978-94-011-4439-1. ISBN 978-94-010-5907-7. S2CID 25401949.



