저친화성 신경증식인자수용체
Low-affinity nerve growth factor receptorp75 뉴로트로핀 수용체(p75NTR)는 p75가 발견되기 전인 1973년에 저친화성 신경 성장인자 수용체(LNGFR)[5][6]로 처음 확인되었다.NTR은 신경 성장 [7][8]인자와 동일하게 다른 신경트로핀과 결합합니다. p75NTR은 신경영양인자 수용체입니다.신경영양인자 수용체는 신경성장인자, 뉴로트로핀-3, 뇌유래 신경영양인자 및 뉴로트로핀-4를 포함한 뉴로트로핀과 결합한다.모든 신경트로핀은 p75NTR에 결합한다.이것은 또한 미성숙한 프로뉴로트로핀 [9][10]형태도 포함한다.p75NTR을 포함한 신경영양인자 수용체는 발달하는 뉴런의 비율에 대한 적절한 밀도를 보장하고 발전하는 더 넓은 지도를 정확한 연결로 정제하는 역할을 한다. p75NTR은 신경생존과 신경사멸을 [7]촉진하는 경로에 관여한다.
수용체 패밀리
p75NTR은 종양괴사인자 수용체 슈퍼패밀리의 일원이다. p75NTR/LNGFR은 종양괴사인자1(TNFR1)과 TNFR2, Fas, RANK, CD40을 포함한 약 25개의 수용체를 포함하고 있는 [5][6][11]이 큰 수용체 패밀리 중 첫 번째 특징이다.TNFR 슈퍼 패밀리의 모든 구성원은 구조적으로 관련된 시스테인이 풍부한 모듈을 ECD에 포함하고 있다. p75NTR은 Tyrosine kinase co-receptor로서 작용하는 능력, 그리고 신경로핀이 구조적으로 리간드와 무관하기 때문에 삼량화보다는 이량화하려는 성향 때문에 이 패밀리의 특이한 구성원이다.TNFR 패밀리를 바인드합니다.실제로 p75NTR을 제외하고 기본적으로 TNFR 패밀리의 모든 구성원은 TNF 리간드 슈퍼 [12]패밀리의 구성원인 구조적으로 관련된 Type II Tembrane 리간드를 우선적으로 결합한다.
구조.
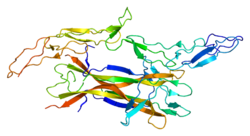
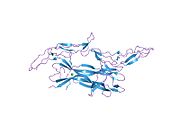
p75NTR은 분자량이 75kDa인 I형 트랜스막 단백질로 세포외 [13]도메인에서 N- 및 O-결합을 통한 글리코실화에 의해 결정된다.세포외 도메인, 막간 도메인 및 세포내 도메인으로 구성됩니다.세포외 도메인은 신경트로핀 결합을 촉진하는 특성인 음전하를 띤 4개의 시스테인이 풍부한 반복 도메인, CRD1, CRD2, CRD3, CRD4를 연결하는 줄기 도메인으로 구성된다.세포 내 부분은 사망 도메인으로 알려진 전지구적 형태의 도메인으로, 3개씩 세트로 배열된 두 세트의 수직 나선형으로 구성되어 있습니다.플렉시블 링커 영역N 터미널 [14]도메인을 통해 트랜스멤브레인 도메인을 연결합니다.다른 TNFR 단백질에서 발견되는 I형 사망 도메인과는 대조적으로 p75NTR의 II형 세포 내 사망 도메인은 자가 연관되거나 하지 않는다는 것을 말하는 것이 중요하다.이것은 p75의 초기 징후였다.NTR은 TNFR 사망 도메인과 동일한 메커니즘을 통해 사망 신호를 보내지 않지만, 다른 두 번째 메신저를 활성화하는 p75NTR 사망 도메인의 능력은 [13]보존된다.
NT-3에 대한 p75ECD 결합 인터페이스는 소수성 상호작용, 염분 브리지 및 수소 결합에 의해 안정화되는 3개의 주요 접촉 부위로 나눌 수 있습니다. NGF의 경우 2개입니다.CDR1과 CDR2 사이의 결합 영역은 5개의 수소 결합과 1개의 소금 브릿지를 포함하는 사이트 1을 형성합니다.사이트 2는 CDR3와 CRD4의 동등한 기여로 형성되며 2개의 소금 브릿지와 2개의 수소 결합을 포함한다.CRD4의 사이트 3에는 소금 [15]브릿지가 1개만 포함되어 있습니다.
기능.
신경트로핀과의 상호작용
p75와 상호작용하는 신경트로핀NTR에는 NGF, NT-3, BDNF 및 NT-4/[7]5가 포함됩니다.p75 활성화 신경트로핀NTR은 (예를 들어, c-Jun N 말단 키나아제 시그널링과 후속 p53, Jax 유사 단백질 및 카스파아제 [13]활성화를 통해) 아포토시스를 시작할 수 있다.이 효과는 TrkA에 [16]의한 항아포토시스 시그널링에 의해 상쇄될 수 있다.p75에 대한 뉴로트로핀 결합NTR은 아포토시스 시그널링 외에도 (예를 들어 NF-kB [17]활성화를 통해) 신경 생존을 촉진할 수 있다.p75NTR 의존 생존을 매개하는 역할을 할 수 있는 Akt의 여러 표적이 있지만, 더 흥미로운 가능성 중 하나는 IkB 키나제 1(IKK1)의 Ant 유도 인산화 작용이 NF-kB의 유도 [12]작용에 있다는 것이다.
프로프로프로트로핀과의 상호작용
NGF 및 BNDF의 프로폼(proNGF 및 proBNDF)은 NGF 및 BNDF의 전구체이며, proNGF 및 proBNDF는 p75NTR과 상호작용하여 TrKA 매개 생존 메커니즘을 활성화하지 않고 p75NTR 매개 아포토시스를 일으킨다.성숙한 신경트로핀으로 프로포름을 분해하면 성숙한 NGF와 BDNF가 TrkA 매개 생존 메커니즘을 [18][19]활성화시킬 수 있습니다.
감각 발달
최근 연구는 눈과 감각 [20][21]뉴런의 발달, 그리고 [22][23][24]성인의 근육과 신경 손상 수복을 포함한 LNGFR의 많은 역할을 제안했습니다.후각 후위화 글루아의 두 개의 구별되는 하위 집단은[25] 저선호도 신경 성장인자 수용체의 높은 또는 낮은 세포 표면 발현으로 확인되었다(p75).
다른 수용체와의 상호작용
소틀린
Sortilin은 많은 아포토시스 촉진 p75에 필요하다.BDNF와 같은 신경트로핀의 결합을 위한 공동 수용체로서 기능하는 NTR 반응. 프로뉴로트로핀(프로BDNF와 같은)은 특히 p75에 잘 결합한다.sortilin이 존재하는 경우의 [26]NTR.
Trk 수용체와의 교잡
p75일 때NTR은 아포토시스를 시작하고, 트로포미오신 수용체 키나제 A(TrkA)에 대한 NGF 결합은 p75를 부정할 수 있다.NTR 아포토시스 효과. NGF가 TrkA에 결합할 때 p75NTR c-Jun 키나제 경로 활성화(아포토시스 유발)가 억제되며, 생존을 촉진하는 NF-kB의 p75NTR 활성화는 TrkA에 [26]결합하는 NGF의 영향을 받지 않는다.
Nogo-66 수용체(NgR1)
p75NTR은 Nogo-66 수용체(NgR1)와 복합체에서 기능하여 Nogo, MAG 또는 OMGP와 같은 CNS 미엘린의 억제 단백질에 노출된 재생 축삭의 RhoA 의존적 성장 억제를 매개한다.p75 미포함NTR, OMgP는 RhoA를 활성화하여 CNS 축삭 재생을 억제할 수 있습니다.p75의 공식NTR 및 OMgP는 RhoA 활성화를 억제합니다.NgR1, p75NTR 및 LINGO1의 복합체는 RhoA를 [27]활성화할 수 있습니다.
p75NTR 매개 신호 경로
NF-kB 활성화
NF-kB는 p75NTR에 의해 활성화될 수 있는 전사 인자입니다.신경성장인자(NGF)는 신경 성장을 촉진하는 신경트로핀으로, NGF가 없으면 뉴런이 죽는다.NF-kB 활성화로 NGF가 없을 때 신경 사망을 예방할 수 있다.인산화 IbB 키나제는 NF-kB에서 분리되기 전에 NF-kB에 결합하고 활성화한다.분리 후 IbB는 분해되고 NF-kB는 핵까지 계속되어 생존 전사를 시작한다.NF-kB는 또한 [17]NGF와 함께 신경 생존을 촉진한다.
NF-kB 활성은 p75NTR에 의해 활성화되며 Trk 수용체를 통해 활성화되지 않는다.NF-kB 활동은 뇌에서 파생된 신경영양인자 신경생존 [17]촉진에 영향을 미치지 않는다.
RhoGDI 및 RhoA
p75NTR은 액틴 어셈블리의 조절제 역할을 합니다.Ras homolog 패밀리 A(RhoA)는 액틴 세포 골격을 경직시켜 성장 원뿔 이동성을 제한하고 신경계의 신경 신장을 억제한다.리간드 결합이 없는 p75NTR은 RhoA를 활성화하고 액틴 어셈블리를 제한하지만 신경트로핀은 p75에 결합한다.NTR은 RhoA를 비활성화하고 액틴 조립을 [28]촉진할 수 있다.p75NTR은 Rho GDP 해리 억제제(RhoGDI)와 관련지어지며, RhoGDI는 RhoA와 관련지어진다.Nogo와의 상호작용은 p75 사이의 연관성을 강화할 수 있다.NTR 및 RhoGDI. p75에 대한 신경트로핀 결합NTR은 RhoGDI와 p75NTR의 결합을 억제하여 RhoA 방출을 억제하고 성장원추신장(RhoA 액틴 억제 억제)[29]을 촉진한다.
JNK 시그널링 패스
p75에 대한 뉴로트로핀 결합NTR은 발달하는 뉴런의 아포토시스를 유발하는 c-Jun N 말단 키나아제(JNK) 신호 경로를 활성화한다.JNK는 일련의 중간체를 통해 p53을 활성화하고 p53은 백스를 활성화하여 아포토시스를 시작합니다.TrkA는 p75NTR 매개 JNK 경로 아포토시스를 [30]예방할 수 있다.
JNK-Bim-EL 신호 경로
JNK는 Bim-EL 아포토시스 활성을 활성화하는 Bcl-2 상호작용 세포사 매개체(Bim)의 스플라이싱 동질체인 Bim-EL을 직접 인산화시킬 수 있다.아포토시스에는 JNK 활성화가 필요하지만 JNK 시그널링 경로의 단백질인 c-jun이 항상 [16]필요한 것은 아니다.
Caspase 의존 시그널링
LNGFR은 또한 신경변성 [31]질환에서 발달 축삭 가지치기 및 축삭 변성을 촉진하는 캐스파아제 의존적 신호 경로를 활성화한다.
아포토시스 경로에서 TNF 수용체 슈퍼패밀리의 구성원은 TRADD 또는 FADD가 수용체의 사망영역에 직접 결합하는 사망유도시그널링복합체(DISC)를 조립함으로써 카스파제8의 응집 및 활성화와 후속 카스파제 캐스케이드 활성화를 가능하게 한다.단, Caspase 8 유도는 p75NTR 매개 아포토시스에는 관여하지 않는 것으로 보이지만 Caspase 9는 p75NTR 매개 살처분 [12]중에 활성화된다.
질병에서의 역할
헌팅턴병
헌팅턴병은 인지장애로 특징지어진다.p75의 표현이 증가하다헌팅턴병 환자(쥐 모델 및 사람 포함)의 해마에서 NTR.p75의 과잉 표현생쥐의 NTR은 헌팅턴병과 유사한 인지장애를 일으킨다. p75NTR은 p75를 통해 해마의 수상돌기 가시의 감소와 관련이 있다.트랜스포밍 단백질 RhoA와의 NTR 상호작용.p75NTR 기능을 조절하는 것은 헌팅턴병을 [32]치료하는데 있어 미래의 방향이 될 수 있다.
근위축성 측삭경화증
근위축성 측삭경화증 ALS는 1차 운동피질, 피질척수관, 뇌간, 척수에서 운동뉴런의 퇴화를 반영하는 진행성 근육마비가 특징인 신경변성 질환이다.심각한 신경 변성을 일으키는 ALS 모델인 Superoxide Dismutase 1(SOD1) 돌연변이 마우스를 사용한 한 연구는 p75의 발현NTR은 변성 정도 및 p75와 상관관계가 있다.NTR 녹다운은 질병의 [33][34][35]진행을 지연시킨다.
알츠하이머병
알츠하이머병은 노인들에게 치매의 가장 흔한 원인이다.AD는 사람의 일상생활과 활동에 지장을 줄 정도로 사고, 기억, 추론 등 인지기능과 행동능력이 상실되는 것이 특징인 신경퇴행성 질환이다.AD의 신경병리학적 특징은 아밀로이드 플라크와 신경섬유 엉킴을 포함하며, 이는 신경계의 죽음을 초래한다.AD의 동물 모델에 대한 연구는 p75를 보여주었습니다.NTR은 아밀로이드 β 유도 신경 [36]손상에 기여한다.AD에 걸린 사람의 경우 p75가 증가한다.TrkA에 상대적인 NTR 발현이 콜린 [37][38]작동성 뉴런의 손실에 책임이 있는 것으로 제안되었다.AD에서 proNGF의 증가는 Neurotrophin 환경이 p75NTR/Sortilin 시그널링에 적합함을 나타내며, proNGF 매개 [35]시그널링으로의 전환에 의해 노화 관련 신경 손상이 촉진된다는 이론을 뒷받침한다.
암줄기세포에서의 역할
p75NTR은 흑색종과 다른 암의 암 줄기세포에 대한 지표로 관여되어 왔다.면역 결핍 마우스 모델에 이식된 흑색종 세포는 흑색종을 [40]성장시키기 위해 CD271의 발현을 필요로 하는 것으로 나타났다.CD271의 유전자 녹다운은 또한 흑색종 세포의 신경능 줄기세포 특성을 폐지하고 유전체 안정성을 감소시켜 이동, 종양 발생, 증식 및 아포토시스 [41][42][43]유도를 감소시키는 것으로 나타났다.또한 뇌 전이성 흑색종 세포에서 CD271의 수치가 증가하는 것이 관찰되었으며, BRAF 억제제인 베무라페니브에 대한 내성이 고악성 뇌 및 폐 메타스타사이징 흑색종 세포를 [44][43][45][46]선택하는 것으로 추정된다.
상호 작용
저친화성 신경 성장인자 수용체는 다음과 상호작용하는 것으로 나타났다.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG000064300 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000000120 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b Johnson D, Lanahan A, Buck CR, Sehgal A, Morgan C, Mercer E, et al. (November 1986). "Expression and structure of the human NGF receptor". Cell. 47 (4): 545–54. doi:10.1016/0092-8674(86)90619-7. PMID 3022937. S2CID 22472119.
- ^ a b Radeke MJ, Misko TP, Hsu C, Herzenberg LA, Shooter EM (1987). "Gene transfer and molecular cloning of the rat nerve growth factor receptor". Nature. 325 (6105): 593–7. Bibcode:1987Natur.325..593R. doi:10.1038/325593a0. PMID 3027580. S2CID 4342838.
- ^ a b c d e f Bibel M, Hoppe E, Barde YA (February 1999). "Biochemical and functional interactions between the neurotrophin receptors trk and p75NTR". The EMBO Journal. 18 (3): 616–22. doi:10.1093/emboj/18.3.616. PMC 1171154. PMID 9927421.
- ^ Frade JM, Barde YA (February 1998). "Nerve growth factor: two receptors, multiple functions". BioEssays. 20 (2): 137–45. doi:10.1002/(SICI)1521-1878(199802)20:2<137::AID-BIES6>3.0.CO;2-Q. PMID 9631659.
- ^ Barker PA (May 2004). "p75NTR is positively promiscuous: novel partners and new insights". Neuron. 42 (4): 529–33. doi:10.1016/j.neuron.2004.04.001. PMID 15157416. S2CID 15080734.
- ^ Chao MV, Bothwell M (January 2002). "Neurotrophins: to cleave or not to cleave". Neuron. 33 (1): 9–12. doi:10.1016/s0896-6273(01)00573-6. PMID 11779474. S2CID 17364992.
- ^ He XL, Garcia KC (May 2004). "Structure of nerve growth factor complexed with the shared neurotrophin receptor p75". Science. 304 (5672): 870–5. Bibcode:2004Sci...304..870H. doi:10.1126/science.1095190. PMID 15131306. S2CID 46060440.
- ^ a b c Roux PP, Barker PA (June 2002). "Neurotrophin signaling through the p75 neurotrophin receptor". Progress in Neurobiology. 67 (3): 203–33. doi:10.1016/S0301-0082(02)00016-3. PMID 12169297. S2CID 8659757.
- ^ a b c Underwood CK, Coulson EJ (30 June 2007). "The p75 neurotrophin receptor". The International Journal of Biochemistry & Cell Biology. 40 (9): 1664–8. doi:10.1016/j.biocel.2007.06.010. PMID 17681869.
- ^ Chen Y, Zeng J, Cen L, Chen Y, Wang X, Yao G, et al. (2009). "Multiple roles of the p75 neurotrophin receptor in the nervous system". The Journal of International Medical Research. 37 (2): 281–8. doi:10.1177/147323000903700201. PMID 19383220. S2CID 40720230.
- ^ Vilar M (29 November 2016). "Structural Characterization of the p75 Neurotrophin Receptor: A Stranger in the TNFR Superfamily". Vitamins and Hormones. 104: 57–87. doi:10.1016/bs.vh.2016.10.007. PMID 28215307.
- ^ a b Becker EB, Howell J, Kodama Y, Barker PA, Bonni A (October 2004). "Characterization of the c-Jun N-terminal kinase-BimEL signaling pathway in neuronal apoptosis". The Journal of Neuroscience. 24 (40): 8762–70. doi:10.1523/JNEUROSCI.2953-04.2004. PMC 6729963. PMID 15470142.
- ^ a b c d Hamanoue M, Middleton G, Wyatt S, Jaffray E, Hay RT, Davies AM (July 1999). "p75-mediated NF-kappaB activation enhances the survival response of developing sensory neurons to nerve growth factor". Molecular and Cellular Neurosciences. 14 (1): 28–40. doi:10.1006/mcne.1999.0770. PMID 10433815. S2CID 25648122.
- ^ a b Lee R, Kermani P, Teng KK, Hempstead BL (November 2001). "Regulation of cell survival by secreted proneurotrophins". Science. 294 (5548): 1945–8. Bibcode:2001Sci...294.1945L. doi:10.1126/science.1065057. PMID 11729324. S2CID 872149.
- ^ Feng D, Kim T, Ozkan E, Light M, Torkin R, Teng KK, et al. (March 2010). "Molecular and structural insight into proNGF engagement of p75NTR and sortilin". Journal of Molecular Biology. 396 (4): 967–84. doi:10.1016/j.jmb.2009.12.030. PMC 2847487. PMID 20036257.
- ^ Nicol GD (October 2008). "Nerve growth factor, sphingomyelins, and sensitization in sensory neurons". Sheng Li Xue Bao. 60 (5): 603–4. PMID 18958367.
- ^ Di Girolamo N, Sarris M, Chui J, Cheema H, Coroneo MT, Wakefield D (December 2008). "Localization of the low-affinity nerve growth factor receptor p75 in human limbal epithelial cells". Journal of Cellular and Molecular Medicine. 12 (6B): 2799–811. doi:10.1111/j.1582-4934.2008.00290.x. PMC 3828893. PMID 19210757.
- ^ Chen LW, Yung KK, Chan YS, Shum DK, Bolam JP (December 2008). "The proNGF-p75NTR-sortilin signalling complex as new target for the therapeutic treatment of Parkinson's disease". CNS & Neurological Disorders Drug Targets. 7 (6): 512–23. doi:10.2174/187152708787122923. PMID 19128208.
- ^ Kocsis JD, Lankford KL, Sasaki M, Radtke C (June 2009). "Unique in vivo properties of olfactory ensheathing cells that may contribute to neural repair and protection following spinal cord injury". Neuroscience Letters. 456 (3): 137–42. doi:10.1016/j.neulet.2008.08.093. PMC 2713444. PMID 19429149.
- ^ Deponti D, Buono R, Catanzaro G, De Palma C, Longhi R, Meneveri R, et al. (August 2009). "The low-affinity receptor for neurotrophins p75NTR plays a key role for satellite cell function in muscle repair acting via RhoA". Molecular Biology of the Cell. 20 (16): 3620–7. doi:10.1091/mbc.E09-01-0012. PMC 2777922. PMID 19553472.
- ^ Honoré A, Le Corre S, Derambure C, Normand R, Duclos C, Boyer O, et al. (March 2012). "Isolation, characterization, and genetic profiling of subpopulations of olfactory ensheathing cells from the olfactory bulb". Glia. 60 (3): 404–13. doi:10.1002/glia.22274. PMID 22161947. S2CID 31230806.
- ^ a b Chen ZY, Ieraci A, Teng H, Dall H, Meng CX, Herrera DG, et al. (June 2005). "Sortilin controls intracellular sorting of brain-derived neurotrophic factor to the regulated secretory pathway". The Journal of Neuroscience. 25 (26): 6156–66. doi:10.1523/JNEUROSCI.1017-05.2005. PMC 1201519. PMID 15987945.
- ^ a b Mi S, Lee X, Shao Z, Thill G, Ji B, Relton J, et al. (March 2004). "LINGO-1 is a component of the Nogo-66 receptor/p75 signaling complex". Nature Neuroscience. 7 (3): 221–8. doi:10.1038/nn1188. PMID 14966521. S2CID 2344794.
- ^ Yamashita T, Tucker KL, Barde YA (November 1999). "Neurotrophin binding to the p75 receptor modulates Rho activity and axonal outgrowth". Neuron. 24 (3): 585–93. doi:10.1016/s0896-6273(00)81114-9. PMID 10595511. S2CID 17271817.
- ^ a b c Yamashita T, Tohyama M (May 2003). "The p75 receptor acts as a displacement factor that releases Rho from Rho-GDI". Nature Neuroscience. 6 (5): 461–7. doi:10.1038/nn1045. PMID 12692556. S2CID 10865814.
- ^ a b Aloyz RS, Bamji SX, Pozniak CD, Toma JG, Atwal J, Kaplan DR, Miller FD (December 1998). "p53 is essential for developmental neuron death as regulated by the TrkA and p75 neurotrophin receptors". The Journal of Cell Biology. 143 (6): 1691–703. doi:10.1083/jcb.143.6.1691. PMC 2132983. PMID 9852160.
- ^ Simon DJ, Weimer RM, McLaughlin T, Kallop D, Stanger K, Yang J, et al. (December 2012). "A caspase cascade regulating developmental axon degeneration". The Journal of Neuroscience. 32 (49): 17540–53. doi:10.1523/JNEUROSCI.3012-12.2012. PMC 3532512. PMID 23223278.
- ^ Brito V, Giralt A, Enriquez-Barreto L, Puigdellívol M, Suelves N, Zamora-Moratalla A, et al. (October 2014). "Neurotrophin receptor p75(NTR) mediates Huntington's disease-associated synaptic and memory dysfunction". The Journal of Clinical Investigation. 124 (10): 4411–28. doi:10.1172/JCI74809. PMC 4191006. PMID 25180603.
- ^ Shepheard SR, Chataway T, Schultz DW, Rush RA, Rogers ML (January 2014). "The extracellular domain of neurotrophin receptor p75 as a candidate biomarker for amyotrophic lateral sclerosis". PLOS ONE. 9 (1): e87398. Bibcode:2014PLoSO...987398S. doi:10.1371/journal.pone.0087398. PMC 3903651. PMID 24475283.
- ^ Turner BJ, Cheah IK, Macfarlane KJ, Lopes EC, Petratos S, Langford SJ, Cheema SS (November 2003). "Antisense peptide nucleic acid-mediated knockdown of the p75 neurotrophin receptor delays motor neuron disease in mutant SOD1 transgenic mice". Journal of Neurochemistry. 87 (3): 752–63. doi:10.1046/j.1471-4159.2003.02053.x. PMID 14535957. S2CID 5901529.
- ^ a b Meeker RB, Williams KS (May 2015). "The p75 neurotrophin receptor: at the crossroad of neural repair and death". Neural Regeneration Research. 10 (5): 721–5. doi:10.4103/1673-5374.156967. PMC 4468762. PMID 26109945.
- ^ Yang T, Knowles JK, Lu Q, Zhang H, Arancio O, Moore LA, et al. (21 July 2008). "Small molecule, non-peptide p75 ligands inhibit Abeta-induced neurodegeneration and synaptic impairment". PLOS ONE. 3 (11): e3604. Bibcode:2008PLoSO...3.3604Y. doi:10.1371/journal.pone.0003604. PMC 2575383. PMID 18978948.
- ^ Costantini C, Scrable H, Puglielli L (May 2006). "An aging pathway controls the TrkA to p75NTR receptor switch and amyloid beta-peptide generation". The EMBO Journal. 25 (9): 1997–2006. doi:10.1038/sj.emboj.7601062. PMC 1456930. PMID 16619032.
- ^ Counts SE, Nadeem M, Wuu J, Ginsberg SD, Saragovi HU, Mufson EJ (October 2004). "Reduction of cortical TrkA but not p75(NTR) protein in early-stage Alzheimer's disease". Annals of Neurology. 56 (4): 520–31. doi:10.1002/ana.20233. PMID 15455399. S2CID 38106502.
- ^ Fahnestock M, Michalski B, Xu B, Coughlin MD (August 2001). "The precursor pro-nerve growth factor is the predominant form of nerve growth factor in brain and is increased in Alzheimer's disease". Molecular and Cellular Neurosciences. 18 (2): 210–20. doi:10.1006/mcne.2001.1016. PMID 11520181. S2CID 8443739.
- ^ Boiko AD, Razorenova OV, van de Rijn M, Swetter SM, Johnson DL, Ly DP, et al. (July 2010). "Human melanoma-initiating cells express neural crest nerve growth factor receptor CD271". Nature. 466 (7302): 133–7. Bibcode:2010Natur.466..133B. doi:10.1038/nature09161. PMC 2898751. PMID 20596026.
- ^ Redmer T, Welte Y, Behrens D, Fichtner I, Przybilla D, Wruck W, et al. (2014). "The nerve growth factor receptor CD271 is crucial to maintain tumorigenicity and stem-like properties of melanoma cells". PLOS ONE. 9 (5): e92596. Bibcode:2014PLoSO...992596R. doi:10.1371/journal.pone.0092596. PMC 4010406. PMID 24799129.
- ^ Redmer T, Walz I, Klinger B, Khouja S, Welte Y, Schäfer R, Regenbrecht C (January 2017). "The role of the cancer stem cell marker CD271 in DNA damage response and drug resistance of melanoma cells". Oncogenesis. 6 (1): e291. doi:10.1038/oncsis.2016.88. PMC 5294251. PMID 28112719.
- ^ a b Radke J, Roßner F, Redmer T (August 2017). "CD271 determines migratory properties of melanoma cells". Scientific Reports. 7 (1): 9834. Bibcode:2017NatSR...7.9834R. doi:10.1038/s41598-017-10129-z. PMC 5574914. PMID 28852061.
- ^ Guo R, Fierro-Fine A, Goddard L, Russell M, Chen J, Liu CZ, et al. (2014). "Increased expression of melanoma stem cell marker CD271 in metastatic melanoma to the brain". International Journal of Clinical and Experimental Pathology. 7 (12): 8947–51. PMC 4313973. PMID 25674270.
- ^ Zubrilov I, Sagi-Assif O, Izraely S, Meshel T, Ben-Menahem S, Ginat R, et al. (May 2015). "Vemurafenib resistance selects for highly malignant brain and lung-metastasizing melanoma cells". Cancer Letters. 361 (1): 86–96. doi:10.1016/j.canlet.2015.02.041. PMID 25725450.
- ^ Redmer T (July 2018). "Deciphering mechanisms of brain metastasis in melanoma - the gist of the matter". Molecular Cancer. 17 (1): 106. doi:10.1186/s12943-018-0854-5. PMC 6064184. PMID 30053879.
- ^ Shonukan O, Bagayogo I, McCrea P, Chao M, Hempstead B (June 2003). "Neurotrophin-induced melanoma cell migration is mediated through the actin-bundling protein fascin". Oncogene. 22 (23): 3616–23. doi:10.1038/sj.onc.1206561. PMID 12789270.
- ^ a b Tcherpakov M, Bronfman FC, Conticello SG, Vaskovsky A, Levy Z, Niinobe M, et al. (December 2002). "The p75 neurotrophin receptor interacts with multiple MAGE proteins". The Journal of Biological Chemistry. 277 (51): 49101–4. doi:10.1074/jbc.C200533200. PMID 12414813.
- ^ Kuwako K, Taniura H, Yoshikawa K (January 2004). "Necdin-related MAGE proteins differentially interact with the E2F1 transcription factor and the p75 neurotrophin receptor". The Journal of Biological Chemistry. 279 (3): 1703–12. doi:10.1074/jbc.M308454200. PMID 14593116.
- ^ Bronfman FC, Tcherpakov M, Jovin TM, Fainzilber M (April 2003). "Ligand-induced internalization of the p75 neurotrophin receptor: a slow route to the signaling endosome". The Journal of Neuroscience. 23 (8): 3209–20. doi:10.1523/JNEUROSCI.23-08-03209.2003. PMC 6742322. PMID 12716928.
- ^ Mukai J, Hachiya T, Shoji-Hoshino S, Kimura MT, Nadano D, Suvanto P, et al. (June 2000). "NADE, a p75NTR-associated cell death executor, is involved in signal transduction mediated by the common neurotrophin receptor p75NTR". The Journal of Biological Chemistry. 275 (23): 17566–70. doi:10.1074/jbc.C000140200. PMID 10764727.
- ^ Nykjaer A, Lee R, Teng KK, Jansen P, Madsen P, Nielsen MS, et al. (February 2004). "Sortilin is essential for proNGF-induced neuronal cell death". Nature. 427 (6977): 843–8. Bibcode:2004Natur.427..843N. doi:10.1038/nature02319. PMID 14985763. S2CID 4343450.
- ^ Higuchi H, Yamashita T, Yoshikawa H, Tohyama M (April 2003). "PKA phosphorylates the p75 receptor and regulates its localization to lipid rafts". The EMBO Journal. 22 (8): 1790–800. doi:10.1093/emboj/cdg177. PMC 154469. PMID 12682012.
- ^ a b Ye X, Mehlen P, Rabizadeh S, VanArsdale T, Zhang H, Shin H, et al. (October 1999). "TRAF family proteins interact with the common neurotrophin receptor and modulate apoptosis induction". The Journal of Biological Chemistry. 274 (42): 30202–8. doi:10.1074/jbc.274.42.30202. PMID 10514511.
- ^ Krajewska M, Krajewski S, Zapata JM, Van Arsdale T, Gascoyne RD, Berern K, et al. (June 1998). "TRAF-4 expression in epithelial progenitor cells. Analysis in normal adult, fetal, and tumor tissues". The American Journal of Pathology. 152 (6): 1549–61. PMC 1858434. PMID 9626059.
추가 정보
- Buxser S, Puma P, Johnson GL (February 1985). "Properties of the nerve growth factor receptor. Relationship between receptor structure and affinity". The Journal of Biological Chemistry. 260 (3): 1917–26. doi:10.1016/S0021-9258(18)89680-6. PMID 2981877.
- Glass DJ, Nye SH, Hantzopoulos P, Macchi MJ, Squinto SP, Goldfarb M, Yancopoulos GD (July 1991). "TrkB mediates BDNF/NT-3-dependent survival and proliferation in fibroblasts lacking the low affinity NGF receptor". Cell. 66 (2): 405–13. doi:10.1016/0092-8674(91)90629-D. PMID 1649703. S2CID 43626580.
- Ibáñez CF (June 2002). "Jekyll-Hyde neurotrophins: the story of proNGF". Trends in Neurosciences. 25 (6): 284–6. doi:10.1016/S0166-2236(02)02169-0. PMID 12086739. S2CID 9449831.
- Radeke MJ, Misko TP, Hsu C, Herzenberg LA, Shooter EM (1987). "Gene transfer and molecular cloning of the rat nerve growth factor receptor". Nature. 325 (6105): 593–7. Bibcode:1987Natur.325..593R. doi:10.1038/325593a0. PMID 3027580. S2CID 4342838.