타크로리무스
Tacrolimus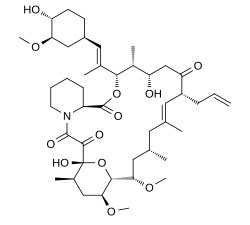 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | Prograf, Advagraf, Protopic 등 |
| 기타 이름 | FK-506, 후지마이신 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a601117 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 국소, 입으로, 정맥주사 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | 24%(5~67%), 지방이 풍부한 음식을 먹은 후 감소 |
| 단백질 결합 | ≥98.8% |
| 신진대사 | 간 CYP3A4, CYP3A5 |
| 제거 반감기 | 이식 환자의 경우 11.3시간(3.5~40.6시간 범위) |
| 배설 | 대부분 배설물 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| PDB 리간드 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.155.367 |
| 화학 및 물리적 데이터 | |
| 공식 | C44H69NO12 |
| 어금질량 | 804.031 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
그중에서도 프로그라프라는 브랜드명으로 판매되는 타크로리무스는 면역억제제다. 제3의 장기이식 후 장기 거부반응의 위험성은 보통이다. 장기거부 위험을 낮추기 위해 타크로리무스를 투여한다. 습진, 건선 등 T세포 매개 질환 치료에서도 국소 의약품으로 판매할 수 있다. 예를 들어 골수이식 후 심한 난치성 우비염, 최소한의 변화병 악화, 기무라의 병, 유리구균 등에 처방된다. 고양이와 개의 안구건조증후군을 치료하는 데 사용할 수 있다.[5][6]
타크로리무스는 인체가 학습한(또는 적응하는) 면역 반응의 일환으로 T세포의 발달과 증식을 촉진하는 분자인 인터루킨-2의 생산에 관여하는 칼시누린을 억제한다.
화학적으로는 1987년 처음 발견된 마크로리이드 락톤으로[7] 스트렙토미시스 츠쿠바엔시스균이 함유된 일본 토양 샘플의 발효 육수에서 나온 것이다.
그것은 세계보건기구의 필수 의약품 목록에 올라 있다.[8]
의학적 용법
장기이식
그것은 시클로스포린과 유사한 면역억제 성질을 가지고 있지만 훨씬 더 강력하다. 타크로리무스를 이용한 면역억제술은 한 연구에서 시클로스포린 기반 면역억제술(30.7% 대 46.4%)에 비해 급성거부율이 현저히 낮은 것과 관련이 있다.[9] 간 이식 첫해에는 치클로스포린보다는 타크로리무스로 임상 결과가 좋다.[10][11] 장기적 성과는 같은 정도로 개선되지 않았다. 타크로리무스는 보통 스테로이드, 마이코페놀레이트, 바실릭시맙과 같은 IL-2 수용체 억제제를 포함한 이식 후 칵테일의 일부로 처방된다. 투약은 투약 후 특정 시기에 혈액 수준을 목표로 적정량을 측정한다.[12]
스킨
연고로 타크로리무스는 습진, 특히 아토피 피부염 치료에 쓰인다. 스테로이드와 비슷한 방법으로 염증을 억제하고, 중위 스테로이드와 마찬가지로 효과가 있다. 타크로리무스의 중요한 장점은 스테로이드와 달리 피부 묽힘( 위축)이나 기타 스테로이드 관련 부작용을 일으키지 않는다는 점이다.[13]
활성병변에서 치유될 때까지 발라주지만 저선량(주 2회)에서도 지속적으로 사용할 수 있으며, 얼굴과 눈꺼풀 위로 얇아진 피부에도 바를 수 있다.[citation needed] 최대 1년의 임상시험이 실시되었다. 최근에는 특히 얼굴의 부위에서 특히 어린이들의 부분적 비틸리고를 치료하는데도 이용되고 있다.[14]
금기사항 및 주의사항
금기사항 및 주의사항에는 다음이 포함된다.[15]
국소적 용법
부작용
구강 또는 정맥주사 사용
부작용은, 감염, 심장 손상, 고혈압, 흐릿한 시야, 간과 신장 질환이 있어 혹독할 수 있(tacrolimus 신독성)[17]고 칼륨혈, 마그네슘 결핍 병, 고 혈당, 당뇨 진성, 가려움, 폐손상(sirolimus 또한 폐 손상을 입히)[18]과 식욕 감퇴, insom 등 다양한 신경 문제.nia, pos테리오반역성 뇌병증, 혼란, 약함, 우울증, 생생한 악몽, 경련, 신경병, 발작, 떨림,[19] 카테토니아.
또한 대상포진 또는 다종종 바이러스 감염과 같은 기존 곰팡이 또는 감염 조건의 심각도를 잠재적으로 증가시킬 수 있다.[15]
발암 및 돌연변이 유발
이식 이식 거부반응을 줄이기 위해 면역억제제를 복용하는 사람들에게서 악성종양(암)의 증가 위험은 인식된 합병증이다.[15] 가장 흔한 암은 비호지킨 림프종과[20] 피부암이다. 그 위험은 치료의 강도 및 기간과 관련이 있는 것으로 보인다.
국소적 용법
국소 타크로리무스 연고 사용과 관련된 가장 일반적인 부작용은 특히 넓은 영역에 걸쳐 사용할 경우 초기 도포 시 타는 듯한 느낌이나 가려움증을 포함하며, 환부에 대한 햇빛과 열에 대한 민감도가 증가한다.[citation needed] 덜 흔한 것은 독감과 같은 증상, 두통, 기침, 불타는 눈이다.[21]
암 위험
타크로리무스와 습진 관련 약품(피메크로리무스)은 아직 논란의 대상이지만 암 위험성이 있다는 의심을 받았다. FDA는 2005년 3월 동물 모델과 소수의 환자를 근거로 이 약에 대한 건강 경고를 발령했다. FDA는 향후 인간 연구가 더 결정적인 결과를 도출할 때까지 사용자에게 잠재적인 위험에 대해 조언할 것을 권고한다. 그러나, 영국의 피부과 의사들이 현재 시행하고 있는 관행은 이것을 심각한 실제 관심사로 여기지 않는 것이며, 그들은 점점 더 이 신약의 사용을 권장하고 있다.[22]
상호작용
또한 사이클로스포린과 마찬가지로, 그것은 광범위한 상호작용을 가지고 있다. 타크로리무스는 주로 간 효소의 시토크롬 P450 계통에 의해 대사되며, 이 계통과 상호작용을 하여 계통의 대사 활동을 유도하거나 억제하는 물질이 많다.[15]
타크로리무스 플라즈마 농도를 높이는 자몽과의 상호작용이 포함된다. 감염은 이식 후 환자의 질병성과 사망률의 주요 원인이므로, 가장 일반적으로[citation needed] 보고되는 상호작용은 항미생물제와의 상호작용을 포함한다. 에리트로마이신, 클라리트로마이신을 포함한 마크로롤라이드 항생제는 물론, 특히 아졸류급(플루코나졸, 보리오나졸)의 몇몇 새로운 항균류들은 시토크롬 효소를 놓고 경쟁함으로써 타크로리무스 수치를 높인다.[15]
약리학
작용기전
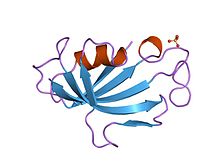
타크로리무스는 마콜라이드 캘시누린 억제제다. T세포에서 T세포 수용체의 활성화는 보통 세포내 칼슘을 증가시키며, 이것은 캘리누린을 통해 작용하여 캘리누린을 활성화시킨다. 그런 다음 캘시누린은 활성 T-세포(NF-AT)의 전사인자 핵인자를 탈인산화하여 T-세포의 핵으로 이동하고 IL-2 및 관련 사이토카인에 대한 유전자 코딩의 활성을 증가시킨다. 타크로리무스는 NF-AT의 탈인산화를 방지한다.[23]
세부적으로 타크로리무스는 면역성 FKBP12(FK506 결합단백질)에 결합해 펩티딜프로롤리멜라제 활성을 줄여 새로운 콤플렉스를 만들어낸다. 이 FKBP12–FK506 복합체는 캘시뉴린과 상호 작용하여 억제하므로 T-림프세포 신호 전달과 IL-2 전사를 모두 억제한다.[24] 이 활동은 사이클로스포린과 유사하지만, 급성 거부반응 발생률은 사이클로스포린 사용보다 타크로리무스 사용에 의해 감소한다.[9] 환자와 이식 생존에 관한 단기 면역억제가 두 약품 사이에 유사한 것으로 밝혀졌지만, 타크롤리무스는 보다 유리한 지질학적 프로파일을 갖게 되며, 이는 이식 생존에 대한 거부반응의 예측적 영향을 고려할 때 중요한 장기적 영향을 미칠 수 있다.[25]
약동학
구강 타크롤리무스는 위장관에서 서서히 흡수되며, 총 생체이용률은 20~25%(그러나 5~67%의 변동), 최고 혈장농도(Cmax)는 1~3시간 후에 도달한다. 특히 지방이 풍부한 약을 식사와 함께 복용하면 재흡수가 느려지고 생체이용률이 낮아진다. 혈액에서 타크로리무스는 주로 홍반과 결합되어 있으며, 5%만이 혈장에서 발견되며, 이 중 98.8% 이상이 혈장 단백질에 결합되어 있다.[15][26]
이 물질은 주로 CYP3A를 통해 간에서 대사되며, 장벽을 통해 대사된다. 혈액순환에서 발견되는 모든 대사물은 활동을 하지 않는다. 생물학적 반감기는 간 이식(12시간)이나 신장 이식(16시간) 환자보다 건강한 사람(평균 43시간)의 경우 간극의 차이로 인해 높은 것으로 보인다. 타크로리무스는 주로 대사물의 형태로 faeces를 통해 제거된다.[15][26]
습진에 국소적으로 적용하면 타크로리무스는 생체이용률이 거의 또는 전혀 없다.[15]
약리유전학
타크로리무스의 신진대사를 담당하는 지배적 효소는 CYP3A5이다. CYP3A5 단백질의 활성도에 변화를 일으키는 CYP3A5 내의 유전적 변화는 체내 타크로리무스의 농도에 영향을 미칠 수 있다. 특히 단일 뉴클레오티드 폴리모르프리즘(SNP) rs776746(CYP3A5 *3/*3)에서 G 알레르기에 동질성이 있는 개인은 비기능성 CYP3A5 단백질을 가지고 있다. G alle의 빈도는 일부 아프리카 인구의 4%에서 백인 인구의 80~90%까지 전 세계적으로 다양하다.[27] 많은 수의 연구에서 G 알레르기에 대한 동란성 개인들은 G 알레르기에 대해 동란성이 아닌 개인들에 비해 더 높은 농도의 타크로리무스를 가지고 있고 더 적은 양의 약물을 필요로 하는 것으로 나타났다. 타크로리무스의 목표 농도를 달성하는 것은 중요하다 – 수치가 너무 낮으면 이식 거부반응의 위험이 있고, 너무 높으면 약물 독성의 위험이 있다. rs776746 유전자형에 근거하여 환자를 투약하면 타크로리무스 목표치를 더 빠르고 빈번하게 달성할 수 있다는 증거가 있다. 그러나 tacrolimus를 복용하는 환자가 치료 약물 모니터링을 받기 때문에 Rs776746 유전자형에 기초한 투여가 임상 결과(이식 거부나 약물 독성의 위험 감소 등)를 개선하는지 여부에 대한 일관된 증거가 부족하다.[28][29][30][31]
NR1I2[32][33](인코딩 PXR)와 같은 CYP3A5 이외의 유전자의 유전자 다형성 역시 타크로리무스의 약동학에 유의미한 영향을 미친다는 연구결과가 나왔다.
역사
타크로리무스는 1987년에 발견되었는데,[34] 1975년 라파 누이(에스터 섬)에서 라파마이신(시로리무스)이 발견된 이후 발견된 최초의 마크로리미드 면역억제제제 중 하나이다.[35] 그것은 토양 박테리아인 스트렙토미세스 츠쿠바엔시스에 의해 생산된다.[36] 타크로리무스라는 이름은 "츠쿠바 마크로리이드 면역억제제"[37]에서 유래되었다.
타크로리머스는 1994년 미국 식품의약국(FDA)에 의해 간 이식에 사용되도록 처음 승인되었다.[38][39] 이 적응증은 신장 이식을 포함하도록 확대되었다.[40] 타크로리무스의 일반 버전은 2017년 미국에서 승인되었다.[41]
타크로리머스는 2002년 유럽연합(EU)에서 중간에서 중증 아토피 피부염 치료를 위해 의료용으로 승인됐다.[42] 2007년에는 성체 신장 또는 간 알로그라프트 수혜자의 이식 거부반응 예방과 성체 내 다른 면역억제 약품과의 치료에 내성이 있는 알로그라프트 거부반응 치료까지 확대되었다.[43] 2009년에는 성인 및 소아, 신장, 간 또는 심장 만능기프트 수혜자의 이식 거부반응 예방과 성인과 어린이의 다른 면역억제 약품과의 치료에 내성이 있는 만능기프트 거부반응 치료까지 그 징후가 확대되었다.[44]
사용 가능한 양식
이 의약품의 브랜드 버전은 아스텔라스파마가 소유하고 있으며, 매일 두 번 주어지는 프로그라프라는 브랜드 이름으로 판매되고 있다. 많은 다른 제조업체들이 2일제 제조의 대체 브랜드에 대한 마케팅 허가를 보유하고 있다.[45]
마케팅 허가가 있는 하루 1회 공식에는 Advagraf(Astellas Pharma)와 Envarsus(Veloxis Pharmethics가 미국에서 Envarsus XR로 판매하고 Chiesi가 유럽에서 판매하는)가 있다.[45] 이러한 제형은 혈액 수준의 약동학적 변화를 줄이고 투약 준수를 용이하게 하기 위한 것이다.[citation needed]
주제제작은 레오파마가 프로토픽이라는 이름으로 시판하고 있다.[45]
생합성
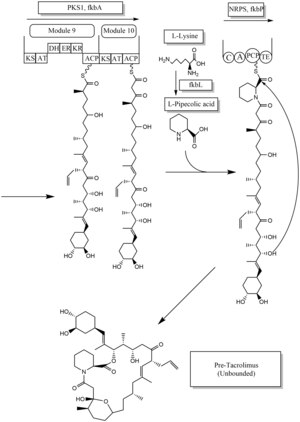
타크로리무스의 생합성은 타입 1 폴리케타이드 신시사이즈(PKS 1)와 비리보솜펩타이드 신디즈(NRPS)의 하이브리드 합성이다. 연구는 하이브리드 합성이 1종 폴리케타이드 신타아제의 10개 모듈과 비리보솜 펩타이드 신타아제의 1개 모듈로 구성되어 있다는 것을 보여준다. 타크로리무스를 위한 합성효소는 fkb라는 이름의 19개의 유전자 군집들에서 발견된다. 19개의 유전자는 fkbQ, fkbN, fkbM, fkbD, fkbA, fkbP, fkbO, fkbB, fkbC, fkbL, fkbK, fkbJ, fkbI, fkbH, fkbG, allD, allK, allK, allA이다.[46]
타크로리무스의 생합성에는 몇 가지 가능한 방법이 있다. 생합성을 위한 기본 단위는 다음과 같다: 시작단위로 4,5-dihydroxycylohex-1-eneckarboxylic acid, 4개의 malonyl-CoA, 5개의 methylmalonyl-CoA, 1개의 allimalonylonyl-CoA 분자. 그러나, 두 개의 악성 코아 분자는 두 개의 메톡시말론 코아 분자로 대체될 수 있다. 일단 두 개의 악성코닐-CoA 분자가 교체되면, 두 개의 메톡시말론 CoA 분자가 대체되는 곳에서 더 이상 사후 싱타아제 맞춤화 단계가 필요하지 않다. 아킬 캐리어 단백질에 대한 메톡시말로닐 CoA의 생합성은 5개의 효소(fkbG, fkbH, fkbI, fkbJ, fKBK)에 의해 진행된다. 알리엘말로닐코아(Alilmalonyl-CoA)도 프로피오닐말로닐코아(Propionylmalonyl-CoA)로 교체할 수 있다.[46]
초리기 단위인 초리스마산 DHC는 fkbO 효소에 의해 형성되어 CoA-ligase 도메인(CoL)에 로드된다. 그 후, NADPH 의존적 감소(ER)로 진행한다. Three enzymes, fkbA,B,C enforce processes from the loading module to the module 10, the last step of PKS 1. fkbB enzyme is responsible of allylmalonyl-CoA synthesis or possibly propionylmalonyl-CoA at C21, which it is an unusual step of general PKS 1. As mentioned, if two methoxymalonyl CoA molecules are substituted for two malonyl-CoA molecules, 그것들은 모듈 7과 8 (C13과 C15)에서 일어날 것이고, fkbA 효소가 이 과정을 시행할 것이다. PKS 1의 마지막 단계(모듈 10) 후, L-리신에서 L-파이프콜산 분자 1개가 형성되어 fkbL 효소를 통해 촉매 처리되어 모듈 10의 분자와 합성된다. L-파이프콜산 합성의 과정은 fkbP 효소에 의해 NRPS가 시행된다. 전체 서브유닛을 합성한 후 분자는 사이클링된다. 사이클화 후 프리타크로리무스 분자는 산화, S-adenosyl 메티오닌 등 사후 싱타아제 맞춤 단계를 거친다. 특히 fkbM 효소는 DHCHC 시동기 유닛(갈색으로 표시된 탄소 번호 31)의 알코올을 대상으로 한 알코올 메틸화를, fkbD 효소는 C9(녹색으로 퇴적)을 담당한다. 이러한 맞춤화 단계를 거친 후 타크로리무스 분자는 생물학적으로 활동하게 된다.[46][47][48]
리서치
루푸스신염
타크로리무스는 루푸스신염에서 신장기능의 해소를 증가시키면서 심각한 감염의 위험을 감소시키는 것으로 나타났다.[49][50]
궤양성대장염
타크롤리무스는 염증성 장질환의 일종인 궤양성 대장염(UC)과 관련된 염증을 억제하기 위해 사용되어 왔다. 비록 거의 전적으로 실험 사례에서만 사용되지만, 타크로리무스는 UC의 플레어 억제에 상당히 효과적인 것으로 나타났다.[51][52]
참조
- ^ "Tacrolimus Use During Pregnancy". Drugs.com. 3 October 2019. Retrieved 29 April 2020.
- ^ "Prograf- tacrolimus capsule, gelatin coated Prograf- tacrolimus injection, solution Prograf- tacrolimus granule, for suspension". DailyMed. Retrieved 16 July 2021.
- ^ "Advagraf EPAR". European Medicines Agency. Retrieved 16 July 2021.
- ^ "Protopic EPAR". European Medicines Agency. Retrieved 16 July 2021.
- ^ Berdoulay A, English RV, Nadelstein B (2005). "Effect of topical 0.02% tacrolimus aqueous suspension on tear production in dogs with keratoconjunctivitis sicca". Veterinary Ophthalmology. 8 (4): 225–32. doi:10.1111/j.1463-5224.2005.00390.x. PMID 16008701.
- ^ "Tacrolimus for Dogs and Cats".
- ^ Baldo A, Cafiero M, Di Caterino P, Di Costanzo L (January 2009). "Tacrolimus ointment in the management of atopic dermatitis". Clin Cosmet Investig Dermatol. 2: 1–7. doi:10.2147/ccid.s3378. PMC 3047924. PMID 21436963.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ a b McCauley, Jerry (19 May 2004). "Long-Term Graft Survival In Kidney Transplant Recipients". Slide Set Series on Analyses of Immunosuppressive Therapies. Medscape. Retrieved 6 June 2006.
- ^ Haddad EM, McAlister VC, Renouf E, Malthaner R, Kjaer MS, Gluud LL (October 2006). McAlister V (ed.). "Cyclosporin versus tacrolimus for liver transplanted patients". The Cochrane Database of Systematic Reviews. 4 (4): CD005161. doi:10.1002/14651858.CD005161.pub2. PMID 17054241.
- ^ O'Grady JG, Burroughs A, Hardy P, Elbourne D, Truesdale A (October 2002). "Tacrolimus versus microemulsified ciclosporin in liver transplantation: the TMC randomised controlled trial". Lancet. 360 (9340): 1119–25. doi:10.1016/S0140-6736(02)11196-2. PMID 12387959. S2CID 10417106.
- ^ Lee MN, Butani L (June 2007). "Improved pharmacokinetic monitoring of tacrolimus exposure after pediatric renal transplantation". Pediatric Transplantation. 22 (4): 388–93. doi:10.1111/j.1399-3046.2006.00618.x. PMID 17493218. S2CID 23530214.
- ^ a b Haberfeld, H, ed. (2015). Austria-Codex (in German). Vienna: Österreichischer Apothekerverlag. Protopic.
- ^ Silverberg NB, Lin P, Travis L, Farley-Li J, Mancini AJ, Wagner AM, Chamlin SL, Paller AS (November 2004). "Tacrolimus ointment promotes repigmentation of vitiligo in children: a review of 57 cases". Journal of the American Academy of Dermatology. 51 (5): 760–6. doi:10.1016/j.jaad.2004.05.036. PMID 15523355.
- ^ a b c d e f g h Haberfeld, H, ed. (2015). Austria-Codex (in German). Vienna: Österreichischer Apothekerverlag. Prograf.
- ^ Fukatsu S, Fukudo M, Masuda S, Yano I, Katsura T, Ogura Y, Oike F, Takada Y, Inui K (April 2006). "Delayed effect of grapefruit juice on pharmacokinetics and pharmacodynamics of tacrolimus in a living-donor liver transplant recipient". Drug Metabolism and Pharmacokinetics. 21 (2): 122–5. doi:10.2133/dmpk.21.122. PMID 16702731.
- ^ Naesens M, Kuypers DR, Sarwal M (February 2009). "Calcineurin inhibitor nephrotoxicity" (PDF). Clinical Journal of the American Society of Nephrology. 4 (2): 481–508. doi:10.2215/CJN.04800908. PMID 19218475.
- ^ Miwa Y, Isozaki T, Wakabayashi K, Odai T, Matsunawa M, Yajima N, Negishi M, Ide H, Kasama T, Adachi M, Hisayuki T, Takemura T (2008). "Tacrolimus-induced lung injury in a rheumatoid arthritis patient with interstitial pneumonitis". Modern Rheumatology. 18 (2): 208–11. doi:10.1007/s10165-008-0034-3. PMID 18306979. S2CID 39537409.
- ^ O'Donnell MM, Williams JP, Weinrieb R, Denysenko L (2007). "Catatonic mutism after liver transplant rapidly reversed with lorazepam". General Hospital Psychiatry. 29 (3): 280–1. doi:10.1016/j.genhosppsych.2007.01.004. PMID 17484951.
- ^ "Key Statistics for Non-Hodgkin Lymphoma". www.cancer.org. Retrieved 19 February 2020.
- ^ Hanifin JM, Paller AS, Eichenfield L, Clark RA, Korman N, Weinstein G, Caro I, Jaracz E, Rico MJ (August 2005). "Efficacy and safety of tacrolimus ointment treatment for up to 4 years in patients with atopic dermatitis". Journal of the American Academy of Dermatology. 53 (2 Suppl 2): S186–94. doi:10.1016/j.jaad.2005.04.062. PMID 16021174.
- ^ N H Cox & Catherine H Smith (December 2002). "Advice to dermatologists re topical tacrolimus" (PDF). Therapy Guidelines Committee. British Association of Dermatologists. Archived from the original (PDF) on 13 December 2013.
- ^ William F. Ganong (8 March 2005). Review of medical physiology (22nd ed.). Lange medical books. p. 530. ISBN 978-0-07-144040-0.
- ^ Liu J, Farmer JD, Lane WS, Friedman J, Weissman I, Schreiber SL (August 1991). "Calcineurin is a common target of cyclophilin-cyclosporin A and FKBP-FK506 complexes". Cell. 66 (4): 807–15. doi:10.1016/0092-8674(91)90124-H. PMID 1715244. S2CID 22094672.
- ^ Abou-Jaoude MM, Najm R, Shaheen J, Nawfal N, Abboud S, Alhabash M, Darwish M, Mulhem A, Ojjeh A, Almawi WY (September 2005). "Tacrolimus (FK506) versus cyclosporine microemulsion (neoral) as maintenance immunosuppression therapy in kidney transplant recipients". Transplantation Proceedings. 37 (7): 3025–8. doi:10.1016/j.transproceed.2005.08.040. PMID 16213293.
- ^ a b Dinnendahl, V; Fricke, U, eds. (2003). Arzneistoff-Profile (in German). Vol. 9 (18 ed.). Eschborn, Germany: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ Bains, Ripudaman Kaur. "Molecular diversity and population structure at the CYP3A5 gene in Africa" (PDF). University College London. Retrieved 13 June 2016.
- ^ Staatz CE, Tett SE (2004). "Clinical pharmacokinetics and pharmacodynamics of tacrolimus in solid organ transplantation". Clinical Pharmacokinetics. 43 (10): 623–53. doi:10.2165/00003088-200443100-00001. PMID 15244495. S2CID 33877550.
- ^ Staatz CE, Goodman LK, Tett SE (March 2010). "Effect of CYP3A and ABCB1 single nucleotide polymorphisms on the pharmacokinetics and pharmacodynamics of calcineurin inhibitors: Part I". Clinical Pharmacokinetics. 49 (3): 141–75. doi:10.2165/11317350-000000000-00000. PMID 20170205. S2CID 28346861.
- ^ Staatz CE, Goodman LK, Tett SE (April 2010). "Effect of CYP3A and ABCB1 single nucleotide polymorphisms on the pharmacokinetics and pharmacodynamics of calcineurin inhibitors: Part II". Clinical Pharmacokinetics. 49 (4): 207–21. doi:10.2165/11317550-000000000-00000. PMID 20214406. S2CID 27047235.
- ^ Barbarino JM, Staatz CE, Venkataramanan R, Klein TE, Altman RB (October 2013). "PharmGKB summary: cyclosporine and tacrolimus pathways". Pharmacogenetics and Genomics. 23 (10): 563–85. doi:10.1097/fpc.0b013e328364db84. PMC 4119065. PMID 23922006.
- ^ Benkali K, Prémaud A, Picard N, Rérolle JP, Toupance O, Hoizey G, Turcant A, Villemain F, Le Meur Y, Marquet P, Rousseau A (1 January 2009). "Tacrolimus population pharmacokinetic-pharmacogenetic analysis and Bayesian estimation in renal transplant recipients". Clinical Pharmacokinetics. 48 (12): 805–16. doi:10.2165/11318080-000000000-00000. PMID 19902988. S2CID 19900291.
- ^ Choi Y, Jiang F, An H, Park HJ, Choi JH, Lee H (January 2017). "A pharmacogenomic study on the pharmacokinetics of tacrolimus in healthy subjects using the DMETTM Plus platform". The Pharmacogenomics Journal. 17 (1): 105–106. doi:10.1038/tpj.2016.85. PMID 27958377.
- ^ Hatanaka H, Iwami M, Kino T, Goto T, Okuhara M (November 1988). "FR-900520 and FR-900523, novel immunosuppressants isolated from a Streptomyces. I. Taxonomy of the producing strain". The Journal of Antibiotics. 41 (11): 1586–91. doi:10.7164/antibiotics.41.1586. PMID 3198493.
- ^ Kino T, Hatanaka H, Hashimoto M, Nishiyama M, Goto T, Okuhara M, Kohsaka M, Aoki H, Imanaka H (September 1987). "FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics". The Journal of Antibiotics. 40 (9): 1249–55. doi:10.7164/antibiotics.40.1249. PMID 2445721.
- ^ Pritchard DI (May 2005). "Sourcing a chemical succession for cyclosporin from parasites and human pathogens". Drug Discovery Today. 10 (10): 688–91. doi:10.1016/S1359-6446(05)03395-7. PMID 15896681. 팀 정보가 아닌 소스 유기체 지원
- ^ Ponner, B, Cvach, B (후지사와 제약회사) : 프로토픽 업데이트 2005
- ^ "Prograf: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 29 April 2020.
- ^ "Prograf: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 29 April 2020.
- ^ 타크로리무스 (Systemic) 모노그래프. 2021-12-16에 접속.
- ^ "Tacrolimus: FDA-Approved Drugs". U.S. Food and Drug Administration (FDA). Retrieved 29 April 2020.
- ^ "Protopic EPAR". European Medicines Agency (EMA). Retrieved 29 April 2020.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ "Advagraf EPAR". European Medicines Agency (EMA). Retrieved 29 April 2020.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ "Modigraf EPAR". European Medicines Agency (EMA). Retrieved 29 April 2020.
- ^ a b c Joint Formulary Committee. "British National Formulary (online)". London: BMJ Group and Pharmaceutical Press. Retrieved 24 September 2015.
- ^ a b c Ordóñez-Robles M, Santos-Beneit F, Martín JF (May 2018). "omic Approaches". Antibiotics. 7 (2): 39. doi:10.3390/antibiotics7020039. PMC 6022917. PMID 29724001.
- ^ Chen D, Zhang L, Pang B, Chen J, Xu Z, Abe I, Liu W (May 2013). "FK506 maturation involves a cytochrome p450 protein-catalyzed four-electron C-9 oxidation in parallel with a C-31 O-methylation". Journal of Bacteriology. 195 (9): 1931–9. doi:10.1128/JB.00033-13. PMC 3624582. PMID 23435975.
- ^ Mo S, Ban YH, Park JW, Yoo YJ, Yoon YJ (December 2009). "Enhanced FK506 production in Streptomyces clavuligerus CKD1119 by engineering the supply of methylmalonyl-CoA precursor". Journal of Industrial Microbiology & Biotechnology. 36 (12): 1473–82. doi:10.1007/s10295-009-0635-7. PMID 19756799. S2CID 32967249.
- ^ Singh JA, Hossain A, Kotb A, Wells G (September 2016). "Risk of serious infections with immunosuppressive drugs and glucocorticoids for lupus nephritis: a systematic review and network meta-analysis". BMC Medicine. 14 (1): 137. doi:10.1186/s12916-016-0673-8. PMC 5022202. PMID 27623861.
- ^ Singh, Jasvinder A.; Hossain, Alomgir; Kotb, Ahmed; Wells, George A. (2016). "Comparative effectiveness of immunosuppressive drugs and corticosteroids for lupus nephritis: a systematic review and network meta-analysis". Systematic Reviews. 5 (1): 155. doi:10.1186/s13643-016-0328-z. ISSN 2046-4053. PMC 5020478. PMID 27619512.
- ^ Baumgart DC, Pintoffl JP, Sturm A, Wiedenmann B, Dignass AU (May 2006). "Tacrolimus is safe and effective in patients with severe steroid-refractory or steroid-dependent inflammatory bowel disease--a long-term follow-up". The American Journal of Gastroenterology. 101 (5): 1048–56. PMID 16573777.
- ^ Baumgart DC, Macdonald JK, Feagan B (July 2008). Baumgart DC (ed.). "Tacrolimus (FK506) for induction of remission in refractory ulcerative colitis". The Cochrane Database of Systematic Reviews. 16 (3): CD007216. doi:10.1002/14651858.CD007216. PMID 18646177.
추가 읽기
- Lv X, Qi J, Zhou M, et al. (March 2020). "Comparative efficacy of 20 graft-versus-host disease prophylaxis therapies for patients after hematopoietic stem-cell transplantation: A multiple-treatments network meta-analysis". Crit. Rev. Oncol. Hematol. 150: 102944. doi:10.1016/j.critrevonc.2020.102944. PMID 32247246. S2CID 214794350.
외부 링크
- "Tacrolimus". Drug Information Portal. U.S. National Library of Medicine.
- "Tacrolimus Injection". MedlinePlus.
- "Tacrolimus Topical". MedlinePlus.
- 미국 국립 의학 도서관의 타크로리무스(Tacrolimus) 의료 과목 제목(MesH)
- "FDA Approves New Use of Transplant Drug Based on Real-World Evidence". U.S. Food and Drug Administration (FDA). 30 September 2021.