IPTVO
IPTBO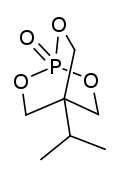 | |
 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 4-(Propan-2-yl)-2,6,7-trioxa-1λ-phosphabyclo5[2.2.2]옥탄-1-1 | |
| 기타 이름 4-이소프로필비시클로인산염 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
펍켐 CID | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C7H13O4P | |
| 어금질량 | 192.168 g·190−1 |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 | 극독성 |
| 치사량 또는 농도(LD, LC): | |
LD50(중간 선량) | 180 μg/kg (mice)[1] |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
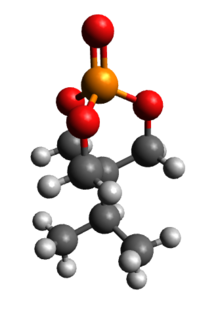
IPTBO(이소프로필비시클로인산염, 또한 IPO[2])는 자전거로 인산염 경련제다.[3] 쥐에게 격렬한 경련을 일으킬 수 있는 극도로 강력한 GABA 수용체 길항제다.[4][5]
IPTBO는 매우 독성이 강한 자전거 인산염 그룹에서 발견된다. 일반적으로 자전거용 인산염은 GABA 수용체를 통한 염화이온 흐름을 방해하여 CNS 과다 자극과 몇 분 내에 치명적인 경련을 일으킨다. IPTBO는 주입, 흡입 또는 섭취 시 이러한 효과를 가지며, 이 길항제 중 독성이 더 강한 유형 중 하나이다.[6]
디스커버리
IPTBO의 파생상품은 분광학적 연구와 (산화반응을 종결시키는 능력 때문에) 난연제, 비닐 수지 안정제, 항산화제로 사용된다. 그것은 이전에 평면 엔진 윤활유로도 사용되었고, "에어로톡스 증후군"[7]에 기여했다.
일반적으로 독성인 에스테르는 살충제나 화학무기(DFP 등)[8]로 사용되지만 대부분의 인 에스테르와 달리 IPTBO는 아세틸콜린세테라제를 억제하지 않는다. IPTBO와 기타 유사한 화합물은 모두 2,6,7-트리옥사-포스파비시클로[2,2]옥탄의 유도체로, 가장 독성이 강한 화합물은 4개의 알킬 그룹을 대체한다. 이 화합물의 중요성은 여전히 연구 대상이며 아데노신 3,5'-모노인산염(즉, 주기성 AMP)에 대한 이 화합물의 구조적 유사성과 다른 알려진 유기인산 독성물질과는 다른 메커니즘을 통한 독성 능력이 연구에 대한 관심의 대상이 되고 있다.[9][7]
합성
IPTBO는 많은 반응 경로를 통해 합성될 수 있다. 모든 합성 경로는 이소프로필 트롤(간극에 3개의 히드록실 그룹이 부착된 이소프로필 그룹)과 "케이드(caged)"되어야 하는 인 시약(즉, 산소 분자로 둘러싸인)의 첨가로 시작하도록 기술되어 있다.[9] 이 특정한 실험은 IPTBO의 다양한 준비 방법에 대한 화학적 귀인 표지를 연구했다. IPTBO를 생산하는 무수한 방법들은 또한 불순물이나 분해물을 포함할 수 있는 많은 다른 측면 제품들의 생산으로 이어진다. 알려진 귀인 인자는 회수된 물질을 생산 방법으로 표시하는 데 사용될 수 있으며, 이는 법의학 연구에 도움이 될 수 있다. IPTBO를 위한 5가지 1차 생산 방법이 있다. 그들은 모두 삼합집단으로 시작하지만 인을 함유하는 화합물에서는 차이가 있다.
기능 및 메커니즘
IPTBO의 주요 기능은 염화 이온이 GABA 수용체에 위치한 이온 채널로 들어가는 것을 차단해 소뇌의 억제제로서 기능하는 것을 근본적으로 막는 것이다. 심층적으로 GABA의 정상적인 결합 메커니즘은 염화 이온에 의존하고 있으며, 염화 이온은 수용체 부지에 대한 H-플유닛라제팜의 결합을 자극하여 GABA에서 더 많은 결합 부위를 이용할 수 있게 한다. IPTBO는 염화 채널을 차단함으로써 이러한 효과에 대응하며, 따라서 H-Flunitrazepam과 GABA의 결합을 방해한다.[10]
구체적으로, IPTVO는 GABAA 수용체를 방해한다. 이 수용체는 GABA에 의해 활성화되며 중추신경계에서 주요 억제 신경전달물질로 작용한다. GABA의 수용체 결합을 통해 활성화되면 염화 이온은 수용체의 모공을 통해 전도된다. 내부 전하가 휴면전위 이하일 때 염화 이온이 유입되고, 휴면전위 이상일 때 염화 이온이 흘러나온다. 이렇게 되면 신경전달에 필요한 내적 전하의 축적이 중단되고, 따라서 작용 전위를 차단하여 신경계에 억제 효과를 초래하게 된다.[11][12]
IPTBO는 경련제와 흥분제 둘 다로서, 본질적으로 뇌에 화학적 신호의 과부하를 유발하고 신경세포의 과열을 유발한다. IPTBO는 뉴런에서 비정상적으로 많은 양의 과열을 유발하기 때문에 GABA는 더 이상 내부 전하의 축적을 막을 수 없어 경련을 유발한다. IPTBO는 비경쟁 GABA 길항제로서 GABA의 수용체 부위와 결합하지 않고 대신 수용체의 물리적 채널에서 염화물이온 흐름을 방해하여 알로스테릭 길항제 역할을 한다. IPTBO는 채널 밖으로 나가는 염화 이온 흐름을 방해하여 전하 축적과 신호 교란을 야기할 뿐만 아니라 뉴런에 과대중화를 유발한다. 뉴런의 과다복용과 염화물이온 억제 모두 경련을 일으킨다.[8]
IPTBO의 기능은 주기성 AMP와 주기성 GMP의 두 가지 물질과 관련이 있다. 각각 세포내 신호 전달의 작용제 역할을 하는 ATP와 GTP의 파생물이다. 마우스에 대한 다양한 IPTBO 선량을 테스트함으로써, 연구원들은 AMP와 GMP 레벨에 대한 해당 효과를 연구할 수 있었다. 모든 선량에 대한 GMP 수준은 비교적 유사했다. 그들은 투약 후 스파이크를 올렸지만, 각각의 복용량은 비슷한 크기의 스파이크를 생성했다. .06 마이크로그램 투여 후 AMP 레벨이 정상보다 감소했고, 이후 모든 큰 용량에 대해 증가하였다. AMP와 GMP는 모두 GABA 수용체 내 염화 이온 채널과 같이 이온 채널의 기능을 조절하는 AMP와의 세포외 상호작용에 의해 발생하는 2차 메신저와 세포내 신호 분자다. AMP는 또한 뇌와 심장의 HCN(공백기 채널)을 조절한다. HCN은 뉴런들이 시냅스 활동에 어떻게 반응하는지를 통제하고 운동 기능에 대한 충동을 전달할 수 있다(HCN 채널이 또 다른 경련 장애인 간질에 영향을 미칠 수 있다는 것을 보여주는 증거가 존재한다).[13]
참고 항목
참조
- ^ Milbrath, Dean S.; Engel, Judith L.; Verkade, John G.; Casida, John E. (February 1979). "Structure-toxicity relationships of 1-substituted-4-alkyl-2,6,7-trioxabicyclo[2.2.2.]octanes". Toxicology and Applied Pharmacology. 47 (2): 287–293. doi:10.1016/0041-008x(79)90323-5. PMID 452023.
- ^ Mendelson, Wallace B.; Martin, Joseph V.; Wagner, Richard; Roseberry, Cynthia; Skolnick, Phil; Weissman, Ben Avi; Squires, Richard (January 1985). "Are the toxicities of pentobarbital and ethanol mediated by the GABA-benzodiazepine receptor-chloride ionophore complex?". European Journal of Pharmacology. 108 (1): 63–70. doi:10.1016/0014-2999(85)90283-3.
- ^ Mattsson, Hillevi (1980). "Bicyclic phosphates increase the cyclic GMP level in rat cerebellum, presumably due to reduced GABA inhibition". Brain Research. 181 (1): 175–84. doi:10.1016/0006-8993(80)91267-6. PMID 6243222. S2CID 614578.
- ^ Mattsson, Hillevi (1980). "The effect of various drug pretreatments on the convulsions and cerebellar cyclic nucleotide changes induced by the convulsant 4-isopropyl-2,6,7-trioxa-1-phosphatbicyclo(2,2,2)octane-1-oxide(IPTBO)". Brain Research. 181 (1): 175–84. doi:10.1016/0006-8993(80)91267-6. PMID 6243222. S2CID 614578.
- ^ Blenkinsop, I.S; Coult, D.B; Davies, W.E; Howells, D.J (1984). "Effects of dose and time after administration of 4-isopropyl-2,6,7-trioxa-1-phosphabicyclo (2,2,2)octane-1-oxide (IPTBO) on cyclic nucleotide concentrations in mouse cerebellum". Neurochemistry International. 6 (4): 453–7. doi:10.1016/0197-0186(84)90114-1. PMID 20488068. S2CID 22319459.
- ^ Lorkea, Dietrich E.; Stegmeier-Petroianu, Anka; Petroianu, Georg A. (July 1, 2016). "Biologic activity of cyclic and caged phosphates: a review". Journal of Applied Toxicology. 2017 (37): 13–22. doi:10.1002/jat.3369. PMID 27612208. S2CID 1756643.
- ^ a b Costa, Lucio G. (Dec 7, 2017). "Organophosphorus Compounds at 80: Some Old and New Issues". Toxicological Sciences. 162 (1): 24–35. doi:10.1093/toxsci/kfx266. PMC 6693380. PMID 29228398.
- ^ a b Bellet, Eugene M.; Casida, John E. (Dec 14, 1973). "Bicyclic Phosphorus Esters: High Toxicity without Cholinesterase Inhibition". Science. 182 (4117): 1135–1136. Bibcode:1973Sci...182.1135B. doi:10.1126/science.182.4117.1135. JSTOR 1737024. PMID 4356280. S2CID 9462533.
- ^ a b Mazzitelli, Carolyn L.; Re, Michael A.; Reaves, Melissa A.; Acevedo, Carlos A.; Straight, Stephen D.; Chipuk, Joseph E. (June 23, 2012). "A Systematic Method for the Targeted Discovery of Chemical Attribution Signatures: Application to Isopropyl Bicyclophosphate Production". Analytical Chemistry. 84 (15): 6661–6671. doi:10.1021/ac300859j. PMID 22725731.
- ^ Karobath, Manfred; Drexler, Gerhard; Supavilai, Porntip (19 January 1981). "Modulation by picrotoxin and IPTBO of 3H-flunitrazepam binding to the GABA/benzodiazepine receptor complex of rat cerebellum". Life Sciences. 28 (3): 307–313. doi:10.1016/0024-3205(81)90738-4. PMID 6111726.
- ^ Bowery, N.G.; Collins, J.F.; Hill, R.G.; Pearson, S. (April 1976). "GABA antagonism as a possible basis for the convulsant action of a series of bicyclic phosphorus esters". Proceedings of the B.P.S. 1–2 (3): 435–436. PMC 1667265. PMID 10031.
- ^ Coult, D.B.; Howells, D.J.; Smith, A.P. (1979). "Cyclic nucleotide concentrations in the brains of mice treated with the convulsant bicyclic organophosphate, 4-isopropyl-2,6,7-trioxa-1 -phosphabicyclo[2,2,2] octane". Biochemical Pharmacology. 28 (2): 193–196. doi:10.1016/0006-2952(79)90502-1. PMID 218587.
- ^ Wang, Jing; Chen, Shan; Nolan, Matthew F.; Siegelbaum, Steven A. (October 24, 2002). "Activity-Dependent Regulation of HCN Pacemaker Channels by Cyclic AMP". Neuron. 36 (3): 451–461. doi:10.1016/S0896-6273(02)00968-6. PMID 12408847. S2CID 2568491. Retrieved 20 May 2019.