데메콜신
Demecolcine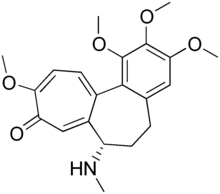 | |
 | |
| 임상자료 | |
|---|---|
| 기타 이름 | 콜체미드 |
| ATC 코드 | |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 켐스파이더 | |
| 유니 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.006.832 |
| 화학 및 물리적 데이터 | |
| 공식 | C21H25NO5 |
| 어금질량 | 371.433 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
| (iii) | |
데메콜신(INN; colcemid라고도 함)은 화학요법에 사용되는 약물이다.아미노 모이에 있는 아세틸 그룹을 메틸로 대체하는 천연 알칼로이드 콜치약과 밀접한 관련이 있지만 독성이 적다.미세 관을 분해하고 미세관 형성을 제한하여(축간섬유 형성을 불활성화함) 은유에서 세포를 고정시켜 세포 수확과 카리오타이핑을 할 수 있게 한다.
세포분열 중 데메콜신은 스핀들 형성을 억제하여 은유효소에서 유사분열을 억제한다.의학적으로 데메콜신은 세포 주기의 방사선에 민감한 단계인 은유효소에서 종양 세포를 동기화함으로써 암 방사선 치료의 결과를 향상시키는데 이용되어 왔다.[1]
동물 복제 절차에서 데메콜신은 난자가 핵을 분출하게 하여 새로운 핵을 삽입할 공간을 만든다.[2]
작용기전
데메콜신은 빈블라스틴과 같은 미세관절하제다.그것은 두 가지 뚜렷한 메커니즘에 의해 작용한다.매우 낮은 농도에서는 마이크로튜브와 엔드에 결합하여 마이크로튜브의 역학을 억제한다.[3]최근의 연구는 고농도 데메콜신에서 미세관 조직 센터에서 미세관 분리를 촉진할 수 있다는 것을 발견했다.보호되지 않은 단부를 뺀 분리된 마이크로튜브 시간 경과에 따라 탈고함.세포의 세포독성은 미세관 분리와 더 잘 상관관계가 있는 것 같다.[4]농도가 낮아지면 미세관 역학 및 세포이동에 영향을 미친다.[4]
연구용도
데메콜신은 세포의 과학적 연구에 사용된다.다양한 방법으로 사용되지만, 최근까지 세포의 유사분열 연구에 주로 사용되었다.예를 들어, 마이크로튜브는 세포의 분열에 필요하다.더 중요한 것은 M상에서의 염색체의 움직임이다.미세관절의 데메콜신 억제는 미세관절들이 떨어져 나가거나 억제된 미생물 세포에서 무우플로이드를 유발하여 염색체를 딸세포로 끌어당기는 기능을 완성할 수 있게 되는데, 염색체의 비접합이라고도 한다.[5]디메콜신은 용량에 따라 미분해 발생 시 미세핵에서 염색체의 DNA 파편을 유발하는 것으로도 밝혀졌다.[6]
참조
- ^ Sutton M (February 1965). "Superior Mediastinal Obstruction Treated with Demecolcine Followed by Radiotherapy". British Medical Journal. 1 (5433): 495–6. doi:10.1136/bmj.1.5433.495. PMC 2165889. PMID 14238680.
- ^ Hou J, Lei T, Liu L, Cui X, An X, Chen Y (2006). "Demecolcine-induced enucleation of sheep meiotically maturing oocytes". Reproduction, Nutrition, Development. 46 (2): 219–26. doi:10.1051/rnd:2006002. PMID 16597428.
- ^ Jordan MA, Wilson L (April 2004). "Microtubules as a target for anticancer drugs". Nature Reviews. Cancer. 4 (4): 253–65. doi:10.1038/nrc1317. PMID 15057285. S2CID 10228718.
- ^ a b Yang H, Ganguly A, Cabral F (October 2010). "Inhibition of cell migration and cell division correlates with distinct effects of microtubule inhibiting drugs". The Journal of Biological Chemistry. 285 (42): 32242–50. doi:10.1074/jbc.M110.160820. PMC 2952225. PMID 20696757.
- ^ Hashimoto K, Todo T (July 2013). "Mitotic slippage underlies the relationship between p53 dysfunction and the induction of large micronuclei by colcemid". Mutagenesis. 28 (4): 457–64. doi:10.1093/mutage/get021. PMID 23702691.
- ^ Yamamoto M, Wakata A, Aoki Y, Miyamae Y, Kodama S (April 2014). "Chromosome loss caused by DNA fragmentation induced in main nuclei and micronuclei of human lymphoblastoid cells treated with colcemid". Mutation Research. 762: 10–6. doi:10.1016/j.mrfmmm.2014.02.002. PMID 24582839.


