자피루카스트
Zafirlukast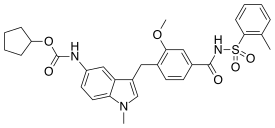 | |
 | |
| 임상 데이터 | |
|---|---|
| 상호 | 아콜레이트[1] |
| AHFS/Drugs.com | 모노그래프 |
| Medline Plus | a697007 |
| 라이선스 데이터 |
|
| 임신 카테고리 |
|
| 루트 행정부. | 오랄 |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 |
|
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 알 수 없는 |
| 단백질 결합 | 99 % > (알부민)[1] |
| 대사 | 간(CYP2C9 매개) |
| 대사물 | 히드록실화 대사물[1] |
| 반감기 제거 | 10시간 |
| 배설물 | 분변[1] |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.189.989 |
| 화학 및 물리 데이터 | |
| 공식 | C31H33N3O6S |
| 몰 질량 | 575.68g/120−1 |
| 3D 모델(JSmol) | |
| 녹는점 | 138 ~ 140 °C (280 ~284 °F) |
| |
| |
| (표준) | |
자필루카스트는 경구 투여된 류코트리엔 수용체 길항제(LTRA)로 천식의 만성 치료에 사용된다.자필루카스트는 일반적으로 잘 견디지만 두통과 배탈이 자주 발생한다.간 기능 부전과 같이 생명을 위협하는 몇 가지 드문 부작용이 발생할 수 있습니다.Churg-Strauss 증후군은 자필루카스트와 관련이 있지만, 그 관계가 본질적으로 원인이라고 생각되지는 않는다.자필루카스트 과다 복용은 자가 제한적인 경향이 있다.
자필루카스트는 다른 LTRA와 마찬가지로 면역체계를 억제함으로써 작용한다.자필루카스트는 폐의 염증세포에 작용함으로써 천식의 병인과 관련된 염증 매개물질의 생성을 감소시킨다.자필루카스트는 CYP2C9라는 효소에 의해 간에서 광범위하게 대사된다. 자필루카스트는 CYP3A4의 작용을 억제하여 CYP3A4에 의해 대사되는 다른 약물과 약물 상호작용을 일으킨다.LTC4 합성효소와 CYP2C9의 유전적 차이는 사람이 자필루카스트 치료에 어떻게 반응하는지를 예측할 수 있다.
Zafirlukast(상표명 Accolate)는 미국에서 승인된 최초의 시스테닐 류코트리엔 수용체 길항제였다.그것은 현재 다른 많은 나라에서 다른 브랜드 이름으로 승인되어 있다.
의료 용도
Zafirlukast는 5세 [1]이상 성인 및 아동의 천식 예방 및 치료에 대해 FDA 승인을 받았습니다.다른 류코트리엔 수용체 길항제들과 마찬가지로, 자필루카스트는 천식의 장기 치료에 유용하다고 생각되지만, 일반적으로 단일 요법(관리 표준) 또는 복합 [2]요법의 장기 작용 베타-2 작용제보다 효과가 낮다.특히 자필루카스트는 급성 천식 [1]발작 시 효과가 없다.
이용 가능한 폼
자필루카스트에는 연령 조정으로 유명한 두 가지 복용 형태가 있습니다.20mg 태블릿은 12세 이상의 성인 및 어린이를 위한 것이고, 10mg 태블릿은 5세에서 [1]12세 사이의 어린이를 위한 것입니다.태블릿은 실온, 직사광선, [1]수분 공급원으로부터 멀리 떨어진 곳에 보관해야 합니다.
알약은 [1]경구 투여 전용입니다.
특정 모집단
소아과
일반적으로 자필루카스트와 같은 류코트리엔 수용체 길항제들은 아토피가 [3]적고 어린 아이들에게 더 효과적이다.아토피는 천식, 꽃가루 알레르기, [4]습진을 포함한 알레르기 질환이 발병하는 성향을 말한다.
노인학
자필루카스트의 간 클리어런스는 65세 이상 성인의 경우 손상되어 최대 혈장 농도와 곡선 아래의 총 면적이 2~3배 증가하였다.Zafirlukast는 감염 위험을 증가시킬 수 있다(각각 7.0% 대 2.9%, Zafirlukast 대 플라시보 발생률), 특히 노인에서 낮은 기도 감염의 위험을 증가시킬 수 있다(예상된 감염은 [1]심각하지 않음).
임신
Zafirlukast는 "임신 범주 B"로 간주됩니다.이것은 부분적으로 기형 발생성을 조사하는 동물 연구에서 자필루카스트의 넓은 안전 여유에 기인한다.사이노몰구스 원숭이의 일일 최대 권장 경구 투여량의 20배에 해당하는 2000mg/kg/일 용량에서 기형 유발성이 관찰되지 않았다.그러나, 용량 자체는 모성 [1]독성이었지만 사이노몰구스 원숭이에서 일일 2000mg/kg의 속도로 자발적 낙태가 발생했다.
수유
모유 [5]수유를 하는 여성들에게 자필루카스트의 사용에 대한 연구는 제한적이다.제조자의 데이터에 따르면, 모유 수유 시 산모 체중 조정 선량의 0.6%가 모유 수유 시에 도달할 것으로 예상된다.[5]
신장 장애
신장 장애는 자필루카스트의 [1]약동학적 프로파일에 영향을 주지 않는 것으로 보인다.
간장애
자필루카스트의 간 클리어런스는 심각한 간 장애로 인해 손상됩니다.간경변은 최대 혈장 농도와 곡선 아래의 총 면적(약물 노출의 척도)을 50-60%[1] 증가시킬 수 있다.
금지 사항
자필루카스트는 [1]과민증이나 알레르기가 있는 사람에게는 금물이다.
부작용
자필루카스트는 일반적으로 잘 견디지만 두통과 위장장애가 발생할 수 있습니다.두통의 발병률은 12~20%로, 이는 자필루카스트의 승인을 이끌어낸 연구에서 위약을 복용하는 환자에게서 발견되는 두통의 발병률과 유사하다.소화기 이상에는 메스꺼움, 위 불쾌감/통증 및 설사가 포함될 수 있습니다.비록 이것은 체내에 흡수되는 약물의 양을 극적으로 손상시킬 수 있지만,[6] 음식과 함께 자필루카스트를 복용함으로써 GI 불만은 줄어들 수 있다.
다른 흔한 부작용으로는 독감과 같은 증상, 수면 장애(이상한 꿈, 불면증), 환각, 낮의 [6]졸음 등이 있다.
신경정신과 효과
신경정신학적 부작용은 자필루카스트와 다른 LTRA의 사용으로 보고되었다.일부 부작용은 덜 심각한 반면(예: 비정상적 꿈), 다른 부작용은 더 심각하다(예: 환각, 떨림, 자살).이러한 효과는 시판 후 보고서를 통해 발견되었는데, 초기 실험은 신경정신학적 [7]부작용을 모니터링하도록 설계되지 않았기 때문이다.
간독성
자필루카스트는 또한 드물지만 급성 간 [8]손상과 같은 심각한 부작용을 일으킬 수 있다.자필루카스트 유도 간독성은 일반적으로 치료를 시작한 후 2-6개월 이내에 발생하지만, 자필루카스트 [8]시작 후 최대 13개월 후에 보고되었다.자필루카스트 유도 간독성은 피로, 메스꺼움, 우측 상부 사분면 통증을 포함한 다양한 간 손상 증상과 함께 어두운 소변, 황달 [8]및 가려움증을 특징으로 한다.간 효소 상승은 일반적이며, 그 패턴은 보통 급성 바이러스성 [8]간염과 유사한 간세포 손상을 반영한다.간독성이 어떻게 발생하는지는 불분명하지만, CYP2C9 효소를 통해 간에서 대사되기 때문에 자필루카스트의 대사 중간체 때문일 수 있다.이 경우 치명적일 수 있으며, 자필루카스트에 다시 노출되면 더 심각한 [8]부상을 입을 수 있습니다.자필루카스트를 동일한 등급(예: 몬텔루카스트) 또는 5-리폭시게나아제 억제제의 관련 등급의 다른 약물로 전환하려고 시도할 수 있지만 주의해야 한다.[8]
AstraZeneca의 "Dear Health Care Provider" 편지에 따르면 자필루카스트에 의해 유발되는 간독성은 [9]주로 여성들에게서 발생했다.
추르그-스트라우스 증후군
알레르기 혈관염과 육아종증으로 알려진 추르그-스트라우스 증후군의 몇몇 사례들은 자필루카스트, 몬텔루카스트, 프라누카스트, 그리고 다른 천식 [10]약물의 사용과 함께 보고되었다.Churg-Strauss 증후군이 발생할 때, 그것은 천식과 축농증, 만성 구강 코르티코스테로이드 사용, 그리고 코르티코스테로이드의 [10]테이퍼화와 함께 새로운 항아스마 치료의 최근 시작과 함께 발생하는 경향이 있다.자필루카스트 시작과 근접한 추르그-스트라우스 증상의 정확한 발병 원인은 알려지지 않았지만, 만성 코르티코스테로이드의 금단은 이전에 발견되지 않았던 질병을 "마스크를 풀어주는" 것으로 생각된다.[10]코르티코스테로이드 금단현상은 새로운 항아스마 약물(자필루카스트 등)을 시작할 때 종종 발생하기 때문에 드물지만 주목할 만한 [10]연관성을 설명합니다.Churg-Strauss 증후군이 급성 천식 [10]악화와 유사한 기도 폐쇄 증상을 유발할 수 있기 때문에 이러한 사례는 오진된 천식을 나타낼 수 있습니다.이러한 천식 같은 증상들이 자필루카스트에 의해 감소됨에 따라, 스테로이드가 [10]제공하는 광범위하고 항염증적인 커버리지의 부족으로 인해 Churg-Strauss의 증상들이 증가한다.
과다 복용
자필루카스트와 함께 보고된 최고 과다 복용량은 200mg이다.약물 과다복용 환자들은 모두 살아남았다.보고된 증상으로는 발진과 [1]배탈이 있었다.
상호 작용
약물-약물 상호작용
Zafirlukast는 간약물 대사효소 시토크롬 P450 패밀리 3 서브패밀리 A멤버 4(CYP3A4)[1]의 저해제이다.자필루카스트는 항응고제 약물인 와파린, 항간질제 약물인 페니트인과 [1]카르바마제핀과 같은 CYP3A4를 통해 대사되는 약물의 농도를 증가시킬 수 있다.
약물-식품 상호작용
자필루카스트의 경구흡수(바이오 어베이러빌리티)는 고지방 또는 고단백질 [1]식사와 함께 섭취할 경우 40% 감소한다.이러한 상호작용을 피하려면 빈속에 자필루카스트를 [6]복용해야 합니다.공복상태는 식사를 [1]하기 1시간 전 또는 2시간 후로 분류된다.
약리학
약역학
자필루카스트는 간질성 폐 대식세포([11]폐의 간질공간에서 작동하는 백혈구) 내에서 폐의 평활근 전반에 걸쳐 발견되는 수용체인 시스테닐류코트리엔 수용체 1(CysLT1)의 길항제이다.CystLT1은 아미노산 시스테인을 [2]포함하는 류코트리엔의 특정 등급에 대한 수용체이다.이러한 시스테이닐 류코트라이엔은 류코트라이엔 C4, 류코트라이엔 D4, 류코트라이엔 E4를 포함하며,[2] 모두 호산구, 호염기구, 폐 대식세포와 같은 염증 세포에 의해 생성된다.CysLT1에 대한 작용을 통해 이들 류코트라이엔은 폐의 기관지 [12]통로가 수축되어 [2]기관지 천식과 관련된 특징적인 반응성 기도 증상으로 이어질 수 있다.점액 클리어런스의 억제와 점액 분비 및 부종의 자극과 같은 류코트리엔의 다른 염증 방지 효과는 알레르기 [2]비염의 특징적인 증상(건초열이라고도[13] 불린다)에 역할을 하는 것으로 생각된다.이들 특정 류코트라이엔의 작용을 억제함으로써 자필루카스트는 류코트라이엔 매개 염증 [2]조건에 대해 항염증 효과를 발휘하는 것으로 생각된다.
약동학
흡수.
자필루카스트는 경구 투여 후 혈류로 빠르게 흡수되며, 투여 [1]후 3시간 이내에 최대 혈장 수치에 도달합니다.최고 혈장 수치는 [14]혈중 자필루카스트의 최대 농도입니다.
분배
자필루카스트는 신체 조직으로 적당히 분포되며, 겉으로 보기에 안정된 상태의 분포 부피는 [1]70리터입니다.자필루카스트는 혈장단백질 결합이 높고 알부민과 [1]99% 결합되어 있습니다.알부민은 인간의 혈장에서 발견되는 가장 풍부한 단백질이며 약물을 [15]몸 전체에 운반하고 운반할 수 있습니다.체내 연구에 따르면 자필루카스트는 혈액-뇌 장벽 [1]침투율이 낮은 것으로 나타났다.혈액-뇌 장벽은 많은 화학물질이 [16]뇌로 들어가는 것을 막는 보호 시스템이다.
대사
Zafirlukast는 비활동 대사물로 [1]광범위한 간 대사를 거친다.자필루카스트는 주로 CYP2C9 효소에 의해 히드록실화 [1]대사물로 대사된다.
소거
자필루카스트는 주로 시간당 20리터의 속도로 담도 배설을 통해 깨끗해집니다.자필루카스트는 소변에서 검출되지 않는다.평균 말기 반감기는 최대 80mg의 [1]선량에 대한 선형 속도론에 따라 8-16시간이다.
약제유전체학
LTC4 합성효소
LTC4 합성효소 프로모터의 유전적 다형성은 자필루카스트에 대한 반응을 예측할 수 있다.심각한 천식 표현형과 관련된 단일핵산 다형성([17]SNP) A444C(유전자상의 444번째 위치에 있는 야생형 DNA 염기 아데닌은 돌연변이되고 대신 시토신은 존재한다)는 자필루카스트(두 유전자 변이가 헤테로지 또는 동종 접합일 때)에 대한 임상 반응을 감소시키는 것으로 나타났다.
CYP2C9
자필루카스트는 간효소 CYP2C9를 통해 대사된다.CYP2C9(CYP2C9*3 및 CYP2C9*13 등)의 기능을 저하시키는 SNP는 자필루카스트의 [18]간 클리어런스를 감소시켜 자필루카스트의 노출을 증가시킬 수 있습니다.특히 CYP2C9*3 다형성은 백인(7.083%), 흑인(1.170%), 아프리카(1.033%), 중동(9.312%), 동아시아(3.36.5%)[19]에 비해 남아시아(10.16%) 혈통에서 더 흔하게 나타난다.
화학
합성
자필루카스트는 다음 방법으로 [20]합성할 수 있습니다.
물리화학적 특성
순수한 자필루카스트는 흰색에서 옅은 노란색의 미세한 비정질 분말로 묘사됩니다.물에 녹지 않고 메탄올에 약간 녹으며 테트라히드로프랑, 디메틸설폭시드 및 아세톤에 [1]자유롭게 녹는다.
역사
자필루카스트는 미국에서 승인된 최초의 [10]시스테닐류코트리엔 수용체 길항제였다.자필루카스트는 [10]1996년에 승인되었다.
사회와 문화
경제학
자필루카스트가 의료 비용을 절감할 수 있다는 예비 증거가 있지만, 자필루카스트의 비용 효율은 [21]확립되지 않았다.
브랜드명
| A | 아콜레이트, 아콜리트, 에어로닉스 |
| B | 베날루코스트 |
| C | |
| D | |
| E | |
| F | 프리시 |
| G | |
| H | |
| I | |
| J | |
| K | |
| L | |
| M | 모노캐스트 |
| N | |
| O | 올모란 |
| P | |
| Q | |
| R | |
| S | |
| T | |
| U | |
| V | 벤테어 |
| W | |
| X | |
| Y | |
| Z | 자프닐, 자루카스트, 주카스트 |
조사.
작용 메커니즘
자필루카스트는 CysLT1 수용체에서 실제로 부분 역작용제로 작용하지만, 자필루카스트는 여전히 이 수용체에서 길항제로서 분류된다.이 효과의 가능한 임상적 의미는 사실일 경우 알려지지 않았다.[17]
기타 표시
자필루카스트가 감기 노출과 같은 알려진 원인이나 알려지지 않은 원인(특발성)[17]에 의해 만성 두드러기( 두드러기) 치료에 유익할 수 있다는 몇 가지 증거가 있다.자필루카스트가 낭포성 섬유증에 [17]어느 정도 도움이 될 수 있다는 시범 연구 결과가 나왔다.폐의 만성 염증으로 특징지어지는 질환인 만성폐쇄성폐질환(COPD)의 환경에서 자필루카스트는 폐 [17]기능을 향상시키는 것으로 나타났다.
수의학에서의 사용
자필루카스트는 [23]때때로 고양이 기관지 천식 치료에 사용된다.
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab "ACCOLATE (zafirlukast) Package Insert" (PDF). www.accessdata.fda.gov. AstraZeneca LP. Retrieved 29 November 2017.
- ^ a b c d e f Mastalerz L, Kumik J (March 2010). "Antileukotriene drugs in the treatment of asthma". Polskie Archiwum Medycyny Wewnetrznej. 120 (3): 103–8. PMID 20332717.
- ^ "Asthma in children". Clinical Overview. Elsevier BV. October 11, 2017.
- ^ "Asthma, Hay Fever and Eczema: How to Cope with Atopic Triad:Inside Children's Blog". Inside Children's Blog. 29 April 2016. Retrieved 7 January 2018.
- ^ a b "LACTMED: ZAFIRLUKAST". toxnet.nlm.nih.gov. U.S. National Library of Medicine. Retrieved 29 November 2017.
- ^ a b c Sorkness C, Schend V (2008). "Monitoring for Side Effects from Treatment". Clinical Asthma. Philadelphia, PA: Mosby. pp. 313–319. ISBN 978-0-323-04289-5.
- ^ Research, Center for Drug Evaluation and. "Drug Safety Information for Heathcare [sic] Professionals – Updated Information on Leukotriene Inhibitors: Montelukast (marketed as Singulair), Zafirlukast (marketed as Accolate), and Zileuton (marketed as Zyflo and Zyflo CR)". www.fda.gov. U.S. Food and Drug Administration. Archived from the original on November 14, 2017. Retrieved 6 December 2017.
- ^ a b c d e f "Zafirlukast". livertox.nlm.nih.gov. U.S. National Library of Medicine. Retrieved 29 November 2017.
- ^ "Accolate (zafirlukast) – Labeling Changes". www.medscape.com. WebMD LLC. Retrieved 29 November 2017.
- ^ a b c d e f g h Wechsler ME, Pauwels R, Drazen JM (October 1999). "Leukotriene modifiers and Churg-Strauss syndrome: adverse effect or response to corticosteroid withdrawal?". Drug Safety. 21 (4): 241–51. doi:10.2165/00002018-199921040-00001. PMID 10514017. S2CID 8124340.
- ^ Rovati GE, Capra V (September 2007). "Cysteinyl-leukotriene receptors and cellular signals". TheScientificWorldJournal. 7: 1375–92. doi:10.1100/tsw.2007.185. PMC 5901261. PMID 17767356.
- ^ "Medical Definition of BRONCHOCONSTRICTION". www.merriam-webster.com. Merriam-Webster, Incorporated. Retrieved 29 November 2017.
- ^ "Medical Definition of ALLERGIC RHINITIS". www.merriam-webster.com. Merriam-Webster, Incorporated. Retrieved 29 November 2017.
- ^ Valentine JL, Shyu WC, Grossman SJ. Comprehensive Toxicology (2 ed.).
Cmax is the maximum concentration of the drug achieved in the plasma following dose administration and Tmax is the time at which Cmax is attained.
- ^ "plasma albumin". TheFreeDictionary.com. Saunders. Retrieved 7 January 2018.
- ^ de Vries HE, Kuiper J, de Boer AG, Van Berkel TJ, Breimer DD (June 1997). "The blood-brain barrier in neuroinflammatory diseases". Pharmacological Reviews. 49 (2): 143–55. PMID 9228664.
- ^ a b c d e Capra V, Thompson MD, Sala A, Cole DE, Folco G, Rovati GE (July 2007). "Cysteinyl-leukotrienes and their receptors in asthma and other inflammatory diseases: critical update and emerging trends". Medicinal Research Reviews. 27 (4): 469–527. doi:10.1002/med.20071. PMID 16894531. S2CID 24103280.
- ^ "Clinical Annotation for CYP2C9*1CYP2C9*13CYP2C9*3 related to zafirlukast". PharmGKB. PharmGKB. Retrieved 29 November 2017.
- ^ "CYP2C9 Allele Functionality Table". PharmGKB. PharmGKB. Retrieved 29 November 2017.
- ^ Goverdhan G, Reddy AR, Himabindu V, Reddy GM (April 2014). "Synthesis and characterization of critical process related impurities of an asthma drug – Zafirlukast". Journal of Saudi Chemical Society. 18 (2): 129–138. doi:10.1016/j.jscs.2011.06.002.
- ^ Dunn CJ, Goa KL (2001). "Zafirlukast: an update of its pharmacology and therapeutic efficacy in asthma". Drugs. 61 (2): 285–315. doi:10.2165/00003495-200161020-00012. PMID 11270943.
- ^ "Zafirlukast - Drugs.com". Drugs.com. Drugs.com. Retrieved 29 November 2017.
- ^ Byers CG, Dhupa N (June 2005). "Feline bronchial asthma: treatment" (PDF). Compend Contin Educ Pract Vet. 27 (6): 426–32.
외부 링크
- "Zafirlukast". Drug Information Portal. U.S. National Library of Medicine.



