5-HT2A 수용체
5-HT2A receptor5-HT2A 수용체는 세로토닌 수용체 계열에 속하는 5-HT2 수용체의 하위 유형으로 G 단백질 결합 수용체(GPCR)입니다.[4] 5-HT2A 수용체는 세포 표면 수용체이지만 [5]여러 세포 내 위치를 가지고 있습니다.[6]
모든 5-HT2 수용체와 마찬가지로 5-HT2A 수용체는q G/G-단백질이11 결합되어 있습니다. 이것은 세로토닌에 대한 GPCR 중 주요 흥분 수용체 아형이지만, 5-HT는2A 시각 피질 및 전전두엽 피질과 같은 특정 영역에 대한 억제 효과도[7] 가질 수 있습니다.[8] 이 수용체는 LSD와 실로사이빈 버섯과 같은 세로토닌성 사이키델릭 약물의 표적으로서의 중요성으로 처음 주목받았습니다. 나중에 그것은 또한 적어도 부분적으로 많은 항정신병 약물, 특히 비정형 약물의 작용을 매개하는 것으로 밝혀졌기 때문에 다시 두각을 나타냈습니다.
시냅스 후 5-HT2A 수용체의 하향 조절은 선택적 세로토닌 재흡수 억제제(SSRI) 및 비정형 항정신병약의 만성 투여에 의해 유발되는 적응 과정입니다. 자살 및 기타 우울증 환자는 정상 환자보다 5-HT2A 수용체가 더 많았습니다. 이러한 연구 결과는 시냅스 후 5-HT2A 과밀도가 우울증의 발병기전에 관여한다는 것을 시사합니다.[9]
역설적으로2A 5-HT 수용체의 하향 조절은 여러 5-HT2A 길항제에서 관찰될 수 있습니다.[10] 따라서 5-HT2A 길항제는 내성 대신 역내성을 기대할 수 있습니다. 그러나 이2A 부위에는 5-HT 수용체를 상향 조절하는 것으로 나타난 길항제가 적어도 하나 있습니다.[10][11] 또한 몇 가지 다른 길항제는 5-HT2A 수용체 수에 영향을 미치지 않을 수 있습니다.[12] 그럼에도 불구하고 규제 상향은 규정이라기보다는 예외입니다. 5-HT2A 길항제의 저속파 수면(SWS) 촉진 효과와 관련하여 사람에게서는 내성이나 반발이 관찰되지 않습니다.[13]
신호 캐스케이드
5-HT2A 수용체는 주로 Gαq 신호 전달 경로에 결합하는 것으로 알려져 있습니다. 작용제로 수용체 자극을 받으면 Gα 및 β-γ 소단위체가 해리되어 다운스트림 이펙터 경로를 시작합니다. Gα는q 인지질분해효소 C(PLC) 활성을 자극하여 디아실글리세롤(DAG) 및 이노시톨 삼인산(IP3)의 방출을 촉진하고, 이는 차례로 단백질 키나제 C(PKC) 활성 및 Ca2+ 방출을 자극합니다.[14]
역사
존 가덤과 피카렐리는 세로토닌에 의한 장내 변화 중 일부는 모르핀에 의해 차단되고 나머지 반응은 디벤질린에 의해 억제되어 각각 M 수용체와 D 수용체가 명명되는 것을 발견하고 5-HT 수용체를 두 부류로 분류했습니다. 5-HT는2A Gaddum과 Picarelli에 의해 원래 5-HT 수용체의 D 아형으로 기술된 것과 일치하는 것으로 생각됩니다.[15] 분자 복제 이전의 시대에, 방사성 리간드 결합과 변위가 유일한 주요 도구였던 스피페론과 LSD는 두 개의 다른 5-HT 수용체를 표지하는 것으로 나타났고, 둘 다 모르핀을 대체하지 않아 LSD, 스피페론 및 모르핀의 고친화성 부위에 해당하는 5-HT1, 5-HT2 및 5-HT3 수용체의 명명으로 이어졌습니다. 각각[16] 나중에 5-HT가2 5-HT에1C 매우 가까웠기 때문에 5-HT를2 5-HT로2A 이름을 바꾸면서 그룹화된 것으로 나타났습니다. 따라서 5-HT2 수용체 계열은 5-HT2A(이전에는 5-HT2 또는 D로 알려짐), 5-HT2B(이전에는 5-HT로2F 알려짐) 및 5-HT2C(이전에는 5-HT로1C 알려짐) 수용체의 세 가지 개별 분자 개체로 구성됩니다.[17]
분배
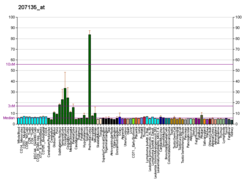
5-HT는2A 중추신경계(CNS)를 통해 광범위하게 발현됩니다.[18] 신피질(주로 전전두엽, 두정엽, 체성감각피질)과 후각 결절을 포함한 세로토닌성 말단 풍부 부위의 대부분에서 발현됩니다. Especially high concentrations of this receptor on the apical dendrites of pyramidal cells in layer V of the cortex may modulate cognitive processes, working memory, and attention[19][20][21] by enhancing glutamate release followed by a complex range of interactions with the 5-HT1A,[22] GABAA,[23] adenosine A1,[24] AMPA,[25] mGluR2/3,[26] mGlu5,[27] and OX2 receptors.[28][29] 쥐의 소뇌에서 이 단백질은 과립층의 골지세포에서도 [30]발견되고, 푸르킨제 세포에서도 발견되고 있습니다.[31][32]
말초에서는 혈소판과 심혈관계의 많은 세포 유형, 섬유아세포, 말초신경계의 뉴런에서 높게 발현됩니다. 또한, 인간 단핵구에서 5-HT2A mRNA 발현이 관찰되었습니다.[33] 5-HT2A/2C 수용체 작용제인 [11C]Cimbi-36의 전신 분포는 여러 내부 장기와 갈색 지방 조직(BAT)에서 흡수를 보여주지만 이것이 특정 5-HT2A 수용체 결합을 나타내는지는 명확하지 않습니다.[34]
영향들
수용체에 의해 매개되는 생리학적 과정은 다음과 같습니다.
- 중추신경계: 신경 흥분, 환각, 신체 밖 경험, 두려움. LSD, DMT 등과 같은 5-HT2A 수용체 작용제와 관련된 사이키델릭 효과를 주로 담당합니다.[35][36]
- 2,5-디메톡시-4-이오도암페타민(DOI)으로 5-HT2A 수용체를 활성화하면 심혈관 및 장을 포함한 여러 조직에서 강력한 항염증 효과가 나타납니다. LSD와 같은 다른 5-HT2A 작용제들도 TNF-알파 유발 염증에 대해 강력한 항염증 효과를 가지고 있습니다.[37][38]
- 시상하부에서 5-HT2A 수용체가 활성화되면 옥시토신, 프로락틴, ACTH, 코르티코스테론, 레닌의 호르몬 수치가 증가합니다.[39][40]
- 기억과 학습에서의[21][41][42] 역할
- 관절통에서의 역할.[43][44]
- 알츠하이머병의 역할.[45]
- 내장의 부드러운 근육 수축.[5]
- 수면 마비에 대한 가능한 역할입니다.[36]
- 노화에 대한 가능한 역할입니다.[46][47]
리간드
아고니스트
5-HT2A 수용체의 활성화는 LSD, 실로신 및 메스칼린과 같은 "고전적" 사이키델릭의 효과를 위해 필요하며, 이는 수용체에서 전체 또는 부분 작용제로 작용하며 각각 5-HT2A 작용제의 세 가지 주요 부류인 에르고린, 트립타민 및 페닐아민을 나타냅니다. 이 세 부류의 매우 큰 파생물 계열이 개발되었으며 이들의 구조-활성 관계가 광범위하게 연구되었습니다.[48][49] 전전두엽 피질의 영역 내 피라미드 세포의 정점 수지상에 위치한 5-HT2A 수용체에서 작용하는 작용제는 환각 활성을 매개하는 것으로 여겨집니다. 일부 연구 결과는 고전적인 사이키델릭의 정신 활성 효과가 단량체 5-HT2A 수용체가 아닌 수용체 이종이량체 5-HT2A–mGlu2에 의해 매개된다는 것을 보여줍니다.[50][51][35] 그러나 새로운 연구에 따르면 5HT와2A mGlu2 수용체는 물리적으로 서로 연관되지 않기 때문에 전자의 연구 결과는 관련성이 의심스럽습니다.[52] 작용제는 PFC의 도파민을 [21]강화하고 기억력을 향상시키며 주의와 학습에 적극적인 역할을 합니다.[53][54]
풀 어고니스트
- 25I-NBOH and its 2-methoxy-analog 25I-NBOMe[55]
- 18FFECIMBI-36 – 5-HT2A/5-HT2C 수용체 분포[56] 매핑을 위한 방사성 표지 작용제 리간드
- TCB-2[57]
- 멕사민 – 여러 세로토닌 수용체에 대한 완전 작용제.
- O-4310 – 5-HT2A selective, 5-HT에2C 비해 100배 선택성을 가지며 5-HT에서2B 비활성화된다고 주장
- PHA-57378 – 이중 5-HT2A/5-HT2C 작용제, 동물 연구에서 항불안 효과.[58]
- 25B-NBOMe – Cimbi-36으로도 알려져 있으며, 5-HT2A 수용체를[59] 시각화하기 위한 PET 이미징 도구로 사용됩니다.
부분작용제
- 25C-NBOMe
- 25CN-NBOH – 5-HT에2C 비해 5-HT에2A 대해 100배 선택성2B, 5-HT에 비해 46배 선택성.[60]
- AAZ-A-154 – 비할루신원성이지만 동물에서 항우울 효과를 유지합니다.[61]
- 브로모-드래곤플라이[62]
- (R)-DOI – 전통적으로 연구에[63] 사용되는 가장 일반적인 5-HT2A 기준 작용제
- 항레트로바이러스제인 에파비렌츠는 5-HT에2A 의해 매개되는 것으로 생각되는 정신과적 부작용을 일으킵니다.[64]
- DMBMPP – 구조적으로 제한된 25B-NBOMe의 유도체로, 5-HT보다2C 5-HT에2A 대해 124배 선택성을 갖는 강력한 부분 작용제로 작용하여 현재까지 확인된 작용제 리간드 중 가장 선택적인 작용제 리간드입니다.[65]
- 리수라이드 – 에르고린 계열의 항파킨슨 도파민 작용제로, 이중 5-HT2A/5-HT2C 작용제이자[66] 5-HT2B 길항제이기도 합니다.[67]
- 항말라리아 약물인 메플로퀸은 또한 5-HT2A 및/또는 5-HT2C 수용체를 통해 매개될 수 있는 정신 의학적 부작용을 생성합니다.[68]
- 메틸에르고노빈의 동족체인 메틸에르고노빈은 편두통 블록 5-HT2A 및 5-HT2C 수용체를 치료하는 데 사용되지만 일부 제제에서는 부분 작용제로 작용하기도 합니다.
- 5-HT2A 및 도파민 D2 수용체 모두에서 부분 작용제로 작용하는 OSU-6162 및 Z3517967757과 같은 피페리딘 유도체.
- 퀴파진 – 5-HT2A 작용제 뿐만 아니라 강력한 5-HT3 작용제.[69]
- SN-22 – 세 가지 5-HT2 하위 유형 모두에서 부분 작용제
- 3-카르복시인돌 PB-22 (1-펜틸-인돌-3-카르복실산) – 합성 칸나비노이드 PB-22의 대사산물, 5-HT에서2A[70] 부분작용제
- SCHEMBL5334361과 같은 일부 벤자제핀 및 로르카세린과 관련된 유사한 화합물은 강력한 5-HT2A 작용제일 뿐만 아니라 5-HT2C 작용제입니다.[71][72][73][74][75]
- IHCH-7113 – 5-HT2A 길항제 항정신병 루마테페론의 단순화에 의해 유도된 5-HT2A 작용제.[76]
- (R)-69,[77] Z4154032166 및 WXVL_BT0793LQ2118과 같은 테트라히드로피리딘 유도체.[78]
- 치환된 테트라하이드로-β-카르볼린
말초 선택적 작용제
5-HT2A 수용체 활성화의 한 가지 효과는 안압의 감소이므로 5-HT2A 작용제는 녹내장 치료에 유용할 수 있습니다. 이것은 눈 안의 압력을 감소시키지만 혈액-뇌 장벽을 넘지 않고 환각성 부작용을 일으키지 않는 AL-34662와 같은 화합물의 개발로 이어졌습니다.[80] 이 화합물에 대한 동물 연구는 최대 30mg/kg 용량에서 환각 효과가 없음을 보여주었지만, 더 친유성 유사체 중 몇 가지가 설치류에서 환각 효과의 특징으로 알려진 헤드 트위치 반응을 생성했습니다.[81]
길항제
- Volinanserin (MDL100907, M100907)[82] – 가장 강력한 5-HT2A 길항제 몇 번의 임상 시험을 거쳤지만 시판된 적은 없었습니다.
- 트라조돈 – 강력한 5-HT2A 길항제 뿐만 아니라 다른 세로토닌 수용체에 길항제.
- Cyclobenzaprine – 5-HT2A 수용체와2C 5-HT 수용체 모두의 강력한 길항제
- 비정형 항정신병 약물인 Brexiprazole은 5-HT 수용체에서 강력한 길항제(K = 0.47nM)입니다.
- 대부분의 삼환계 항우울제(TCA) – 예를 들어, 아미트립틸린, 노르트립틸린, 아목사핀, 클로미프라민, 독세핀, 마프로틸린, 이미프라민, 이프린돌[85]
- 사환계 항우울제 – mianserin,[85] mirtazapine, maprotiline
- 네파조돈 – 시냅스 후 5-HT2A 수용체를 차단하고 시냅스 전 세로토닌과 노르에피네프린 재흡수를 덜 억제합니다.
- 전형적 항정신병약 - 예를 들어 클로자핀, 올란자핀, 케티아핀, 리스페리돈 및 아세나핀은 5-HT의2A 상대적으로 강력한 길항제이며 일부 저효능 구세대/전형적 항정신병약입니다.
- Cyproheptadine
- 피조티펜 – 비선택적 길항제.[86]
- LY-367,265 – 항우울 효과가 있는 이중 5-HT2A 길항제 / SSRI
- 2-alkyl-4-아릴-tetra하이드로-피리미도-아제핀 – 아형 선택적 길항제 (35 g: 60-배).
- AMDA 및 관련 유도체 – 선택적 5-HT2A 길항제 계열.[88][89][90][91][92]
- 대표적인 항정신병 약물 – 예: 할로페리돌 및 클로르프로마진(미량)
- 오피프라몰 – 비정형 항우울제
- 하이드록시진(Atarax)(부효과)
- 5-MeO-NBpBrT
- 니아프라진
- 카리프라진
- 난테닌
- ergot alkaloids는 대부분 비특이적인 5-HT 수용체 길항제이지만 metergoline 및 nicergoline과 같은 몇 가지 ergot 유도체는 5-HT 수용체2 계열의 구성체에 우선적으로 결합합니다.
- 케탄세린의 발견은 5-HT2 수용체의 약리학에서 획기적인 사건이었습니다. 케탄세린은 5-HT 유도 혈소판 부착을 차단할 수 있지만 5-HT2 수용체 계열을 통해 잘 알려진 항고혈압 작용을 매개하는 것이 아니라 알파1 아드레날린 수용체에 대한 높은 친화력을 통해 매개합니다. 또한1 5-HT2A 수용체와 동일한 H 히스타민제 수용체에 대한 높은 친화력을 가지고 있습니다. 리탄세린과 같은 케탄세린과 화학적으로 관련된 화합물은 알파-아드레날린 수용체에 대한 친화도가 낮은 보다 선택적인 5-HT2A 수용체 길항제입니다. 그러나 대부분의 다른 5-HT2A 수용체 길항제와 마찬가지로 리탄세린도 5-HT2C 수용체를 강력하게 억제합니다.
길항제 및 심혈관 질환
관상동맥 혈전증 환자에서 5-HT2A 발현 증가가 관찰되며, 수용체는 죽상동맥경화증에 영향을 미치는 과정과 관련이 있습니다.[93] 5-HT는2A 수용체가 관상동맥에[94] 존재하여 혈관 수축을 매개할 수 있기 때문에 관상동맥 경련과도 연관이 있습니다.[95] 따라서 5-HT 길항제는 심혈관 질환의 예방 가능성이 있지만 아직까지 발표된 연구는 없습니다.[93]
역작용제
- AC-90179 – 5-HT에서2A 강력하고 선택적인 역작용제, 또한 5-HT2C 길항제.[96][97]
- Nelotanserin (APD-125) – Arena Pharmaceuticals가 불면증 치료를 위해 개발한 선택적 5-HT2A inverse agonist. APD-125는 임상시험에서 효과적이고 잘 견디는 것으로 나타났습니다.[98]
- Eplivanserin (Sanofi Aventis) – 임상 2상에 도달한 수면제(그러나 승인 신청이 철회됨)는 선택적 5-HT2A 역작용제 역할을 합니다.
- 피마반세린(ACP-103) – AC-90179보다 더 선택적이고, 경구 활성이며, 생체 내 항정신병적이며, 현재 FDA는 파킨슨병과 관련된 환각 및 망상 치료를 승인했습니다.[99][100][101][102][103]
기능선택성
5-HT-수용체2A 리간드는 형질도입 경로를 차등적으로 활성화할 수 있습니다(위 참조). 연구들은 두 번째 메신저를 통해 PLC와 PLA2라는 두 개의 이펙터의 활성화를 평가했습니다. 보다 뚜렷한 기능적 선택성을 나타내는 화합물은 2,5-DMA 및 2C-N입니다. 전자는 PLA2 매개 반응을 활성화하지 않고 IP 축적을 유도하는 반면, 후자는 PLC 매개 반응을 활성화하지 않고 AA 방출을 유도합니다.[104]


최근의 연구는 쥐에서 머리 떨림을 생성하는2A 5-HT 작용제와 리수라이드와 같이 그렇지 않은 작용제 사이의 체세포 감각 피질 내에서 잠재적인 신호 전달 차이를 제안했는데, 이들 작용제는 활성 5-HT2A 작용제임에도 불구하고 인간에게 비할루신원성이기 때문입니다.[105][106] 신호 전달의 차이에 대한 한 가지 알려진 예는 베타-아레스트린이라고 불리는 세포 내 단백질의 차등 모집을 포함하는 두 가지 5-HT2A 작용제 세로토닌과 DOI 사이의 것입니다.[107][108] (-)-19와 같은 사이클로프로필메탄올아민 유도체는 또한 β-arrestin 모집과 비교하여 Gq 매개 신호 전달에 대한 기능적 선택성을 갖는 5-HT2A/2C 작용제로 작용하는 것으로 나타났습니다.[109]
유전학

5-HT2A 수용체는 HTR2A 유전자에 의해 코딩됩니다. 인간의 경우 이 유전자는 13번 염색체에 위치해 있습니다. 이 유전자는 이전에 두 개의 관련된 유전자 HTR2B와 HTR2C가 기술되기 전까지 단지 HTR2라고 불렸습니다. HTR2A에 대해 몇 가지 흥미로운 다형성이 확인되었습니다: A-1438G (rs6311), C102T (rs6313) 및 His452Tyr (rs6314). 유전자에는 더 많은 다형성이 존재합니다. 2006년 논문에는 255개가 기재되어 있습니다.[110][62]
5 유전자의 T102C 다형성으로서 섬유근육통에서의 가능한 역할HT2A는 섬유근육통 환자에서 흔했습니다.[111]
인간의 HTR2A 유전자는 3개의 인트론과 4개의 엑손으로 구성되며 18개의 엑손으로 구성된 인간 유전자 HTR2A-AS1과 겹치는 것으로 생각됩니다.[112] 인간의 HTR2A와 이종상동체를 가지고 있는 생물은 200종이 넘습니다. 현재 HTR2A 유전자에 대해 가장 잘 기록된 이종상동체는 쥐와 [113]제브라피쉬입니다.[114] HTR2A 유전자에는 8개의 파라로그가 있습니다. HTR2A 유전자는 GNA14, GNAI1, GNAI3, GNAQ, GNAZ 등의 G-단백질 유전자와 상호작용하여 활성화시키는 것으로 알려져 있습니다.[115] 이러한 상호 작용은 많은 유기체에서 세포 신호[116][117] 전달 및 항상성에 중요합니다.[119]
인간의 뇌 조직에서 HTR2A의 조절은 전두엽 피질, 편도체, 시상, 뇌간 및 소뇌의 [112]영역에 따라 다릅니다. 2016년의 논문에서, 그들은 HTR2A가 대체 스플라이스 수용체 부위의 활용, 엑손 스킵, 희귀 엑손 사용 및 인트론 보유를 포함한 다양한 다양한 스플라이싱 이벤트를 겪는다는 것을 발견했습니다.[112]
규제의 메커니즘
특정 전사체 결합 부위에서 DNA 메틸화에 의해 조절되는 것과 같은 HTR2A 유전자에 대한 조절 메커니즘은 몇 가지가 있습니다.[120][121] 유전자 발현의 올바른 조절을 위한 또 다른 메커니즘은 대체 스플라이싱을 통해 달성됩니다. 이는 공동 전사 과정으로 하나의 코딩 단위에서 여러 형태의 mRNA 전사체를 생성할 수 있으며 유전자 발현의 중요한 조절점으로 떠오르고 있습니다. 이 과정에서 엑손 또는 인트론은 전구체-mRNA에 포함되거나 배제되어 여러 개의 성숙한 mRNA 변이체를 생성할 수 있습니다.[122] 이러한 mRNA 변이체는 길항 기능 또는 차등 발현 패턴을 가질 수 있는 다른 이소형을 생성하여 세포에 대한 가소성 및 적응성을 산출합니다.[123] 한 연구는 일반적인 유전적 변이체 r6311이 확장된 5' UTR을 포함하는 HTR2A 전사체의 발현을 조절한다는 것을 발견했습니다.[112]
정신 질환과의 연관성
여러 연구에서 -1438G/A 다형성과 조울증 및[124] 주요 우울증과 같은 기분 장애 사이의 연관성이 발견되었습니다.[125] T102C 다형성과 조현병 사이에 1.3의 오즈비를 가진 약한 연결고리가 발견되었습니다.[126] 이러한 다형성은 자살 시도와 관련하여 연구되기도 했는데, 자살 시도자 중 C/C 유전자형이 과다하다는 연구 결과가 나왔습니다.[127] 다른 많은 연구들은 조현병과 유전자의 연관성을 찾는 데 전념했으며 결과는 다양했습니다.[128]
그러나 이러한 개별 연구는 전체적인 그림을 제공하지 못할 수 있습니다. 별도의 연구에서 보고된 다양한 SNP의 효과를 조사한 2007년의 리뷰는 유전자의 유전적 변이에 대한 관여가 없거나 작거나 복제되지 않은 역할로 [정신 질환이 있는 HTR2A 유전자 변이체의] 유전적 연관성 연구가 상충되고 일반적으로 부정적인 결과를 보고한다고 말했습니다.[129]
초기 성장 반응 3(EGR3)을 코딩하는 프로모터 유전자의 다형성은 조현병과 관련이 있습니다. 연구들은 EGR3와 HTR2A, 그리고 형질전환 동물들의 조현병과 같은 행동들 사이의 관계를 증명했습니다.[130][131] 이러한 결과가 정확히 어떻게 조현병에 대한 추가적인 생검 심리학적 이해로 이어지는지는 여전히 널리 논의되고 있습니다.[132][133] HTR2A의 기능 장애가 약리학적 개입에 영향을 미칠 수 있다는 일부 증거가 있습니다.[134]
여러 연구에서 5-하이드록시트립타민(세로토닌) 2A 수용체(5-HTR2A) 유전자 다형성과 자살 행동의 위험 증가 사이의 관계를 평가했습니다. 한 연구에서는 T102C 다형성이 자살 행동과 관련이 있다고 밝혔으나 다른 연구에서는 이러한 결과를 복제하지 못했으며 다형성과 자살 행동 사이의 연관성을 찾지 못했습니다.[136]
치료반응
유전학은 또한 주요 우울증 질환의 치료에 있어서 부작용의 양과 어느 정도 연관되어 있는 것으로 보입니다.[137]
약물 남용과의 연관성
5-HT2A 수용체 코딩 유전자 HTR2A(rs6313 및 s6311)의 다형성은 알코올 오남용과 상충되는 연관성을 가지고 있는 것으로 나타났습니다. 예를 들어, 5-HT2A 수용체 코딩 유전자 HTR2A (rs6313)의 다형성은 120명의 젊은 성인 표본에서 더 낮은 양성 알코올 기대, 더 높은 거부 자기 효능, 그리고 더 낮은 알코올 오용을 예측하는 것으로 보고되었습니다. 그러나 이러한 다형성은 충동성, 인지, 알코올 오용 사이의 연관성을 조절하지 못했습니다.[138] 다른 연구에서 T102C 다형성 알코올 오남용 사이의 연관성을 발견했기 때문에 상반된 결과가 있습니다.[139][140]
유전자 발현에 대한 약물 영향
메틸화 패턴이 자극제를 사용하는 사람들의 재발 행동에 기여할 수 있다는 몇 가지 증거가 있습니다.[141] 쥐에서 DOI, LSD, DOM 및 DOB와 같은 향정신성 약물은 여러 다른 뇌 영역 사이에서 다른 전사 패턴을 생성합니다.[131]
수용체 분석 방법
수용체는 신경 영상, 방사선 리간드, 유전자 분석, 이온 흐름 측정 및 기타 방법으로 분석할 수 있습니다.
신경영상
5-HT2A 수용체는 신경 수용체에 결합하는 불소-18-알탄세린,[142] MDL 100,907[143] 또는 11[C]Cimbi-36[59][144] 방사선 리간드를 사용하여 PET-스캐너로 이미지화될 수 있습니다. 예를 들어, 한 연구에서는 주요 우울증 환자의 해마에서 특히 알탄세린의 결합이 감소했다고 보고했습니다.[145]
알탄세린 흡수는 나이가 들수록 감소하는데, 이는 나이가 들수록 특정 5-HT2A 수용체의 손실을 반영합니다.[146][147][148]
다른.
친화성 정제 항체를 사용한 웨스턴 블롯 및 전기영동에 의한 5-HT2A 수용체 단백질 샘플의 검사에 대해 설명했습니다. 5-HT2A 수용체의 면역조직화학염색도 가능합니다.[5]
참고문헌
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000102468 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Cook EH, Fletcher KE, Wainwright M, Marks N, Yan SY, Leventhal BL (August 1994). "Primary structure of the human platelet serotonin 5-HT2A receptor: identify with frontal cortex serotonin 5-HT2A receptor". Journal of Neurochemistry. 63 (2): 465–469. doi:10.1046/j.1471-4159.1994.63020465.x. PMID 8035173. S2CID 40207336.
- ^ a b c Kling A (2013). 5-HT2A: a serotonin receptor with a possible role in joint diseases (PDF). Umeå: Umeå Universitet. ISBN 978-91-7459-549-9.
- ^ Raote I (2007). "Serotonin 2A (5-HT2A) Receptor Function: Ligand-Dependent Mechanisms and Pathways". Ishier. Frontiers in Neuroscience. Press/Taylor & Francis. ISBN 9780849339776. PMID 21204452.
- ^ Martin P, Waters N, Schmidt CJ, Carlsson A, Carlsson ML (1998). "Rodent data and general hypothesis: antipsychotic action exerted through 5-HT2A receptor antagonism is dependent on increased serotonergic tone". Journal of Neural Transmission. 105 (4–5): 365–396. doi:10.1007/s007020050064. PMID 9720968. S2CID 20944107.
- ^ De Almeida RM, Rosa MM, Santos DM, Saft DM, Benini Q, Miczek KA (May 2006). "5-HT(1B) receptors, ventral orbitofrontal cortex, and aggressive behavior in mice". Psychopharmacology. 185 (4): 441–450. doi:10.1007/s00213-006-0333-3. PMID 16550387. S2CID 33274637.
- ^ Eison AS, Mullins UL (1996). "Regulation of central 5-HT2A receptors: a review of in vivo studies". Behavioural Brain Research. 73 (1–2): 177–181. doi:10.1016/0166-4328(96)00092-7. PMID 8788498. S2CID 4048975.
- ^ a b Yadav PN, Kroeze WK, Farrell MS, Roth BL (October 2011). "Antagonist functional selectivity: 5-HT2A serotonin receptor antagonists differentially regulate 5-HT2A receptor protein level in vivo". The Journal of Pharmacology and Experimental Therapeutics. 339 (1): 99–105. doi:10.1124/jpet.111.183780. PMC 3186284. PMID 21737536.
- ^ Rinaldi-Carmona M, Congy C, Simiand J, Oury-Donat F, Soubrie P, Breliere JC, Le Fur G (January 1993). "Repeated administration of SR 46349B, a selective 5-hydroxytryptamine2 antagonist, up-regulates 5-hydroxytryptamine2 receptors in mouse brain". Molecular Pharmacology. 43 (1): 84–89. PMID 8423772.
- ^ Gray JA, Roth BL (November 2001). "Paradoxical trafficking and regulation of 5-HT(2A) receptors by agonists and antagonists". Brain Research Bulletin. 56 (5): 441–451. doi:10.1016/s0361-9230(01)00623-2. PMID 11750789. S2CID 271925.
- ^ Vanover KE, Davis RE (28 July 2010). "Role of 5-HT2A receptor antagonists in the treatment of insomnia". Nature and Science of Sleep. 2: 139–150. doi:10.2147/nss.s6849. PMC 3630942. PMID 23616706.
- ^ Urban JD, Clarke WP, von Zastrow M, Nichols DE, Kobilka B, Weinstein H, et al. (January 2007). "Functional selectivity and classical concepts of quantitative pharmacology". The Journal of Pharmacology and Experimental Therapeutics. 320 (1): 1–13. doi:10.1124/jpet.106.104463. PMID 16803859. S2CID 447937.
- ^ Sanders-Bush E, Mayer SE (2006). "Chapter 11: 5-Hydroxytryptamine (Serotonin): Receptor Agonists and Antagonists". In Brunton LL, Lazo JS, Parker K (eds.). Goodman & Gilman's the Pharmacological Basis of Therapeutics (11th ed.). New York: McGraw-Hill. ISBN 0-07-142280-3.
- ^ Siegel GJ, Albers RW (2005). Basic neurochemistry: molecular, cellular, and medical aspects. Vol. 1 (7th ed.). Academic Press. p. 241. ISBN 0-12-088397-X.
- ^ Hoyer D, Hannon JP, Martin GR (April 2002). "Molecular, pharmacological and functional diversity of 5-HT receptors". Pharmacology, Biochemistry, and Behavior. 71 (4): 533–554. doi:10.1016/S0091-3057(01)00746-8. PMID 11888546. S2CID 25543069.
- ^ Beliveau, Vincent; Ganz, Melanie; Feng, Ling; Ozenne, Brice; Højgaard, Liselotte; Fisher, Patrick M.; Svarer, Claus; Greve, Douglas N.; Knudsen, Gitte M. (4 January 2017). "A High-Resolution In Vivo Atlas of the Human Brain's Serotonin System". Journal of Neuroscience. 37 (1): 120–128. doi:10.1523/JNEUROSCI.2830-16.2016. ISSN 0270-6474. PMC 5214625. PMID 28053035.
- ^ Aghajanian GK, Marek GJ (April 1999). "Serotonin, via 5-HT2A receptors, increases EPSCs in layer V pyramidal cells of prefrontal cortex by an asynchronous mode of glutamate release". Brain Research. 825 (1–2): 161–171. doi:10.1016/S0006-8993(99)01224-X. PMID 10216183. S2CID 20081913.
- ^ Marek GJ, Wright RA, Gewirtz JC, Schoepp DD (2001). "A major role for thalamocortical afferents in serotonergic hallucinogen receptor function in the rat neocortex". Neuroscience. 105 (2): 379–392. doi:10.1016/S0306-4522(01)00199-3. PMID 11672605. S2CID 19764312.
- ^ a b c Bortolozzi A, Díaz-Mataix L, Scorza MC, Celada P, Artigas F (December 2005). "The activation of 5-HT receptors in prefrontal cortex enhances dopaminergic activity". Journal of Neurochemistry. 95 (6): 1597–1607. doi:10.1111/j.1471-4159.2005.03485.x. hdl:10261/33026. PMID 16277612. S2CID 18350703.
- ^ Amargós-Bosch M, Bortolozzi A, Puig MV, Serrats J, Adell A, Celada P, et al. (March 2004). "Co-expression and in vivo interaction of serotonin1A and serotonin2A receptors in pyramidal neurons of prefrontal cortex". Cerebral Cortex. 14 (3): 281–299. doi:10.1093/cercor/bhg128. PMID 14754868.
- ^ Feng J, Cai X, Zhao J, Yan Z (September 2001). "Serotonin receptors modulate GABA(A) receptor channels through activation of anchored protein kinase C in prefrontal cortical neurons". The Journal of Neuroscience. 21 (17): 6502–6511. doi:10.1523/JNEUROSCI.21-17-06502.2001. PMC 6763081. PMID 11517239.
- ^ Marek GJ (June 2009). "Activation of adenosine(1) (A(1)) receptors suppresses head shakes induced by a serotonergic hallucinogen in rats". Neuropharmacology. 56 (8): 1082–1087. doi:10.1016/j.neuropharm.2009.03.005. PMC 2706691. PMID 19324062.
- ^ Zhang C, Marek GJ (January 2008). "AMPA receptor involvement in 5-hydroxytryptamine2A receptor-mediated pre-frontal cortical excitatory synaptic currents and DOI-induced head shakes". Progress in Neuro-Psychopharmacology & Biological Psychiatry. 32 (1): 62–71. doi:10.1016/j.pnpbp.2007.07.009. PMID 17728034. S2CID 44889209.
- ^ Gewirtz JC, Marek GJ (November 2000). "Behavioral evidence for interactions between a hallucinogenic drug and group II metabotropic glutamate receptors". Neuropsychopharmacology. 23 (5): 569–576. doi:10.1016/S0893-133X(00)00136-6. PMID 11027922.
- ^ Marek GJ, Zhang C (September 2008). "Activation of metabotropic glutamate 5 (mGlu5) receptors induces spontaneous excitatory synaptic currents in layer V pyramidal cells of the rat prefrontal cortex". Neuroscience Letters. 442 (3): 239–243. doi:10.1016/j.neulet.2008.06.083. PMC 2677702. PMID 18621097.
- ^ Lambe EK, Liu RJ, Aghajanian GK (November 2007). "Schizophrenia, hypocretin (orexin), and the thalamocortical activating system". Schizophrenia Bulletin. 33 (6): 1284–1290. doi:10.1093/schbul/sbm088. PMC 2779889. PMID 17656637.
- ^ Liu RJ, Aghajanian GK (January 2008). "Stress blunts serotonin- and hypocretin-evoked EPSCs in prefrontal cortex: role of corticosterone-mediated apical dendritic atrophy". Proceedings of the National Academy of Sciences of the United States of America. 105 (1): 359–364. Bibcode:2008PNAS..105..359L. doi:10.1073/pnas.0706679105. PMC 2224217. PMID 18172209.
- ^ Geurts FJ, De Schutter E, Timmermans JP (June 2002). "Localization of 5-HT2A, 5-HT3, 5-HT5A and 5-HT7 receptor-like immunoreactivity in the rat cerebellum". Journal of Chemical Neuroanatomy. 24 (1): 65–74. doi:10.1016/S0891-0618(02)00020-0. PMID 12084412. S2CID 16510169.
- ^ Maeshima T, Shutoh F, Hamada S, Senzaki K, Hamaguchi-Hamada K, Ito R, Okado N (August 1998). "Serotonin2A receptor-like immunoreactivity in rat cerebellar Purkinje cells". Neuroscience Letters. 252 (1): 72–74. doi:10.1016/S0304-3940(98)00546-1. PMID 9756362. S2CID 28549709.
- ^ Maeshima T, Shiga T, Ito R, Okado N (December 2004). "Expression of serotonin2A receptors in Purkinje cells of the developing rat cerebellum". Neuroscience Research. 50 (4): 411–417. doi:10.1016/j.neures.2004.08.010. PMID 15567478. S2CID 5772490.
- ^ Dürk T, Panther E, Müller T, Sorichter S, Ferrari D, Pizzirani C, et al. (May 2005). "5-Hydroxytryptamine modulates cytokine and chemokine production in LPS-primed human monocytes via stimulation of different 5-HTR subtypes". International Immunology. 17 (5): 599–606. doi:10.1093/intimm/dxh242. PMID 15802305.
- ^ Johansen A, Holm S, Dall B, Keller S, Kristensen JL, Knudsen GM, Hansen HD (July 2019). "Human biodistribution and radiation dosimetry of the 5-HT2A receptor agonist Cimbi-36 labeled with carbon-11 in two positions". EJNMMI Research. 9 (1): 71. doi:10.1186/s13550-019-0527-4. PMC 6669221. PMID 31367837.
- ^ a b Moreno JL, Holloway T, Albizu L, Sealfon SC, González-Maeso J (April 2011). "Metabotropic glutamate mGlu2 receptor is necessary for the pharmacological and behavioral effects induced by hallucinogenic 5-HT2A receptor agonists". Neuroscience Letters. 493 (3): 76–79. doi:10.1016/j.neulet.2011.01.046. PMC 3064746. PMID 21276828.
- ^ a b Jalal B (November 2018). "The neuropharmacology of sleep paralysis hallucinations: serotonin 2A activation and a novel therapeutic drug". Psychopharmacology. 235 (11): 3083–3091. doi:10.1007/s00213-018-5042-1. PMC 6208952. PMID 30288594.
- ^ Yu B, Becnel J, Zerfaoui M, Rohatgi R, Boulares AH, Nichols CD (November 2008). "Serotonin 5-hydroxytryptamine(2A) receptor activation suppresses tumor necrosis factor-alpha-induced inflammation with extraordinary potency". The Journal of Pharmacology and Experimental Therapeutics. 327 (2): 316–323. doi:10.1124/jpet.108.143461. PMID 18708586. S2CID 25374241.
- ^ Nau F, Yu B, Martin D, Nichols CD (2013). "Serotonin 5-HT2A receptor activation blocks TNF-α mediated inflammation in vivo". PLOS ONE. 8 (10): e75426. Bibcode:2013PLoSO...875426N. doi:10.1371/journal.pone.0075426. PMC 3788795. PMID 24098382.
- ^ Van de Kar LD, Javed A, Zhang Y, Serres F, Raap DK, Gray TS (May 2001). "5-HT2A receptors stimulate ACTH, corticosterone, oxytocin, renin, and prolactin release and activate hypothalamic CRF and oxytocin-expressing cells". The Journal of Neuroscience. 21 (10): 3572–3579. doi:10.1523/JNEUROSCI.21-10-03572.2001. PMC 6762485. PMID 11331386.
- ^ Zhang Y, Damjanoska KJ, Carrasco GA, Dudas B, D'Souza DN, Tetzlaff J, et al. (November 2002). "Evidence that 5-HT2A receptors in the hypothalamic paraventricular nucleus mediate neuroendocrine responses to (-)DOI". The Journal of Neuroscience. 22 (21): 9635–9642. doi:10.1523/JNEUROSCI.22-21-09635.2002. PMC 6758011. PMID 12417689.
- ^ Harvey JA (2003). "Role of the serotonin 5-HT(2A) receptor in learning". Learning & Memory. 10 (5): 355–362. doi:10.1101/lm.60803. PMC 218001. PMID 14557608.
- ^ Williams GV, Rao SG, Goldman-Rakic PS, Foresta M, Ropolo M, Degan P, et al. (March 2010). "Defective repair of 5-hydroxy-2'-deoxycytidine in Cockayne syndrome cells and its complementation by Escherichia coli formamidopyrimidine DNA glycosylase and endonuclease III". Free Radical Biology & Medicine. 48 (5): 681–690. doi:10.1016/j.freeradbiomed.2009.12.007. PMC 6758292. PMID 11923449.
- ^ Passier A, van Puijenbroek E (November 2005). "Mirtazapine-induced arthralgia". British Journal of Clinical Pharmacology. 60 (5): 570–572. doi:10.1111/j.1365-2125.2005.02481.x. PMC 1884949. PMID 16236049.
- ^ Adwan MH (August 2016). "An update on drug-induced arthritis". Rheumatology International. 36 (8): 1089–1097. doi:10.1007/s00296-016-3462-y. PMID 27000044. S2CID 25401280.
- ^ Herth MM, Knudsen GM (June 2015). "Current radiosynthesis strategies for 5-HT2A receptor PET tracers". Journal of Labelled Compounds & Radiopharmaceuticals. 58 (7): 265–273. doi:10.1002/jlcr.3288. PMID 25997728.
- ^ Beer R (13 June 2023). "Anblick von toten Fliegen lässt Fliegen altern". science.ORF.at (in German). Retrieved 14 June 2023.
- ^ Gendron CM, Chakraborty TS, Duran C, Dono T, Pletcher SD (June 2023). "Ring neurons in the Drosophila central complex act as a rheostat for sensory modulation of aging". PLOS Biology. 21 (6): e3002149. doi:10.1371/journal.pbio.3002149. PMC 10263353. PMID 37310911.
- ^ Nichols DE (February 2004). "Hallucinogens". Pharmacology & Therapeutics. 101 (2): 131–181. doi:10.1016/j.pharmthera.2003.11.002. PMID 14761703.
- ^ Blaazer AR, Smid P, Kruse CG (September 2008). "Structure-activity relationships of phenylalkylamines as agonist ligands for 5-HT(2A) receptors". ChemMedChem. 3 (9): 1299–1309. doi:10.1002/cmdc.200800133. PMID 18666267. S2CID 7537908.
- ^ Moreno JL, Muguruza C, Umali A, Mortillo S, Holloway T, Pilar-Cuéllar F, et al. (December 2012). "Identification of three residues essential for 5-hydroxytryptamine 2A-metabotropic glutamate 2 (5-HT2A·mGlu2) receptor heteromerization and its psychoactive behavioral function". The Journal of Biological Chemistry. 287 (53): 44301–44319. doi:10.1074/jbc.M112.413161. PMC 3531745. PMID 23129762.
- ^ González-Maeso J, Ang RL, Yuen T, Chan P, Weisstaub NV, López-Giménez JF, et al. (March 2008). "Identification of a serotonin/glutamate receptor complex implicated in psychosis". Nature. 452 (7183): 93–97. Bibcode:2008Natur.452...93G. doi:10.1038/nature06612. PMC 2743172. PMID 18297054.
- ^ Taddeucci A, Olivero G, Roggeri A, Milanese C, Giorgio FP, Grilli M, et al. (September 2022). "Presynaptic 5-HT2A-mGlu2/3 Receptor-Receptor Crosstalk in the Prefrontal Cortex: Metamodulation of Glutamate Exocytosis". Cells. 11 (19): 3035. doi:10.3390/cells11193035. PMC 9562019. PMID 36230998.
- ^ Wingen M, Kuypers KP, Ramaekers JG (February 2007). "The role of 5-HT1a and 5-HT2A receptors in attention and motor control: a mechanistic study in healthy volunteers". Psychopharmacology. 190 (3): 391–400. doi:10.1007/s00213-006-0614-x. PMID 17124621. S2CID 25125461.
- ^ Wingen M, Kuypers KP, Ramaekers JG (July 2007). "Selective verbal and spatial memory impairment after 5-HT1A and 5-HT2A receptor blockade in healthy volunteers pre-treated with an SSRI". Journal of Psychopharmacology. 21 (5): 477–485. doi:10.1177/0269881106072506. PMID 17092965. S2CID 19575488.
- ^ Braden MR, Parrish JC, Naylor JC, Nichols DE (December 2006). "Molecular interaction of serotonin 5-HT2A receptor residues Phe339(6.51) and Phe340(6.52) with superpotent N-benzyl phenethylamine agonists". Molecular Pharmacology. 70 (6): 1956–1964. doi:10.1124/mol.106.028720. PMID 17000863. S2CID 15840304.
- ^ Prabhakaran J, Solingapuram Sai KK, Zanderigo F, Rubin-Falcone H, Jorgensen MJ, Kaplan JR, et al. (January 2017). "In vivo evaluation of [18F]FECIMBI-36, an agonist 5-HT2A/2C receptor PET radioligand in nonhuman primate". Bioorganic & Medicinal Chemistry Letters. 27 (1): 21–23. doi:10.1016/j.bmcl.2016.11.043. PMC 5348621. PMID 27889455.
- ^ McLean TH, Parrish JC, Braden MR, Marona-Lewicka D, Gallardo-Godoy A, Nichols DE (September 2006). "1-Aminomethylbenzocycloalkanes: conformationally restricted hallucinogenic phenethylamine analogues as functionally selective 5-HT2A receptor agonists". Journal of Medicinal Chemistry. 49 (19): 5794–5803. doi:10.1021/jm060656o. PMID 16970404.
- ^ Ennis MD, Hoffman RL, Ghazal NB, Olson RM, Knauer CS, Chio CL, et al. (July 2003). "2,3,4,5-tetrahydro- and 2,3,4,5,11,11a-hexahydro-1H-[1,4]diazepino[1,7-a]indoles: new templates for 5-HT(2C) agonists". Bioorganic & Medicinal Chemistry Letters. 13 (14): 2369–2372. doi:10.1016/S0960-894X(03)00403-7. PMID 12824036.
- ^ a b Ettrup A, da Cunha-Bang S, McMahon B, Lehel S, Dyssegaard A, Skibsted AW, et al. (July 2014). "Serotonin 2A receptor agonist binding in the human brain with [¹¹C]Cimbi-36". Journal of Cerebral Blood Flow and Metabolism. 34 (7): 1188–1196. doi:10.1038/jcbfm.2014.68. PMC 4083382. PMID 24780897.
- ^ "Design and Synthesis of Selective Serotonin Receptor Agonists for Positron Emission Tomography Imaging of the Brain (Revised, Duplex print).pdf". Google Docs.
- ^ Dong C, Ly C, Dunlap LE, Vargas MV, Sun J, Hwang IW, et al. (May 2021). "Psychedelic-inspired drug discovery using an engineered biosensor". Cell. 184 (10): 2779–2792.e18. doi:10.1016/j.cell.2021.03.043. PMC 8122087. PMID 33915107.
- ^ a b Chambers JJ, Kurrasch-Orbaugh DM, Parker MA, Nichols DE (March 2001). "Enantiospecific synthesis and pharmacological evaluation of a series of super-potent, conformationally restricted 5-HT(2A/2C) receptor agonists". Journal of Medicinal Chemistry. 44 (6): 1003–1010. doi:10.1021/jm000491y. PMID 11300881.
- ^ Canal CE, Morgan D (July 2012). "Head-twitch response in rodents induced by the hallucinogen 2,5-dimethoxy-4-iodoamphetamine: a comprehensive history, a re-evaluation of mechanisms, and its utility as a model". Drug Testing and Analysis. 4 (7–8): 556–576. doi:10.1002/dta.1333. PMC 3722587. PMID 22517680.
- ^ Gatch MB, Kozlenkov A, Huang RQ, Yang W, Nguyen JD, González-Maeso J, et al. (November 2013). "The HIV antiretroviral drug efavirenz has LSD-like properties". Neuropsychopharmacology. 38 (12): 2373–2384. doi:10.1038/npp.2013.135. PMC 3799056. PMID 23702798.
- ^ Juncosa JI, Hansen M, Bonner LA, Cueva JP, Maglathlin R, McCorvy JD, et al. (January 2013). "Extensive rigid analogue design maps the binding conformation of potent N-benzylphenethylamine 5-HT2A serotonin receptor agonist ligands". ACS Chemical Neuroscience. 4 (1): 96–109. doi:10.1021/cn3000668. PMC 3547484. PMID 23336049.
- ^ Egan CT, Herrick-Davis K, Miller K, Glennon RA, Teitler M (April 1998). "Agonist activity of LSD and lisuride at cloned 5HT2A and 5HT2C receptors". Psychopharmacology. 136 (4): 409–414. doi:10.1007/s002130050585. PMID 9600588. S2CID 3021798.
- ^ Hofmann C, Penner U, Dorow R, Pertz HH, Jähnichen S, Horowski R, et al. (2006). "Lisuride, a dopamine receptor agonist with 5-HT2B receptor antagonist properties: absence of cardiac valvulopathy adverse drug reaction reports supports the concept of a crucial role for 5-HT2B receptor agonism in cardiac valvular fibrosis". Clinical Neuropharmacology. 29 (2): 80–86. doi:10.1097/00002826-200603000-00005. PMID 16614540. S2CID 33849447.
- ^ Janowsky A, Eshleman AJ, Johnson RA, Wolfrum KM, Hinrichs DJ, Yang J, et al. (July 2014). "Mefloquine and psychotomimetics share neurotransmitter receptor and transporter interactions in vitro". Psychopharmacology. 231 (14): 2771–2783. doi:10.1007/s00213-014-3446-0. PMC 4097020. PMID 24488404.
- ^ de la Fuente Revenga M, Shah UH, Nassehi N, Jaster AM, Hemanth P, Sierra S, et al. (March 2021). "Psychedelic-like Properties of Quipazine and Its Structural Analogues in Mice". ACS Chemical Neuroscience. 12 (5): 831–844. doi:10.1021/acschemneuro.0c00291. PMC 7933111. PMID 33400504.
- ^ Åstrand A, Guerrieri D, Vikingsson S, Kronstrand R, Green H (December 2020). "In vitro characterization of new psychoactive substances at the μ-opioid, CB1, 5HT1A, and 5-HT2A receptors-On-target receptor potency and efficacy, and off-target effects". Forensic Science International. 317: 110553. doi:10.1016/j.forsciint.2020.110553. PMID 33160102.
- ^ Ennis MD, Hoffman RL, Ghazal NB, Olson RM, Knauer CS, Chio CL, et al. (July 2003). "2,3,4,5-tetrahydro- and 2,3,4,5,11,11a-hexahydro-1H-[1,4]diazepino[1,7-a]indoles: new templates for 5-HT(2C) agonists". Bioorganic & Medicinal Chemistry Letters. 13 (14): 2369–2372. doi:10.1016/s0960-894x(03)00403-7. PMID 12824036.
- ^ Smith BM, Smith JM, Tsai JH, Schultz JA, Gilson CA, Estrada SA, et al. (March 2005). "Discovery and SAR of new benzazepines as potent and selective 5-HT(2C) receptor agonists for the treatment of obesity". Bioorganic & Medicinal Chemistry Letters. 15 (5): 1467–1470. doi:10.1016/j.bmcl.2004.12.080. PMID 15713408.
- ^ WO WO 2007149728, Mohapatra S, Hellberg MR, Feng Z, "아릴 및 헤테로아릴 테트라하이드로벤자제핀 유도체 및 그 녹내장 치료용", Alcon Manufacturing Ltd.
- ^ Smith BM, Smith JM, Tsai JH, Schultz JA, Gilson CA, Estrada SA, et al. (January 2008). "Discovery and structure-activity relationship of (1R)-8-chloro-2,3,4,5-tetrahydro-1-methyl-1H-3-benzazepine (Lorcaserin), a selective serotonin 5-HT2C receptor agonist for the treatment of obesity". Journal of Medicinal Chemistry. 51 (2): 305–313. doi:10.1021/jm0709034. PMID 18095642.
- ^ Jensen AA, Plath N, Pedersen MH, Isberg V, Krall J, Wellendorph P, et al. (February 2013). "Design, synthesis, and pharmacological characterization of N- and O-substituted 5,6,7,8-tetrahydro-4H-isoxazolo[4,5-d]azepin-3-ol analogues: novel 5-HT(2A)/5-HT(2C) receptor agonists with pro-cognitive properties". Journal of Medicinal Chemistry. 56 (3): 1211–1227. doi:10.1021/jm301656h. PMID 23301527.
- ^ Cao D, Yu J, Wang H, Luo Z, Liu X, He L, et al. (January 2022). "Structure-based discovery of nonhallucinogenic psychedelic analogs". Science. 375 (6579): 403–411. Bibcode:2022Sci...375..403C. doi:10.1126/science.abl8615. PMID 35084960. S2CID 246360313.
- ^ Kaplan AL, Confair DN, Kim K, Barros-Álvarez X, Rodriguiz RM, Yang Y, et al. (October 2022). "Bespoke library docking for 5-HT2A receptor agonists with antidepressant activity". Nature. 610 (7932): 582–591. Bibcode:2022Natur.610..582K. doi:10.1038/s41586-022-05258-z. PMC 9996387. PMID 36171289. S2CID 252598838.
- ^ Lyu J, Kapolka N, Gumpper R, Alon A, Wang L, Jain MK, et al. (December 2023). "AlphaFold2 structures template ligand discovery". bioRxiv. doi:10.1101/2023.12.20.572662. PMC 10769324. PMID 38187536.
- ^ Orr MJ, et al. 헤테로요힘빈 천연물에서 영감을 받은 강력한 세로토닌 5-HT2 수용체 작용제의 발견. ACS Med. 켐. Lett. 2022; 13(4):648–657. doi:10.1021/acsmedchemlett.1c00694
- ^ Sharif NA, McLaughlin MA, Kelly CR (February 2007). "AL-34662: a potent, selective, and efficacious ocular hypotensive serotonin-2 receptor agonist". Journal of Ocular Pharmacology and Therapeutics. 23 (1): 1–13. doi:10.1089/jop.2006.0093. PMID 17341144.
- ^ May JA, Dantanarayana AP, Zinke PW, McLaughlin MA, Sharif NA (January 2006). "1-((S)-2-aminopropyl)-1H-indazol-6-ol: a potent peripherally acting 5-HT2 receptor agonist with ocular hypotensive activity". Journal of Medicinal Chemistry. 49 (1): 318–328. doi:10.1021/jm050663x. PMID 16392816.
- ^ Marek GJ, Martin-Ruiz R, Abo A, Artigas F (December 2005). "The selective 5-HT2A receptor antagonist M100907 enhances antidepressant-like behavioral effects of the SSRI fluoxetine". Neuropsychopharmacology. 30 (12): 2205–2215. doi:10.1038/sj.npp.1300762. PMID 15886717.
- ^ Ishima T, Futamura T, Ohgi Y, Yoshimi N, Kikuchi T, Hashimoto K (April 2015). "Potentiation of neurite outgrowth by brexpiprazole, a novel serotonin-dopamine activity modulator: a role for serotonin 5-HT1A and 5-HT2A receptors". European Neuropsychopharmacology. 25 (4): 505–511. doi:10.1016/j.euroneuro.2015.01.014. PMID 25687838.
- ^ Das S, Barnwal P, Winston AB, Mondal S, Saha I (February 2016). "Brexpiprazole: so far so good". Therapeutic Advances in Psychopharmacology. 6 (1): 39–54. doi:10.1177/2045125315614739. PMC 4749739. PMID 26913177.
- ^ a b Pälvimäki EP, Roth BL, Majasuo H, Laakso A, Kuoppamäki M, Syvälahti E, Hietala J (August 1996). "Interactions of selective serotonin reuptake inhibitors with the serotonin 5-HT2c receptor". Psychopharmacology. 126 (3): 234–240. doi:10.1007/bf02246453. PMID 8876023. S2CID 24889381.
- ^ Rang HP (2003). Pharmacology. Edinburgh: Churchill Livingstone. ISBN 0-443-07145-4. 187페이지
- ^ Shireman BT, Dvorak CA, Rudolph DA, Bonaventure P, Nepomuceno D, Dvorak L, et al. (March 2008). "2-Alkyl-4-aryl-pyrimidine fused heterocycles as selective 5-HT2A antagonists". Bioorganic & Medicinal Chemistry Letters. 18 (6): 2103–2108. doi:10.1016/j.bmcl.2008.01.090. PMID 18282705.
- ^ Westkaemper RB, Runyon SP, Bondarev ML, Savage JE, Roth BL, Glennon RA (September 1999). "9-(Aminomethyl)-9,10-dihydroanthracene is a novel and unlikely 5-HT2A receptor antagonist". European Journal of Pharmacology. 380 (1): R5–R7. doi:10.1016/S0014-2999(99)00525-7. PMID 10513561.
- ^ Westkaemper RB, Glennon RA (June 2002). "Application of ligand SAR, receptor modeling and receptor mutagenesis to the discovery and development of a new class of 5-HT(2A) ligands". Current Topics in Medicinal Chemistry. 2 (6): 575–598. doi:10.2174/1568026023393741. PMID 12052195. S2CID 23576058.
- ^ Peddi S, Roth BL, Glennon RA, Westkaemper RB (December 2003). "Spiro[9,10-dihydroanthracene]-9,3'-pyrrolidine-a structurally unique tetracyclic 5-HT2A receptor antagonist". European Journal of Pharmacology. 482 (1–3): 335–337. doi:10.1016/j.ejphar.2003.09.059. PMID 14660041.
- ^ Runyon SP, Mosier PD, Roth BL, Glennon RA, Westkaemper RB (November 2008). "Potential modes of interaction of 9-aminomethyl-9,10-dihydroanthracene (AMDA) derivatives with the 5-HT2A receptor: a ligand structure-affinity relationship, receptor mutagenesis and receptor modeling investigation". Journal of Medicinal Chemistry. 51 (21): 6808–6828. doi:10.1021/jm800771x. PMC 3088499. PMID 18847250.
- ^ Wilson KJ, van Niel MB, Cooper L, Bloomfield D, O'Connor D, Fish LR, MacLeod AM (May 2007). "2,5-Disubstituted pyridines: the discovery of a novel series of 5-HT2A ligands". Bioorganic & Medicinal Chemistry Letters. 17 (9): 2643–2648. doi:10.1016/j.bmcl.2007.01.098. PMID 17314044.
- ^ a b Marcinkowska M, Kubacka M, Zagorska A, Jaromin A, Fajkis-Zajaczkowska N, Kolaczkowski M (January 2022). "Exploring the antiplatelet activity of serotonin 5-HT2A receptor antagonists bearing 6-fluorobenzo[d]isoxazol-3-yl)propyl) motif- as potential therapeutic agents in the prevention of cardiovascular diseases". Biomedicine & Pharmacotherapy. 145: 112424. doi:10.1016/j.biopha.2021.112424. PMID 34785417. S2CID 244111116.
- ^ Nilsson T, Longmore J, Shaw D, Pantev E, Bard JA, Branchek T, Edvinsson L (May 1999). "Characterisation of 5-HT receptors in human coronary arteries by molecular and pharmacological techniques". European Journal of Pharmacology. 372 (1): 49–56. doi:10.1016/S0014-2999(99)00114-4. PMID 10374714.
- ^ Nagatomo T, Rashid M, Abul Muntasir H, Komiyama T (October 2004). "Functions of 5-HT2A receptor and its antagonists in the cardiovascular system". Pharmacology & Therapeutics. 104 (1): 59–81. doi:10.1016/j.pharmthera.2004.08.005. PMID 15500909.
- ^ Weiner DM, Burstein ES, Nash N, Croston GE, Currier EA, Vanover KE, et al. (October 2001). "5-hydroxytryptamine2A receptor inverse agonists as antipsychotics". The Journal of Pharmacology and Experimental Therapeutics. 299 (1): 268–276. PMID 11561089.
- ^ Vanover KE, Harvey SC, Son T, Bradley SR, Kold H, Makhay M, et al. (September 2004). "Pharmacological characterization of AC-90179 [2-(4-methoxyphenyl)-N-(4-methyl-benzyl)-N-(1-methyl-piperidin-4-yl)-acetamide hydrochloride]: a selective serotonin 2A receptor inverse agonist". The Journal of Pharmacology and Experimental Therapeutics. 310 (3): 943–951. doi:10.1124/jpet.104.066688. PMID 15102927. S2CID 12205122.
- ^ Rosenberg R, Seiden DJ, Hull SG, Erman M, Schwartz H, Anderson C, et al. (December 2008). "APD125, a selective serotonin 5-HT(2A) receptor inverse agonist, significantly improves sleep maintenance in primary insomnia". Sleep. 31 (12): 1663–1671. doi:10.1093/sleep/31.12.1663. PMC 2603489. PMID 19090322.
- ^ Vanover KE, Weiner DM, Makhay M, Veinbergs I, Gardell LR, Lameh J, et al. (May 2006). "Pharmacological and behavioral profile of N-(4-fluorophenylmethyl)-N-(1-methylpiperidin-4-yl)-N'-(4-(2-methylpropyloxy)phenylmethyl) carbamide (2R,3R)-dihydroxybutanedioate (2:1) (ACP-103), a novel 5-hydroxytryptamine(2A) receptor inverse agonist". The Journal of Pharmacology and Experimental Therapeutics. 317 (2): 910–918. doi:10.1124/jpet.105.097006. PMID 16469866. S2CID 22681576.
- ^ Gardell LR, Vanover KE, Pounds L, Johnson RW, Barido R, Anderson GT, et al. (August 2007). "ACP-103, a 5-hydroxytryptamine 2A receptor inverse agonist, improves the antipsychotic efficacy and side-effect profile of haloperidol and risperidone in experimental models". The Journal of Pharmacology and Experimental Therapeutics. 322 (2): 862–870. doi:10.1124/jpet.107.121715. PMID 17519387. S2CID 28861527.
- ^ Vanover KE, Betz AJ, Weber SM, Bibbiani F, Kielaite A, Weiner DM, et al. (October 2008). "A 5-HT2A receptor inverse agonist, ACP-103, reduces tremor in a rat model and levodopa-induced dyskinesias in a monkey model". Pharmacology, Biochemistry, and Behavior. 90 (4): 540–544. doi:10.1016/j.pbb.2008.04.010. PMC 2806670. PMID 18534670.
- ^ Abbas A, Roth BL (December 2008). "Pimavanserin tartrate: a 5-HT2A inverse agonist with potential for treating various neuropsychiatric disorders". Expert Opinion on Pharmacotherapy. 9 (18): 3251–3259. doi:10.1517/14656560802532707. PMID 19040345. S2CID 71240383.
- ^ Office of the Commissioner (10 September 2019). "FDA approves first drug to treat hallucinations and delusions associated with Parkinson's disease". FDA.
- ^ Moya PR, Berg KA, Gutiérrez-Hernandez MA, Sáez-Briones P, Reyes-Parada M, Cassels BK, Clarke WP (June 2007). "Functional selectivity of hallucinogenic phenethylamine and phenylisopropylamine derivatives at human 5-hydroxytryptamine (5-HT)2A and 5-HT2C receptors". The Journal of Pharmacology and Experimental Therapeutics. 321 (3): 1054–1061. doi:10.1124/jpet.106.117507. PMID 17337633. S2CID 11651502.
- ^ González-Maeso J, Weisstaub NV, Zhou M, Chan P, Ivic L, Ang R, et al. (February 2007). "Hallucinogens recruit specific cortical 5-HT(2A) receptor-mediated signaling pathways to affect behavior". Neuron. 53 (3): 439–452. doi:10.1016/j.neuron.2007.01.008. PMID 17270739. S2CID 16309730.
- ^ Cussac D, Boutet-Robinet E, Ailhaud MC, Newman-Tancredi A, Martel JC, Danty N, Rauly-Lestienne I (October 2008). "Agonist-directed trafficking of signalling at serotonin 5-HT2A, 5-HT2B and 5-HT2C-VSV receptors mediated Gq/11 activation and calcium mobilisation in CHO cells". European Journal of Pharmacology. 594 (1–3): 32–38. doi:10.1016/j.ejphar.2008.07.040. PMID 18703043.
- ^ Schmid CL, Raehal KM, Bohn LM (January 2008). "Agonist-directed signaling of the serotonin 2A receptor depends on beta-arrestin-2 interactions in vivo". Proceedings of the National Academy of Sciences of the United States of America. 105 (3): 1079–1084. doi:10.1073/pnas.0708862105. PMC 2242710. PMID 18195357.
- ^ Abbas A, Roth BL (January 2008). "Arresting serotonin". Proceedings of the National Academy of Sciences of the United States of America. 105 (3): 831–832. Bibcode:2008PNAS..105..831A. doi:10.1073/pnas.0711335105. PMC 2242676. PMID 18195368.
- ^ Zhang G, Cheng J, McCorvy JD, Lorello PJ, Caldarone BJ, Roth BL, Kozikowski AP (July 2017). "Discovery of N-Substituted (2-Phenylcyclopropyl)methylamines as Functionally Selective Serotonin 2C Receptor Agonists for Potential Use as Antipsychotic Medications". Journal of Medicinal Chemistry. 60 (14): 6273–6288. doi:10.1021/acs.jmedchem.7b00584. PMC 7374938. PMID 28657744.
- ^ Bonis J, Furlong LI, Sanz F (October 2006). "OSIRIS: a tool for retrieving literature about sequence variants". Bioinformatics. 22 (20): 2567–2569. doi:10.1093/bioinformatics/btl421. PMID 16882651.
Supplementary material to article
- ^ Goldstein AT, Pukall C, Goldstein IL (2020). "Fibromyalgia and Female Sexual Pain Disorders". Female Sexual Pain Disorders: Evaluation and Management (2 ed.). Wiley. ISBN 978-1119482666.
- ^ a b c d Ruble CL, Smith RM, Calley J, Munsie L, Airey DC, Gao Y, et al. (January 2016). "Genomic structure and expression of the human serotonin 2A receptor gene (HTR2A) locus: identification of novel HTR2A and antisense (HTR2A-AS1) exons". BMC Genetics. 17 (1): 16. doi:10.1186/s12863-015-0325-6. PMC 4702415. PMID 26738766.
- ^ Medrihan L, Sagi Y, Inde Z, Krupa O, Daniels C, Peyrache A, Greengard P (August 2017). "Initiation of Behavioral Response to Antidepressants by Cholecystokinin Neurons of the Dentate Gyrus". Neuron. 95 (3): 564–576.e4. doi:10.1016/j.neuron.2017.06.044. PMID 28735749.
- ^ Griffin A, Hamling KR, Knupp K, Hong S, Lee LP, Baraban SC (March 2017). "Clemizole and modulators of serotonin signalling suppress seizures in Dravet syndrome". Brain. 140 (3): 669–683. doi:10.1093/brain/aww342. PMC 6075536. PMID 28073790.
- ^ Giulietti M, Vivenzio V, Piva F, Principato G, Bellantuono C, Nardi B (July 2014). "How much do we know about the coupling of G-proteins to serotonin receptors?". Molecular Brain. 7 (1): 49. doi:10.1186/s13041-014-0049-y. PMC 4105882. PMID 25011628.
- ^ Lal D, May P, Perez-Palma E, Samocha KE, Kosmicki JA, Robinson EB, et al. (March 2020). "Gene family information facilitates variant interpretation and identification of disease-associated genes in neurodevelopmental disorders". Genome Medicine. 12 (1): 28. doi:10.1186/s13073-020-00725-6. PMC 7079346. PMID 32183904.
- ^ Gao W, Guo N, Zhao S, Chen Z, Zhang W, Yan F, et al. (November 2020). "HTR2A promotes the development of cardiac hypertrophy by activating PI3K-PDK1-AKT-mTOR signaling". Cell Stress & Chaperones. 25 (6): 899–908. doi:10.1007/s12192-020-01124-x. PMC 7591670. PMID 32519137.
- ^ Cao X, Wang Y, Shu D, Qu H, Luo C, Hu X (October 2020). "Food intake-related genes in chicken determined through combinatorial genome-wide association study and transcriptome analysis". Animal Genetics. 51 (5): 741–751. doi:10.1111/age.12980. PMID 32720725. S2CID 220839883.
- ^ Garza-Brenner E, Sifuentes-Rincón AM, Randel RD, Paredes-Sánchez FA, Parra-Bracamonte GM, Arellano Vera W, et al. (August 2017). "Association of SNPs in dopamine and serotonin pathway genes and their interacting genes with temperament traits in Charolais cows". Journal of Applied Genetics. 58 (3): 363–371. doi:10.1007/s13353-016-0383-0. PMID 27987181. S2CID 34463383.
- ^ Cheah SY, Lawford BR, Young RM, Morris CP, Voisey J (January 2017). "mRNA Expression and DNA Methylation Analysis of Serotonin Receptor 2A (HTR2A) in the Human Schizophrenic Brain". Genes. 8 (1): 14. doi:10.3390/genes8010014. PMC 5295009. PMID 28054990.
- ^ Falkenberg VR, Gurbaxani BM, Unger ER, Rajeevan MS (March 2011). "Functional genomics of serotonin receptor 2A (HTR2A): interaction of polymorphism, methylation, expression and disease association". Neuromolecular Medicine. 13 (1): 66–76. doi:10.1007/s12017-010-8138-2. PMC 3044825. PMID 20941551.
- ^ Kelemen O, Convertini P, Zhang Z, Wen Y, Shen M, Falaleeva M, Stamm S (February 2013). "Function of alternative splicing". Gene. 514 (1): 1–30. doi:10.1016/j.gene.2012.07.083. PMC 5632952. PMID 22909801.
- ^ Wang ET, Ward AJ, Cherone JM, Giudice J, Wang TT, Treacy DJ, et al. (June 2015). "Antagonistic regulation of mRNA expression and splicing by CELF and MBNL proteins". Genome Research. 25 (6): 858–871. doi:10.1101/gr.184390.114. PMC 4448682. PMID 25883322.
- ^ Chee IS, Lee SW, Kim JL, Wang SK, Shin YO, Shin SC, et al. (September 2001). "5-HT2A receptor gene promoter polymorphism -1438A/G and bipolar disorder". Psychiatric Genetics. 11 (3): 111–114. doi:10.1097/00041444-200109000-00001. PMID 11702051. S2CID 39214172.
- ^ Choi MJ, Lee HJ, Lee HJ, Ham BJ, Cha JH, Ryu SH, Lee MS (2004). "Association between major depressive disorder and the -1438A/G polymorphism of the serotonin 2A receptor gene". Neuropsychobiology. 49 (1): 38–41. doi:10.1159/000075337. PMID 14730199. S2CID 19528052.
- ^ Williams J, Spurlock G, McGuffin P, Mallet J, Nöthen MM, Gill M, et al. (May 1996). "Association between schizophrenia and T102C polymorphism of the 5-hydroxytryptamine type 2a-receptor gene. European Multicentre Association Study of Schizophrenia (EMASS) Group". Lancet. 347 (9011): 1294–1296. doi:10.1016/s0140-6736(96)90939-3. PMID 8622505. S2CID 8510590.
- ^ Vaquero-Lorenzo C, Baca-Garcia E, Diaz-Hernandez M, Perez-Rodriguez MM, Fernandez-Navarro P, Giner L, et al. (July 2008). "Association study of two polymorphisms of the serotonin-2A receptor gene and suicide attempts". American Journal of Medical Genetics. Part B, Neuropsychiatric Genetics. 147B (5): 645–649. doi:10.1002/ajmg.b.30642. PMID 18163387. S2CID 31504282.
- ^ 2009년 2월 21일, HTR2A를 위한 모든 출판된 조현병-협회 연구의 유전자 개요는 조현병 연구 포럼의 웨이백 머신 – SzGene 데이터베이스에 보관되어 있습니다.
- ^ Serretti A, Drago A, De Ronchi D (2007). "HTR2A gene variants and psychiatric disorders: a review of current literature and selection of SNPs for future studies". Current Medicinal Chemistry. 14 (19): 2053–2069. doi:10.2174/092986707781368450. PMID 17691947.
- ^ Maple AM, Zhao X, Elizalde DI, McBride AK, Gallitano AL (July 2015). "Htr2a Expression Responds Rapidly to Environmental Stimuli in an Egr3-Dependent Manner". ACS Chemical Neuroscience. 6 (7): 1137–1142. doi:10.1021/acschemneuro.5b00031. PMC 4565721. PMID 25857407.
- ^ a b Williams AA, Ingram WM, Levine S, Resnik J, Kamel CM, Lish JR, et al. (September 2012). "Reduced levels of serotonin 2A receptors underlie resistance of Egr3-deficient mice to locomotor suppression by clozapine". Neuropsychopharmacology. 37 (10): 2285–2298. doi:10.1038/npp.2012.81. PMC 3422493. PMID 22692564.
- ^ Latorre E, Mesonero JE, Harries LW (November 2019). "Alternative splicing in serotonergic system: Implications in neuropsychiatric disorders". Journal of Psychopharmacology. 33 (11): 1352–1363. doi:10.1177/0269881119856546. PMID 31210090. S2CID 190531249.
- ^ Spies M, Nasser A, Ozenne B, Jensen PS, Knudsen GM, Fisher PM (November 2020). "Common HTR2A variants and 5-HTTLPR are not associated with human in vivo serotonin 2A receptor levels". Human Brain Mapping. 41 (16): 4518–4528. doi:10.1002/hbm.25138. PMC 7555071. PMID 32697408.
- ^ Qesseveur G, Petit AC, Nguyen HT, Dahan L, Colle R, Rotenberg S, et al. (June 2016). "Genetic dysfunction of serotonin 2A receptor hampers response to antidepressant drugs: A translational approach". Neuropharmacology. 105: 142–153. doi:10.1016/j.neuropharm.2015.12.022. PMID 26764241. S2CID 15031564.
- ^ Ghasemi A, Seifi M, Baybordi F, Danaei N, Samadi Rad B (June 2018). "Association between serotonin 2A receptor genetic variations, stressful life events and suicide". Gene. 658: 191–197. doi:10.1016/j.gene.2018.03.023. PMID 29526601. S2CID 4854262.
- ^ Videtic A, Pungercic G, Pajnic IZ, Zupanc T, Balazic J, Tomori M, Komel R (September 2006). "Association study of seven polymorphisms in four serotonin receptor genes on suicide victims". American Journal of Medical Genetics. Part B, Neuropsychiatric Genetics. 141B (6): 669–672. doi:10.1002/ajmg.b.30390. PMID 16856120. S2CID 9279191.
- ^ Laje G, McMahon FJ (December 2007). "The pharmacogenetics of major depression: past, present, and future". Biological Psychiatry. 62 (11): 1205–1207. doi:10.1016/j.biopsych.2007.09.016. PMID 17949692. S2CID 37225993.
- ^ Leamy TE, Connor JP, Voisey J, Young RM, Gullo MJ (December 2016). "Alcohol misuse in emerging adulthood: Association of dopamine and serotonin receptor genes with impulsivity-related cognition". Addictive Behaviors. 63: 29–36. doi:10.1016/j.addbeh.2016.05.008. PMID 27399274.
- ^ Jakubczyk A, Wrzosek M, Lukaszkiewicz J, Sadowska-Mazuryk J, Matsumoto H, Sliwerska E, et al. (January 2012). "The CC genotype in HTR2A T102C polymorphism is associated with behavioral impulsivity in alcohol-dependent patients". Journal of Psychiatric Research. 46 (1): 44–49. doi:10.1016/j.jpsychires.2011.09.001. PMC 3224206. PMID 21930285.
- ^ da Silva Junior FC, Araujo RM, Sarmento AS, de Carvalho MM, Fernandes HF, Yoshioka FK, Pinto GR, Motta FJ, Canalle R (December 2020). "The association of A-1438G and T102C polymorphisms in HTR2A and 120 bp duplication in DRD4 with alcoholic dependence in a northeastern Brazilian male population". Gene Reports. 21: 100889. doi:10.1016/j.genrep.2020.100889. S2CID 224859807.
- ^ Land MA, Ramesh D, Miller AL, Pyles RB, Cunningham KA, Moeller FG, Anastasio NC (10 June 2020). "Methylation Patterns of the HTR2A Associate With Relapse-Related Behaviors in Cocaine-Dependent Participants". Frontiers in Psychiatry. 11: 532. doi:10.3389/fpsyt.2020.00532. PMC 7299072. PMID 32587535.
- ^ Lemaire C, Cantineau R, Guillaume M, Plenevaux A, Christiaens L (December 1991). "Fluorine-18-altanserin: a radioligand for the study of serotonin receptors with PET: radiolabeling and in vivo biologic behavior in rats". Journal of Nuclear Medicine. 32 (12): 2266–2272. PMID 1744713.
- ^ Lundkvist C, Halldin C, Ginovart N, Nyberg S, Swahn CG, Carr AA, et al. (1996). "[11C]MDL 100907, a radioligland for selective imaging of 5-HT(2A) receptors with positron emission tomography". Life Sciences. 58 (10): PL 187-PL 192. doi:10.1016/0024-3205(96)00013-6. PMID 8602111.
- ^ Johansen A, Hansen HD, Svarer C, Lehel S, Leth-Petersen S, Kristensen JL, et al. (April 2018). "The importance of small polar radiometabolites in molecular neuroimaging: A PET study with [11C]Cimbi-36 labeled in two positions". Journal of Cerebral Blood Flow and Metabolism. 38 (4): 659–668. doi:10.1177/0271678x17746179. PMC 5888860. PMID 29215308.
- ^ Mintun MA, Sheline YI, Moerlein SM, Vlassenko AG, Huang Y, Snyder AZ (February 2004). "Decreased hippocampal 5-HT2A receptor binding in major depressive disorder: in vivo measurement with [18F]altanserin positron emission tomography". Biological Psychiatry. 55 (3): 217–224. doi:10.1016/j.biopsych.2003.08.015. PMID 14744461. S2CID 24849671.
- ^ Rosier A, Dupont P, Peuskens J, Bormans G, Vandenberghe R, Maes M, et al. (November 1996). "Visualisation of loss of 5-HT2A receptors with age in healthy volunteers using [18F]altanserin and positron emission tomographic imaging". Psychiatry Research. 68 (1): 11–22. doi:10.1016/S0925-4927(96)02806-5. PMID 9027929. S2CID 32317795.
- ^ Meltzer CC, Smith G, Price JC, Reynolds CF, Mathis CA, Greer P, et al. (November 1998). "Reduced binding of [18F]altanserin to serotonin type 2A receptors in aging: persistence of effect after partial volume correction". Brain Research. 813 (1): 167–171. doi:10.1016/S0006-8993(98)00909-3. PMID 9824691. S2CID 21884218.
- ^ Adams KH, Pinborg LH, Svarer C, Hasselbalch SG, Holm S, Haugbøl S, et al. (March 2004). "A database of [(18)F]-altanserin binding to 5-HT(2A) receptors in normal volunteers: normative data and relationship to physiological and demographic variables". NeuroImage. 21 (3): 1105–1113. doi:10.1016/j.neuroimage.2003.10.046. PMID 15006678. S2CID 24403109.
더보기
- Perez-Aguilar JM, Shan J, LeVine MV, Khelashvili G, Weinstein H (November 2014). "A functional selectivity mechanism at the serotonin-2A GPCR involves ligand-dependent conformations of intracellular loop 2". Journal of the American Chemical Society. 136 (45): 16044–16054. doi:10.1021/ja508394x. PMC 4235374. PMID 25314362.
외부 링크
- "5-HT2A". IUPHAR Database of Receptors and Ion Channels. International Union of Basic and Clinical Pharmacology.