로돕신
Rhodopsin| RHO | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 에일리어스 | RHO, CSNBAD1, OPN2, RP4, 로돕신, 로돕신, 비주얼 퍼플 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 외부 ID | OMIM: 180380 MGI: 97914 HomoloGene: 68068 GeneCard: RHO | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
비주얼 퍼플로도 알려진 로돕신은 시각적 광전달을 수반하는 빛에 민감한 수용체 단백질이다.이것의 이름은 분홍빛을 띠기 때문에 "장미"를 뜻하는 고대 그리스어 로돈과 "시각"[5]을 뜻하는 "시스(pspsis)에서 유래했다.로돕신은 망막의 막대에서 발견되는 생물학적 색소로 G단백질결합수용체(GPCR)이다.포토스위치 가능한 opsin 그룹에 속합니다.Rhodopsin은 빛에 매우 민감하기 때문에 낮은 조도 [6]조건에서도 시력을 유지할 수 있습니다.로돕신이 빛에 노출되면, 그것은 즉시 광탈색을 한다.인간의 경우, 약 30분 안에 완전히 재생되고, 그 이후에는 막대가 더 [7]민감해진다.
로돕신은 1876년 [8][9]프란츠 크리스티안 볼에 의해 발견되었다.
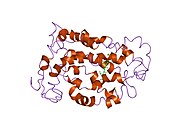
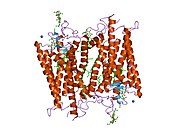
구조.
로돕신은 또한 스코탑신이라고도 불리는 단백질 분자와 레티날이라고 불리는 공유 결합 보조 인자의 두 가지 성분으로 구성되어 있습니다.Scotopsin은 7개의 단백질 트랜스막 도메인을 사용하여 세포막의 지질 이중층에 내장된 빛에 민감한 G 단백질 결합 수용체인 옵신이다.이러한 도메인은 광반응 색소체인 레티날(retinal)이 세포막에 수평으로 놓여 단백질의 7번째 막 통과 영역의 리신 잔기와 연결된 포켓을 형성합니다.수천 개의 로돕신 분자가 숙주 세포 각각의 바깥 부분 디스크에서 발견됩니다.망막은 망막에서 레티놀로부터 생성된다.빛에 의한 11-시스-레티날로의 이성화는 옵신의 일련의 구조 변화('표백')를 일으켜 최종적으로 메타호돕신II(Meta II)라고 불리는 형태로 유도되며, 이는 관련된 G단백질 트랜스듀신을 활성화하여 고리형 구아노신 모노인산(CMP) [7][10][11]2차 전달자를 트리거한다.
로돕신은 녹색과 푸른 빛을 가장 강하게 흡수하기 때문에 붉은 보라색을 띠기 때문에 "시각적 보라색"[12]이라고도 불립니다.그것은 [7]어둠 속에서 단색의 시력을 발생시킨다.
몇몇 밀접하게 관련된 옵신들은 오직 몇 개의 아미노산과 그들이 가장 강하게 흡수하는 빛의 파장에서만 다릅니다.인간은 로돕신 외에 크립토크롬(빛에 민감하지만 옵신은 [13][14]아니다) 8가지 다른 옵신을 가지고 있다.
포토옵신은 망막의 원추세포에서 발견되며 색각의 기초가 된다.그들은 황록색(포탑신I), 녹색(포탑신II), 청자색(포탑신II) 빛에 대한 흡수 최대치를 가지고 있다.나머지 옵신인 멜라놉신은 감광성 신경절 세포에서 발견되며 푸른 빛을 가장 강하게 흡수합니다.
로돕신에서 레티날 알데히드기는 프로톤화 쉬프염기(-NH+=CH-)[15]에서 단백질상의 리신잔기의 아미노기와 공유결합한다.로돕신이 빛을 흡수할 때 망막 보조인자는 11-cis에서 전트랜스 구성으로 이성화되며, 그 후 단백질은 이성화 보조인자의 변화된 형상을 수용하기 위해 일련의 이완을 거친다.이 과정에서 형성된 중간체들은 1967년 [16]노벨상을 받은 조지 월드의 연구실에서 처음 조사되었다.광이성화 역학은 이후 시간 분해 IR 분광법과 UV/Vis 분광법으로 연구되었다.조사 후 200펨토초 이내에 포토호돕신이라고 불리는 첫 번째 광생성이 형성되고, 뒤이어 왜곡된 전트랜스 결합을 가진 바토호돕신이라고 불리는 두 번째 광생성이 피코초 내에 형성된다.이 중간체는 극저온 온도에서 포착되어 연구될 수 있으며, 처음에는 preplumirhodopsin이라고 [17]불렸다.후속 중간체 루미르호돕신 및 메타호돕신I에서는 전트랜스망막에 대한 쉬프의 염기결합이 양성자화된 상태로 유지되며 단백질은 불그스름한 색을 유지한다.신경 들뜸을 시작하는 중요한 변화는 메타호돕신 I을 메타호돕신 II로 변환하는 것을 포함하는데, 이것은 쉬프의 염기의 탈양성화 및 빨간색에서 [18]노란색으로의 색 변화와 관련이 있습니다.
Rhodopsin의 구조는 Rhodopsin [19]결정의 X선 결정학을 통해 상세하게 연구되었다.여러 모델(예: 자전거 페달 메커니즘, 훌라 트위스트 메커니즘)은 망막 그룹이 포위된 로돕신 단백질 [20][21][22]포켓과 충돌하지 않고 어떻게 구조를 바꿀 수 있는지를 설명하려고 시도한다.최근 데이터는 로돕신이 이합체 대신 기능성 단량체라는 것을 뒷받침하는데, 이는 수년간 [23]G단백질 결합 수용체의 패러다임이었다.
광전송
로돕신은 광전달을 위한 필수 G단백질 결합 수용체이다.
기능.
빛 활성화의 산물인 메타호돕신 II는 G단백질 트랜스신(Gt)을 자극하여 시각적 광전달 경로를 개시하여 α 서브유닛을 해방시킨다.이 GTP 결합 서브유닛은 차례로 cGMP 포스포디에스테라아제를 활성화한다.cGMP 포스포디에스테라아제는 cGMP를 가수분해(분해)하여 cGMP 의존성 양이온 채널을 더 이상 활성화할 수 없도록 국소 농도를 낮춘다.이것은 광수용체 세포의 과분극으로 이어져 전달체를 방출하는 속도를 변화시킨다.
비활성화
메타II(메타호돕신II)는 로돕신인산화효소 및 아레스틴에 [24]의해 트랜스신을 활성화한 후 빠르게 비활성화된다.로돕신 색소는 추가 광전달을 위해 재생되어야 합니다.즉, 모든 트랜스 레티날(trans-retinal)을 11-cis-retinal(cis-retinal)로 대체하고, 이 과정에서 Meta II의 붕괴가 매우 중요합니다.Meta II의 붕괴 동안, 일반적으로 모든 트랜스 레티날과 아포단백질 옵신(aporhodopsin)을 유지하는 쉬프 염기 연결은 가수분해되어 Meta III가 된다.로드 외측 세그먼트에서 Meta III는 별도의 All-trans-retinal 및 opsin으로 [24]분해됩니다.Meta II 붕괴의 두 번째 산물은 전경망막 복합체이며, 전경망막 복합체는 전경망막 결합 부위로 이동되었다.Meta II 붕괴가 Meta III로 가는지 아니면 전망막 옵신 복합체로 가는지 여부는 반응의 pH에 따라 달라지는 것으로 보인다.높은 pH는 Meta [24]III를 향해 붕괴 반응을 일으키는 경향이 있다.
망막병
로돕신 유전자의 돌연변이는 색소성 망막염과 같은 다양한 망막 질환의 주요 원인이다.일반적으로 질병을 일으키는 단백질은 포접체 내의 유비퀴틴과 함께 응집되어 중간 필라멘트 네트워크를 교란시키고 세포의 기능하지 않는 단백질 분해 능력을 손상시켜 광수용체 아포토시스를 [25]일으킨다.로돕신의 [26]색소 결합 포켓 주변에서 돌연변이가 발생할 경우, 주로 구성 활성화에 의해 X-연관 선천성 고정 야맹증으로 이어진다.로돕신과 관련된 몇 가지 다른 병리학적 상태가 발견되었는데, 여기에는 골기 후 교통 불량, 조절 불능 활성화, 로드 외측 세그먼트의 불안정성 및 아레스틴 [26]결합이 포함된다.
미생물 로돕신
일부 원핵생물들은 광축성을 [27]수행하기 위해 박테리올호돕신, 아르카에르호돕신, 프로테오르호돕신, 헬리오르호돕신, 크산토르호돕신이라고 불리는 양성자 펌프를 발현시킨다.동물성 시각 색소와 마찬가지로, 이것들은 망막 색소를 포함하고 있고 (비록 11-cis 형태가 아닌 전-트랜스이지만) 7개의 막 통과 알파 나선을 가지고 있다. 그러나 그것들은 G 단백질과 결합되지 않는다.원핵생물 할로호돕신은 빛으로 활성화된 염화물 [27]펌프이다.단세포 편모조류는 이종 시스템에서 발현될 때 광 게이트 양이온 채널로 작용하는 채널로돕신을 포함하고 있습니다.다른 많은 친핵생물 및 진핵생물(특히 Neurospora와 같은 균류)은 아직 알려지지 않은 기능의 로돕신 이온 펌프 또는 감각 로돕신을 발현한다.최근에 구아닐 사이클라아제 활성을 가진 미생물 로돕신이 발견되었다.[28][29][30]모든 미생물 로돕신은 서로에 대해 유의한 배열 상동성을 가지지만, 동물 시각 로돕신이 속한 G-단백질 결합 수용체(GPCR) 패밀리에 대한 검출 가능한 배열 상동성을 가지지 않는다.그럼에도 불구하고 미생물 로돕신과 GPCR은 3차원 구조의 유사성에 기초하여 진화적으로 관련이 있을 수 있다.따라서 단백질 구조분류(SCOP)[31]에서 동일한 슈퍼패밀리에 할당되었다.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000163914 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000030324 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Guest Editorial Essay, Perception, 2008, p. 1
- ^ Litmann BJ, Mitchell DC (1996). "Rhodopsin structure and function". In Lee AG (ed.). Rhodopsin and G-Protein Linked Receptors, Part A (Vol 2, 1996) (2 Vol Set). Greenwich, Conn: JAI Press. pp. 1–32. ISBN 978-1-55938-659-3.
- ^ a b c Stuart JA, Brige RR (1996). "Characterization of the primary photochemical events in bacteriorhodopsin and rhodopsin". In Lee AG (ed.). Rhodopsin and G-Protein Linked Receptors, Part A (Vol 2, 1996) (2 Vol Set). Greenwich, Conn: JAI Press. pp. 33–140. ISBN 978-1-55938-659-3.
- ^ Encyclopedia of the Neurological Sciences. Academic Press. 29 April 2014. pp. 441–. ISBN 978-0-12-385158-1.
- ^ Giese AC (24 September 2013). Photophysiology: General Principles; Action of Light on Plants. Elsevier. p. 9. ISBN 978-1-4832-6227-7. Retrieved 23 September 2015.
- ^ Hofmann KP, Heck M (1996). "Light-induced protein-protein interactions on the rod photoreceptor disc membrane". In Lee AG (ed.). Rhodopsin and G-Protein Linked Receptors, Part A (Vol 2, 1996) (2 Vol Set). Greenwich, Conn: JAI Press. pp. 141–198. ISBN 978-1-55938-659-3.
- ^ Kolb H, Fernandez E, Nelson R, Jones BW (1 March 2010). "Webvision: Photoreceptors". University of Utah. Archived from the original on 16 August 2000.
- ^ Rogers K. "Rhodopsin". Encyclopædia Britannica. Britannica.com. Retrieved 30 January 2016.
- ^ Terakita A (2005). "The opsins". Genome Biology. 6 (3): 213. doi:10.1186/gb-2005-6-3-213. PMC 1088937. PMID 15774036.
- ^ Foley LE, Gegear RJ, Reppert SM (June 2011). "Human cryptochrome exhibits light-dependent magnetosensitivity". Nature Communications. 2: 356. Bibcode:2011NatCo...2..356F. doi:10.1038/ncomms1364. PMC 3128388. PMID 21694704.
- ^ Bownds D, Wald G (January 1965). "Reaction of the rhodopsin chromophore with sodium borohydride". Nature. 205 (4968): 254–7. Bibcode:1965Natur.205..254B. doi:10.1038/205254a0. PMID 14270706. S2CID 4226447.
- ^ The Nobel Foundation. "The Nobel Prize in Physiology or Medicine 1967". Nobelprize.org. Nobel Media AB 2014. Retrieved 12 December 2015.
- ^ Yoshizawa T, Wald G (March 1963). "Pre-lumirhodopsin and the bleaching of visual pigments". Nature. 197 (Mar 30): 1279–86. Bibcode:1963Natur.197.1279Y. doi:10.1038/1971279a0. PMID 14002749. S2CID 4263392.
- ^ Matthews RG, Hubbard R, Brown PK, Wald G (November 1963). "Tautomeric forms of metarhodopsin". The Journal of General Physiology. 47 (2): 215–40. doi:10.1085/jgp.47.2.215. PMC 2195338. PMID 14080814.
- ^ Gulati S, Jastrzebska B, Banerjee S, Placeres ÁL, Miszta P, Gao S, Gunderson K, Tochtrop GP, Filipek S, Katayama K, Kiser PD, Mogi M, Stewart PL, Palczewski K (March 2017). "Photocyclic behavior of rhodopsin induced by an atypical isomerization mechanism". Proceedings of the National Academy of Sciences. 114 (13): E2608-15. doi:10.1073/pnas.1617446114. PMC 5380078. PMID 28289214.
- ^ Nakamichi H, Okada T (June 2006). "Crystallographic analysis of primary visual photochemistry". Angewandte Chemie. 45 (26): 4270–3. doi:10.1002/anie.200600595. PMID 16586416.
- ^ Schreiber M, Sugihara M, Okada T, Buss V (June 2006). "Quantum mechanical studies on the crystallographic model of bathorhodopsin". Angewandte Chemie. 45 (26): 4274–7. doi:10.1002/anie.200600585. PMID 16729349.
- ^ Weingart O (September 2007). "The twisted C11=C12 bond of the rhodopsin chromophore--a photochemical hot spot". Journal of the American Chemical Society. 129 (35): 10618–9. doi:10.1021/ja071793t. PMID 17691730.
- ^ Chabre M, le Maire M (July 2005). "Monomeric G-protein-coupled receptor as a functional unit". Biochemistry. 44 (27): 9395–403. doi:10.1021/bi050720o. PMID 15996094.
- ^ a b c Heck M, Schädel SA, Maretzki D, Bartl FJ, Ritter E, Palczewski K, Hofmann KP (January 2003). "Signaling states of rhodopsin. Formation of the storage form, metarhodopsin III, from active metarhodopsin II". The Journal of Biological Chemistry. 278 (5): 3162–9. doi:10.1074/jbc.M209675200. PMC 1364529. PMID 12427735.
- ^ Saliba RS, Munro PM, Luthert PJ, Cheetham ME (July 2002). "The cellular fate of mutant rhodopsin: quality control, degradation and aggresome formation". Journal of Cell Science. 115 (Pt 14): 2907–18. doi:10.1242/jcs.115.14.2907. PMID 12082151.
- ^ a b Mendes HF, van der Spuy J, Chapple JP, Cheetham ME (April 2005). "Mechanisms of cell death in rhodopsin retinitis pigmentosa: implications for therapy". Trends in Molecular Medicine. 11 (4): 177–85. doi:10.1016/j.molmed.2005.02.007. PMID 15823756.
- ^ a b Bryant DA, Frigaard NU (November 2006). "Prokaryotic photosynthesis and phototrophy illuminated". Trends in Microbiology. 14 (11): 488–96. doi:10.1016/j.tim.2006.09.001. PMID 16997562.
- ^ Gao SQ, Nagpal J, Schneider MW, Kozjak-Pavlovic V, Nagel G, Gottschalk A (July 2015). "Optogenetic manipulation of cGMP in cells and animals by the tightly light-regulated guanylyl-cyclase opsin CyclOp". Nature Communications. 6 (8046): 8046. Bibcode:2015NatCo...6.8046G. doi:10.1038/ncomms9046. PMC 4569695. PMID 26345128.
- ^ Scheib U, Stehfest K, Gee CE, Körschen HG, Fudim R, Oertner TG, Hegemann P (August 2015). "The rhodopsin-guanylyl cyclase of the aquatic fungus Blastocladiella emersonii enables fast optical control of cGMP signaling". Science Signaling. 8 (389): rs8. doi:10.1126/scisignal.aab0611. PMID 26268609. S2CID 13140205.
- ^ Scheib U, Broser M, Constantin OM, Yang S, Gao S, Mukherjee S, et al. (May 2018). "Rhodopsin-cyclases for photocontrol of cGMP/cAMP and 2.3 Å structure of the adenylyl cyclase domain". Nature Communications. 9 (1): 2046. Bibcode:2018NatCo...9.2046S. doi:10.1038/s41467-018-04428-w. PMC 5967339. PMID 29799525.
- ^ "Superfamily: Bacterial photosystem II reaction centre, L and M subunits". SCOP.
추가 정보
- Humphries P, Kenna P, Farrar GJ (May 1992). "On the molecular genetics of retinitis pigmentosa". Science. 256 (5058): 804–8. Bibcode:1992Sci...256..804H. doi:10.1126/science.1589761. PMID 1589761.
- Edwards SC (July 1995). "Involvement of cGMP and calcium in the photoresponse in vertebrate photoreceptor cells". The Journal of the Florida Medical Association. 82 (7): 485–8. PMID 7673885.
- al-Maghtheh M, Gregory C, Inglehearn C, Hardcastle A, Bhattacharya S (1993). "Rhodopsin mutations in autosomal dominant retinitis pigmentosa". Human Mutation. 2 (4): 249–55. doi:10.1002/humu.1380020403. PMID 8401533. S2CID 28459589.
- Garriga P, Manyosa J (September 2002). "The eye photoreceptor protein rhodopsin. Structural implications for retinal disease". FEBS Letters. 528 (1–3): 17–22. doi:10.1016/S0014-5793(02)03241-6. PMID 12297272. S2CID 41860711.
- Inglehearn CF, Keen TJ, Bashir R, Jay M, Fitzke F, Bird AC, Crombie A, Bhattacharya S (April 1992). "A completed screen for mutations of the rhodopsin gene in a panel of patients with autosomal dominant retinitis pigmentosa". Human Molecular Genetics. 1 (1): 41–5. doi:10.1093/hmg/1.1.41. PMID 1301135.
- Farrar GJ, Findlay JB, Kumar-Singh R, Kenna P, Humphries MM, Sharpe E, Humphries P (December 1992). "Autosomal dominant retinitis pigmentosa: a novel mutation in the rhodopsin gene in the original 3q linked family". Human Molecular Genetics. 1 (9): 769–71. doi:10.1093/hmg/1.9.769. PMID 1302614.
- Robinson PR, Cohen GB, Zhukovsky EA, Oprian DD (October 1992). "Constitutively active mutants of rhodopsin". Neuron. 9 (4): 719–25. doi:10.1016/0896-6273(92)90034-B. PMID 1356370. S2CID 13172583.
- Fujiki K, Hotta Y, Hayakawa M, Sakuma H, Shiono T, Noro M, Sakuma T, Tamai M, Hikiji K, Kawaguchi R (June 1992). "Point mutations of rhodopsin gene found in Japanese families with autosomal dominant retinitis pigmentosa (ADRP)". The Japanese Journal of Human Genetics. 37 (2): 125–32. doi:10.1007/BF01899733. PMID 1391967.
- Olsson JE, Gordon JW, Pawlyk BS, Roof D, Hayes A, Molday RS, Mukai S, Cowley GS, Berson EL, Dryja TP (November 1992). "Transgenic mice with a rhodopsin mutation (Pro23His): a mouse model of autosomal dominant retinitis pigmentosa". Neuron. 9 (5): 815–30. doi:10.1016/0896-6273(92)90236-7. PMID 1418997. S2CID 37524461.
- Andréasson S, Ehinger B, Abrahamson M, Fex G (September 1992). "A six-generation family with autosomal dominant retinitis pigmentosa and a rhodopsin gene mutation (arginine-135-leucine)". Ophthalmic Paediatrics and Genetics. 13 (3): 145–53. doi:10.3109/13816819209046483. PMID 1484692.
- Inglehearn CF, Lester DH, Bashir R, Atif U, Keen TJ, Sertedaki A, Lindsey J, Jay M, Bird AC, Farrar GJ (March 1992). "Recombination between rhodopsin and locus D3S47 (C17) in rhodopsin retinitis pigmentosa families". American Journal of Human Genetics. 50 (3): 590–7. PMC 1684283. PMID 1539595.
- Fishman GA, Stone EM, Gilbert LD, Sheffield VC (May 1992). "Ocular findings associated with a rhodopsin gene codon 106 mutation. Glycine-to-arginine change in autosomal dominant retinitis pigmentosa". Archives of Ophthalmology. 110 (5): 646–53. doi:10.1001/archopht.1992.01080170068026. PMID 1580841.
- Keen TJ, Inglehearn CF, Lester DH, Bashir R, Jay M, Bird AC, Jay B, Bhattacharya SS (September 1991). "Autosomal dominant retinitis pigmentosa: four new mutations in rhodopsin, one of them in the retinal attachment site". Genomics. 11 (1): 199–205. doi:10.1016/0888-7543(91)90119-Y. PMID 1765377.
- Dryja TP, Hahn LB, Cowley GS, McGee TL, Berson EL (October 1991). "Mutation spectrum of the rhodopsin gene among patients with autosomal dominant retinitis pigmentosa". Proceedings of the National Academy of Sciences of the United States of America. 88 (20): 9370–4. Bibcode:1991PNAS...88.9370D. doi:10.1073/pnas.88.20.9370. PMC 52716. PMID 1833777.
- Gal A, Artlich A, Ludwig M, Niemeyer G, Olek K, Schwinger E, Schinzel A (October 1991). "Pro-347-Arg mutation of the rhodopsin gene in autosomal dominant retinitis pigmentosa". Genomics. 11 (2): 468–70. doi:10.1016/0888-7543(91)90159-C. PMID 1840561.
- Sung CH, Davenport CM, Hennessey JC, Maumenee IH, Jacobson SG, Heckenlively JR, Nowakowski R, Fishman G, Gouras P, Nathans J (August 1991). "Rhodopsin mutations in autosomal dominant retinitis pigmentosa". Proceedings of the National Academy of Sciences of the United States of America. 88 (15): 6481–5. Bibcode:1991PNAS...88.6481S. doi:10.1073/pnas.88.15.6481. PMC 52109. PMID 1862076.
- Jacobson SG, Kemp CM, Sung CH, Nathans J (September 1991). "Retinal function and rhodopsin levels in autosomal dominant retinitis pigmentosa with rhodopsin mutations". American Journal of Ophthalmology. 112 (3): 256–71. doi:10.1016/s0002-9394(14)76726-1. PMID 1882937.
- Sheffield VC, Fishman GA, Beck JS, Kimura AE, Stone EM (October 1991). "Identification of novel rhodopsin mutations associated with retinitis pigmentosa by GC-clamped denaturing gradient gel electrophoresis". American Journal of Human Genetics. 49 (4): 699–706. PMC 1683182. PMID 1897520.