죽상경화증
Atherosclerosis| 죽상경화증 | |
|---|---|
| 기타이름 | 동맥경화성 혈관질환(ASVD) |
 | |
| 죽상동맥경화증의 진행(좁은 과장) | |
| 전문 | 심장학, 혈관학 |
| 증상 | 없음[1] |
| 합병증 | 관상동맥질환, 뇌졸중, 말초동맥질환, 신장문제[1] |
| 보통발병 | 청춘(나이가 들수록 나빠짐)[2] |
| 원인들 | 알[1] 수 없음 |
| 위험요소 | 고혈압, 당뇨병, 흡연, 비만, 가족력, 건강하지 못한 식단(특히 트랜스지방), 만성 비타민C 결핍[3][4] |
| 예방 | 건강한 식단, 운동, 금연, 정상 체중[5] 유지 |
| 약 | 스타틴, 혈압약, 아스피린[6] |
| 빈도수. | ≈100%(>65세) |
동맥경화증은 동맥벽에 병변이라는 이상이 생기는 [8]것이 특징인 동맥경화증의 한 형태입니다. 이러한 병변은 동맥의 혈전성 플라크 축적으로 인해 동맥벽이 좁아질 수 있습니다.[9][10] 초기에는 보통 증상이 없지만 발병하면 일반적으로 중년 무렵에 증상이 시작됩니다.[1] 심할 경우, 영향을 받는 동맥이 신체의 어느 부분에 위치하는지에 따라 관상동맥 질환, 뇌졸중, 말초동맥 질환, 신장 장애를 초래할 수 있습니다.[1]
죽상동맥경화증의 정확한 원인은 알려지지 않았으며 다인성으로 제안됩니다.[1] 위험 요소에는 비정상적인 콜레스테롤 수치, 염증 바이오마커 수치 상승,[11] 고혈압, 당뇨병, 흡연(적극적인 흡연과 수동적인 흡연 모두), 비만, 유전적 요인, 가족력, 생활 습관, 건강하지 못한 식단이 포함됩니다.[4] 플라크는 혈액에서 발견되는 지방, 콜레스테롤, 칼슘 및 기타 물질로 구성되어 있습니다.[9] 동맥이 좁아지는 것은 산소가 풍부한 혈액의 흐름을 신체의 일부로 제한합니다.[9] 진단은 신체 검사, 심전도 및 운동 스트레스 테스트 등을 기반으로 합니다.[12]
예방 지침에는 건강한 식단 섭취, 운동, 금연, 정상 체중 유지 등이 포함됩니다.[5] 확립된 질병의 치료에는 스타틴과 같은 콜레스테롤을 낮추는 약물, 혈압약, 혈전 형성의 위험을 줄이기 위한 항응고 요법이 포함될 수 있습니다.[6] 질병 상태가 진행됨에 따라 경피적 관상동맥 중재술, 관상동맥 우회 이식술 또는 경동맥 내막 절제술과 같은 침습적인 전략이 적용됩니다.[6] 유전적 요인도 질병 과정에 강하게 관련되어 있습니다; 그것은 전적으로 생활 방식의 선택에 근거하지 않습니다.[13]
죽상경화증은 일반적으로 젊었을 때 시작되어 나이가 들면서 악화됩니다.[2] 거의 모든 사람들이 65세의 나이에 어느 정도 영향을 받습니다.[7] 선진국의 사망과 장애 원인 1위입니다.[14][15][16] 1575년에 처음 기술되었지만요.[17]이 질병 상태가 유전적으로 더 광범위한 인간 집단에 내재되어 있음을 시사하는 증거가 있으며, 그 기원은 현대 인류의 조상인 호미닌이 진화하는 동안 2백만 년 이상 전에 발생했을 수 있는 유전적 돌연변이로 거슬러 올라갑니다.[18]
징후 및 증상
동맥이 모든 플라크 위치에서 확장되어 혈류에 영향이 없기 때문에 죽상경화증은 수십 년 동안 증상이 없습니다.[19] 혈전으로 인해 동맥이 충분히 좁아지거나 닫힐 때까지 대부분의 플라크 파열은 증상을 나타내지 않습니다. 증상을 유발할 정도로 심한 협착이나 폐쇄가 다른 장기로의 혈류 흐름을 방해한 후에야 징후와 증상이 나타납니다.[20] 대부분의 경우, 환자들은 뇌졸중이나 심장마비와 같은 다른 심혈관 질환을 경험해야만 자신이 이 질병에 걸렸다는 것을 깨닫게 됩니다. 그러나 이러한 증상은 어떤 동맥이나 기관이 영향을 받는지에 따라 여전히 다릅니다.[21]
초기 죽상경화 과정은 어린 시절부터 시작될 가능성이 높습니다. 소아의 관상동맥에서 섬유성 및 젤라틴성 병변이 관찰되었습니다.[22] 지방줄기가 청소년의 관상동맥에서 관찰되었습니다.[22]관상동맥질환은 여성보다 남성에게 더 많이 발병하지만, 뇌동맥의 죽상동맥경화증과 뇌졸중은 남녀 모두에게 똑같이 영향을 미칩니다.[23]
산소화된 혈액을 심장으로 가져오는 역할을 하는 관상동맥이 현저하게 좁아지면 협심증의 흉통과 호흡 곤란, 땀, 메스꺼움, 현기증 또는 현기증, 호흡 곤란 또는 두근거림과 같은 증상이 나타날 수 있습니다.[21] 허혈의 또 다른 결과는 심장이 너무 느리게 혹은 너무 빨리 뛰는 부정맥이라고 불리는 비정상적인 심장 리듬입니다.[24]
경동맥은 뇌와 목에 혈액을 공급합니다.[24] 경동맥의 현저한 협착은 다음과 같은 증상을 나타낼 수 있습니다: 쇠약감; 직설적인 생각을 할 수 없음; 말을 할 수 없음; 어지러움; 직설적으로 걷거나 일어설 수 없음; 시야가 흐려짐; 얼굴, 팔, 다리의 저림, 심한 두통 및 의식 상실. 이러한 증상은 뇌졸중(뇌세포의 사망)과도 관련이 있습니다. 뇌졸중은 뇌로 가는 동맥의 현저한 좁아짐 또는 폐쇄로 인해 발생합니다. 적절한 혈액 공급의 부족은 영향을 받은 조직의 세포의 죽음으로 이어집니다.[25]
다리와 팔, 골반에 혈액을 공급하는 말초동맥도 플라크 파열과 응혈로 눈에 띄게 좁아지는 증상이 나타납니다. 좁아지는 증상은 통증뿐만 아니라 팔이나 다리가 저리는 것입니다. 플라크 형성의 또 다른 중요한 위치는 신장에 혈액을 공급하는 신장 동맥입니다. 플라크의 발생과 축적은 신장 혈류 감소와 만성 신장 질환을 유발하는데, 다른 모든 부위와 마찬가지로 일반적으로 후기까지 무증상입니다.[21]
2004년 미국 데이터에 따르면 남성의 ~66%, 여성의 ~47%에서 죽상경화성 심혈관 질환의 첫 번째 증상은 심장마비 또는 갑작스러운 심장 사망(증상 시작 후 1시간 이내 사망으로 정의됨)이었습니다.[26]
사례 연구에는 2차 세계 대전과 한국 전쟁에서 사망한 미군들의 부검이 포함되었습니다. 많은 사람들이 인용하는 보고서는 한국에서 사망한 300명의 미군들의 부검과 관련이 있습니다. 남성의 평균 나이는 22.1세였지만 77.3%는 "관상동맥경화증의 심각한 증거"를 가지고 있었습니다.[27]
위험요소

죽상경화 과정은 잘 알려져 있지 않습니다. 죽상경화증은 저밀도 지단백(LDL) 입자가 남아있는 혈관벽의 내피 세포에서 염증 과정과 관련이 있습니다.[28][29] 이러한 저류는 근본적인 염증 과정의 원인, 결과 또는 둘 다일 수 있습니다.[30]
플라크의 존재는 혈관의 근육 세포가 늘어나도록 유도하여 추가적인 벌크를 보상합니다. 그런 다음 내피 안감이 두꺼워져 플라크와 내강 사이의 분리가 증가합니다. 두꺼워지는 것은 플라크의 성장으로 인한 좁아지는 것을 다소 상쇄하지만, 더욱이 벽이 뻣뻣해지고 심장박동마다 스트레칭에 덜 순응하게 됩니다.[31]
수정가능
수정 불가
작거나 불확실함
- 혈소판증가증[39][40][41]
- 포화지방[32][42]
- 탄수화물[32][43] 과다
- 중성지방[32] 증가
- 전신염증[44]
- 고인슐린혈증[45]
- 수면부족[46]
- 대기오염[47][48]
- 좌식생활[32]
- 비소중독[49]
- 술[32][failed 확인]
- 만성 스트레스[32]
- 갑상선기능저하증[50]
- 치주질환[51]
식이요법
식이 지방과 죽상경화증의 관계는 논란의 여지가 있습니다. USDA는 식품 피라미드에서 총 칼로리에서 약 64%의 탄수화물을 섭취하는 식단을 장려합니다. 미국 심장 협회, 미국 당뇨병 협회, 그리고 미국 콜레스테롤 교육 프로그램도 비슷한 권고를 합니다. 대조적으로, 월터 윌렛 교수(하버드 공중 보건 대학, 두 번째 간호사 건강 연구의 PI)는 훨씬 더 높은 수준의 지방, 특히 단불포화 지방과 다불포화 지방을 권장합니다.[52] 그러나 이러한 식이 권장 사항은 트랜스 지방 섭취에 대해 합의에 도달합니다.[citation needed]
인간에게 산화된 지방(란산 지방)을 섭취하는 역할은 명확하지 않습니다. 산딸기 지방을 먹인 토끼는 죽상경화증이 더 빨리 발생합니다.[53] DHA 함유 오일을 먹인 쥐들은 항산화 시스템에 현저한 장애를 겪었고, 그들의 혈액, 간, 신장에 상당한 양의 인지질 과산화물을 축적했습니다.[54]
다양한 오일이 함유된 무테로겐성 식단을 먹인 토끼는 다중불포화 오일을 통해 LDL의 산화적 민감성을 가장 많이 겪는 것으로 나타났습니다.[55] 또 다른 연구에서 가열된 대두유를 먹인 토끼들은 "심각하게 동맥경화를 유발하고 현저한 간 손상이 조직학적, 임상적으로 입증되었습니다."[56] 하지만 프레드 쿰메로우는 원인이 식이 콜레스테롤이 아니라 튀긴 음식과 흡연에서 나온 옥시스테롤, 즉 산화 콜레스테롤이라고 주장합니다.[57]
부패한 지방과 기름은 소량으로도 매우 불쾌한 맛이 나기 때문에 사람들은 그것들을 먹지 않습니다.[58] 이 물질들의 실제 인체 소비량을 측정하거나 추정하는 것은 매우 어렵습니다.[59] 생선 기름과 같은 고도 불포화 오메가-3가 풍부한 기름은 알약 형태로 판매될 때 존재할 수 있는 산화되거나 산패된 지방의 맛을 숨길 수 있습니다. 미국에서는 건강식품 산업의 식이보충제를 자체 규제하고 FDA 규제를 벗어난다.[60] 불포화지방을 산화로부터 적절히 보호하기 위해서는 산소가 없는 환경에서 시원하게 유지하는 것이 가장 좋습니다.[61]
병태생리학
죽상형성은 죽상성 플라크의 발달 과정입니다. 동맥의 리모델링을 통해 플라크라는 지방질 물질이 내피하에 축적되는 것이 특징입니다. 죽상성 플라크의 축적은 동맥벽 내에서 발생하고 다양한 국소 혈관 순환 인자에 대한 반응으로 복잡한 일련의 세포 사건을 통해 몇 년 동안 발달되는 느린 과정입니다. 최근의 한 가설은 알려지지 않은 이유로 단핵구나 호염구와 같은 백혈구가 심장 근육에서 동맥 내강의 내피를 공격하기 시작한다는 것을 암시합니다. 그에 따른 염증은 내피와 튜니카 중막 사이에 위치한 혈관 벽의 영역인 동맥 튜니카 인티마에 죽종성 플라크를 형성합니다. 이러한 병변의 대부분은 과도한 지방, 콜라겐 및 엘라스틴으로 구성됩니다. 처음에는 플라크가 커지면서 좁아지지 않고 벽이 두꺼워지기만 합니다. 협착은 늦게 일어나는 사건으로 결코 발생하지 않을 수 있으며 반복적인 플라크 파열과 치유 반응의 결과인 경우가 많습니다.[62]
무선 전화의
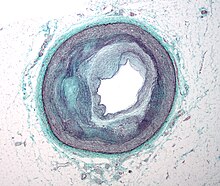
초기 죽상형성은 혈액 순환 단핵구(백혈구의 일종)가 혈관층 내피, 내피하 공간으로 이동하고 단핵구 유래 대식세포로 추가 활성화되는 것을 특징으로 합니다.[63] 이 과정의 주요 동인은 내피 세포 아래의 벽 내에서 산화된 지단백질 입자이지만, 혈당의 상위 정상 또는 상승된 농도도 중요한 역할을 하며 모든 요인이 완전히 이해되지는 않습니다. 지방이 많은 줄무늬가 나타났다 사라질 수도 있습니다.[citation needed]
혈장 내 저밀도 지단백(LDL) 입자가 내피를 침범해 산화돼 심혈관계 질환 위험이 생깁니다. 복잡한 일련의 생화학적 반응은 LDL의 산화를 조절하는데, Lp-LpA2와 같은 효소와 내피의 활성산소를 포함합니다.[64]
내피의 초기 손상은 염증 반응으로 이어집니다. 단핵구는 혈소판이 모욕 부위에 부착된 채 혈류에서 동맥벽으로 들어갑니다. 이는 순환하는 단핵구를 모집하는 VCAM-1 및 단핵구가 대식세포로 분화하는 데 선택적으로 필요한 M-CSF와 같은 인자의 산화환원 신호전달 유도에 의해 촉진될 수 있습니다. 단핵구는 대식세포로 분화하여 국소적으로 증식하고 [65]산화된 LDL을 섭취하여 천천히 큰 "폼 세포"로 변합니다. 이는 수많은 내부 세포질 소포와 그로 인한 높은 지질 함량으로 인한 변화된 외관 때문입니다. 현미경 아래에서 병변은 이제 지방이 많은 줄무늬로 나타납니다. 거품 세포는 결국 죽고 염증 과정을 더 전파합니다.[citation needed]
이러한 세포 활동 외에도 손상된 내피 세포에서 분비되는 사이토카인에 반응하여 튜니카 배지에서 내막으로의 원활한 근육 증식과 이동도 있습니다. 이로 인해 지방이 많은 줄무늬를 덮는 섬유질 캡슐이 형성됩니다. 온전한 내피는 산화질소를 방출하여 이러한 부드러운 근육 증식을 방지할 수 있습니다.[citation needed]
석회화 및 지질
석회화는 주변 근육층의 혈관 평활근 세포 사이에서 형성되며, 특히 죽종에 인접한 근육 세포와 죽종 플라크 및 조직의 표면에서 형성됩니다.[66] 시간이 지나면 세포가 죽으면서 근육벽과 죽상반의 바깥 부분 사이에 세포외 칼슘 침전물이 생깁니다. 죽상 플라크가 칼슘 침착의 조절을 방해하면서 축적되고 결정화됩니다. 동맥경화의 초기 단계의 그림을 나타내는 유사한 형태의 교내 석회화는 항증식 작용 메커니즘을 갖는 많은 약물에 의해 유도되는 것으로 보입니다(Rainer Lidtke 2008).[citation needed]
콜레스테롤은 콜레스테롤이 함유된 저밀도 지단백(LDL) 입자에 의해 혈관 벽으로 전달됩니다. 대식세포를 끌어들이고 자극하기 위해서는 LDL 입자에서 콜레스테롤이 방출되어 산화되어야 하는데, 이는 진행 중인 염증 과정의 핵심 단계입니다. 조직에서 콜레스테롤을 제거해 다시 간으로 운반하는 지단백 입자인 고밀도 지단백(HDL)이 부족하면 과정이 악화됩니다.[64]
거품 세포와 혈소판은 평활근 세포의 이동과 증식을 촉진하고, 이는 다시 지질을 섭취하고 콜라겐으로 대체되어 거품 세포 자체로 변형됩니다. 보호 섬유질 캡은 일반적으로 지방 퇴적물과 동맥 내막(내막) 사이에 형성됩니다.[citation needed]
이렇게 덮인 지방 퇴적물(현재는 '죽종'이라고 함)은 시간이 지남에 따라 동맥을 확장시키는 효소를 생성합니다. 동맥이 충분히 확장되어 동맥의 추가 두께를 보상하는 한 개구("lumen")의 좁아짐("협착")은 발생하지 않습니다. 동맥은 달걀 모양의 단면으로 확장되고, 여전히 원형의 개구를 가지고 있습니다. 확대가 동맥류 두께에 비례하지 않는 경우 동맥류가 생성됩니다.[67]
눈에 보이는 특징

동맥은 일반적으로 현미경으로 연구되지 않지만 두 가지 플라크 유형을 구별할 수 있습니다.[68]
- 섬유지질(섬유지방) 플라크는 동맥 내막 아래에 지질이 풍부한 세포가 축적되는 것이 특징이며, 일반적으로 동맥벽의 경계 근육층의 보상적 확장으로 인해 내강이 좁아지지 않습니다. 내피 아래에는 플라그의 죽상 "핵"을 덮고 있는 "섬유질 캡"이 있습니다. 핵심은 조직 콜레스테롤과 콜레스테롤 에스테르 함량이 상승한 지질이 풍부한 세포(대식세포와 평활근 세포), 피브린, 프로테오글리칸, 콜라겐, 엘라스틴, 세포 잔해로 구성됩니다. 발달된 플라크에서 플라크의 중심 코어는 일반적으로 세포외 콜레스테롤 침전물(죽은 세포에서 방출되는)을 포함하고 있으며, 이들은 빈 바늘 모양의 틈으로 콜레스테롤 결정의 영역을 형성합니다. 플라크의 주변에는 더 젊은 "포밍" 세포와 모세혈관이 있습니다. 이러한 플라크는 파열될 때 일반적으로 개인에게 가장 큰 손상을 입힙니다. 콜레스테롤 결정도 역할을 할 수 있습니다.[69]
- 섬유 플라크는 또한 동맥 벽 내의 내막 아래에 국한되어 벽이 두꺼워지고 확장되며 때로는 근육층의 약간의 위축과 함께 내강의 점박이 국소적인 좁아짐을 초래합니다. 섬유 플라크에는 콜라겐 섬유(에오시노필릭), 칼슘 침전물(헤마톡실리노필릭), 드물게 지질이 풍부한 세포가 포함되어 있습니다.[citation needed]
실제로 동맥벽의 근육 부분은 존재하는 동맥종을 유지할 수 있을 정도로 충분히 큰 작은 동맥류를 형성합니다. 동맥벽의 근육 부분은 죽상성 플라크를 보완하기 위해 개조한 후에도 보통 강하게 유지됩니다.[citation needed]
그러나 혈관 벽 내의 동맥류는 부드럽고 탄성이 거의 없는 연약합니다. 동맥은 심장박동, 즉 맥박에 따라 끊임없이 팽창하고 수축합니다. 또한 동맥 바깥쪽 부분과 근육벽 사이에 석회화 퇴적물이 진행되면서 탄성을 잃고 동맥 전체가 경직됩니다.[citation needed]
석회화 침착물은 충분히 진행된 후,[70] 관상동맥 컴퓨터 단층촬영 또는 전자선 단층촬영(EBT)에서 방사선 밀도가 증가된 고리로 부분적으로 볼 수 있으며, 동맥벽 내에서 죽상성 플라크의 외부 가장자리 주위에 후광을 형성합니다. CT에서 하운스필드 척도의 130단위 이상(일부는 90단위를 주장함)은 일반적으로 동맥 내 조직 석회화를 명확하게 나타내는 것으로 받아들여지는 방사선 밀도입니다. 이러한 침전물은 동맥의 내강이 혈관 조영술로 정상인 경우가 많음에도 불구하고 비교적 진행된 질병의 명백한 증거를 보여줍니다.[citation needed]
파열 및 협착

질병 과정은 수십 년에 걸쳐 천천히 진행되는 경향이 있지만, 일반적으로 죽종이 궤양을 일으킬 때까지 무증상 상태를 유지하며, 이는 죽종 궤양 부위에 즉각적인 혈액 응고로 이어집니다. 이것은 응고 확대로 이어지는 일련의 사건을 유발하여 혈액의 흐름을 빠르게 방해할 수 있습니다. 완전히 막히면 심근(심장) 근육의 허혈과 손상으로 이어집니다. 이 과정이 심근경색 또는 "심쿵"입니다.[71]
심장마비가 치명적이지 않은 경우, 내강 내 응고의 섬유성 조직이 발생하여 파열을 덮지만 내강의 협착 또는 폐쇄를 유발하거나 시간이 지남에 따라 반복적인 파열 후에도 동맥 내강의 지속적이고 일반적으로 국소적인 협착 또는 차단이 발생합니다. 협착증은 천천히 진행될 수 있는 반면, 플라크 궤양은 "불안정한" 더 얇고 약한 섬유질 캡이 있는 동맥류에서 특히 발생하는 갑작스러운 사건입니다.[71]
반복적인 플라크 파열, 전체 내강 폐쇄를 초래하지 않는 것, 파열 및 치유 반응을 통해 혈전 패치와 결합하여 혈전을 안정화하는 것은 시간이 지남에 따라 대부분의 협착을 생성하는 과정입니다. 협착 부위는 이러한 협착에서 증가된 유속에도 불구하고 더 안정적인 경향이 있습니다. 대부분의 주요 혈류 중단 사건은 큰 플라크에서 발생하며, 파열되기 전에는 협착이 거의 발생하지 않았습니다.[citation needed]
임상 시험에서 20%는 플라크의 평균 협착이며, 이후 완전한 동맥 폐쇄와 함께 파열됩니다. 대부분의 심각한 임상적 사건은 고등급 협착을 생성하는 플라크에서 발생하지 않습니다. 임상 실험에서 심장마비의 14%만이 혈관이 닫히기 전에 75% 이상의 협착을 생성하는 플라크에서 동맥 폐쇄로 인해 발생합니다.[citation needed]
동맥 내 혈류에서 부드러운 죽종을 분리하는 섬유질 캡이 파열되면 조직 파편이 노출되어 방출됩니다. 이 조직 조각들은 콜라겐과 조직 인자를 포함하는 매우 응고 촉진 작용을 합니다. 혈소판을 활성화시키고 응고 시스템을 활성화시킵니다. 그 결과 죽상동맥 위에 혈전(혈전)이 형성되어 혈액의 흐름을 급격히 방해합니다. 혈류의 방해로 하류 조직은 산소와 영양분이 부족합니다. 이것이 심근(심근) 협심증(심근통)이나 심근경색(심근통)이 발생합니다.[citation needed]
플라크의 성장 가속화
동맥 내피의 일부에서 죽상경화반의 분포는 균일하지 않습니다. 죽상경화성 변화의 다중적이고 초점적인 발달은 뇌의 아밀로이드 플라크와 피부의 검버섯의 발달과 유사합니다. 잘못된 수리-축적 노화 이론은 잘못된 수리 메커니즘이[72][73] 죽상동맥경화증의 초점 발달에 중요한 역할을 한다는 것을 암시합니다.[74] 플라크가 생기는 것은 손상된 내피가 회복된 결과입니다. 아내피에 지질을 주입하기 때문에 수리는 국소 내피의 변형된 리모델링으로 끝나야 합니다. 이것은 잘못된 수리의 표시입니다. 중요한 것은 이 변경된 리모델링으로 인해 국소 내피가 손상되기 쉽고 수리 효율이 저하된다는 것입니다. 결과적으로 내피의 이 부분은 부상을 입고 부적절하게 수리될 위험성이 증가합니다. 따라서 내피의 잘못된 수리 축적은 초점화되고 자체 가속화됩니다. 이런 식으로 플라크의 성장도 스스로 가속화됩니다. 동맥벽의 일부 내에서 가장 오래된 플라크는 항상 가장 크고 국소 동맥의 폐색을 일으키는 가장 위험한 플라크입니다.[citation needed]
구성 요소들
플라크는 세 가지 별개의 구성 요소로 나뉩니다.
- 동맥의 내강에 가장 가까운 대식세포로 구성된 큰 플라크의 중심에 부드럽고 벗겨지고 노란 물질이 결절적으로 축적된 것으로, 그리스 ἀθήρα (athera)에서 유래한 죽종("gurel lump of gurel")
- 콜레스테롤 결정의[citation needed] 기저 영역
- 오래되거나 진행된 병변의 바깥쪽 기저부에 석회화. 죽상경화성 병변 또는 죽상경화성 플라크는 크게 두 가지로 구분됩니다. 안정적이고 불안정합니다(취약계층이라고도 함).[75] 죽상경화성 병변의 병태생물학은 매우 복잡하지만, 일반적으로 증상이 없는 경향이 있는 안정된 죽상경화반은 세포외 기질과 평활근 세포가 풍부합니다. 반면 불안정한 플라크는 대식세포와 거품세포가 풍부하고, 병변을 동맥 내강으로부터 분리하는 세포외 기질(일명 섬유모)은 대개 약하고 파열되기 쉽습니다.[76] 섬유질 캡의 파열은 콜라겐과 [77]같은 혈전 생성 물질을 순환계에 노출시키고 결국 내강에 혈전 형성을 유도합니다. 관강내 혈전은 형성되면 동맥을 완전히 폐쇄할 수 있지만(예: 관상동맥 폐색), 더 자주 분리되고 순환계로 이동하며 결국 더 작은 하류 가지를 폐쇄하여 혈전색전증을 유발합니다.[citation needed]
혈전색전증과 별개로 만성적으로 확장되는 죽상경화성 병변은 내강의 완전 폐쇄를 유발할 수 있습니다. 만성적으로 확장되는 병변은 종종 내강 협착이 너무 심해서(보통 80% 이상) 하류 조직에 대한 혈액 공급이 부족하여 허혈을 초래할 때까지 무증상입니다. 진행성 죽상동맥경화증의 이러한 합병증은 만성적이고 천천히 진행되며 누적됩니다. 가장 일반적으로 부드러운 플라크가 갑자기 파열되어(취약 플라크 참조), 혈전이 형성되어 혈액의 흐름이 급격히 느려지거나 중단되어 동맥에 의해 공급된 조직이 약 5분 만에 사망에 이르게 됩니다. 이 사건을 경색이라고 합니다.[citation needed]
진단.


협착이 심하고 혈관조영술로 감지할 수 있으며, 그 정도는 덜하지만, 일반적으로 심혈관 질환에 대한 인간 진단 기술의 초점이 되어 왔습니다. 하지만 이런 방법들은 근본적인 죽상동맥경화증이 아닌 심각한 협착만을 발견하는 데 초점을 맞추고 있습니다.[78] 인간 임상 연구에서 입증된 바와 같이 대부분의 심각한 사건은 플라크가 무거운 위치에서 발생하지만 갑자기 쇠약해지는 사건이 발생하기 전에 존재하는 내강이 거의 또는 전혀 좁아지지 않습니다. 플라크 파열은 몇 초에서 몇 분 이내에 동맥 내강 폐색으로 이어질 수 있으며 잠재적인 영구적인 쇠약을 초래할 수 있으며 때로는 갑자기 사망할 수도 있습니다.[citation needed]
파열된 플라크를 합병증이라고 합니다. 병변의 세포외 기질은 일반적으로 병변과 동맥 내강을 분리하는 섬유질 캡의 어깨에서 깨지며, 여기서 주로 콜라겐의 노출된 혈전 생성 성분이 혈전 형성을 유발합니다. 그런 다음 혈전은 다른 혈관으로 하류로 이동하여 혈전이 부분적으로 또는 완전히 혈류를 차단할 수 있습니다. 혈류가 완전히 막히면 인근 세포에 산소가 공급되지 않아 세포사멸이 일어나 괴사합니다.[79] 혈액의 흐름이 좁아지거나 막히는 것은 신체 내의 어떤 동맥에서도 일어날 수 있습니다. 심장 근육에 공급하는 동맥이 막히면 심장마비가 오고, 뇌에 공급하는 동맥이 막히면 허혈성 뇌졸중이 발생합니다.[citation needed]

협심증의 반복되는 에피소드와 스트레스 테스트의 이상은 협착의 특정 중증도에서만 감지할 수 있기 때문에 과거에는 75% 이상의 내강 협착이 임상적으로 중요한 질병의 특징으로 여겨졌습니다. 그러나 임상적으로 쇠약해지는 사건의 약 14%만이 협착이 75% 이상인 부위에서 발생하는 것으로 임상시험에서 밝혀졌습니다. 죽종 플라크의 갑작스러운 파열과 관련된 대부분의 심혈관 사건은 내강의 명백한 좁아짐을 나타내지 않습니다. 따라서 1990년대 후반부터 "취약한 플라크"에 더 많은 관심이 집중되었습니다.[80]
혈관조영술이나 스트레스 검사와 같은 전통적인 진단 방법 외에도 죽상경화증의 조기 발견을 위해 지난 수십 년 동안 다른 검출 기술이 개발되었습니다. 일부 탐지 접근 방식에는 해부학적 탐지 및 생리학적 측정이 포함됩니다.[citation needed]
해부학적 검출 방법의 예로는 CT에 의한 관상동맥 칼슘 채점, 초음파에 의한 경동맥 IMT(중막내 두께) 측정, 혈관내 초음파(IVUS) 등이 있습니다. 생리학적 측정 방법의 예로는 지단백 서브클래스 분석, HbA1c, hs-CRP, 호모시스테인 등이 있습니다.[citation needed] 해부학적 방법과 생리학적 방법 모두 증상이 나타나기 전에 조기에 발견하고 질병 병기를 설정하고 질병 진행을 추적할 수 있습니다. 해부학적 방법은 더 비싸고 그 중 일부는 IVUS와 같은 본질적으로 침습적입니다. 반면에 생리학적 방법은 더 저렴하고 안전한 경우가 많습니다. 그러나 질병의 현재 상태를 정량화하거나 진행 상태를 직접 추적하지는 않습니다. 최근 몇 년 동안 PET 및 SPECT와 같은 핵 영상 기술의 발전으로 죽상경화반의 중증도를 추정할 수 있는 방법이 제공되었습니다.[78]
예방
확립된 위험 인자를 피한다면 심혈관 질환의 90%까지 예방할 수 있습니다.[81][82] 죽상동맥경화증의 의학적 관리에는 우선 위험 요소에 대한 수정이 수반됩니다. 예를 들어, 금연 및 식이 제한을 통해. 그렇다면 예방은 일반적으로 건강한 식단을 섭취하고, 운동을 하고, 담배를 피우지 않고, 정상 체중을 유지하는 것입니다.[5]
다이어트
식단의 변화는 동맥경화증의 발병을 예방하는 데 도움이 될 수 있습니다. 잠정적인 증거는 유제품이 포함된 식단이 심혈관 질환의 위험에 영향을 미치거나 감소시키지 않는다는 것을 시사합니다.[83][84]
과일과 채소가 많이 함유된 식단은 심혈관 질환과 사망의 위험을 줄여줍니다.[85] 지중해식 식단이 심혈관 결과를 개선할 수 있다는 증거가 있습니다.[86] 또한 심혈관 위험 요소(예: 콜레스테롤 수치 및 혈압 저하)에 장기적인 변화를 가져오는데 있어 지중해식이 저지방식보다 더 나을 수 있다는 증거도 있습니다.[87]
운동
조절된 운동 프로그램은 혈관의 순환과 기능을 향상시켜 동맥경화를 퇴치합니다. 운동은 비만, 혈압 저하, 콜레스테롤 감소 환자의 체중 관리에도 사용됩니다. 종종 생활 습관 수정은 약물 요법과 결합됩니다. 예를 들어, 스타틴은 콜레스테롤을 낮추는 데 도움을 줍니다. 아스피린과 같은 항혈소판제는 혈전을 예방하는 데 도움이 되며, 혈압을 조절하기 위해 다양한 항고혈압제가 일상적으로 사용됩니다. 위험 요소 수정과 약물 요법의 결합된 노력이 증상을 통제하거나 허혈성 사건의 임박한 위협과 싸우기에 충분하지 않을 경우 의사는 중재적 또는 외과적 절차에 의존하여 폐쇄를 교정할 수 있습니다.[88]
치료
확립된 질병의 치료에는 스타틴과 같은 콜레스테롤을 낮추는 약물, 혈압약 또는 아스피린과 같이 응고를 감소시키는 약물이 포함될 수 있습니다.[6] 경피적 관상동맥 중재술, 관상동맥 우회 이식술, 경동맥 내막 절제술 등 여러 시술도 시행할 수 있습니다.[6]
의학적 치료는 종종 증상 완화에 초점을 둡니다. 그러나 단순히 증상을 치료하는 것보다 근본적인 죽상동맥경화증을 줄이는 데 중점을 둔 조치가 더 효과적입니다.[89] 비약적 수단은 대개 금연과 규칙적인 운동을 실천하는 것과 같은 첫 번째 치료 방법입니다.[90][91] 이러한 방법들이 효과가 없다면, 의약품은 대개 심혈관 질환을 치료하는 다음 단계이며, 개선과 함께 장기적으로 가장 효과적인 방법이 되고 있습니다.[92]
보다 효과적인 접근법의 핵심은 여러 가지 다른 치료 전략을 결합하는 것입니다.[93] 또한, 가장 성공적인 것으로 나타난 지단백질 수송 행동과 같은 접근법의 경우, 매일 시행되는 보다 공격적인 병용 치료 전략을 채택하고 일반적으로 더 나은 결과를 나타냈습니다, 특히 사람들이 증상을 보이기 전과 후 모두 말입니다.[89]
스타틴스
스타틴이라 불리는 약들은 죽상경화증 치료에 널리 처방됩니다. 그들은 부작용이 거의 없는 높은 콜레스테롤을 가진 사람들의 심혈관 질환과 사망률을 줄이는 이점을 보여주었습니다.[94] 고강도 스타틴과 아스피린이 포함된 2차 예방요법은 관상동맥질환, 허혈성 뇌졸중, 말초동맥질환 등의 재발을 예방하기 위해 ASCVD(죽상경화성 심혈관질환) 병력이 있는 모든 환자를 대상으로 다사회 지침에 의해 권장됩니다.[95][96] 그러나 특히 젊은 환자와 여성들 사이에서 이러한 가이드라인에 부합하는 치료법의 처방과 준수가 부족합니다.[97][98]
스타틴은 콜레스테롤의 생화학적 생성 경로에서 간 속도 제한 효소인 HMG-CoA(hydroxymethylglutaryl-coenzyme A) 환원효소를 억제함으로써 작용합니다. 이 속도 제한 효소를 억제함으로써 우리 몸은 내생적으로 콜레스테롤을 생성하지 못하고, 따라서 혈청 LDL-콜레스테롤을 감소시킵니다. 이렇게 감소된 내인성 콜레스테롤 생산은 신체가 다른 세포 공급원으로부터 콜레스테롤을 뽑아내 혈청 HDL-콜레스테롤을 향상시킵니다.[citation needed] 이러한 데이터는 주로 중년 남성을 대상으로 하며 결론은 여성과 70세 이상의 사람들에게 덜 명확합니다.[99]
수술.
죽상동맥경화증이 심해져 말초동맥질환의 경우 조직 소실 등 비가역적 허혈을 일으킨 경우에는 수술을 지시할 수 있습니다. 혈관 우회 수술은 동맥의 병든 부분 주위의 흐름을 다시 확립할 수 있고, 스텐트를 사용하거나 사용하지 않는 혈관 성형술은 좁아진 동맥을 다시 열고 혈류를 개선할 수 있습니다. 상행 대동맥의 조작 없이 관상동맥 우회 이식술을 시행한 결과, 기존의 펌프 내 관상동맥 재관류술에 비해 수술 후 뇌졸중 및 사망률이 감소한 것으로 나타났습니다.[100]
다른.
비타민K 대사를 방해해 혈전 형성을 억제하는 일부 항응고제, 특히 와파린은 단기적으로 혈전 형성을 감소시킴에도 불구하고 장기적으로 동맥 석회화를 촉진할 수 있다는 증거가 있습니다.[101][102][103][104][excessive citations] 또한 3-하이드록시벤즈알데히드, 프로토카테추산알데히드와 같은 작은 분자들은 동맥경화의 위험을 줄이는 혈관 보호 효과를 보여주었습니다.[105][106]
역학
주로 죽상경화증의 임상 증상인 심혈관 질환은 전 세계적으로 사망의 주요 원인 중 하나입니다.[107]
선진국에서 10세 이상의 거의 모든 어린이들은 대동맥 지방 줄무늬를 가지고 있으며, 관상동맥 지방 줄무늬는 청소년기에 시작됩니다.[108][109][110]
1953년, 한국전쟁에서 전사한 미군들을 대상으로 300회의 부검 결과를 조사한 연구가 발표되었습니다. 병사들의 평균 나이가 22세에 불과했음에도 불구하고 77%가 관상동맥경화증의 눈에 띄는 징후를 보였습니다. 이 연구는 심장병이 더 어린 나이에 사람들에게 영향을 미칠 수 있고 노인들만의 문제가 아니라는 것을 보여주었습니다.[111][112][113]
1992년, 보고서에 따르면 10-14세 어린이의 50% 이상이 왼쪽 전방 하행 동맥에서 미세한 지방 줄무늬가 보였고 8%는 세포외 지질이 더 많이 축적되어 훨씬 더 진행된 병변을 가지고 있었습니다.[114]
1985년에서 1995년 사이에 수행된 연구의 2005년 보고서에서 5-14세 그룹의 대동맥의 약 87%와 관상동맥의 30%가 나이가 들수록 증가하는 지방 줄무늬를 가지고 있는 것으로 나타났습니다.[115]
어원
다음의 용어는 철자와 의미 모두 비슷하면서도 구별되는 것으로, 쉽게 혼동할 수 있는 것이 동맥경화증, 동맥경화증, 죽상경화증입니다. 동맥경화는 그리스 ἀρτηρία (예술 ē리아) '동맥'에서 나온 중간 또는 큰 동맥의 경화(및 탄성 손실)를 설명하는 일반적인 용어입니다. 그리고 σκλήρωσις (경련) '경련'; 동맥경화증은 동맥(작은 동맥)의 경화(및 탄력성 상실); 동맥경화증은 특히 죽상성 플라크(고대 그리스 ἀθήρα (ath ḗra) 'gruel'에서 유래)로 인해 동맥이 경화되는 것입니다. 무테로겐이라는 용어는 무테롬의 형성을 유발하는 물질이나 과정에 사용됩니다.[116]
경제학
2011년, 관상동맥 죽상동맥경화증은 미국에서 입원 기간 동안 가장 비싼 10대 질환 중 하나로, 총 입원비가 104억 달러에 달했습니다.[117]
조사.
지질
동맥경화에 대한 고밀도 지단백질(HDL)의 역할에 대한 징후는 이 HDL 단백질의 희귀한 Apo-A1 Milano 인간 유전자 변이와 관련이 있습니다. 불안정한 협심증을 가진 사람들에게 박테리아 합성 인간 Apo-A1 Milano HDL을 사용한 소규모 단기 실험은 위약으로 무작위 배정된 사람들의 일반적인 플라크 부피 증가에 비해 단 6주 만에 측정된 관상동맥 플라크 부피에서 상당히 극적인 감소를 나타냈습니다. 이 실험은 2006년 초에 JAMA에서 발표되었습니다.[citation needed] 1990년대에 시작된 지속적인 작업은 아마도 약 2008년까지 인간 임상 시험으로 이어질 수 있습니다.[needs update] 이들은 합성된 Apo-A1 Milano HDL을 직접 사용하거나 유전자 전달 방법을 사용하여 Apo-A1 Milano HDL 지단백질을 합성하는 능력을 전달할 수 있습니다.[citation needed]
일부 동물 연구에서 동맥류를 크게 반전시켜 제거하는 HDL 입자 농도를 높이는 방법이 개발 및 연구되고 있습니다.[citation needed] 그러나 어떤 방법으로든 HDL을 높이는 것이 반드시 도움이 되는 것은 아닙니다. 예를 들어, 약물인 torcetrapib은 현재 HDL(최대 60%)을 상승시키는 것으로 알려진 가장 효과적인 약제입니다. 하지만 임상시험에서도 사망률을 60%나 높였습니다. 이 약물에 관한 모든 연구는 2006년 12월에 중단되었습니다.[118]
대식세포의 작용으로 죽상경화반 진행을 유도합니다. 죽상동맥경화증의 면역조절은 이 대식세포 작용을 억제하기 위해 면역체계 기능을 조절하는 기술을 일컫는 말입니다.[119]
동맥[120] 생성에 지질 과산화 연쇄 반응의 관여는 일반 PUFA(H-PUFA)보다 산화되기 쉬운 중동위원소(탈환된) 고도불포화 지방산(D-PUFA)의 보호 역할에 대한 연구를 촉발했습니다. PUFA는 필수 영양소입니다. 음식을 섭취할 때 바로 그 형태로 신진대사에 관여합니다. 인간과 유사한 지단백질 대사 모델인 형질전환 마우스에서 식이에 D-PUFA를 추가하면 실제로 체중 증가가 감소하고 콜레스테롤 처리가 개선되었으며 대동맥의 동맥경화 손상이 감소했습니다.[121][122]
miRNA
마이크로RNA(miRNA)는 단백질 코딩 유전자의 표적 mRNA의 3' UTR과 5' UTR에 상보적인 서열을 가지며, mRNA 절단 또는 번역 기계의 억제를 유발합니다. 질병에 걸린 혈관에서 miRNA는 조절이 잘 안되고 고도로 발현됩니다. miR-33은 심혈관 질환에서 발견됩니다.[123] 지질대사, 인슐린 신호전달 및 포도당 항상성, 세포형 진행 및 증식, 골수성 세포 분화를 포함한 죽상경화성 개시 및 진행에 관여합니다. 설치류에서 miR-33의 억제가 HDL 수치를 상승시키고 miR-33의 발현이 죽상경화반을 가진 사람에게서 하향 조절된다는 것이 발견되었습니다.[124][125][126]
miR-33a 및 miR-33b는 22번 염색체의 인간 스테롤 조절 요소 결합 단백질 2(SREBP2) 유전자의 인트론 16과 17번 염색체의 SREBP1 유전자의 인트론 17에 위치합니다.[127] miR-33a/b는 3'에서 결합함으로써 콜레스테롤/지질 항상성을 조절합니다.ATP 결합 카세트(ABC) 수송체와 같은 콜레스테롤 수송에 관여하는 유전자의 UTR은 그 발현을 향상시키거나 억제합니다. 연구에 따르면 ABCA1은 말초 조직에서 Apolipoprotein-1로 콜레스테롤의 수송을 매개하며 콜레스테롤이 말초 조직에서 간으로 전달되어 배설되기 전에 담즙으로 배설되거나 담즙산으로 전환될 수 있는 역 콜레스테롤 수송 경로에서도 중요합니다.[123] 따라서 ABCA1이 대식세포의 콜레스테롤 축적을 막는 데 중요한 역할을 한다는 것을 알고 있습니다. miR-33 기능을 강화하여 ABCA1의 수준을 감소시켜 세포 콜레스테롤 유출을 apoA-1로 감소시킵니다. 반면 miR-33 기능을 억제하여 ABCA1의 수치를 증가시키고 콜레스테롤 유출량을 apoA-1로 증가시킵니다. miR-33의 억제는 ABCA1 발현의 조절을 통해 세포 콜레스테롤의 감소와 혈장 HDL 수치의 증가로 이어질 것입니다.[128]
당인 사이클로덱스트린은 고지방 식단을 먹인 쥐의 동맥에 쌓여 있던 콜레스테롤을 제거했습니다.[129]
DNA손상
노화는 심혈관 질환의 가장 중요한 위험 요소입니다. 노화가 다른 인식된 위험 요소와 무관하게 영향을 매개하는 원인 기반은 아직 결정되지 않았습니다. 혈관 노화에서 DNA 손상의 핵심적인 역할에 대한 증거가 검토되었습니다.[130][131][132] DNA의 흔한 산화 손상 유형인 8-oxoG는 플라크 혈관 평활근 세포, 대식세포 및 내피 세포에 [133]축적되어 DNA 손상을 플라크 형성과 연결시키는 것으로 밝혀졌습니다. 죽상경화반에서도 DNA 가닥 파손이 증가했습니다.[133] 베르너 증후군(WS)은 인간의 조기 노화 질환입니다.[134] WS는 RecQ 헬리케이스의 유전적 결함에 의한 것으로, DNA의 손상을 제거하는 여러 복구 과정에서 사용됩니다. WS 환자는 관상동맥과 대동맥에 죽상경화반 플라크가 상당히 많이 발생하는데, 대동맥 판막의 석회화도 자주 관찰됩니다.[131] 이러한 발견은 과도한 복구되지 않은 DNA 손상을 조기 노화 및 조기 죽상경화반 발달과 연관시킵니다(노화의 DNA 손상 이론 참조).[citation needed]
미생물
인체의 모든 미생물인 미생물은 면역체계의 조절, 신진대사의 변화, 영양소의 처리, 혈액순환으로 들어갈 수 있는 특정 대사산물의 생산 등 여러 가지 방법으로 죽상경화증에 기여할 수 있습니다.[135] 장내 세균에 의해 생성되는 이러한 대사산물 중 하나는 트리메틸아민 N-옥사이드(TMAO)입니다. 그 수치는 인간의 연구에서 죽상경화증과 관련이 있으며 동물 연구에서는 인과 관계가 있을 수 있음을 시사합니다. TMAO 생성에 관여하는 효소인 트리메틸아민 분해효소를 암호화하는 박테리아 유전자와 죽상경화증 사이의 연관성이 주목되었습니다.[136][135]
혈관 평활근 세포
혈관 평활근 세포는 죽상형성에 핵심적인 역할을 하며, 역사적으로 보호 섬유질 캡을 형성하고 강도를 부여하는 세포외 기질 성분을 합성함으로써 플라크 안정성에 유익한 것으로 여겨졌습니다.[137][138] 그러나 섬유질 캡 외에도 혈관 평활근 세포는 플라크 코어 내에서 발견되는 많은 세포 유형을 생성하고 이들의 표현형을 조절하여 플라크 안정성을 촉진하고 감소시킬 수 있습니다.[137][139][140][141] 혈관 평활근 세포는 죽상경화반 내에서 뚜렷한 가소성을 나타내며 대식세포, 근섬유아세포, 중간엽줄기세포 및 골연골세포를 포함한 다양한 다른 세포 유형과 유사하도록 유전자 발현 프로파일을 수정할 수 있습니다.[142][143][137] 중요한 것은 유전자 계통 ‐ 추적 실험에서 플라크 상주 세포의 40-90%가 혈관 평활근 세포 유래임을 분명히 보여주었기 때문에 새로운 치료 표적을 확인하기 위해서는 동맥경화증에서 혈관 평활근 세포의 역할을 연구하는 것이 중요합니다.
참고문헌
- ^ a b c d e f "What Are the Signs and Symptoms of Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 5 November 2017.
- ^ a b "What Causes Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 6 November 2017.
- ^ "New Concept of Heart Disease Posits Vitamin C Deficiency as Culprit". DAIC (Diagnostic and Interventional Cardiology). 27 April 2015. Retrieved 2022-02-06.
- ^ a b "Who Is at Risk for Atherosclerosis?". www.nhlbi.nih.gov. 22 June 2016. Retrieved 5 November 2017.
- ^ a b c "How Can Atherosclerosis Be Prevented or Delayed? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 6 November 2017.
- ^ a b c d e "How Is Atherosclerosis Treated? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 6 November 2017.
- ^ a b Aronow WS, Fleg JL, Rich MW (2013). Tresch and Aronow's Cardiovascular Disease in the Elderly, Fifth Edition. CRC Press. p. 171. ISBN 978-1-84214-544-9.
- ^ "Arteriosclerosis / atherosclerosis - Symptoms and causes". Mayo Clinic. Retrieved 2021-05-06.
- ^ a b c "What Is Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 6 November 2017.
- ^ Tsukahara, Tamotsu; Tsukahara, Ryoko; Haniu, Hisao; Matsuda, Yoshikazu; Murakami-Murofushi, Kimiko (2015-09-05). "Cyclic phosphatidic acid inhibits the secretion of vascular endothelial growth factor from diabetic human coronary artery endothelial cells through peroxisome proliferator-activated receptor gamma". Molecular and Cellular Endocrinology. 412: 320–329. doi:10.1016/j.mce.2015.05.021. hdl:10069/35888. ISSN 0303-7207. PMID 26007326. S2CID 10454566.
- ^ Lind L (August 2003). "Circulating markers of inflammation and atherosclerosis". Atherosclerosis. 169 (2): 203–214. doi:10.1016/s0021-9150(03)00012-1. PMID 12921971.
- ^ "How Is Atherosclerosis Diagnosed? - NHLBI, NIH". www.nhlbi.nih.gov. 22 June 2016. Retrieved 6 November 2017.
- ^ Information (US), National Center for Biotechnology (1998), "Atherosclerosis", Genes and Disease [Internet], National Center for Biotechnology Information (US), retrieved 2023-11-21
- ^ Roth GA, Mensah GA, Johnson CO, Addolorato G, Ammirati E, Baddour LM, et al. (December 2020). "Global Burden of Cardiovascular Diseases and Risk Factors, 1990-2019: Update From the GBD 2019 Study". Journal of the American College of Cardiology. 76 (25): 2982–3021. doi:10.1016/j.jacc.2020.11.010. PMC 7755038. PMID 33309175.
- ^ Song P, Fang Z, Wang H, Cai Y, Rahimi K, Zhu Y, et al. (May 2020). "Global and regional prevalence, burden, and risk factors for carotid atherosclerosis: a systematic review, meta-analysis, and modelling study". The Lancet. Global Health. 8 (5): e721–e729. doi:10.1016/S2214-109X(20)30117-0. PMID 32353319. S2CID 218474949.
- ^ Topol EJ, Califf RM (2007). Textbook of Cardiovascular Medicine. Lippincott Williams & Wilkins. p. 2. ISBN 978-0-7817-7012-5.
- ^ Shor A (2008). Chlamydia Atherosclerosis Lesion: Discovery, Diagnosis and Treatment. Springer Science & Business Media. p. 8. ISBN 978-1-84628-810-4.
- ^ "Evolutionary gene loss may help explain why only humans are prone to heart attacks". ScienceDaily. Retrieved 2023-11-21.
- ^ Ross R (April 1993). "The pathogenesis of atherosclerosis: a perspective for the 1990s". Nature. 362 (6423): 801–9. Bibcode:1993Natur.362..801R. doi:10.1038/362801a0. PMID 8479518. S2CID 4282916.
- ^ 죽상경화증. 하버드 보건 간행물 하버드 보건 간행물. 건강 주제 A – Z, (2011)
- ^ a b c "Atherosclerosis". National Heart, Lung and Blood Institute. 2011.
- ^ a b Velican D, Velican C (June 1979). "Study of fibrous plaques occurring in the coronary arteries of children". Atherosclerosis. 33 (2): 201–205. doi:10.1016/0021-9150(79)90117-5. PMID 475879.
- ^ Flora GC, Baker AB, Loewenson RB, Klassen AC (November 1968). "A comparative study of cerebral atherosclerosis in males and females". Circulation. 38 (5): 859–69. doi:10.1161/01.CIR.38.5.859. PMID 5697685.
- ^ a b 부정맥. 심장 및 뇌졸중 재단. "Heart disease - Arrhythmia - Heart and Stroke Foundation of Canada". Archived from the original on 2014-02-03. Retrieved 2014-01-31. (2011)
- ^ Sims NR, Muyderman H (January 2010). "Mitochondria, oxidative metabolism and cell death in stroke" (PDF). Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1802 (1): 80–91. doi:10.1016/j.bbadis.2009.09.003. PMID 19751827.
- ^ Roquer, J.; Ois, Angel (2010), Preedy, Victor R.; Watson, Ronald R. (eds.), "Atherosclerotic Burden and Mortality", Handbook of Disease Burdens and Quality of Life Measures, New York, NY: Springer, pp. 899–918, doi:10.1007/978-0-387-78665-0_51, ISBN 978-0-387-78665-0, retrieved 2023-11-10
- ^ Enos WF, Holmes RH, Beyer J (1953). "Coronary disease among United States soldiers killed in action in Korea: Preliminary Report". JAMA. 152 (12): 1090–93. doi:10.1001/jama.1953.03690120006002. PMID 13052433. 평균 나이는 군인 200세부터 계산했습니다. 그 남자들 중 거의 100명의 나이는 기록되지 않았습니다.
- ^ Li X, Fang P, Li Y, Kuo YM, Andrews AJ, Nanayakkara G, Johnson C, Fu H, Shan H, Du F, Hoffman NE, Yu D, Eguchi S, Madesh M, Koch WJ, Sun J, Jiang X, Wang H, Yang X (June 2016). "Mitochondrial Reactive Oxygen Species Mediate Lysophosphatidylcholine-Induced Endothelial Cell Activation". Arteriosclerosis, Thrombosis, and Vascular Biology. 36 (6): 1090–100. doi:10.1161/ATVBAHA.115.306964. PMC 4882253. PMID 27127201.
- ^ Botts SR, Fish JE, Howe KL (December 2021). "Dysfunctional Vascular Endothelium as a Driver of Atherosclerosis: Emerging Insights Into Pathogenesis and Treatment". Frontiers in Pharmacology. 12: 787541. doi:10.3389/fphar.2021.787541. PMC 8727904. PMID 35002720.
- ^ Williams KJ, Tabas I (May 1995). "The response-to-retention hypothesis of early atherogenesis". Arteriosclerosis, Thrombosis, and Vascular Biology. 15 (5): 551–61. doi:10.1161/01.ATV.15.5.551. PMC 2924812. PMID 7749869.
- ^ Aviram M, Fuhrman B (November 1998). "LDL oxidation by arterial wall macrophages depends on the oxidative status in the lipoprotein and in the cells: role of prooxidants vs. antioxidants". Molecular and Cellular Biochemistry. 188 (1–2): 149–59. doi:10.1023/A:1006841011201. PMID 9823020. S2CID 12222110.
- ^ a b c d e f g h i j k l m n o p q "Atherosclerosis NHLBI, NIH". 24 March 2022.
- ^ Campbell LA, Rosenfeld ME (July 2015). "Infection and Atherosclerosis Development". Arch Med Res. 46 (5): 339–50. doi:10.1016/j.arcmed.2015.05.006. PMC 4524506. PMID 26004263.
- ^ Sinha A, Feinstein MJ (March 2019). "Coronary Artery Disease Manifestations in HIV: What, How, and Why". The Canadian Journal of Cardiology. 35 (3): 270–279. doi:10.1016/j.cjca.2018.11.029. PMC 9532012. PMID 30825949. S2CID 73469601.
- ^ Enas EA, Kuruvila A, Khanna P, Pitchumoni CS, Mohan V (October 2013). "Benefits & risks of statin therapy for primary prevention of cardiovascular disease in Asian Indians - a population with the highest risk of premature coronary artery disease & diabetes". The Indian Journal of Medical Research. 138 (4): 461–91. PMC 3868060. PMID 24434254.
- ^ 인도 심장 협회 왜 남아시아 사람들이 사실인가 웹 2015년 4월 30일 http://indianheartassociation.org/why-indians-why-south-asians/overview/
- ^ Tyrrell DJ, Blin MB, Song J, Wood SC, Zhang M, Beard DA, Goldstein DR (January 2020). "Age-Associated Mitochondrial Dysfunction Accelerates Atherogenesis". Circulation Research. 126 (3): 298–314. doi:10.1161/CIRCRESAHA.119.315644. PMC 7006722. PMID 31818196.
- ^ Velican C, Velican D (March 1985). "Differences in the pattern of atherosclerotic involvement between non-branched regions and adjacent branching points of human coronary arteries". Atherosclerosis. 54 (3): 333–342. doi:10.1016/0021-9150(85)90126-1. PMID 3994786.
- ^ Borissoff JI, Spronk HM, Heeneman S, ten Cate H (June 2009). "Is thrombin a key player in the 'coagulation-atherogenesis' maze?". Cardiovascular Research. 82 (3): 392–403. doi:10.1093/cvr/cvp066. PMID 19228706.
- ^ Borissoff JI, Heeneman S, Kilinç E, Kassák P, Van Oerle R, Winckers K, Govers-Riemslag JW, Hamulyák K, Hackeng TM, Daemen MJ, ten Cate H, Spronk HM (August 2010). "Early atherosclerosis exhibits an enhanced procoagulant state". Circulation. 122 (8): 821–30. doi:10.1161/CIRCULATIONAHA.109.907121. PMID 20697022.
- ^ Borissoff JI, Spronk HM, ten Cate H (May 2011). "The hemostatic system as a modulator of atherosclerosis". The New England Journal of Medicine. 364 (18): 1746–60. doi:10.1056/NEJMra1011670. PMID 21542745.
- ^ Food and nutrition board, institute of medicine of the national academies (2005). Dietary Reference Intakes for Energy, Carbohydrate, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids (Macronutrients). National Academies Press. pp. 481–484. doi:10.17226/10490. ISBN 978-0-309-08525-0.
- ^ Mozaffarian D, Rimm EB, Herrington DM (November 2004). "Dietary fats, carbohydrate, and progression of coronary atherosclerosis in postmenopausal women". The American Journal of Clinical Nutrition. 80 (5): 1175–84. doi:10.1093/ajcn/80.5.1175. PMC 1270002. PMID 15531663.
- ^ Bhatt DL, Topol EJ (July 2002). "Need to test the arterial inflammation hypothesis". Circulation. 106 (1): 136–40. doi:10.1161/01.CIR.0000021112.29409.A2. PMID 12093783.
- ^ Griffin M, Frazer A, Johnson A, Collins P, Owens D, Tomkin GH (June 1998). "Cellular cholesterol synthesis--the relationship to post-prandial glucose and insulin following weight loss". Atherosclerosis. 138 (2): 313–8. doi:10.1016/S0021-9150(98)00036-7. PMID 9690914.
- ^ King CR, Knutson KL, Rathouz PJ, Sidney S, Liu K, Lauderdale DS (December 2008). "Short sleep duration and incident coronary artery calcification". JAMA. 300 (24): 2859–66. doi:10.1001/jama.2008.867. PMC 2661105. PMID 19109114.
- ^ Provost EB, Madhloum N, Int Panis L, De Boever P, Nawrot TS (2015). "Carotid intima-media thickness, a marker of subclinical atherosclerosis, and particulate air pollution exposure: the meta-analytical evidence". PLOS ONE. 10 (5): e0127014. Bibcode:2015PLoSO..1027014P. doi:10.1371/journal.pone.0127014. PMC 4430520. PMID 25970426.
- ^ Adar SD, Sheppard L, Vedal S, Polak JF, Sampson PD, Diez Roux AV, Budoff M, Jacobs DR, Barr RG, Watson K, Kaufman JD (April 23, 2013). "Fine particulate air pollution and the progression of carotid intima-medial thickness: a prospective cohort study from the multi-ethnic study of atherosclerosis and air pollution". PLOS Medicine. 10 (4): e1001430. doi:10.1371/journal.pmed.1001430. PMC 3637008. PMID 23637576.
This early analysis from MESA suggests that higher long-term PM2.5 concentrations are associated with increased IMT progression and that greater reductions in PM2.5 are related to slower IMT progression.
- ^ Wang CH, Jeng JS, Yip PK, Chen CL, Hsu LI, Hsueh YM, et al. (April 2002). "Biological gradient between long-term arsenic exposure and carotid atherosclerosis". Circulation. 105 (15): 1804–1809. doi:10.1161/01.cir.0000015862.64816.b2. PMID 11956123. S2CID 535580.
- ^ "Treating Hypothyroidism Reduces Atherosclerosis Risk". American Family Physician. 69 (3): 656. 1 February 2004.
- ^ Bale BF, Doneen AL, Vigerust DJ (April 2017). "High-risk periodontal pathogens contribute to the pathogenesis of atherosclerosis". Postgraduate Medical Journal. 93 (1098): 215–220. doi:10.1136/postgradmedj-2016-134279. PMC 5520251. PMID 27899684.
- ^ "Food Pyramids: Nutrition Source, Harvard School of Public Health". Archived from the original on 26 December 2007. Retrieved 2007-11-25.
- ^ Staprãns I, Rapp JH, Pan XM, Hardman DA, Feingold KR (April 1996). "Oxidized lipids in the diet accelerate the development of fatty streaks in cholesterol-fed rabbits". Arteriosclerosis, Thrombosis, and Vascular Biology. 16 (4): 533–8. doi:10.1161/01.atv.16.4.533. PMID 8624775.
- ^ Song JH, Fujimoto K, Miyazawa T (December 2000). "Polyunsaturated (n-3) fatty acids susceptible to peroxidation are increased in plasma and tissue lipids of rats fed docosahexaenoic acid-containing oils". The Journal of Nutrition. 130 (12): 3028–33. doi:10.1093/jn/130.12.3028. PMID 11110863.
- ^ Yap SC, Choo YM, Hew NF, Yap SF, Khor HT, Ong AS, Goh SH (December 1995). "Oxidative susceptibility of low density lipoprotein from rabbits fed atherogenic diets containing coconut, palm, or soybean oils". Lipids. 30 (12): 1145–50. doi:10.1007/BF02536616. PMID 8614305. S2CID 3960289.
- ^ Greco AV, Mingrone G (1990). "Serum and biliary lipid pattern in rabbits feeding a diet enriched with unsaturated fatty acids". Experimental Pathology. 40 (1): 19–33. doi:10.1016/S0232-1513(11)80281-1. PMID 2279534.
- ^ "Scientist, 98, challenges orthodoxy on causes of heart disease". medicalxpress.com.
- ^ Mattes RD (December 2005). "Fat taste and lipid metabolism in humans". Physiology & Behavior. 86 (5): 691–7. doi:10.1016/j.physbeh.2005.08.058. PMID 16249011. S2CID 33916150.
The rancid odor of an oxidized fat is readily detectable
- ^ Dobarganes C, Márquez-Ruiz G (March 2003). "Oxidized fats in foods". Current Opinion in Clinical Nutrition and Metabolic Care. 6 (2): 157–163. doi:10.1097/00075197-200303000-00004. PMID 12589185. S2CID 21085461.
- ^ "Dietary Supplements". Food and Drug Administration. 4 February 2020.
- ^ Khan-Merchant N, Penumetcha M, Meilhac O, Parthasarathy S (November 2002). "Oxidized fatty acids promote atherosclerosis only in the presence of dietary cholesterol in low-density lipoprotein receptor knockout mice". The Journal of Nutrition. 132 (11): 3256–3262. doi:10.1093/jn/132.11.3256. PMID 12421837.
- ^ "Atherosclerosis". The Lecturio Medical Concept Library. Retrieved 2 July 2021.
- ^ Schwartz CJ, Valente AJ, Sprague EA, Kelley JL, Cayatte AJ, Mowery J (December 1992). "Atherosclerosis. Potential targets for stabilization and regression". Circulation. 86 (6 Suppl): III117–23. PMID 1424045.
- ^ a b Linton MF, Yancey PG, Davies SS, Jerome WG, Linton EF, Song WL, et al. (2000). "The Role of Lipids and Lipoproteins in Atherosclerosis". Endotext. PMID 26844337. NBK343489.
- ^ Robbins CS, Hilgendorf I, Weber GF, Theurl I, Iwamoto Y, Figueiredo JL, Gorbatov R, Sukhova GK, Gerhardt LM, Smyth D, Zavitz CC, Shikatani EA, Parsons M, van Rooijen N, Lin HY, Husain M, Libby P, Nahrendorf M, Weissleder R, Swirski FK (September 2013). "Local proliferation dominates lesional macrophage accumulation in atherosclerosis". Nature Medicine. 19 (9): 1166–72. doi:10.1038/nm.3258. PMC 3769444. PMID 23933982.
- ^ Miller JD (June 2013). "Cardiovascular calcification: Orbicular origins". Nature Materials. 12 (6): 476–478. Bibcode:2013NatMa..12..476M. doi:10.1038/nmat3663. PMID 23695741.
- ^ Glagov S, Weisenberg E, Zarins CK, Stankunavicius R, Kolettis GJ (May 1987). "Compensatory enlargement of human atherosclerotic coronary arteries". The New England Journal of Medicine. 316 (22): 1371–5. doi:10.1056/NEJM198705283162204. PMID 3574413.
- ^ "Coronary atherosclerosis — the fibrous plaque with calcification". www.pathologyatlas.ro. Retrieved 2010-03-25.
- ^ Janoudi A, Shamoun FE, Kalavakunta JK, Abela GS (July 2016). "Cholesterol crystal-induced arterial inflammation and destabilization of atherosclerotic plaque". European Heart Journal. 37 (25): 1959–67. doi:10.1093/eurheartj/ehv653. PMID 26705388.
- ^ Maton A, Hopkins RL, McLaughlin CW, Johnson S, Warner MQ, LaHart D, et al. (1993). Human Biology and Health. Englewood Cliffs, NJ: Prentice Hall. ISBN 978-0-13-981176-0. OCLC 32308337.
- ^ a b "What Are the Signs and Symptoms of Coronary Heart Disease?". www.nhlbi.nih.gov. September 29, 2014. Archived from the original on 24 February 2015. Retrieved 2 July 2021.
- ^ Wang J, Michelitsch T, Wunderlin A, Mahadeva R (6 April 2009). "Aging as a consequence of misrepair -- A novel theory of aging". Nature Precedings. arXiv:0904.0575. doi:10.1038/npre.2009.2988.2. S2CID 2179468.
- ^ Wang-Michelitsch J, Michelitsch T (2015). "Aging as a process of accumulation of Misrepairs". arXiv:1503.07163 [q-bio.TO].
- ^ Wang-Michelitsch J, Michelitsch TM (2015). "Misrepair mechanism in the development of atherosclerotic plaques". arXiv:1505.01289 [q-bio.TO].
- ^ Ross R (January 1999). "Atherosclerosis--an inflammatory disease". The New England Journal of Medicine. 340 (2): 115–26. doi:10.1056/NEJM199901143400207. PMID 9887164.
- ^ Finn AV, Nakano M, Narula J, Kolodgie FD, Virmani R (July 2010). "Concept of vulnerable/unstable plaque". Arteriosclerosis, Thrombosis, and Vascular Biology. 30 (7): 1282–92. doi:10.1161/ATVBAHA.108.179739. PMID 20554950.
- ^ Didangelos A, Simper D, Monaco C, Mayr M (May 2009). "Proteomics of acute coronary syndromes". Current Atherosclerosis Reports. 11 (3): 188–95. doi:10.1007/s11883-009-0030-x. PMID 19361350. S2CID 41219190.
- ^ a b Tarkin JM, Dweck MR, Evans NR, Takx RA, Brown AJ, Tawakol A, et al. (February 2016). "Imaging Atherosclerosis". Circulation Research. 118 (4): 750–769. doi:10.1161/CIRCRESAHA.115.306247. PMC 4756468. PMID 26892971.
- ^ Stary HC, Chandler AB, Dinsmore RE, Fuster V, Glagov S, Insull W, et al. (September 1995). "A definition of advanced types of atherosclerotic lesions and a histological classification of atherosclerosis. A report from the Committee on Vascular Lesions of the Council on Arteriosclerosis, American Heart Association". Circulation. 92 (5): 1355–1374. doi:10.1161/01.CIR.92.5.1355. PMID 7648691.
- ^ Maseri A, Fuster V (April 2003). "Is there a vulnerable plaque?". Circulation. 107 (16): 2068–71. doi:10.1161/01.CIR.0000070585.48035.D1. PMID 12719286.
- ^ McGill HC, McMahan CA, Gidding SS (March 2008). "Preventing heart disease in the 21st century: implications of the Pathobiological Determinants of Atherosclerosis in Youth (PDAY) study". Circulation. 117 (9): 1216–27. doi:10.1161/CIRCULATIONAHA.107.717033. PMID 18316498.
- ^ McNeal CJ, Dajani T, Wilson D, Cassidy-Bushrow AE, Dickerson JB, Ory M (January 2010). "Hypercholesterolemia in youth: opportunities and obstacles to prevent premature atherosclerotic cardiovascular disease". Current Atherosclerosis Reports. 12 (1): 20–8. doi:10.1007/s11883-009-0072-0. PMID 20425267. S2CID 37833889.
- ^ Rice BH (2014). "Dairy and Cardiovascular Disease: A Review of Recent Observational Research". Current Nutrition Reports. 3 (2): 130–138. doi:10.1007/s13668-014-0076-4. PMC 4006120. PMID 24818071.
- ^ Kratz M, Baars T, Guyenet S (February 2013). "The relationship between high-fat dairy consumption and obesity, cardiovascular, and metabolic disease". European Journal of Nutrition. 52 (1): 1–24. doi:10.1007/s00394-012-0418-1. PMID 22810464. S2CID 1360916.
- ^ Wang X, Ouyang Y, Liu J, Zhu M, Zhao G, Bao W, Hu FB (July 2014). "Fruit and vegetable consumption and mortality from all causes, cardiovascular disease, and cancer: systematic review and dose-response meta-analysis of prospective cohort studies". BMJ. 349: g4490. doi:10.1136/bmj.g4490. PMC 4115152. PMID 25073782.
- ^ Walker C, Reamy BV (April 2009). "Diets for cardiovascular disease prevention: what is the evidence?". American Family Physician. 79 (7): 571–8. PMID 19378874.
- ^ Nordmann AJ, Suter-Zimmermann K, Bucher HC, Shai I, Tuttle KR, Estruch R, Briel M (September 2011). "Meta-analysis comparing Mediterranean to low-fat diets for modification of cardiovascular risk factors". The American Journal of Medicine. 124 (9): 841–51.e2. doi:10.1016/j.amjmed.2011.04.024. PMID 21854893.
- ^ Paul P, Williams B, eds. (2009). "Cardiovascular, Circulatory, and Hematologic Function". Brunner & Suddarth's Textbook of Canadian Medical-surgical Nursing. Lippincott Williams & Wilkins. pp. 730–1047. ISBN 978-0-7817-9989-8.
- ^ a b Fonarow G (2003). "Aggressive treatment of atherosclerosis: The time is now". Cleve. Clin. J. Med. 70 (5): 431–434. doi:10.3949/ccjm.70.5.431. PMID 12785316.
- ^ Ambrose JA, Barua RS (May 2004). "The pathophysiology of cigarette smoking and cardiovascular disease: an update". Journal of the American College of Cardiology. 43 (10): 1731–7. doi:10.1016/j.jacc.2003.12.047. PMID 15145091.
- ^ Pigozzi F, Rizzo M, Fagnani F, Parisi A, Spataro A, Casasco M, Borrione P (June 2011). "Endothelial (dys)function: the target of physical exercise for prevention and treatment of cardiovascular disease". The Journal of Sports Medicine and Physical Fitness. 51 (2): 260–267. PMID 21681161.
- ^ Gupta, Keshav Kumar; Ali, Shair; Sanghera, Ranjodh Singh (June 2019). "Pharmacological Options in Atherosclerosis: A Review of the Existing Evidence". Cardiology and Therapy. 8 (1): 5–20. doi:10.1007/s40119-018-0123-0. ISSN 2193-8261. PMC 6525235. PMID 30543029.
- ^ Koh KK, Han SH, Oh PC, Shin EK, Quon MJ (April 2010). "Combination therapy for treatment or prevention of atherosclerosis: focus on the lipid-RAAS interaction". Atherosclerosis. 209 (2): 307–13. doi:10.1016/j.atherosclerosis.2009.09.007. PMC 2962413. PMID 19800624.
- ^ Taylor F, Huffman MD, Macedo AF, Moore TH, Burke M, Davey Smith G, et al. (January 2013). "Statins for the primary prevention of cardiovascular disease". The Cochrane Database of Systematic Reviews. 1 (1): CD004816. doi:10.1002/14651858.CD004816.pub5. PMC 6481400. PMID 23440795.
- ^ Virani SS, Smith SC, Stone NJ, Grundy SM (April 2020). "Secondary Prevention for Atherosclerotic Cardiovascular Disease: Comparing Recent US and European Guidelines on Dyslipidemia". Circulation. 141 (14): 1121–1123. doi:10.1161/CIRCULATIONAHA.119.044282. PMID 32250694.
- ^ Grundy SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal RS, et al. (June 2019). "2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the Management of Blood Cholesterol: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines". Journal of the American College of Cardiology. 73 (24): e285–e350. doi:10.1016/j.jacc.2018.11.003. PMID 30423393.
- ^ Nanna MG, Wang TY, Xiang Q, Goldberg AC, Robinson JG, Roger VL, et al. (August 2019). "Sex Differences in the Use of Statins in Community Practice". Circulation: Cardiovascular Quality and Outcomes. 12 (8): e005562. doi:10.1161/CIRCOUTCOMES.118.005562. PMC 6903404. PMID 31416347.
- ^ Lee MT, Mahtta D, Ramsey DJ, Liu J, Misra A, Nasir K, et al. (July 2021). "Sex-Related Disparities in Cardiovascular Health Care Among Patients With Premature Atherosclerotic Cardiovascular Disease". JAMA Cardiology. 6 (7): 782–790. doi:10.1001/jamacardio.2021.0683. PMC 8060887. PMID 33881448.
- ^ Vos E, Rose CP (November 2005). "Questioning the benefits of statins". CMAJ. 173 (10): 1207, author reply 1210. doi:10.1503/cmaj.1050120. PMC 1277053. PMID 16275976.
- ^ Zhao DF, Edelman JJ, Seco M, Bannon PG, Wilson MK, Byrom MJ, Thourani V, Lamy A, Taggart DP, Puskas JD, Vallely MP (February 2017). "Coronary Artery Bypass Grafting With and Without Manipulation of the Ascending Aorta: A Network Meta-Analysis". Journal of the American College of Cardiology. 69 (8): 924–936. doi:10.1016/j.jacc.2016.11.071. PMID 28231944.
- ^ Vlasschaert C, Goss CJ, Pilkey NG, McKeown S, Holden RM (September 2020). "Vitamin K Supplementation for the Prevention of Cardiovascular Disease: Where Is the Evidence? A Systematic Review of Controlled Trials". Nutrients. 12 (10): 2909. doi:10.3390/nu12102909. PMC 7598164. PMID 32977548.
- ^ Price PA, Faus SA, Williamson MK (February 2000). "Warfarin-induced artery calcification is accelerated by growth and vitamin D". Arteriosclerosis, Thrombosis, and Vascular Biology. 20 (2): 317–327. doi:10.1161/01.ATV.20.2.317. PMID 10669626.
- ^ Geleijnse JM, Vermeer C, Grobbee DE, Schurgers LJ, Knapen MH, van der Meer IM, et al. (November 2004). "Dietary intake of menaquinone is associated with a reduced risk of coronary heart disease: the Rotterdam Study". The Journal of Nutrition. 134 (11): 3100–3105. doi:10.1093/jn/134.11.3100. PMID 15514282.
- ^ "Vitamin K". Linus Pauling Institute at Oregon State University. Archived from the original on 7 April 2010. Retrieved 2010-03-25.
- ^ Kong BS, Cho YH, Lee EJ (2014). "G protein-coupled estrogen receptor-1 is involved in the protective effect of protocatechuic aldehyde against endothelial dysfunction". PLOS ONE. 9 (11): e113242. Bibcode:2014PLoSO...9k3242K. doi:10.1371/journal.pone.0113242. PMC 4239058. PMID 25411835.
- ^ Kong BS, Im SJ, Lee YJ, Cho YH, Do YR, Byun JW, et al. (2016). "Vasculoprotective Effects of 3-Hydroxybenzaldehyde against VSMCs Proliferation and ECs Inflammation". PLOS ONE. 11 (3): e0149394. Bibcode:2016PLoSO..1149394K. doi:10.1371/journal.pone.0149394. PMC 4803227. PMID 27002821.
- ^ "The top 10 causes of death". www.who.int. Retrieved 2020-01-26.
- ^ 쿠마르, 비나이, 아바스, 아불 K., Fausto, Nelson & Mitchell, Richard N. (2007) 로빈스 기초 병리학 (8번째). Saunders Elsevier. pp. 348-351 ISBN 978-1-4160-2973-1
- ^ Strong, J. P.; McGill, H. C. (1969-05-06). "The pediatric aspects of atherosclerosis". Journal of Atherosclerosis Research. 9 (3): 251–265. doi:10.1016/S0368-1319(69)80020-7. ISSN 0368-1319. PMID 5346899.
- ^ Zieske, Arthur W.; Malcom, Gray T.; Strong, Jack P. (January 2002). "Natural history and risk factors of atherosclerosis in children and youth: The PDAY study". Pediatric Pathology & Molecular Medicine. 21 (2): 213–237. doi:10.1080/pdp.21.2.213.237. ISSN 1522-7952. PMID 11942537. S2CID 218896145.
- ^ Enos, William F. (1953-07-18). "Coronary Disease Among United States Soldiers Killed in Action in Korea". Journal of the American Medical Association. 152 (12): 1090–1093. doi:10.1001/jama.1953.03690120006002. ISSN 0002-9955. PMID 13052433.
- ^ "Stopping Heart Disease in Childhood". NutritionFacts.org. 15 July 2014. Retrieved 2022-12-08.
- ^ Wilson, Don P. (2000), Feingold, Kenneth R.; Anawalt, Bradley; Boyce, Alison; Chrousos, George (eds.), "Is Atherosclerosis a Pediatric Disease?", Endotext, South Dartmouth (MA): MDText.com, Inc., PMID 27809437, retrieved 2022-12-08
- ^ Strong, Jack P.; Malcom, Gray T.; Newman, William P.; Oalmann, Margaret C. (June 1992). "Early Lesions of Atherosclerosis in Childhood and Youth: Natural History and Risk Factors". Journal of the American College of Nutrition. 11 (sup1): 51S–54S. doi:10.1080/07315724.1992.10737984. ISSN 0731-5724. PMID 1619200.
- ^ Mendis, Shanthi; Nordet, P.; Fernandez-Britto, J.E.; Sternby, N. (2005-03-01). "Atherosclerosis in children and young adults: An overview of the World Health Organization and International Society and Federation of Cardiology study on Pathobiological Determinants of Atherosclerosis in Youth study (1985–1995)". Global Heart. 1 (1): 3. doi:10.1016/j.precon.2005.02.010. ISSN 2211-8179.
- ^ "Atherogenic". Merriam-Webster Dictionary.
- ^ Pfuntner A, Wier LM, Steiner C (December 2013). "Costs for Hospital Stays in the United States, 2011". HCUP Statistical Brief #168. Rockville, MD: Agency for Healthcare Research and Quality. PMID 24455786.
- ^ Barter PJ, Caulfield M, Eriksson M, Grundy SM, Kastelein JJ, Komajda M, Lopez-Sendon J, Mosca L, Tardif JC, Waters DD, Shear CL, Revkin JH, Buhr KA, Fisher MR, Tall AR, Brewer B (November 2007). "Effects of torcetrapib in patients at high risk for coronary events". The New England Journal of Medicine. 357 (21): 2109–22. doi:10.1056/NEJMoa0706628. PMID 17984165.
- ^ Nilsson J, Hansson GK, Shah PK (January 2005). "Immunomodulation of atherosclerosis: implications for vaccine development". Arteriosclerosis, Thrombosis, and Vascular Biology. 25 (1): 18–28. doi:10.1161/01.ATV.0000149142.42590.a2. PMID 15514204.
- ^ Spiteller G (November 2005). "The relation of lipid peroxidation processes with atherogenesis: a new theory on atherogenesis". Molecular Nutrition & Food Research. 49 (11): 999–1013. doi:10.1002/mnfr.200500055. PMID 16270286.
- ^ Berbée JF, Mol IM, Milne GL, Pollock E, Hoeke G, Lütjohann D, Monaco C, Rensen PC, van der Ploeg LH, Shchepinov MS (September 2017). "Deuterium-reinforced polyunsaturated fatty acids protect against atherosclerosis by lowering lipid peroxidation and hypercholesterolemia". Atherosclerosis. 264: 100–107. doi:10.1016/j.atherosclerosis.2017.06.916. PMID 28655430. S2CID 21408028.
- ^ Tsikas D (September 2017). "Combating atherosclerosis with heavy PUFAs: Deuteron not proton is the first". Atherosclerosis. 264: 79–82. doi:10.1016/j.atherosclerosis.2017.07.018. PMID 28756876.
- ^ a b Chen WJ, Yin K, Zhao GJ, Fu YC, Tang CK (June 2012). "The magic and mystery of microRNA-27 in atherosclerosis". Atherosclerosis. 222 (2): 314–23. doi:10.1016/j.atherosclerosis.2012.01.020. PMID 22307089.
- ^ Sacco J, Adeli K (June 2012). "MicroRNAs: emerging roles in lipid and lipoprotein metabolism". Current Opinion in Lipidology. 23 (3): 220–5. doi:10.1097/MOL.0b013e3283534c9f. PMID 22488426. S2CID 23814795.
- ^ Bommer GT, MacDougald OA (March 2011). "Regulation of lipid homeostasis by the bifunctional SREBF2-miR33a locus". Cell Metabolism. 13 (3): 241–7. doi:10.1016/j.cmet.2011.02.004. PMC 3062104. PMID 21356514.
- ^ Rayner KJ, Sheedy FJ, Esau CC, Hussain FN, Temel RE, Parathath S, van Gils JM, Rayner AJ, Chang AN, Suarez Y, Fernandez-Hernando C, Fisher EA, Moore KJ (July 2011). "Antagonism of miR-33 in mice promotes reverse cholesterol transport and regression of atherosclerosis". The Journal of Clinical Investigation. 121 (7): 2921–31. doi:10.1172/JCI57275. PMC 3223840. PMID 21646721.
- ^ Iwakiri Y (March 2012). "A role of miR-33 for cell cycle progression and cell proliferation". Cell Cycle. 11 (6): 1057–8. doi:10.4161/cc.11.6.19744. PMID 22395363.
- ^ Singaraja RR, Stahmer B, Brundert M, Merkel M, Heeren J, Bissada N, Kang M, Timmins JM, Ramakrishnan R, Parks JS, Hayden MR, Rinninger F (August 2006). "Hepatic ATP-binding cassette transporter A1 is a key molecule in high-density lipoprotein cholesteryl ester metabolism in mice". Arteriosclerosis, Thrombosis, and Vascular Biology. 26 (8): 1821–7. doi:10.1161/01.ATV.0000229219.13757.a2. PMID 16728652.
- ^ Zimmer S, Grebe A, Bakke SS, Bode N, Halvorsen B, Ulas T, Skjelland M, De Nardo D, Labzin LI, Kerksiek A, Hempel C, Heneka MT, Hawxhurst V, Fitzgerald ML, Trebicka J, Björkhem I, Gustafsson JÅ, Westerterp M, Tall AR, Wright SD, Espevik T, Schultze JL, Nickenig G, Lütjohann D, Latz E (April 2016). "Cyclodextrin promotes atherosclerosis regression via macrophage reprogramming". Science Translational Medicine. 8 (333): 333ra50. doi:10.1126/scitranslmed.aad6100. PMC 4878149. PMID 27053774.
- 요약 정리 위치:
- ^ Wu H, Roks AJ (February 2014). "Genomic instability and vascular aging: a focus on nucleotide excision repair". Trends in Cardiovascular Medicine. 24 (2): 61–8. doi:10.1016/j.tcm.2013.06.005. PMID 23953979.
- ^ a b Bautista-Niño PK, Portilla-Fernandez E, Vaughan DE, Danser AH, Roks AJ (May 2016). "DNA Damage: A Main Determinant of Vascular Aging". International Journal of Molecular Sciences. 17 (5): 748. doi:10.3390/ijms17050748. PMC 4881569. PMID 27213333.
- ^ Shah AV, Bennett MR (December 2017). "DNA damage-dependent mechanisms of ageing and disease in the macro- and microvasculature". European Journal of Pharmacology. 816: 116–128. doi:10.1016/j.ejphar.2017.03.050. PMID 28347738. S2CID 1034518.
- ^ a b Martinet W, Knaapen MW, De Meyer GR, Herman AG, Kockx MM (August 2002). "Elevated levels of oxidative DNA damage and DNA repair enzymes in human atherosclerotic plaques". Circulation. 106 (8): 927–32. doi:10.1161/01.cir.0000026393.47805.21. PMID 12186795.
- ^ Ishida T, Ishida M, Tashiro S, Yoshizumi M, Kihara Y (2014). "Role of DNA damage in cardiovascular disease". Circulation Journal. 78 (1): 42–50. doi:10.1253/circj.CJ-13-1194. PMID 24334614.
- ^ a b Barrington WT, Lusis AJ (December 2017). "Atherosclerosis: Association between the gut microbiome and atherosclerosis". Nature Reviews. Cardiology. 14 (12): 699–700. doi:10.1038/nrcardio.2017.169. PMC 5815826. PMID 29099096.
- ^ Jie Z, Xia H, Zhong SL, Feng Q, Li S, Liang S, et al. (October 2017). "The gut microbiome in atherosclerotic cardiovascular disease". Nature Communications. 8 (1): 845. Bibcode:2017NatCo...8..845J. doi:10.1038/s41467-017-00900-1. PMC 5635030. PMID 29018189.
- ^ a b c Harman JL, Jørgensen HF (October 2019). "The role of smooth muscle cells in plaque stability: Therapeutic targeting potential". British Journal of Pharmacology. 176 (19): 3741–3753. doi:10.1111/bph.14779. PMC 6780045. PMID 31254285.
- ^ Bennett MR, Sinha S, Owens GK (February 2016). "Vascular Smooth Muscle Cells in Atherosclerosis". Circulation Research. 118 (4): 692–702. doi:10.1161/CIRCRESAHA.115.306361. PMC 4762053. PMID 26892967.
- ^ Gomez D, Shankman LS, Nguyen AT, Owens GK (February 2013). "Detection of histone modifications at specific gene loci in single cells in histological sections". Nature Methods. 10 (2): 171–177. doi:10.1038/nmeth.2332. PMC 3560316. PMID 23314172.
- ^ a b Wang Y, Dubland JA, Allahverdian S, Asonye E, Sahin B, Jaw JE, et al. (May 2019). "Smooth Muscle Cells Contribute the Majority of Foam Cells in ApoE (Apolipoprotein E)-Deficient Mouse Atherosclerosis". Arteriosclerosis, Thrombosis, and Vascular Biology. 39 (5): 876–887. doi:10.1161/ATVBAHA.119.312434. PMC 6482082. PMID 30786740.
- ^ a b Chappell J, Harman JL, Narasimhan VM, Yu H, Foote K, Simons BD, et al. (December 2016). "Extensive Proliferation of a Subset of Differentiated, yet Plastic, Medial Vascular Smooth Muscle Cells Contributes to Neointimal Formation in Mouse Injury and Atherosclerosis Models". Circulation Research. 119 (12): 1313–1323. doi:10.1161/CIRCRESAHA.116.309799. PMC 5149073. PMID 27682618.
- ^ Durham AL, Speer MY, Scatena M, Giachelli CM, Shanahan CM (March 2018). "Role of smooth muscle cells in vascular calcification: implications in atherosclerosis and arterial stiffness". Cardiovascular Research. 114 (4): 590–600. doi:10.1093/cvr/cvy010. PMC 5852633. PMID 29514202.
- ^ Basatemur GL, Jørgensen HF, Clarke MC, Bennett MR, Mallat Z (December 2019). "Vascular smooth muscle cells in atherosclerosis". Nature Reviews. Cardiology. 16 (12): 727–744. doi:10.1038/s41569-019-0227-9. PMID 31243391. S2CID 195657448.


