프로게스테론의 약동학
Pharmacokinetics of progesterone | |
| 임상자료 | |
|---|---|
| 경로: 행정 | • 입으로(캡슐) • 하위 언어(표) • 경피(크림, 젤) • 질(캡슐, 태블릿, 젤, 임시, 반지) • 직장(보조) • 주입(오일 용액) • 주사()aq. soln. • 자궁내()IUD |
| 마약류 | 프로게스테로이드; 안티미노코르티코이드; 신경스테로이드 |
| 약동학 데이터 | |
| 생체이용가능성 | 구술:[1] <2.4% 질: 4~8%[2][3][4] |
| 단백질 결합 | 98–99%:[5][6] • 알부민: 80% • CBG: 18% • SHBG: <1% • 무료: 1~2% |
| 신진대사 | 주로 간: • 5α 및 5β-저감효소 • 및 • 및 • 결합 • 17α-히드록실라아제 • 21-히드록실라아제 • (예: CYP3A4) |
| 대사물 | • 디히드롭로게스테론 • 임페아놀론 • 임페라네디올스 • 20α-히드록시프로게스테론 • 17α-히드록시프로게스테론 • 임페아네트리올스 • 11-Deoxycorticosterone (그리고 글루쿠로니드/술파테콘쥬게이트) |
| 제거 반감기 | • 경구: 5~10시간(식량 포함)[7][8] • 하위 언어: 6-7시간[9] • 질: 14-50시간[10][9] • 경피: 30~40시간[11] • : 20~28시간[12][10][13] • : 13~18시간[13] • : 3~90분[14] |
| 배설 | 담즙과 소변[15][16] |
프로게스테론의 약동학은 프로게스테론의 약동학, 약동학, 그리고 프로게스테론의 다양한 투여경로에 관한 것이다.[17][18]
프로게스테론은 자연적으로 발생하며 생물학적 정체성 있는 프로게스테론 또는 프로게스테론 수용체의 작용제로 내생성 프로게스테론 같은 프로게스테론균의 생물학적 표적이다.[17]프로게스테론은 또한 항미노코르티코이드와 억제 신경스테로이드 활동을 하는 반면, 글루코코르티코이드나 항안드로겐 활동을 거의 또는 전혀 하지 않고 안드로겐 활동을 하지 않는 것으로 보인다.[17]프로게스테론은 프로게스테론의 프로게스테론 활동 때문에 자궁, 자궁경부, 질과 같은 특정 조직에서 기능적인 항에스트로겐 효과가 있다.[17]또 프로게스테론은 프로게스테론의 원발적인 활동으로 인해 항원항산화 효과가 있으며, 생식 억제와 성호르몬 생성을 억제할 수 있다.[17]프로게스테론은 메드록시프로게스테론 아세테이트나 노레시스테론 같은 프로게스틴(합성 프로게스테론)과 다르며 약역학 및 약동학뿐 아니라 효능, 허용성, 안전성에 대한 함의가 있다.[17]
프로게스테론은 입으로, 질로, 근육이나 지방으로 주입하여 복용할 수 있다.[17]프로게스테론 질 링과 프로게스테론 자궁내 장치도 의약품으로 이용할 수 있다.[19][20]
정상 수준
프로게스테론은 프로게스테론 수치가 낮은 사람들에게 호르몬 대체요법의 일부로 사용된다.정상적인 생리학적 상황과 비교하기 위해 프로게스테론의 루테론 위상 수준은 4~30ng/mL인 반면 프로게스테론의 엽상 위상 수준은 0.02~0.9ng/mL, 갱년기 위상 수준은 0.03~0.3ng/mL, 남성의 프로게스테론 수준은 0.12~0.3ng/mL이다.[21][22]임신 기간 중 처음 4~8주간의 프로게스테론 수치는 25~75ng/mL이며, 일반적으로 기간은 140~200ng/mL 정도다.[23][21]임신 말기에 체내에서 프로게스테론의 생산량은 하루에 약 250mg이며, 그 중 90%가 산모 순환에 도달한다.[24]
행정경로
| 경로 | 형태 | 복용량 | Cmax (ng/mL) | Tmax (시간) | t1/2 (시간) | ||
|---|---|---|---|---|---|---|---|
| 구강 | 캡슐 | 200mg | 4.3–11.7 | 2–2.5 | ? | ||
| 하위 언어 | 태블릿[a] | 100mg | 13.5 | 1–4 | ~6–7 | ||
| 현수 | 100mg | 17.6 | 0.5–1 | ? | |||
| 질내 | 태블릿[a] | 100mg | 10.9 | 6–7 | 13.7 | ||
| 캡슐 | 100mg | 9.7 | 1–3 | ? | |||
| 근육내 주사제 | 오일 용액 | 50mg | 14.3 | 8.7 | ? | ||
| 100mg | 113 | 6.7 | 22.3 | ||||
| Aq. 해결책[b] | 100mg | 440 | 0.88 | 14.3 | |||
| 피하지방 주사제 | Aq. 솔루션[b] | 25mg | 57.8 | 0.92 | 13.1 | ||
| 50mg | 103 | 0.92 | 17.2 | ||||
| 100mg | 235–300 | 0.92 | 17.2–17.6 | ||||
| 경로 | 형태 | 복용량 | 브랜드명 | 가용성[b] |
|---|---|---|---|---|
| 구강 | 캡슐 | 100, 200, 300 mg | 프로메트리움[c] | 널리 퍼진 |
| 태블릿()SR | 200, 300, 400 mg | 두바게스트 SR[c] | 인도 | |
| 하위 언어 | 태블릿 | 10, 25, 50, 100 mg | 루테이나[c] | 유럽[d] |
| 경피 | 젤[e] | 1%(25mg) | 프로게스토겔 | 유럽 |
| 질내 | 캡슐 | 100, 200 mg | 우트로게스탄 주 | 널리 퍼진 |
| 태블릿 | 100mg | 엔도메트린[c] | 널리 퍼진 | |
| 젤 | 4, 8%(45, 90mg) | 크리노네[c] | 널리 퍼진 | |
| 임시방편 | 200, 400 mg | 사이클로게스트 | 유럽 | |
| 울리다 | 1일[f] 10mg | 연마[c] | 남아메리카[g] | |
| 직장 | 임시방편 | 200, 400 mg | 사이클로게스트 | 유럽 |
| 자궁 | IUD | 38mg | 프로게스타서트 | 중단됨 |
| 근육내 주사제 | 오일 용액 | 2, 5, 10, 20, 25, 50, 100 mg/ml | 프로루톤[c] | 널리 퍼진 |
| Aq. susp. | 12.5, 30, 100 mg/ml | 아골루틴[c] | 유럽[h] | |
| 에멀전 | 5, 10, 25 mg/ml | 디프로 에멀전 | 중단됨 | |
| 마이크로스프. | 20, 100 mg/ml | 프로스피어[c] | 멕시코 | |
| 피하지방 | Aq. soln. (inj.) | 25mg/vial | 프로루텍스 | 유럽 |
| 임플란트 | 50, 100 mg | 프로루톤[c] | 중단됨 | |
| 정맥주사 | Aq. soln. (inj.) | 20 mg/mL | 프리몰루트 | 중단됨 |
출처 및 각주: | ||||
프로게스테론의 약동학은 그 투여경로에 따라 달라진다.이 약은 경구 투여를 위해 미크론화 프로게스테론, "구강 미크론화 프로게스테론" ("OMP") 또는 간단히 "구강 프로게스테론"이라고 불리는 오일이 함유된 캡슐 형태로 승인된다.[41]질 또는 직장용 부관, 질젤, 근육내 주입을 위한 오일 용액, 피하주사를 위한 수용액 등의 형태로도 이용할 수 있다.[41][13][42]
프로게스테론이 사용된 투여경로는 경구, 경피, 질, 직장, 근육내, 피하 및 정맥주사를 포함한다.[13]구강 프로게스테론은 흡수율(낮음)과 간극률(급속) 면에서 질·근내 프로게스테론보다 낮은 것으로 나타났다.[13]질 프로게스테론은 프로게스테론 젤, 링, 그리고 보조관이나 페세리의 형태로 이용 가능하다.[13]경구 투여에 비해 경구내 프로게스테론의 장점은 생체이용률, 빠른 흡수, 1차 통과 대사 기피, 혈장 농도 지속, 국소내막 효과 등이 있으며, 경구내 주입에 비해 경구내 프로게스테론의 장점은 보다 편리하고 주사시트가 부족하다는 것이다.e [13]고통
비강 스프레이로서의 프로게스테론은 치료 수준 달성에 효과가 있는 것으로 밝혀졌으며, 비강 자극과는 관련이 없지만, 스프레이의 불쾌한 맛과 관련이 있었다.[13]직장, 근육내, 정맥내 노선은 특히 장기 치료에 불편할 수 있다.[13]프로게스테론의 혈장 수준은 투여경로가 다르지만 질 투여 후와 직장 투여 후 유사하며, 직장 투여는 질 감염, 방광염, 최근 출산, 장벽 피임 방법 사용 시 질 프로게스테론의 대안이다.[13]프로게스테론의 근육내 주입은 정상 루테랄상 농도 및 다른 경로로 달성한 수준보다 훨씬 높은 프로게스테론 수준을 달성할 수 있다.[13]
구강행정
연구의 방법론적 문제
구강 프로게스테론의 약동학에 대한 지식은 결함 있는 분석 기법의 사용으로 인해 복잡해졌다.[43][44][45]프로게스테론을 구강으로 복용하면 1차 통과대사로 인해 대사물이 매우 높은 수준으로 발생한다.[43][44][45]대부분의 이전 연구들은 프로게스테론 수치를 측정하기 위해 면역측정법(IA)으로 알려진 방법을 사용해 왔다.[43][44][45]그러나 크로마토그래픽 분리(CS)가 없는 IA는 교차반응도가 높아 프로게스테론과 올롭 메탄올론, 임페아놀론 등 대사물을 구분할 수 없다.[43][44][45]그 결과, IA를 이용하여 경구 프로게스테론의 약동학을 평가한 연구에서는 프로게스테론 수치가 거짓으로 높고 부정확한 종속 약동학 매개변수가 보고되었다.[43][44][45]
적절한 CS와 함께 액상 크로마토그래피-질량분석법(LC-MS), IA와 같은 신뢰할 수 있고 정확한 방법을 사용한 비교 연구에서는 CS가 없는 IA가 프로게스테론 수준을 5~8배 과대평가한다는 것을 발견했다.[43][44][45]이 때문에 구강 프로게스테론의 약동학을 연구할 때는 신뢰성 있는 어세이 사용이 필수적이며, 이러한 방법론적 문제에 대한 인식도 구강 프로게스테론의 약동학을 정확하게 이해하는데 필수적이다.[43][44][45]반대로 질 투여와 근육내 주입과 같은 프로게스테론의 파렌테론 경로에는 동일한 문제가 적용되지 않는다. 왜냐하면 이러한 경로는 최초 통과의 대상이 아니며 상대적으로 낮은 수준의 프로게스테론 대사물이 형성되기 때문이다.[43][44][45]
흡수, 생물학적 가용성 및 수준
프로게스테론의 구강 생체이용률은 매우 낮다.[46]IA를 이용한 연구는 일반적으로 경구 프로게스테론의 생체이용률을 10% [46]미만으로 측정했으며, 한 연구에서는 6.2~[47][12]8.6%의 값을 보고하였다.그러나 이러한 값은 과대평가된 것이다. LC-MS를 사용한 연구에서는 경구 프로게스테론의 생체이용률이 질 프로게스테론 젤에 비해 2.4%에 불과하다는 것을 발견했다.[1]더구나 이는 질 프로게스테론보다 생체이용률이 훨씬 높은 분자주사에 의한 프로게스테론 표준과는 비교가 되지 않았다.[48][4]구강 프로게스테론의 생체이용률이 매우 낮은 것은 위장관에서 잘 흡수되지 않고 대량의 신진대사를 거치게 되어 간을 통과하는 첫 번째 통과 동안에 거의 완전한 비활성화가 일어나기 때문이다.[46][49]경구 생체이용률이 낮기 때문에 매우 많은 양의 프로게스테론이 경구 경로에 의해 사용되어야 상당한 순환 프로게스테론 레벨을 달성할 수 있다.[46]게다가 오늘날 구강 프로게스테론은 항상 미크론화 되어 기름에 매달려 있다.[46][41][48][50]이를 통해 경구용 프로게스테론의 생체이용성이 일반 제분제 프로게스테론에 비해 현저히 향상되고, 이를 실제 용량으로 사용할 수 있다.[46]"도덕적 프로게스테론"이라는 용어를 사용할 때 임상적으로 사용되는 것과 달리 언급되지 않는 한 거의 항상 언급되고 있는 것은 석유에 매달려 있는 미세화된 프로게스테론이다.[46][17][43]
미크론화(micronization)는 고체 물질의 입자의 평균 직경을 줄이는 과정이다.[33]프로게스테론을 미세화함으로써 입자가 작아지고(주로 <10μM>) 표면적이 늘어나 장으로부터의 흡수를 강화한다.[46][33]중사슬 지방산을 함유한 오일에서 프로게스테론의 중지 및 부분 용해도[51] 마찬가지로 경구 프로게스테론의 생체이용성을 향상시킨다.[17][52][53]프로게스테론은 지방질 화합물로, 기름에서 프로게스테론의 정지가 림프계에 의한 흡수를 개선하여 구강 프로게스테론의 일부가 간을 통해 첫 번째 통과를 우회하여 생체이용성을 높일 수 있다는 이론이 제기되어 왔다.[46][54][55][56]일반분쇄 프로게스테론 대비 200mg 경구 투여 1회 이후 프로게스테론의 최고 수위는 미크론화 1.4배, 석유정류 1.2배, 석유정류 3.2배 증가했다.[56]구강 미크론화 프로게스테론은 기름에 매달린 채 장에서 거의 완전히 흡수된다.[14]구강 프로게스테론의 생체이용률에는 개인간 변동성이 매우 크다.[17][12]프로게스테론은 생체이용성이 떨어져 수십 년간 구강으로 사용되지 않아(1980년 오일 충전 젤라틴 캡슐에 구강 미크론화 프로게스테론이 도입되기 전까지) 대사 안정성이 향상되고 구강 생체이용률이 높은 구강 프로게스틴(합성 프로게스테론)이 개발돼 임상적으로 사용돼 왔다.[48][57]
일반적인 임상 용량에서 구강 프로게스테론을 사용할 경우 신뢰할 수 있는 방법을 사용하여 매우 낮은 수준의 프로게스테론만 측정한다.[43][44][45]경구용 프로게스테론 단회 용량에 이어, 100 mg의 프로게스테론 1.5~2.4 ng/mL와 200 mg의 2.8~4.7 ng/mL의 최고 수준은 LC–MS, 액체 크로마토그래피-tandem 질량분석(LC–MS/MS), 적절한 CS의 IA를 사용하여 측정되었다.[43][58][1]그러한 한 연구에서, 100mg의 경구 프로게스테론 투여 후 프로게스테론의 최고 수위는 2.2ng/mL였지만, 프로게스테론 수치는 약 4시간 미만으로 유의하게 상승하였고, 24시간 동안의 평균 프로게스테론 수치는 0.14ng/mL에 불과했다.[45][1]비교를 위해 LC–MS/MS를 사용한 월경 주기의 루터상에서의 정상 프로게스테론 수치는 6.7~22.2ng/mL이다.[59]경구 프로게스테론 프로게스테론 수치 측정에 IA만 사용했을 때, 각각 단일 100, 200, 300mg 투여 후 6.5~10.2ng/mL, 13.8ng/mL에서 19.9ng/mL, 32.3~49.8ng/mL의 피크가 관찰되었다.[47][12]한 IA 기반 연구에서는 경구 프로게스테론 단 300mg으로 최대 프로게스테론 수치가 16~626ng/mL(평균 247ng/mL)인 것으로 보고되기도 했다.[60][61]
구강 프로게스테론을 금식 대신 음식과 함께 복용하면 프로게스테론의 최고치 및 전반적인 수준이 현저히 높아진다.[8][12][7]LC-MS/MS를 이용한 연구에서는 고지방 식사를 시작한 지 30분 이내에 100mg의 구강 프로게스테론을 복용했을 때 프로게스테론의 최고 수위는 2.6배, 면적당 1.8배 높은 것으로 나타났다.[8]또 다른 연구에서는 200mg의 구강 프로게스테론을 음식과 함께 섭취했을 때 프로게스테론의 최고 수위는 5배, 면적당 최저 수위는 2배 증가했다.[12]그러나 이 연구는 프로게스테론 수준을 정량화하기 위해 신뢰할 수 없는 IA 방법을 사용했다.[12]구강 프로게스테론은 식용으로 섭취하면 생체이용률이 높아지지만 IA로 측정해도 전체 생체이용률은 여전히 낮다.[18]구강 프로게스테론을 음식과 함께 섭취할 때 프로게스테론 수치가 향상되는 것은 림프 흡수가 강화되어 구강 프로게스테론이 1차 통과 신진대사를 부분적으로 우회할 수 있기 때문일 수 있다고 제안되었다.[12][46][54][55]
제거 및 지속시간
구강 프로게스테론이 있는 프로게스테론 수치는 신뢰할 수 없는 IA 방법에 의해 12시간에서 24시간 동안 상승된 상태로 측정되었다.[1][41]검사 방법과 상관없이 경구 프로게스테론 투여 후 프로게스테론의 최고 수위는 약 1-3시간 후에 발생한다.[44]순환 중 프로게스테론의 제거 반감기는 약 3분에서 90분의 범위에서 매우 짧다.[14]IA를 사용한 이전의 연구들은 약 16시간에서 18시간의 구강 프로게스테론의 반감기를 과대평가했다고 보고했다.[41]고성능 액체 크로마토그래피-탄뎀 질량 분석법(HPLC–MS/MS) 및 이와 유사한 방법을 사용한 후속 연구 결과, 프로게스테론의 반감기를 제거했으며, 구강 프로게스테론은 약 4.6~5.2시간, 식품과 함께 섭취했을 때 9.98시간이었다.[7][8]구강 프로게스테론의 반감기와 작용 지속시간이 짧기 때문에 하루 2 3회 분량으로도 복용할 수 있다.[41][62][63]
1차 통과 효과 및 신경 스테로이드
프로게스테론은 알로프 메탄올론과 임페탄올론으로 대사되는데, 이는 신경 스테로이드와 GABAA 수용체의 전위제다.[65][66]프로게스테론의 이러한 대사물로의 변환은 효소 5α와 5β-감소효소 및 3α-히드록시스테로이드 탈수소효소에 의해 촉매되며, 주로 간에서 발생하지만 생식 내분비 조직, 피부, 뇌 및 기타 조직에서도 발생한다.[67]구강 프로게스테론과의 광범위한 1차 통과 대사 때문에 약 80~90% 이상의 프로게스테론이 이들 대사물로 급속하게 변형되고, 그 결과 이들 신경 스테로이드의 대량이 형성되어 몸과 뇌 전체에 순환된다.[68][69][70][71]구강 프로게스테론의 흔히 보고되는 부작용으로는 어지럼증, 졸음, 진정, 졸음, 피로 등이 있다.[65][66]경구 및 충분히 많은 양의 근육내 프로게스테론 모두 이러한 진정작용을 일으킬 수 있다.[72][73][74]그러나, 구강 프로게스테론과 비교했을 때, 이러한 신경 스테로이드의 수치는 질이나 근육내 프로게스테론 같은 종두 경로로 인해 매우 낮은 것으로 밝혀졌다.[64][75]경구 프로게스테론의 생체이용률과 마찬가지로 경구 프로게스테론을 사용한 알롭페르놀론과 임페놀론의 형성과 수준에 있어 개인간 변동성이 높다.[17]결과적으로, 어떤 개인은 구강 프로게스테론(구강 프로게스테론)으로 상당한 중심적 우울증 효과를 경험할 수 있는 반면, 다른 개인은 그러한 영향을 최소화할 수 있다.[17]
프로게스테론의 경구 투여로 알롭페르놀론과 임페롤놀론은 프로게스테론보다 더 높은 농도로 순환한다.[17][64]프로게스테론의 이러한 신경스테로이드 대사물은 순환하는 데 생물학적 반감기가 비교적 짧다.[76][77]이 때문에 알롭 메탄올론과 임페탄올론 농도에 극적이고 고도로 초자연적인 스파이크가 나타나고 프로게스테론 경구 섭취 시마다 급격한 감소 현상이 나타난다.[69][70][64]이와 같이 신경스테로이드 수치는 경구 프로게스테론 치료와 함께 비위생적인 방식으로 크게 변동한다(예: 알로프 메탄올론의 경우 15배).[69][71]또한, 구강 프로게스테론이 함유된 식품의 섭취는 흡수를 2배 증가시키며, 이는 특히 프로게스테론이 함유된 식품의 섭취가 용량에서 용량까지 일관되지 않는 경우 신경 스테로이드 수준의 변동을 더욱 증폭시킬 수 있다.[12]
구강 투여와 달리, 질 투여와 같은 파렌탈 프로게스테론은 1차 통과 효과를 피하며, 신경스테로이드 대사물의 초산혈학적 수준과 관련이 없으며, 신경스테로이드 수준의 스파이크 또는 현저한 변동과 관련이 없다.[69]파렌터럴 루트는 경구 투여 대신 사용하면 문제가 있는 것으로 판명될 경우 신경스테로이드 변동과 관련된 부작용을 피할 수 있다.[71][17]경구 프로게스테론의 낮은 용량(예: 100 mg/일)도 신경스테로이드 대사물의 비교적 낮은 형성과 관련이 있으며, 이와 유사하게 이러한 부작용을 완화하는데 도움이 될 수 있다.[17]또 프로게스테론에서 나오는 알롭 메탄올론(임신아놀론은 아니지만)의 생산을 차단하는 5α 저감효소 억제제 두타스테라이드도 월경 전 증후군의 증상을 감소시키는 것으로 나타났다.[78]
프로게스테론의 처방전 없이 사용할 수 있는 보충제이자 친밀한 아날로그인 임페놀론은 프로게스테론과 유사한 경구 투여로 올롭페르놀론, 임페놀론 등 신경 스테로이드로 광범위하게 전환된다.[79][80][81][82]반대로, 이것은 임신의 경피적 투여에서는 볼 수 없었다.[82]
임상 Progestengency 효력 및 효과
IA를 사용한 연구 때문에, 구강 프로게스테론이 프로게스테론 또는 그 이상의 루테론 위상 수준을 쉽게 달성할 수 있고 상당한 프로게스테론 효과를 낼 수 있다고 여러 해 동안 잘못 믿어졌다.[43][44][45]실제로 LC-MS와 같은 신뢰할 수 있는 방법으로 측정했을 때 경구 투여 시 매우 낮은 수준의 프로게스테론은 강력한 프로게스테론 효과에 불충분해 보인다.[45][1]이는 거의 모든 프로게스틴과 대조적으로 구강 프로게스테론이 갱년기 호르몬 치료에서 에스트로겐과 결합할 때 자궁내막암의 위험 증가가 관찰되었다는 사실에서 증명된다.[45][1]이 결과는 경구 프로게스테론의 일반적인 임상 선량이 완전한 자궁내막 보호에 불충분할 수 있음을 시사한다.[45][1]그러나, 달성한 프로게스테론의 매우 낮은 수준에도 불구하고, 구강 프로게스테론의 전형적인 임상 선량은 에스트로겐에 의한 자궁내막증후군을 예방하는 데 효과적이다.[43][44]한편, 구강 프로게스테론은 완전한 자궁내막 분비 변환을 생성하지 못하여 보조 생식에 사용하기에 부적합하다고 간주되는 반면 질과 근육내 프로게스테론은 효과적이다.[83][68]300~600mg/day 구강 프로게스테론 조차도 보조 번식의 후두부 지원에 300~600mg/day 구강 프로게스테론 조차도 완전한 후두상 자궁내막 변화를 일으키지 못하고 있다.[71][68]구강 비미크론화 프로게스테론이 열유발 효과가 있는지에 대한 연구는 서로 다른 연구에서 상반된 연구 결과를 보여주었다.[84]
구강 프로게스테론이 함유된 프로게스테론의 낮은 수치는 또한 폐경 후 여성의 에스트로겐 치료에 첨가되었을 때 프로게스균에 비해 유방암과 정맥 혈전증의 위험의 차이를 설명할 수 있다.[45]이러한 위험은 프로게스테론과 유사한 PR 작용제인 프로게스틴에 의해 증가되지만, 구강 프로게스테론에 의해 증가하거나 전혀 증가하지 않는 것으로 밝혀졌다.[44][45]경구 프로게스테론의 전형적인 임상 선량은 매우 낮은 수준의 프로게스테론을 달성하고, 루테랄 위상 프로게스테론 수준의 프로게스테론 요법은 충분히 큰 임상 연구에서 적절하게 평가된 적이 없기 때문에 프로게스테론이 프로게스틴과 다소 다르며 유방 c의 위험을 증가시키지 않는다고 알려져 왔다.혈관 또는 정맥 혈전증은 근거가 없다.[44][45][58]더욱이 적절한 데이터가 없는 경우 프로게스테론은 최소한 프로게스틴과 동등한 것으로 그러한 합병증의 잠재적 위험요인으로 간주하는 것이 합리적일 것이다.[44][45][58]실제로 프리클리닉 연구는 유방 프로게스테론의 발암성 역할을 시사하고 있으며,[85] 프랑스 E3N 연구는 장기 (>5년) 투여 후 폐경 후 여성에게서 에스트로겐과 구강 프로게스테론 요법으로 유방암의 위험성이 현저히 높다는 것을 관찰했다.[44][45]이것은 유방암 위험의 증가를 나타내기 위해 더 긴 노출 기간이 필요할 수 있는 구강 프로게스테론의 약한 증식 효과와 잠재적으로 일치한다.[44][45]
지속 릴리즈 제형
구강 미크론화 프로게스테론(구강 천연 미크론화 프로게스테론 지속 릴리즈 또는 "오랄 NMP SR"로도 알려져 있음)의 지속 출시 태블릿 제형이 인도에서 Dubagest SR, Gessofit SR, Susten SR이라는 브랜드 이름으로 출시되었다.[86][87][88][89][90][91][92][93][94]프로게스테론 방출이 24시간 이상 느리고 매끄러운 모습을 보여주며 제거 반감기는 18시간이다.[86][93]이것은 진정제와 같은 경구 프로게스테론의 신경스테로이드 관련 부작용을 최소화할 뿐만 아니라 안정적이고 지속적인 프로게스테론 수준을 초래한다.[86][93]
북칼 행정
프로게스테론은 Buccal 행정부에서 사용하기 위해 연구되어 왔다.[17][95][96][97][98][99][100]이 약은 프로게스테론 링구소브스, 루토실롤, 멤브레트, 이승스트렛스라는 상표명으로 부칼정제 형태로 시판되었다.[101][102]부칼 프로게스테론의 임상 복용량은 근내 주입의 경우 하루 5~60mg/일에 비해 10~50mg/day로 설명되어 왔다.[101]
하위 언어 관리
루테리나라는 브랜드명으로 시판되는 프로게스테론의 미세화된 태블릿 제형은 질 경로 외에 언어별 행정에서 사용하도록 표시되며 폴란드와 우크라이나에서 사용이 승인된다.[105]하위 언어 프로게스테론은 미국과 같은 국가의 복합 약국에서도 이용할 수 있다.[106]프로게스테론은 하루 3, 4회 50~150mg의 용량으로 하위 언어 루트에 의해 사용된다.[105][9]루테리나의 단일 100mg 하위 언어 선량은 1~4시간 후 13.5ng/mL의 평균 피크 프로게스테론 수준에 도달하고, 제거 반감기는 약 6~7시간인 것으로 밝혀졌다.[105][9]
많은 다른 연구들은 또한 하위 언어행정에 의한 프로게스테론의 사용을 조사해왔다.[107][108][109][104]오래된 연구들은 또한 하위 언어의 프로게스테론을 탐구해왔다.[110][111][112][113]배아 전이가 진행 중인 환자에 대한 언어보조 프로게스테론 연구결과 1 mL 정지에 용해된 프로게스테론 50 또는 100 mg의 언어보조 프로게스테론 투여 후 30~60분 만에 프로게스테론의 최고 수치에 도달했고 100 mg 용량으로 평균 17.61 ± 3.78 ng/mL에 도달했다.[107][108]다만 6시간 동안 5ng/mL 미만으로 지속시간이 짧았고, 하루 종일 프로게스테론의 적정 순환수치가 유지되려면 하루 2, 3회 재행정을 해야 했다.[107][108]또 다른 연구는 100 mg/일 분자 내 프로게스테론이 생산한 것과 유사한 순환 수준을 달성하기 위해 언어 내 프로게스테론을 8시간마다 400 mg의 용량으로 투여해야 한다는 것을 발견했다.[107]한 연구에서는 하루에 3회 400mg 아언어 프로게스테론을 투여했으며 평균 프로게스테론 수치인 57.8±37.4ng/mL를 달성했는데, 이는 50mg/일 근내 프로게스테론에서 생성된 수치와 유사했다.[108]
인트라나스 행정
프로게스테론은 한 연구에서 비강 스프레이 형태의 비강내 경로에 의해 평가되었다.[107][17][114][115]프로게스테론 수치는 자궁내막 변화 측면에서 낮고 불충분했다.[71]
경피행정
경피용 프로게스테론은 미국 식품의약국(FDA)이 승인하지 않았다.[116][117][58]복수의 제약사가 전신 경피 프로게스테론 제형의 개발을 추진했지만, 궁극적으로 임상용으로 개발·소개된 것은 하나도 없다.[118]전신 사용 승인을 받은 경피 프로게스테론의 공식은 없지만, 유방에서의 국소적 사용을 위한 1% 국소 겔 제형은 다양한 국가에서 Progestogel이라는 상표명으로 유방 통증을 치료할 수 있도록 승인되었다.[119][48][120]
전신 사용이 허가된 경피 프로게스테론의 공식은 없지만, 일부 국가에서는 맞춤형 복합 약국에서 크림과 젤 형태로 경피 프로게스테론이 제공되고 있으며, 미국에서도 처방전 없이 장외에서 구입할 수 있다.[116][117][58]트랜스더말 프로게스테론은 미국과 유럽에서 수천 명의 여성들이 갱년기 호르몬 치료의 성분으로 사용되어 왔다.[116]그러나 이러한 제품들은 규제되지 않고 임상적으로 테스트되지 않았으며, 종종 약동학에 대해 거의 알려져 있지 않다.[116]또한 성분의 차이가 매우 크기 때문에 경피 프로게스테론의 흡수는 제형에 따라 크게 다를 수 있다.[117]게다가 치료적 프로게스테론의 치료적 프로게스테론 효과, 가장 중요한 것은 에스트로겐에 대한 적절한 자궁내막 보호의 시스템적 효과에 대한 논란이 있다.[116][117]
일부 비규제 경피 프로게스테론 제품에는 디오스코레아 빌로사(Diosgenin, 산업적으로 프로게스테론을 생산하기 위해 화학적으로 전환되는 식물 스테로이드)[121]에서 유래한 '야생 야마 추출물'이 들어 있지만 인체가 활성 성분(diosgenin, 산업적으로 프로게스테론을 생산하기 위해 화학적으로 전환되는 식물)을 프로게스테론(progesterone)으로 전환할 수 있다는 증거는 없다.[122][123]
흡수 및 분배

화합물의 피부 투과성은 화학적 특성, 특히 지방질과 수질을 기반으로 한다.[17][124]일반적으로 스테로이드에 존재하는 하이드록실(hydroxyl) 그룹과 같은 극성 그룹일수록 수분이 많고 지방질이 적을수록 피부 투과성이 낮아진다.[17][124]이 때문에 프로게스테론과 에스트론은 피부 투과성이 높고 에스트라디올은 피부 투과성이 중간 정도며 에스트리올과 코티솔은 피부 투과성이 낮다.[17]유방에 적용된 프로게스테론의 경피 생체이용률은 [118][125][126][127]약 10%이다.이것은 다른 피부 부위에 적용되기는 하지만 에스트라디올과 테스토스테론의 일반적인 경피 흡수와 거의 같다.[118][128][129][130]경피 프로게스테론의 도포 부위는 그 흡수에 영향을 미칠 수 있다.[117]프로게스테론은 투여 직후 유방에 경피 연고로 도포됐지만 허벅지나 복부 등 다른 부위에는 도포하지 않아 순환수치가 크게 증가하는 것을 관찰한 연구결과가 있다.[117]
에스트라디올은 피코몰라 범위의 수준(pg/mL)에서 순환하는 반면 프로게스테론은 나노몰라 범위의 농도(ng/mL)에서 순환하며, 이러한 수준을 생성하기 위해서는 비교적 큰 선량이 필요하다.[131][71]신체는 루테랄 단계에서 하루 평균 약 25mg의 프로게스테론을 합성한다.[18][107][71]무게에 의한 이 비교적 많은 양은 흡수 역학에 근거하여 유사한 양의 프로게스테론을 전달하기 위해 약 50%의 신체를 흡수 표면으로 사용해야 한다고 주장되어 왔다.[18][107]이와 같이, 경피 경로는 적절한 순환 프로게스테론 레벨을 쉽게 달성할 수 없으며, 이는 경피 프로게스테론이 전신 치료에 비실용적이 되게 한다.[18][107][131][71]임상 연구에서는 경피 프로게스테론의 사용으로 프로게스테론의 순환 수준이 매우 낮다는 것을 발견했으며, 이러한 수치는 에스트로겐에 대한 자궁내막 보호를 제공하기에 불충분하다고 생각된다.[116][117]다양한 경피 프로게스테론의 제형과 용량으로 임상 연구에서 관찰된 프로게스테론의 순환 수준 범위는 0.38~3.5ng/mL이다.[48][116]
비록 매우 낮은 수치의 프로게스테론이 경피 프로게스테론이 있는 정맥혈에서 관찰되었지만, 매우 높고 사실 상당히 많은 프로게스테론의 수치의 프로게스테론은 예상외로 침과 모세혈관혈액에서 발견되었다.[116][117][132]한 연구에서, 침과 모세혈관의 프로게스테론 수치는 정맥혈의 수치보다 각각 10배와 100배 높았다.[116][117][132]관찰된 침엽 프로게스테론의 수준은 2.9 - 2,840 ng/mL이다.[48]프로게스테론의 높은 침샘 및 모세혈관 혈액 수치는 프로게스테론의 낮은 순환 수준에도 불구하고 프로게스테론의 전신 분포와 호르몬에 대한 일부 조직의 상당한 노출이 어떻게든 경피 프로게스테론과 함께 발생할 수 있음을 시사한다.[116][117][132]다만 경피 프로게스테론이 자궁내막에 미치는 영향을 평가한 몇 안 되는 임상연구는 엇갈린 결과가 나왔으며, 갱년기 호르몬 치료의 성분으로 적절한 자궁내막 보호를 부여할 수 있을지를 결정하기 위해서는 추가 연구가 필요하다.[116][117]
경피 프로게스테론은 보통 크림과 수성 젤 형태로 공급되는데, 경피 프로게스테론과 함께 매우 낮은 수준의 프로게스테론이 유통되는 것을 관찰한 연구는 이러한 제형을 사용했다.[116][117]알콜 기반 젤 형태의 100 mg/day 경피 프로게스테론에 대한 한 연구에서는 루탈 위상 수준에 해당하는 비교적 고농도의 프로게스테론이 유통되고 있는 것을 발견했다.[116][117]프로게스테론의 최고 수위는 8ng/mL로 이론적으로 자궁내막 보호를 제공하기에 충분했다.[116][117]이러한 연구 결과는 비록 단일 연구에 기초하지만 알코올에 기초한 프로게스테론겔이 비교적 높은 수준의 순환 프로게스테론을 산출할 수 있음을 시사한다.[116][117]그 차이에 대한 한 가지 가능한 설명은 프로게스테론 크림은 지방질이 풍부하고 피부 아래 지방층에 흡수되는 것을 선호할 수 있다는 것이다.[117]반대로 알코올을 함유한 젤은 수용성이 높으며 피부의 미세순환에 빠르게 분포한 다음 일반 순환에 분포할 수 있다.[117]그러나 친수성, 지방성 또는 에멀전성 염기 중 하나를 사용하여 경피 프로게스테론의 약동학을 조사한 또 다른 연구에서는 세 가지 사례 모두에서 농도가 최고조에 이르는 시간이 약 4시간이며 관찰된 정맥혈 수치가 매우 낮다는 것이 밝혀졌다.[11]
침과 모세혈관의 높은 수치
일부 연구자들은 경피 프로게스테론과 정맥혈에서 관찰된 매우 낮은 수준의 프로게스테론을 근거로 경피 프로게스테론은 잘 흡수되지 않으며 적절한 자궁내막 보호를 허용하지 않을 것이라고 결론지었다.[132][117]그러나, 순환하는 프로게스테론의 매우 낮은 수준에도 불구하고, 타액 및/또는 모세혈관의 프로게스테론의 수치를 경피 프로게스테론과 함께 측정했던 연구는 그것들이 극적으로 상승하고 있으며, 사실 매우 초자연적이라는 것을 발견했다.[116][117][132]유화 크림이나 수성 젤을 사용한 한 연구에서 프로게스테론의 침엽수 및 손끝 모세혈관은 각각 정맥혈수치보다 약 10배, 100배 높은 것으로 나타났다.[116][132]The exact levels of progesterone were 4 to 12 ng/mL in saliva and 62 to 96 ng/mL in capillary blood; the reference ranges of progesterone in saliva and capillary blood from a cited laboratory were 0.75 to 2.5 ng/mL and 3.3 to 22.5 ng/mL for premenopausal women in the luteal phase and 0.12 to 1.0 ng/mL and 0.1 to 0.8 ng/mL in postmenopausal women,각각[116][132]이와 같이, 이러한 데이터는 순환하는 프로게스테론의 수치가 매우 낮음에도 불구하고 트랜스피어 프로게스테론이 있는 적어도 특정 조직에 프로게스테론의 분포를 확인하며, 정맥혈의 프로게스테론 수치가 반드시 프로게스테론의 조직 노출 지수로 사용될 수 없음을 나타낸다.[116][117]이러한 발견들은 어떻게 일부 연구들이 경피 프로게스테론(transdermal progesterone)을 가진 자궁내막에서 항정신병적 및 위축성 변화를 발견했는지에 대한 가능한 설명을 제공한다.[132][117]그러나 경피 프로게스테론이 있는 자궁내막 내 프로게스테론의 상승 수준은 아직 입증되지 않았다.[117]
이러한 조직 내 프로게스테론의 초자연적 수준의 영향이 알려져 있지 않아 부작용 가능성을 배제하지 않고 있다는 점에서 경피 프로게스테론에 대한 우려가 제기되었다.[116]경피 프로게스테론을 사용하는 여성의 프로게스테론 수치에 대한 침습적인 모니터링과 필요에 따라 복용량을 조절하는 것이 잠재적 부작용을 예방하는 데 도움이 되는 가능한 수단으로 제안되었다.[116]
낮은 순환수치에도 불구하고 크림과 수성 젤에 들어있는 트랜스더피 프로게스테론이 매우 높은 침엽수 및 모세혈관 혈액을 생성하는 메커니즘은 잘 이해되지 않는다.[116]그러나 적어도 두 가지 가설이 제시되었다.[117][133]프로게스테론을 포함한 스테로이드 호르몬은 알부민, 성호르몬 결합 글로불린, 코르티코스테로이드 결합 글로불린 등의 혈청 운반 단백질 외에 적혈구에 의해 운반되는 것으로 밝혀졌으며, 전혈에 있는 전체 스테로이드 호르몬 함량의 15-35% 정도가 적혈구에 국한될 수 있다.[117]그 가설에 따르면, 매우 높은 국소농도의 프로게스테론은 경피적용 후 피부 모세혈관에서 발생하며 적혈구에 의해 흡수된다.[117]모세혈관에서 나오는 적혈구의 전달시간과 적혈구에서 나오는 스테로이드 호르몬의 방출은 둘 다 매우 빠르므로 프로게스테론은 전신혈액과 평형을 이룰 시간 없이 적혈구를 통해 조직에 전달되는 것이 제안된다.[117]이것은 모세혈관과 침의 수치가 매우 높음에도 불구하고 잠재적으로 정맥혈의 프로게스테론의 낮은 수치를 설명할 수 있다.[117]그러나 한 연구에서는 적혈구의 프로게스테론 수치를 경피 프로게스테론(transdermal progesterone)으로 평가한 결과 크게 증가했지만 여전히 매우 낮은 것으로 나타났다.[117]그럼에도 불구하고, 다른 저자들에 따르면, "그 연구의 연구자들은 적혈구의 프로게스테론 수치가 너무 낮아서 조직을 대상으로 프로게스테론을 전달하는데 있어서 중요하지 않다고 결론내렸지만, 적혈구가 차지하는 프로게스테론의 양이 적혈구가 차지하는 양이 적혈구가 차지하는 양이 적혈구가 차지하는 양이 매우 중요할 수 있다는 것을 깨달아야 한다.모세혈관에서 나오는 적혈구의 시간은 매우 빠르다. [...] 그러나 스테로이드 호르몬 수송에서 적혈구의 역할은 철저히 연구되지 않았고, 그런 연구가 정당하다고 말했다.[117]
포르신 피부와 여러 가지 형태의 경피 프로게스테론을 이용한 시험관내 연구에서 미세한 양의 프로게스테론만이 피부를 통해 침투하지만, 피부 조직에는 프로게스테론이 상당 부분 분할되어 있다는 것을 발견했다.[133]연구진에 따르면, 그 결과는 피부의 림프 순환이 경피 프로게스테론의 전신 분포를 설명할 수 있다는 것을 시사했다.[133]
신진대사 및 제거
5α-감소효소는 프로게스테론의 신진대사에 관여하는 주요 효소로 피부에 고량으로 발현되는 것으로 알려져 있다.[134][117]이 때문에 프로게스테론의 빠른 신진대사가 5α-감소효소 작용에 의해 생성되는 순환 프로게스테론의 낮은 수준을 설명할 수 있다는 의견이 제시되었다.[117]프로게스테론에 대한 연구는 프로게스테론을 트랜스데르몰리 투여할 때 80%가 피부에서 대사되고 20%만이 피부 장벽을 통과할 가능성이 있다고 보고했다.[135][136]이 선들을 따라, 방사성동위원소 프로게스테론의 연구 결과, 5β 감소된 임신이벤디올 배설은 정맥내 프로게스테론보다 8배 높았지만, 모든 임신이벤디올 배설은 경피 프로게스테론보다 약간 높았다.[137]피부에 있는 프로게스테론의 대사물은 호르몬 활동이 없는 것처럼 보인다.[135]5α-감소효소 외에도 20α-히드록시스테로이드 탈수소효소와 같은 다른 효소는 피부의 프로게스테론을 대사한다.[134]프로게스테론 및/또는 5α-디히드로게스테론과 같은 대사물은 피부에서 3α와 3β-히드록시스테로이드 탈수소화물의 5α-감소효소 억제제 및 억제제로 작용한다.[134]
반면에, 다른 연구들은 프로게스테론이 피부에서 강하게 대사된다는 개념에 의문을 제기한다.[117]한 연구는 알코올을 함유한 젤에 함유된 경피 프로게스테론이 높은 수준의 순환 프로게스테론을 생성했다고 보고했다.[117]이는 신진대사가 아닌 제형이 경피 프로게스테론의 생체이용에 중요한 제한 요인이 될 수 있음을 시사한다.[117]소변에서 프로게스테론의 주요 대사물인 임태니돌 글루쿠로니드의 비뇨기 수치를 평가한 연구결과에 따르면 경피 프로게스테론 치료 후 순환 프로게스테론 수치와 임태니돌 글루쿠로니드의 비뇨기 수치가 증가했지만 그럼에도 불구하고 두 가지 수치는 모낭상 및 모낭상 범위에 머물러 있었다.그래서 매우 낮았다.[117]사례보고서에 따르면 5α-감소효소 억제제 피나스테라이드는 트랜스말 프로게스테론에서 생성되는 순환 프로게스테론 수치나 비뇨기 임신에디올 글루쿠로니드 수치를 증가시키지 않았다.[117]마찬가지로 5α-감소효소 억제제 듀타스테라이드도 경피 프로게스테론 함유량이 약간 높을 뿐이라는 연구 결과가 나왔다.[138][139][140][48]마지막으로 5α-감소효소 역시 테스토스테론의 신진대사에 관여하는 주요 효소지만, 경피 테스토스테론은 안드로겐 대체요법으로 승인되어 테스토스테론 수치를 높이는 데 매우 효과적이다.[141]
제거의 관점에서, 친수성, 지방성 또는 에멀전성 기지를 이용한 경피 프로게스테론의 약동학을 조사한 연구에서 세 가지 경우 모두 제거 반감기의 범위가 30~40시간인 것으로 나타났다.[11]
전신 임상 효과
적어도 7개의 연구가 경피 프로게스테론을 평가했다.[116][117]이 연구에서, 작용의 프로게스테론의 크림과 수성 젤(브랜드 이름 Pro-Gest, Progestelle, Pro-Femme뿐만 아니라 악화되)을 포함한 다른 형태, 다른 표본 크기, 다른 마시면(하루에 15~80mg)에(nx6nx40), 그리고 치료(1.4에서 24주)의 다른 항공기에 사용되었다.[116][117]5개 연구에서 정맥혈 프로게스테론 수치를 평가하고 보고했으며, 모든 경우 낮은 수치였고 3.5 ng/mL를 초과하지 않는 것으로 밝혀졌다.[116][117]비록 일부 연구자들이 이러한 주장에 대해 이의를 제기하였지만,[116] 자궁내막의 유사분열을 억제하고 분비물 변화를 유도하기 위해서는 5 ng/mL의 프로게스테론 수치가 필요하다는 것이 일반적으로 받아들여지고 있다.[117]세 가지 연구에서 경피 프로게스테론의 자궁내막에 미치는 영향을 자궁내막 조직검사를 통해 평가하고 그 결과를 혼합했다.[116][117]한 연구에서는 효과가 없었고, 다른 연구에서는 항정신병 효과가 관찰되었으며, 마지막 연구에서는 위축 상태가 관찰되었지만 여성의 40명 중 28명(70%)에서만 관찰되었다.[116][117]순환 프로게스테론 수치는 첫 번째 연구에서는 3.5 ng/mL 미만으로 보고되었고, 두 번째 연구에서는 낮고 광범위하게 변동했으며, 세 번째 연구에서는 제시되지 않았다.[116][117]더욱이 아무런 효과도 관찰되지 않은 연구 기간은 2주에 불과해 짧았고, 자궁내막 변화를 일으키기 위해서는 4주에서 6주의 긴 치료 기간이 필요하다.[116][117]또한 프로게스테론이 작용하기 위한 자궁내막의 적절한 프라이밍을 허용하기에는 에스트로겐의 복용량이 충분하지 않았을 수 있다는 제안도 제기되었다.[117]종합하면, 자궁내막에 대한 경피 프로게스테론의 보호 효과를 적절히 확립하기 위한 추가 연구가 필요하다.[116]
유방에 국소 도포
전신 치료를 목적으로 하는 프로게스테론의 경피적 용도는 국소적 치료와 동일시해서는 안 된다.[48]경피 프로게스테론 도포 부위가 흡수에 큰 영향을 미치는 것으로 밝혀졌다.[117]유방에 경피 프로게스테론을 바르면 유방 조직 내 고농축이 관찰됐다.[118]한 연구에서는 폐경 전 여성에서 알코올/수분 기반 젤에 50mg의 트랜스더말 프로게스테론 성분이 유방 내 국소 프로게스테론 수치가 3~5배 증가한 것을 관찰했다.[118][125][142]또 다른 연구에서는, 폐경 전 여성의 유방에 수알콜성 젤을 바르는 것으로 유방의 국소농도가 70배에서 110배 증가된 것을 측정했다.[143][144]프로게스테론이 젖가슴에 국소 연고로 사용되었을 때, 허벅지나 복부와 같은 다른 부위에는 바르지 않았을 때, 프로게스테론의 순환수치가 크게 증가하는 것을 관찰한 연구결과가 있다.[117]그러나 다른 두 연구에서는 프로게스테론이 유방에 경피적으로 도포되면서 프로게스테론의 순환 수치의 뚜렷한 증가를 관찰하지 않았다.[143][125]유방에 도포되었을 때 10%의 경피 생물학적 이용가능성에 기초하여, 50mg의 프로게스테론이 트랜스더몰리적으로 도포되면 5mg에 해당하는 유방에 프로게스테론의 국소농도가 발생할 수 있다.[118][142]
경피 프로게스테론은 갱년기 호르몬 치료나 전신 약물로서 사용이 승인되지 않은 반면, 일부 국가에서는 생리 전 유방 통증을 치료하기 위해 유방에 직접 국부적으로 바르는 1% 젤(10mg/g)로 등록되어 있다.[119][48][127]이 약은 에스트로겐에 의한 유방 상피 세포의 증식을 억제하고 양성 유방 질환 치료에 매우 효과적이며 유방 결절성을 현저하게 감소시키며, 그 질환을 가진 여성의 유방 통증과 부드러움을 거의 완전히 완화시키는 것으로 임상 연구에서 밝혀져 왔다.[48][118][125][127]반대로 경피 프로게스테론은 섬유소성 유방질환, 유방 낭포, 유방 섬유소 등에 거의 완전히 효과가 없는 것으로 나타났으며, 구강 프로게스틴은 상당한 효과가 있는 것으로 밝혀졌다.[118]프로게스테론과 다른 프로게스테르균이 유방 질환 치료에 미치는 효과는 유방의 기능적인 항에스트로겐 효과 때문일 수 있다.[118][125]
질 행정

프로게스테론은 캡슐(우트로게스탄), 겔(크리논, 프로치브), 압구스(사이클로게스트), 삽입/테이블트(엔도메트린, 루티누스), 반지(페르팅, 프로빙) 형태로 질 투여가 가능하다.[146][147][148]게다가, 구강 미크론 프로게스테론 캡슐은 성공적으로 질적으로 투여되었다.[149]
질 미크론화 프로게스테론의 생체이용률은 약 4~8%[2][3][4]이다.프로게스테론의 질 흡수는 질 위축증이 있는 폐경 후 여성에게서 낮다.[145]질 프로게스테론의 생체이용률은 구강 프로게스테론보다 약 40배 높다.[150][1]여성에서 질 프로게스테론 단일 25, 50, 100mg 투여 후 프로게스테론의 최대 순환수치는 2~3시간 이내에 발생했으며 각각 7.27±2.8ng/mL, 8.84±3.14ng/mL, 9.82±9.8ng/mL이었다.[145]최고 레벨 이후 프로게스테론 레벨은 점차 감소했고, 제거 반감기는 6-12시간이었다.[145]프로게스테론 수치는 24시간 후 3회 용량 모두에 대해 3 ng/mL 미만이었다.[145]연구진은 하루 3회 100mg 투여 시 25mg과 50mg 투여량이 2회 투여에 적합한 반면 100mg 투여량은 1일 3회 투여에 적합하다는 결론을 내렸다.[145]
질 프로게스테론과의 자궁 퍼스트패스 효과가 있어 자궁 내 프로게스테론 수치가 순환보다 자궁 내 훨씬 높다.[48]자궁내막의 완전한 분비물 변환은 질 프로게스테론 투여에 의해 생성되어 프로게스테론 수치가 1~3ng/mL로 순환되는 결과를 초래한 반면, 다른 자궁경로(근육내 및 장내)는 그에 비해 효과가 적었다.[145]그 차이는 질 프로게스테론과의 자궁내막 1차 통과 효과에 기인할 수 있다.[145]
직장 행정

프로게스테론은 직장 행정으로 복용할 수 있다.[151][18][22]질 경로 외에 직장에 사용할 수 있도록 사이클로게스트라는 브랜드명으로 판매되는 부설물이 표시된다.[33][152][153]프로게스테론의 일일 직장 투여는 불편하고 장기요법으로도 잘 받아들여지지 않는다.[47][151]그럼에도 불구하고 직장 프로게스테론은 질 감염, 방광염, 최근의 출산 또는 장벽 피임 방법이 사용될 때 질 경로에 유용한 대안이 될 수 있다.[151]
많은 연구들이 직업 경로에 따라 프로게스테론을 평가해 왔다.[154][155][156][157][158][114][159][160]직장 투여 후 프로게스테론 수치는 25mg의 단일 투여 후 6.4ng/mL, 100mg 투여 후 22.5ng/mL, 200mg 투여 후 20.0ng/mL로 나타났다.[151][157]직장 경로의 흡수는 가변적이며, 100 mg 프로게스테론의 단일 직장 선량 후 최대 농도 15~52 ng/mL 프로게스테론의 광범위한 범위가 있다.[18][156]프로게스테론 수치는 6~8시간 후 정점을 찍은 뒤 점차 낮아진다.[18][151]프로게스테론 수치는 여러 연구에서 직장 및 질 부화관을 투여한 후 유사하고 유의미하지 않은 것으로 밝혀졌다.[151]
프로게스테론은 직장의 하부에 흡수되어 하직맥과 중직맥에 의해 운반될 때 순환으로 직접 전달된다.[18]반대로 직장 상부에 흡수될 경우 프로게스테론은 우월한 직장정맥을 통해 간장포털시스템에 진입해 간 1차 통과대사를 받게 된다.[18]이와 같이 직장 행정은 파렌테랄적인 경로임에도 불구하고 여전히 구강 프로게스테론과 유사한 일부 1차 통과 신진대사의 대상이 될 수 있다.[18]
근육 주사
| 화합물 | 형태 | 특정 용도에 대한 선량(mg)[c] | DOA[d] | |||
|---|---|---|---|---|---|---|
| TFD[e] | POICD[f] | CICD[g] | ||||
| 알제스톤 아세토페니드 | 오일 솔렌. | - | – | 75–150 | 14-32 d | |
| 게스토노론 카프로이트 | 오일 솔렌. | 25–50 | – | – | 8-13 d | |
| 히드록시프로제스트.아세테이트의[h] | Aq. 정지. | 350 | – | – | 9-16 d | |
| 히드록시프로제스트. 카프로이트 | 오일 솔렌. | 250–500[i] | – | 250–500 | 5–21 d | |
| 메드록시프로그아세테이트의 | Aq. 정지. | 50–100 | 150 | 25 | 14-50+d | |
| 메게스트롤 아세테이트 | Aq. 정지. | - | – | 25 | >14 d | |
| 노리스테론 에난산염 | 오일 솔렌. | 100–200 | 200 | 50 | 11-52 d | |
| 프로게스테론 | 오일 솔렌. | 200[i] | – | – | 2–6 d | |
| Aq. soln. | ? | – | – | 1-2d | ||
| Aq. 정지. | 50–200 | – | – | 7-14 d | ||
| 참고 및 출처:
| ||||||
오일 용액
근육내 주입에 이용될 때 프로게스테론은 장과 간에서 1차대사를 우회하여 매우 높은 순환 프로게스테론 수치를 얻는다.[17][48]자궁 1차 통과 효과(약 1.5ng/mL, 약 12ng/mL)로 인해 자궁 내 국소 프로게스테론 수치가 질 경로와 함께 10배 높았지만(각각 약 70ng/mL, 약 12ng/mL) 100mg/mg의 프로게스테론 수치가 실질적으로 높았다.…[48]을 속여서프로게스테론의 지속기간은 지방조직에 국소적으로 저장하는 디포 효과로 인해 근육내 경로에 의해 연장되며, 1~3일에 한 번 투여할 수 있다.[18]근육내 프로게스테론의 반감기는 상팔의 델토이드 근육보다는 엉덩이의 활공근에 주사하면 상당히 길다.[18]질내 프로게스테론 또한 사용되고 효과적이긴 하지만, 근육내 프로게스테론은 전통적으로 미국에서 보조 생식 시 루테론 지원에 사용되는 가장 인기 있는 프로게스테론 형태였다.[48][18]
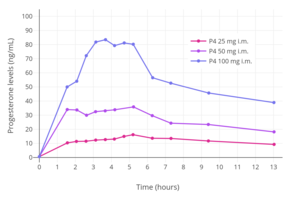
식물성 기름에 프로게스테론 10mg을 분자 내 주입하면 투여 후 약 8시간 후에 최대 혈장 농도(Cmax)에 도달하고 혈청 수치가 약 24시간 동안 기준치 이상으로 유지된다.[42]근육내 주입을 통한 10, 25, 50 mg의 선량은 각각 평균 최대 농도 7, 28, 50 ng/mL인 것으로 밝혀졌다.[42]분자 내 주입으로 25mg을 투여하면 8시간 이내에 프로게스테론의 정상적인 루테랄 위상 혈청 수준이 나타나며, 100mg 투여하면 피크 시 40~80ng/mL의 중간 조도 수준이 발생한다.[22]이러한 선량에서 프로게스테론의 수준은 기준치 이상 48시간 이상(100mg의 경우 현 시점에서 6ng/mL),[22] 제거 반감기는 약 22시간이다.[13]
달성된 고농도 때문에, 통상적인 임상 선량 범위에서 분자 내 주입에 의한 프로게스테론은 뇌하수체에서 고나도트로핀 분비를 억제할 수 있어 항원성 스테로이드 효능(따라서 고나달 성 스테로이드 생성 억제)을 나타낸다.[42]
근육내 프로게스테론은 주사할 때 통증을 유발하는 경우가 많다.[18]조직을 자극하며 피부색, 통증, 홍조, 일시적인 움푹 들어간 곳(염증에 의한), 에크시모시스(브루징/탈색) 등의 주사부위 반응과 관련이 있다.[181][18]드물게 무균 종기가 발생할 수 있다.[18]예를 들어 100mg과 같은 근육내 주입에 의한 많은 양의 프로게스테론은 중간에서 심각까지의 주사 부위 반응과 관련이 있다.[182]
수성 정지
프로게스테론은 유화용액보다 마이크로크리스탈린 수용액 서스펜션(결정크기 0.02~0.1mm) 형태로 투여했을 때 분자주사로 작용하는 작용기간이 상당히 긴 것으로 밝혀졌다.[183][184][185][186][187]오일 용액에서 25~350mg 프로게스테론의 단일 근육내 주입은 여성의 자궁 내 임상 생물학적 효과 측면에서 2~6일의 지속시간을 갖는 반면, 수용성 정지에서 50~300mg 마이크로크리스탈린 프로게스테론의 단일 근육내 주입은 7~14일의 지속시간을 가진다.[167][164][161]그 결과, 오일 용액의 근육 내 프로게스테론은 일반적인 임상 용량에서 1~3일마다 한 번씩 투여되는 반면,[18] 수성 정지의 근육 내 마이크로크리스탈린 프로게스테론은 매주 1회 또는 더 긴 간격으로 투여할 수 있다.[167][161][188]마이크로크리스탈린 수용성 정지의 지속시간은 약물 농도와 결정 크기에 따라 달라진다.[189][190][191][192]스테로이드의 수용성 정지를 위해 더 큰 바늘 크기가 필요하다. 스테로이드의 결정체가 바늘 루멘을 통과할 수 있도록.[193]20 또는 21 게이지 바늘이 마이크로크리스탈린 프로게스테론의 수성 정지를 주입하는 데 적합한 것으로 보고되었다.[194]
1950년대 플라보우탄, 루토산, 루토시클린M, 루트렌 등 다양한 브랜드 이름으로 분자주사를 통한 장기적 디포 사용을 위한 수성정지의 마이크로크리스탈린 프로게스테론 제형이 출시되었다.[195]또 다른 준비물은 아골루틴 디포인데, 1960년에 도입되어 오늘날 체코와 슬로바키아에서 시판되고 있는 것으로 보인다.[196][197][198][186][199]시스토시클린은 1950년대에 시판된 수성 정지에 10mg의 마이크로크리스탈린 에스트라디올 벤조이트와 200mg의 마이크로크리스탈린 프로게스테론이 함유된 제품의 브랜드 이름이었다.[200][201][202][203]이 의약품은 원액 내 에스트라디올 벤조이트와 프로게스테론의 경우 단 2일의 기간과 비교하여 프로게스테론 성분의 측면에서 10일에서 12일의 작용 기간을 갖는 것으로 보고되었다.[204][205]불행히도, 프로게스테론과 다른 스테로이드의 수성 정지를 근육내 주입하는 것은 고통스럽고, 종종 그렇게 심하게 한다.[206][207][208]그 결과, 그들은 석유 용액에서의 프로게스테론이나 더 오래 작용하는 프로게스틴과 같은 다른 준비물에 호의적으로 대부분 중단되었다.[206][169][208]
근육내 주입에 의한 수성 정체에서의 프로게스테론은 근육내 주입에 의한 오일 용액에서 프로게스테론보다 프로게스테론 발생 효과 면에서 더 강력한 것으로 보인다.[209]여성에게서 해독을 유도하기 위해 미세결정체로서 프로게스테론 25mg이 필요한 반면, 오일 속 프로게스테론에는 35~50mg의 선량이 필요했다.[209]이는 오일 용액에 비해 수성 정지를 통해 프로게스테론 수치가 안정적이고 오래 지속되기 때문으로 분석됐다.[209]
Medroxyprogesterone acetate (brand names Depo-Provera, Depo-SubQ Provera 104), a progestin and structural modification of progesterone with a methyl group at the C6α position and an acetoxy group at the C17α position, is formulated as a microcrystalline aqueous suspension for use by intramuscular or subcutaneous injection.[210][211]프로게스테론과 마찬가지로 메드록시프로게스테론 아세테이트의 형성은 그 지속시간을 극적으로 연장시킨다.[210][173]50mg의 용량으로 16~50일의 지속시간을 가지며,[167] 150mg의 지속시간은 최소 3개월, 길게는 6~9개월이다.[210][173]
유화
스테로이드의 수분 주입 유화 작용은 1940년대 후반과 1950년대에 연구되었다.[191][212][213][214][215][216][217][218]프로게스테론의 장시간 작용 유화 작용은 1950년대까지 프로게스틴이라는 브랜드명으로 분자주사를 단독으로 사용하고 디프로-에멀전이라는 브랜드명으로 에스트라디올 벤조이트와 함께 사용하기 위해 도입되었다.[195][219][220][221][222]근육내 주입에 의한 스테로이드 유무는 수성정지와 지속시간 등 유사한 성질을 갖는 것으로 보고되고 있다.[191][212][213]
마이크로스피어
마이크로스페어에 캡슐화된 프로게스테론의 수성 정지는 멕시코의 ProSphere라는 브랜드명으로 근육내 주입에 사용되도록 시판되고 있다.[181][223][224]표시에 따라 매주 1회 또는 매월 1회 관리한다.[181]예를 들어, 위협적인 유산 치료를 위해 7일에 한 번씩 근육내 주입으로 100~300mg의 용량으로 약을 투여한다.[36]마이크로스피어의 크기는 33~75μg이며 20 게이지 38mm 바늘로 미리 채워진 주사기를 이용해 전달된다.[181]ProSphere의 100 또는 200mg 근육내 주입 후 프로게스테론의 최고 수위는 약 1.5일 후에 발생한다.[36]이 제형으로 프로게스테론의 반감기는 약 8일이다.[36]200mg의 근육내 주입 한 번으로 프로게스테론 수치가 5~7일 동안 10ng/mL 이상 유지된다.[36]ProSphere는 주입 사이트 반응 측면에서 잘 용인된다.[181]
근육내 주입에 사용할 수 있는 수성정지로 마이크로스피어 내에 캡슐화된 에스트라디올과 프로게스테론의 조합이 멕시코의 후베넘이라는 브랜드명으로 시판되었다.[225][226][227]이 공식에 대한 연구들이 발표되었다.[228][229]
마이크로스피어에 캡슐화된 에스트라디올과 프로게스테론은 월 1회 복합주사 피임약으로 사용하기 위해 연구되어 왔으나 의학용으로 추가 개발되거나 도입되지는 않았다.[230][231][232][233][234][235]
갤러리
피하 주사

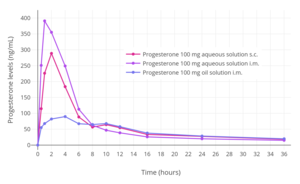
프로게스테론은 피하주사로 투여할 수 있으며, 유럽에서 시판되고 있는 프로게스테론의 수용액인 프롤루텍스는 이 경로로 하루 한 번 투여할 수 있다.[13][236][237]이 제형은 빠르게 흡수되며, 근육내 주입에 의해 오일 용액의 프로게스테론에 비해 프로게스테론의 피크 레벨이 높은 것으로 밝혀졌다.[237]또 프로게스테론의 피하주사는 프로게스테론의 근육내 주입에 비해 주사부위 반응 위험이 적어 쉽고 안전하며 통증이 적은 것으로 평가된다.[237]이 제형의 제거 반감기는 13~18시간이며,[13] 오일 용액에서 프로게스테론의 분자내 주입에 20~28시간이다.[12][10][13]
피하 이식

프로게스테론은 1950년대와 1960년대에 플라보우탄, 루테오시드, 루토시드, 프롤루톤이라는 상표명으로 50, 100mg의 피하 펠릿 임플란트 형태로 시판된 바 있다.[195][239]그러나 오늘날 의약품으로 남아 있는 에스트라디올과 테스토스테론 임플란트와는 대조적으로 프로게스테론 임플란트 제품은 단종되어 더 이상 의약품으로 사용할 수 없는 것으로 보인다.[240][94]그러나 프로게스테론 임플란트는 일부 복합 약국에서 구입할 수 있다. 단, 이러한 제품은 품질이나 효과에 대한 규제를 받지 않는다.[241][242][243]
인간에게 프로게스테론 임플란트에 대한 초기 연구는 1930년대부터 1950년대에 실시되었다.[244][245][246][247][248][249][250][251]프로게스테론의 피하 삽입물은 무균 종기, 압출 등이 임플란트의 15~20%에서 발생하는 등 잘 견디지 못하는 것으로 나타났다.[252]그러나 제조 공정마다 압출 속도가 다르다는 연구 결과가 나왔다.[238]프로게스테론 임플란트도 1980년대 여성에게서 호르몬 분만 조절의 한 형태로 연구되었지만, 결국 시장화되지는 않았다.[253][254][255][256]프로게스테론 100mg을 각각 함유한 6개의 펠릿(총 600mg)을 이식한 결과, 프로게스테론 수치가 약 3ng/mL로 비교적 낮은 것으로 나타났으며, 프로게스테론 수치는 약 5개월 동안 지속되었다.[254][255][256][238]프로게스테론의 피하 삽입은 동물들에서도 연구되어 왔다.[257]피하 펠릿 임플란트는 약물이 매우 낮은 용량에서 활성 상태일 때 가장 실용적이다.[190]
프로게스테론 임플란트는 의약품 조제물로 사용할 수 없지만, etonogestrel(임플란온/넥스플라논), 레보노게스트렐(자델/노르플랜트) 등 프로게스틴의 피하 임플란트는 의약품으로 구입할 수 있다.[258][259]그것들은 호르몬 분비를 오래 지속시키는 형태로 사용된다.[258][259]
자궁내 투여
호르몬 분비를 위한 1년 프로게스테론 자궁내 장치(IUD)는 이전에 미국과 몇몇 다른 국가에서 Progestasert라는 브랜드로 사용 가능했다.[260][261]그것은 1976년과 2001년 사이에 판매되었다.[260]IUD는 2.9%의 비교적 높은 피임 실패율과 연간 교체 요건으로 인해 결코 널리 사용되지 않았다.[260]프로게스테론 38mg을 함유하고 하루 65μg의 프로게스테론(총 35mg까지 1년 후)을 자궁에 방출했다.[260][261]비교를 위해, 여성의 몸은 루테랄 단계에서 하루 평균 약 25mg의 프로게스테론을 생산한다.[18][107]피임의 한 형태로서 효과가 있고 생리 출혈과 불편함을 줄이는데 효과가 있지만, 장수 IUD는 기본적으로 하루에 적은 양의 프로게스테론만 전달할 수 있으며, 따라서 자궁 내 프로게스테론 수치는 적절한 순환 프로게스테론 수준을 달성할 수 없으며 전신 치료의 한 형태로 적합하지 않다.[107]프로게스테론 외에도 레보노게스트렐(Mirena/Levosert/Skyla)과 같은 프로게스틴의 IUD도 이용할 수 있다.[262]
정맥주사
프로게스테론은 정맥주사를 맞았을 때 약 3분에서 90분 정도의 매우 짧은 제거 반감기를 가지고 있다.[14]
정맥주사에 사용할 프로게스테론의 수용액은 한때 스크링 AG에 의해 프리몰루트 정맥주사로 판매되었다.[38][39]
일반
흡수
분배
프로게스테론은 혈액-뇌 장벽을 통과한다.[263]혈장 단백질 결합의 관점에서 프로게스테론은 순환 중에 98~99%의 단백질 결합이다.[5][6]알부민에 80%, 코르티코스테로이드 바인딩 글로불린에 18%, 성호르몬 바인딩 글로불린에 1% 미만으로 결합되며, 나머지 1~2%의 분율은 자유 또는 결합되지 않고 순환한다.[5][6]
신진대사
구강 투여로 프로게스테론은 위장관과 간에서 빠르게 대사된다.[119]프로게스테론에서 경구 섭취를 통해 형성되는 대사물은 무려 30여개에 이르는 것으로 조사됐다.[119]투여경로와 관계없이 5α-감소효소는 프로게스테론의 신진대사에 관여하는 주요 효소로 그 신진대사의 약 60~65%를 담당한다.[69]5β-감소효소 또한 프로게스테론의 신진대사에 중요한 효소다.[69]5α-프로게스테론의 감소는 주로 장(특히 십이지장)에서 발생하는 반면, 5β 감소는 거의 간에서만 발생한다.[69]프로게스테론의 대사물은 각각 5α-저감산화효소와 5β-저감산화효소(3α-히드록시스테로이드 탈수소효소에 의한 추가변형 후)에 의해 생성된다.[119]프로게스테론의 경구 투여를 통해, 그것들은 매우 높은 순환에서 발생하며, 실제로 프로게스테론 자체의 농도를 훨씬 초과하는 수프라피질생리학적 농도로서 발생한다(프로게스테론 단 200mg 경구 투여 후 4시간 후 프로게스테론의 경우 최고농도 30ng/mL, 임페놀론의 경우 60ng/mL의 농도).게스테론[119]한 연구에서 프로게스테론의 200mg 경구 투여 한 번으로 2시간 후 약 1ng/mL의 피크 레벨이 20α-디드롭로게스테론의 피크 레벨이 나왔다.[264]
프로게스테론과 그 대사물의 구성 비율은 단일 100 mg 경구 또는 질 프로게스테론 용량에 대해 결정되었다.[71]경구 투여로 프로게스테론은 순환 선량의 20% 미만을 차지하며, allope definalanoone, imalanolone과 같이 5α와 5β 감소 제품이 약 80%[71]를 차지한다.질 투여 시 프로게스테론은 선량의 약 50%를 차지하고 5α 및 5β 감소 대사물은 [71]약 40%를 차지한다.
소량의 프로게스테론은 21-히드록실라아제에 의해 11-데옥시코르티코스테론으로 변환된다.[265][69]프로게스테론이 질이나 근육내 주입과 같은 종양 루트를 통해 전달되는 것과는 반대로 구강으로 투여될 때 11-데옥시코르티코스테론 수치의 증가가 현저하게 더 높다.[69]프로게스테론의 11데옥시코르티코스테론으로의 변환은 장(특히 십이지장)과 신장에서 발생한다 [265][69]21-히드로록시라제가 간에서 없는 것으로 나타나므로 프로게스테론의 11데옥시코르티코스테론으로의 변환은 신체의 이 부분에서는 일어나지 않는 것으로 생각된다.[69]
내생성 프로게스테론은 코퍼스 루테룸의 5α-디하이드롭로게스테론에 약 50%, 간에서 3β-디하이드롭로게스테론에 35%, 20α-디하이드롭로게스테론에 10%가 대사된다.[61]
하나 이상의 사용 가능한 히드록실 그룹을 가진 프로게스테론의 대사물은 글루쿠로니드화 및/또는 황화를 통해 결합되어 배설된다.[266][33]
순환하는 프로게스테론의 생물학적 반감기는 매우 짧다. 정맥주사를 맞았을 때, 그 반감기는 다양한 연구에서 3분에서 90분까지 광범위하게 분포되어 있다.[14]프로게스테론의 대사간극률은 하루 2,100~2,800 L/일이며, 월경 주기에 걸쳐 일정하다.[14][208]
제거
프로게스테론은 담즙과 소변에서 제거된다.[15][16]
참고 항목
참조
- ^ a b c d e f g h i Levine H, Watson N (March 2000). "Comparison of the pharmacokinetics of Crinone 8% administered vaginally versus Prometrium administered orally in postmenopausal women(3)". Fertil. Steril. 73 (3): 516–21. doi:10.1016/S0015-0282(99)00553-1. PMID 10689005.
- ^ a b Griesinger G, Tournaye H, Macklon N, Petraglia F, Arck P, Blockeel C, van Amsterdam P, Pexman-Fieth C, Fauser BC (February 2019). "Dydrogesterone: pharmacological profile and mechanism of action as luteal phase support in assisted reproduction". Reprod. Biomed. Online. 38 (2): 249–259. doi:10.1016/j.rbmo.2018.11.017. PMID 30595525.
- ^ a b Pandya MR, Gopeenathan P, Gopinath PM, Das SK, Sauhta M, Shinde V (2016). "Evaluating the clinical efficacy and safety of progestogens in the management of threatened and recurrent miscarriage in early pregnancy-A review of the literature". Indian Journal of Obstetrics and Gynecology Research. 3 (2): 157. doi:10.5958/2394-2754.2016.00043.6. ISSN 2394-2746.
- ^ a b c Paulson RJ, Collins MG, Yankov VI (November 2014). "Progesterone pharmacokinetics and pharmacodynamics with 3 dosages and 2 regimens of an effervescent micronized progesterone vaginal insert". J. Clin. Endocrinol. Metab. 99 (11): 4241–9. doi:10.1210/jc.2013-3937. PMID 24606090.
- ^ a b c Fritz MA, Speroff L (28 March 2012). Clinical Gynecologic Endocrinology and Infertility. Lippincott Williams & Wilkins. pp. 44–. ISBN 978-1-4511-4847-3.
- ^ a b c Marshall WJ, Bangert SK (2008). Clinical Chemistry. Elsevier Health Sciences. pp. 192–. ISBN 978-0-7234-3455-9.
- ^ a b c Pickar JH, Bon C, Amadio JM, Mirkin S, Bernick B (December 2015). "Pharmacokinetics of the first combination 17β-estradiol/progesterone capsule in clinical development for menopausal hormone therapy". Menopause. 22 (12): 1308–16. doi:10.1097/GME.0000000000000467. PMC 4666011. PMID 25944519.
- ^ a b c d https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/210132s000lbl.pdf
- ^ a b c d e Хомяк, Н. В., Мамчур, В. И., & Хомяк, Е. В. (2014).Клинико-фармакологические особенности современных лекарственных форм микронизированного прогестерона, применяющихся во время беременности.здоо, (4), 90. https://web.archive.org/web/20180808140010/http://health-ua.com/wp-content/uploads/2015/09/MAZG2-2015_28-35.pdf
- ^ a b c http://www.accessdata.fda.gov/drugsatfda_docs/label/2013/020701s026lbl.pdf
- ^ a b c Mircioiu C, Perju A, Griu E, Calin G, Neagu A, Enachescu D, Miron DS (1998). "Pharmacokinetics of progesterone in postmenopausal women: 2. Pharmacokinetics following percutaneous administration". European Journal of Drug Metabolism and Pharmacokinetics. 23 (3): 397–402. doi:10.1007/bf03192300. PMID 9842983. S2CID 32772029.
- ^ a b c d e f g h i j Simon JA, Robinson DE, Andrews MC, Hildebrand JR, Rocci ML, Blake RE, Hodgen GD (July 1993). "The absorption of oral micronized progesterone: the effect of food, dose proportionality, and comparison with intramuscular progesterone". Fertility and Sterility. 60 (1): 26–33. doi:10.1016/S0015-0282(16)56031-2. PMID 8513955.
- ^ a b c d e f g h i j k l m n o p q r Cometti B (November 2015). "Pharmaceutical and clinical development of a novel progesterone formulation". Acta Obstetricia et Gynecologica Scandinavica. 94 (Suppl 161): 28–37. doi:10.1111/aogs.12765. PMID 26342177.
- ^ a b c d e f Aufrère MB, Benson H (June 1976). "Progesterone: an overview and recent advances". Journal of Pharmaceutical Sciences. 65 (6): 783–800. doi:10.1002/jps.2600650602. PMID 945344.
- ^ a b http://www.accessdata.fda.gov/drugsatfda_docs/label/1998/20843lbl.pdf
- ^ a b http://www.accessdata.fda.gov/drugsatfda_docs/label/2007/017362s104lbl.pdf
- ^ a b c d e f g h i j k l m n o p q r s t u v Kuhl H (August 2005). "Pharmacology of estrogens and progestogens: influence of different routes of administration" (PDF). Climacteric. 8 Suppl 1: 3–63. doi:10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ a b c d e f g h i j k l m n o p q r s Unfer V, di Renzo GC, Gerli S, Casini ML (2006). "The Use of Progesterone in Clinical Practice: Evaluation of its Efficacy in Diverse Indications Using Different Routes of Administration". Current Drug Therapy. 1 (2): 211–219. doi:10.2174/157488506776930923.
- ^ Whitaker A, Gilliam M (2014). Contraception for Adolescent and Young Adult Women. Springer. p. 98. ISBN 9781461465799.
- ^ Chaudhuri SK (2007). Practice Of Fertility Control: A Comprehensive Manual (7th ed.). Elsevier India. p. 153. ISBN 978-81-312-1150-2.
- ^ a b Josimovich J (11 November 2013). Gynecologic Endocrinology. Springer Science & Business Media. pp. 9, 25–29, 139. ISBN 978-1-4613-2157-6.
- ^ a b c d Sampson GA (1981). "An appraisal of the role of progesterone in the therapy of premenstrual syndrome". In van Keep PA, Utian WH (eds.). The Premenstrual Syndrome: Proceedings of a workshop held during the Sixth International Congress of Psychosomatic Obstetrics and Gynecology, Berlin, September 1980. pp. 51–69. doi:10.1007/978-94-011-6255-5_4. ISBN 978-94-011-6257-9.
- ^ Strauss JF, Barbieri RL (2009). Yen and Jaffe's Reproductive Endocrinology: Physiology, Pathophysiology, and Clinical Management. Elsevier Health Sciences. pp. 807–. ISBN 978-1-4160-4907-4.
- ^ Blackburn S (14 April 2014). Maternal, Fetal, & Neonatal Physiology. Elsevier Health Sciences. pp. 92–. ISBN 978-0-323-29296-2.
- ^ Stricker R, Eberhart R, Chevailler MC, Quinn FA, Bischof P, Stricker R (2006). "Establishment of detailed reference values for luteinizing hormone, follicle stimulating hormone, estradiol, and progesterone during different phases of the menstrual cycle on the Abbott ARCHITECT analyzer". Clin. Chem. Lab. Med. 44 (7): 883–7. doi:10.1515/CCLM.2006.160. PMID 16776638. S2CID 524952.
- ^ Sizonenko, Pierre C. (July 1978). "Endocrinology in Preadolescents and Adolescents". American Journal of Diseases of Children. 132 (7): 704–12. doi:10.1001/archpedi.1978.02120320064015. ISSN 0002-922X. PMID 149498.
- ^ Sizonenko, P. C. (1984). "Endocrine Aspects of Normal Pubertal Development". Paediatric Endocrinology in Clinical Practice. pp. 175–182. doi:10.1007/978-94-009-5610-0_11. ISBN 978-94-010-8974-6.
- ^ Gerhard, I.; Heinrich, U. (1994). "Die Pubertät und ihre Störungen" [Puberty and its Disorders]. Gynäkologische Endokrinologie und Fortpflanzungsmedizin [Gynecological Endocrinology and Reproductive Medicine]. pp. 263–303. doi:10.1007/978-3-662-07635-4_6. ISBN 978-3-662-07636-1.
- ^ Tulchinsky D, Hobel CJ, Yeager E, Marshall JR (April 1972). "Plasma estrone, estradiol, estriol, progesterone, and 17-hydroxyprogesterone in human pregnancy. I. Normal pregnancy". Am. J. Obstet. Gynecol. 112 (8): 1095–100. doi:10.1016/0002-9378(72)90185-8. PMID 5025870.
- ^ "Drugs@FDA: FDA Approved Drug Products". United States Food and Drug Administration. Retrieved 26 July 2018.
- ^ Engel J, Kleemann A, Kutscher B, Reichert D (14 May 2014). Pharmaceutical Substances, 5th Edition, 2009: Syntheses, Patents and Applications of the most relevant APIs. Thieme. pp. 1145–. ISBN 978-3-13-179275-4.
- ^ Becker KL (2001). Principles and Practice of Endocrinology and Metabolism. Lippincott Williams & Wilkins. pp. 2168–. ISBN 978-0-7817-1750-2.
- ^ a b c d e Anita MV, Jain S, Goel N (31 July 2018). Use of Progestogens in Clinical Practice of Obstetrics and Gynecology. JP Medical Ltd. pp. 4–. ISBN 978-93-5270-218-3.
- ^ Sauer MV (1 March 2013). Principles of Oocyte and Embryo Donation. Springer Science & Business Media. pp. 7, 117–118. ISBN 978-1-4471-2392-7.
- ^ Elder K, Dale B (2 December 2010). In-Vitro Fertilization. Cambridge University Press. pp. 26–. ISBN 978-1-139-49285-0.
- ^ a b c d e https://web.archive.org/web/20191230051017/https:///mx.prvademecum.com/medicamento/prosphere-11003/
- ^ Heinrich Kahr (8 March 2013). Konservative Therapie der Frauenkrankheiten: Anzeigen, Grenzen und Methoden Einschliesslich der Rezeptur. Springer-Verlag. pp. 21–. ISBN 978-3-7091-5694-0.
- ^ a b Basic Sex Hormone Therapy. Schering A.G. 1962. p. 96.
- ^ a b Current Medicine and Drugs. 1962. p. 40.
Primolut Intravenous (Schering A.G. Berlin)
- ^ Haleem S, Khan MI (March 2015). "Changing Indian Market Trends of NMP: A Review" (PDF). International Journal of Pharma Research & Review. 4 (3): 28–30. ISSN 2278-6074.
- ^ a b c d e f Zutshi V, Rathore AM, Sharma K (2005). Hormones in Obstetrics and Gynaecology. Jaypee Brothers, Medical Publishers. pp. 74–75. ISBN 978-81-8061-427-9. Archived from the original on 2020-05-01. Retrieved 2018-12-20.
It has been observed that micronized progesterone has no suppressive effects on high-density lipoprotein-cholesterol (HDL-C). Jensen et al have proved that oral micronized progesterone has no adverse effect on serum lipids. These preparations have the same antiestrogenic and antimineralocorticoid effect but no androgenic action. It does not affect aldosterone synthesis, blood pressure, carbohydrate metabolism or mood changes. No side effects have been reported as far as lipid profile, coagulation factors and blood pressure are concerned.
- ^ a b c d Progesterone - Drugs.com, retrieved 2015-08-23
- ^ a b c d e f g h i j k l m Kuhl H (2011). "Pharmacology of Progestogens" (PDF). Journal für Reproduktionsmedizin und Endokrinologie-Journal of Reproductive Medicine and Endocrinology. 8 (1): 157–177.
- ^ a b c d e f g h i j k l m n o p q Kuhl H, Schneider HP (August 2013). "Progesterone – promoter or inhibitor of breast cancer". Climacteric. 16 Suppl 1: 54–68. doi:10.3109/13697137.2013.768806. PMID 23336704. S2CID 20808536.
- ^ a b c d e f g h i j k l m n o p q r s t Davey DA (March 2018). "Menopausal hormone therapy: a better and safer future". Climacteric. 21 (5): 454–461. doi:10.1080/13697137.2018.1439915. PMID 29526116. S2CID 3850275.
- ^ a b c d e f g h i j Fotherby K (August 1996). "Bioavailability of orally administered sex steroids used in oral contraception and hormone replacement therapy". Contraception. 54 (2): 59–69. doi:10.1016/0010-7824(96)00136-9. PMID 8842581.
Progesterone is rapidly metabolized which leads to a low bioavailability and the necessity for high doses (200 mg); its pharmacological actions, except upon reproductive processes, are weak. [...] For many years after its isolation and synthesis, progesterone could only be used therapeutically by intramuscular injection of large doses since it was quickly recognized that, after oral administration, progesterone was poorly absorbed and rapidly metabolized in the gastrointestinal tract, liver and most tissues, and then eliminated. However, like estradiol, the absorption of progesterone can be improved by micronization.16 This led to the development of formulations of progesterone, mainly of particle size <10 μg, dissolved in oil in a gelatin capsule. [...] five formulations differing in particle size and vehicle were compared; all led to significant absorption of progesterone and with similar plasma progesterone concentrations 6 hours after administration, but only the micronized or oil vehicle preparations improved absorption (probably by increasing lymphatic absorption and thus avoiding some of the first-pass effect). [...] Plasma progesterone concentrations may be higher when the formulation is administered with food but, even under the best conditions, bioavailability appears to be very low since the AUC after intramuscular injection of progesterone is at least ten times higher than after oral intake.21
- ^ a b c de Lignières B (1999). "Oral micronized progesterone". Clin Ther. 21 (1): 41–60, discussion 1–2. doi:10.1016/S0149-2918(00)88267-3. PMID 10090424.
- ^ a b c d e f g h i j k l m n Ruan X, Mueck AO (November 2014). "Systemic progesterone therapy—oral, vaginal, injections and even transdermal?". Maturitas. 79 (3): 248–55. doi:10.1016/j.maturitas.2014.07.009. PMID 25113944.
- ^ Wecker L (31 May 2018). Brody's Human Pharmacology E-Book. Elsevier Health Sciences. pp. 419–. ISBN 978-0-323-59662-6.
- ^ Anita MV, Jain S, Goel N (31 July 2018). Use of Progestogens in Clinical Practice of Obstetrics and Gynecology. JP Medical Ltd. pp. 4, 15–20. ISBN 978-93-5270-218-3.
Progesterone is also available in the forms of vaginal or rectal suppositories or pessaries (Cyclogest), [...]
- ^ Hauss DJ (8 June 2007). Oral Lipid-Based Formulations: Enhancing the Bioavailability of Poorly Water-Soluble Drugs. CRC Press. pp. 17–. ISBN 978-1-4200-1726-7.
- ^ Micozzi MS, Dog TL (19 August 2004). Women's Health in Complementary and Integrative Medicine E-Book: A Clinical Guide. Elsevier Health Sciences. pp. 69–. ISBN 0-7020-3598-X.
- ^ Porter CJ, Pouton CW, Cuine JF, Charman WN (March 2008). "Enhancing intestinal drug solubilisation using lipid-based delivery systems". Adv. Drug Deliv. Rev. 60 (6): 673–91. doi:10.1016/j.addr.2007.10.014. PMID 18155801.
- ^ a b Humberstone AJ, Charman WN (1997). "Lipid-based vehicles for the oral delivery of poorly water soluble drugs". Advanced Drug Delivery Reviews. 25 (1): 103–128. doi:10.1016/S0169-409X(96)00494-2. ISSN 0169-409X.
- ^ a b Kincl FA, Ciaccio LA, Benagiano G (January 1978). "Increasing oral bioavailability of progesterone by formulation". J. Steroid Biochem. 9 (1): 83–4. doi:10.1016/0022-4731(78)90106-1. PMID 628211.
- ^ a b Hargrove JT, Maxson WS, Wentz AC (October 1989). "Absorption of oral progesterone is influenced by vehicle and particle size". Am. J. Obstet. Gynecol. 161 (4): 948–51. doi:10.1016/0002-9378(89)90759-X. PMID 2801843.
- ^ Schindler AE, Campagnoli C, Druckmann R, Huber J, Pasqualini JR, Schweppe KW, Thijssen JH (2008). "Classification and pharmacology of progestins" (PDF). Maturitas. 61 (1–2): 171–80. doi:10.1016/j.maturitas.2008.11.013. PMID 19434889.[영구적 데드링크]
- ^ a b c d e f Hermann AC, Nafziger AN, Victory J, Kulawy R, Rocci ML, Bertino JS (2005). "Over-the-counter progesterone cream produces significant drug exposure compared to a food and drug administration-approved oral progesterone product". J Clin Pharmacol. 45 (6): 614–9. doi:10.1177/0091270005276621. PMID 15901742. S2CID 28399314.
- ^ Jameson JL, De Groot LJ (25 February 2015). Endocrinology: Adult and Pediatric E-Book. Elsevier Health Sciences. pp. 2660–. ISBN 978-0-323-32195-2.
- ^ McAuley JW, Kroboth FJ, Kroboth PD (1996). "Oral administration of micronized progesterone: a review and more experience". Pharmacotherapy. 16 (3): 453–7. doi:10.1002/j.1875-9114.1996.tb02977.x (inactive 31 October 2021). PMID 8726605.
{{cite journal}}: CS1 maint : 2021년 10월 현재 DOI 비활성화(링크) - ^ a b Anderson GD, Odegard PS (October 2004). "Pharmacokinetics of estrogen and progesterone in chronic kidney disease". Adv Chronic Kidney Dis. 11 (4): 357–60. doi:10.1053/j.ackd.2004.07.001. PMID 15492972.
- ^ Integrative Medicine. Elsevier Health Sciences. 2012. p. 343. ISBN 978-1-4377-1793-8.
- ^ Shoham Z, Kopernik G (June 2004). "Tools for making correct decisions regarding hormone therapy. part I: background and drugs". Fertil. Steril. 81 (6): 1447–57. doi:10.1016/j.fertnstert.2003.10.052. PMID 15193460.
- ^ a b c d e de Lignieres B, Dennerstein L, Backstrom T (April 1995). "Influence of route of administration on progesterone metabolism". Maturitas. 21 (3): 251–7. doi:10.1016/0378-5122(94)00882-8. PMID 7616875.
- ^ a b Wang-Cheng R, Neuner JM, Barnabei VM (2007). Menopause. ACP Press. p. 97. ISBN 978-1-930513-83-9.
- ^ a b Bergemann N, Ariecher-Rössler A (27 December 2005). Estrogen Effects in Psychiatric Disorders. Springer Science & Business Media. p. 179. ISBN 978-3-211-27063-9.
- ^ Reddy DS (2010). "Neurosteroids: endogenous role in the human brain and therapeutic potentials". Progress in Brain Research. 186: 113–37. doi:10.1016/B978-0-444-53630-3.00008-7. PMC 3139029. PMID 21094889.
- ^ a b c Alam V, Vega M, Rísquez F (2001). "Luteal phase support". Reprod. Biomed. Online. 3 (3): 250–262. doi:10.1016/S1472-6483(10)62044-5. PMID 12513863.
- ^ a b c d e f g h i j k Nahoul K, Dehennin L, Jondet M, Roger M (May 1993). "Profiles of plasma estrogens, progesterone and their metabolites after oral or vaginal administration of estradiol or progesterone". Maturitas. 16 (3): 185–202. doi:10.1016/0378-5122(93)90064-O. PMID 8515718.
- ^ a b Warren MP, Shantha S (1999). "Uses of progesterone in clinical practice". Int J Fertil Womens Med. 44 (2): 96–103. PMID 10338267.
- ^ a b c d e f g h i j k de Ziegler D, Fanchin R (2000). "Progesterone and progestins: applications in gynecology". Steroids. 65 (10–11): 671–9. doi:10.1016/s0039-128x(00)00123-9. PMID 11108875. S2CID 5867301.
- ^ Söderpalm AH, Lindsey S, Purdy RH, Hauger R, Wit de H (2004). "Administration of progesterone produces mild sedative-like effects in men and women". Psychoneuroendocrinology. 29 (3): 339–54. doi:10.1016/s0306-4530(03)00033-7. PMID 14644065. S2CID 21796848.
- ^ de Wit H, Schmitt L, Purdy R, Hauger R (2001). "Effects of acute progesterone administration in healthy postmenopausal women and normally-cycling women". Psychoneuroendocrinology. 26 (7): 697–710. doi:10.1016/s0306-4530(01)00024-5. PMID 11500251. S2CID 20611661.
- ^ van Broekhoven F, Bäckström T, Verkes RJ (2006). "Oral progesterone decreases saccadic eye velocity and increases sedation in women". Psychoneuroendocrinology. 31 (10): 1190–9. doi:10.1016/j.psyneuen.2006.08.007. PMID 17034954. S2CID 40466952.
- ^ a b de Wit H, Schmitt L, Purdy R, Hauger R (October 2001). "Effects of acute progesterone administration in healthy postmenopausal women and normally-cycling women". Psychoneuroendocrinology. 26 (7): 697–710. doi:10.1016/s0306-4530(01)00024-5. PMID 11500251. S2CID 20611661.
- ^ Turkmen S, Backstrom T, Wahlstrom G, Andreen L, Johansson IM (2011). "Tolerance to allopregnanolone with focus on the GABA-A receptor". Br. J. Pharmacol. 162 (2): 311–27. doi:10.1111/j.1476-5381.2010.01059.x. PMC 3031054. PMID 20883478.
- ^ Timby E, Balgård M, Nyberg S, Spigset O, Andersson A, Porankiewicz-Asplund J, Purdy RH, Zhu D, Bäckström T, Poromaa IS (2006). "Pharmacokinetic and behavioral effects of allopregnanolone in healthy women". Psychopharmacology. 186 (3): 414–24. doi:10.1007/s00213-005-0148-7. PMID 16177884. S2CID 16928783.
- ^ Pearlstein T (2016). "Treatment of Premenstrual Dysphoric Disorder: Therapeutic Challenges". Expert Rev Clin Pharmacol. 9 (4): 1–4. doi:10.1586/17512433.2016.1142371. PMID 26766596. S2CID 12172042.
A recent study with a 5α-reductase inhibitor dutasteride, that blocks the conversion of progesterone to ALLO, reported that dutasteride 2.5 mg daily decreased several premenstrual symptoms [7].
- ^ Sripada RK, Marx CE, King AP, Rampton JC, Ho SS, Liberzon I (2013). "Allopregnanolone elevations following pregnenolone administration are associated with enhanced activation of emotion regulation neurocircuits". Biol. Psychiatry. 73 (11): 1045–53. doi:10.1016/j.biopsych.2012.12.008. PMC 3648625. PMID 23348009.
- ^ Ducharme N, Banks WA, Morley JE, Robinson SM, Niehoff ML, Mattern C, Farr SA (2010). "Brain distribution and behavioral effects of progesterone and pregnenolone after intranasal or intravenous administration". Eur. J. Pharmacol. 641 (2–3): 128–34. doi:10.1016/j.ejphar.2010.05.033. PMC 3008321. PMID 20570588.
- ^ Saudan C, Desmarchelier A, Sottas PE, Mangin P, Saugy M (2005). "Urinary marker of oral pregnenolone administration". Steroids. 70 (3): 179–83. doi:10.1016/j.steroids.2004.12.007. PMID 15763596. S2CID 25490229.
- ^ a b Piper T, Schlug C, Mareck U, Schänzer W (2011). "Investigations on changes in ¹³C/¹²C ratios of endogenous urinary steroids after pregnenolone administration". Drug Test Anal. 3 (5): 283–90. doi:10.1002/dta.281. PMID 21538944.
- ^ Sauer MV (1 March 2013). Principles of Oocyte and Embryo Donation. Springer Science & Business Media. pp. 117–. ISBN 978-1-4471-2392-7.
- ^ Frank R, Guterman HS (1954). "Comparison of progesterone preparations in secondary amenorrhea". Fertil. Steril. 5 (4): 374–81. doi:10.1016/S0015-0282(16)31687-9. PMID 13183192.
- ^ Trabert B, Sherman ME, Kannan N, Stanczyk FZ (September 2019). "Progesterone and breast cancer". Endocr. Rev. 41 (2): 320–344. doi:10.1210/endrev/bnz001. PMC 7156851. PMID 31512725.
- ^ a b c Malik S, Krishnaprasad K (February 2016). "Natural Micronized Progesterone Sustained Release (SR) and Luteal Phase: Role Redefined!!". Journal of Clinical and Diagnostic Research. 10 (2): QE01-4. doi:10.7860/JCDR/2016/17278.7212. PMC 4800604. PMID 27042538.
- ^ Purandare AC, Hajare A, Krishnaprasad K, Bhargava A (2014). "Prescription event monitoring study to assess the safety profile of oral natural micronized progesterone sustained release in India". International Journal of Medical Research & Health Sciences. 3 (4): 975. doi:10.5958/2319-5886.2014.00034.4. ISSN 2319-5886.
- ^ Haleem S, Khan MI (March 2015). "Changing Indian Market Trends of NMP: A Review" (PDF). International Journal of Pharma Research & Review. 4 (3): 28–30. ISSN 2278-6074. S2CID 74224514. Archived from the original (PDF) on 2020-08-19.
- ^ Nigam A (2018). "Luteal Phase Support: Why, When and How" (PDF). Pan Asian Journal of Obstetrics & Gynecology. 1 (2): 79–83. Archived from the original (PDF) on 2020-08-19.
- ^ Malhotra J, Krishnaprasad K (January 2016). "Open-label, Prospective, Investigator Initiated Study to Assess the Clinical Role of Oral Natural or Synthetic Progesterone During Stimulated IUI Cycles for Unexplained Infertility". Journal of Clinical and Diagnostic Research. 10 (1): QC08-10. doi:10.7860/JCDR/2016/17058.7106. PMC 4740654. PMID 26894126.
- ^ Prabhat P, Korukonda K (2018). "A Drug Utilisation Surveillance Study to Assess the Clinical Utility and Safety of Oral Natural Micronized Progesterone SR in High Risk Pregnancies: NAP-DELAY Study". Journal of Clinical and Diagnostic Research. doi:10.7860/JCDR/2018/34886.12118. ISSN 2249-782X.
- ^ Singh N, Reddy A (April–June 2015). "Current Concepts in Management of Preterm Labour - A Review Article". Indian Obstetrics and Gynaecology. 5 (2).
- ^ a b c Kirk EP, Serat S, Burrows LJ, Mott LA, Yeo KJ, Fitzmaurice T, Lewis LD (1997). "A pharmacokinetic study of micronized natural progesterone extended release tablets". Restore Health. Archived from the original on 2019-03-04.
- ^ a b "Progesterone".
- ^ Wren BG, Day RO, McLachlan AJ, Williams KM (June 2003). "Pharmacokinetics of estradiol, progesterone, testosterone and dehydroepiandrosterone after transbuccal administration to postmenopausal women". Climacteric. 6 (2): 104–11. doi:10.1080/cmt.6.2.104.111. PMID 12841880. S2CID 26455195.
- ^ Jain SK, Jain A, Gupta Y, Kharya A (February 2008). "Design and development of a mucoadhesive buccal film bearing progesterone". Pharmazie. 63 (2): 129–35. doi:10.1691/ph.2008.7114. PMID 18380399.
- ^ Whitelaw MJ (January 1955). "Effects of Parenteral, Oral, Buccal, and Vaginal Progesterone on the Endometrium". Journal of Clinical Endocrinology & Metabolism. 15 (7): 881–882. ISSN 0021-972X.
- ^ Soule SD, Yanow M (July 1953). "Recovery of pregnanediol from urine following administration of oral anhydrohydroxyprogesterone, buccal progesterone, and intramuscular progesterone". Obstet Gynecol. 2 (1): 68–72. PMID 13073082.
- ^ Maddox DH, Burnside BA, Keith AD (1990). "Buccal delivery of progesterone". Proceedings of the International Symposium on Controlled Release of Bioactive Materials. Vol. 17. pp. 291–292.
- ^ Voorspoels J, Comhaire F, De Sy W, Remon JP (1997). "Buccal absorption of progesterone in the dog". Proceedings of the International Symposium on Controlled Release of Bioactive Materials. Vol. 24. pp. 185–186.
- ^ a b Hans Hermann Julius Hager; Walther Kern; Paul Heinz List; Hermann Josef Roth (1969). Hagers Handbuch der Pharmazeutischen Praxis: Für Apotheker, Arzneimittelhersteller, Ärzte und Medizinalbeamte: Wirkstoffgruppen II Chemikalien und Drogen (A-AL). Springer-Verlag. pp. 178–. ISBN 978-3-662-25655-8.
- ^ Ashton Leroy Welsh (1951). Dermatological Formulary: A Guide for Medical Students and Resident Physicians in Dermatology. Educational Publishers. p. 155.
- ^ a b Chakmakjian ZH, Zachariah NY (June 1987). "Bioavailability of progesterone with different modes of administration". The Journal of Reproductive Medicine. 32 (6): 443–8. PMID 3612635.
- ^ a b Villanueva B, Casper RF, Yen SS (April 1981). "Intravaginal administration of progesterone: enhanced absorption after estrogen treatment". Fertil. Steril. 35 (4): 433–7. doi:10.1016/S0015-0282(16)45439-7. PMID 7215569.
- ^ a b c Zygmunt M, Sapa Y (2017). "Progesterone – a new look at an old drug". Reproductive Endocrinology (33): 17–25. doi:10.18370/2309-4117.2017.33.17-25. ISSN 2411-1295.
[In other pharmacokinetic studies it has been proven that after administration of 100 mg of progesterone the hormone reached its maximum concentration in the plasma after 1-4 hours, which was on average 13.5 ng/mL.]
- ^ Bhavnani BR, Stanczyk FZ (March 2012). "Misconception and concerns about bioidentical hormones used for custom-compounded hormone therapy". J Clin Endocrinol Metab. 97 (3): 756–9. doi:10.1210/jc.2011-2492. PMID 22205711.
- ^ a b c d e f g h i j Unfer V, Casini ML, Marelli G, Costabile L, Gerli S, Di Renzo GC (2005). "Different routes of progesterone administration and polycystic ovary syndrome: a review of the literature". Gynecol. Endocrinol. 21 (2): 119–27. doi:10.1080/09513590500170049. PMID 16109599. S2CID 24890723.
- ^ a b c d Stovall DW, Van Voorhis BJ, Mattingly KL, Sparks AE, Chapler FK, Syrop CH (May 1996). "The effectiveness of sublingual progesterone administration during cryopreserved embryo transfer cycles: results of a matched follow-up study". Fertil. Steril. 65 (5): 986–91. doi:10.1016/S0015-0282(16)58274-0. PMID 8612862.
- ^ Chakmakjian ZH, Zachariah NY (June 1987). "Bioavailability of progesterone with different modes of administration". J Reprod Med. 32 (6): 443–8. ISSN 0024-7758. PMID 3612635.
- ^ Bickers W (August 1949). "Progesterone; a comparison of intramuscular, oral and sublingual routes of administration". J. Clin. Endocrinol. Metab. 9 (8): 736–42. doi:10.1210/jcem-9-8-736. PMID 18133494.
- ^ Corner GW (1944). "The Absorption of Steroid Hormones from the Oral Mucous Membranes, with Special Reference to the Sublingual Administration of Progesterone". American Journal of Obstetrics and Gynecology. 47 (5): 670–677. doi:10.1016/S0002-9378(16)40321-2.
- ^ Greenblatt RB (1944). "Sublingual Absorption of Progesterone and Anhydrohydroxyprogesterone". The Journal of Clinical Endocrinology & Metabolism. 4 (4): 156–158. doi:10.1210/jcem-4-4-156. ISSN 0021-972X.
- ^ Greenblatt RB (1944). "Perlingual Absorption of Progesterone and Anhydrohydroxyprogesterone". The Journal of Clinical Endocrinology & Metabolism. 4 (7): 321–325. doi:10.1210/jcem-4-7-321. ISSN 0021-972X.
- ^ a b Steege JF, Rupp SL, Stout AL, Bernhisel M (October 1986). "Bioavailability of nasally administered progesterone". Fertil. Steril. 46 (4): 727–9. doi:10.1016/S0015-0282(16)49661-5. PMID 3758397.
- ^ Posaci C, Smitz J, Camus M, Osmanagaoglu K, Devroey P (June 2000). "Progesterone for the luteal support of assisted reproductive technologies: clinical options". Hum. Reprod. 15 Suppl 1: 129–48. doi:10.1093/humrep/15.suppl_1.129. PMID 10928425.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae Stanczyk FZ (2014). "Treatment of postmenopausal women with topical progesterone creams and gels: are they effective?". Climacteric. 17 Suppl 2: 8–11. doi:10.3109/13697137.2014.944496. PMID 25196424. S2CID 20019151.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au Stanczyk FZ, Paulson RJ, Roy S (2005). "Percutaneous administration of progesterone: blood levels and endometrial protection". Menopause. 12 (2): 232–7. doi:10.1097/00042192-200512020-00019. PMID 15772572. S2CID 10982395.
- ^ a b c d e f g h i Sitruk-Ware R (January 1989). "Transdermal delivery of steroids". Contraception. 39 (1): 1–20. doi:10.1016/0010-7824(89)90012-7. PMID 2642780.
- ^ a b c d e f Bińkowska M, Woroń J (June 2015). "Progestogens in menopausal hormone therapy". Przeglad Menopauzalny = Menopause Review. 14 (2): 134–43. doi:10.5114/pm.2015.52154. PMC 4498031. PMID 26327902.
- ^ https://www.drugs.com/international/progestogel.html
- ^ Marker RE, Krueger J (1940). "Sterols. CXII. Sapogenins. XLI. The Preparation of Trillin and its Conversion to Progesterone". J. Am. Chem. Soc. 62 (12): 3349–3350. doi:10.1021/ja01869a023.
- ^ Zava DT, Dollbaum CM, Blen M (March 1998). "Estrogen and progestin bioactivity of foods, herbs, and spices". Proceedings of the Society for Experimental Biology and Medicine. 217 (3): 369–78. doi:10.3181/00379727-217-44247. PMID 9492350. S2CID 20673587.
- ^ Komesaroff PA, Black CV, Cable V, Sudhir K (June 2001). "Effects of wild yam extract on menopausal symptoms, lipids and sex hormones in healthy menopausal women". Climacteric. 4 (2): 144–50. doi:10.1080/713605087. PMID 11428178.
- ^ a b Sitruk-Ware R (February 1993). "Percutaneous and transdermal oestrogen replacement therapy". Annals of Medicine. 25 (1): 77–82. doi:10.3109/07853899309147862. PMID 8435193.
- ^ a b c d e Mauvais-Jarvis P, Sitruk-Ware R, Kuttenn F (1981). "Benign Breast Disease". Breast Cancer 4. pp. 51–94. doi:10.1007/978-1-4615-6571-0_3. ISBN 978-1-4615-6573-4.
- ^ De Boever J, Verheugen C, van Maele G, Vandekerckhove D (1983). "Steroid Concentrations in Serum, Glandular Breast Tissue, and Breast Cyst Fluid of Control and Progesterone-Treated Patients" (PDF). In Alberto Angeli (ed.). Endocrinology of Cystic Breast Disease. Raven Press. pp. 93–99.
- ^ a b c Taubert HD (1989). "Lokaltherapie mit Sexualsteroiden". Gießener Gynäkologische Fortbildung 1989. pp. 214–224. doi:10.1007/978-3-642-50217-0_25. ISBN 978-3-540-51234-9.
- ^ Wiedersberg S, Guy RH (September 2014). "Transdermal drug delivery: 30+ years of war and still fighting!" (PDF). Journal of Controlled Release. 190: 150–6. doi:10.1016/j.jconrel.2014.05.022. PMID 24852092.
- ^ Jones H (25 September 2008). Testosterone Deficiency in Men. OUP Oxford. pp. 89–. ISBN 978-0-19-954513-1.
- ^ Rastrelli G, Reisman Y, Ferri S, Prontera O, Sforza A, Maggi M, Corona G (2019). "Testosterone Replacement Therapy". Sexual Medicine. pp. 79–93. doi:10.1007/978-981-13-1226-7_8. ISBN 978-981-13-1225-0. S2CID 240176927.
- ^ a b Potts RO, Lobo RA (May 2005). "Transdermal drug delivery: clinical considerations for the obstetrician-gynecologist". Obstet Gynecol. 105 (5 Pt 1): 953–61. doi:10.1097/01.AOG.0000161958.70059.db. PMID 15863530. S2CID 23411589.
- ^ a b c d e f g h Du JY, Sanchez P, Kim L, Azen CG, Zava DT, Stanczyk FZ (2013). "Percutaneous progesterone delivery via cream or gel application in postmenopausal women: a randomized cross-over study of progesterone levels in serum, whole blood, saliva, and capillary blood". Menopause. 20 (11): 1169–75. doi:10.1097/GME.0b013e31828d39a2. PMID 23652031. S2CID 33857615.
- ^ a b c Heustess A, Asbill S, Eagerton D, Arnold J (2014). "In vitro skin penetration and skin content of progesterone from various topical formulations". Int J Pharm Compd. 18 (6): 512–5. PMID 25906629.
- ^ a b c Wright F, Mauvais-Jarvis P (1989). "Metabolism of Sex Steroids in Handbook of Experimental Pharmacology". Handbook of Experimental Pharmacology Continuation of Handbuch der Experimentellen Pharmakologie. 87 / 1: 247–255. doi:10.1007/978-3-642-73797-8_15. ISSN 0171-2004.
- ^ a b Mauvais-Jarvis P, Kuttenn F, Ohlgiesser C (April 1974). "Résultats du traitement de mastodynies et de mastopathies par la progestérone percutanée" [Results of treating mastodynias and mastopathies with percutaneous progesterone]. Nouv Presse Med (in French). 3 (16): 1027–8. PMID 4836479.
- ^ Mauvais-Jarvis P, Kuttenn F, Baudot N (January 1974). "Inhibition of testosterone conversion to dihydrotestosterone in men treated percutaneously by progesterone". J. Clin. Endocrinol. Metab. 38 (1): 142–7. doi:10.1210/jcem-38-1-142. PMID 4809637.
- ^ Mauvais-Jarvis P, Baudot N, Bercovici JP (December 1969). "In vivo studies on progesterone metabolism by human skin". J. Clin. Endocrinol. Metab. 29 (12): 1580–5. doi:10.1210/jcem-29-12-1580. PMID 5347688.
- ^ Zargar-Shoshtari S, Wahhabaghei H, Mehrsai A, Wen J, Alany R (2010). "Transdermal delivery of bioidentical progesterone using dutasteride (A 5α-reductase inhibitor): a pilot study". J Pharm Pharm Sci. 13 (4): 626–36. doi:10.18433/j3rw2h. PMID 21486536.
- ^ Zargar-Shoshtari S, Wahhabaghei H, Mehrsai A, Wen J, Alany R (2011). "Transdermal Delivery of Bioidentical Progesterone with a Steroid 5α-Reductase Inhibitor (Dutasteride): a Pilot Study". Journal of Pharmacy & Pharmaceutical Sciences. 13 (4): 626–36. doi:10.18433/J3RW2H. ISSN 1482-1826. PMID 21486536.
- ^ 자르가-쇼쉬타리, S. (2011년)Progesterone의 경피 전달(의사 논문).http://hdl.handle.net/2292/8199
- ^ Rakel D (2012). Integrative Medicine. Elsevier Health Sciences. pp. 330–. ISBN 978-1-4377-1793-8.
- ^ a b De Boever, J.; Desmet, B.; Vandekerckhove, D. (1980). "Variation of progesterone, 20α-dihydroprogesterone and oestradiol concentrations in human mammary tissue and blood after topical administration of progesterone". In P. Mauvais-Jarvis (ed.). Percutaneous absorption of steroids. Academic Press. pp. 259–265. ISBN 9780124806801.
- ^ a b Chang KJ, Lee TT, Linares-Cruz G, Fournier S, de Ligniéres B (April 1995). "Influences of percutaneous administration of estradiol and progesterone on human breast epithelial cell cycle in vivo". Fertil. Steril. 63 (4): 785–91. doi:10.1016/S0015-0282(16)57482-2. PMID 7890063.
- ^ Spicer DV, Ursin G, Pike MC (May 1996). "Progesterone concentrations--physiologic or pharmacologic?". Fertil. Steril. 65 (5): 1077–8. doi:10.1016/s0015-0282(16)58295-8. PMID 8612843.
- ^ a b c d e f g h von Eye Corleta H, Capp E, Ferreira MB (2004). "Pharmacokinetics of natural progesterone vaginal suppository". Gynecol. Obstet. Invest. 58 (2): 105–8. doi:10.1159/000078842. PMID 15192285. S2CID 46611378.
- ^ Rao K, Carp HJ, Fischer R (30 September 2013). Principles & Practice of Assisted Reproductive Technology (3 Vols). JP Medical Ltd. p. 1025–. ISBN 978-93-5090-736-8.
Vaginal administration of progesterone can take many routes such as micronized vaginal suppositories (e.g. Utrogestan or Cyclogest 600 mg daily), foam release vaginal inserts (Endometrin) or vaginal gels (Crinone 8% gel containing 90 mg micronized progesterone one or two applications daily).
- ^ Racowsky C, Schlegel PN, Fauser BC, Barnard L (7 June 2011). Biennial Review of Infertility. Springer Science & Business Media. pp. 84–85. ISBN 978-1-4419-8456-2.
There are currently three standardized vaginal progesterone formulations commercially available for use in IVF. Micronized progesterone capsules (Utrogestan/Prometrium) are available and widely used in Europe and South America, but not FDA approved for use in IVF/ART in the United States. The two progesterone formulations approved by FDA for use in IVF are Crinone 8% vaginal gel, and more recently – Endometrin 100 mg (natural progesterone in capsules).
- ^ Friend DR (October 2016). "Development of controlled release systems over the past 50 years in the area of contraception". J Control Release. 240: 235–241. doi:10.1016/j.jconrel.2015.12.043. PMID 26732558.
- ^ Miles RA, Paulson RJ, Lobo RA, Press MF, Dahmoush L, Sauer MV (September 1994). "Pharmacokinetics and endometrial tissue levels of progesterone after administration by intramuscular and vaginal routes: a comparative study". Fertil. Steril. 62 (3): 485–90. doi:10.1016/s0015-0282(16)56935-0. PMID 8062942.
- ^ Schmidt JW, Wollner D, Curcio J, Riedlinger J, Kim LS (October 2006). "Hormone replacement therapy in menopausal women: Past problems and future possibilities". Gynecol. Endocrinol. 22 (10): 564–77. doi:10.1080/09513590600927017. PMID 17135036. S2CID 11567574.
- ^ a b c d e f Goletiani NV, Keith DR, Gorsky SJ (October 2007). "Progesterone: review of safety for clinical studies". Exp Clin Psychopharmacol. 15 (5): 427–44. doi:10.1037/1064-1297.15.5.427. PMID 17924777.
- ^ Sills ES (7 September 2015). Screening the Single Euploid Embryo: Molecular Genetics in Reproductive Medicine. Springer. pp. 276–277. ISBN 978-3-319-16892-0.
- ^ Tatford EP (6 December 2012). Problems in Gynaecology. Springer Science & Business Media. pp. 85–. ISBN 978-94-009-4125-0.
Progesterone can also be given by rectal or vaginal suppository (Cyclogest) in a dose of 400 mg daily.
- ^ Aghsa MM, Rahmanpour H, Bagheri M, Davari-Tanha F, Nasr R (October 2012). "A randomized comparison of the efficacy, side effects and patient convenience between vaginal and rectal administration of Cyclogest(®) when used for luteal phase support in ICSI treatment". Archives of Gynecology and Obstetrics. 286 (4): 1049–54. doi:10.1007/s00404-012-2410-7. PMID 22714063. S2CID 12892111.
- ^ Khrouf M, Slimani S, Khrouf MR, Braham M, Bouyahia M, Berjeb KK, et al. (2016). "Progesterone for Luteal Phase Support in In Vitro Fertilization: Comparison of Vaginal and Rectal Pessaries to Vaginal Capsules: A Randomized Controlled Study". Clinical Medicine Insights. Women's Health. 9: 43–47. doi:10.4137/CMWH.S32156. PMC 5217976. PMID 28096703.
- ^ a b Tay PY, Lenton EA (June 2005). "The impact of luteal supplement on pregnancy outcome following stimulated IVF cycles" (PDF). The Medical Journal of Malaysia. 60 (2): 151–7. PMID 16114155.
- ^ a b van der Meer YG, van Loenen AC, Loendersloot EW, Jaszmann LJ (October 1982). "Plasma progesterone levels after using high dose suppositories. A preliminary report". Pharmaceutisch Weekblad. Scientific Edition. 4 (5): 135–6. doi:10.1007/BF01959031. PMID 7145597. S2CID 19671703.
- ^ a b Nillius SJ, Johansson ED (June 1971). "Plasma levels of progesterone after vaginal, rectal, or intramuscular administration of progesterone". American Journal of Obstetrics and Gynecology. 110 (4): 470–7. doi:10.1016/0002-9378(71)90686-7. PMID 5582003.
- ^ Hamburger C (1965). "Administration of progesterone in the form of suppositories". Acta Endocrinologica. 49 (3_Suppl): S101. doi:10.1530/acta.0.049S101. ISSN 0804-4643.
- ^ Van der Meer YG, Benedek-Jaszmann LJ, Van Loenen AC (2009). "Effect of high-dose progesterone on the pre-menstrual syndrome; a double-blind cross-over trial". Journal of Psychosomatic Obstetrics & Gynecology. 2 (4): 220–222. doi:10.3109/01674828309088321. ISSN 0167-482X.
- ^ a b c Knörr K, Beller FK, Lauritzen C (17 April 2013). Lehrbuch der Gynäkologie. Springer-Verlag. pp. 214–. ISBN 978-3-662-00942-0.
- ^ Knörr K, Knörr-Gärtner H, Beller FK, Lauritzen C (8 March 2013). Geburtshilfe und Gynäkologie: Physiologie und Pathologie der Reproduktion. Springer-Verlag. pp. 583–. ISBN 978-3-642-95583-9.
- ^ A. Labhart (6 December 2012). Clinical Endocrinology: Theory and Practice. Springer Science & Business Media. pp. 554–. ISBN 978-3-642-96158-8.
- ^ a b Horský J, Presl J (1981). "Hormonal Treatment of Disorders of the Menstrual Cycle". In Horsky J, Presl K (eds.). Ovarian Function and its Disorders: Diagnosis and Therapy. Springer Science & Business Media. pp. 309–332. doi:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Joachim Ufer (1969). The Principles and Practice of Hormone Therapy in Gynaecology and Obstetrics. de Gruyter. p. 49.
17α-Hydroxyprogesterone caproate is a depot progestogen which is entirely free of side actions. The dose required to induce secretory changes in primed endometrium is about 250 mg. per menstrual cycle.
- ^ Willibald Pschyrembel (1968). Praktische Gynäkologie: für Studierende und Ärzte. Walter de Gruyter. pp. 598, 601. ISBN 978-3-11-150424-7.
- ^ a b c d Ferin J (September 1972). "Effects, Duration of Action and Metabolism in Man". In Tausk M (ed.). Pharmacology of the Endocrine System and Related Drugs: Progesterone, Progestational Drugs and Antifertility Agents. Vol. II. Pergamon Press. pp. 13–24. ISBN 978-0080168128. OCLC 278011135.
- ^ Henzl MR, Edwards JA (10 November 1999). "Pharmacology of Progestins: 17α-Hydroxyprogesterone Derivatives and Progestins of the First and Second Generation". In Sitruk-Ware R, Mishell DR (eds.). Progestins and Antiprogestins in Clinical Practice. Taylor & Francis. pp. 101–132. ISBN 978-0-8247-8291-7.
- ^ a b Janet Brotherton (1976). Sex Hormone Pharmacology. Academic Press. p. 114. ISBN 978-0-12-137250-7.
- ^ Sang GW (April 1994). "Pharmacodynamic effects of once-a-month combined injectable contraceptives". Contraception. 49 (4): 361–85. doi:10.1016/0010-7824(94)90033-7. PMID 8013220.
- ^ Toppozada MK (April 1994). "Existing once-a-month combined injectable contraceptives". Contraception. 49 (4): 293–301. doi:10.1016/0010-7824(94)90029-9. PMID 8013216.
- ^ Bagade O, Pawar V, Patel R, Patel B, Awasarkar V, Diwate S (2014). "Increasing use of long-acting reversible contraception: safe, reliable, and cost-effective birth control" (PDF). World J Pharm Pharm Sci. 3 (10): 364–392. ISSN 2278-4357. Archived from the original (PDF) on 2017-08-10. Retrieved 2016-08-24.
- ^ a b c Goebelsmann U (1986). "Pharmacokinetics of Contraceptive Steroids in Humans". In Gregoire AT, Blye RP (eds.). Contraceptive Steroids: Pharmacology and Safety. Springer Science & Business Media. pp. 67–111. doi:10.1007/978-1-4613-2241-2_4. ISBN 978-1-4613-2241-2.
- ^ Becker H, Düsterberg B, Klosterhalfen H (1980). "[Bioavailability of cyproterone acetate after oral and intramuscular application in men (author's transl)]" [Bioavailability of Cyproterone Acetate after Oral and Intramuscular Application in Men]. Urologia Internationalis. 35 (6): 381–5. doi:10.1159/000280353. PMID 6452729.
- ^ Moltz L, Haase F, Schwartz U, Hammerstein J (May 1983). "[Treatment of virilized women with intramuscular administration of cyproterone acetate]" [Efficacy of Intra muscularly Applied Cyproterone Acetate in Hyperandrogenism]. Geburtshilfe Und Frauenheilkunde. 43 (5): 281–7. doi:10.1055/s-2008-1036893. PMID 6223851.
- ^ Wright JC, Burgess DJ (29 January 2012). Long Acting Injections and Implants. Springer Science & Business Media. pp. 114–. ISBN 978-1-4614-0554-2.
- ^ Chu YH, Li Q, Zhao ZF (April 1986). "Pharmacokinetics of megestrol acetate in women receiving IM injection of estradiol-megestrol long-acting injectable contraceptive". The Chinese Journal of Clinical Pharmacology.
The results showed that after injection the concentration of plasma MA increased rapidly. The meantime of peak plasma MA level was 3rd day, there was a linear relationship between log of plasma MA concentration and time (day) after administration in all subjects, elimination phase half-life t1/2β = 14.35 ± 9.1 days.
- ^ Runnebaum BC, Rabe T, Kiesel L (6 December 2012). Female Contraception: Update and Trends. Springer Science & Business Media. pp. 429–. ISBN 978-3-642-73790-9.
- ^ Artini PG, Genazzani AR, Petraglia F (11 December 2001). Advances in Gynecological Endocrinology. CRC Press. pp. 105–. ISBN 978-1-84214-071-0.
- ^ King TL, Brucker MC, Kriebs JM, Fahey JO (21 October 2013). Varney's Midwifery. Jones & Bartlett Publishers. pp. 495–. ISBN 978-1-284-02542-2.
- ^ a b c d e Bernardo-Escudero R, Cortés-Bonilla M, Alonso-Campero R, Francisco-Doce MT, Chavarín-González J, Pimentel-Martínez S, Zambrano-Tapia L (2012). "Observational study of the local tolerability of injectable progesterone microspheres". Gynecol. Obstet. Invest. 73 (2): 124–9. doi:10.1159/000330711. PMID 21997608. S2CID 5163167.
- ^ Tyler ET, Olson HJ (April 1959). "Fertility promoting and inhibiting effects of new steroid hormonal substances". J Am Med Assoc. 169 (16): 1843–54. doi:10.1001/jama.1959.03000330015003. PMID 13640942.
- ^ Ferin J (September 1972). "Effects, Duration of Action and Metabolism in Man". In Tausk M (ed.). Pharmacology of the Endocrine System and Related Drugs: Progesterone, Progestational Drugs and Antifertility Agents. Vol. II. Pergamon Press. pp. 13–24. ISBN 978-0080168128. OCLC 278011135.
- ^ Horský J, Presl J (1981). "Hormonal Treatment of Disorders of the Menstrual Cycle". In J. Horsky, J. Presl (eds.). Ovarian Function and its Disorders: Diagnosis and Therapy. Springer Science & Business Media. pp. 309–332. doi:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Knörr K, Beller FK, Lauritzen C (17 April 2013). Lehrbuch der Gynäkologie. Springer-Verlag. pp. 214–. ISBN 978-3-662-00942-0.
- ^ a b Henzl M, Horský J, Presl J (1965), "Racionální Léčba Gestageny v Gynekologii" [Rational Treatment by Gestagens in Gynecology], Československá Gynekologie (in Czech), 30/44 (1/2): 10–16, ISSN 0374-6852,
Rational indications for the use of pure progesterone and some gestagens. These are depot microcrystal drugs (Agolutin depot), Neolutin and the new, perorally effective gestagens (nor-steroids, Superlutin). [...]
- ^ Ober KG, Klein I, Weber M (1954). "[The problem of progesterone therapy; experimental studies on the Hooker-Forbes test and clinical observations on crystalline suspensions]" [On the question of progesterone treatment: experimental studies with the Hooker-Forbes test and clinical observations with crystal suspensions]. Archiv für Gynakologie. 184 (5): 543–616. doi:10.1007/BF00976991. PMID 13198154. S2CID 42832785.
- ^ Engelking E (13 March 2013). Der Deutschen Ophthalmologischen Gesellschaft: In München 1950 [The German Ophthalmological Society: In Munich 1950]. Springer-Verlag. pp. 145–146. ISBN 978-3-642-47081-3.
Intramuskulare Injektionen öliger Progesteronlösungen erzielen wohl eine hohe Stoßwirkung, der Dauereffekt ist jedoch nur gering. So kann die Wirkung einer Injektion von 10 mg [intramuskulär] in schweren Glaukomfällen schon nach etwa 6 Stunden vergehen. Das Ergebnis ist dann ein Wiederhochschnellen des Augendruckes. Um den Hormonspiegel nicht zu rasch wieder abfallen zu lassen und gleichzeitig eine Stoßwirkung zu erzielen, mischen wir aus diesem Grunde gerne die ölige Lösung mit einer Kristallsuspension. Wir injizierten meist in den Deltoideus. Bei Hormonkristallsuspensionen braucht man ziemlich dicke Nadeln und benützt am besten eine 1 ccm Spritze. Für die augenärztliche Praxis ist letztere Art der Depotbehandlung am zweckmäßigsten. In schwereren Fällen mit chronischer hoher Drucksteigerung wirken [zum Beispiel] bei Verwendung von [Ampulle] mit je 30 mg [Kristallsuspension] die ersten Injektionen nur wenige Tage; mit zunehmender Dauer der Behandlung kann man dann jedoch die Zeitabstände zswischen den einzelnen Spritzen bis auf mehrere Wochen erhöhen. Die meisten Patienten spuren selbst deutlich, wenn die Depotwirkung nachläßt und kommen spontan, sich eine neue Injektion zu holen. [...] Depot: Flavolutan (Boehringer & Söhne) Kristallsuspension amp a 30 mg.
- ^ Shearman RP (June 1975). "The development of depot contraceptives". Journal of Steroid Biochemistry. 6 (6): 899–902. doi:10.1016/0022-4731(75)90323-4. PMID 1177432.
- ^ a b Edkins RP (1959). "The Modification of the Duration of Drug Action". Journal of Pharmacy and Pharmacology. 11 (S1): 54T–66T. doi:10.1111/j.2042-7158.1959.tb10412.x. ISSN 0022-3573. S2CID 78850713.
- ^ a b c Lens J, Overbeek GA, Polderman J (1949). "The effect of sex hormones in some organic solvents; emulsified in water". Acta Endocrinologica. 2 (4): 396–404. doi:10.1530/acta.0.0020396. PMID 18140399.
- ^ Herrmann U (1958). "Abhängigkeit der durch Oestrogen- und Progesteron-Kristalle induzierten Abbruchblutung von der Korngröße". Gynecologic and Obstetric Investigation. 146 (4): 318–323. doi:10.1159/000306607. ISSN 1423-002X.
- ^ Rappaport F, Lass N (August 1947). "Injectable crystalline hormones". Lancet. 2 (6469): 296–297. doi:10.1016/s0140-6736(47)92066-7. PMID 20344499.
- ^ Masters WH, Grody MH, Magallon DT (November 1952). "Progesterone in aqueous crystalline suspension versus progesterone in oil; comparison by withdrawal bleeding tests in the human female". The Journal of Clinical Endocrinology and Metabolism. 12 (11): 1445–53. doi:10.1210/jcem-12-11-1445. PMID 12999984.
- ^ a b c Kahr H (8 March 2013). Konservative Therapie der Frauenkrankheiten: Anzeigen, Grenzen und Methoden Einschliesslich der Rezeptur. Springer-Verlag. pp. 20–21. ISBN 978-3-7091-5694-0.
- ^ "Archived copy" (PDF). www.sukl.cz. Archived from the original (PDF) on 19 May 2019. Retrieved 15 January 2022.
{{cite web}}: CS1 maint: 타이틀로 보관된 사본(링크) - ^ Články v českých časopisech. Statni knihovna ČSSR. 1960. pp. 1601, 1642.
- ^ Plzensky lekarsky sbornik. Supplementum. 1961. p. 169.
- ^ Review of Czechoslovak Medicine. Avicenum - Czechoslovak Medical Press. 1973. p. 5.
Progesterone, aqueous microcrystalline suspension (Agolutin Depot SPOFA)
- ^ Ufer J (1968). "Die therapeutische Anwendung der Gestagene beim Menschen" [Therapeutic Use of Progestagens in Humans]. Die Gestagene [Progestogens]. Springer-Verlag. pp. 1026–1124. doi:10.1007/978-3-642-99941-3_7. ISBN 978-3-642-99941-3.
C. Dysfunktionelle Uterusblutungen. [...] 1. Depotinjektionen. 1. Originalmethode nach KAUFMANN und OBER. Es wird 1 Amp. mit 200 mg Progesteron und 10 mg Oestradiol-Monobenzoat als Kristallsuspension (Sistocyclin) injiziert [676, 678, 679, 295, 482, 365, 434, 563, 400]. [...] Beispiele. KAUFMANN et al. [485]: 400 mg Progesteron + 20 mg Oestradiolmonobenzoat Kristallsuspension. ELERT [224] U. HERRMANN [363]: 200 mg Progesteron + 10 mg Oestradiolmono benzoat Kristallsuspension.
- ^ Ciba Symposium. Ciba. 1957.
CIBA's range of hormone preparations has been increased with the advent of "Sistocyclin", one ampoule of which contains 200 mg progesterone and 10 mg oestradiol monobenzoate in crystalline suspension; it thus meets the requirements—in line with the most recent findings of the KAUFMANN Clinic—of cases marked by deficiency of corpus luteum hormone, e. g. in functional bleeding such as metropathia haemorrhagica.
- ^ Ciba Zeitschrift. 1957. p. 3001.
Sistocyclin - a microcrystal suspension containing 200 mg progesterone and 10 mg oestradiol monobenzoate per ampoule - has become particularly useful in the treatment of so-called, functional [...]
- ^ Willibald Pschyrembel (1968). Praktische Gynäkologie: für Studierende und Ärzte. Walter de Gruyter. pp. 601–. ISBN 978-3-11-150424-7.
- ^ Joachim Ufer (1960). Hormontherapie in der Frauenheilkunde: Grundlagen und Praxis. Gruyter. p. 153. ISBN 9783111138770.
- ^ Willibald Pschyrembel (15 June 2011). Praktische Gynäkologie: für Studierende und Ärzte. Walter de Gruyter. pp. 601–. ISBN 978-3-11-150424-7.
- ^ a b Swyer GI (January 1960). "Progestogens and their clinical uses: Part I". Br Med J. 1 (5165): 48–9. doi:10.1136/bmj.1.5165.48. PMC 1966392. PMID 13836156.
- ^ Janet Brotherton (1976). Sex Hormone Pharmacology. Academic Press. p. 38. ISBN 978-0-12-137250-7.
- ^ a b c Ian S. Fraser (1998). Estrogens and Progestogens in Clinical Practice. Churchill Livingstone. pp. 13, 92. ISBN 978-0-443-04706-0.
- ^ a b c Bradbury JT, Long RC, Durham WC (1953). "Progesterone and estrogen requirements to induce and maintain decidua". Fertil. Steril. 4 (1): 63–75. doi:10.1016/s0015-0282(16)31145-1. PMID 13021207.
- ^ a b c Mishell DR (May 1996). "Pharmacokinetics of depot medroxyprogesterone acetate contraception". The Journal of Reproductive Medicine. 41 (5 Suppl): 381–90. PMID 8725700. Archived from the original on 2020-07-29. Retrieved 2019-05-19.
- ^ Goebelsmann U (1986). "Pharmacokinetics of Contraceptive Steroids in Humans". In Gregoire AT, Blye RP (eds.). Contraceptive Steroids: Pharmacology and Safety. Springer Science & Business Media. pp. 67–111. doi:10.1007/978-1-4613-2241-2_4. ISBN 978-1-4613-2241-2.
- ^ a b Ferin J (January 1952). "Relative duration of action of natural and synthetic estrogens administered parenterally in women with estrogen deficiency". The Journal of Clinical Endocrinology and Metabolism. 12 (1): 28–35. doi:10.1210/jcem-12-1-28. PMID 14907837.
- ^ a b Overbeek CA (1952). "Some Data on Emulsions of Steroid Hormones". Ciba Foundation Symposium - Steroid Hormone Administration (Book II of Colloquia on Endocrinology, Vol. 3). Novartis Foundation Symposia. pp. 254–262. doi:10.1002/9780470715154.ch2. ISBN 9780470715154. ISSN 1935-4657.
- ^ Hamburger C (1952). "17-Ketosteroid Excretion and Modes of Administering Testosterone Preparations". Ciba Foundation Symposium - Steroid Hormone Administration (Book II of Colloquia on Endocrinology, Vol. 3). Novartis Foundation Symposia. pp. 304–322. doi:10.1002/9780470715154.ch7. ISBN 9780470715154. ISSN 1935-4657.
- ^ Hamburger C (1949). "Testosterone treatment and 17-ketosteroid excretion; administration of testosterone propionate, emulsified in water". Acta Endocrinologica. 3 (2): 119–28, illust. doi:10.1530/acta.0.0030119. PMID 15397391.
- ^ Eversole WJ, Leathem JH, Schraer H (December 1950). "Testosterone preparations with prolonged activity". Endocrinology. 47 (6): 448–53. doi:10.1210/endo-47-6-448. PMID 14802345.
- ^ Hamburger C, Birket-Smith E, Kaee S (January 1952). "Testosterone treatment and 17-ketosteroid excretion. III. Comparison of the time of absorption and excretion of testosterone propionate, testosterone-iso-butyrate, and testosterone-n-valerate". Acta Endocrinologica. 9 (1): 79–98. doi:10.1530/acta.0.0090079. PMID 14932696.
- ^ Hamburger C (August 1956). "Testosterone treatment and 17-ketosteroid excretion. IV. Administration of testosterone beta-cyclopentylpropionate, testosterone furanate, and testosterone oenanthate". Acta Endocrinologica. 22 (4): 379–89. doi:10.1530/acta.0.0220379. PMID 13354228.
- ^ Josef Kimmig (14 March 2013). Therapie der Haut- und Geschlechtskrankheiten. Springer-Verlag. pp. 508–. ISBN 978-3-642-94850-3.
- ^ Arthur Jores; Henryk Nowakowski (1960). Praktische Endokrinologie. G. Thieme. p. 295.
- ^ Von Numers C (1951). "Simultaneous treatment of secondary amenorrhoea with oestrogen and progesterone". Acta Endocrinologica. 6 (1): 67–89. doi:10.1530/acta.0.0060067. PMID 14810456.
- ^ "Neue Spezialitäten". Klinische Wochenschrift. 36 (17): 833. 1958. doi:10.1007/BF01481957. ISSN 0023-2173. S2CID 42166026.
- ^ Tobías GM, Usabiaga RA, Riaño JD, Espinoza AB, Tovar SR, Martínez ER (2008). "Progesterona en Microesferas para el Tratamiento en Infertilidad" (PDF). Acta Médica Grupo Ángeles. 6 (1): 8.
- ^ Tobías GM, Martínez ER (2009). "Técnica para Aplicación de Fármacos con Microesferas en Suspensión" (PDF). Acta Médica Grupo Ángeles. 7 (1): 13.
- ^ "Juvenum (estradiol/progesterone) - Medicamentos PLM". Medicamentos PLM. Archived from the original on 2018-09-18. Retrieved 2018-09-17.
- ^ "Estradiol/Progesterone injection - Laboratorios Carnot - AdisInsight".
- ^ https://www.drugs.com/international/juvenum.html
- ^ Cortés-Bonilla M, Alonso-Campero R, Bernardo-Escudero R, Francisco-Doce MT, Chavarín-González J, Pérez-Cuevas R, Chedraui P (October 2016). "Improvement of quality of life and menopausal symptoms in climacteric women treated with low-dose monthly parenteral formulations of non-polymeric microspheres of 17β-estradiol/progesterone". Gynecol. Endocrinol. 32 (10): 831–834. doi:10.1080/09513590.2016.1183628. PMID 27187320. S2CID 22688585.
- ^ Cortés-Bonilla M, Bernardo-Escudero R, Alonso-Campero R, Francisco-Doce MT, Hernández-Valencia M, Celis-González C, Márquez-Oñate R, Chedraui P, Uribe JA (July 2015). "Treatment of menopausal symptoms with three low-dose continuous sequential 17β-estradiol/progesterone parenteral monthly formulations using novel non-polymeric microsphere technology". Gynecol. Endocrinol. 31 (7): 552–9. doi:10.3109/09513590.2015.1019853. PMC 4776687. PMID 26062108.
- ^ Toppozada MK (April 1994). "Existing once-a-month combined injectable contraceptives". Contraception. 49 (4): 293–301. doi:10.1016/0010-7824(94)90029-9. PMID 8013216.
- ^ Garza-Flores J (April 1994). "Pharmacokinetics of once-a-month injectable contraceptives". Contraception. 49 (4): 347–59. doi:10.1016/0010-7824(94)90032-9. PMID 8013219.
- ^ Bagade O, Pawar V, Patel R, Patel B, Awasarkar V, Diwate S (2014). "Increasing use of long-acting reversible contraception: safe, reliable, and cost-effective birth control" (PDF). World J Pharm Pharm Sci. 3 (10): 364–392. ISSN 2278-4357. Archived from the original (PDF) on 2017-08-10. Retrieved 2019-05-19.
- ^ Newton JR, D'arcangues C, Hall PE (1994). "A review of "once-a-month" combined injectable contraceptives". J Obstet Gynaecol (Lahore). 4 Suppl 1: S1–34. doi:10.3109/01443619409027641. PMID 12290848.
- ^ Garza-Flores J, Fatinikun T, Hernandez L, Ramos I, Cardenas M, Menjivar M (July 1991). "A pilot study on the assessment of a progesterone/estradiol sustained release as once-a-month-injectable contraceptive". Contraception. 44 (1): 45–59. doi:10.1016/0010-7824(91)90105-O. PMID 1893701.
- ^ Garza-Flores J, Hall PE, Perez-Palacios G (1991). "Long-acting hormonal contraceptives for women". J. Steroid Biochem. Mol. Biol. 40 (4–6): 697–704. doi:10.1016/0960-0760(91)90293-E. PMID 1958567. S2CID 26021562.
- ^ Lockwood G, Griesinger G, Cometti B (2014). "Subcutaneous progesterone versus vaginal progesterone gel for luteal phase support in in vitro fertilization: a noninferiority randomized controlled study". Fertil. Steril. 101 (1): 112–119.e3. doi:10.1016/j.fertnstert.2013.09.010. PMID 24140033.
- ^ a b c Baker VL, Jones CA, Doody K, Foulk R, Yee B, Adamson GD, Cometti B, DeVane G, Hubert G, Trevisan S, Hoehler F, Jones C, Soules M (2014). "A randomized, controlled trial comparing the efficacy and safety of aqueous subcutaneous progesterone with vaginal progesterone for luteal phase support of in vitro fertilization". Hum. Reprod. 29 (10): 2212–20. doi:10.1093/humrep/deu194. PMC 4164149. PMID 25100106.
- ^ a b c Croxatto, Horacio B.; Diaz, Soledad; Peralta, Octavio; Juez, Gabriela; Herreros, Carmen; Casado, Maria-Eugenia; Salvatierra, Ana-Maria; Miranda, Patricia (1984). "Subdermal Progesterone Implants for Fertility Regulation in Nursing Women". In Zatuchni, Gerald I.; Goldsmith, Alfredo; Shelton, James D.; Sciarra, John J. (eds.). Long-Acting Contraceptive Delivery Systems: Proceedings of an International Workshop on Long-Acting Contraceptive Delivery Systems, May 31-June 3, 1983, New Orleans, Louisiana. Philadelphia: Harper & Row. pp. 543–549. ISBN 978-0-06-142905-7. OCLC 1022572860.
- ^ Kimmig J (1962). Therapie der Haut- und Geschlechtskrankheiten. Springer-Verlag. pp. 507–. ISBN 978-3-642-94850-3.
- ^ Lobo RA, Kelsey J, Marcus R (22 May 2000). Menopause: Biology and Pathobiology. Academic Press. pp. 619–. ISBN 978-0-08-053620-0.
- ^ Pinkerton JV, Pickar JH (February 2016). "Update on medical and regulatory issues pertaining to compounded and FDA-approved drugs, including hormone therapy". Menopause. 23 (2): 215–23. doi:10.1097/GME.0000000000000523. PMC 4927324. PMID 26418479.
- ^ Santoro N, Braunstein GD, Butts CL, Martin KA, McDermott M, Pinkerton JV (April 2016). "Compounded Bioidentical Hormones in Endocrinology Practice: An Endocrine Society Scientific Statement". J. Clin. Endocrinol. Metab. 101 (4): 1318–43. doi:10.1210/jc.2016-1271. PMID 27032319.
- ^ Pinkerton JV (December 2014). "What are the concerns about custom-compounded "bioidentical" hormone therapy?". Menopause. 21 (12): 1298–300. doi:10.1097/GME.0000000000000376. PMID 25387347.
- ^ Mishell DR (1941). "A clinical study of progesterone therapy by pellet implantation". American Journal of Obstetrics and Gynecology. 41 (4): 687–693. doi:10.1016/S0002-9378(41)90665-8. ISSN 0002-9378.
- ^ Bishop PM (1944). "Endocrine Therapy in Gynaecology and Obstetrics". BJOG: An International Journal of Obstetrics and Gynaecology. 51 (1): 51–63. doi:10.1111/j.1471-0528.1944.tb07317.x. ISSN 1470-0328. S2CID 71319436.
- ^ Foss GL (1943). "Implantation of Sex Hormone Tablets in Man". British Medical Bulletin. 1 (2): 21–22. doi:10.1093/oxfordjournals.bmb.a070135. ISSN 1471-8391.
- ^ Greenblatt RB, Hair LQ (1945). "Absorption of Pellets of Progesterone". The Journal of Clinical Endocrinology & Metabolism. 5 (1): 38–39. doi:10.1210/jcem-5-1-38.
- ^ Greenblatt RB, Suran RR (February 1949). "Indications for hormonal pellets in the therapy of endocrine and gynecic disorders". Am. J. Obstet. Gynecol. 57 (2): 294–301. doi:10.1016/0002-9378(49)90429-9. PMID 18123090.
- ^ Bishop PM, Richards NA, Doll R (July 1950). "Habitual abortion; prophylactic value of progesterone pellet implantation". Br Med J. 2 (4671): 130–3. doi:10.1136/bmj.2.4671.130. PMC 2038208. PMID 15434335.
- ^ Bishop PM, Folley SJ (August 1951). "Absorption of hormone implants in man". Lancet. 2 (6676): 229–32. doi:10.1016/S0140-6736(51)93237-0. PMID 14862159.
- ^ Bishop PM, Richards NA (February 1952). "Habitual abortion; further observations on the prophylactic value of progesterone pellet implantation". Br Med J. 1 (4752): 244–6. doi:10.1136/bmj.1.4752.244. PMC 2022587. PMID 14896102.
- ^ Scow RO, Ebling FJ, Henderson IW (1973). Endocrinology: Proceedings of the Fourth International Congress of Endocrinology, Washington, D.C., June 18-24, 1972. Excerpta Medica. p. 978. ISBN 978-90-219-0166-4.
Subdermal implants. Another way to obtain prolonged activity is by using subcutaneous implants made by compressing crystalline hormones. However, progesterone pellets are poorly tolerated and sterile abscesses or extrusion may occur in about 15—20% of cases (Greenblatt, personal communication, 1969). For this reason it appears that implants made of pure progestational steroids have little chance of finding a place in contraceptive therapy. [...]
- ^ Croxatto HB, Díaz S (1987). "The place of progesterone in human contraception". J. Steroid Biochem. 27 (4–6): 991–4. doi:10.1016/0022-4731(87)90179-8. PMID 3320572.
- ^ a b Shaaban MM (1991). "Contraception with progestogens and progesterone during lactation". J. Steroid Biochem. Mol. Biol. 40 (4–6): 705–10. doi:10.1016/0960-0760(91)90294-F. PMID 1835650. S2CID 25152238.
- ^ a b Croxatto HB, Díaz S, Peralta O, Juez G, Casado ME, Salvatierra AM, Durán E (September 1982). "Fertility regulation in nursing women. II. Comparative performance of progesterone implants versus placebo and copper T". Am. J. Obstet. Gynecol. 144 (2): 201–8. doi:10.1016/0002-9378(82)90628-7. PMID 7114130.
- ^ a b Díaz S, Peralta O, Juez G, Herreros C, Casado ME, Salvatierra AM, Miranda P, Croxatto HB (October 1984). "Fertility regulation in nursing women. VI. Contraceptive effectiveness of a subdermal progesterone implant". Contraception. 30 (4): 311–25. doi:10.1016/S0010-7824(84)80023-2. PMID 6509984.
- ^ Mannino CA, South SM, Inturrisi CE, Quinones-Jenab V (December 2005). "Pharmacokinetics and effects of 17beta-estradiol and progesterone implants in ovariectomized rats". J Pain. 6 (12): 809–16. doi:10.1016/j.jpain.2005.07.007. PMID 16326369.
- ^ a b Benagiano G, Gabelnick H, Farris M (September 2008). "Contraceptive devices: subcutaneous delivery systems". Expert Rev Med Devices. 5 (5): 623–37. doi:10.1586/17434440.5.5.623. PMID 18803473. S2CID 207201811.
- ^ a b Freeman S, Shulman LP (February 2010). "Considerations for the use of progestin-only contraceptives". Journal of the American Academy of Nurse Practitioners. 22 (2): 81–91. doi:10.1111/j.1745-7599.2009.00473.x. PMID 20132366. S2CID 36724865.
- ^ a b c d Falcone T, Hurd WW (1 January 2007). Clinical Reproductive Medicine and Surgery. Elsevier Health Sciences. pp. 406–. ISBN 978-0-323-03309-1.
- ^ a b Sloane E (2002). Biology of Women. Cengage Learning. pp. 445–. ISBN 0-7668-1142-5.
- ^ Aiken AR, Trussell J (2014). "Recent advances in contraception". F1000Prime Rep. 6: 113. doi:10.12703/P6-113. PMC 4251416. PMID 25580267.
- ^ Lobo RA (5 June 2007). Treatment of the Postmenopausal Woman: Basic and Clinical Aspects. Elsevier. pp. 210–. ISBN 978-0-08-055309-2.
- ^ Sitruk-Ware R, Bricaire C, De Lignieres B, Yaneva H, Mauvais-Jarvis P (October 1987). "Oral micronized progesterone. Bioavailability pharmacokinetics, pharmacological and therapeutic implications--a review". Contraception. 36 (4): 373–402. doi:10.1016/0010-7824(87)90088-6. PMID 3327648.
- ^ a b Simon JA (December 1995). "Micronized progesterone: vaginal and oral uses". Clinical Obstetrics and Gynecology. 38 (4): 902–14. doi:10.1097/00003081-199538040-00024. PMID 8616985.
- ^ Stanczyk FZ, Hapgood JP, Winer S, Mishell DR (April 2013). "Progestogens used in postmenopausal hormone therapy: differences in their pharmacological properties, intracellular actions, and clinical effects". Endocr. Rev. 34 (2): 171–208. doi:10.1210/er.2012-1008. PMC 3610676. PMID 23238854.
- ^ Aufrère MB, Benson H (June 1976). "Progesterone: an overview and recent advances". Journal of Pharmaceutical Sciences. 65 (6): 783–800. doi:10.1002/jps.2600650602. PMID 945344.
추가 읽기
- Langecker H (1968). "Resorption, Verteilung und Ausscheidung der Gestagene" [Absorption, Distribution, and Excretion of Progestogens]. Die Gestagene [The Progestogens]. Springer-Verlag. pp. 264–351. doi:10.1007/978-3-642-99941-3_3. ISBN 978-3-642-99941-3.
- Sitruk-Ware R, Bricaire C, De Lignieres B, Yaneva H, Mauvais-Jarvis P (October 1987). "Oral micronized progesterone. Bioavailability pharmacokinetics, pharmacological and therapeutic implications--a review". Contraception. 36 (4): 373–402. doi:10.1016/0010-7824(87)90088-6. PMID 3327648.
- Simon JA (December 1995). "Micronized progesterone: vaginal and oral uses". Clinical Obstetrics and Gynecology. 38 (4): 902–14. doi:10.1097/00003081-199538040-00024. PMID 8616985.
- Ruan X, Mueck AO (November 2014). "Systemic progesterone therapy--oral, vaginal, injections and even transdermal?". Maturitas. 79 (3): 248–55. doi:10.1016/j.maturitas.2014.07.009. PMID 25113944.