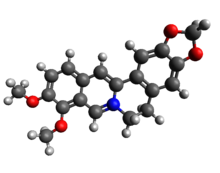
베르베린
Berberine | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 9,10-Dimethoxy-7,8,13,13a-tetradehydro-2′H-[1,3]dioxolo[4′,5′:2,3]berbin-7-ium | |
| 체계적 IUPAC 이름 9,10-Dimethoxy-5,6-dihydro-2H-7λ5-[1,3]dioxolo[4,5-g]isoquinolino[3,2-a]isoquinolin-7-ylium[2] | |
| 기타이름 | |
| 식별자 | |
3D 모델(Jsmol) | |
| 3570374 | |
| ChEBI | |
| CHEMBL | |
| 켐스파이더 | |
| 드럭뱅크 | |
| ECHA 인포카드 | 100.016.572 |
| EC 번호 |
|
| KEGG | |
펍켐 CID | |
| 유니아이 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C20H18NO4+ | |
| 어금니 질량 | 336.366 g·mol−1 |
| 외모 | 노란색 고체 |
| 융점 | 145 °C (293 °F; 418 K)[3] |
| 천천히 용해됨[3] | |
달리 명시된 경우를 제외하고는 표준 상태(25°C [77°F], 100kPa)에 있는 재료에 대한 데이터가 제공됩니다. | |
베르베린(Berberine)은 벤질이소퀴놀린 알칼로이드의 프로토베르베린 그룹에서 추출한 4차 암모늄 염입니다.
베르베리스는 노란색 때문에 양모, 가죽, 나무를 염색하는 데 사용되었습니다.[4] 자외선 하에서 베르베린은 강한 노란색 형광을 [5]나타내어 비만세포에서 헤파린을 염색하는 데 조직학에 유용합니다.[6] 천연 염료로서 베르베린의 색상 지수는 75160입니다.
조사.
베르베린의 특성에 대한 연구는 예비 기초 연구입니다: 일부 연구는 세포 배양 또는 동물 모델에 대해 수행되는 반면, 사람에게 베르베린의 사용을 조사하는 임상 시험은 제한적입니다.[7] 2023년 리뷰 연구에서는 베르베린이 지질 농도를 개선할 수 있다고 말했습니다.[8] 다양한 건강 상태에서 베르베린의 효과와 안전성을 제대로 평가하기 위해서는 고품질의 대규모 임상 연구가 필요한데, 기존 연구로는 신뢰할 만한 결론을 도출하기에 부족하기 때문입니다.[7]
베르베린 보충제는 미국에서 널리 구할 수 있지만, 미국 식품의약국(FDA)으로부터 특정 의료 용도에 대한 승인을 받지 못했습니다. 연구원들은 베르베린과 추정되는 건강상의 이점을 연결하는 연구는 제한적이라고 공개적으로 경고합니다. 또한 베르베린 보충제의 품질은 브랜드마다 다를 수 있습니다. 2017년에 수행된 연구에 따르면 미국에서 판매되는 15개의 다른 제품 중에서 베르베린 함량이 최소 90% 이상인 제품은 6개에 불과했습니다.[9][10]
생물학적 출처
베르베린은 Berberis bulgalis (barberry), Berberis aristata (나무 강황), Berberis thunbergii, Mahonia aquifolium (Oregon 포도), Hydrastis canadensis (goldensal), Xanthorhiza simplicissima (yellow root), Phellodendron amurense (Amur cork tree),[11] Coptis chinensis (Chinese goldthread), Tinospora cordifolia, 아르게모네 멕시카나(약귀비), 에슈콜지 캘리포니아(캘리포니아 양귀비). 베르베린은 보통 뿌리, 뿌리줄기, 줄기, 나무껍질에서 발견됩니다.[12]
생합성

알칼로이드 베르베린은 벤질테트라하이드로이소퀴놀린 시스템에서 유래된 테트라사이클릭 골격을 가지며, 추가 탄소 원자를 브릿지로 포함하는 것을 특징으로 하는 알칼로이드 베르베린. S-아데노실 메티오닌(SAM)에 의해 공급된 N-메틸기가 산화되어, 페놀기에 의해 방향족 고리로의 고리화가 일어나는 산화 과정으로서, 베르베린 가교의 형성이 합리화된다.[13]
레티쿨린은 식물에서 프로토베르베린 알칼로이드의 즉각적인 전구체입니다.[14] 베르베린은 티로신에서 유래한 알칼로이드입니다. L-DOPA와 4-하이드록시피루브산은 모두 L-티로신에서 유래합니다. 생합성 경로에는 2개의 티로신 분자가 사용되지만, DOPA를 통해 테트라하이드로이소퀴놀린 고리 시스템의 페닐아민 단편만 형성되고, 나머지 탄소 원자는 4-하이드록시페닐아세트알데히드를 통해 티로신에서 나옵니다. L-DOPA는 이산화탄소를 손실하여 도파민 1을 형성합니다. 마찬가지로, 4-하이드록시피루브산도 이산화탄소를 잃어 4-하이드록시페닐아세트알데히드 2를 형성합니다. 그리고 나서 도파민 1은 4-하이드록시-페닐아세트알데히드 2와 반응하여 만니히 반응과 유사한 반응으로 (S)-노르코클라우린 3을 형성합니다. SAM에 의해 산화 및 메틸화된 후, (S)-레티쿨린 4가 생성됩니다. (S)-레티쿨린은 다른 알칼로이드의 중추적인 중간체 역할을 합니다. 그러면 3차 아민의 산화가 일어나며 5번의 미니뮴 이온이 생성됩니다. 만니치와 유사한 반응에서 페놀에 대한 오르토 위치는 친핵성이고 전자는 밀어 6을 형성합니다. 생성물 6은 케토-에놀 오토머러스화를 거쳐 (S)-스쿨러린을 형성하고 SAM에 의해 메틸화되어 (S)-테트라하이드로콜럼바민 7을 형성합니다. 생성물 7은 산화되어 오르토-메톡시페놀로부터 메틸화된 다이옥시 고리를 형성합니다. O-2, NADPH- 및 시토크롬 P450-의존성 효소를 통해 (S)-카나딘 8을 생성하고, (S)-카나딘을 산화시켜 베르베린의 4차 이소퀴놀리늄 시스템을 생성하는 것을 특징으로 하는 효소. 이것은 분자 산소를 필요로 하는 두 개의 개별 산화 단계에서 발생하며, 연속적인 과정에서 HO와22 HO가2 생성됩니다.[15]
참고문헌
- ^ a b c 머크 지수, 14번째, 1154. 베르베린
- ^ IUPAC Chemical Nomenclature and Structure Representation Division (2013). "P-73.3.1". In Favre HA, Powell WH (eds.). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. IUPAC–RSC. ISBN 978-0-85404-182-4.
- ^ a b 머크 지수, 제10판 (1983), p.165, Rahway: 머크앤코
- ^ Gulrajani ML (2001). "Present status of natural dyes". Indian Journal of Fibre & Textile Research. 26: 191–201 – via NISCAIR Online Periodicals Repository.
- ^ Weiß D (2008). "Fluoreszenzfarbstoffe in der Natur" (in German). Retrieved 17 July 2009.
- ^ "B3251 Berberine chloride form". Sigma-Aldrich. 2013. Retrieved 2 Aug 2013.
- ^ a b Song D, Hao J, Fan D (October 2020). "Biological properties and clinical applications of berberine". Front Med. 14 (5): 564–582. doi:10.1007/s11684-019-0724-6. PMID 32335802. S2CID 216111561.
- ^ Hernandez AV, Hwang J, Nasreen I, et al. (2023). "Impact of Berberine or Berberine Combination Products on Lipoprotein, Triglyceride and Biological Safety Marker Concentrations in Patients with Hyperlipidemia: A Systematic Review and Meta-Analysis". J Diet Suppl: 1–18. doi:10.1080/19390211.2023.2212762. PMID 37183391. S2CID 258687419.
- ^ Funk RS, Singh RK, Winefield RD, Kandel SE, Ruisinger JF, Moriarty PM, Backes JM (May 2018). "Variability in Potency Among Commercial Preparations of Berberine". J Diet Suppl. 15 (3): 343–351. doi:10.1080/19390211.2017.1347227. PMC 5807210. PMID 28792254.
- ^ Subbaraman N (14 June 2023). "The Cheaper Weight-Loss Alternative Riding the Ozempic Wave". Wall Street Journal.
- ^ Cicero AF, Baggioni A (2016). "Berberine and Its Role in Chronic Disease". Advances in Experimental Medicine and Biology. Vol. 928. Cham: Springer International Publishing. pp. 27–45. doi:10.1007/978-3-319-41334-1_2. ISBN 978-3-319-41332-7. ISSN 0065-2598. PMID 27671811.
- ^ "Berberine". PubChem, National Library of Medicine, US National Institutes of Health. March 9, 2020. Retrieved March 10, 2020.
- ^ Dewick P (2009). Medicinal Natural Products: A Biosynthetic Approach (3rd ed.). West Sussex, England: Wiley. p. 357. ISBN 978-0-471-49641-0.
- ^ Park SU, Facchini PJ (June 2000). "Agrobacterium rhizogenes-mediated transformation of opium poppy, Papaver somniferum l., and California poppy, Eschscholzia californica cham., root cultures". Journal of Experimental Botany. 51 (347): 1005–16. doi:10.1093/jexbot/51.347.1005. PMID 10948228.
- ^ Dewick P (2009). Medicinal Natural Products: A Biosynthetic Approach (3rd ed.). West Sussex, England: Wiley. p. 358. ISBN 978-0-471-49641-0.


