모르핀
Morphine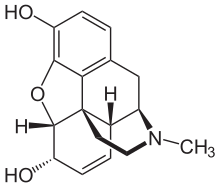 | |
 | |
| 임상 데이터 | |
|---|---|
| 발음 | /mo(rfi)n/ |
| 상호 | Statex, MS Continue, MST Continue, Oramorph, Sevredol[1] 등 |
| AHFS/Drugs.com | 모노그래프 |
| 임신 카테고리 |
|
| 의존성 책임 | 높은 |
| 중독 책임 | 높다[3] |
| 루트 행정부. | 흡입(흡연), 흡입(흡연), 구강(PO), 직장, 피하(SC), 근육내(IM), 정맥내(IV), 경막외(경막외), 경막외(IT) |
| 약물 클래스 | 오피오이드 |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 | |
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 20~40%(입에 의한), 36~71%(직접),[4] 100%(IV/IM) |
| 단백질 결합 | 30–40% |
| 대사 | 간 90 % |
| 조치의 개시 | 5분(IV), 15분(IM),[5] 20분(PO)[6] |
| 반감기 제거 | 2~3시간 |
| 작업 기간 | 3~7시간[7][8] |
| 배설물 | 신장 90%, 담도 10% |
| 식별자 | |
| |
| CAS 번호 |
|
| PubChem CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| PDB배위자 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.000.291 |
| 화학 및 물리 데이터 | |
| 공식 | C17H19NO3 |
| 몰 질량 | 285.343g/120−1 |
| 3D 모델(JSmol) | |
| 물에 녹는 정도 | HCl & Sulf.: 60 mg/mL (20 °C) |
| |
| |
| (표준) | |
모르핀은 아편에서 자연적으로 발견되는 아편 계열의 진통제입니다. 아편은 양귀비에 들어있는 암갈색 수지입니다.모르핀을 투여하기 위해 사용되는 방법은 구강; 설하; 흡입; 근육에 주사; 피부 밑 주사; 정맥 주사; 척수 주변 공간에 주사; 경피; 또는 직장 [7][9]좌약을 통한 많은 방법이 있습니다.그것은 진통을 유도하고 통증에 대한 지각과 감정 반응을 변화시키기 위해 중추신경계에 직접 작용한다.신체적, 심리적 의존성과 내성은 반복 [7]투여에 의해 발달할 수 있다.급성통증과 만성통증에 모두 복용할 수 있으며 심근경색, 신장결석, [7]진통 중 통증에 자주 사용됩니다.최대 효과는 정맥 내 투여 시 약 20분, 구강 내 투여 시 약 60분 후에 나타나며, 효과는 3~7시간이다.[7][8]모르핀의 장기 작용 제제는 MS-Continue, Kadian 및 기타 브랜드 이름뿐만 아니라 일반적으로도 [7]사용할 수 있습니다.
모르핀의 잠재적으로 심각한 부작용은 호흡 노력의 감소, 구토, 메스꺼움, 그리고 [7]저혈압을 포함한다.모르핀은 중독성이 있고 [7]남용되기 쉽다.장기 복용 후 복용량이 줄어들면 오피오이드 금단 증상이 나타날 [7]수 있다.모르핀의 일반적인 부작용에는 졸음, 구토, [7]변비가 포함된다.임신 중 또는 모유 수유 중 모르핀을 사용할 경우 [7][2]아기의 건강에 영향을 미칠 수 있으므로 주의하시기 바랍니다.
모르핀은 1803년과 1805년 사이에 독일의 약사 프리드리히 세르튀르너에 [10]의해 처음 분리되었다.이것은 일반적으로 [11]식물에서 유효성분의 첫 번째 분리라고 여겨진다.Merck는 1827년에 [10]그것을 상업적으로 판매하기 시작했다.모르핀은 1853-1855년 [10][12]피하 주사기의 발명 이후 더 널리 사용되었습니다.세르튀르너는 원래 [12][13]수면의 원인이 되는 성질을 가지고 있기 때문에 그리스 꿈의 신 모페우스의 이름을 따서 모르피움이라는 물질 이름을 지었다.
모르핀의 주요 공급원은 양귀비의 [14]양귀비 빨대로부터 격리하는 것이다.2013년에는 약 523톤의 모르핀이 [15]생산되었다.약 45톤이 통증에 직접 사용되었는데, 이는 지난 20년간 [15]400% 증가한 수치입니다.이 목적을 위한 대부분의 용도는 [15]선진국에서 사용되었습니다.모르핀의 약 70%는 하이드로모르폰, 옥시모르폰,[15][16][17] 헤로인과 같은 다른 오피오이드를 만드는데 사용된다.미국에서는 [16]Schedule II,[18] 영국에서는 Class [19]A, 캐나다에서는 Schedule I이다.그것은 세계보건기구의 필수 [20]의약품 목록에 있다.모르핀은 많은 상표명으로 [1]판매된다.2019년, 300만 건 이상의 [21][22]처방으로 미국에서 163번째로 많이 처방된 의약품이었다.
의료 용도
고통
모르핀은 주로 급성 및 만성적인 극심한 통증을 치료하는데 사용된다.진통제 지속시간은 약 [7][8]3시간에서 7시간이다.메스꺼움과 변비의 부작용은 치료를 중단할 만큼 심각한 경우는 드물다.
심근경색으로 인한 통증이나 진통 [23]등에 사용합니다.그러나 모르핀이 비 ST 상승 [24]심근경색의 경우 사망률을 높일 수 있다는 우려가 있다.모르핀은 또한 전통적으로 급성 [23]폐부종의 치료에 사용되어 왔다.그러나 2006년 리뷰에서는 이 [25]관행을 뒷받침하는 증거가 거의 발견되지 않았다.2016년 코크란 리뷰는 모르핀이 암 [26]통증 완화에 효과적이라는 결론을 내렸다.
숨이 차다
모르핀은 암과 비암으로 [27][28]인한 호흡곤란 증상을 줄이는데 효과적이다.호흡곤란이 정지 상태이거나 진행 중인 암이나 말기 심폐 질환과 같은 조건에서 최소한의 노력으로 호흡곤란을 일으킬 때, 정기적인 저선량 지속형 모르핀은 시간이 [29][30]지남에 따라 그 장점이 유지되면서 안전하게 호흡곤란을 감소시킨다.
오피오이드 사용 장애
모르핀은 또한 메타돈이나 부프레놀핀을 [31]견딜 수 없는 오피오이드 중독을 가진 사람들을 위해 오스트리아, 독일, 불가리아, 슬로베니아 및 캐나다에서 아편 대체 요법(OST)의 완발성 제제로도 이용 가능하다.
금지 사항
모르핀에 대한 상대적 금기는 다음과 같다.
부작용
- 공통 및 단기
- 다른.
변비
로페라미드와 다른 오피오이드처럼 모르핀은 장내근총에 작용하여 장운동성을 감소시키고 변비를 일으킨다.모르핀의 위장 효과는 주로 장의 μ-오피오이드 수용체에 의해 매개된다.모르핀은 위가 배출되는 것을 억제하고 장의 촉진성 연동기를 감소시킴으로써 장의 통과 속도를 감소시킨다.장내 분비 감소와 장내 수분 흡수 증가도 변비 효과에 기여한다.오피오이드는 또한 일산화질소 [34]생성 억제 후 강장성 장경련을 통해 간접적으로 장에 작용할 수 있다.이 효과는 일산화질소 전구체인 L-arginine이 장 운동성의 [35]모르핀 유도 변화를 역전시켰을 때 동물에서 나타났다.
호르몬 불균형
임상 연구들은 모르핀이 다른 오피오이드와 마찬가지로 종종 남녀의 만성 사용자에게 저고나디즘과 호르몬 불균형을 일으킨다는 결론을 일관되게 내리고 있다.이 부작용은 용량에 따라 다르며 치료 및 레크리에이션 사용자 모두에서 발생한다.모르핀은 황체화 호르몬의 수치를 억제함으로써 여성의 생리를 방해할 수 있다.많은 연구들은 만성 오피오이드 사용자의 대부분(아마도 90%)이 오피오이드 유도성 저고나디즘을 가지고 있다고 시사한다.이 효과는 만성 모르핀 사용자에게서 관찰되는 골다공증 및 골절의 증가 가능성을 유발할 수 있습니다.연구결과에 따르면 그 효과는 일시적이다.2013년 현재[update], 모르핀의 저용량 또는 급성 사용이 내분비계에 미치는 영향은 [36][37]명확하지 않다.
인간 성과에 미치는 영향
대부분의 리뷰는 오피오이드가 감각, 운동 또는 주의력 테스트에서 인간 수행에 최소한의 손상을 발생시킨다고 결론지었다.하지만, 최근의 연구들은 모르핀이 중추신경계 억제제라는 것을 고려할 때, 모르핀에 의해 야기된 몇몇 장애를 보여줄 수 있었다.모르핀은 임계 깜박임 빈도(전체 CNS 각성의 측정치)의 기능 저하와 Maddox 날개 테스트(눈의 시각 축의 편차 측정치)의 성능 저하를 초래했다.모르핀이 운동 능력에 미치는 영향을 조사한 연구는 거의 없지만, 모르핀의 높은 복용량은 손가락 두드리기를 손상시킬 수 있고 등각력(즉, 미세 운동 제어가 손상됨)의 낮은 [38]일정 수준을 유지하는 능력을 손상시킬 수 있다(즉, 모르핀과 총 운동 능력 사이의 상관관계를 보여주는 연구는 없다.
인지 능력의 측면에서, 한 연구는 모르핀이 전장기억과 역행 [39]기억력에 부정적인 영향을 미칠 수 있다는 것을 보여주었지만, 이러한 영향은 미미하고 일시적인 것이다.전반적으로, 비내성 피험자의 급성 오피오이드는 일부 감각 및 운동 능력, 그리고 아마도 주의력과 인지 능력에서 작은 영향을 미치는 것으로 보인다.모르핀의 효과는 만성 오피오이드 사용자보다 오피오이드 순진 피험자에서 더 두드러질 수 있다.
중증 만성 통증 관리를 위한 만성 오피오이드 진통 요법(COAT)과 같은 만성 오피오이드 사용자에서 행동 테스트는 대부분의 경우 지각, 인지, 조정 및 행동에 대한 정상적인 기능을 보여주었다.2000년[40] 한 연구에서는 COAT 환자를 분석하여 자동차를 안전하게 운전할 수 있는지 여부를 판단했습니다.이 연구의 결과는 안정적인 오피오이드 사용이 운전 고유의 능력을 크게 손상시키지 않는다는 것을 시사한다(이것은 신체적, 인지적, 지각적 기술을 포함한다).COAT 환자는 성공적인 수행을 위해 응답 속도를 요구하는 작업(예: 레이 복합 그림 테스트)을 신속하게 완료했지만 대조군보다 더 많은 오류를 범했다.COAT 환자는 (WAIS-R 블록 설계 테스트에 나타난 바와 같이) 시각 공간 지각 및 조직에는 결함이 없었지만 (레이 복합 그림 테스트 – 리콜에 나타난 바와 같이) 즉시 및 단기 시각 기억력이 손상되었다.이러한 환자들은 고차 인지 능력(즉, 계획)에서 장애를 보이지 않았다.COAT 환자는 지침을 따르는 데 어려움을 겪고 충동적인 행동을 하는 경향을 보였지만, 이는 통계적으로 유의하지 않았다.이 연구는 COAT 환자에게 도메인 특이적 결손이 없음을 밝혀주며, 이는 만성 오피오이드 사용이 정신운동, 인지 또는 신경심리학적 기능에 작은 영향을 미친다는 개념을 뒷받침한다.
보강 장애
중독

모르핀은 중독성이 강한 물질이다.이전에 아편제에 중독된 사람들의 헤로인과 모르핀의 생리적, 주관적 효과를 비교한 대조 연구에서, 피실험자들은 다른 약보다 한 가지 약물에 대한 선호도를 보이지 않았다.등기능, 주입된 선량은 피험자의 행복감, 야망, 신경과민, 이완, 졸음, [41]졸음 등의 자기평가된 느낌에 차이가 없이 비슷한 행동 과정을 거쳤다.같은 연구자들에 의한 단기 중독 연구는 내성이 헤로인과 모르핀 둘 다와 비슷한 속도로 발달한다는 것을 증명했다.오피오이드 하이드로몰폰, 펜타닐, 옥시코돈, 페티딘/메페리딘과 비교했을 때, 이전의 중독자들은 헤로인과 모르핀에 대한 강한 선호도를 보여 헤로인과 모르핀이 특히 남용과 중독에 취약하다는 것을 시사했다.모르핀과 헤로인은 또한 이러한 다른 [41]오피오이드들에 비해 행복감과 다른 긍정적인 주관적인 효과를 낼 가능성이 훨씬 더 높았다.이전의 약물 중독자들이 다른 오피오이드보다 헤로인과 모르핀을 선택하는 것은 헤로인(모핀 디아세트산, 디아모르핀 또는 디아세틸 모르핀으로도 알려져 있음)이 모르핀과 모르핀 프로드러그의 에스테르이기 때문에 본질적으로 그들이 생체 내에서 동일한 약물임을 의미하기 때문일 수도 있다.헤로인은 뇌와 척수의 오피오이드 수용체에 결합하기 전에 모르핀으로 전환되는데, 여기서 모르핀은 중독된 사람들이 추구하는 [42]주관적인 효과를 일으킨다.
공차
여러 가설이 어떻게 관용을 개발하고, 오피오이드 수용체 인산화(는 수용기 모양을 바꿀 것이다), 수용체의 G-proteins에서 기능별 해결(수용체탈 민감성에)[43]μ-opioid 수용체 내면화 또는 수용체 down-regulation(사용 가능한 감각 기관의 수를 줄이는 f. 등이 주어진다또는 m작용하기 위한 오르핀) 및 cAMP 경로(오피오이드 효과에 대한 역조절 메커니즘)의 상향 조절(이러한 과정의 검토는 코흐 및 홀트 참조).[44]CCK는 오피오이드 내성을 담당하는 일부 역조절 경로를 중재할 수 있다.CCK 항고제, 특히 프로글루미드는 모르핀에 대한 내성의 발달을 늦추는 것으로 나타났다.
의존과 탈퇴
모르핀 투여 중단은 바르비투르산염, 벤조디아제핀, 알코올 또는 진정제-최고혈압제와는 달리 건강한 사람에게는 그 자체로 치명적이지 않은 원형 오피오이드 금단증후군을 일으킨다.
급성 모르핀 금단은 다른 오피오이드와 함께 여러 단계를 거친다.다른 오피오이드들은 각각의 강도와 길이가 다르며, 약한 오피오이드와 혼합작용제-안타고니스트는 최고 수준에 이르지 않는 급성 이탈 증후군을 가질 수 있다.일반적으로[by whom?] 인용되는 것은 다음과 같습니다.
- 1단계, 마지막 투여 후 6시간~14시간: 약물 갈망, 불안, 과민성, 발한, 경미하고 중간 정도의 디스포리아
- 단계 II, 마지막 선량 후 14시간 ~ 18시간:하품, 진땀, 가벼운 우울증, 눈물, 울음, 두통, 콧물, 소화불량, 상기 증상의 격화, '엔수면'(깨어있는 무아지경)
- 단계 III, 마지막 선량 후 16시간 ~ 24시간:콧물(콧물)과 위의 다른 것들의 증가, 동공 확장, 필로 교정(소름 - '감기 칠면조'라는 문구의 유래로 알려져 있지만, 사실은 그 문구는 약물 [45]치료 이외의 것으로 알려져 있음), 근육통, 홍조, 냉증, 뼈와 근육통, 식욕부진, 그리고 장경련의 시작
- 단계 IV, 마지막 투여 후 24시간 ~ 36시간:심한 경련과 비자발적인 다리 움직임("안절부절못하는 다리 증후군"이라고도 함), 느슨한 변, 불면증, 혈압 상승, 체온 상승, 호흡 및 조수량 증가, 빈맥(맥박 상승), 불안, 메스꺼움 등 위의 모든 증상 증가
- 마지막 투여 후 36시간 ~ 72시간 후 V단계:위의 증가, 태아 위치, 구토, 자유롭고 빈번한 액체 설사, 때때로 음식물의 입에서 체외로 전달 시간을 앞당길 수 있음, 24시간당 2kg에서 5kg의 체중 감소, 백혈구 수 증가 및 기타 혈액 변화
- 스테이지 VI, 상기의 완료 후:식욕과 정상적인 장 기능의 회복, 주로 심리적인 증상이지만 통증, 고혈압, 대장염 또는 운동성과 관련된 다른 위장 질환에 대한 민감성 증가, 그리고 어느 방향의 체중 조절 문제를 포함할 수 있다.
금단 단계에서는 일부 환자에서 초음파상 췌장염의 증거가 입증되었으며 아마도 [46]Oddi의 췌장 괄약근 경련에 기인한 것으로 추정된다.
모르핀 중독과 관련된 금단 증상은 보통 다음 예정된 투여 시간 직전에, 때로는 마지막 투여 후 몇 시간 이내에 (보통 6시간에서 12시간까지) 경험된다.초기 증상에는 눈물, 불면증, 설사, 콧물, 하품, 소화불량, 땀, 그리고 어떤 경우에는 강한 약물 욕구가 포함된다.심각한 두통, 초조함, 과민성, 식욕부진, 몸살, 심한 복통, 메스꺼움과 구토, 떨림, 그리고 심지어 더 강렬하고 강한 약물 욕구가 증후군이 진행됨에 따라 나타난다.심한 우울증과 구토는 매우 흔하다.급성 금단 기간 동안, 수축기 및 확장기 혈압은 보통 프리모르핀 수치를 넘어 증가하며, 심장 박동수는 [47]심장 마비, 혈전 또는 뇌졸중을 일으킬 수 있습니다.
소름이 돋는 오한이나 냉기가 홍조(핫플래시), 발차기 동작([42]습관을 깨는 것), 과도한 땀 흘리는 것 등도 [48]특징적인 증상이다.등과 사지의 뼈와 근육에 심한 통증이 나타나며 근육 경련도 일어난다.이 과정 중 어느 시점에서든 금단 증상을 극적으로 반전시키는 적절한 마취제를 투여할 수 있습니다.주요 금단 증상은 마지막 투여 후 48시간에서 96시간 사이에 최고조에 달하고 약 8일에서 12일 후에 가라앉는다.건강이 좋지 않은 의존도가 높은 사용자가 갑자기 탈퇴하는 경우는 거의 없습니다.모르핀 금단술은 알코올, 바르비투르산염 또는 벤조디아제핀 [49][50]금단술보다 덜 위험한 것으로 간주된다.
모르핀 중독과 관련된 심리적 의존은 복잡하고 오래 간다.모르핀에 대한 신체적 요구가 지나간 지 오래 후에, 중독자는 보통 모르핀의 사용에 대해 계속 생각하고 이야기하며 모르핀의 영향을 받지 않고 일상 활동에 대처하는 것이 이상하거나 압도감을 느낄 것이다.모르핀의 심리적 금지는 보통 매우 길고 고통스러운 과정이다.중독자들은 종종 심각한 우울증, 불안, 불면증, 기분 변화, 기억상실, 낮은 자존감, 혼란, 편집증, 그리고 다른 심리적 장애를 겪는다.개입이 없으면 증후군은 서서히 진행되며 심리적 의존을 포함해 7~10일 안에 증상이 대부분 사라진다.모르핀 금단 후 신체적 환경이나 남용의 원인이 된 행동 동기가 변경되지 않았을 때 재발 가능성이 높다.모르핀의 중독성과 강화성에 대한 증거는 모르핀의 재발률이다.모르핀(및 헤로인) 남용자는 일부 [51]의학 전문가들의 추정으로는 최대 98%에 이르는 모든 약물 사용자 중 가장 높은 재발률을 가지고 있다.
독성
| 모르핀의 특성 | |||||
|---|---|---|---|---|---|
| 몰 질량[52] | 285.338 g/g | ||||
| 산도(pKa)[52] |
| ||||
| 용해성[52] | 20 °C에서 0.15 g/L | ||||
| 녹는점[52] | 255°C | ||||
| 비등점[52] | 190°C 서브라이임 | ||||
과다 복용은 [53]즉시 치료를 받지 않으면 질식사와 호흡기 우울증을 일으킬 수 있다.과다 복용 치료에는 나록손의 투여가 포함된다.후자는 모르핀의 효과를 완전히 역전시키지만, 아편 중독 피험자의 금단현상을 즉시 일으킬 수 있다.모르핀의 작용 기간이 나록손의 [54]작용 기간보다 길기 때문에 여러 개의 용량이 필요할 수 있다.
황산 모르핀과 다른 제제의 인간 LD는50 확실히 알려져 있지 않다.병사들의 모르핀 과다복용에 대한 한 저품질 연구는 치사량이 남성의 경우 0.78mcg/ml(평균 90kg 남성의 경우 약 71mg), 여성의 경우 0.98mcg/ml(평균 75kg 여성의 경우 약 74mg)로 보고되었다.선량이 경구, 비경구 또는 [55]IV인지 여부는 명시되지 않았다.실험 동물 연구는 보통 문헌에서 인용된다.심각한 약물 의존성(고내성)에서는 하루에 2000~3000mg이 [56]허용될 수 있다.
약리학
약역학
| 컴파운드 | 친화력()Ki | 비율 | 참조 | ||
|---|---|---|---|---|---|
| MOR | DOR | KOR | MOR: DOR:KOR | ||
| 모르핀 | 1.8nM | 90nM | 317nM | 1:50:176 | [57] |
| (-)-모르핀 | 1.24nM | 145nM | 23.4nM | 1:117:19 | [58] |
| (+)-모르핀 | 10μM 이상 | 100 μM 이상 | 300μM 이상 | ND | [58] |
| 컴파운드 | 경로 | 양 |
|---|---|---|
| 코데인 | PO | 200밀리그램 |
| 하이드로코돈 | PO | 20~30밀리그램 |
| 하이드로모르폰 | PO | 7.5mg |
| 하이드로모르폰 | IV | 1.5밀리그램 |
| 모르핀 | PO | 30밀리그램 |
| 모르핀 | IV | 10밀리그램 |
| 옥시코돈 | PO | 20밀리그램 |
| 옥시코돈 | IV | 10밀리그램 |
| 옥시모르폰 | PO | 10밀리그램 |
| 옥시모르폰 | IV | 1밀리그램 |
모르핀은 원형 오피오이드이며 다른 오피오이드를 [62]검사하는 표준입니다.이는 주로 μ-γ-오피오이드(Mu-Delta) 수용체 [63][64]헤테로머와 상호작용한다.μ결합 부위는 후편도체, 시상하부, 시상하부, 핵카우다투스, 창상 및 특정 피질 영역에 고밀도로 인간의 뇌에 이산적으로 분포되어 있다.그들은 또한 척수의 층 I과 II(실질적인 젤라틴) 내의 1차 구심점의 말단 축삭과 삼차 [65]신경의 척수핵에서 발견됩니다.
모르핀은 페넌트렌 오피오이드 수용체 작용제이며, 그 주효과는 중추신경계의 μ-Opioid 수용체(MOR)에 결합하고 활성화하는 것이다.MOR에서의 고유 활성은 검사 및 테스트 대상 조직에 크게 의존하며, 일부 상황에서는 완전 작용제인 반면 다른 상황에서는 부분 작용제 또는 심지어 길항제일 [66]수 있습니다.임상 환경에서 모르핀은 중추신경계와 위장관에 주요 약리학적 효과를 발휘한다.치료적 가치가 있는 주요 작용은 진통제와 진정제이다.MOR의 활성화는 진통제, 진정제, 행복감, 신체적 의존성 및 호흡저하와 관련이 있다.모르핀은 또한 γ-오피오이드 수용체(KOR)와 γ-오피오이드 수용체(DOR) 작용제이다.KOR의 활성화는 척추 진통, miosis(핀포인트 동공) 및 정신 자극 효과와 관련이 있습니다.DOR는 [65]진통제에 중요한 역할을 하는 것으로 생각된다.모르핀은 γ수용체에 결합하지 않지만, β수용체 작용제(+)-펜타조신(Pentazocine)이 모르핀 진통제를 억제하고, β수용체 길항제(β수용체 길항제)가 모르핀 [67]진통제를 증강시켜 β수용체가 모르핀 작용에 관여하는 것을 시사한다.
모르핀의 효과는 나록손 및 나르트렉손과 같은 오피오이드 수용체 길항제들로 대항할 수 있으며, 모르핀에 대한 내성은 케타민 또는 덱스트로메토르판과 [68]같은 NMDA 수용체 길항제들에 의해 억제될 수 있다.통증의 장기 치료에서 화학적으로 다른 오피오이드를 가진 모르핀의 회전은 장기적으로 내성의 성장을 늦출 것이며, 특히 레볼파놀, 케토베미돈, 피리트라미드, 메타돈과 같은 모르핀과 그 유도체와 상당히 불완전한 교차 내성을 가진 것으로 알려진 약물과 이러한 모든 약물들 또한 느려질 것이다.NMDA 길항제 특성을 가집니다.모르핀과의 교차 내성이 가장 불완전한 강한 오피오이드는 메타돈 또는 [citation needed]덱스트로모라미드인 것으로 생각된다.
유전자 발현
모르핀이 많은 유전자의 발현을 바꿀 수 있다는 연구결과가 나왔다.모르핀을 한 번 주입하면 미토콘드리아 호흡에 관여하는 단백질과 세포골격 관련 [69]단백질의 두 가지 주요 유전자 그룹의 발현을 바꾸는 것으로 나타났다.
면역 체계에 미치는 영향
모르핀은 오랫동안 중추신경계의 세포에서 발현되는 수용체에 작용하여 통증 완화와 진통을 일으키는 것으로 알려져 왔다.1970년대와 80년대에, 오피오이드 약물 중독자들이 폐렴, 결핵, 그리고 HIV/AIDS의 증가와 같은 감염의 위험을 보여준다는 증거는 과학자들이 모르핀이 면역 체계에도 영향을 미칠 수 있다고 믿게 만들었다.이러한 가능성은 면역 체계에 대한 만성 모르핀의 영향에 대한 관심을 증가시켰다.
모르핀이 면역계에 영향을 미칠 수 있다는 것을 결정하는 첫 번째 단계는 중추신경계의 세포에서 발현되는 것으로 알려진 아편 수용체가 면역계의 세포에서도 발현된다는 것을 확립하는 것이었다.한 연구는 선천적인 면역체계의 일부인 수지상 세포가 아편 수용체를 보인다는 것을 성공적으로 보여주었다.수지상 세포는 면역 체계에서 의사소통을 위한 도구인 사이토카인을 생성하는 역할을 한다.이 같은 연구는 분화 동안 모르핀으로 만성적으로 처리된 수지상세포가 T세포의 증식, 성장, 분화를 촉진하는 역할을 하는 사이토카인 인터류킨-12(IL-12)와 프로모에 관여하는 사이토카인 인터류킨-10(IL-10)을 더 적게 생산한다는 것을 보여주었다.B세포 면역 반응을 자극한다(B세포는 [70]감염을 물리치기 위해 항체를 생성한다).
사이토카인의 이러한 조절은 p38 MAPKs(미토겐 활성화 단백질 키나제) 의존 경로를 통해 일어나는 것으로 보인다.일반적으로 수지상 세포 내의 p38은 리간드 LPS(리포다당류)를 통해 활성화되는 TLR 4(톨형 수용체 4)를 발현한다.이로 인해 p38 MAPK가 인산화된다.이 인산화 작용은 p38 MAPK를 활성화하여 IL-10과 IL-12를 생성하기 시작합니다.수지상 세포가 분화 과정에서 모르핀에 만성적으로 노출되고 LPS로 처리되면 사이토카인의 생산은 달라진다.모르핀 처리 후 p38 MAPK는 IL-10을 생성하지 않고 IL-12 생성을 선호합니다.한 사이토카인의 생산이 다른 사이토카인보다 유리하게 증가하는 정확한 메커니즘은 알려져 있지 않다.모르핀은 p38 MAPK의 인산화 증가를 일으킬 가능성이 높다.IL-10과 IL-12 사이의 전사 수준 상호작용은 IL-10이 생성되지 않을 때 IL-12의 생성을 더욱 증가시킬 수 있습니다.IL-12의 생산 증가는 T세포 면역 반응을 증가시킨다.
면역 체계에 대한 모르핀의 영향에 대한 추가 연구는 모르핀이 호중구와 다른 사이토카인의 생산에 영향을 미친다는 것을 보여주었다.사이토카인은 즉각적인 면역 반응(염증)의 일부로 생성되기 때문에 통증에도 영향을 미칠 수 있다고 제안되어 왔다.이러한 방식으로, 사이토카인은 진통제 발달의 논리적 표적이 될 수 있다.최근 한 연구는 급성 면역 반응에 대한 모르핀 투여의 효과를 관찰하기 위해 동물 모델(힌드-파우 절개)을 사용했다.뒷발 절개 후 통증 임계값과 사이토카인 생성을 측정했다.일반적으로 감염과 싸우고 치료를 제어하기 위해(그리고 통증을 제어하기 위해) 상처 부위 내 및 주변의 사이토카인 생산량이 증가하지만, 절개 전 모르핀 투여(0.1mg/kg~10.0mg/kg)는 용량 의존적인 방식으로 상처 주변에서 발견되는 사이토카인의 수를 감소시켰다.저자들은 급성 부상 후 모르핀 투여가 감염에 대한 저항력을 떨어뜨리고 [71]상처의 회복을 저해할 수 있다고 제안한다.
약동학
흡수 및 대사
모르핀은 경구, 경구, 경구, 직장, 피하, 비강내, 정맥주사, 경구내 또는 표피내 및 분무기를 통해 흡입할 수 있다.레크리에이션 약물로서, 숨을 들이마시는 것이 보편화되고 있지만, 의학적인 목적으로는 정맥주사(IV)가 가장 일반적인 방법이다.모르핀은 광범위한 퍼스트패스 대사(간에서 많은 부분이 분해됨)를 거치므로 경구 복용 시 40~50%만 중추신경계에 도달한다.피하주사(SC), 근육주사(IM) 및 IV주사 후 생성된 혈장 수준은 모두 유사하다.IM 또는 SC 주입 후 모르핀 혈장 수치는 약 20분 후에 최고조에 달하고 경구 투여 후 약 30분 [72]후에 최고치에 도달한다.모르핀은 주로 간에서 대사되며 투여 후 72시간 이내에 약 87%의 모르핀이 소변으로 배출된다.모르핀은 2상 대사효소 UDP-글루쿠로노실전달효소-2B7(UGT2B7)에 의해 글루쿠로니화를 통해 모르핀-3-글루쿠로니드(M3G)와 모르핀-6-글루쿠로니드(M6G)[73]로 주로 대사된다.모르핀의 약 60%는 M3G로, 6~10%[74]는 M6G로 전환되며, 신진대사는 간뿐만 아니라 뇌와 신장에서도 이루어질 수 있습니다.M3G는 오피오이드 수용체 결합을 하지 않으며 진통제 효과가 없다.M6G는 [74]μ 수용체에 결합하고 인체에서 모르핀보다 진통제가 절반 정도 강력합니다.모르핀은 또한 소량의 노르모르핀, 코데인, 하이드로모르폰으로 대사될 수 있다.대사율은 성별, 나이, 식단, 유전자 구성, 질병 상태(있는 경우) 및 기타 약물의 사용에 따라 결정됩니다.모르핀의 제거 반감기는 약 120분이지만, 남성과 여성 사이에 약간의 차이가 있을 수 있습니다.모르핀은 지방에 저장될 수 있고, 따라서 죽은 후에도 검출될 수 있다.모르핀은 혈액-뇌 장벽을 넘을 수 있지만, 지질 용해성 저하, 단백질 결합, 글루쿠론산과의 빠른 결합 및 이온화 때문에 쉽게 교차하지 않는다.모르핀에서 파생된 헤로인은 혈액-뇌 장벽을 더 쉽게 넘고,[75] 더 강력해집니다.
확장 릴리즈
효과가 더 오래 지속되는 경구 투여 모르핀의 연장 방출 제제가 있는데, 하루에 한 번 투여할 수 있습니다.이 모르핀 제제의 브랜드명에는 [76]Avinza,[76] Kadian[76], MS Continue 및 [77]Dolcontinue가 포함됩니다.지속적인 통증의 경우,[78] 연장 방출 모르핀을 24시간마다 1회(Kadian의 경우) 또는 2회(MS [78]Continue의 경우) 투여하는 효과는 즉시 방출 모르핀을 [79]여러 번 투여하는 것과 거의 동일합니다.일반적으로 각각 24시간 연장 방출 투여량의 5%에서 15%로 구성되는 획기적인 통증의 경우 필요에 따라 즉시 방출 모르핀의 "구제 용량"[79]과 함께 연장 방출 모르핀을 투여할 수 있다.
체액 검출
모르핀과 그 주요 대사물인 모르핀-3-글루쿠로니드 및 모르핀-6-글루쿠로니드는 면역측정법을 사용하여 혈액, 혈장, 모발 및 소변에서 검출될 수 있다.크로마토그래피는 이러한 각 물질에 대해 개별적으로 테스트하는 데 사용될 수 있습니다.일부 테스트 절차는 면역측정 전에 대사 생성물을 모르핀으로 가수분해하는데, 이는 별도로 발표된 결과의 모르핀 수치를 비교할 때 고려되어야 한다.모르핀은 또한 고체상 추출(SPE)에 의해 전혈 샘플로부터 분리될 수 있으며 액체 크로마토그래피 질량 분석(LC-MS)을 사용하여 검출될 수 있다.
코데인이나 양귀비 씨앗이 함유된 음식을 섭취하면 잘못된 [80]양성이 나올 수 있다.
1999년 리뷰에서는 사용 [81]후 1~1.5일 동안 표준 소변 검사를 통해 상대적으로 낮은 용량(모르핀으로 즉시 대사됨)의 헤로인을 검출할 수 있다고 추정했다.2009년 리뷰에서 분석물이 모르핀이고 검출 한도가 1ng/ml일 때 20mg의 정맥주사(IV) 선량이 12-24시간 동안 검출된다는 것이 확인되었다.0.6ng/ml의 검출 한계에서도 유사한 [82]결과가 나왔다.
자연발생
모르핀은 아편에서 발견되는 가장 풍부한 아편제이며, 파파버 솜니페럼 양귀비의 익지 않은 씨팟을 얕게 채점하여 추출한 건조 라텍스입니다.모르핀은 일반적으로 아편 [83]건조 중량의 8~14%를 차지하지만, 특수 재배 품종은 26%에 이르거나 전혀 모르핀을 생성하지 않는다(1% 미만, 아마도 0.04%까지 감소).아편 양귀비의 '프젬코'와 '노르만' 품종을 포함한 후자의 품종은 옥시코돈과 에톨핀과 같은 반합성 및 합성 오피오이드의 제조에 사용되는 두 개의 다른 알칼로이드, 즉 테바인과 오리파빈을 생산하는데 사용된다.P. bracteatum은 모르핀, 코데인 또는 기타 마취성 페넌트렌 타입의 알칼로이드를 포함하지 않는다.이 종은 오히려 테바인의 [84]근원이다.일부 홉과 뽕나무 종뿐만 아니라 다른 파파베랄레스와 파파베라과에서 모르핀의 발생은 확인되지 않았다.모르핀은 식물의 수명 주기 초기에 가장 많이 생산된다.추출의 최적점을 지나 식물 내의 다양한 과정은 코데인, 테바인을 생성하며, 일부 경우에는 무시할 수 있는 양의 하이드로모르핀, 디히드로모르핀, 디히드로코데인, 테트라히드로테바인 및 하이드로코돈을 생성한다(이러한 화합물은 오히려 테바인과 오리파빈에서 합성된다).
포유류의 뇌에서 모르핀은 미량 정상상태 [9]농도에서 검출된다.인체는 또한 엔도르핀을 생산하는데, 엔도르핀은 화학적으로 연관된 내인성 오피오이드 펩타이드로 신경펩타이드로 기능하며 [85]모르핀과 유사한 효과를 가지고 있다.
인간생합성
본 섹션은 표준 프레젠테이션, 교재 구성도 없이 주요 효소, 경로 지점 등을 포함한 확장이 필요하다.추가하시면 됩니다. (2016년 10월) |
모르핀은 백혈구를 [9][86][87]포함한 다양한 인간 세포에 의해 합성되고 방출될 수 있는 인간의 내인성 오피오이드이다.시토크롬 P450 이소엔자임인 CYP2D6는 [9][88]인간에서 모르핀의 생합성 경로를 따라 코데인에서 모르핀, 티라민에서 도파민의 생합성을 촉매한다.사람의 모르핀 생합성 경로는 다음과 [9]같이 발생한다.
L-티로신 → 파라-티라민 또는 L-DOPA → 도파민 → (S)-노를라우단오솔린 → (S)-레티쿨린 → (R)-레티쿨린 → 살루타리딘 → 살루타리돌 → 더바인 코드이논 → 네오폰
(S)-노를라우다노솔린(일명 테트라히드로파파베롤린)은 L-DOPA 및 [9]도파민의 대사물인 3,4-디히드록시페닐아세트알데히드(DOPAL)로부터 합성할 수도 있다.파킨슨병 [9]치료를 위해 L-DOPA를 복용하는 개인에서 내인성 코데인과 모르핀의 소변 농도가 유의하게 증가하는 것으로 밝혀졌다.
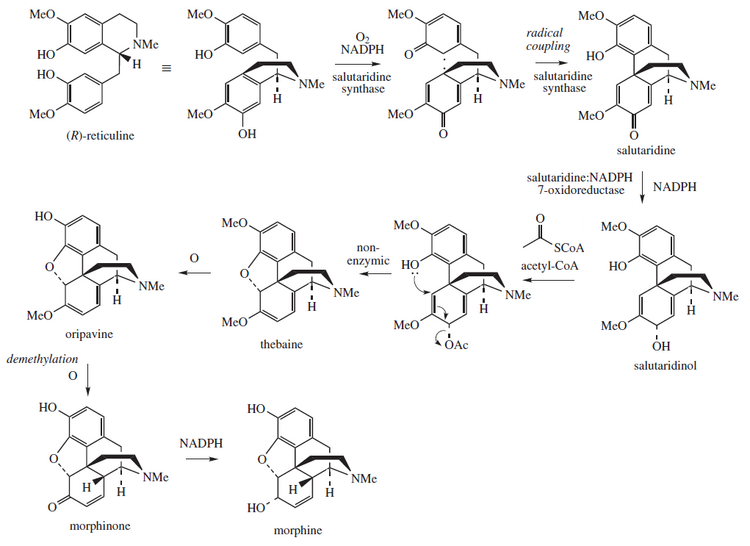
아편 양귀비 생합성
모르핀은 테트라히드로이소퀴놀린 레티쿨린으로부터 아편 양귀비에서 생합성된다.그것은 살루타리딘, 테바인, 그리고 오리파빈으로 변환된다.이 과정에 관여하는 효소는 살루타리딘 합성효소, 살루타리딘이다.NADPH7-산화환원효소 및 코데논환원효소.[89]연구원들은 유전자 조작 [90]효모에서 모르핀을 생성하는 생합성 경로를 재현하려고 시도하고 있다.2015년 6월에는 당에서 S-레티큘린을 제조할 수 있었고 R-레티큘린은 모르핀으로 전환될 수 있었지만 중간 반응은 수행할 [91]수 없었다.2015년 8월 효모에서 테바인과 하이드로코돈의 완전한 합성이 최초로 보고되었지만, 상업적인 [92][93]사용에 적합하기 위해서는 생산성이 10만 배 이상 향상되어야 한다.
화학
모르핀 구조의 요소는 모르핀 계열(레보르판올, 덱스트로메토르판 및 기타) 및 모르핀과 유사한 [citation needed]성질을 가진 많은 구성원을 가진 다른 그룹과 같은 완전한 합성 약물을 생성하기 위해 사용되어 왔다.모르핀과 앞서 언급한 합성물의 변형은 또한 구토학, 자극제, 항충제, 항콜린제, 근육 이완제, 국소 마취제, 일반 마취제,[citation needed] 기타와 같은 다른 용도를 가진 비약물 약물을 발생시켰다.모르핀 유래 작용제-항작용제 약물도 개발되었다.[citation needed]
구조설명


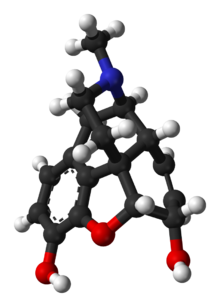
모르핀은 두 개의 추가적인 고리 [94]폐쇄가 있는 벤질리소퀴놀린 알칼로이드이다.Harrison 대학의 Harrison School of Pharmacology의 Jack DeRuiter는 2000년 가을 과정에 이전 부서의 "Drug Action의 원리 2" 과정에 대해 "모르핀 분자의 검사에서 다음과 같은 구조적 특징이 드러난다.약리학적 프로파일...
- 벤젠 고리(A), 2개의 부분불포화 시클로헥산 고리(B, C), 피페리딘 고리(D) 및 테트라히드로프랑 고리(E)로 이루어진 강체 5환 구조.링 A, B 및 C는 페넌트렌 고리계이다.이 링 시스템은 구조상의 유연성이 거의 없습니다...
- C3-페놀기 [히드록실기](pKa 9.9)와 C6-알릴기 [히드록실기]의 두 가지 수산기,
- C4와 C5 사이의 에테르 링크
- C7과 C8 사이의 포화 상태
- 위치 17의 기본 [일기]-아민 함수 [및]
- [[95][better source needed][needs update]5] 진통작용의 높은 입체선택성을 나타내는 모르핀과 함께 키랄리티 중심(C5, C6, C9, C13 및 C14)을 나타낸다.
모르핀 및 그 유도체의 대부분은 광학 이성질체를 나타내지 않지만, 모르핀 계열(레보르판올, 덱스토판 및 라세미칼 모화학 라세모판)[96]과 같은 보다 먼 친척은 존재하며, 위에서 언급한 바와 같이 생체 내 입체선택성은 [citation needed]중요한 문제이다.
용도 및 파생상품
생산되는 대부분의 리싯 모르핀은 메틸화에 [97]의해 코데인을 만드는데 사용된다.또한 헤로인(3,6-디아세틸모르핀), 하이드로모르폰(디히드로모르핀), 옥시모르폰(14-히드록시디히드로모르핀)[citation needed]을 포함한 많은 약물의 전구체이다.대부분의 반합성 오피오이드는 모르핀 서브그룹과 코데인 서브그룹 모두 다음 [citation needed]중 하나 이상을 수정하여 생성됩니다.
- 모르핀 탄소 골격의 1번 또는 2번 위치에서 할로겐화 또는 기타 변형.
- 모르핀을 코데인으로 만드는 메틸기는 제거되거나 다시 첨가되거나, 모르핀 유래 약물의 코데인 유사체를 만들기 위해 에틸과 다른 기능성 기로 대체될 수 있고, 그리고 그 반대도 마찬가지입니다.모르핀 기반 약물의 코데인 유사체는 코데인과 모르핀, 하이드로코돈과 하이드로모르폰, 옥시코돈과 옥시모르폰, 니코코데인과 니코모르핀, 디히드로모르핀 등과 같이 종종 더 강한 약물의 프로드럭 역할을 한다.
- 위치 7과 8 사이의 결합에 대한 포화, 개방 또는 기타 변화뿐만 아니라 이러한 위치에 관능기를 추가, 제거 또는 수정한다. 7-8 결합을 포화, 환원, 제거 또는 수정하고 14에서 관능기를 부착하면 히드로몰피놀을 생성한다. 카르보닐과 창기에 수산기를 산화시킨다.ng 7-8 결합에서 단일 결합으로 이중 코데인을 옥시코돈으로 변화시킨다.
- 3위 또는 6위(디히드로코데인 및 관련, 하이드로코돈, 니코모르핀)에 대한 기능기 부착, 제거 또는 수정. 메틸 기능기를 3위에서 6위로 이동할 경우 코데인은 헤테로코데인이 되며, 이는 모르핀보다 72배 강하며, 따라서 6배 강합니다.
- 위치 14에 기능기 부착 또는 기타 수정(옥시모르폰, 옥시코돈, 나록손)
- 2, 4, 5 또는 17위에서의 변형. 보통 모르핀 골격의 다른 분자에 대한 다른 변화와 함께.이것은 종종 촉매 환원, 수소화, 산화 등에 의해 생성되는 약물로 이루어지며 모르핀과 코데인의 강한 유도체를 생성한다.
또한 많은 모르핀 유도체들은 테바인 또는 코데인을 출발 [citation needed]재료로 사용하여 제조될 수 있다.모르핀의 N-메틸기를 N-페닐에틸기로 치환하면 아편작용제 [citation needed]효력에서 모르핀보다 18배 더 강력한 제품이 생성된다.이 변형을 6-히드록실기를 6-메틸렌기로 치환하면 모르핀보다 약 1,443배 더 강력한 화합물이 생성되며, 이는 에톨핀(M99, 이모빌론 트라우실라이저 다트)과 같은 벤틀리 화합물보다 몇 가지 측정값으로 [citation needed]더 강하다.모르핀과 밀접한 관련이 있는 것은 더 [citation needed]이상 일반적으로 사용되지 않는 약품인 오피오이드 모르핀-N-옥사이드(genomorphine)와 [citation needed]아편에 존재하는 알칼로이드인 pseudomorphine은 모르핀의 분해 산물로 형성된다.
이 분자의 광범위한 연구와 사용의 결과로, 코데인과 관련 약물을 계수하는 250개 이상의 모르핀 유도체가 [citation needed]19세기 이후 개발되었다.이 약들 25%는 코데인(모르핀의 힘의 약간 2%이상)의 진통제 힘은 모르핀의 수천배가 국력이 강성해, 강력한 오피오이드 길항제에서 낼럭손(Narcan),naltrexone(Trexan),diprenorphine(M5050, 이모 빌론. 창 모양이 연속적으로 엇갈려reversing제)과nalorphine(Nalline)등 다양하다.[표창 필요한]일부 오피오이드 작용제-항고니스트, 부분작용제 및 역작용제도 [citation needed]모르핀에서 유래한다.반합성 모르핀 유도체의 수용체 활성화 프로파일은 매우 다양하며 아포모르핀과 같은 일부는 마취 [citation needed]효과가 없다.
소금
모르핀과 그 수화 형태 모두 물에 [98]잘 녹지 않는다.이 때문에 제약회사들은 황산염과 염산염을 생산하고 있는데, 둘 다 [clarification needed][citation needed]모분자보다 수용성이 300배 이상 높다.포화 모르핀 하이드레이트 용액의 pH는 8.5인 반면, 소금은 [citation needed]산성이다.강한 산이지만 약한 염기로부터 유도되기 때문에 둘 다 pH =[clarification needed][citation needed] 5 정도이며, 그 결과 모르핀염은 소량의 NaOH와 혼합되어 [citation needed]주입에 적합하다.
모르핀의 염류에는 염산염, 황산염, 주석산염 및 [citation needed]구연산염이 많이 사용되며, 메토브롬화물, 하이드로브롬화물, 하이드로요오드화물, 젖산염, 염화물 및 비타르트산염 및 기타는 아래에 [citation needed]열거되어 있습니다.모르핀 디아세테이트(헤로인)는 소금이 아니라 오히려 [citation needed]더 유도체이다.[99]
모르핀 메코네이트는 양귀비에서 알칼로이드의 주요 형태이며, 모르핀 펙틴산염, 질산염, 황산염, 그리고 다른 [citation needed]것들도 마찬가지입니다.코데인,dihydrocodeine과 다른(특히 나이 든)의 마취제처럼, 모르핀은 살리실산 메틸 소금으로 약간의 공급자 그리고 쉽게 둘 다 opioid과 NSAID의 치료 장점을 교묘히 전달하는, 모르핀[표창 필요한]여러 바르비투르 소금은 과거에, was/is은 모르핀 valerate, sa로 사용했던 것이 복리로 계산될 수 있어 사용되어 왔다.이는 산성 b의발레리안의 [citation needed]능동적 원리를 보여줍니다.모르페네이트 칼슘은 모르핀 제조의 다양한 라텍스 및 양귀비 스트로 방법의 중간체이며, 보다 드물게 모르페네이트 나트륨이 [citation needed]그 자리를 차지합니다.모르핀 아스코르브산염과 타네이트, 구연산염 및 아세트산염, 인산염, 발레이트 및 기타 염은 [citation needed][100]제조 방법에 따라 양귀비차에 존재할 수 있다.
미국 의약품 집행국이 보고 목적으로 나열한 소금은 다른 몇 가지 외에 다음과 같다.[citation needed]
| CSA(Controlled Substances Act) 스케줄, ACSCN(Administrative Controlled Substances Code Number) 및 프리베이스 전환 [clarification needed][citation needed]비율에 따라 모르핀 염을 선택합니다. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
생산.
아편 양귀비에서 알칼로이드는 메콘산에 결합되어 있다.메콘산보다 강한 산이지만 알칼로이드 분자와 반응하기에는 그리 강하지 않은 희석 황산으로 분쇄된 식물에서 추출하는 방법이다.추출은 여러 단계로 이루어집니다(파쇄된 식물 1개를 최소 6~10회 추출하기 때문에 실질적으로 모든 알칼로이드가 용액에 들어갑니다).마지막 추출공정에서 얻은 용액에서 수산화암모늄 또는 탄산나트륨 중 하나로 알칼로이드를 침전시킨다.마지막 단계는 다른 아편 알칼로이드로부터 모르핀을 정제하고 분리하는 것이다.다소 유사한 그레고리의 과정은 2차 세계대전 동안 영국에서 개발되었는데, 이것은 대부분의 경우 뿌리와 잎을 보통 또는 약간 산성화된 물에 삶아낸 후 농축, 추출, 알칼로이드 [citation needed]정제 단계를 거친다."팝피 빨대"(즉, 말린 꼬투리 및 줄기)를 처리하는 다른 방법으로는 증기, 여러 종류의 알코올 또는 기타 유기 용제를 사용합니다.
양귀비 빨대법은 유럽 대륙과 영연방에서 우세하며, 라텍스법은 인도에서 가장 일반적으로 사용된다.라텍스 방법은 익지 않은 팟을 2-5개의 날이 있는 칼로 수직 또는 수평으로 슬라이스할 수 있으며, 이를 위해 특별히 개발된 가드가 밀리미터의 몇 분의 1 깊이까지 개발되어 팟의 스코어링을 최대 5회 수행할 수 있습니다.과거 중국에서 사용되던 대체 라텍스 방법은 양귀비 머리를 잘라내고 큰 바늘로 찔러 2448시간 후에 말린 [citation needed]라텍스를 채취하는 것이다.
인도에서는 허가받은 양귀비 농가에 의해 수확된 아편을 정부 가공 센터에서 균일한 수준의 수화물로 탈수시킨 후 아편에서 모르핀을 추출하는 제약 회사에 판매한다.하지만, 터키와 태즈메이니아에서는, 양귀비 빨대라고 불리는 줄기가 붙어 있는 완전히 성숙한 마른 씨앗 꼬투리를 수확하고 가공함으로써 모르핀을 얻습니다.터키에서는 물 추출 공정을, 태즈메이니아에서는 용제 추출 공정을 사용한다.[citation needed]
아편 양귀비에는 적어도 50종류의 알칼로이드가 함유되어 있지만 대부분은 농도가 매우 낮다.모르핀은 생 아편의 주요 알칼로이드이며 건조 중량으로 아편의 약 8-19%를 구성한다.[75]특정 목적으로 개발된 양귀비 변종들은 현재 [citation needed]무게로 최대 26%의 모르핀을 함유하고 있는 아편을 생산하고 있다.분쇄 건조 양귀비 빨대의 모르핀 함량을 결정하기 위한 대략적인 경험칙은 라텍스 방법을 통해 균주 또는 작물에 예상되는 비율을 8 또는 [citation needed]경험적으로 결정된 인자로 나누는 것이다.또한 태즈메이니아에서 개발된 Norman 변종 P. Somniferum은 0.04%의 모르핀을 생성하지만, 훨씬 더 많은 양의 테바인과 오리파빈이 함유되어 있어 자극제, 구토학, 오피오이드 길항제, 항콜린제,[citation needed] 평활근제 등의 다른 약물을 합성하는데 사용될 수 있다.
1950년대와 1960년대에 헝가리는 유럽 전체 의약품 목적 모르핀 생산량의 60%를 공급했다.오늘날까지 헝가리에서 양귀비 농사는 합법이지만 양귀비 농장은 법으로 2에이커(8,100m2)로 제한되어 있다.꽃집에서 꽃꽂이에 사용하기 위해 말린 양귀비를 파는 것도 합법이다.
1973년 미국 국립보건원(National Institute of Health)의 한 팀이 콜타르를 원료로 모르핀, 코데인, 테바인의 총합성 방법을 개발했다고 발표했다.코데인 하이드로코돈급 기침 억제제(모두 코데인 또는 테바인뿐만 아니라 모르핀에서 1개 이상의 단계로 만들어질 수 있음)의 부족이 연구의 첫 번째 이유였습니다.
전 세계에서 약용으로 생산된 대부분의 모르핀은 생 아편과 양귀비 빨대의 농도가 모르핀의 농도보다 훨씬 낮기 때문에 실제로 코데인으로 전환된다; 대부분의 국가에서 코데인의 사용은 적어도 무게 기준으로 모르핀의 농도보다 같거나 더 크다.
화학 합성
마샬 D가 고안한 최초의 모르핀 전체 합성. 1952년 게이츠 주니어는 전합성 [101]사례로 널리 사용되고 있다.라이스,[102] [103]에반스, [104]훅스, 파커,[105] 오버맨,[106] 멀저-트라우너,[107] 화이트,[108] 타버,[109] 트로스트,[110] 후쿠야마,[111] 길루,[112] [113]황새 등의 연구 그룹에 의해 여러 가지 다른 합성물이 보고되었다.이 다환 구조에 의해 제시되는 입체화학적 복잡성과 그에 따른 합성 도전 때문에, 마이클 프리맨틀은 화학 합성이 [114]아편 양귀비로부터 모르핀을 생산하는 비용과 경쟁할 수 있을 정도로 비용 효율이 "매우 낮다"는 견해를 표명했다.
다른 오피오이드 전구체
제약
이 섹션은 확대되어야 한다: 브리엘피(brielfy)가 모르핀이 의학이나 연구에 유용한 다른 화합물을 생산하기 위해 산업적으로 그리고 세계적으로 어떻게 사용되는지를 요약한 소스 콘텐츠.추가해서 도와주시면 됩니다. (2020년 2월) |
모르핀은 많은 반합성 [115]유도체를 가진 코데인뿐만 아니라 디히드로모르핀, 하이드로모르폰, 하이드로코돈, 옥시코돈과 같은 많은 오피오이드 제조의 선구자이다.
불법
불법 모르핀은 드물게 처방전 없이 살 수 있는 기침약과 [citation needed]진통제에서 발견되는 코데인으로 생산된다.또 다른 불법 공급원은 장기 방출성 모르핀 [116]제품에서 추출된 모르핀이다.그런 다음 화학 반응을 사용하여 모르핀, 디히드로모르핀 및 하이드로코돈을 헤로인 또는 다른 오피오이드[예: 디아세틸디히드로모르핀(Paralaudin) 및 테바콘][citation needed]로 전환할 수 있습니다.모르핀을 하이드로모르핀 클래스의 케톤이나 디히드로모르핀(파라모르판), 데소모르핀(페르모르핀), 메토폰 등 기타 파생상품으로, 코데인을 하이드로코돈(디코디드), 디히드로코데인(파라코딘) 등으로 은밀하게 변환하려면 보다 많은 전문지식, 종류 및 화학기기가 필요하다.입수하기 어렵기 때문에 불법적으로 사용되는 경우는 거의 없습니다(단,[citation needed] 사례가 기록되어 있습니다).
역사
아편을 기반으로 한 영약은 비잔틴 시대의 연금술사들에 의해 만들어진 것으로 여겨져 왔지만, 그 구체적인 공식은 오스만 제국의 콘스탄티노플 정복 동안 없어졌다.[117]1522년 경, 파라셀수스는 아편을 기반으로 한 영약을 언급했는데, 그는 그것을 "찬미하다"는 뜻의 라틴어 로다르에서 "로다눔"이라고 불렀습니다. 그는 그것을 강력한 진통제로 묘사했지만, 사용을 자제할 것을 권고했습니다.주어진 레시피는 현대의 라우다눔과 [118]상당히 다르다.
모르핀은 1804년 12월 독일의 약사 프리드리히 세르튀르너가 [11][119]파더보른의 양귀비 식물에서 추출한 최초의 활성 알칼로이드로 발견했다.1817년, 세르튀르너는 모르핀을 자신과 세 명의 어린 소년, 세 마리의 개, 그리고 쥐에게 투여한 실험을 보고했는데, 네 명 모두 [120]거의 죽을 뻔했다.세르튀르너는 원래 잠을 잘 [12][121]수 있다는 이유로 그리스 꿈의 신 모피우스(Morpheus)의 이름을 따 모르피움이라는 물질 이름을 붙였다.세르튀르너의 모르핀은 아편보다 6배나 강했다.그는 그 약의 낮은 복용량이 필요하기 때문에, 그것은 덜 중독적일 것이라고 가설을 세웠다.그러나 세르튀르너는 "재앙을 [122]피하기 위해 모르피움이라고 부르는 이 신물질의 끔찍한 효과에 관심을 끄는 것이 나의 의무라고 생각한다"고 경고하며 이 약물에 중독되었다.
이 약은 1817년 세르튀르너와 컴퍼니에 의해 진통제이자 아편과 알코올 중독 치료제로 일반에 처음 판매되었다.그것은 1822년 프랑스의 에드미 카스테잉 박사가 [123]환자를 살해한 혐의로 유죄 판결을 받았을 때 처음으로 독극물로 사용되었습니다.상업적인 생산은 1827년 독일의 다름슈타트에서 제약 회사인 Merck에 의해 시작되었고, 모르핀 판매는 초기 성장의 [124][125]큰 부분을 차지했다.1850년대에 알렉산더 우드는 그의 아내 레베카에게 실험 삼아 모르핀을 주사했다고 보고했다; 속설은 이것이 호흡기 [120]우울증 때문에 그녀를 죽였다는 것이지만, 그녀는 남편보다 10년 [126]더 오래 살았다고 한다.
나중에 모르핀이 알코올이나 아편보다 중독성이 더 강하다는 것이 밝혀졌고, 남북 전쟁 동안 모르핀이 광범위하게 사용되면서 40만 명 이상의[127] 사람들이 모르핀 [128]중독의 "병사병"에 걸렸다고 한다.이 생각은 논란의 대상이 되어왔다. 그러한 질병이 실제로 조작된 것이라는 암시가 있었기 때문이다; "군인의 병"이라는 문구의 문서화된 첫 사용은 [129][130]1915년이었다.
디아세틸모르핀은 1874년에 모르핀으로부터 합성되어 1898년에 바이어에 의해 시장에 나왔다.헤로인은 모르핀 무게보다 1.5배에서 2배 정도 강력합니다.디아세틸모르핀의 지질 용해성 때문에 모르핀보다 혈액-뇌 장벽을 더 빨리 넘을 수 있으며,[131] 이후 중독의 강화 성분을 증가시킨다.다양한 주관적이고 객관적인 척도를 사용하여, 한 연구는 사후 약물들에게 정맥에 투여된 모르핀에 대한 헤로인의 상대적 효력을 1.80–2.66mg의 모르핀 황산염에 1mg의 디아모르핀 염산염(헤로인)[41]으로 추정했다.
모르핀은 1914년 해리슨 마약세법에 의해 미국에서 통제된 약물이 되었고, 미국에서 처방전 없이 소지하는 것은 형사 범죄이다.모르핀은 헤로인이 합성되어 사용되기 전까지 세계에서 가장 흔하게 남용되는 마약성 진통제였다.일반적으로,dihydromorphine(C.1900년), opioids(1920년대)의dihydromorphinone 클래스 및 oxycodone(1916년)그리고 유사한 약품들의 합성을 때까지, 같은 효능 범위의 아편, 모르핀, 헤로인 어떤 다른 마약, 인조 섬유가 여전히 몇년 그 중(페티딘 독일에서 1937년에 발명되었다)과 오피오이드 길항근다. semi-synthetics는 디히드로코데인(파라코딘), 에틸모르핀(디오닌), 벤질모르핀(페로닌)과 같은 코데인의 유사체 및 유도체였다.심지어 오늘날에도 모르핀은 헤로인이 부족할 때 헤로인 중독자들이 가장 많이 찾는 마약이다; 지역 조건과 사용자의 선호는 히드로모르폰, 옥시코돈, 또는 메타돈뿐만 아니라 1970년대 호주와 같은 특정 사례에서 덱스트로모라미드를 발생시킬 수 있다.절대 다수의 헤로인 중독자들이 사용하는 임시 약물은 아마도 코데인이며, 디히드로코데인, 양귀비 꼬투리와 양귀비 씨 차와 같은 양귀비 빨대 유도체, 프로옥시펜, 그리고 트라마돌도 많이 사용된다.
모르핀의 구조식은 1925년에 로버트 [133]로빈슨에 의해 결정되었다.콜타르와 석유 증류액과 같은 원료에서 모르핀을 합성하는 최소 3가지 방법이 마셜 D에 의해 1952년에 처음 발표되었습니다. 로체스터 [134]대학의 게이츠 주니어그럼에도 불구하고, 대부분의 모르핀은 양귀비의 잘 익지 않은 꼬투리로부터 라텍스를 채취하는 전통적인 방법 또는 식물의 마른 꼬투리와 줄기인 양귀비 빨대를 사용하는 방법에 의해 양귀비에서 추출되며, 그 중 가장 널리 알려진 것은 1925년 헝가리에서 발명되어 1930년 헝가리 약리학자 잔에 의해 발표되었다.os Kabay.[135]
2003년에는 인체에서 자연적으로 발생하는 내인성 모르핀이 발견되었다.모르핀에만 반응하는 것으로 보이는 수용체, 즉 [136]인체 조직의3 μ-오피오이드 수용체가 있었기 때문에 이 주제에 대해 30년 동안 추측이 이루어졌습니다.암성 신경아세포종 세포에 반응하여 형성되는 인간 세포는 미량의 내인성 [87]모르핀을 함유하고 있는 것으로 밝혀졌다.
사회와 문화
법적 상태
- 호주에서 모르핀은 다양한 제목의 주 및 지역 독극물 법에 따라 스케줄 8 약물로 분류됩니다.
- 캐나다에서 모르핀은 규제 약물 및 물질법에 따라 스케줄 I 약물로 분류된다.
- 프랑스에서 모르핀은 1970년 12월 프랑스 규제 물질법에 근거해 가장 엄격한 규제 물질 스케줄에 있다.
- 독일에서 모르핀은 Betaubungsmittelgesetz의 [137]Anlage III(CSA 부칙 II에 상당)에 열거된 Verkehrsféhiges und verschreibungsféhiges Betaubungsmittel이다.
- 스위스에서 모르핀은 독일의 합법적 약물 분류와 비슷하게 예정되어 있다.
- 일본에서는 모르핀이 마약 및 정신약물 단속법(마야쿠오세이신야쿠 토리시마리호)에 따라 마약으로 분류된다.
- 네덜란드에서 모르핀은 아편법에 따라 제1급 마약으로 분류된다.
- 뉴질랜드에서 모르핀은 1975년 [138]약물남용법에 따라 B급 약물로 분류된다.
- 영국에서 모르핀은 1971년 약물남용법에 따른 A급 약물과 2001년 약물남용규정에 따른 부칙 2 통제 약물로 분류된다.
- 미국에서 모르핀은 주요 관리 통제 물질 코드 번호 9300에 따라 통제 물질 법에 따라 부칙 II 통제 물질로 분류됩니다.모르핀 의약품은 연간 제조 할당량을 적용받는다. 2017년에는 판매용 생산량 35.0톤과 다른 [139]의약품으로의 전환을 위한 중간 또는 화학적 전구체로서의 생산량 27.3톤이었다.극도로 희석된 제제에 사용하기 위해 생산된 모르핀은 제조 할당량에서 [citation needed]제외된다.
- 국제적으로(UN) 모르핀은 마약에 [140]관한 단일 협약에 따른 부칙 I 약물이다.
비의료용
그 행복감, 괴로움의 종합적인 완화하는 것이고 따라서 고통, 사교성의 승진과 감정 이입,"몸 높은", anxiolysis은 opioids 등 마약류가 제공하는 모든 측면 많은 양의 고통의 없는 상태에서 사용자의 약을 병적인 갈망을 전할 수 있는 장기간에 걸친 기간의 사용을 일으킬 수 있다.[표창 필요한]전체 오피오이드 등급의 약물의 원형으로서 모르핀은 오남용을 초래할 수 있는 특성을 가지고 있다.모르핀 중독은 중독에 대한 현재의 인식이 [medical citation needed]바탕이 되는 모델이다.
동물과 인간의 연구와 임상 경험은 모르핀이 알려진 가장 행복한 약들 중 하나이며, 헤로인이 전신 모르핀의 전달을 위한 프로드러그이기 때문에 IV 경로를 제외한 모든 것을 통해 헤로인과 모르핀을 구별할 수 없다는 주장을 뒷받침한다.모르핀 분자에 대한 화학적 변화는 각각 디히드로모르핀, 하이드로모르폰(Dilaudid, Hydromorphone, Hydromorphone), 옥시모르폰(Opana)과 같은 다른 행복유전성 물질과 후자의 메틸화 당량 디히드로코돈, 하이드로코돈 및 옥시코디코돈(oxycododone)을 생성한다.e 및 니코모르핀과 같은 3,6 모르핀 디에스터 범주의 다른 성분 및 데소모르핀, 하이드로모르피놀 등과 같은 기타 유사한 반염색 아편제. 그러나 드물게 [medical citation needed]불법적으로 생산되기도 한다.
일반적으로 모르핀의 비의학적 사용은 소정 이상 또는 의학적 감독 밖에서 복용, 경구제제 주입, 알코올, 코카인 등의 미승인 전위제와의 혼합, 또는 알약을 씹거나 코웃음을 치거나 주사제를 제조하기 위한 분말로 변함으로써 연장 방출 메커니즘을 파괴하는 것을 수반한다.후자의 방법은 아편을 피우는 전통적인 방법만큼이나 시간이 많이 걸리고 관련될 수 있다.그리고 간이 첫 번째 단계에서 약물의 많은 부분을 파괴한다는 사실은 많은 고객들이 바늘을 꽂는 사용자가 아니고 약을 경구 섭취하는 것에 실망했을 수 있기 때문에 비밀 재판매에 대한 수요 측면에 영향을 미친다.모르핀은 많은 경우 옥시코돈만큼 돌리기 어렵거나 어렵기 때문에, 어떤 형태의 모르핀도 길거리에서는 흔치 않지만,[medical citation needed] 모르핀 주사, 순수한 약용 모르핀 분말, 그리고 수용성 다목적 정제가 가능한 경우라면 매우 인기가 있습니다.
모르핀은 또한 헤로인의 생산에 사용되는 페이스트에 들어 있는데, 헤로인은 스스로 훈제되거나 용해성 소금으로 바뀌어 주입될 수 있습니다; 곤포트(폴란드 헤로인)와 블랙 타르 공정의 마지막 제품에서도 마찬가지입니다.양귀비 빨대뿐만 아니라 아편도 양귀비 차에서부터 거의 약품 등급의 모르핀까지 그 자체로 또는 50개 이상의 다른 알칼로이드와 함께 순도 수준의 모르핀을 생산할 수 있습니다.그것은 또한 아편과 그것의 모든 형태, 파생물, 그리고 유사물의 활성 마약 성분이며 헤로인의 분해로부터 형성되며, 불완전한 [medical citation needed]아세틸화의 결과로 다른 많은 불법 헤로인에 존재한다.
이름
모르핀은 세계 [1]각지에서 다양한 상표명으로 판매되고 있다.그것은 이전에는 영국 영어로 [141]Morphia라고 불렸다.
모르핀의 비공식 명칭은 다음과 같다.큐브 주스, 도프, 드리머, 엠셀, 퍼스트 라인, 신의 약품, 하드 스터프, 호커스, 하우스, 리디아, 리딕, M, 미스 엠마, 미스터 블루, 몽키, 모프, 모피드, 모피드, 모피드, 모피드, 모포, MS, 뉴 머드.
MS Continue 태블릿은 misties, 100mg 확장 릴리스 태블릿은 grey 및 블록버스터로 알려져 있습니다."스피드볼"은 오피오이드 성분으로 모르핀을 사용할 수 있는데, 오피오이드 성분은 코카인, 암페타민, 메틸페니다이트 또는 유사한 약물과 결합됩니다."블루 벨벳"은 주사하여 섭취한 항히스타민 트리페나민(피라벤자민, PBZ, 펠라민)과 모르핀을 혼합한 것으로, 삼키거나 보존 관장제로 사용할 때 혼합물을 지칭하는 명칭이다."모르피아"는 몰핀의 더 오래된 공식 용어이며 속어로도 사용된다."Driving Emma"는 모르핀을 정맥에 투여하는 것입니다.다용도 태블릿(혀 밑에 삼키거나 녹이거나 뺨과 턱 사이에 있는 수용성 피하 태블릿)은 일부 하이드로모르폰 브랜드와 마찬가지로 쉐이크 & 베이크 또는 쉐이크 & 샷으로 알려져 있다.
모르핀은 특히 디아세틸모르핀(헤로인)을 훈제할 수 있으며, 가장 일반적인 방법은 "용의 체이싱" 방법이다.사용 직전에 모르핀을 헤로인 및 관련 약물로 변환하기 위해 아세틸화를 수행하는 것은 AAing(아세트산 무수물의 경우) 또는 홈베이크(Home-bake) 또는 블루 헤로인(Blue Magic 헤로인, 블루 모르핀, 블루 모르핀, 블루 모르핀 또는 블루 폰 또는 블루 벨벳으로 알려진 린커스(Linktus)이라고도 한다.를 참조해 주세요).
개발도상국에서의 접근
모르핀은 값이 싸지만 가난한 나라 사람들은 종종 모르핀에 접근할 수 없다.2005년 국제 마약 관리 위원회의 추정에 따르면, 6개국(호주, 캐나다, 프랑스, 독일, 영국, 미국)이 세계 모르핀의 79%를 소비하고 있다.세계 인구의 80%를 차지하는 부유한 국가들은 전 세계 모르핀 [143]공급의 약 6%만을 소비했다.어떤[which?] 나라는 모르핀을 거의 수입하지 않고 있고,[144] 다른 나라에서는[which?] 죽을 때 심한 통증을 완화시키는 약도 거의 없다.
통증 관리 전문가들은 모르핀의 저분포는 중독과 남용의 가능성에 대한 정당한 두려움 때문이라고 보고 있다.모르핀이 분명히 중독성이 있는 반면, 서양 의사들은 그 약을 사용하고 치료가 [145]끝나면 환자를 떼어내는 것이 가치 있다고 믿는다.
레퍼런스
- ^ a b c drugs.com Wayback Machine 페이지의 Morpin Archived 2015년 6월 14일 국제 리스트 2015년 6월 2일 액세스
- ^ a b "Morphine Use During Pregnancy". Drugs.com. 14 October 2019. Retrieved 21 August 2020.
- ^ Bonewit-West K, Hunt SA, Applegate E (2012). Today's Medical Assistant: Clinical and Administrative Procedures. Elsevier Health Sciences. p. 571. ISBN 9781455701506.
- ^ Jonsson T, Christensen CB, Jordening H, Frølund C (April 1988). "The bioavailability of rectally administered morphine". Pharmacology & Toxicology. 62 (4): 203–5. doi:10.1111/j.1600-0773.1988.tb01872.x. PMID 3387374.
- ^ Whimster F (1997). Cambridge textbook of accident and emergency medicine. Cambridge: Cambridge University Press. p. 191. ISBN 978-0-521-43379-2. Archived from the original on 8 September 2017.
- ^ Liben S (2012). Oxford textbook of palliative care for children (2 ed.). Oxford: Oxford University Press. p. 240. ISBN 978-0-19-959510-5. Archived from the original on 8 September 2017.
- ^ a b c d e f g h i j k l m n "Morphine sulfate". The American Society of Health-System Pharmacists. Archived from the original on 2 May 2015. Retrieved 1 June 2015.
- ^ a b c Rockwood CA (2009). Rockwood and Wilkins' fractures in children (7th ed.). Philadelphia, Pa.: Lippincott Williams & Wilkins. p. 54. ISBN 978-1-58255-784-7. Archived from the original on 8 September 2017.
- ^ a b c d e f g Stefano GB, Ptáček R, Kuželová H, Kream RM (2012). "Endogenous morphine: up-to-date review 2011" (PDF). Folia Biologica. 58 (2): 49–56. PMID 22578954. Archived from the original (PDF) on 24 August 2016. Retrieved 10 October 2016.
Positive evolutionary pressure has apparently preserved the ability to synthesize chemically authentic morphine, albeit in homeopathic concentrations, throughout animal phyla.
- ^ a b c Courtwright DT (2009). Forces of habit drugs and the making of the modern world (1 ed.). Cambridge, Mass.: Harvard University Press. pp. 36–37. ISBN 978-0-674-02990-3. Archived from the original on 8 September 2017.
- ^ a b Luch A, ed. (2009). Molecular, clinical and environmental toxicology. Springer. p. 20. ISBN 978-3-7643-8335-0.
- ^ a b c Mosher CJ (2013). Drugs and Drug Policy: The Control of Consciousness Alteration. SAGE Publications. p. 123. ISBN 978-1-4833-2188-2. Archived from the original on 8 September 2017.
- ^ Fisher GL (2009). Encyclopedia of substance abuse prevention, treatment, & recovery. Los Angeles: SAGE. p. 564. ISBN 978-1-4522-6601-5. Archived from the original on 8 September 2017.
- ^ Narcotic Drugs Estimated World Requirements for 2008, Statistics for 2006. New York: United Nations Pubns. 2008. p. 77. ISBN 9789210481199. Archived from the original on 8 September 2017.
- ^ a b c d Narcotic Drugs 2014 (PDF). INTERNATIONAL NARCOTICS CONTROL BOARD. 2015. pp. 21, 30. ISBN 9789210481571. Archived (PDF) from the original on 2 June 2015.
- ^ a b Triggle DJ (2006). Morphine. New York: Chelsea House Publishers. pp. 20–21. ISBN 978-1-4381-0211-5.
- ^ Karch SB (2006). Drug abuse handbook (2nd ed.). Boca Raton: CRC/Taylor & Francis. pp. 7–8. ISBN 978-1-4200-0346-8.
- ^ Macpherson G, ed. (2002). Black's medical dictionary. Nature. Vol. 87 (40th ed.). p. 162. Bibcode:1911Natur..87R.313.. doi:10.1038/087313b0. ISBN 978-0-7136-5442-4. S2CID 3979058. Archived from the original on 8 September 2017.
- ^ Davis's Canadian Drug Guide for Nurses. F.A. Davis. 2014. p. 1409. ISBN 978-0-8036-4086-3.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ "The Top 300 of 2019". ClinCalc. Retrieved 16 October 2021.
- ^ "Morphine - Drug Usage Statistics". ClinCalc. Retrieved 16 October 2021.
- ^ a b "Morphine Sulfate". The American Society of Health-System Pharmacists. Archived from the original on 3 March 2011. Retrieved 3 April 2011.
- ^ Meine TJ, Roe MT, Chen AY, Patel MR, Washam JB, Ohman EM, et al. (June 2005). "Association of intravenous morphine use and outcomes in acute coronary syndromes: results from the CRUSADE Quality Improvement Initiative". American Heart Journal. 149 (6): 1043–9. doi:10.1016/j.ahj.2005.02.010. PMID 15976786.
- ^ Sosnowski MA. "BestBets: Does the application of opiates, during an attack of Acute Cardiogenic Pulmonary Oedma, reduce patients' mortality and morbidity?". BestBets. Best Evidence Topics. Archived from the original on 16 June 2010. Retrieved 6 December 2008.
- ^ Wiffen PJ, Wee B, Moore RA (April 2016). "Oral morphine for cancer pain". The Cochrane Database of Systematic Reviews. 4 (3): CD003868. doi:10.1002/14651858.CD003868.pub4. PMC 6540940. PMID 27105021.
- ^ Schrijvers D, van Fraeyenhove F (2010). "Emergencies in palliative care". Cancer Journal. 16 (5): 514–20. doi:10.1097/PPO.0b013e3181f28a8d. PMID 20890149.
- ^ Naqvi F, Cervo F, Fields S (August 2009). "Evidence-based review of interventions to improve palliation of pain, dyspnea, depression". Geriatrics. 64 (8): 8–10, 12–4. PMID 20722311.
- ^ Parshall MB, Schwartzstein RM, Adams L, Banzett RB, Manning HL, Bourbeau J, et al. (February 2012). "An official American Thoracic Society statement: update on the mechanisms, assessment, and management of dyspnea". American Journal of Respiratory and Critical Care Medicine. 185 (4): 435–52. doi:10.1164/rccm.201111-2042ST. PMC 5448624. PMID 22336677.
- ^ Mahler DA, Selecky PA, Harrod CG, Benditt JO, Carrieri-Kohlman V, Curtis JR, et al. (March 2010). "American College of Chest Physicians consensus statement on the management of dyspnea in patients with advanced lung or heart disease". Chest. 137 (3): 674–91. doi:10.1378/chest.09-1543. PMID 20202949. S2CID 26739450.
- ^ Mattick RP, Digiusto E, Doran C, O'Brien S, Kimber J, Henderson N, Breen B, Shearer J, Gates J, Shakeshaft A, NEPOD Trial Investigators (2004). National Evaluation of Pharmacotherapies for Opioid Dependence (NEPOD): Report of Results and Recommendation (PDF). Monograph Series No. 52. Australian Government. ISBN 978-0-642-82459-2. Archived from the original (PDF) on 10 October 2012.
- ^ Thompson DR (April 2001). "Narcotic analgesic effects on the sphincter of Oddi: a review of the data and therapeutic implications in treating pancreatitis". The American Journal of Gastroenterology. 96 (4): 1266–72. doi:10.1111/j.1572-0241.2001.03536.x. PMID 11316181. S2CID 13209026.
- ^ a b c d e f Furlan AD, Sandoval JA, Mailis-Gagnon A, Tunks E (May 2006). "Opioids for chronic noncancer pain: a meta-analysis of effectiveness and side effects". CMAJ. 174 (11): 1589–94. doi:10.1503/cmaj.051528. PMC 1459894. PMID 16717269.
- ^ Stefano GB, Zhu W, Cadet P, Bilfinger TV, Mantione K (March 2004). "Morphine enhances nitric oxide release in the mammalian gastrointestinal tract via the micro(3) opiate receptor subtype: a hormonal role for endogenous morphine". Journal of Physiology and Pharmacology. 55 (1 Pt 2): 279–88. PMID 15082884.
- ^ Calignano A, Moncada S, Di Rosa M (December 1991). "Endogenous nitric oxide modulates morphine-induced constipation". Biochemical and Biophysical Research Communications. 181 (2): 889–93. doi:10.1016/0006-291X(91)91274-G. PMID 1755865.
- ^ Brennan MJ (March 2013). "The effect of opioid therapy on endocrine function". The American Journal of Medicine. 126 (3 Suppl 1): S12-8. doi:10.1016/j.amjmed.2012.12.001. PMID 23414717.
- ^ Colameco S, Coren JS (January 2009). "Opioid-induced endocrinopathy". The Journal of the American Osteopathic Association. 109 (1): 20–5. PMID 19193821.
- ^ Kerr B, Hill H, Coda B, Calogero M, Chapman CR, Hunt E, et al. (November 1991). "Concentration-related effects of morphine on cognition and motor control in human subjects". Neuropsychopharmacology. 5 (3): 157–66. PMID 1755931.
- ^ Friswell J, Phillips C, Holding J, Morgan CJ, Brandner B, Curran HV (June 2008). "Acute effects of opioids on memory functions of healthy men and women". Psychopharmacology. 198 (2): 243–50. doi:10.1007/s00213-008-1123-x. PMID 18379759. S2CID 2126631.
- ^ Galski T, Williams JB, Ehle HT (March 2000). "Effects of opioids on driving ability". Journal of Pain and Symptom Management. 19 (3): 200–8. doi:10.1016/S0885-3924(99)00158-X. PMID 10760625.
- ^ a b c Martin WR, Fraser HF (September 1961). "A comparative study of physiological and subjective effects of heroin and morphine administered intravenously in postaddicts". The Journal of Pharmacology and Experimental Therapeutics. 133: 388–99. PMID 13767429.
- ^ a b National Institute on Drug Abuse (NIDA) (April 2013). "Heroin". DrugFacts. U.S. National Institutes of Health. Archived from the original on 30 November 2005. Retrieved 29 April 2008.
- ^ Roshanpour M, Ghasemi M, Riazi K, Rafiei-Tabatabaei N, Ghahremani MH, Dehpour AR (February 2009). "Tolerance to the anticonvulsant effect of morphine in mice: blockage by ultra-low dose naltrexone". Epilepsy Research. 83 (2–3): 261–4. doi:10.1016/j.eplepsyres.2008.10.011. PMID 19059761. S2CID 21651602.
- ^ Koch T, Höllt V (February 2008). "Role of receptor internalization in opioid tolerance and dependence". Pharmacology & Therapeutics. 117 (2): 199–206. doi:10.1016/j.pharmthera.2007.10.003. PMID 18076994.
- ^ "Why do We Quit 'Cold Turkey'?". Archived from the original on 21 November 2016. Retrieved 21 November 2016.
- ^ "Opiate Withdrawal Stages". Archived from the original on 5 June 2014. Retrieved 13 June 2014.
- ^ Chan R, Irvine R, White J (February 1999). "Cardiovascular changes during morphine administration and spontaneous withdrawal in the rat". European Journal of Pharmacology. 368 (1): 25–33. doi:10.1016/S0014-2999(98)00984-4. PMID 10096766.
- ^ "Morphine (and Heroin)". Drugs and Human Performance Fact Sheets. U.S. National Traffic Safety Administration. Archived from the original on 3 October 2006. Retrieved 17 May 2007.
- ^ "Narcotics". DEA Briefs & Background, Drugs and Drug Abuse, Drug Descriptions. U.S. Drug Enforcement Administration. Archived from the original on 14 January 2012.
{{cite web}}: CS1 유지보수: 부적합한 URL(링크) - ^ Dalrymple T (2006). Romancing Opiates: Pharmacological Lies and the Addiction Bureaucracy. Encounter. pp. 160. ISBN 978-1-59403-087-1.
- ^ O'Neil MJ (2006). The Merck index : an encyclopedia of chemicals, drugs, and biological. Whitehouse Station, N.J.: Merck. ISBN 978-0-911910-00-1.
- ^ a b c d e Lide DR, ed. (2004). CRC handbook of chemistry and physics: a ready-reference book of chemical and physical data (85 ed.). Boca Ratan Florida: CRC Press. ISBN 978-0-8493-0485-9.
- ^ Medline Plus – 2016년 5월 24일 Wayback Machine 업데이트 날짜: 2009년 3월 2일에 모르핀 과다 복용이 보관되었습니다.갱신자: John E.둘드너 주니어, MD
- ^ Boyer EW (July 2012). "Management of opioid analgesic overdose". The New England Journal of Medicine. 367 (2): 146–155. doi:10.1056/NEJMra1202561. PMC 3739053. PMID 22784117.
- ^ DrugBank – 2017년 7월 11일 Wayback Machine 업데이트 날짜: 2017년 7월 11일 Morpin 아카이브 완료.
- ^ Macchiarelli L, Arbarello Cave Bondi P, Di Luca NM, Feola T (2002). Medicina Legale (compendio) (II ed.). Italy, Turin: Minerva Medica Publications.
- ^ Corbett AD, Paterson SJ, Kosterlitz HW (1993). Opioids. Handbook of Experimental Pharmacology. Vol. 104 / 1. Berlin, Heidelberg: Springer. pp. 645–679. doi:10.1007/978-3-642-77460-7_26. ISBN 978-3-642-77462-1. ISSN 0171-2004.
- ^ a b Codd EE, Shank RP, Schupsky JJ, Raffa RB (September 1995). "Serotonin and norepinephrine uptake inhibiting activity of centrally acting analgesics: structural determinants and role in antinociception". The Journal of Pharmacology and Experimental Therapeutics. 274 (3): 1263–70. PMID 7562497.
- ^ King TL, Brucker MC (25 October 2010). Pharmacology for Women's Health. Jones & Bartlett Publishers. pp. 332–. ISBN 978-1-4496-1073-9.
- ^ Flood P, Aleshi P (28 February 2014). "Postoperative and chronic pain: systemic and regional pain techniques". In Chestnut DH, Wong CA, Tsen KC, Ngan Kee WD, Beilin Y, Mhyre J (eds.). Chestnut's Obstetric Anesthesia: Principles and Practice E-Book. Elsevier Health Sciences. pp. 611–. ISBN 978-0-323-11374-8.
- ^ Tiziani AP (1 June 2013). Havard's Nursing Guide to Drugs. Elsevier Health Sciences. pp. 933–. ISBN 978-0-7295-8162-2.
- ^ Ogura T, Egan TD (2013). "Chapter 15 – Opioid Agonists and Antagonists". Pharmacology and physiology for anesthesia : foundations and clinical application. Philadelphia, PA: Elsevier/Saunders. doi:10.1016/B978-1-4377-1679-5.00015-6. ISBN 978-1-4377-1679-5.
- ^ Yekkirala AS, Kalyuzhny AE, Portoghese PS (February 2010). "Standard opioid agonists activate heteromeric opioid receptors: evidence for morphine and [d-Ala(2)-MePhe(4)-Glyol(5)]enkephalin as selective μ-δ agonists". ACS Chemical Neuroscience. 1 (2): 146–54. doi:10.1021/cn9000236. PMC 3398540. PMID 22816017.
- ^ Yekkirala AS, Banks ML, Lunzer MM, Negus SS, Rice KC, Portoghese PS (September 2012). "Clinically employed opioid analgesics produce antinociception via μ-δ opioid receptor heteromers in Rhesus monkeys". ACS Chemical Neuroscience. 3 (9): 720–7. doi:10.1021/cn300049m. PMC 3447399. PMID 23019498.
- ^ a b "MS-Contin (Morphine Sulfate Controlled-Release) Drug Information: Clinical Pharmacology". Prescribing Information. RxList. Archived from the original on 15 May 2007.
- ^ Kelly E (August 2013). "Efficacy and ligand bias at the μ-opioid receptor". British Journal of Pharmacology. 169 (7): 1430–46. doi:10.1111/bph.12222. PMC 3724102. PMID 23646826.
- ^ Chien CC, Pasternak GW (May 1995). "Sigma antagonists potentiate opioid analgesia in rats". Neuroscience Letters. 190 (2): 137–9. doi:10.1016/0304-3940(95)11504-P. PMID 7644123. S2CID 10033780.
- ^ Herman BH, Vocci F, Bridge P (December 1995). "The effects of NMDA receptor antagonists and nitric oxide synthase inhibitors on opioid tolerance and withdrawal. Medication development issues for opiate addiction". Neuropsychopharmacology. 13 (4): 269–93. doi:10.1016/0893-133X(95)00140-9. PMID 8747752.
- ^ Loguinov AV, Anderson LM, Crosby GJ, Yukhananov RY (August 2001). "Gene expression following acute morphine administration". Physiological Genomics. 6 (3): 169–81. doi:10.1152/physiolgenomics.2001.6.3.169. PMID 11526201. S2CID 9296949.
- ^ Messmer D, Hatsukari I, Hitosugi N, Schmidt-Wolf IG, Singhal PC (2006). "Morphine reciprocally regulates IL-10 and IL-12 production by monocyte-derived human dendritic cells and enhances T cell activation". Molecular Medicine. 12 (11–12): 284–90. doi:10.2119/2006-00043.Messmer. PMC 1829197. PMID 17380193.
- ^ Clark JD, Shi X, Li X, Qiao Y, Liang D, Angst MS, Yeomans DC (October 2007). "Morphine reduces local cytokine expression and neutrophil infiltration after incision". Molecular Pain. 3: 1744-8069–3-28. doi:10.1186/1744-8069-3-28. PMC 2096620. PMID 17908329.
- ^ Trescot AM, Datta S, Lee M, Hansen H (March 2008). "Opioid pharmacology". Pain Physician. 11 (2 Suppl): S133-53. doi:10.36076/ppj.2008/11/S133. PMID 18443637.
- ^ Kilpatrick GJ, Smith TW (September 2005). "Morphine-6-glucuronide: actions and mechanisms". Medicinal Research Reviews. 25 (5): 521–44. doi:10.1002/med.20035. PMID 15952175. S2CID 20887610.
- ^ a b van Dorp EL, Romberg R, Sarton E, Bovill JG, Dahan A (June 2006). "Morphine-6-glucuronide: morphine's successor for postoperative pain relief?". Anesthesia and Analgesia. 102 (6): 1789–97. doi:10.1213/01.ane.0000217197.96784.c3. PMID 16717327. S2CID 18890026. Archived from the original on 1 December 2008.
- ^ a b Jenkins AJ (2008) 특정 약물의 약물역학.Karch SB(Ed), 약물역학 및 약물역학.CRC 프레스: Boca Raton.
- ^ a b c "Morphine, slow release (By mouth)". University of Maryland Medical Center. Archived from the original on 22 December 2015.
- ^ Pedersen L, Fredheim O (February 2015). "Opioids for chronic noncancer pain: still no evidence for superiority of sustained-release opioids". Clinical Pharmacology and Therapeutics. 97 (2): 114–5. doi:10.1002/cpt.26. PMID 25670511. S2CID 5603973. 최종 리뷰는 2015년 11월 18일
- ^ a b "Dosing & Uses". Medscape. Archived from the original on 31 October 2015. Retrieved 21 December 2015.
- ^ a b "EndLink: An Internet-based End of Life Care Education Program – Morphine Dosing" (PDF). Northwestern University. Archived (PDF) from the original on 4 March 2016.
- ^ Baselt RC (2008). Disposition of Toxic Drugs and Chemicals in Man (8th ed.). Foster City, CA: Biomedical Publications. pp. 1057–1062. ISBN 978-0-9626523-7-0.
- ^ Vandevenne M, Vandenbussche H, Verstraete A (2000). "Detection time of drugs of abuse in urine". Acta Clinica Belgica. 55 (6): 323–33. doi:10.1080/17843286.2000.11754319. PMID 11484423. S2CID 43808583.
- ^ Verstraete AG (April 2004). "Detection times of drugs of abuse in blood, urine, and oral fluid". Therapeutic Drug Monitoring. 26 (2): 200–5. doi:10.1097/00007691-200404000-00020. PMID 15228165. S2CID 385874.
- ^ Kapoor L (1995). Opium Poppy: Botany, Chemistry, and Pharmacology. United States: CRC Press. p. 164. ISBN 978-1-56024-923-8.
- ^ Vincent PG, Bare CE, Gentner WA (December 1977). "Thebaine content of selections of Papaver bracteatum Lindl. at different ages". Journal of Pharmaceutical Sciences. 66 (12): 1716–9. doi:10.1002/jps.2600661215. PMID 925935.
- ^ Stewart O (2000). Functional Neuroscience. New York: Springer. p. 116. ISBN 978-0-387-98543-5.
- ^ "μ receptor". IUPHAR/BPS Guide to PHARMACOLOGY. International Union of Basic and Clinical Pharmacology. 15 March 2017. Archived from the original on 7 November 2017. Retrieved 28 December 2017.
Morphine occurs endogenously
- ^ a b Poeaknapo C, Schmidt J, Brandsch M, Dräger B, Zenk MH (September 2004). "Endogenous formation of morphine in human cells". Proceedings of the National Academy of Sciences of the United States of America. 101 (39): 14091–6. Bibcode:2004PNAS..10114091P. doi:10.1073/pnas.0405430101. PMC 521124. PMID 15383669.
Without doubt, human cells can produce the alkaloid morphine.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). "The endogenous substrates of brain CYP2D". European Journal of Pharmacology. 724: 211–8. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
Additionally, CYP2D is involved in the synthesis of endogenous morphine from various precursors, including L-3,4-dihydroxyphenylalanine (L-DOPA), reticulin, tetrahydropapaveroline (THP), and tyramine (Kulkarni, 2001; Mantione et al., 2008; Zhu, 2008).
- ^ Novak B, Hudlicky T, Reed J, Mulzer J, Trauner D (March 2000). "Morphine Synthesis and Biosynthesis-An Update" (PDF). Current Organic Chemistry. 4 (3): 343–362. CiteSeerX 10.1.1.515.9096. doi:10.2174/1385272003376292. Archived (PDF) from the original on 19 June 2012.
- ^ Le Page M (18 May 2015). "Home-brew heroin: soon anyone will be able to make illegal drugs". New Scientist. Archived from the original on 13 April 2016.
- ^ Service RF (25 June 2015). "Final step in sugar-to-morphine conversion deciphered". Science. Archived from the original on 21 August 2015.
- ^ Galanie S, Thodey K, Trenchard IJ, Filsinger Interrante M, Smolke CD (September 2015). "Complete biosynthesis of opioids in yeast". Science. 349 (6252): 1095–100. Bibcode:2015Sci...349.1095G. doi:10.1126/science.aac9373. PMC 4924617. PMID 26272907.
- ^ "Yeast-Based Opioid Production Completed". 13 August 2015. Archived from the original on 7 September 2015. Retrieved 15 August 2015.
- ^ Olawale DO, Okoli OO, Fontenot RS, Hollerman WA (2016). Triboluminescence: Theory, Synthesis, and Application (illustrated ed.). Springer. p. 193. ISBN 9783319388427. 193페이지 발췌
- ^ DeRuiter J (Fall 2000). "Narcotic analgesics: morphine and "peripherally modified" morphine analogs" (PDF). Principles of Drug Action 2. Auburn University. Archived (PDF) from the original on 11 January 2012.
- ^ Way EL, Adler TK (1962). "The biological disposition of morphine and its surrogates". Bulletin of the World Health Organization. 27: 359–394. PMC 2555766. PMID 13999272.
- ^ "UNODC - Bulletin on Narcotics - 1958 Issue 3 - 005". United Nations : Office on Drugs and Crime. Retrieved 11 February 2022.
- ^ Loftsson T (2013). Drug Stability for Pharmaceutical Scientists. Elsevier Science & Technology. p. 82. OCLC 1136560730.
- ^ 제가 내용물을 통치하고 그래서 임상적으로 미국에서 사용되지 않는다 헤로인(모르핀 이초산염)은 일정, 영국, 캐나다에서[표창 필요한]그것은 인정된 약물과 유럽 대륙의 일부 국가, 그것의 사용 특히 일반적인(그 염산 소금의 정도에 이르게 해)[해명 필요한]에. 영본국[표창 필요한]
- ^ 모르핀 발라테는 수년 전 유럽과 트리발린이라고 불리는 다른 곳에서 인기 있었던 경구 및 비경구 투여에 사용할 수 있는 약물의 성분 중 하나였습니다. - 카페인과 [citation needed]코카인의 발라테이트를 포함한 현재의, 관련이 없는 허브 제제와 혼동하지 마십시오.코데인발라테를 제4성분으로 함유하는 버전을 테트라발린이라는 [citation needed]이름으로 배포한다.
- ^ Gates M, Tschudi G (April 1956). "The Synthesis of Morphine". Journal of the American Chemical Society. 78 (7): 1380–1393. doi:10.1021/ja01588a033.
- ^ Rice KC (July 1980). "Synthetic opium alkaloids and derivatives. A short total synthesis of (±)-dihydrothebainone, (±)-dihydrocodeinone, and (±)-nordihydrocodeinone as an approach to a practical synthesis of morphine, codeine, and congeners". The Journal of Organic Chemistry. 45 (15): 3135–3137. doi:10.1021/jo01303a045.
- ^ Evans DA, Mitch CH (January 1982). "Studies directed towards the total synthesis of morphine alkaloids". Tetrahedron Letters. 23 (3): 285–288. doi:10.1016/S0040-4039(00)86810-0.
- ^ Toth JE, Hamann PR, Fuchs PL (September 1988). "Studies culminating in the total synthesis of (dl)-morphine". The Journal of Organic Chemistry. 53 (20): 4694–4708. doi:10.1021/jo00255a008.
- ^ Parker KA, Fokas D (November 1992). "Convergent synthesis of (±)-dihydroisocodeine in 11 steps by the tandem radical cyclization strategy. A formal total synthesis of (±)-morphine". Journal of the American Chemical Society. 114 (24): 9688–9689. doi:10.1021/ja00050a075.
- ^ Hong CY, Kado N, Overman LE (November 1993). "Asymmetric synthesis of either enantiomer of opium alkaloids and morphinans. Total synthesis of (−)- and (+)-dihydrocodeinone and (−)- and (+)-morphine". Journal of the American Chemical Society. 115 (23): 11028–11029. doi:10.1021/ja00076a086.
- ^ Mulzer J, Dürner G, Trauner D (December 1996). "Formal Total Synthesis of(—)-Morphine by Cuprate Conjugate Addition". Angewandte Chemie International Edition in English. 35 (2324): 2830–2832. doi:10.1002/anie.199628301.
- ^ White JD, Hrnciar P, Stappenbeck F (October 1999). "Asymmetric Total Synthesis of (+)-Codeine via Intramolecular Carbenoid Insertion". The Journal of Organic Chemistry. 64 (21): 7871–7884. doi:10.1021/jo990905z.
- ^ Taber DF, Neubert TD, Rheingold AL (October 2002). "Synthesis of (-)-morphine". Journal of the American Chemical Society. 124 (42): 12416–7. doi:10.1021/ja027882h. PMID 12381175. S2CID 32048193.
- ^ Trost BM, Tang W (December 2002). "Enantioselective synthesis of (-)-codeine and (-)-morphine". Journal of the American Chemical Society. 124 (49): 14542–3. doi:10.1021/ja0283394. PMID 12465957.
- ^ Uchida K, Yokoshima S, Kan T, Fukuyama T (November 2006). "Total synthesis of (+/-)-morphine". Organic Letters. 8 (23): 5311–3. doi:10.1021/ol062112m. PMID 17078705.
- ^ Varin M, Barré E, Iorga B, Guillou C (2008). "Diastereoselective total synthesis of (+/-)-codeine". Chemistry. 14 (22): 6606–8. doi:10.1002/chem.200800744. PMID 18561354.
- ^ Stork G, Yamashita A, Adams J, Schulte GR, Chesworth R, Miyazaki Y, Farmer JJ (August 2009). "Regiospecific and stereoselective syntheses of (+/-) morphine, codeine, and thebaine via a highly stereocontrolled intramolecular 4 + 2 cycloaddition leading to a phenanthrofuran system". Journal of the American Chemical Society. 131 (32): 11402–6. doi:10.1021/ja9038505. PMID 19624126.
- ^ Freemantle M (20 June 2005). "The Top Pharmaceuticals That Changed The World-Morphine". Chemical and Engineering News.
- ^ "Narcotics (Opioids) DEA". www.dea.gov. Retrieved 21 January 2021.
- ^ Crews JC, Denson DD (December 1990). "Recovery of morphine from a controlled-release preparation. A source of opioid abuse". Cancer. 66 (12): 2642–4. doi:10.1002/1097-0142(19901215)66:12<2642::AID-CNCR2820661229>3.0.CO;2-B. PMID 2249204.
- ^ Ramoutsaki IA, Askitopoulou H, Konsolaki E (December 2002). "Pain relief and sedation in Roman Byzantine texts: Mandragoras officinarum, Hyoscyamos niger and Atropa belladonna". International Congress Series. 1242: 43–50. doi:10.1016/S0531-5131(02)00699-4.
- ^ Sigerist HE (1941). "Laudanum in the Works of Paracelsus" (PDF). Bull. Hist. Med. 9: 530–544. Retrieved 5 September 2018.
- ^ Friedrich Sertürner (1805) (편집자에게 보내는 무제 편지) 2016년 8월 17일 Wayback Machine, Journal der Pharmacie für Aerzte, Apotherker und Chemeren (의사, 약사, 약사 및 화학자를 위한 약학 저널), 13:9-243 참조III. Saure im App. 234–235 그리고 "I.나흐트락 주르 샤라크테리스틱 데르 사우레 임 아편", 236–241페이지.
- ^ a b Dahan A, Aarts L, Smith TW (January 2010). "Incidence, Reversal, and Prevention of Opioid-induced Respiratory Depression". Anesthesiology. 112 (1): 226–38. doi:10.1097/ALN.0b013e3181c38c25. PMID 20010421.
- ^ 세르튀르너는 세르튀르너(1817년)에서 모르피움이라는 용어를 만들었다: "에베르 다스 모르피움, 에인느 살즈페히게 그룬들라지, 운드 다이 메콘새어, 알스 합베스트랑데아편" (모르핀, 즉 새로운 염분성, 기본 성분인 메콘산 성분)프랑스 화학자이자 Anales de Chimie et de Feechety의 편집자인 게이-루삭은 세르튀너의 독일어 원문을 프랑스어 번역본에서 모르핀이라는 단어를 만들었다.Sertuener(1817) "로피움 분석: "De la morpin et de l'acide meconique, commés parties essentielles de l'opium"(아편 분석:모르핀 및 아편의 필수 성분으로 간주되는 메콘산에 대하여 Annales de Chimie et de Ficeture, 두 번째 시리즈, 5:21~42.22페이지부터: "... car il pour cette 물질, que j'appel morpium(모르피움), ce qui n'et qu'en combinaison l'acide de l'opium." (... 즉, 프랑스의 화학자이자 약사인 Charles Derosne(1780–1846)은 이 활성 물질로 섭취했다.아편산과의 화합물)
- ^ Offit P (March–April 2017). "God's Own Medicine". Skeptical Inquirer. 41 (2): 44.
- ^ Annual Register. J. Dodsley. 1824. p. 1. Retrieved 1 September 2015.
Edme.
- ^ Kirsch, Donald R. (2016). Drug Hunters. Arcade Publishing. ISBN 978-1-62872-719-7. OCLC 966360188.
- ^ Cocaine global histories. Paul Gootenberg. London: Routledge. 1999. p. 90. ISBN 92-9078-018-5. OCLC 1162209949.
{{cite book}}: CS1 유지보수: 기타 (링크) - ^ Davenport-Hines R (2003). The Pursuit of Oblivion: A Global History of Narcotics. W.W. Norton. p. 68. ISBN 978-0-393-32545-4.
- ^ Vassallo SA (July 2004). "Lewis H. Wright Memorial Lecture". ASA Newsletter. 68 (7): 9–10. Archived from the original on 2 February 2014.
- ^ "Opiate Narcotics". The Report of the Canadian Government Commission of Inquiry into the Non-Medical Use of Drugs. Canadian Government Commission. Archived from the original on 4 April 2007.
- ^ Mandel J. "Mythical Roots of US Drug Policy – Soldier's Disease and Addicts in the Civil War". Archived from the original on 5 April 2007.
- ^ "Soldiers Disease A Historical Hoax?". iPromote Media Inc. 2006. Archived from the original on 27 September 2007.
- ^ Winger G, Hursh SR, Casey KL, Woods JH (May 2002). "Relative reinforcing strength of three N-methyl-D-aspartate antagonists with different onsets of action". The Journal of Pharmacology and Experimental Therapeutics. 301 (2): 690–7. doi:10.1124/jpet.301.2.690. PMID 11961074. S2CID 17860947.
- ^ "Morphine Easy Home Cure". Overland Monthly. 35 (205): 14. 1900. Archived from the original on 1 February 2014.
- ^ Gulland JM, Robinson R (1925). "Constitution of codeine and thebaine". Memoirs and Proceedings of the Literary and Philosophical Society of Manchester. 69: 79–86.
- ^ Dickman S (3 October 2003). "Marshall D. Gates, Chemist to First Synthesize Morphine, Dies". Press Release. University of Rochester. Archived from the original on 1 December 2010.
- ^ Bayer I (July 1987). "[János Kabay and the poppy straw process. Commemoration on the 50th anniversary of his death]". Acta Pharmaceutica Hungarica. 57 (3–4): 105–10. PMID 3314338.
- ^ Zhu W, Cadet P, Baggerman G, Mantione KJ, Stefano GB (December 2005). "Human white blood cells synthesize morphine: CYP2D6 modulation". Journal of Immunology. 175 (11): 7357–62. doi:10.4049/jimmunol.175.11.7357. PMID 16301642.
- ^ Anlage III (zu 11 Abs. 1) verkehrsféhige und verschreibungsféhige Betaeubungsmittel 2014년 4월 28일 웨이백 머신에 보관
- ^ "Misuse of Drugs Act 1975, sch 2". 13 January 2022. Archived from the original on 27 January 2021.
- ^ 82 FR 51293
- ^ "List of narcotic drugs under international control" (PDF). Yellow List (PDF) (50th ed.): 5. March 2011. Archived (PDF) from the original on 22 December 2014.
- ^ "Morphia Definition of Morphia by Lexico". Lexico Dictionaries English. Retrieved 14 September 2019.
- ^ Miller RL (1 January 2002). The Encyclopedia of Addictive Drugs. Greenwood Publishing Group. p. 306. ISBN 978-0-313-31807-8.
- ^ Milani B. Scholten (3rd ed.). Switzerland: World Health Organization. pp. 1–22. Archived from the original on 5 June 2018. Retrieved 17 January 2018.
- ^ Human Rights Watch (2 June 2011). "Global State of Pain Treatment; Access to Palliative Care as a Human Right". Human Rights Watch. Retrieved 27 January 2020.
- ^ McNeil Jr DG (10 September 2007). "Drugs Banned, Many of World's Poor Suffer in Pain". New York Times. Archived from the original on 11 May 2011. Retrieved 11 September 2007.
외부 링크
- "Morphine". Drug Information Portal. U.S. National Library of Medicine.
- 주기율표 비디오의 모르핀과 헤로인(노팅엄 대학)
- 비디오: 정맥내 모르핀 로드(Vimeo)(YouTube)– 건강 전문가에게 진통제, 특히 모르핀의 정맥내 로딩에 관한 요점을 가르치는 짧은 교육 비디오.