RB-101
RB-101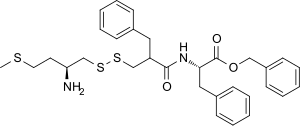 | |
 | |
| 임상자료 | |
|---|---|
| 기타 이름 | RB-101; 페닐메틸(2S)-2-[(2S)-2-아미노-4-메틸설파닐부틸]-3-페닐프로필아미노산염)-3-페닐프로필아미노산염]-3-페닐프로필산염 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 켐스파이더 | |
| CompTox 대시보드 (EPA) | |
| 화학 및 물리적 데이터 | |
| 공식 | C31H38N2O3S3 |
| 어금질량 | 582.84 g·190−1 |
| 3D 모델(JSmol) | |
| |
| |
| (iii) | |
RB-101은 과학 연구에 사용되는 뇌파화효소 억제제 역할을 하는 약물이다.
RB-101은 이황화합물에서 뇌 내부를 한 번 분열시켜 두 가지 선택적 효소 억제제를 형성하고 아연-금속활소화효소 엥케팔리네아제 효소를 모두 차단하는 작용을 하는 프로드러제다. 이것은 엔케팔린으로 알려진 내생성 오피오이드 펩타이드의 분해를 억제한다.[1] 이 두 효소인 아미노펩티다아제 N(APN)과 중성 엔도펩타아제 24.11(NEP)는 체내에서 자연적으로 발견되는 두 종류의 엥케팔린이 모두 분해되는 원인이므로 RB-101은 메트-엥팔린과 르우-엥팔핀의 축적을 일으킨다.[2][3]
이러한 펩타이드들은 주로 델타 오피오이드 수용체에 작용하지만, 다른 펩타이드 셸시스토키닌과의 델타-오피오이드 수용체 매개 상호작용을 통해서도 뮤오피오이드 수용체를 어느 정도 자극하고, RB-101의 효소 억제 효과는 따라서 이 두 오피오이드 수용체 아형의 간접 자극을 생성한다.[4] 이로 인해 RB-101은 프로글루미드와 같은 첼시스토킨 대항제와 강한 시너지 효과를 발휘하게 된다.[5][6]
주변 작용만 하고 지사작용도 하지 않는 더 흔히 사용되는 뇌파 억제제 레이스카도트릴과 달리 RB-101은 뇌에 들어갈 수 있어 다양한 효과를 만들어 진통제, 항불안제, 항우울제 역할을 한다.[7] 항우울제와 항불안제 작용은 델타 오피오이드 수용체를 통해 매개되는 것으로 생각되며, 진통 효과는 mu와 델타 활성의 혼합에서 발생할 가능성이 가장 높다.[8] 동물 연구에서는 RB-101이 급성 오피오이드 철수의[9] 증상 완화와 오피오이드 의존성 관리에도 유용할 가능성이 있다고 보고 있다.[10][11][12]
오피오이드 수용체를 외생성 약물로 자극하기보다는 내생성 오피오이드 펩타이드의 분해를 억제할 수 있는 유의적인 장점은 오피오이드 펩타이드의 수치가 자연수준에서 약간만 증가하여 오피오이드 수용체의 과도한 자극과 하한을 피한다는 것이다. 이는 RB-101을 장시간 고선량으로 사용해도 약물에 대한 의존성이나 진통 효과에 대한 내성이 발달하지 않는다는 것을 의미한다.[13][14] 따라서 RB-101은 오피오이드 시스템을 통해 강력한 진통 효과를 낼 수 있지만 중독성이 없을 것으로 보인다.[15][16]
기존 오피오이드 작용제와 달리 RB-101도 호흡기 우울증을 일으키지 못해 기존 오피오이드 진통제보다 훨씬 안전한 약물이 될 수 있음을 시사했다.[17] RB-101은 또한 이부프로펜과 모르핀과 같은 전통적인 진통제의 효과를 강력하게 촉진시켰으며, 그렇지 않으면 효과가 없을 수 있는 낮은 용량의 정상 오피오이드의 작용을 촉진시키는데 사용될 수 있음을 시사했다.[18]
RB-101 자체는 구강 활성화가 아니므로 인체에서 의료용으로 개발되지 않았지만, 이 약물의 변경으로 인해 RB-120과 RB-3007과 같은 구강 작용 화합물이 새로 생겨 임상시험에 성공할 경우 의료용으로 채택될 가능성이 더 높다.[19][20][21][22][23]
참고 항목
참조
- ^ Roques BP (April 1992). "Peptidomimetics as receptors agonists or peptidase inhibitors: A structural approach in the field of enkephalins, ANP and CCK". Biopolymers. 32 (4): 407–10. doi:10.1002/bip.360320417. PMID 1320419.
- ^ Noble F, Soleilhac JM, Soroca-Lucas E, Turcaud S, Fournie-Zaluski MC, Roques BP (April 1992). "Inhibition of the enkephalin-metabolizing enzymes by the first systemically active mixed inhibitor prodrug RB 101 induces potent analgesic responses in mice and rats". The Journal of Pharmacology and Experimental Therapeutics. 261 (1): 181–90. PMID 1560364.
- ^ Fournié-Zaluski MC, Coric P, Turcaud S, Lucas E, Noble F, Maldonado R, Roques BP (Jun 1992). "Mixed inhibitor-prodrug" as a new approach toward systemically active inhibitors of enkephalin-degrading enzymes". Journal of Medicinal Chemistry. 35 (13): 2473–81. doi:10.1021/jm00091a016. PMID 1352352.
- ^ Noble F, Smadja C, Roques BP (December 1994). "Role of endogenous cholecystokinin in the facilitation of mu-mediated antinociception by delta-opioid agonists". The Journal of Pharmacology and Experimental Therapeutics. 271 (3): 1127–34. PMID 7996417.
- ^ Valverde O, Maldonado R, Fournie-Zaluski MC, Roques BP (July 1994). "Cholecystokinin B antagonists strongly potentiate antinociception mediated by endogenous enkephalins". The Journal of Pharmacology and Experimental Therapeutics. 270 (1): 77–88. PMID 8035345.
- ^ Honore P, Buritova J, Fournié-Zaluski MC, Roques BP, Besson JM (April 1997). "Antinociceptive effects of RB101, a complete inhibitor of enkephalin-catabolizing enzymes, are enhanced by a cholecystokinin type B receptor antagonist, as revealed by noxiously evoked spinal c-Fos expression in rats". The Journal of Pharmacology and Experimental Therapeutics. 281 (1): 208–17. PMID 9103499.
- ^ Jutkiewicz EM, Torregrossa MM, Sobczyk-Kojiro K, et al. (February 2006). "Behavioral and neurobiological effects of the enkephalinase inhibitor RB101 relative to its antidepressant effects". European Journal of Pharmacology. 531 (1–3): 151–9. doi:10.1016/j.ejphar.2005.12.002. PMC 1828120. PMID 16442521.
- ^ Jutkiewicz EM (2007). "RB101-mediated Protection of Endogenous Opioids: Potential Therapeutic Utility?" (PDF). CNS Drug Reviews. 13 (2): 192–205. doi:10.1111/j.1527-3458.2007.00011.x. PMC 6726351. PMID 17627672.
- ^ Maldonado R, Valverde O, Ducos B, Blommaert AG, Fournie-Zaluski MC, Roques BP (March 1995). "Inhibition of morphine withdrawal by the association of RB 101, an inhibitor of enkephalin catabolism, and the CCKB antagonist PD-134,308". British Journal of Pharmacology. 114 (5): 1031–9. doi:10.1111/j.1476-5381.1995.tb13309.x. PMC 1510310. PMID 7780637.
- ^ Ruiz F, Fournié-Zaluski MC, Roques BP, Maldonado R (September 1996). "Similar decrease in spontaneous morphine abstinence by methadone and RB 101, an inhibitor of enkephalin catabolism". British Journal of Pharmacology. 119 (1): 174–82. doi:10.1111/j.1476-5381.1996.tb15691.x. PMC 1915744. PMID 8872371.
- ^ Roques BP, Noble F (November 1996). "Association of enkephalin catabolism inhibitors and CCK-B antagonists: a potential use in the management of pain and opioid addiction". Neurochemical Research. 21 (11): 1397–410. doi:10.1007/bf02532381. PMID 8947930.
- ^ Cordonnier L, Sanchez M, Roques BP, Noble F (May 2007). "Blockade of morphine-induced behavioral sensitization by a combination of amisulpride and RB101, comparison with classical opioid maintenance treatments". British Journal of Pharmacology. 151 (1): 94–102. doi:10.1038/sj.bjp.0707195. PMC 2012985. PMID 17351659.
- ^ Noble F, Turcaud S, Fournié-Zaluski MC, Roques BP (November 1992). "Repeated systemic administration of the mixed inhibitor of enkephalin-degrading enzymes, RB101, does not induce either antinociceptive tolerance or cross-tolerance with morphine". European Journal of Pharmacology. 223 (1): 83–9. doi:10.1016/0014-2999(92)90821-K. PMID 1478260.
- ^ Noble F, Coric P, Turcaud S, Fournié-Zaluski MC, Roques BP (March 1994). "Assessment of physical dependence after continuous perfusion into the rat jugular vein of the mixed inhibitor of enkephalin-degrading enzymes, RB 101". European Journal of Pharmacology. 253 (3): 283–7. doi:10.1016/0014-2999(94)90203-8. PMID 8200422.
- ^ Noble F, Fournié-Zaluski MC, Roques BP (January 1993). "Unlike morphine the endogenous enkephalins protected by RB101 are unable to establish a conditioned place preference in mice". European Journal of Pharmacology. 230 (2): 139–49. doi:10.1016/0014-2999(93)90796-K. PMID 8422896.
- ^ Stein, edited by Christoph (1999). Opioids in pain control : basic and clinical aspects. Cambridge, UK: Cambridge University Press. ISBN 978-0521622691.CS1 maint: 추가 텍스트: 작성자 목록(링크)
- ^ Boudinot E, Morin-Surun M, Foutz AS, Fournié-Zaluski M, Roques BP, Denavit-Saubié M (February 2001). "Effects of the potent analgesic enkephalin-catabolizing enzyme inhibitors RB101 and kelatorphan on respiration". Pain. 90 (1–2): 7–13. doi:10.1016/S0304-3959(00)00382-1. PMID 11166965.
- ^ Nieto MM, Wilson J, Walker J, et al. (September 2001). "Facilitation of enkephalins catabolism inhibitor-induced antinociception by drugs classically used in pain management". Neuropharmacology. 41 (4): 496–506. doi:10.1016/S0028-3908(01)00077-6. PMID 11543770.
- ^ Noble F, Smadja C, Valverde O, et al. (December 1997). "Pain-suppressive effects on various nociceptive stimuli (thermal, chemical, electrical and inflammatory) of the first orally active enkephalin-metabolizing enzyme inhibitor RB 120". Pain. 73 (3): 383–91. doi:10.1016/S0304-3959(97)00125-5. PMID 9469529.
- ^ Le Guen S, Mas Nieto M, Canestrelli C, et al. (July 2003). "Pain management by a new series of dual inhibitors of enkephalin degrading enzymes: long lasting antinociceptive properties and potentiation by CCK2 antagonist or methadone". Pain. 104 (1–2): 139–48. doi:10.1016/S0304-3959(02)00486-4. PMID 12855323.
- ^ Le Guen S, Mas Nieto M, Canestrelli C, Chen H, Fournié-Zaluski MC, Cupo A, Maldonado R, Roques BP, Noble F (July 2003). "Pain management by a new series of dual inhibitors of enkephalin degrading enzymes: long lasting antinociceptive properties and potentiation by CCK2 antagonist or methadone". Pain. 104 (1–2): 139–48. doi:10.1016/S0304-3959(02)00486-4. PMID 12855323.
- ^ Noble F, Roques BP (February 2007). "Protection of endogenous enkephalin catabolism as natural approach to novel analgesic and antidepressant drugs". Expert Opinion on Therapeutic Targets. 11 (2): 145–59. doi:10.1517/14728222.11.2.145. PMID 17227231.
- ^ Thanawala V, Kadam VJ, Ghosh R (October 2008). "Enkephalinase inhibitors: potential agents for the management of pain". Current Drug Targets. 9 (10): 887–94. doi:10.2174/138945008785909356. PMID 18855623.


