티로신
Tyrosine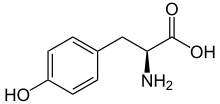 L-티로신의 골격식 | |||
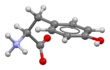
 생리학적 pH에서 L-Tyrosine | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC명 (S-티로신 | |||
| 기타명 L-2-아미노-3-(4-하이드록시페닐)프로판산 | |||
| 식별자 | |||
| |||
3D 모델(JSmol) | |||
| ChEBI | |||
| CHEMBL | |||
| 켐스파이더 | |||
| 드럭뱅크 | |||
| ECHA 인포카드 | 100.000.419 | ||
| 케그 | |||
펍켐 CID | |||
| 유니 | |||
CompTox 대시보드 (EPA) | |||
| |||
| |||
| 특성. | |||
| C9H11NO3 | |||
| 어금니 질량 | 181.191 g·mol−1 | ||
| 외모 | 흰 고체 | ||
| .0453 g/100 mL | |||
| -105.3·10−6 cm3/mol | |||
| 위험성 | |||
| NFPA 704 (파이어다이아몬드) | |||
| 보충자료페이지 | |||
| 티로신(데이터페이지) | |||
달리 명시된 경우를 제외하고 표준 상태의 재료에 대한 데이터가 제공됩니다(25°C [77°F], 100kPa). | |||
L-티로신 또는 티로신(기호 Tyr 또는 Y)[2] 또는 4-하이드록시페닐알라닌은 세포가 단백질을 합성하는 데 사용하는 20가지 표준 아미노산 중 하나입니다. 극성 측기를 가진 비필수 아미노산입니다. "티로신"이라는 단어는 1846년 독일 화학자 유스투스 폰 리비히가 치즈의 단백질 카제인에서 처음 발견했기 때문에 치즈를 의미하는 그리스어 티로스에서 유래되었습니다.[3][4] 작용기 또는 측쇄라고 할 때 티로실이라고 합니다. 티로신은 일반적으로 소수성 아미노산으로 분류되지만 페닐알라닌보다 친수성이 강합니다.[5] 메신저 RNA의 코돈 UAC와 UAU에 의해 암호화됩니다.
한 글자 기호 Y는 사용 가능한 문자 중 알파벳으로 가장 가깝기 때문에 티로신에 할당되었습니다. T는 구조적으로 더 단순한 트레오닌에 할당되었고, U는 발린에 대해 V와 유사성 때문에 회피되었으며, W는 트립토판에 할당된 반면 X는 미결정 또는 비정형 아미노산에 대해 예약되었습니다.[6] 기억력 있는 Yrosine도 제안되었습니다.[7]
기능들
티로신은 단백질 생성 아미노산 외에도 페놀 기능 때문에 특별한 역할을 합니다. 히드록시기는 특히 인산염과 에스테르 결합을 형성할 수 있습니다. 인산기는 단백질 키나제를 통해 티로신 잔기로 전달됩니다. 이것은 번역 후 수정 중 하나입니다. 인산화된 티로신은 신호 전달 과정의 일부인 단백질에서 발생합니다.
세린과 트레오닌에서도 비슷한 기능성이 나타나는데, 이들의 측쇄는 하이드록시기를 가지지만 알코올입니다. 이 세 아미노산의 부분(티로신 포함)의 인산화는 이들의 말단에 음전하를 생성하는데, 이는 음전하를 띤 유일한 아스파르트산과 글루탐산의 음전하보다 더 큽니다. 인산화된 단백질은 포스포티로신, 포스포세린 및 포스포트레오닌을 통해 보다 신뢰할 수 있는 단백질-단백질 상호작용에 유용한 이러한 특성을 유지합니다.[8]
신호 전달 인단백질의 결합 부위는 화학적 구조가 다양할 수 있습니다.[9]
하이드록실 그룹의 인산화는 표적 단백질의 활성을 변화시키거나 SH2 도메인 결합을 통한 신호 전달 캐스케이드의 일부를 형성할 수 있습니다.[10]
티로신 잔기는 광합성에서도 중요한 역할을 합니다. 엽록체(광계 II)에서는 산화된 엽록소의 환원에 전자 공여체 역할을 합니다. 이 과정에서 페놀성 OH-기의 수소 원자를 잃게 됩니다. 이 라디칼은 이후 네 개의 코어 망간 클러스터에 의해 광계 II에서 감소됩니다.[11]
식이 요구 사항 및 출처
티로신의 식이 기준 섭취량은 일반적으로 페닐알라닌과 함께 추정됩니다. 추정 방법에 따라 다르지만 인체는 이와 같은 성분을 가지고 있으므로 이 두 아미노산의 이상적인 비율은 60:40(페닐알라닌:티로신)으로 생각됩니다.[12] 페닐알라닌으로부터 체내에서도 합성될 수 있는 티로신은 고기, 생선, 치즈, 코티지 치즈, 우유, 요구르트, 땅콩, 아몬드, 호박씨, 참깨, 콩 단백질 및 리마콩과 같은 많은 고단백 식품에서 발견됩니다.[13][14] 예를 들어, 달걀의 흰자는 달걀 한 개당 약 250mg을 가지고 있는 반면,[15] 쇠고기, 양고기, 돼지고기, 참치, 연어, 닭고기, 칠면조는 3온스(85g) 당 약 500-1000mg을 포함하고 있습니다.[15][16]
생합성

티로신은 식물과 대부분의 미생물에서 시키메이트 경로의 중간체인 프리페네이트를 통해 생성됩니다. 프리페네이트는 산화적으로 하이드록실기의 보유와 함께 탈카르복실화되어 p-하이드록시페닐피루브산을 제공하며, 이는 질소 공급원으로 글루타메이트를 사용하여 티로신과 α-케토글루타레이트를 제공하기 위해 트랜스아민화됩니다.
포유류는 음식에서 유래한 필수 아미노산 페닐알라닌(Phe)에서 티로신을 합성합니다. Phe에서 Tyr로의 전환은 모노옥시게나제인 효소 페닐알라닌 하이드록실라제에 의해 촉매됩니다. 이 효소는 페닐알라닌의 6-탄소 방향족 고리의 말단에 하이드록실기를 추가하여 티로신이 되는 반응을 촉매합니다.
대사

인산화 및 황산화
티로신 잔기 중 일부는 단백질 키나제에 의해 인산기(인산화)로 태그(hydroxyl group)될 수 있습니다. 티로신은 인산화된 형태로 포스포티로신이라고 불립니다. 티로신 인산화는 신호 전달 및 효소 활성 조절의 핵심 단계 중 하나로 간주됩니다. 포스포티로신은 특정 항체를 통해 검출될 수 있습니다. 티로신 잔기는 또한 티로신 설페이트화로 알려진 과정인 황산염기의 첨가에 의해 변형될 수 있습니다.[17] 티로신 황산화는 티로실 단백질 황전이효소(TPST)에 의해 촉매됩니다. 상기 포스포티로신 항체들과 마찬가지로, 최근에는 설포티로신을 특이적으로 검출하는 항체들이 기술되고 있습니다.[18]
신경전달물질 및 호르몬의 전구물질
뇌의 도파민성 세포에서 티로신은 티로신 하이드록실화효소(TH)에 의해 L-DOPA로 전환됩니다. 이것은 신경전달물질 도파민의 합성에 관여하는 속도 제한 효소입니다. 도파민은 이후 노르에피네프린(노레피네프린)과 에피네프린(아드레날린)과 같은 다른 카테콜아민으로 전환될 수 있습니다.
갑상선의 콜로이드에 있는 갑상선 호르몬인 트라이아이오도티로닌(T3)과 티록신(T4)도 티로신에서 유래합니다.
기타 화합물의 전구체
아편 양귀비인 Papaver somniferum의 라텍스는 티로신을 알칼로이드 모르핀으로 전환시키는 것으로 나타났으며 생체 합성 경로는 카본-14 방사성 표지 티로신을 사용하여 생체 내 합성 경로를 추적하여 티로신에서 모르핀으로 확립되었습니다.[22]티로신 암모니아 분해효소(TAL)는 천연 페놀 생합성 경로의 효소입니다. L-티로신을 p-쿠마린산으로 변환시킵니다.티로신은 멜라닌 색소의 전구체이기도 합니다. 티로신(또는 그 전구체 페닐알라닌)은 조효소 Q10의 일부를 형성하는 벤조퀴논 구조를 합성하는 데 필요합니다.[23][24]
열화

[citation 필요]
L-티로신(syn. para-hydroxyphenylalanine)의 분해는 티로신 트랜스아미나제를 통해 파라-하이드록시페닐피루브산으로 α-케토글루타레이트 의존성 트랜스아미네이션으로 시작됩니다. 위치 설명 파라, 약칭 p는 페닐 고리의 하이드록시기와 측쇄가 서로 교차한다는 것을 의미합니다(아래 그림 참조).
다음 산화 단계는 p-하이드록시페닐피루브산 다이옥시게나제와 CO2 호모젠티세이트(2,5-디하이드록시페닐-1-아세테이트)를 분리하여 촉매합니다.[25] 호모젠티세이트의 방향족 고리를 쪼개기 위해서는 호모젠티세이트 1,2-다이옥시게나제가 더 필요합니다. 이로써, 추가적인2 O 분자의 혼입을 통해 말레일레이스가 아세테이트로 생성됩니다.
푸마릴아세토아세테이트는 산화를 통해 하이드록실기에서 생성된 카르복실기의 회전을 통해 말레일아세토아세토아세테이트 시스-트랜스-이성질화효소에 의해 생성됩니다. 이 시스-트랜스-이성질화효소는 글루타티온을 조효소로 함유하고 있습니다. 푸마릴락토아세테이트는 물 분자를 첨가하여 최종적으로 푸마릴락토아세테이트 가수분해효소에 의해 분리됩니다.
이로써 푸마르산염(시트르산 회로의 대사산물이기도 함)과 아세토아세테이트(3-케토부티로에이트)가 유리됩니다. 아세토아세테이트는 숙시닐-CoA로 활성화된 케톤체로, 이후 아세틸-CoA로 전환되어 시트르산 회로에 의해 산화되거나 지방산 합성에 사용될 수 있습니다.
플로레틱산은 쥐의 티로신의 소변 대사산물이기도 합니다.[26]
오르토- 및 메타티로신

L-tyrosine의 구조 이성질체는 3가지로 알려져 있습니다. 파라 이성질체인 공통 아미노산 L-티로신(para-tyr, p-tyr 또는 4-하이드록시페닐알라닌) 외에도 자연에서 발생하는 메타-티로신(meta-tyrosine, L-m-tyr 및 m-tyr이라고도 함)과 오르토-티로신(o-tyr 또는 2-하이드록시페닐알라닌)의 두 가지 추가 영역 이성질체가 있습니다. 드물지만 m-tyr 및 o-tyr 이성질체는 산화 스트레스 조건에서 페닐알라닌의 비효소적 자유 라디칼 하이드록실화를 통해 발생합니다.[27][28]
의료용
티로신은 신경전달물질의 전구물질이며 혈장 신경전달물질 수치(특히 도파민과 노르에피네프린)[29]를 증가시키지만 정상적인 피험자의 기분에는 거의 영향을 미치지 않습니다.[30][31][32]
2015년 체계적인 검토에 따르면 "티로신 부하는 극한 날씨나 인지 부하와 같은 까다로운 상황 조건에 의해 유발되는 작업 기억 및 정보 처리의 감소에 급성으로 대응한다"며 따라서 "티로신은 까다로운 상황 조건에 노출된 건강한 개인에게 도움이 될 수 있다"고 합니다.[33]
산업합성
L-티로신은 의약품, 식이보충제 및 식품첨가물에 사용됩니다. 이전에 L-티로신을 제조하는 데 두 가지 방법이 사용되었습니다. 첫 번째는 화학적 접근법을 사용하여 단백질 가수분해물로부터 원하는 아미노산을 추출하는 것입니다. 두 번째는 티로신 페놀 분해효소를 사용하여 페놀, 피루브산 및 암모니아로부터 효소 합성을 활용합니다.[34] 유전공학의 발전과 산업 발효의 출현으로 L-tyrosine의 합성이 E. coli의 조작된 균주의 사용으로 전환되었습니다.[35][34]
참고 항목
참고문헌
- ^ a b Frey MN, Koetzle TF, Lehmann MS, Hamilton WC (1973). "Precision neutron diffraction structure determination of protein and nucleic acid components. X. A comparison between the crystal and molecular structures of L-tyrosine and L-tyrosine hydrochloride". J. Chem. Phys. 58 (6): 2547–2556. Bibcode:1973JChPh..58.2547F. doi:10.1063/1.1679537.
- ^ "Nomenclature and Symbolism for Amino Acids and Peptides". IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. Archived from the original on 9 October 2008. Retrieved 5 March 2018.
- ^ "Tyrosine". The Columbia Electronic Encyclopedia, 6th ed. Infoplease.com — Columbia University Press. 2007. Retrieved 2008-04-20.
- ^ Harper D (2001). "Tyrosine". Online Etymology Dictionary. Retrieved 2008-04-20.
- ^ "Amino Acids - Tyrosine". www.biology.arizona.edu. Retrieved 2018-01-31.
- ^ "IUPAC-IUB Commission on Biochemical Nomenclature A One-Letter Notation for Amino Acid Sequences". Journal of Biological Chemistry. 243 (13): 3557–3559. 10 July 1968. doi:10.1016/S0021-9258(19)34176-6.
- ^ Saffran M (April 1998). "Amino acid names and parlor games: from trivial names to a one-letter code, amino acid names have strained students' memories. Is a more rational nomenclature possible?". Biochemical Education. 26 (2): 116–118. doi:10.1016/S0307-4412(97)00167-2.
- ^ Hunter T (2012-09-19). "Why nature chose phosphate to modify proteins". Philosophical Transactions of the Royal Society B: Biological Sciences. 367 (1602): 2513–2516. doi:10.1098/rstb.2012.0013. ISSN 0962-8436. PMC 3415839. PMID 22889903.
- ^ Lu ZC, Jiang F, Wu YD (2021-12-11). "Phosphate binding sites prediction in phosphorylation-dependent protein-protein interactions". Bioinformatics (Oxford, England). 37 (24): 4712–4718. doi:10.1093/bioinformatics/btab525. ISSN 1367-4811. PMID 34270697.
- ^ Liu BA, Nash PD (2012-09-19). "Evolution of SH2 domains and phosphotyrosine signalling networks". Philosophical Transactions of the Royal Society B: Biological Sciences. 367 (1602): 2556–2573. doi:10.1098/rstb.2012.0107. ISSN 0962-8436. PMC 3415846. PMID 22889907.
- ^ Barry BA (January 2015). "Reaction dynamics and proton coupled electron transfer: studies of tyrosine-based charge transfer in natural and biomimetic systems". Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1847 (1): 46–54. doi:10.1016/j.bbabio.2014.09.003. ISSN 0006-3002. PMID 25260243.
- ^ Pencharz PB, Hsu JW, Ball RO (June 2007). "Aromatic amino acid requirements in healthy human subjects". The Journal of Nutrition. 137 (6 Suppl 1): 1576S–1578S, discussion 1597S-1598S. doi:10.1093/jn/137.6.1576S. PMID 17513429.
- ^ 영양 순위 도구. MyFoodData.com . https://tools.myfooddata.com/nutrient-ranking-tool/tyrosine/all/highest
- ^ "Tyrosine". University of Maryland Medical Center. Archived from the original on 2013-06-04. Retrieved 2011-03-17.
- ^ a b 티로신이 가장 많이 함유된 10대 식품
- ^ 영양 순위 도구. MyFoodData.com . https://tools.myfooddata.com https://tools.myfooddata.com/nutrient-ranking-tool/tyrosine/meats/highest/ounces/common/no
- ^ Hoffhines AJ, Damoc E, Bridges KG, Leary JA, Moore KL (December 2006). "Detection and purification of tyrosine-sulfated proteins using a novel anti-sulfotyrosine monoclonal antibody". The Journal of Biological Chemistry. 281 (49): 37877–87. doi:10.1074/jbc.M609398200. PMC 1764208. PMID 17046811.
- ^ Kanan Y, Hamilton RA, Sherry DM, Al-Ubaidi MR (December 2012). "Focus on molecules: sulfotyrosine". Experimental Eye Research. 105: 85–6. doi:10.1016/j.exer.2012.02.014. PMC 3629733. PMID 22406006.
- ^ Broadley KJ (March 2010). "The vascular effects of trace amines and amphetamines". Pharmacology & Therapeutics. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (May 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends in Pharmacological Sciences. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). "The endogenous substrates of brain CYP2D". European Journal of Pharmacology. 724: 211–218. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ Battersby AR, Binks R, Harper BJ (1962-01-01). "692. Alkaloid biosynthesis. Part II. The biosynthesis of morphine". Journal of the Chemical Society: 3534–3544. doi:10.1039/JR9620003534. ISSN 0368-1769.
- ^ Bentinger M, Tekle M, Dallner G (May 2010). "Coenzyme Q--biosynthesis and functions". Biochemical and Biophysical Research Communications. 396 (1): 74–9. doi:10.1016/j.bbrc.2010.02.147. PMID 20494114.
- ^ Acosta MJ, Vazquez Fonseca L, Desbats MA, Cerqua C, Zordan R, Trevisson E, et al. (2016). "Coenzyme Q biosynthesis in health and disease". Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1857 (8): 1079–1085. doi:10.1016/j.bbabio.2016.03.036. PMID 27060254.
- ^ Zea-Rey AV, Cruz-Camino H, Vazquez-Cantu DL, Gutiérrez-García VM, Santos-Guzmán J, Cantú-Reyna C (27 November 2017). "The Incidence of Transient Neonatal Tyrosinemia Within a Mexican Population". Journal of Inborn Errors of Metabolism and Screening. 5: 232640981774423. doi:10.1177/2326409817744230.
- ^ Booth AN, Masri MS, Robbins DJ, Emerson OH, Jones FT, DeEds F (1960). "Urinary phenolic acid metabolities of tyrosine". Journal of Biological Chemistry. 235 (9): 2649–2652. doi:10.1016/S0021-9258(19)76930-0.
- ^ Molnár GA, Wagner Z, Markó L, Kó Szegi T, Mohás M, Kocsis B, et al. (November 2005). "Urinary ortho-tyrosine excretion in diabetes mellitus and renal failure: evidence for hydroxyl radical production". Kidney International. 68 (5): 2281–7. doi:10.1111/j.1523-1755.2005.00687.x. PMID 16221230.
- ^ Molnár GA, Nemes V, Biró Z, Ludány A, Wagner Z, Wittmann I (December 2005). "Accumulation of the hydroxyl free radical markers meta-, ortho-tyrosine and DOPA in cataractous lenses is accompanied by a lower protein and phenylalanine content of the water-soluble phase". Free Radical Research. 39 (12): 1359–66. doi:10.1080/10715760500307107. PMID 16298866. S2CID 31154432.
- ^ Rasmussen DD, Ishizuka B, Quigley ME, Yen SS (October 1983). "Effects of tyrosine and tryptophan ingestion on plasma catecholamine and 3,4-dihydroxyphenylacetic acid concentrations". The Journal of Clinical Endocrinology and Metabolism. 57 (4): 760–3. doi:10.1210/jcem-57-4-760. PMID 6885965.
- ^ Leathwood PD, Pollet P (1982). "Diet-induced mood changes in normal populations". Journal of Psychiatric Research. 17 (2): 147–54. doi:10.1016/0022-3956(82)90016-4. PMID 6764931.
- ^ Deijen JB, Orlebeke JF (1994). "Effect of tyrosine on cognitive function and blood pressure under stress". Brain Research Bulletin. 33 (3): 319–23. doi:10.1016/0361-9230(94)90200-3. PMID 8293316. S2CID 33823121.
- ^ Lieberman HR, Corkin S, Spring BJ, Wurtman RJ, Growdon JH (August 1985). "The effects of dietary neurotransmitter precursors on human behavior". The American Journal of Clinical Nutrition. 42 (2): 366–70. doi:10.1093/ajcn/42.2.366. PMID 4025206.
- ^ Jung SE, Hase A, ann het Rot M (2015). "Behavioral and cognitive effects of tyrosine intake in healthy human adults". Pharmacology Biochemistry and Behavior. 133: 1–6. doi:10.1016/j.pbb.2015.03.008. PMID 25797188. S2CID 30331663.
- ^ a b Lütke-Eversloh T, Santos CN, Stephanopoulos G (December 2007). "Perspectives of biotechnological production of L-tyrosine and its applications". Applied Microbiology and Biotechnology. 77 (4): 751–62. doi:10.1007/s00253-007-1243-y. PMID 17968539. S2CID 23088822.
- ^ Chavez-Bejar M, Baez-Viveros J, Martinez A, Bolivar F, Gosset G (2012). "Biotechnological production of L-tyrosine and derived compounds". Process Biochemistry. 47 (7): 1017–1026. doi:10.1016/j.procbio.2012.04.005.
외부 링크
- 티로신 MS 스펙트럼
- 2019-07-26 웨이백 머신에서 보관된 티로신 대사
- 페닐알라닌 및 티로신 생합성
- 2021-05-06 웨이백 머신에서 페닐알라닌, 티로신, 트립토판 생합성 보관