경피
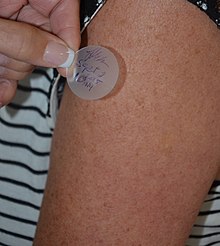
Transdermal경피란 전신 분배를 위해 피부에 활성 성분이 전달되는 투여 경로다. 예를 들어, 약품 전달에 사용되는 경피 패치를 들 수 있다. 약물은 전신적 효과를 위해 약물을 순환하는 패치나 연고 형태로 투여한다.
기술
장애물
비록 피부는 약물 전달의 크고 논리적인 목표물이지만, 그것의 기본 기능은 이러한 목적을 위한 효용을 제한한다. 피부는 주로 외부 침투(유해물질, 미생물 등)로부터 신체를 보호하고 모든 체액을 함유하는 기능을 한다.
인간의 피부에는 (1) 표피와 (2) 진피라는 두 가지 중요한 층이 있다. 경피 전달을 위해서는 약물이 표피의 두 하위층을 통과해야 진피의 미세순환에 도달할 수 있다.
각질층은 피부의 최상층이며, 몸의 부위에 따라 약 10마이크로미터에서 수백마이크로미터까지 두께가 다양하다.[1] 지질 행렬로 둘러싸인 죽은 납작한 각질세포 층으로 이루어져 있는데, 이 층이 함께 침투하기 어려운 벽돌과 사계의 역할을 한다.[2]
각질층은 확산에 가장 중요한 장벽을 제공한다. 실제로 각질층은 경피 약물의 약 90%를 사용하는 데 장벽이 된다. 그러나 거의 모든 분자가 어느 정도까지 침투한다.[3] 각질층 아래에는 생존 가능한 표피가 있다. 이 층은 각질층의 10배 정도 두께가 되지만, 생존 가능한 표피의 살아있는 세포의 수화도가 높아 확산이 훨씬 빠르다. 표피 아래에는 약 1밀리미터 두께로 각질층 두께의 100배인 진피가 있다. 진피에는 약물을 전신 순환으로 분산시키고 피부의 미세순환으로 알려진 계통인 온도를 조절하는 작은 혈관이 들어 있다.[2][3]
경피 경로
약물이 피부를 가로질러 전신 순환에 도달할 수 있는 두 가지 주요 경로가 있다. 더 직접적인 경로는 세포간 경로로 알려져 있다.
초세포 경로
이 경로로 약물은 각질층을 구성하는 죽은 각질세포의 인광피질막과 세포질 모두를 직접 통과하여 피부를 가로지른다.
비록 이것이 최단거리의 길이지만, 약물은 침투에 대한 상당한 저항력을 경험한다. 이 저항은 약물이 각 세포의 지방질막을 통과해야 하고, 그 다음 케라틴을 함유한 친수성 세포 내용물, 그리고 그 다음 세포의 인지질 빌레이어를 한 번 더 통과해야 하기 때문에 발생한다. 이 일련의 단계는 각질층의 전체 두께를 가로지르기 위해 수없이 반복된다.[1][2]
세포간 경로
피부를 관통하는 또 다른 일반적인 통로는 세포간 경로를 통해서이다. 이 경로를 통해 피부를 가로지르는 약물은 피부 세포 사이의 작은 공간을 통과해야 하며, 경로를 더 꼬불꼬불하게 만든다. 각질층의 두께는 약 20µm에 불과하지만, 대부분의 분자가 피부를 가로지르는 실제 확산 경로는 400µm에 이른다.[4] 실제 분자 투과 경로가 20배 증가하면 약물 투과율이 크게 줄어든다.[3]
최근의 연구는 활성 의약품 성분을 용해하는 시스템의 물리적 화학에 참여함으로써 세포간 경로를 극적으로 향상시킬 수 있고, 유하중 전달이 획기적으로 더 효율적이며, 이 경로를 통해 대부분의 화합물을 전달할 수 있다는 것을 입증했다.[5][6][7]
미크로네들스
각질층을 뚫는 세 번째 길은 많은 브랜드와 변형이 있는 의료용 마이크로 니들링 장치에 의해 만들어진 작은 마이크로 채널을 통해서이다.[8] 독일 마르부르크 대학교에서 표준 프란츠 확산 세포를 사용한 조사는 이 접근법이 친수성 화합물뿐만 아니라 지방질 성분의 피부 침투 능력을 강화하는데 효율적이라는 것을 보여주었다.[9]
마이크로 니들링 접근법은 '미래 백신'으로도 보인다.[10] 마이크로네들은 속이 비거나, 단단하거나, 코팅되거나, 용해되거나, 하이드로겔이 형성될 수 있다.[11] 어떤 사람들은 규제 승인을 받는다.[11] 마이크로네들 장치/패치를 나노입자 의약품 전달에 사용할 수 있다.[12]
장치 및 제형식
치환성 물질에 대한 장치 및 제형은 다음을 포함한다.
- 경피 패치
- 경피 젤
- 특수 공식
참조
- ^ a b 플린, G.L. (1996년) "피부 및 경피 전달: 전달 프로세스 및 시스템" Modern Pharmaceutics, Banker, G.S & Rodes, C.T, 에드, 뉴욕: 마르셀 데커, 239-299m
- ^ a b c McCarley K.D, Bunge A.L. (2001). "Review of pharmacokinetic models of dermal absorption". J Pharm Sci. 90 (11): 1699–1719. doi:10.1002/jps.1120. PMID 11745728.
- ^ a b c Morganti P., Ruocco E., Wolf R., Ruocco V. (2001). "Percutaneous absorption and delivery systems". Clin Dermatol. 19 (4): 489–501. doi:10.1016/s0738-081x(01)00183-3. PMID 11535394.
{{cite journal}}: CS1 maint : 복수이름 : 작성자 목록(링크) - ^ Hadgraft J (2001). "Modulation of the barrier function of the skin". Skin Pharmacol Appl Skin Physiol. 14 (1): 72–81. doi:10.1159/000056393. PMID 11509910. S2CID 33920480.
- ^ A. T. 터커, 1 Z 치크, 2 L. 마이클스, 3 K. 커비, 4 M. P. 씨드, 5 A. 존스턴2, C. A. S. Alam5 정맥 마취에 대한 경피적 국소 마취와 TDS 시스템의 결합에 대한 연구, 2006, 61, 페이지 123–126
- ^ Z. Chick, A. Johnston, A. T. 터커, S. L. 츄, L. Michaels & C. A. A. A. Alam 약동학 건강한 남성의 새로운 테스토스테론 경피 전달 시스템인 TDS ® -testosterone의 건강한 남성 도이:10.111/j.1365-2125.2005.02542.x
- ^ Z. Chick, A. Johnston, K. Kirby, A.T. 터커와 C.A. Alam;테스토스테론의 내인성 농도를 교정하는 것은 생물학적 동등성에 영향을 미치고 2009년 4월 47일 (4):262-8에 대한 TDS®-테스토스테론의 우수성을 보여준다.
- ^ 콜리, C.S., 칼리, H., 데사이, N.N. & 뱅가, A.K. (2007)"각질층 장벽을 뚫기 위한 대체 수단으로서의 더마롤러." 애틀랜타 GA 30341, 미국 머서대학교 약학보건과학대학
- ^ Verma, D.D. & Fahr. A. "피부의 더 깊은 층으로 물질이 축적되는 새로운 장치의 효과에 대한 조사: Dermaroller' Institute für Famazeutische Technologie und Biopharmazie, Philips-Universitett Marburg, 독일 마르부르크.
- ^ Giudice EL, Campbell JD (2006). "Needle-free vaccine delivery". Adv Drug Deliv Rev. 58 (1): 68–89. doi:10.1016/j.addr.2005.12.003. PMID 16564111.
- ^ a b Ita, K (2015). "Transdermal Delivery of Drugs with Microneedles—Potential and Challenges". Pharmaceutics. 7 (3): 90–105. doi:10.3390/pharmaceutics7030090. PMC 4588187. PMID 26131647.
- ^ Larrañeta; et al. (2016). "Microneedles: A New Frontier in Nanomedicine Delivery". Pharm. Res. 33 (5): 1055–73. doi:10.1007/s11095-016-1885-5. PMC 4820498. PMID 26908048.