단백질 c-Fos
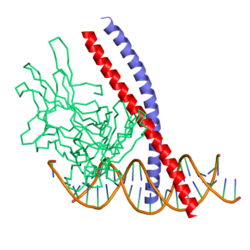
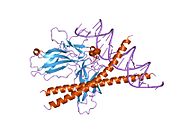
Protein c-Fos단백질 c-Fos는 레트로바이러스 종양 유전자 v-fos의 [5]인간 호몰로그인 원종 유전자이다.그것은 FOS 유전자에 의해 인간에게 암호화된다.FBJ MSV(Finkel-Biskis-Jinkins murine 골원성 육종 바이러스)의 변형 유전자로 쥐 섬유아세포에서 처음 발견되었다(Curran and Tech, 1982).이것은 c-Fos, FosB, Fra-1 및 [6]Fra-2를 포함하는 더 큰 Fos 계열의 전사 인자의 일부입니다.이는 염색체 영역 14q21→q31에 매핑되었다. c-Fos는 62 kDa 단백질을 암호화하여 c-jun(전사인자 Jun 계열의 일부)과 헤테로디머를 형성한다.결과적으로 표적 유전자의 프로모터 및 인핸서 영역에서 AP-1 특정 부위에서 DNA를 결합하고 세포 외 신호를 유전자 [7]발현 변화로 변환하는 AP-1 복합체(Activator Protein-1)가 형성된다.그것은 많은 세포 기능에서 중요한 역할을 하며 다양한 암에서 과압된 것으로 밝혀졌다.
구조 및 기능
c-Fos는 380개의 아미노산 단백질로, 이합체화 및 DNA 결합을 위한 기본 류신 지퍼 영역과 C 말단에서 트랜스활성화 도메인을 가지며, Jun 단백질과 마찬가지로 호모디머를 [8]형성할 수 있다.시험관내 연구에 따르면 Jun-Fos 헤테로디머는 Jun-Jun 호모디머보다 [9]안정적이고 DNA 결합 활성이 강한 것으로 나타났다.
혈청, 성장인자, 종양촉진제, 사이토카인, 자외선을 포함한 다양한 자극이 그들의 발현을 유도한다.c-fos mRNA와 단백질은 일반적으로 가장 먼저 발현되는 유전자 중 하나이며, 따라서 즉시 초기 유전자로 언급된다.자극 [10]후 15분 이내에 빠르고 일시적으로 유도된다.또한 단백질 안정성, DNA 결합 활성 및 전사 [11][12][13]인자의 전이 활성화 가능성에 영향을 미치는 MAPK, CDC2, PKA 또는 PKC와 같은 다른 키나제에 의한 인산화로 인한 번역 후 변형에 의해 활성이 조절된다.그것은 유전자 활성화뿐만 아니라 유전자 억제를 일으킬 수 있지만, 비록 두 과정 모두에 다른 영역이 관여하는 것으로 알려져 있다.
그것은 세포 증식, 분화, 생존, 저산소증과 관련된 유전자,[14] 그리고 혈관신생을 포함한 중요한 세포 사건들과 관련되어 있다. 이것은 조절 장애를 암 발병의 중요한 요소로 만든다.그것은 또한 세포 극성의 상실과 상피-간막 전이를 유도하여 유방 상피 [15]세포의 침습적이고 전이적인 성장을 이끌 수 있다.
생물학적 맥락에서 c-fos의 중요성은 항감각 mRNA, 항c-fos 항체, c-fos mRNA를 절단하는 리보자임 또는 c-fos의 지배적인 음성 돌연변이를 사용하여 내인성 기능을 제거함으로써 결정되었다.이렇게 생성된 트랜스제닉 마우스는 세포 증식의 c-fos의존성 및 독립적 경로가 있음을 보여주지만 골다공증, 지연된 생식기형성, 림프감소증 및 행동 이상을 포함한 조직 특이적 발달 결함의 범위를 나타낸다.
임상적 의의
AP-1 복합체는 암의 변형과 진행에 관여해 왔다.골육종과 자궁내막암에서 c-Fos 과발현은 높은 등급의 병변과 나쁜 예후와 관련이 있었다.또한 자궁경부 전암 병변과 침습성 자궁경부암을 비교하였을 때, 전암 병변에서 c-Fos 발현이 유의미하게 낮았다. 또한 c-Fos는 유방암 [23]생존 감소의 독립적 예측요인으로 확인되었다.
트랜스제닉 마우스에서 클래스 I MHC 프로모터에서 c-fos가 과다 발현되면 골아세포 증식이 증가하여 골육종이 형성되는 반면, 다른 Jun과 Fos 단백질의 이소성 발현은 악성 종양을 유발하지 않는 것으로 밝혀졌다.생쥐에서 c-Fos 트랜스유전자가 활성화되면 체외 및 체내 모두 골아세포와 연골세포에서 사이클린 D1, A, E가 과다 발현되어 종양을 유도하는 통제되지 않은 성장에 기여할 수 있다.c-fos 발현에 대해 분석된 인간 골육종은 사례의 절반 이상에서 양성 반응을 보였으며, c-fos 발현은 더 높은 재발 빈도와 화학 요법에 대한 반응 불량과 관련이 있었다.
몇몇 연구들은 c-Fos가 종양 억제 활성을 가지고 있을 수도 있고, 종양 발생을 억제할 수도 있다는 생각을 제기했습니다.이를 뒷받침하는 것은 난소암종에서 c-Fos 발현 상실이 질병 진행과 관련이 있다는 관측이다.이러한 이중 작용은 종양 세포와 그 환경(예: 이량화 파트너, 공동 활성제 및 촉진제 아키텍처)의 차등 단백질 구성에 의해 가능해질 수 있다.종양을 억제하는 활동이 프로아포토시스 기능에 의한 것일 수 있습니다.c-Fos가 아포토시스에 기여하는 정확한 메커니즘은 명확하게 이해되지 않지만, 인간 간세포암세포의 관찰 결과 c-Fos는 c-myc 유도 세포사망의 매개체이며 p38 MAP 키나제 경로를 통해 아포토시스를 유도할 수 있다.Fas 리간드(FASLG 또는 FasL)와 종양 괴사인자 관련 아포토시스 유도 리간드(TNFSF10 또는 TRAIL)는 인간 T세포 백혈병 세포 라인에서 관찰된 바와 같이 c-Fos에 의해 유도된 추가적인 아포토시스 메커니즘을 반영할 수 있다.종양 억제에 c-Fos가 관여하는 또 다른 가능한 메커니즘은 가족성 유방암과 난소암에서 잘 확립된 요인인 BRCA1의 직접 조절일 수 있다.
또한 자궁내막암, 자궁경부암, 중피종, 대장암, 폐암, 흑색종, 갑상선암, 식도암, 간세포암 등에서 c-fos 및 기타 Fos족 단백질의 역할도 연구되어 왔다.
코카인, 필로폰,[24] [25]모르핀 및 기타 정신작용[26][27] 약물들은 중피질 경로(전전두피질)뿐만 아니라 중피질 보상 경로(핵 어큐벤스)에서 c-Fos 생성을 증가시키고 사전 [27]감작에 따라 변동성을 보이는 것으로 나타났다.accumbens의 D1형 배지 가시 뉴런 내의 δFosB의 AP-1 복합체에 의한 c-Fos 억제는 δFosB의 만성 유도를 가능하게 하는 분자 스위치로 작용하여 보다 빠르게 축적된다.이와 같이 c-Fos 프로모터는 약물중독 연구 전반에서 이용을 발견함과 동시에 약물추구 및 만성 약물복용과 관련된 다른 행동변화에 대한 상황유도적 재발을 발견한다.
짝짓기 [citation needed]후 랫드에서 안드로겐 수용체를 포함한 뉴런의 c-Fos 생산 증가가 관찰되었다.
적용들
c-fos의 표현은 뉴런이 활동전위를 [28][29]방출할 때 종종 표현되기 때문에 뉴런 활동의 간접적인 지표이다.뉴런에서 c-fos mRNA의 상향 조절은 최근의 [30]활동을 나타낸다.
c-fos 프로모터는 약물 남용 연구에도 이용되었다.과학자들은 이 프로모터를 사용하여 쥐의 유전자 변환을 활성화하고, 쥐가 약물과 관련된 기억과 [31]행동에서 그들의 역할을 평가하기 위해 특정 신경 앙상블을 조작할 수 있도록 합니다.이 신경 제어는 광유전학 또는 DREADD로 복제할 수 있습니다.
상호 작용
c-Fos는 다음과 상호작용하는 것으로 나타났습니다.
- BCL3,[33]
- 코브라1,[34]
- CSNK2A1,[35]
- CSNK2A2,[35]
- DDIT3,[36]
- 준[37][38][39][40][41][42][43]
- NCOA1,[44][45]
- NCOR2,[46]
- RELA,[37]
- RUNX1,[47][48]
- RUNX2,[47][48]
- SMAD3 [49]및
- TBP[50]
 |

「 」를 참조해 주세요.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000170345 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000021250 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Curran, T: c-fos 원종 유전자.인: Reddy EP, Skalka AM, Curran T (eds)Oncogen Handbook 1988 엘세비어, 뉴욕, 페이지 307–327
- ^ Milde-Langosch K (November 2005). "The Fos family of transcription factors and their role in tumourigenesis". Eur. J. Cancer. 41 (16): 2449–61. doi:10.1016/j.ejca.2005.08.008. PMID 16199154.
- ^ Chiu R, Boyle WJ, Meek J, Smeal T, Hunter T, Karin M (August 1988). "The c-Fos protein interacts with c-Jun/AP-1 to stimulate transcription of AP-1 responsive genes". Cell. 54 (4): 541–52. doi:10.1016/0092-8674(88)90076-1. PMID 3135940. S2CID 43078284.
- ^ Szalóki N, Krieger JW, Komáromi I, Tóth K, Vámosi G (November 2015). "Evidence for homodimerization of the c-Fos transcription factor in live cells revealed by fluorescence microscopy and computer modeling". Mol. Cell. Biol. 35 (21): 3785–98. doi:10.1128/MCB.00346-15. PMC 4589601. PMID 26303532.
- ^ Halazonetis TD, Georgopoulos K, Greenberg ME, Leder P (December 1988). "c-Jun dimerizes with itself and with c-Fos, forming complexes of different DNA binding affinities" (PDF). Cell. 55 (5): 917–24. doi:10.1016/0092-8674(88)90147-X. PMID 3142692. S2CID 19876513.
- ^ Hu E, Mueller E, Oliviero S, Papaioannou VE, Johnson R, Spiegelman BM (July 1994). "Targeted disruption of the c-fos gene demonstrates c-fos-dependent and -independent pathways for gene expression stimulated by growth factors or oncogenes". EMBO J. 13 (13): 3094–103. doi:10.1002/j.1460-2075.1994.tb06608.x. PMC 395200. PMID 8039503.
- ^ Gruda MC, Kovary K, Metz R, Bravo R (September 1994). "Regulation of Fra-1 and Fra-2 phosphorylation differs during the cell cycle of fibroblasts and phosphorylation in vitro by MAP kinase affects DNA binding activity". Oncogene. 9 (9): 2537–47. PMID 8058317.
- ^ Hurd TW, Culbert AA, Webster KJ, Tavaré JM (December 2002). "Dual role for mitogen-activated protein kinase (Erk) in insulin-dependent regulation of Fra-1 (fos-related antigen-1) transcription and phosphorylation". Biochem. J. 368 (Pt 2): 573–80. doi:10.1042/BJ20020579. PMC 1223008. PMID 12197835.
- ^ Rosenberger SF, Finch JS, Gupta A, Bowden GT (January 1999). "Extracellular signal-regulated kinase 1/2-mediated phosphorylation of JunD and FosB is required for okadaic acid-induced activator protein 1 activation". J. Biol. Chem. 274 (2): 1124–30. doi:10.1074/jbc.274.2.1124. PMID 9873060.
- ^ Tulchinsky E (July 2000). "Fos family members: regulation, structure and role in oncogenic transformation". Histol. Histopathol. 15 (3): 921–8. PMID 10963134.
- ^ Fialka I, Schwarz H, Reichmann E, Oft M, Busslinger M, Beug H (March 1996). "The estrogen-dependent c-JunER protein causes a reversible loss of mammary epithelial cell polarity involving a destabilization of adherens junctions". J. Cell Biol. 132 (6): 1115–32. doi:10.1083/jcb.132.6.1115. PMC 2120757. PMID 8601589.
- ^ a b c Renthal W, Nestler EJ (September 2009). "Chromatin regulation in drug addiction and depression". Dialogues in Clinical Neuroscience. 11 (3): 257–268. PMC 2834246. PMID 19877494.
[Psychostimulants] increase cAMP levels in striatum, which activates protein kinase A (PKA) and leads to phosphorylation of its targets. This includes the cAMP response element binding protein (CREB), the phosphorylation of which induces its association with the histone acetyltransferase, CREB binding protein (CBP) to acetylate histones and facilitate gene activation. This is known to occur on many genes including fosB and c-fos in response to psychostimulant exposure. ΔFosB is also upregulated by chronic psychostimulant treatments, and is known to activate certain genes (eg, cdk5) and repress others (eg, c-fos) where it recruits HDAC1 as a corepressor. ... Chronic exposure to psychostimulants increases glutamatergic [signaling] from the prefrontal cortex to the NAc. Glutamatergic signaling elevates Ca2+ levels in NAc postsynaptic elements where it activates CaMK (calcium/calmodulin protein kinases) signaling, which, in addition to phosphorylating CREB, also phosphorylates HDAC5.
그림 2: 정신 자극제에 의한 시그널링 이벤트 - ^ Broussard JI (January 2012). "Co-transmission of dopamine and glutamate". The Journal of General Physiology. 139 (1): 93–96. doi:10.1085/jgp.201110659. PMC 3250102. PMID 22200950.
Coincident and convergent input often induces plasticity on a postsynaptic neuron. The NAc integrates processed information about the environment from basolateral amygdala, hippocampus, and prefrontal cortex (PFC), as well as projections from midbrain dopamine neurons. Previous studies have demonstrated how dopamine modulates this integrative process. For example, high frequency stimulation potentiates hippocampal inputs to the NAc while simultaneously depressing PFC synapses (Goto and Grace, 2005). The converse was also shown to be true; stimulation at PFC potentiates PFC–NAc synapses but depresses hippocampal–NAc synapses. In light of the new functional evidence of midbrain dopamine/glutamate co-transmission (references above), new experiments of NAc function will have to test whether midbrain glutamatergic inputs bias or filter either limbic or cortical inputs to guide goal-directed behavior.
- ^ Kanehisa Laboratories (10 October 2014). "Amphetamine – Homo sapiens (human)". KEGG Pathway. Retrieved 31 October 2014.
Most addictive drugs increase extracellular concentrations of dopamine (DA) in nucleus accumbens (NAc) and medial prefrontal cortex (mPFC), projection areas of mesocorticolimbic DA neurons and key components of the "brain reward circuit". Amphetamine achieves this elevation in extracellular levels of DA by promoting efflux from synaptic terminals. ... Chronic exposure to amphetamine induces a unique transcription factor delta FosB, which plays an essential role in long-term adaptive changes in the brain.
- ^ Cadet JL, Brannock C, Jayanthi S, Krasnova IN (2015). "Transcriptional and epigenetic substrates of methamphetamine addiction and withdrawal: evidence from a long-access self-administration model in the rat". Molecular Neurobiology. 51 (2): 696–717 (Figure 1). doi:10.1007/s12035-014-8776-8. PMC 4359351. PMID 24939695.
- ^ a b c Robison AJ, Nestler EJ (November 2011). "Transcriptional and epigenetic mechanisms of addiction". Nature Reviews Neuroscience. 12 (11): 623–637. doi:10.1038/nrn3111. PMC 3272277. PMID 21989194.
ΔFosB serves as one of the master control proteins governing this structural plasticity. ... ΔFosB also represses G9a expression, leading to reduced repressive histone methylation at the cdk5 gene. The net result is gene activation and increased CDK5 expression. ... In contrast, ΔFosB binds to the c-fos gene and recruits several co-repressors, including HDAC1 (histone deacetylase 1) and SIRT 1 (sirtuin 1). ... The net result is c-fos gene repression.
그림 4: 유전자 발현 약물 조절 후생학적 기초 - ^ a b c Nestler EJ (December 2012). "Transcriptional mechanisms of drug addiction". Clinical Psychopharmacology and Neuroscience. 10 (3): 136–143. doi:10.9758/cpn.2012.10.3.136. PMC 3569166. PMID 23430970.
The 35-37 kD ΔFosB isoforms accumulate with chronic drug exposure due to their extraordinarily long half-lives. ... As a result of its stability, the ΔFosB protein persists in neurons for at least several weeks after cessation of drug exposure. ... ΔFosB overexpression in nucleus accumbens induces NFκB ... In contrast, the ability of ΔFosB to repress the c-Fos gene occurs in concert with the recruitment of a histone deacetylase and presumably several other repressive proteins such as a repressive histone methyltransferase
- ^ Nestler EJ (October 2008). "Transcriptional mechanisms of addiction: Role of ΔFosB". Philosophical Transactions of the Royal Society B: Biological Sciences. 363 (1507): 3245–3255. doi:10.1098/rstb.2008.0067. PMC 2607320. PMID 18640924.
Recent evidence has shown that ΔFosB also represses the c-fos gene that helps create the molecular switch—from the induction of several short-lived Fos family proteins after acute drug exposure to the predominant accumulation of ΔFosB after chronic drug exposure
- ^ Mahner S, Baasch C, Schwarz J, Hein S, Wölber L, Jänicke F, Milde-Langosch K (October 2008). "C-Fos expression is a molecular predictor of progression and survival in epithelial ovarian carcinoma". Br. J. Cancer. 99 (8): 1269–75. doi:10.1038/sj.bjc.6604650. PMC 2570515. PMID 18854825.
- ^ Graybiel AM, Moratalla R, Robertson HA (September 1990). "Amphetamine and cocaine induce drug-specific activation of the c-fos gene in striosome-matrix compartments and limbic subdivisions of the striatum". Proc. Natl. Acad. Sci. U.S.A. 87 (17): 6912–6. Bibcode:1990PNAS...87.6912G. doi:10.1073/pnas.87.17.6912. PMC 54648. PMID 2118661.
- ^ Curran EJ, Akil H, Watson SJ (November 1996). "Psychomotor stimulant- and opiate-induced c-fos mRNA expression patterns in the rat forebrain: comparisons between acute drug treatment and a drug challenge in sensitized animals". Neurochem. Res. 21 (11): 1425–35. doi:10.1007/BF02532384. PMID 8947933. S2CID 6727581.
- ^ Nichols CD, Sanders-Bush E (May 2002). "A single dose of lysergic acid diethylamide influences gene expression patterns within the mammalian brain". Neuropsychopharmacology. 26 (5): 634–42. doi:10.1016/S0893-133X(01)00405-5. PMID 11927188.
- ^ a b Singewald N, Salchner P, Sharp T (February 2003). "Induction of c-Fos expression in specific areas of the fear circuitry in rat forebrain by anxiogenic drugs". Biol. Psychiatry. 53 (4): 275–83. doi:10.1016/S0006-3223(02)01574-3. PMID 12586446. S2CID 29821546.
- ^ VanElzakker M, Fevurly RD, Breindel T, Spencer RL (2008). "Environmental novelty is associated with a selective increase in c-fos expression in the output elements of the hippocampal formation and the perirhinal cortex". Learn. Mem. 15 (12): 899–908. doi:10.1101/lm.1196508. PMC 2632843. PMID 19050162.
- ^ Dragunow M, Faull R (1989). "The use of c-fos as a metabolic marker in neuronal pathway tracing". Journal of Neuroscience Methods. 29 (3): 261–265. doi:10.1016/0165-0270(89)90150-7. PMID 2507830. S2CID 3804201.
- ^ Day HE, Kryskow EM, Nyhuis TJ, Herlihy L, Campeau S (September 2008). "Conditioned Fear Inhibits c-fos mRNA Expression in the Central Extended Amygdala". Brain Res. 1229: 137–46. doi:10.1016/j.brainres.2008.06.085. PMC 2605076. PMID 18634767.
- ^ Koya E, Golden SA, Harvey BK, Guez-Barber DH, Berkow A, Simmons DE, Bossert JM, Nair SG, Uejima JL, Marin MT, Mitchell TB, Farquhar D, Ghosh SC, Mattson BJ, Hope BT (August 2009). "Targeted disruption of cocaine-activated nucleus accumbens neurons prevents context-specific sensitization". Nat. Neurosci. 12 (8): 1069–73. doi:10.1038/nn.2364. PMC 2752202. PMID 19620976.
- ^ Garner, Aleena (March 2012). "Generation of a Synthetic Memory Trace". Science. 335 (6075): 1513–1516. Bibcode:2012Sci...335.1513G. doi:10.1126/science.1214985. PMC 3956300. PMID 22442487.
- ^ Na SY, Choi JE, Kim HJ, Jhun BH, Lee YC, Lee JW (October 1999). "Bcl3, an IkappaB protein, stimulates activating protein-1 transactivation and cellular proliferation". J. Biol. Chem. 274 (40): 28491–6. doi:10.1074/jbc.274.40.28491. PMID 10497212.
- ^ Zhong H, Zhu J, Zhang H, Ding L, Sun Y, Huang C, Ye Q (December 2004). "COBRA1 inhibits AP-1 transcriptional activity in transfected cells". Biochem. Biophys. Res. Commun. 325 (2): 568–73. doi:10.1016/j.bbrc.2004.10.079. PMID 15530430.
- ^ a b Yamaguchi Y, Wada T, Suzuki F, Takagi T, Hasegawa J, Handa H (August 1998). "Casein kinase II interacts with the bZIP domains of several transcription factors". Nucleic Acids Res. 26 (16): 3854–61. doi:10.1093/nar/26.16.3854. PMC 147779. PMID 9685505.
- ^ Ubeda M, Vallejo M, Habener JF (November 1999). "CHOP enhancement of gene transcription by interactions with Jun/Fos AP-1 complex proteins". Mol. Cell. Biol. 19 (11): 7589–99. doi:10.1128/MCB.19.11.7589. PMC 84780. PMID 10523647.
- ^ a b Yang X, Chen Y, Gabuzda D (September 1999). "ERK MAP kinase links cytokine signals to activation of latent HIV-1 infection by stimulating a cooperative interaction of AP-1 and NF-kappaB". J. Biol. Chem. 274 (39): 27981–8. doi:10.1074/jbc.274.39.27981. PMID 10488148.
- ^ Ito T, Yamauchi M, Nishina M, Yamamichi N, Mizutani T, Ui M, Murakami M, Iba H (January 2001). "Identification of SWI.SNF complex subunit BAF60a as a determinant of the transactivation potential of Fos/Jun dimers". J. Biol. Chem. 276 (4): 2852–7. doi:10.1074/jbc.M009633200. PMID 11053448.
- ^ Pognonec P, Boulukos KE, Aperlo C, Fujimoto M, Ariga H, Nomoto A, Kato H (May 1997). "Cross-family interaction between the bHLHZip USF and bZip Fra1 proteins results in down-regulation of AP1 activity". Oncogene. 14 (17): 2091–8. doi:10.1038/sj.onc.1201046. PMID 9160889.
- ^ Glover JN, Harrison SC (January 1995). "Crystal structure of the heterodimeric bZIP transcription factor c-Fos-c-Jun bound to DNA". Nature. 373 (6511): 257–61. Bibcode:1995Natur.373..257G. doi:10.1038/373257a0. PMID 7816143. S2CID 4276971.
- ^ Nomura N, Zu YL, Maekawa T, Tabata S, Akiyama T, Ishii S (February 1993). "Isolation and characterization of a novel member of the gene family encoding the cAMP response element-binding protein CRE-BP1". J. Biol. Chem. 268 (6): 4259–66. doi:10.1016/S0021-9258(18)53604-8. PMID 8440710.
- ^ Finkel T, Duc J, Fearon ER, Dang CV, Tomaselli GF (January 1993). "Detection and modulation in vivo of helix-loop-helix protein-protein interactions". J. Biol. Chem. 268 (1): 5–8. doi:10.1016/S0021-9258(18)54105-3. PMID 8380166.
- ^ Venugopal R, Jaiswal AK (December 1998). "Nrf2 and Nrf1 in association with Jun proteins regulate antioxidant response element-mediated expression and coordinated induction of genes encoding detoxifying enzymes". Oncogene. 17 (24): 3145–56. doi:10.1038/sj.onc.1202237. PMID 9872330.
- ^ Lee SK, Na SY, Jung SY, Choi JE, Jhun BH, Cheong J, Meltzer PS, Lee YC, Lee JW (June 2000). "Activating protein-1, nuclear factor-kappaB, and serum response factor as novel target molecules of the cancer-amplified transcription coactivator ASC-2". Mol. Endocrinol. 14 (6): 915–25. doi:10.1210/mend.14.6.0471. PMID 10847592.
- ^ Lee SK, Kim HJ, Na SY, Kim TS, Choi HS, Im SY, Lee JW (July 1998). "Steroid receptor coactivator-1 coactivates activating protein-1-mediated transactivations through interaction with the c-Jun and c-Fos subunits". J. Biol. Chem. 273 (27): 16651–4. doi:10.1074/jbc.273.27.16651. PMID 9642216.
- ^ Lee SK, Kim JH, Lee YC, Cheong J, Lee JW (April 2000). "Silencing mediator of retinoic acid and thyroid hormone receptors, as a novel transcriptional corepressor molecule of activating protein-1, nuclear factor-kappaB, and serum response factor". J. Biol. Chem. 275 (17): 12470–4. doi:10.1074/jbc.275.17.12470. PMID 10777532.
- ^ a b Hess J, Porte D, Munz C, Angel P (June 2001). "AP-1 and Cbfa/runt physically interact and regulate parathyroid hormone-dependent MMP13 expression in osteoblasts through a new osteoblast-specific element 2/AP-1 composite element". J. Biol. Chem. 276 (23): 20029–38. doi:10.1074/jbc.M010601200. PMID 11274169.
- ^ a b D'Alonzo RC, Selvamurugan N, Karsenty G, Partridge NC (January 2002). "Physical interaction of the activator protein-1 factors c-Fos and c-Jun with Cbfa1 for collagenase-3 promoter activation". J. Biol. Chem. 277 (1): 816–22. doi:10.1074/jbc.M107082200. PMID 11641401.
- ^ Zhang Y, Feng XH, Derynck R (August 1998). "Smad3 and Smad4 cooperate with c-Jun/c-Fos to mediate TGF-beta-induced transcription". Nature. 394 (6696): 909–13. Bibcode:1998Natur.394..909Z. doi:10.1038/29814. PMID 9732876. S2CID 4393852.
- ^ Metz R, Bannister AJ, Sutherland JA, Hagemeier C, O'Rourke EC, Cook A, Bravo R, Kouzarides T (September 1994). "c-Fos-induced activation of a TATA-box-containing promoter involves direct contact with TATA-box-binding protein". Mol. Cell. Biol. 14 (9): 6021–9. doi:10.1128/MCB.14.9.6021. PMC 359128. PMID 8065335.
추가 정보
- Murphy LC, Alkhalaf M, Dotzlaw H, Coutts A, Haddad-Alkhalaf B (June 1994). "Regulation of gene expression in T-47D human breast cancer cells by progestins and antiprogestins". Hum. Reprod. 9 Suppl 1: 174–80. doi:10.1093/humrep/9.suppl_1.174. PMID 7962462.
- Pompeiano M, Cirelli C, Arrighi P, Tononi G (1995). "c-Fos expression during wakefulness and sleep". Neurophysiol Clin. 25 (6): 329–41. doi:10.1016/0987-7053(96)84906-9. PMID 8904195. S2CID 23760149.
- Herrera DG, Robertson HA (October 1996). "Activation of c-fos in the brain". Prog. Neurobiol. 50 (2–3): 83–107. doi:10.1016/S0301-0082(96)00021-4. PMID 8971979. S2CID 31105978.
- Velazquez Torres A, Gariglio Vidal P (2002). "[Possible role of transcription factor AP1 in the tissue-specific regulation of human papillomavirus]". Rev. Invest. Clin. (in Spanish). 54 (3): 231–42. PMID 12183893.
외부 링크
- 미국 국립 의학 도서관 의학 과목 제목(MeSH)의 c-fos+단백질
- 미국 국립 의학 도서관 의학 주제 제목(MeSH)의 c-fos+Genes
- 팩터북 c-Fos
- 드로소필라 카약 - 인터랙티브 플라이
- UCSC Genome Browser의 인간 FOS 게놈 위치 및 FOS 유전자 상세 페이지.
- PDB for UniProt: P01100(Phuman Proto-oncogen c-Fos)에서 PDBe-KB에 제공되는 모든 구조 정보의 개요.
- PDB for UniProt: P01101(Mouse Proto-oncogen c-Fos)에서 PDBe-KB에 있는 모든 구조 정보의 개요.