페르옥시좀증식제활성화수용체
Peroxisome proliferator-activated receptor분자생물학 분야에서 페르옥시좀 증식자 활성화 수용체(PPAR)는 [1]유전자의 발현을 조절하는 전사인자로 기능하는 핵수용체 단백질의 그룹이다.PPAR은 세포 분화, 발달 및 신진대사의[3] 조절에 필수적인 역할을 한다.[2][4][5]
명명 및 조직 분포
| 페르옥시좀증식제활성화수용체α | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | PPARA | ||||||
| Alt. | PPAR | ||||||
| NCBI유전자 | 5465 | ||||||
| HGNC | 9232 | ||||||
| 옴 | 170998 | ||||||
| 참조 | NM_001001928 | ||||||
| 유니프로트 | Q07869 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 22장 q12-q13.1 | ||||||
| |||||||
| 페르옥시좀증식제활성화수용체 감마 | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| 식별자 | |||||||
| 기호. | PPARG | ||||||
| NCBI유전자 | 5468 | ||||||
| HGNC | 9236 | ||||||
| 옴 | 601487 | ||||||
| 참조 | NM_005037 | ||||||
| 유니프로트 | P37231 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 제3장 p25 | ||||||
| |||||||
| 페르옥시좀증식제활성화수용체델타 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | PPARD | ||||||
| NCBI유전자 | 5467 | ||||||
| HGNC | 9235 | ||||||
| 옴 | 600409 | ||||||
| 참조 | NM_006238 | ||||||
| 유니프로트 | Q03181 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 제6장 페이지 21.2 | ||||||
| |||||||
PPAR에는 알파, 감마 및 델타(베타)[4]의 3가지 유형이 식별되었다.
- α(알파) - 간, 신장, 심장, 근육, 지방 조직 및 기타로[6] 발현됨
- β/아세틸(아세틸/아세틸) - 많은 조직, 특히 뇌, 지방 조직 및 피부에서 발현되는
- γ (감마) - 이 PPAR은 동일한 유전자에 의해 전사되지만 대체 스플라이싱을 통해 세 가지 형태로 발현된다.
역사
PPAR은 원래 [7]Xenopus 개구리에서 세포에서 퍼옥시좀의 증식을 유도하는 수용체로 확인되었다.첫 번째 PPAR(PPARα)는 인슐린 [8]민감성 개선과는 별도로 설치류 간 조직에서 과산화소체 수를 증가시켰기 때문에 과산화소체 증식자로 지칭되는 약물의 분자 표적을 찾는 동안 발견되었다.약리학적으로 섬유질과 관련된 이 약제들은 1980년대 초에 발견되었다.PPARs가 생물학에서 훨씬 더 다재다능한 역할을 한다는 것이 밝혀졌을 때, 그 약들은 차례로 PPAR 리간드라고 불렸다.가장 잘 알려진 PPAR 리간드는 티아졸리디온입니다.자세한 것은, 이하를 참조해 주세요.
1992년 [9]인간에서 PPARta(델타)가 확인된 후, 이는 이전에 양서류인 Xenopus에서 설명한 PPARβ(베타)와 밀접한 관련이 있는 것으로 밝혀졌다."PPAR""이라는 용어는 일반적으로 미국에서 사용되지만, "PPARβ"의 사용은 Xenopus에서 처음 발견된 유럽에서도 여전히 사용되고 있다.
PPARs는 설치류에서 페르옥시좀 증식을 유도하는 것으로 발견되었기 때문에 그렇게 이름 붙여졌지만,[10][11] 이러한 페르옥시좀 증식의 유도는 사람에게서 일어나는 것으로 여겨지지 않는다.
생리 기능
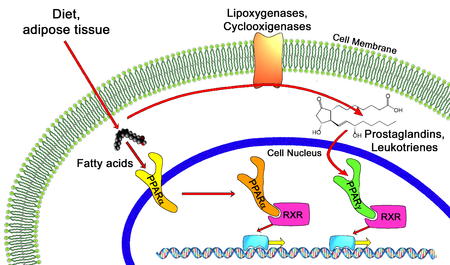
모든 PPAR은 레티노이드 X 수용체(RXR)로 헤테로다이머화되어 표적 유전자의 DNA 상의 특정 영역에 결합한다.이러한 DNA 서열을 PPRE(peroxisome 증식 호르몬 반응 요소)라고 합니다.DNA 컨센서스 배열은 AGGTCANAGGTCA이며, N은 모든 뉴클레오티드이다.일반적으로 이 배열은 유전자의 프로모터 영역에서 발생하며 PPAR이 배위자를 결합할 때 유전자에 따라 표적 유전자의 전사가 증가하거나 감소한다.또한 RXR은 많은 다른 수용체(예: 비타민 D 및 갑상선 호르몬)와 함께 헤테로디머를 형성한다.
PPAR의 기능은 리간드 결합에 의해 유도되는 리간드 결합 도메인의 정확한 형태(아래 참조)와 수용체 기능을 각각 [12]자극하거나 억제할 수 있는 다수의 공동활성화제 및 코어프레서 단백질에 의해 수정된다.
PPAR의 내인성 리간드는 유리지방산, 에이코사노이드 및 비타민 B3를 포함한다.PPAR is은 PGJ(프로스타글란딘) 및 5-옥소-15([13]S)-HETE 및 5-옥소-ETE를 포함한 아라키돈산 대사물의 5-HETE 패밀리의 특정 멤버에 의해2 활성화된다.반면 PPARα는 류코트리엔B에4 의해 활성화된다.15(S)-HETE, 15(R)-HETE 및 15-HpETE를 포함한 아라키돈산 대사물의 15-히드록시이코사테트라엔산군의 특정 구성원은 PPAR 알파, 베타/델타 및 감마까지 활성화된다.또한 PPAR was는 암 발생 및 [14][15]성장에 관여하는 것으로 보고되었다.작용제 RS5444에 의한 PPAR activ 활성화는 과민성 갑상선암 [16]성장을 억제할 수 있다.암에서[17] PPAR 감마선의 역할에 대한 검토 및 비판은 를 참조하십시오.
유전학
PPAR의 세 가지 주요 형태는 서로 다른 유전자로부터 전사된다.
- PPARα - 염색체 22q12-13.1 (OMIM 170998)
- PPARβ/γ - 염색체 6p21.2-21.1 (OMIM 600409)
- PPAR - - 염색체 3p25(OMIM 601487)
이들 3가지 PPAR의 유전장애는 일반적으로 기능상실 및 부수적인 지방질영양증, 인슐린 내성 및/또는 비칸토시스 니그리칸을 [18]초래하는 것으로 기술되어 있다.PPAR,에서는 인슐린 저항의 위험을 감소시키는 Pro12Ala라는 기능 게인 변이가 설명 및 연구되었다.일부 [19]모집단에서 대립 유전자 빈도가 0.03~0.12일 정도로 상당히 널리 알려져 있다.반면 pro115gln은 비만과 관련이 있다.PPAR의 다른 특정 다형성은 체질량 지수가 높은 모집단에서 높은 발병률을 나타낸다.
구조.
다른 핵 수용체와 마찬가지로 PPAR은 구조적으로 모듈화되어 있으며 다음과 같은 기능 도메인을 포함한다.
DBD는 수용체가 활성화될 때 호르몬 반응 요소로 알려진 DNA의 특정 배열에 결합하는 두 개의 아연 손가락 모티브를 포함합니다.
LBD는 13개의 알파 나선형 및 베타 [20]시트로 구성된 광범위한 2차 구조를 가지고 있습니다.자연배위자와 합성배위자 모두 수용체의 활성을 활성화하거나 억제하면서 LBD에 결합할 수 있다.
약리 및 PPAR 변조기
PPARα와 PPAR are은 시판되는 여러 약물의 분자 표적이다.예를 들어 저지방혈증 섬유화물은 PPARα를 활성화하고, 항당뇨병성 티아졸리디오네스는 PPARγ를 활성화한다.합성 화학 물질인 과플루오로옥탄산(perfluoroctanoic acid)은 PPARα를 활성화하고, 합성 과플루오로늄산(perfluoronanoic acid)은 PPARα와 PPARpar를 활성화한다.베르베린은 PPAR,와 다른 화학 [21][22]등급의 다른 천연 화합물을 활성화시킨다.
「 」를 참조해 주세요.
레퍼런스
- ^ Michalik L, Auwerx J, Berger JP, Chatterjee VK, Glass CK, Gonzalez FJ, Grimaldi PA, Kadowaki T, Lazar MA, O'Rahilly S, Palmer CN, Plutzky J, Reddy JK, Spiegelman BM, Staels B, Wahli W (2006). "International Union of Pharmacology. LXI. Peroxisome proliferator-activated receptors". Pharmacol. Rev. 58 (4): 726–41. doi:10.1124/pr.58.4.5. PMID 17132851. S2CID 2240461.
- ^ Dunning, Kylie R.; Anastasi, Marie R.; Zhang, Voueleng J.; Russell, Darryl L.; Robker, Rebecca L. (2014-02-05). "Regulation of Fatty Acid Oxidation in Mouse Cumulus-Oocyte Complexes during Maturation and Modulation by PPAR Agonists". PLOS ONE. 9 (2): e87327. Bibcode:2014PLoSO...987327D. doi:10.1371/journal.pone.0087327. ISSN 1932-6203. PMC 3914821. PMID 24505284.
- ^ Belfiore A, Genua M, Malaguarnera R (2009). "PPAR-gamma Agonists and Their Effects on IGF-I Receptor Signaling: Implications for Cancer". PPAR Res. 2009: 830501. doi:10.1155/2009/830501. PMC 2709717. PMID 19609453.
- ^ a b Berger J, Moller DE (2002). "The mechanisms of action of PPARs". Annu. Rev. Med. 53: 409–35. doi:10.1146/annurev.med.53.082901.104018. PMID 11818483.
- ^ Feige JN, Gelman L, Michalik L, Desvergne B, Wahli W (2006). "From molecular action to physiological outputs: peroxisome proliferator-activated receptors are nuclear receptors at the crossroads of key cellular functions". Prog. Lipid Res. 45 (2): 120–59. doi:10.1016/j.plipres.2005.12.002. PMID 16476485.
- ^ Tyagi S, Gupta P, Saini AS, Kaushal C, Sharma S (October 2011). "The peroxisome proliferator-activated receptor: A family of nuclear receptors role in various diseases". J Adv Pharm Technol Res. 2 (4): 236–40. doi:10.4103/2231-4040.90879. PMC 3255347. PMID 22247890.
- ^ Dreyer C, Krey G, Keller H, Givel F, Helftenbein G, Wahli W (1992). "Control of the peroxisomal beta-oxidation pathway by a novel family of nuclear hormone receptors". Cell. 68 (5): 879–87. doi:10.1016/0092-8674(92)90031-7. PMID 1312391. S2CID 3148132.
- ^ Issemann I, Green S (1990). "Activation of a member of the steroid hormone receptor superfamily by peroxisome proliferators". Nature. 347 (6294): 645–50. Bibcode:1990Natur.347..645I. doi:10.1038/347645a0. PMID 2129546. S2CID 4306126.
- ^ Schmidt A, Endo N, Rutledge SJ, Vogel R, Shinar D, Rodan GA (1992). "Identification of a new member of the steroid hormone receptor superfamily that is activated by a peroxisome proliferator and fatty acids". Mol. Endocrinol. 6 (10): 1634–41. doi:10.1210/mend.6.10.1333051. PMID 1333051.
- ^ Corton JC, Peters JM, Klaunig JE (2018). "The PPARα-dependent rodent liver tumor response is not relevant to humans: addressing misconceptions". Journal of Molecular Endocrinology. 92 (1): 83–119. doi:10.1007/s00204-017-2094-7. PMC 6092738. PMID 29197930.
- ^ Sugden MC, Caton PW, Holness MJ, Miller JJ (2021). "Peroxisome Proliferator-Activated Receptors". Reference Module in Life Sciences. Vol. 17. Elsevier. pp. 574–583. doi:10.1016/B978-0-12-819460-7.00200-0. ISBN 9780128096338. S2CID 241510571.
{{cite book}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Yu S, Reddy JK (2007). "Transcription coactivators for peroxisome proliferator-activated receptors". Biochim. Biophys. Acta. 1771 (8): 936–51. doi:10.1016/j.bbalip.2007.01.008. PMID 17306620.
- ^ 바이오침.생물 물리학.액타 1736:228-236, 2005
- ^ Ezzeddini R, Taghikhani M, Salek Farrokhi A, Somi MH, Samadi N, Esfahani A, Rasaee, MJ (May 2021). "Downregulation of fatty acid oxidation by involvement of HIF-1α and PPARγ in human gastric adenocarcinoma and its related clinical significance". Journal of Physiology and Biochemistry. 77 (2): 249–260. doi:10.1007/s13105-021-00791-3. PMID 33730333. S2CID 232300877.
- ^ Mol. Pharmacol. 77-171-184, 2010
- ^ Marlow LA, Reynolds LA, Cleland AS, Cooper SJ, Gumz ML, Kurakata S, Fujiwara K, Zhang Y, Sebo T, Grant C, McIver B, Wadsworth JT, Radisky DC, Smallridge RC, Copland JA (February 2009). "Reactivation of suppressed RhoB is a critical step for the inhibition of anaplastic thyroid cancer growth". Cancer Res. 69 (4): 1536–44. doi:10.1158/0008-5472.CAN-08-3718. PMC 2644344. PMID 19208833.
- ^ Curr. Mol. Med. 7:532-540, 2007
- ^ Meirhaeghe A, Amouyel P (2004). "Impact of genetic variation of PPARgamma in humans". Mol. Genet. Metab. 83 (1–2): 93–102. doi:10.1016/j.ymgme.2004.08.014. PMID 15464424.
- ^ Buzzetti R, Petrone A, Ribaudo MC, Alemanno I, Zavarella S, Mein CA, Maiani F, Tiberti C, Baroni MG, Vecci E, Arca M, Leonetti F, Di Mario U (2004). "The common PPAR-gamma2 Pro12Ala variant is associated with greater insulin sensitivity". European Journal of Human Genetics. 12 (12): 1050–4. doi:10.1038/sj.ejhg.5201283. PMID 15367918.
- ^ Zoete V, Grosdidier A, Michielin O (2007). "Peroxisome proliferator-activated receptor structures: ligand specificity, molecular switch and interactions with regulators". Biochim. Biophys. Acta. 1771 (8): 915–25. doi:10.1016/j.bbalip.2007.01.007. PMID 17317294.
- ^ Atanasov AG, Wang JN, Gu SP, Bu J, Kramer MP, Baumgartner L, Fakhrudin N, Ladurner A, Malainer C, Vuorinen A, Noha SM, Schwaiger S, Rollinger JM, Schuster D, Stuppner H, Dirsch VM, Heiss EH (2013). "Honokiol: a non-adipogenic PPARγ agonist from nature". Biochim. Biophys. Acta. 1830 (10): 4813–9. doi:10.1016/j.bbagen.2013.06.021. PMC 3790966. PMID 23811337.
- ^ Atanasov AG, Blunder M, Fakhrudin N, Liu X, Noha SM, Malainer C, Kramer MP, Cocic A, Kunert O, Schinkovitz A, Heiss EH, Schuster D, Dirsch VM, Bauer R (2013). "Polyacetylenes from Notopterygium incisum--new selective partial agonists of peroxisome proliferator-activated receptor-gamma". PLOS ONE. 8 (4): e61755. Bibcode:2013PLoSO...861755A. doi:10.1371/journal.pone.0061755. PMC 3632601. PMID 23630612.
외부 링크
- [1] (펜주립대 PPAR 자원 페이지).
- [2] (핵수용체 자원)
- PPAR 참조 개요(Rutgers University).
- 미국 국립의학도서관(MeSH)의 Peroxisome+Proliferator-Activated+Receptors(프로필레이터 활성화+수용체)
- 프로테오피디아 페르옥시좀_프로리퍼레이터-활성화_수용체 - 인터랙티브 3D에서의 페르옥시좀 증식자-활성화 수용체 구조