Rev-ErbA 베타판
Rev-ErbA beta| NR1D2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 에일리어스 | NR1D2, BD73, EAR-1R, RVR, 핵수용체 서브패밀리 1 그룹 D 멤버 2, REVERBB, REVERBeta | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 외부 ID | OMIM: 602304 MGI: 2449205 HomoloGene: 3763 GeneCard: NR1D2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| 위키데이터 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
핵수용체 서브패밀리 1 그룹 D 멤버 2(NR1D2)로도 알려진 Rev-Erb 베타(Rev-Erbβ)는 Rev-Erb 단백질 패밀리의 구성원이다.Rev-Erbα와 마찬가지로 Rev-Erbβ는 전사인자의 핵수용체 슈퍼패밀리에 속하며 유전자 [5]촉진제와의 결합을 통해 유전자 발현을 변조할 수 있다.Rev-Erbα와 함께 Rev-Erbβ는 일주기 클럭의 주요 조절기 역할을 합니다.이 두 단백질은 부분적으로 [6]중복된다.현재의 연구는 Rev-Erbβ가 Rev-Erbα보다 일주기 클럭을 유지하는 데 덜 중요하다는 것을 시사한다. Rev-Erbα의 녹아웃 연구는 상당한 일주기 교란을 초래하지만 Rev-Erbβ에서도 동일한 사실이 발견되지 않았다.Rev-Erbα에 대한 Rev-Erbβ 보상은 조직마다 다르며 Rev-Erbβ의 [7]분리 역할을 설명하기 위해서는 추가 연구가 필요하다.
이 유전자는 중추신경계와 말초신경계, 비장, 하악상악돌기, 혈도에서 발현된다.Rev-Erbβ는 분화 [5]뉴런을 제어하는 데 도움이 되는 유도 신호의 전도에서 중요한 역할을 한다.
검출
Rev-Erbβ는 1994년 B에 발견되었다.Dumas 등은 cDNA를 분리하여 새로운 수용체를 BD73으로 [5]명명했다.Rev-Erbβ라는 이름은 몇 달 후 Eva Enmark, Tommi Kainu, Markku Tapio Pelto-Huikko, Jan ǻke Gustafsson에 의해 쥐의 [8]뇌에서 Rev-Erb 알파-DNA를 분리한 논문에서 만들어졌습니다.
Rev-Erbβ 2라는 이름의 Rev-Erbβ의 새로운 동소 형태는 몇 달 후인 1995년 N. Giambagi와 [7]동료들에 의해 쥐 cDNA를 사용하여 발견되었다.그들은 Rev-Erbβ 1 단백질이 Rev-Erbβ 2 단백질보다 195 아미노산이 더 길다는 점을 제외하고 Rev-Erbβ 1과 동일한 것을 발견했다.그러나 추가 연구에 따르면 발견된 Rev-Erbβ 2 cDNA는 대체 스플라이싱과 다른 폴리아데닐화 부위의 사용을 통해 발생한 Nr1d2 유전자의 스플라이스 변형일 가능성이 있다.
유전학과 진화
포유동물에서 NR1D2(핵수용체 서브패밀리 1군 D멤버 2) 유전자는 Rev-Erbβ 단백질을 부호화한다.NR1D1과는 달리, NR1D2의 반대편 가닥은 유의한 판독 프레임을 가지지 않으며, 유전자는 염색체 [9]3의 앞 가닥에 위치한다.서로 다른 위치에도 불구하고, NR1D1과 NR1D2 유전자는 매우 상동적이며 [5]게놈 내에서 평행하다.사람의 경우 NR1D2 유전자 자체는 5231개의 염기쌍(NR1D2-201)에서 600개의 염기쌍(NR1D2-204)에 이르는 5개의 스플라이스 변이체(NR1D2-205)를 형성하는 10개의 엑손(exon)을 포함한다.단, NR1D2-201만이 기능성 단백질을 생성한다.포유동물에서 NR1D2(Rev-Erbβ)는 뇌, 간, 골격근 및 지방조직을 포함한 여러 조직에서 [9]높은 발현으로 발현된다.
인간의 NR1D2 염기서열을 다른 종과 비교한 결과 쥐, 닭, 도마뱀, 제브라피쉬를 포함한 472개의 철자가 발견되어 동물 전반에 걸쳐 높은 수준의 보존이 이루어졌습니다.NR1D1과 유사하게, 이는 NR1D2가 가장 최근의 공통 동물 조상에 존재했음을 시사한다.NR1D2는 인간에서 오직 하나의 평행체, 즉 17번 염색체에 위치한 NR1D1 유전자와 밀접하게 관련되어 있지만, 그것은 갑상선 호르몬 수용체 베타(THRB), 페르옥시좀 증식자 활성화 수용체 델타(PPARD) 및 레티노산 수용체 유전자와 기능적으로 관련이 있다.엡토르 베타(RARB).연계 분석 결과 NR1D2와 TRB는 염색체 3에 근접하여 높은 연관성을 보이며, 둘 다 RARB와 관련이 있는 것으로 나타났다.NR1D1/THRA 궤적과 RARA 유전자 사이의 연결과 결합하면, 이는 이 두 유전자 클러스터가 복제 [10]사건에서 발생했음을 시사한다.
구조.
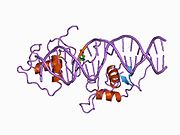
인간 NR1D2 유전자는 579개의 아미노산으로 이루어진 단백질 생성물(REV-ERBβ)을 생성한다.Rev-Erbβ는 전사 억제의 구조와 메커니즘 모두에서 Rev-Erbα와 유사하다.Rev-Erbα와 마찬가지로 Rev-Erbβ는 핵수용체 단백질에 공통적인 3가지 주요 기능 도메인을 가지며, 여기에는 C 말단의 DNA 결합 도메인(DBD)과 리간드 결합 도메인(LBD)이 있으며, 이들 도메인은 Rev-Erb Orthologs에 고도로 보존되어 있어 변조를 [11]가능하게 하는 N 말단 도메인이 포함된다.
Rev-Erbα와 마찬가지로 Rev-Erbβ는 두 개의 C4형 아연 [12]핑거를 포함하는 DBD를 통해 두 가지 종류의 DNA 반응 요소에 결합할 수 있습니다.이 두 가지 등급에는 전사 활성제인 레티노산 수용체 관련 고아 수용체(ROR)[13]와의 상호작용으로 인해 일반적으로 RORE로 지칭되는 DNA 염기서열과 RevDR2로 알려진 RORE의 직접 반복 2 요소가 포함됩니다.Rev-Erb 단백질은 LBD를 통한 핵 수용체에 의한 공동 활성제 모집 및 활성화에 필요한 C 말단에 나선이 없다는 점에서 다른 핵 수용체와는 다르다.대신 Rev-Erbs는 구성전사활성제 ROR의 결합을 방지함으로써 단일 RORE 요소에서의 경쟁결합을 통해 모노머로서의 전사를 억제하거나 RevDR2 [14]부위와의 결합을 통해 호모디머로서의 전사를 억제할 수 있다.Rev-Erb 호모디머는 레티노이드 및 갑상선 수용체(SMRT)의 사일런싱 매개체(Silencing Mediator)와의 상호작용에 필요하다.NCoR과의 상호작용은 Rev-Erb 리간드 결합 포켓에 결합하는 헴과의 상호작용에 의해 안정화된다.Rev-Erbβ는 나선 3, 7, 11이 헴을 수용하기 위해 리간드 결합 포켓을 확대하기 위해 움직인다는 것을 나타내기 때문에 헴과 복합되었을 때 구조변화를 겪는다.Rev-Erb 단백질에 의한 억제는 또한 클래스 I 히스톤 탈아세틸화효소 3(HDAC3)과 NCoR의 상호작용을 필요로 하며, 이는 히스톤 탈아세틸화를 [12]통한 유전자 억제를 초래한다.
기능.
일주 발진기
Rev-Erbβ는 Rev-Erbα와 동일하거나 유사한 일일 프로파일을 가진 게놈 Rev-Erbα 결합 부위에 결합한다.또한 이 단백질은 클럭 및 대사 유전자 조절을 유지하고 Rev-Erbα가 없을 때 시스템 기능을 보호합니다.Rev-Erbβ는 Rev-Erbα가 상실된 경우 대사 장애로 인한 기능 상실을 보상한다.Rev-Erbα가 누락되고 Rev-Erbβ가 존재하는 경우에도 간 및 대사 과정이 계속 실행될 수 있습니다.Rev-Erbα와 Rev-Erbβ를 모두 잃으면 세포가 부정맥이 [15]된다.
Rev-Erbβ가 누락되면 급격한 효과와 함께 대사 활동의 성능에 큰 변화가 있을 수 있다.예를 들어 다음과 같습니다.
- Rev-Erbβ 결핍은 핵심 클럭 유전자 발현이 진동하는 동안 유전자 발현에 대한 일주기 네트워크의 결합 형성에 급격한 차이를 일으킨다.
- Rev-Erbα 또는 Rev-Erbβ가 없는 것은 코어 클럭 유전자의 발현 리듬에 영향을 주지 않지만 다른 리드미컬하게 발현되는 출력 유전자에 영향을 미친다.
- Rev-Erbβ 결핍은 PER2의 [15]일주기 발현 리듬을 바꾸지 않는다.
대사
Rev-Erbβ는 레티노산 관련 고아 수용체α(RORα)의 트랜스 활성화를 차단하는 역할을 하며, RORα는 리포단백질 콜레스테롤, 지질 항상성 및 염증의 조절에 관여한다.Rev-Erbβ와 RORα는 모두 골격근과 같은 유사한 조직에서 발현된다.그들은 골격근 내의 유사한 발현 패턴, 표적 유전자, 그리고 동족 서열을 가지고 있다.Rev-Erbβ는 지질 흡수를 돕는 여러 유전자가 발현을 감소시킨다.Rev-Erbβ는 골격근의 지질과 에너지 균질성을 조절한다.Rev-Erbβ는 이상지질혈증의 치료 및 근육 [16]성장 조절에 유용할 수 있다.
Rev-Erbβ는 또한 일주기 조절 유전자이며, mRNA는 생체 내 및 혈청 동기 세포 배양에서 리듬감 있는 발현을 나타낸다.그러나 Rev-Erbβ가 핵심 일주기 클럭의 진동에 어느 정도 기여하는지는 현재 알려져 있지 않다.그러나 헴은 유전자 억제를 매개하는 관련된 Rev-Erbα 수용체를 통해 간 글루코네제닉 유전자 발현과 포도당 출력을 억제하는 것으로 나타났다.따라서 Rev-Erbα 수용체는 헴을 검출하여 세포 클럭, 포도당 항상성 및 에너지 [17]대사를 조정한다.
Rev-Erbβ는 골격근 미토콘드리아 생물 형성에 역할을 한다.원래 Rev-Erbβ는 Rev-Erbα의 기능적으로 중복되는 것으로 생각되었지만, 최근의 연구 결과는 미묘한 차이가 있음을 증명한다.Rev-Erbβ배위자는 대사증후군과 같은 대사장애 치료에 사용될 수 있다.그것은 골격근의 신진대사와 치료 [18]옵션에서 유익할 수 있는 에너지를 통제한다.
Rev-Erbβ 유전자는 특정 KO 돌연변이를 생성함으로써 클럭 출력 유전자의 하류 조절에 기여한다.Rev-Erbβ가 주기의 핵심 시계에서 가지는 모든 기능과 Rev-Erbα와 정확히 어떻게 다른지는 아직 알려지지 않았다.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000174738 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000021775 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c d Dumas B, Harding HP, Choi HS, Lehmann KA, Chung M, Lazar MA, Moore DD (August 1994). "A new orphan member of the nuclear hormone receptor superfamily closely related to Rev-Erb". Molecular Endocrinology. 8 (8): 996–1005. doi:10.1210/mend.8.8.7997240. PMID 7997240.
- ^ Koh YS, Moore DD (April 1999). "Linkage of the nuclear hormone receptor genes NR1D2, THRB, and RARB: evidence for an ancient, large-scale duplication". Genomics. 57 (2): 289–92. doi:10.1006/geno.1998.5683. PMID 10198169.
- ^ a b Giambiagi N, Cassia R, Petropoulos I, Part D, Cereghini S, Zakin MM, Ochoa A (December 1995). "Rev-erb beta 2, a novel isoform of the Rev-erb family of orphan nuclear receptors". Biochemistry and Molecular Biology International. 37 (6): 1091–1102. PMID 8747539.
- ^ Enmark E, Kainu T, Pelto-Huikko M, Gustafsson JA (October 1994). "Identification of a novel member of the nuclear receptor superfamily which is closely related to Rev-ErbA". Biochemical and Biophysical Research Communications. 204 (1): 49–56. doi:10.1006/bbrc.1994.2424. PMID 7945391.
- ^ a b Yates AD, Achuthan P, Akanni W, Allen J, Allen J, Alvarez-Jarreta J, et al. (January 2020). "Ensembl 2020". Nucleic Acids Research. 48 (D1): D682–D688. doi:10.1093/nar/gkz966. PMC 7145704. PMID 31691826.
- ^ Burris TP (July 2008). "Nuclear hormone receptors for heme: REV-ERBalpha and REV-ERBbeta are ligand-regulated components of the mammalian clock". Molecular Endocrinology. 22 (7): 1509–20. doi:10.1210/me.2007-0519. PMC 5419435. PMID 18218725.
- ^ Woo EJ, Jeong DG, Lim MY, Jun Kim S, Kim KJ, Yoon SM, et al. (October 2007). "Structural insight into the constitutive repression function of the nuclear receptor Rev-erbbeta". Journal of Molecular Biology. 373 (3): 735–44. doi:10.1016/j.jmb.2007.08.037. PMID 17870090.
- ^ a b Pardee KI, Xu X, Reinking J, Schuetz A, Dong A, Liu S, et al. (February 2009). "The structural basis of gas-responsive transcription by the human nuclear hormone receptor REV-ERBbeta". PLOS Biology. 7 (2): e43. doi:10.1371/journal.pbio.1000043. PMC 2652392. PMID 19243223.
- ^ "NR1D1 Gene NR1D1 Protein NR1D1 Antibody". GeneCards. Retrieved 2021-05-06.
- ^ Zhao Q, Khorasanizadeh S, Miyoshi Y, Lazar MA, Rastinejad F (May 1998). "Structural elements of an orphan nuclear receptor-DNA complex". Molecular Cell. 1 (6): 849–61. doi:10.1016/s1097-2765(00)80084-2. PMID 9660968.
- ^ a b Bugge A, Feng D, Everett LJ, Briggs ER, Mullican SE, Wang F, et al. (April 2012). "Rev-erbα and Rev-erbβ coordinately protect the circadian clock and normal metabolic function". Genes & Development. 26 (7): 657–67. doi:10.1101/gad.186858.112. PMC 3323877. PMID 22474260.
- ^ a b Ikeda R, Tsuchiya Y, Koike N, Umemura Y, Inokawa H, Ono R, et al. (July 2019). "REV-ERBα and REV-ERBβ function as key factors regulating Mammalian Circadian Output". Scientific Reports. 9 (1): 10171. doi:10.1038/s41598-019-46656-0. PMC 6629614. PMID 31308426.
- ^ Ramakrishnan SN, Lau P, Burke LJ, Muscat GE (March 2005). "Rev-erbbeta regulates the expression of genes involved in lipid absorption in skeletal muscle cells: evidence for cross-talk between orphan nuclear receptors and myokines". The Journal of Biological Chemistry. 280 (10): 8651–9. doi:10.1074/jbc.M413949200. PMID 15623503.
- ^ Yin L, Wu N, Curtin JC, Qatanani M, Szwergold NR, Reid RA, et al. (December 2007). "Rev-erbalpha, a heme sensor that coordinates metabolic and circadian pathways". Science. 318 (5857): 1786–9. doi:10.1126/science.1150179. PMID 18006707. S2CID 84073753.
추가 정보
- Ramakrishnan SN, Lau P, Crowther LM, Cleasby ME, Millard S, Leong GM, Cooney GJ, Muscat GE (October 2009). "Rev-erb beta regulates the Srebp-1c promoter and mRNA expression in skeletal muscle cells". Biochemical and Biophysical Research Communications. 388 (4): 654–9. doi:10.1016/j.bbrc.2009.08.045. PMID 19682428.
외부 링크
- NR1D2+단백질+인간(미국 국립의학도서관 의학 과목 표제(MeSH))