비타민C
Vitamin C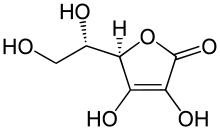 | |
 | |
| 임상자료 | |
|---|---|
| 발음 | /əˈskɔːrbɪk/, /əˈskɔːrbeɪt, -bɪt/ |
| 상호 | 아스코르, 세콘, 세발린, 기타 |
| 기타명 | l-아스코르브산, 아스코르브산, 아스코르브산 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a682583 |
| 라이센스 데이터 | |
| 경로: 행정부. | 입으로, 근육내(IM), 정맥내(IV), 피하 |
| ATC코드 | |
| 법적 지위 | |
| 법적 지위 | |
| 약동학적 데이터 | |
| 생체이용률 | 용량이[4] 증가함에 따라 빠르게 감소합니다. |
| 단백질 결합 | 무시할 수 있음 |
| 탈락 반감기 | 플라즈마 농도에 따라 차이가 있음 |
| 배설 | 신장 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드럭뱅크 | |
| 켐스파이더 | |
| 유니 |
|
| 케그 | |
| ChEBI |
|
| CHEMBL |
|
| NIAID ChemDB | |
| PDB 리간드 | |
| E수 | E300 (항산화제, ...) |
| CompTox 대시보드 (EPA) | |
| ECHA 인포카드 | 100.000.061 |
| 화학 및 물리 데이터 | |
| 공식 | C6H8O6 |
| 어금니 질량 | 176.124g·mol−1 |
| 3D 모델(JSmol) | |
| 밀도 | 1.694g/cm3 |
| 융점 | 190~192°C(374~378°F) |
| 끓는점 | 552.7 °C (1,026.9 °F) [5] |
| |
| |
| (verify) | |
비타민 C(아스코르브산 및 아스코르브산으로도 알려져 있음)는 감귤류 및 기타 과일, 딸기류 및 야채에서 발견되는 수용성 비타민입니다. 또한 일반 처방 의약품이며 일부 국가에서는 비처방 식이 보충제로 판매됩니다. 치료제로 비타민C 결핍으로 인한 질환인 괴혈병을 예방하고 치료하는 데 사용됩니다.
비타민 C는 조직의 복구, 콜라겐 형성 및 특정 신경 전달 물질의 효소 생성에 관여하는 필수 영양소입니다. 여러 효소의 기능에 필요하며 면역계 기능에 중요합니다.[6] 항산화 기능도 합니다. 비타민 C는 입으로 섭취하거나 근육 내, 피하 또는 정맥 주사로 섭취할 수 있습니다. 비타민C가 적당히 결핍되면 감기, 암, 코로나19 등 질병 위험이 높아진다는 근거로 다양한 건강 주장이 존재합니다. 비타민 C가 부족하다고 생각되지 않는 사람들의 권장 식이 섭취량을 초과하여 비타민 C를 보충함으로써 얻을 수 있는 이점에 대한 주장도 있습니다. 비타민 C는 일반적으로 내약성이 좋습니다. 다량 복용 시 위장 불편, 두통, 수면 장애, 피부 홍조 등이 나타날 수 있습니다. 미국 의학 연구소는 많은 양을 섭취하지 말 것을 권장합니다.[7]: 155–165
대부분의 동물은 자신의 비타민 C를 합성할 수 있습니다. 그러나 유인원(인간 포함)과 원숭이(모든 영장류는 아님), 대부분의 박쥐, 대부분의 물고기, 일부 설치류 및 특정 다른 동물은 합성 효소의 유전자가 기능을 상실하게 만드는 돌연변이를 가지고 있기 때문에 식이 공급원으로부터 획득해야 합니다.
1912년에 비타민 C가 발견되었고 1928년에 분리되었으며 1933년에 화학적으로 생산된 최초의 비타민이었습니다. 부분적으로 알베르트 스젠트-예르지는 이 발견으로 1937년 노벨 생리학·의학상을 수상했습니다.
화학
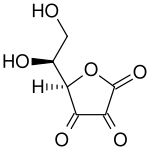
"비타민 C"라는 이름은 항상 아스코르브산과 그 산화된 형태인 디하이드로아스코르브산(DHA)의 l- 거울상이성질체를 나타냅니다. 따라서 달리 기재되지 않는 한, 영양 문헌에서 "아스코르브산" 및 "아스코르브산"은 각각 l-아스코르브산 및 l-아스코르브산을 지칭합니다. 아스코르브산은 포도당과 구조적으로 관련된 약당산입니다. 생물학적 시스템에서 아스코르브산은 낮은 pH에서만 발견될 수 있지만 pH 5 이상의 용액에서는 이온화된 형태인 아스코르브산이 주로 발견됩니다.[8]
아스코르브산 검출을 위한 수많은 분석 방법이 개발되었습니다. 예를 들어, 과일 주스와 같은 식품 샘플의 비타민 C 함량은 디클로로페놀인도페놀(DCPIP) 용액을 탈색시키는 데 필요한 샘플의 부피를 측정한 다음 알려진 비타민 C 농도와 비교하여 결과를 보정하여 계산할 수 있습니다.[9][10]
결핍증
혈장 비타민 C는 비타민 C 상태에 대해 가장 널리 적용되는 검사입니다.[8] 적절한 수준은 거의 50μmol/L로 정의됩니다. 비타민 C의 저혈당증은 23μmol/L 미만, 결핍은 11.4μmol/L 미만으로 정의됩니다.[11] 미국 2017-18년 국민건강영양조사 자료에서 20세 이상의 경우 평균 혈청 농도가 53.4μmol/L로 나타났습니다. 부족하다고 보고된 사람의 비율은 5.9%[12]였습니다. 전 세계적으로 비타민 C 결핍은 저소득 및 중간 소득 국가에서 흔하며 고소득 국가에서도 드물지 않습니다. 후자의 경우 여성보다 남성에서 유병률이 더 높습니다.[13]
혈장 수준은 약 65μmol/L로 포화 상태로 간주되며, 이는 권장 섭취량을 훨씬 초과하는 100~200mg/일 섭취량으로 달성됩니다. 흡수 효율이 떨어지고 흡수된 초과분은 소변으로 배출되기 때문에 경구 섭취량이 많아도 혈장이나 조직 농도가 더 높아지지 않습니다.[8]
진단검사
혈장 중 비타민 C 함량은 비타민 상태를 판단하는 데 사용됩니다. 연구 목적으로, 백혈구와 조직에서 농도를 평가할 수 있는데, 백혈구는 에너지 의존성 수송 시스템을 통해 혈장보다 더 높은 크기로 정상적으로 유지되고, 식이 결핍 시 혈장 농도보다 더 느리게 고갈되고, 식이 보충 시 더 빠르게 회복됩니다.[7]: 103–109 그러나 이러한 분석은 측정하기 어렵기 때문에 표준 진단 테스트의 일부가 아닙니다.[8][14]
다이어트
권장소비량
성인의 비타민 C 섭취 권장 사항은 여러 국가 기관에서 설정했습니다.
- 40mg/일 : 하이데라바드[15], 인도 국립영양연구소
- 45 mg/day 또는 300 mg/week : 세계보건기구[16]
- 80mg/day : 유럽 영양표시위원회[17]
- 90mg/일(males) 및 75mg/일(females): 2007년[18] 캐나다 보건
- 90mg/일(males) 및 75mg/일(females): 미국 국립과학원.[7]: 134–152
- 100 mg/[19]day : 일본 국립 보건 영양 연구소
- 110mg/일(males) 및 95mg/일(females): 유럽식품안전청[20]
| 미국 비타민C 권장량 (1일 mg)[7]: 134–152 | |
|---|---|
| RDA(1~3세 아동) | 15 |
| RDA(4~8세 아동) | 25 |
| RDA(9~13세 어린이) | 45 |
| RDA(14~18세 여아) | 65 |
| RDA(14~18세 남아) | 75 |
| RDA(성체여) | 75 |
| RDA(성인 남성) | 90 |
| RDA(임신) | 85 |
| RDA(액정) | 120 |
| UL(성체여) | 2,000 |
| UL(성인 남성) | 2,000 |
2000년에 북미 식생활 참조섭취의 비타민 C 장이 업데이트되어 성인 남성의 경우 권장식이 허용량(RDA)을 하루 90mg, 성인 여성의 경우 75mg/일, 성인의 경우 허용 상한 섭취량(UL)을 2,000mg/일로 설정했습니다.[7]: 134–152 표(오른쪽)는 어린이의 경우 미국과 캐나다의 RDA,[7]: 134–152 임신부와 수유부의 경우 성인의 경우 UL을 보여줍니다.
유럽 연합의 경우, EFSA는 성인과 어린이에게 더 높은 권장 사항을 설정했습니다. 1-3세의 경우 20mg/일, 4-6세의 경우 30mg/일, 7-10세의 경우 45mg/일, 11-14세의 경우 70mg/일, 15-17세의 경우 100mg/일, 15-17세의 경우 90mg/일입니다. 임신 100 mg/day, 수유 155 mg/[20]day.
반면 인도는 1세부터 성인까지 40mg/day, 임신 60mg/day, 수유 80mg/day로 권장량을 훨씬 낮게 설정했습니다.[15] 분명히 국가 간에 합의가 이루어지지 않고 있습니다.
흡연자와 간접흡연에 노출된 사람들은 비흡연자보다 혈청 비타민 C 수치가 낮습니다.[11] 연기를 흡입하면 산화적 손상을 일으켜 이 항산화 비타민을 고갈시킨다는 생각입니다.[7]: 152–153 미국 의학 연구소는 흡연자들이 비흡연자들보다 하루에 35mg의 비타민 C를 더 필요로 한다고 추정했지만, 공식적으로 흡연자들에게 더 높은 RDA를 설정하지는 않았습니다.[7]: 152–153 비타민 C 섭취와 폐암 사이에는 역의 관계가 관찰되었지만, 이러한 관찰을 확인하기 위해서는 더 많은 연구가 필요하다는 결론이 나왔습니다.[21]
미국 국립 보건 통계 센터는 미국 내 성인과 어린이의 건강 및 영양 상태를 평가하기 위해 매년 NHANES(National Health and Nutrition Examination Survey)를 실시하고 있습니다. 일부 결과는 미국에서 우리가 먹는 것으로 보고됩니다. 2013-2014년 조사에 따르면 20세 이상 성인의 경우 남성은 평균 83.3 mg/d, 여성은 75.1 mg/d를 섭취했습니다. 이는 여성의 절반과 남성의 절반 이상이 비타민 C를 위한 RDA를 섭취하지 않고 있다는 것을 의미합니다.[22] 같은 조사에 따르면 성인의 약 30%가 비타민 C 식이 보충제 또는 비타민 C가 포함된 종합 비타민/미네랄 보충제를 섭취했으며 이러한 사람들의 총 섭취량은 300~400mg/d 사이라고 보고했습니다.[23]
허용 가능한 상한 흡기 레벨
2000년 미국 국립과학원 의학연구소는 성인의 허용 상한 섭취 수준(UL)을 2,000 mg/day로 설정했습니다. 이 양은 인간 실험에서 설사 및 기타 위장 장애를 하루에 3,000 mg 이상 섭취한 것으로 보고되었기 때문에 선택되었습니다. 이는 LOAEL(Lowest-Observed-Adverse-Effect Level)이었으며, 이는 다른 부작용이 훨씬 더 높은 섭취량에서 관찰되었음을 의미합니다. UL은 더 어린 아이들과 더 어린 아이들에게 점진적으로 낮아집니다.[7]: 155–165 2006년 유럽식품안전청(EFSA)도 그 용량 수준의 장애를 지적했지만,[24] 2010년 일본 국립보건영양연구소와 마찬가지로 비타민 C의 UL을 설정할 충분한 증거가 없다는 결론에 도달했습니다.[19]
식품표시
미국 식품 및 식이 보충제 라벨링을 위해 1회 제공량은 일일 가치(%DV)의 백분율로 표시됩니다. 비타민 C 표시 목적으로 Daily Value의 100%는 60 mg 이었지만 2016년 5월 27일자로 RDA와 합의하기 위해 90 mg으로 수정되었습니다.[25][26] Reference Daily Inket에는 신구 성인 일일 값 표가 제공됩니다.
유럽 연합 규정은 라벨에 에너지, 단백질, 지방, 포화 지방, 탄수화물, 설탕 및 소금을 표시하도록 요구합니다. 상당한 양이 존재하는 경우 자발적인 영양소가 나타날 수 있습니다. 일일 값 대신 양은 RI(Reference Input)의 백분율로 표시됩니다. 비타민 C의 경우 2011년 100% RI가 80mg으로 설정되었습니다.[27]
원천
다른 식물성 식품에도 존재하지만 비타민 C의 가장 풍부한 천연 공급원은 과일과 채소입니다.[6] 비타민은 가장 널리 섭취되는 식이 보충제입니다.[6]
식물원
"식물성 식품은 일반적으로 비타민 C의 좋은 공급원이지만, 식물 유래 식품의 양은 식물의 다양성, 토양 상태, 자란 기후, 선택된 후의 기간, 저장 조건 및 준비 방법에 따라 다릅니다."[28] 예를 들어, 유기농 감귤류는 기존에 재배된 감귤류보다 비타민 C 함량이 더 높을 수 있습니다.[28] 다음 표는 근사치이며 다양한 원시 식물 공급원의 상대적 존재비를 보여줍니다.[29][30] 그 양은 과일이나 야채의 먹을 수 있는 부분의 100그램 당 밀리그램으로 표시됩니다.
| 원플랜트원[31] | 양 (mg/100g) |
|---|---|
| 카카두 자두 | 1000–5300[32] |
| 카무카무 | 2800[30][33] |
| 아세롤라 | 1677[34] |
| 인도구스베리 | 445[35][36] |
| 로즈힙 | 426 |
| 참다랑어 | 400[37] |
| 구아바 | 228 |
| 블랙커런트 | 200 |
| 황피망/캡시쿰 | 183 |
| 홍피망/캡시쿰 | 128 |
| 케일 | 120 |
| 브로콜리 | 90 |
| 키위프루트 | 90 |
| 원플랜트원[31] | 양 (mg/100g) |
|---|---|
| 피망/캡시쿰 | 80 |
| 브뤼셀 새싹 | 80 |
| 로건베리, 레드커런트 | 80 |
| 클라우드베리, 엘더베리 | 60 |
| 딸기 | 60 |
| 파파야. | 60 |
| 오렌지, 레몬 | 53 |
| 콜리플라워 | 48 |
| 파인애플. | 48 |
| 캔탈루프 | 40 |
| 열정과일, 복분자 | 30 |
| 자몽, 라임 | 30 |
| 양배추, 시금치 | 30 |
| 원플랜트원[31] | 양 (mg/100g) |
|---|---|
| 망고 | 28 |
| 블랙베리, 카사바 | 21 |
| 감자 | 20 |
| 참외 | 20 |
| 토마토 | 14 |
| 크랜베리 | 13 |
| 블루베리,포도 | 10 |
| 살구, 매실, 수박 | 10 |
| 아보카도 | 8.8 |
| 양파 | 7.4 |
| 체리, 복숭아 | 7 |
| 사과 | 6 |
| 당근, 아스파라거스 | 6 |
동물원
식물 공급원에 비해 동물성 식품은 비타민 C를 그렇게 많이 제공하지 않으며, 그것이 요리될 때 사용되는 열에 의해 크게 파괴됩니다. 예를 들어 생닭 간에는 17.9mg/100g이 함유되어 있지만 튀겨내면 그 함량이 2.7mg/100g으로 줄어듭니다. 비타민 C는 사람의 모유에 5.0mg/100g으로 존재합니다. 소젖에는 1.0mg/100g이 함유되어 있는데 저온살균의 열이 이를 파괴합니다.[38]
음식 준비
비타민 C는 특정 조건에서 화학적으로 분해되는데, 그 중 많은 부분이 음식을 조리하는 과정에서 발생할 수 있습니다. 다양한 식품 물질의 비타민 C 농도는 저장되는 온도에 비례하여 시간이 지남에 따라 감소합니다.[39] 요리를 하면 야채의 비타민 C 함량이 60% 정도 감소할 수 있는데, 이는 효소 파괴가 증가했기 때문일 수 있습니다.[40] 조리 시간이 길어지면 이러한 효과가 더 커질 수 있습니다.[41] 음식으로 인한 비타민 C 손실의 또 다른 원인은 침출수인데, 침출수는 비타민 C를 요리수로 전달하는데, 침출수는 침출수를 따라내고 먹지 않습니다.[42]
보충제
비타민 C 식이 보충제는 정제, 캡슐, 음료 믹스 패킷, 멀티 비타민/미네랄 제형, 항산화 제형 및 결정성 분말로 제공됩니다.[43] 비타민 C는 또한 일부 과일 주스와 주스 음료에 첨가됩니다. 정제 및 캡슐 함량은 1회 제공량당 25mg에서 1500mg입니다. 가장 일반적으로 사용되는 보충제 화합물은 아스코르브산, 아스코르브산나트륨 및 아스코르브산칼슘입니다.[43] 비타민 C 분자는 지방산 팔미테이트에 결합되어 아스코빌 팔미테이트를 생성하거나 리포좀에 통합될 수도 있습니다.[44]
식량강화
국가들은 알려진 결핍을 해결하기 위해 영양소로 음식을 강화합니다.[45] 많은 국가들이 밀가루, 옥수수(옥수수) 밀가루 또는 쌀을 비타민과 함께 강화하기 위해 의무적이거나 자발적인 프로그램을 가지고 있지만,[46] 그러한 프로그램에 비타민 C를 포함하는 국가는 없습니다.[46] 식량 원조 상품의 비타민 C 강화(1997)에서 설명한 바와 같이, 미국은 나중에 평화를 위한 식량법과 인도주의 지원국의 대리인으로 국제 식량 구호 프로그램에 배급을 제공합니다.[47] 비타민 C는 옥수수-콩 블렌드 및 밀-콩 블렌드 제품에 40mg/100g으로 첨가됩니다. (미네랄 및 기타 비타민과 함께). 이러한 고도로 강화된 혼합 식품의 보충제는 캠프의 난민과 실향민 및 주로 어머니와 어린이를 대상으로 하는 개발 사료 프로그램의 수혜자에게 제공됩니다.[42] 보고서는 다음과 같이 덧붙였습니다. "비타민 C (L-아스코르브산)는 식품에서 가장 불안정한 비타민 중 하나이기 때문에 안정성이 우려됩니다. 처리 및 보관 중에 발생하는 주요 손실은 빛, 산소, 열, pH 증가, 높은 수분 함량(수분 활성) 및 구리 또는 제1철 염의 존재에 의해 가속화되는 산화에 기인합니다. 상품 강화에 사용되는 비타민 C는 산화를 줄이기 위해 에틸셀룰로오스(2.5%)로 코팅됩니다. 식품 가공 및 준비 과정에서도 산화적 손실이 발생하며, 조리액에 녹았다가 버려지면 비타민 C가 추가로 손실될 수 있습니다."[42]
식품 보존 첨가제
아스코르브산과 그 염 및 에스테르의 일부는 주로 산화 및 효소 갈변을 늦추기 위해 통조림 과일과 같은 다양한 식품에 첨가되는 일반적인 첨가제입니다.[48] 빵 제조에 사용되는 밀가루 처리제로 사용할 수 있습니다.[49] 식품 첨가물로서 안전성 평가 및 유럽 식품 안전청의 승인과 함께 E 번호가 부여됩니다.[50] 관련 E 번호는 다음과 같습니다.
- E300 아스코르브산(영국,[51] 미국[52] 캐나다,[53] 호주 및 뉴질랜드에서[54] 식품 첨가물로 사용 승인됨)
- E301 아스코르브산나트륨(영국,[51] 미국,[55] 캐나다,[53] 호주 및 뉴질랜드에서[54] 식품 첨가물로 사용 승인됨)
- E302 칼슘 아스코르브산염(영국,[51] 미국[52] 캐나다,[53] 호주 및 뉴질랜드에서[54] 식품 첨가물로 사용 승인됨)
- E303 포타슘 아스코르브산염 (호주 및 뉴질랜드에서 [54]승인되었지만 영국, 미국 또는 캐나다에서는 승인되지 않음)
- 아스코르빌 팔미테이트와 같은 아스코르브산의 E304 지방산 에스테르(영국,[51] 미국,[52] 캐나다,[53] 호주 및 뉴질랜드에서[54] 식품 첨가물로 사용 승인됨)
비타민 C의 입체 이성질체는 사람에게는 효능이 없음에도 불구하고 식품에서도 비슷한 효과를 보입니다. 에리트로브산과 그 나트륨염(E315, E316)을 포함합니다.[51]
약리학
약동학은 약물 – 이 경우 비타민 C – 가 유기체에 어떤 영향을 미치는지에 대한 연구인 반면, 약동학은 유기체가 약물에 어떤 영향을 미치는지에 대한 연구입니다.
약동학
약역학에는 비타민 C가 보조인자인 효소가 포함되며, 기능이 결핍 상태에서 잠재적으로 손상될 수 있으며, 정상적인 요구 사항을 초과하여 비타민 C의 경구 또는 주입에 의해 영향을 받는 효소 보조인자 또는 기타 생리학적 기능이 포함됩니다. 정상적인 생리학적 농도에서 비타민 C는 효소 기질 또는 보조 인자 및 전자 공여체 항산화제 역할을 합니다. 효소 기능에는 콜라겐, 카르니틴 및 신경전달물질의 합성, 티로신의 합성 및 이화작용, 마이크로솜의 대사가 포함됩니다. 비효소적인 기능에서는 환원제 역할을 하여 산화된 분자에 전자를 공여하고 산화를 방지하여 철과 구리 원자를 환원 상태로 유지합니다.[8] 정맥 투여에 의해 달성되는 비생리학적 농도에서 비타민 C는 암세포에 대한 치료 독성과 함께 산화방지제로서 기능할 수 있습니다.[56][57]
비타민 C는 다음과 같은 효소의 보조인자로서 기능합니다.[8]
- 콜라겐 합성에서 프롤린과 라이신의 하이드록실화에 필요한 세 그룹의 효소(프롤릴-3-하이드록실화효소, 프롤릴-4-하이드록실화효소 및 라이실 하이드록실화효소). 이러한 반응은 프롤릴 하이드록실화효소와 라이실 하이드록실화효소를 통해 콜라겐 분자의 아미노산 프롤린 또는 라이신에 하이드록실기를 추가하며, 둘 다 보조인자로 비타민 C를 필요로 합니다. 보조인자로서의 비타민 C의 역할은 프롤릴 하이드록실라제와 리실 하이드록실라제를 Fe에서2+ Fe로3+ 산화시키고 Fe에서3+ Fe로2+ 환원시키는 것입니다. 하이드록실화는 콜라겐 분자가 3중 나선 구조를 가정할 수 있도록 하므로, 비타민 C는 흉터 조직, 혈관 및 연골의 발달 및 유지에 필수적입니다.
- 카르니틴의 합성에는 두 가지 효소(ε-N-트리메틸-L-라이신 하이드록실라제와 γ-부티로베타인 하이드록실라제)가 필요합니다. 카르니틴은 ATP 생성을 위해 지방산을 미토콘드리아로 수송하는 데 필수적입니다.
- 저산소증-유도 인자-프롤린 다이옥시게나제 효소(동형: EGLN1, EGLN2 및 EGLN3)는 세포가 낮은 농도의 산소에 생리적으로 반응할 수 있도록 합니다.
- 도파민 베타-하이드록실라제는 도파민으로부터 노르에피네프린의 생합성에 참여합니다.
- 펩티딜글리신 알파-아미드화 모노옥시게나제는 c-말단 글리신 잔기에서 글리옥실레이트 잔기를 제거하여 펩티드 호르몬을 아미드화합니다. 이는 펩타이드 호르몬의 안정성과 활성을 증가시킵니다.
항산화제로서 아스코르브산염은 활성 산소와 질소 화합물을 제거하여 이러한 자유 라디칼 화합물의 잠재적인 조직 손상을 중화합니다. 산화된 형태인 디하이드로아스코르브산염은 글루타티온과 같은 내인성 항산화제에 의해 다시 아스코르브산염으로 재활용됩니다.[7]: 98–99 눈에서 아스코르브산염은 광분해로 발생하는 자유 라디칼 손상으로부터 보호하는 것으로 생각됩니다; 혈장 아스코르브산염이 높을수록 애벌레의 위험이 감소하는 것과 관련이 있습니다.[58] 아스코르브산염은 또한 α-토코페롤과 같은 다른 생물학적 항산화제를 활성 상태로 재생함으로써 간접적으로 항산화 보호를 제공할 수 있습니다.[7]: 98–99 또한 아스코르브산염은 약물 및 환경 발암 물질과 같은 매우 다양한 기질을 비활성화하는 마이크로솜 약물-대사 시스템에서 복합 기능 산화효소에 대한 비효소적 환원제로서도 기능합니다.[7]: 98–99
약동학
아스코르브산은 단순 확산과 능동 수송에 의해 체내에 흡수됩니다.[59] 비타민 C의 약 70%–90%는 30–180 mg/day의 적당한 섭취량으로 흡수됩니다. 그러나 1,000 mg/day 이상의 용량에서는 능동 수송 시스템이 포화됨에 따라 흡수율이 50% 미만으로 떨어집니다.[4] 능동 수송은 나트륨-아스코르브산염 공동 수송 단백질(SVCT)과 육탄당 수송 단백질(GLUT)에 의해 관리됩니다. SVCT1 및 SVCT2는 원형질막을 가로질러 아스코르브산염을 수입합니다.[60] 육탄당 수송 단백질 GLUT1, GLUT3 및 GLUT4는 비타민 C의 산화된 탈아스코르브산(DHA) 형태만을 전달합니다.[61][62] 세포가 빠르게 DHA를 아스코르브산염으로 환원시키기 때문에 정상 조건에서 혈장과 조직에서 발견되는 DHA의 양은 낮습니다.[63]
SVCT는 체내 비타민 C 수송을 위한 주요 시스템입니다.[60] 비타민 C 합성기(예: 쥐) 및 비합성기(예: 인간) 세포 모두에서 혈장에서 발견되는 약 50 마이크로몰/리터(µ mol/L)보다 훨씬 높은 아스코르브산 농도를 유지합니다. 예를 들어, 뇌하수체와 부신의 아스코르브산 함량은 2,000 µmol/L를 초과할 수 있으며, 근육은 200-300 µmol/L입니다. 아스코르브산의 알려진 조효소 기능은 그렇게 높은 농도를 필요로 하지 않으므로 아직 알려지지 않은 다른 기능이 있을 수 있습니다. 이 모든 고농도 장기 함량의 결과는 혈장 비타민 C가 전신 상태를 나타내는 좋은 지표가 아니며, 비타민 C가 매우 낮은 식단을 섭취할 때 결핍 증상을 보이는 데 필요한 시간이 다를 수 있다는 것입니다.[64]
소변을 통한 배설은 아스코르브산과 대사산물입니다. 대사되지 않은 아스코르브산으로 배설되는 분획은 섭취량이 증가함에 따라 증가합니다. 또한, 아스코르브산은 (가역적으로) DHA로 전환되고, 그 화합물로부터 2,3-디케토굴로네이트 및 옥살레이트로 비가역적으로 전환됩니다. 이 세 가지 대사산물은 소변을 통해서도 배출됩니다. 식이 섭취가 적은 시간 동안 비타민 C는 배설되기보다는 신장에 의해 재흡수됩니다. 이 복구 과정은 결핍의 발생을 지연시킵니다. 인간은 기니피그보다 DHA를 다시 아스코르브산으로 전환하는 데 더 뛰어나기 때문에 비타민 C 결핍이 되는 데 훨씬 더 오랜 시간이 걸립니다.[8][62]
합성
대부분의 동물과 식물은 효소 주도의 일련의 단계를 통해 비타민 C를 합성할 수 있으며, 이 단계는 단당류를 비타민 C로 전환시킵니다. 효모는 l-아스코르브산을 만들지 않고 입체 이성질체인 에리트로브산을 만듭니다.[65] 식물에서 합성은 만노스 또는 갈락토오스를 아스코르브산으로 전환함으로써 이루어집니다.[66][67] 동물에서 출발 물질은 포도당입니다. 간에서 아스코르브산을 합성하는 일부 종(포유류 및 횃불새 포함)에서 포도당은 글리코겐으로부터 추출되며, 아스코르브산 합성은 글리코겐 분해 의존적 과정입니다.[68] 인간과 비타민C를 합성할 수 없는 동물에서 생합성의 마지막 단계를 촉매하는 효소 l-굴로놀락톤 산화효소(GULO)는 고도로 변이되고 비기능적입니다.[69][70][71][72]
동물합성
비타민 C를 합성할 수 있는 동물 종에서 유지되는 혈청 비타민 C 농도에 대한 정보가 있습니다. 여러 품종의 개를 대상으로 한 한 연구에서는 평균 35.9μmol/L을 보고했습니다.[73] 염소, 양, 소에 대한 보고서는 각각 100–110, 265–270 및 160–350 μmol/L의 범위를 보고했습니다.[74]
척추동물에서 아스코르브산의 생합성은 UDP-글루쿠론산의 형성에서 시작됩니다. UDP-글루쿠론산은 UDP-글루코스가 효소 UDP-글루코스 6-탈수소효소에 의해 촉매되는 두 번의 산화를 겪을 때 형성됩니다. UDP-포도당 6-탈수소효소는 보조인자 NAD를+ 전자 수용체로 사용합니다. transferase UDP-glucuronate pyrophosphorylase는 UMP를 제거하고 글루쿠로노키나아제는 보조인자 ADP와 함께 d-glucuronic acid로 이어지는 최종 인산염을 제거합니다. 이 화합물의 알데히드기는 글루쿠론산 환원효소와 보조인자 NADPH를 사용하여 1차 알코올로 환원되어 l-굴론산을 생성합니다. 이어서 C1의 카르보닐과 C4의 하이드록실기 사이에 가수분해효소 글루코노락토나아제를 이용한 락톤 형성이 뒤따릅니다. l-굴로노락톤은 산소와 반응하여 L-굴로노락톤 산화효소(인간 및 다른 하플로르히니 영장류에서 기능하지 않음; Unitary pseudogenes 참조)와 보조인자 FAD+에 의해 촉매됩니다. 이 반응은 2-옥소굴로노락톤(2-케토-굴로노락톤)을 생성하며, 이는 자발적으로 에놀화를 거쳐 아스코르브산을 형성합니다.[67][75][62] 파충류와 오래된 새들은 신장에서 아스코르브산을 만듭니다. 최근 조류와 대부분의 포유류가 간에서 아스코르브산을 만듭니다.[67]
비합성기
일부 포유류는 비타민 C를 합성하는 능력을 상실했는데, 이는 함께 두 개의 주요 영장류 아목인 하플로히니(Haplorhini) 중 하나를 구성하는 유인원과 찌르레기를 포함합니다. 이 그룹에는 인간이 포함됩니다. 다른 더 원시적인 영장류 (Strepsirrhini)는 비타민 C를 만드는 능력을 가지고 있습니다. 합성은 기니피그와 카피바라를 포함하는 설치류 과 Caviidae의 일부 종에서는 발생하지 않지만 쥐와 쥐를 포함한 다른 설치류에서는 발생합니다.[76]
합성은 대부분의 박쥐 종에서 일어나지 않지만,[77] 비타민 C 생산 능력을 유지(또는 회복)하는 육식성 박쥐 Rousettus leschenaultii와 식충성 박쥐 Hipposideros Armiger의 적어도 두 종이 있습니다.[78][79] 많은 종의 패서린 조류도 합성하지는 않지만 모두 합성하지는 않으며, 명확한 관련이 없는 것은 조류에서 여러 번 별도로 능력이 손실되었다고 제안되었습니다.[80] 특히 비타민C를 합성하는 능력이 상실됐다가 나중에 재취득된 것으로 추정되는 경우는 적어도 두 가지 경우입니다.[81] 현존하는 어류[82](테리오스트)의 약 96%에서 비타민 C 합성 능력도 상실되었습니다.[81]
체중 기준으로 킬로그램당 섭취하는 밀리그램의 경우, 합성하지 않은 유인원 종은 정부가 인간에게 권장하는 것보다 10배에서 20배 많은 양의 비타민을 섭취합니다.[83] 이러한 불일치는 인간 권장 식이 허용량이 너무 낮게 설정되었다는 논란의 일부 근거를 구성했습니다.[84] 그러나 유인원 소비는 유인원 요구 사항을 나타내지 않습니다. 머크의 수의학 매뉴얼에 따르면 비타민 C를 매일 3-6mg/kg 섭취하면 인간이 아닌 영장류의 괴혈병을 예방할 수 있습니다.[85] 비교하자면, 여러 국가에서 성인 인간의 권장 식이 섭취량은 1-2mg/kg 범위입니다.
동물 합성의 진화
아스코르브산은 콜라겐 합성에 사용되는 포유류의 일반적인 효소 보조인자일 뿐만 아니라 다수의 활성산소종(ROS)을 빠르게 제거할 수 있는 강력한 환원제입니다. 아스코르브산염이 이러한 중요한 기능을 가지고 있다는 것을 감안할 때, 이 분자를 합성하는 능력이 항상 보존되어 있지는 않았다는 것은 놀라운 일입니다. 사실, 유인원 영장류, 카비아 포르셀루스 (기니피그), 텔레오스트 물고기, 대부분의 박쥐, 그리고 일부 패서린 새들은 모두 독립적으로 신장이나 간에서 내부적으로 비타민 C를 합성하는 능력을 상실했습니다.[86][81] 아스코르브산 영양요구성에서 유전체 분석이 이루어진 모든 경우에서 변화의 기원은 위에서 설명한 아스코르브산 경로의 마지막 단계를 촉매하는 효소인 L-굴로노-γ-락톤 산화효소를 암호화하는 유전자의 기능 상실 돌연변이에서 기인하는 것으로 밝혀졌습니다. 비타민 C 합성 능력의 반복적인 상실에 대한 한 가지 설명은 그것이 유전적 표류의 결과라는 것입니다; 식단에 비타민 C가 풍부하다고 가정한다면, 자연적인 선택은 그것을 보존하는 작용을 하지 않을 것입니다.[88][89]
유인원의 경우, 비타민 C를 만드는 능력의 상실은 인류나 심지어 유인원의 출현보다 훨씬 이전의 진화 역사에서 발생했을 것으로 생각되는데, 이는 분명히 최초의 영장류가 출현한 직후에 발생했기 때문입니다. 그러나 초기 영장류가 두 개의 주요 아목인 하플로르히니(비타민 C를 만들 수 없음)와 비타민 C를 만들 수 있는 능력을 유지한 비-타르족 프로시미언의 자매 아목인 스트렙시르히니("젖은 코" 영장류)로 분열된 지 얼마 되지 않았습니다.[90] 분자 시계 연대 측정에 따르면, 이 두 개의 영장류 아목 가지는 약 6천 3백만 년에서 6천만 년 전에 갈라졌습니다.[91] 진화론적 관점에서 볼 때, 약 300만년에서 500만년 후(5천 8백만년 전), 불과 얼마 지나지 않아, 타르시에과(Tarsiidae)의 유일한 과가 남아있는 타르시에폼(Tarsiiformes)은 다른 일배체에서 분기되었습니다.[92][93] 타르시어는 또한 비타민 C를 만들 수 없기 때문에, 이것은 돌연변이가 이미 발생했다는 것을 의미하며, 따라서 이 두 표지자 지점 사이에서 발생했을 것입니다 (6,300만년에서 5,[90]800만년 전).
또한 아스코르브산염을 합성하는 능력의 상실은 영장류의 특징이기도 한 요산을 분해할 수 없는 것과 현저하게 유사하다는 것이 주목되었습니다. 요산과 아스코르브산염은 모두 강력한 환원제입니다. 이것은 고등 영장류에서 요산이 아스코르브산염의 일부 기능을 대체했다는 제안으로 이어졌습니다.[94]
식물합성

식물에는 아스코르브산으로 가는 다양한 생합성 경로가 있습니다. 대부분은 해당과정 및 기타 대사 경로의 생성물을 통해 진행됩니다. 예를 들어, 하나의 경로는 식물 세포벽 중합체를 활용합니다.[69] 주요 식물 아스코르브산 생합성 경로는 l-갈락토오스를 통한 것으로 보입니다. l-갈락토오스 탈수소효소는 락톤으로의 전반적인 산화와 락톤의 C4-하이드록실기로의 이성질화를 촉매하여 l-갈락토노-1,4-락톤을 생성합니다.[75] l-갈락토노-1,4-락톤은 미토콘드리아 플라보엔자임 l-갈락토놀락톤 탈수소효소와[95] 반응하여 아스코르브산을 생성합니다.[75] l-아스코르브산은 시금치의 l-갈락토오스 탈수소효소에 대해 부정적인 피드백을 가지고 있습니다.[96] 쌍자엽 식물의 배아에 의한 아스코르브산 유출은 철 환원의 잘 확립된 메커니즘이며 철 흡수에 필수적인 단계입니다.[a]
모든 식물은 아스코르브산을 합성합니다. 아스코르브산은 광합성, 식물 호르몬 합성에 관여하는 효소의 보조인자, 항산화제 및 기타 항산화제의 재생제로서 기능합니다.[98] 식물은 비타민 C를 합성하기 위해 여러 경로를 사용합니다. 주요 경로는 포도당, 과당 또는 만노스(모든 단순 당)에서 시작하여 l-갈락토오스, l-갈락토노락톤 및 아스코르브산으로 진행됩니다.[98][99] 이 생합성은 주간 리듬에 따라 조절됩니다.[99] 효소 발현은 한낮의 햇빛 강도가 높은 아스코르브산 농도를 요구할 때 생합성을 지원하기 위해 아침에 최고조에 달합니다.[99][100] 작은 경로는 식물의 특정 부분에 특이적일 수 있으며, 이는 척추동물 경로(GLO 효소 포함)와 동일하거나 이노시톨로 시작하여 l-갈락톤산에서 l-갈락토노락톤으로 아스코르브산으로 이동할 수 있습니다.[98]
산업합성
비타민 C는 포도당으로부터 크게 두 가지 경로를 통해 생산될 수 있습니다. 1930년대에 개발된 라이히슈타인 공정은 더 이상 사용되지 않았으며, 단일 발효 후 순수한 화학적 경로를 사용했습니다. 1960년대에 중국에서 처음 개발된 현대의 2단계 발효 과정은 이후의 화학 단계의 일부를 대체하기 위해 추가 발효를 사용합니다. 라이히슈타인 공정과 현대의 2단계 발효 공정은 모두 포도당을 출발 물질로 사용하여 소르비톨로 전환한 다음 발효를 이용하여 소르보오스로 전환합니다.[101] 그런 다음 2단계 발효 과정은 다른 발효 단계를 통해 소르보스를 2-케토-1-굴론산(KGA)으로 전환하여 추가적인 중간체를 피합니다. 두 과정 모두 포도당 시작점에서 약 60%의 비타민 C를 생성합니다.[102] 연구원들은 한 단계 발효를 위한 수단을 모색하고 있습니다.[103][104]
중국은 세계 비타민 C 시장의 약 70%를 생산하고 있습니다. 나머지는 유럽연합, 인도, 북미로 나누어져 있습니다. 세계 시장은 2024년에 14만 1천 톤을 넘어설 것으로 예상됩니다.[105] 미국 달러로 미터톤(1000kg)당 비용은 상하이에서 2,220달러, 함부르크에서 2,850달러, 미국에서 3,490달러였습니다.[106]
의료용

비타민 C는 비타민 C 결핍으로 인한 질병인 괴혈병을 치료하는 데 결정적인 역할을 합니다. 그 외에도 다양한 질병에 대한 예방 또는 치료로서 비타민 C의 역할이 논란이 되고 있으며, 리뷰는 종종 상반된 결과를 보고합니다. 전체 사망률에 대한 비타민 C 보충 효과는 보고되지 않았습니다.[107] 세계보건기구 필수 의약품 목록과 세계보건기구 모델 포럼에 등재되어 있습니다.[108] 2021년에는 미국에서 255번째로 많이 처방된 약으로 100만 건 이상의 처방을 받았습니다.[109]
괴혈병
괴혈병은 비타민 C의 결핍으로 인한 질병입니다. 이 비타민이 없으면 몸에서 만들어진 콜라겐이 너무 불안정해 제 기능을 하지 못하고 몸 안에 있는 다른 여러 효소들이 제대로 작동하지 못합니다. 초기 증상은 권태감과 무기력증으로 진행되어 호흡 곤란, 뼈 통증, 타박상에 취약합니다. 병이 진행되면서 피부 밑에 반점이 생기고 피가 나고 잇몸에서 피가 나는 것이 특징입니다. 피부 병변은 허벅지와 다리에 가장 풍부합니다. 병에 걸린 사람은 창백하고 우울하며 부분적으로 고정되어 있습니다. 진행성 괴혈병에서는 오래된 상처가 벌리고 화농하며 치아가 상실되고 경련을 일으키며 결국 사망할 수 있습니다. 건강한 콜라겐이 결함이 있는 콜라겐을 비타민C 보충으로 대체하기 때문에 질병이 꽤 늦게까지 손상은 되돌릴 수 있습니다.[6][43][110]
실험적으로 유도된 괴혈병에 대한 주목할 만한 인간 식이 연구는 영국에서 제2차 세계 대전 동안 양심적인 반대자들과 1960년대 후반에서 1980년대 아이오와 주 포로들에 대해 수행되었습니다. 교도소 연구의 남성들은 비타민 C가 없는 식단을 시작한 지 약 4주 후에 괴혈병의 첫 징후가 나타난 반면, 초기 영국 연구에서는 6~8개월이 필요했는데, 이는 아마도 스코르부틱 식단이 공급되기 전 6주 동안 70mg/day 보충제를 이 그룹에 미리 탑재했기 때문일 수 있습니다. 두 연구에서 남성들은 괴혈병 징후가 나타날 때까지 정확하게 측정하기에는 아스코르브산의 혈중 농도가 너무 낮았습니다. 이 두 연구는 하루에 10mg만 보충하면 괴혈병의 모든 명백한 증상을 완전히 되돌릴 수 있다고 보고했습니다.[111][112] 괴혈병의 치료는 비타민 C가 포함된 식품이나 식이보충제 또는 주사를 사용할 수 있습니다.[43][7]: 101
패혈증
패혈증에 걸린 사람들은 낮은 수준의 비타민 C를 포함하여 미세 영양소 결핍을 가질 수 있습니다.[113] 패혈증이나 심한 화상을 입은 사람들의 혈장 농도를 정상적으로 유지하기 위해서는 정맥 투여가 필요한 3.0 g/day의 섭취가 필요한 것으로 보입니다.[114][115] 패혈증 사망률은 정맥 비타민 C 투여로 감소합니다.[116][117]
감기

일반 감기의 비타민 C에 대한 연구는 예방, 기간, 중증도에 대한 효과로 나누어졌습니다. 정기적으로 복용하는 200 mg/day 이상의 경구 섭취는 감기 예방에 효과적이지 않았습니다. 최소 1000 mg/day를 사용한 시험으로 분석을 제한해도 예방 효과가 없었습니다. 그러나 비타민 C 보충제를 정기적으로 복용하면 성인의 평균 질병 기간이 8%, 어린이의 평균 질병 기간이 14% 감소했으며 감기의 중증도도 감소했습니다.[118] 정기적으로 복용하는 비타민C는 중증 증상의 지속 기간은 줄었지만 경증 증상의 지속 기간에는 영향을 미치지 않았습니다.[119] 사람들이 감기의 시작을 느끼기 시작하지 않는 한 비타민이 시작되지 않았다는 것을 의미하는 치료적 사용은 질병의 지속 기간이나 심각성에 영향을 미치지 않았습니다.[118]
비타민 C는 면역세포에 고농도로 쉽게 분포되어 자연살해세포의 활동을 촉진하고 림프구의 증식을 촉진하며 감염 시 빠르게 고갈되어 면역계 기능에 중요한 역할을 한다는 것을 시사하는 효과입니다.[120] 유럽 식품 안전청은 비타민 C의 식이 섭취와 성인과 3세 미만 어린이의 정상적인 면역 체계 기능 사이에 인과 관계가 있다고 결론 내렸습니다.[121][122]
코로나19
2020년 3월부터 7월까지, 비타민 C는 COVID-19의 예방 및/또는 치료를 위한 주장에 대해 다른 어떤 성분보다 많은 미국 FDA 경고 서한의 대상이 되었습니다.[123] 2021년 4월, 미국 국립보건원(NIH) COVID-19 치료 지침은 "COVID-19의 예방 또는 치료를 위한 비타민 C의 사용에 대해 찬성하거나 반대할 데이터가 부족하다"고 밝혔습니다.[124] 2022년 12월에 게시된 업데이트에서 NIH의 입장은 변경되지 않았습니다.
- 코로나19 치료 지침 패널(패널)이 입원하지 않은 환자의 코로나19 치료를 위한 비타민C 사용에 대해 찬성 또는 반대를 권고할 근거가 부족합니다.
- 패널이 입원 환자의 COVID-19 치료를 위한 비타민 C 사용에 대한 찬성 또는 반대를 권고하기에는 증거가 부족합니다.[125]
중증 COVID-19로 입원한 사람들의 경우 비타민 C를 투여하지 않는 것에 비해 비타민 C를 투여하면 모든 원인에 의한 병원 내 사망 위험이 크게 감소한다는 보고가 있습니다. 두 그룹 간에 환기 발생률, 입원 기간 또는 중환자실 체류 기간에는 유의한 차이가 없었습니다. 이러한 메타 분석에 포함된 대부분의 시험은 비타민의 정맥 투여를 사용했습니다.[126][127][128] 급성 신장 손상은 비타민 C 치료를 받은 사람들이 더 낮았습니다. 비타민으로 인한 다른 이상반응의 빈도에는 차이가 없었습니다.[128] 결론은 최신 지침과 권고 사항을 발표하기 전에 사망률 이점을 확인하기 위해서는 더 많은 대규모 연구가 필요하다는 것이었습니다.[126][127][128]
암
비타민C 보충이 건강한 사람이나 흡연이나 석면 노출로 인한 고위험군의 폐암 위험을 감소시킨다는 증거는 없습니다.[129] 전립선암 위험에 영향을 미치지 않으며,[130] 비타민C 보충이 대장암이나[131] 유방암 위험에 영향을 미친다는 좋은 증거가 없습니다.[132]
병용요법으로 고용량 정맥 비타민C를 투여하면 종양 재발, 전이, 내화학성을 담당하는 암 줄기세포가 억제되는지 조사하는 연구가 있습니다.[133][134]
심혈관질환
순환하는 비타민 C 수치나 식이 비타민 C 수치가 높고 뇌졸중 위험이 낮은 것과 연관성이 있을 수 [135]있지만 비타민 C 보충이 심혈관 질환의 위험을 감소시킨다는 증거는 없습니다.[136] 하루에 500mg 이상을 복용하면 비타민C가 내피 기능 장애에 긍정적인 영향을 줍니다. (내피는 혈관의 내부 표면을 따라 늘어선 세포층입니다.)[137]
혈압
혈청 비타민 C는 정상혈압에 비해 고혈압 환자에서 15.13μmol/L 더 낮은 것으로 보고되었습니다. 비타민은 수축기 혈압(SBP)과 이완기 혈압(DBP) 모두와 역으로 연관되어 있었습니다.[138] 비타민의 경구 보충은 고혈압이 있는 사람들의 SBP를 매우 완만하지만 통계적으로 유의하게 감소시켰습니다.[139][140] 제안된 설명은 비타민 C가 강력한 혈관 확장제인 산화질소의 생성을 촉진하는 내피 산화질소 합성효소 보조인자인 테트라하이드로바이옵테린의 세포 내 농도를 증가시킨다는 것입니다. 비타민 C 보충은 또한 산화질소 합성효소 억제제 NG-모노메틸-L-아르기닌 1을 역전시킬 수 있으며, 비타민 C가 혈관 확장제인 산화질소의 생물학적 활성을 직접적으로 향상시킨다는 증거도 있습니다.[139]
제2형 당뇨병
상반된 평가가 있습니다. 첫째, 제2형 당뇨병 관리를 위해 비타민 C 보충을 권장할 수 없습니다.[141] 그러나 또 다른 사람은 고용량의 비타민 C를 보충하면 혈당, 인슐린 및 헤모글로빈 A1c를 감소시킬 수 있다고 보고했습니다.[142]
철결핍
철분 결핍성 빈혈의 원인 중 하나는 철분의 흡수 감소입니다. 철분 흡수는 철분을 함유한 음식이나 보충제와 함께 비타민 C를 섭취함으로써 향상될 수 있습니다. 비타민 C는 철분을 환원된 제1철 상태로 유지하는 데 도움이 되며, 이는 용해도가 더 높고 흡수가 더 쉽습니다.[143]
피부 노화 징후 예방을 위한 국소 도포
인간의 피부에는 비타민 C가 함유되어 콜라겐 합성을 지원하고 콜라겐 분해를 감소시키며 광암 발생을 포함한 UV 유도 광노화에 대한 항산화 보호를 돕습니다. 이 지식은 종종 얼굴 피부 노화, 기미(진한 색소 반점) 및 주름을 예방하거나 치료하기 위한 국소 "세럼" 성분으로서 비타민 C의 마케팅에 대한 근거로 사용됩니다. 이 메커니즘은 항산화제로 기능하여 햇빛 노출, 대기 오염 물질 또는 정상적인 대사 과정으로부터 활성 라디칼을 중화한다는 것입니다.[144] 경구 섭취와 달리 국소 치료의 효능은 잘 알려져 있지 않습니다.[145][146] 임상시험 문헌은 건강 주장을 뒷받침하기에 부족하다는 특징이 있는데, 한 가지 이유는 "모든 연구가 비타민 C를 다른 성분이나 치료 메커니즘과 결합하여 사용하여 비타민 C의 효능에 대한 특정 결론을 복잡하게 만들었다"는 것입니다.[147] 더 많은 연구가 필요합니다.[148]
인지장애와 알츠하이머병
정상적인 인지능력을 가진 사람들에 비해 인지장애와 알츠하이머병을 가진 사람들에게서 낮은 혈장 비타민 C 농도가 보고되었습니다.[149][150][151]
눈 건강
비타민 C의 높은 식이 섭취는 나이와 관련된 백내장의 위험을 낮추는 것과 관련이 있었습니다.[152][153] 비타민C 보충은 나이와 관련된 황반변성을 예방하지 못했습니다.[154]
치주질환
낮은 섭취량과 낮은 혈청 농도는 치주 질환의 더 큰 진행과 관련이 있었습니다.[155][156]
부작용
요구량을 초과하는 식이보충제로서의 경구섭취량은 흡수가 잘 되지 않고,[4] 혈액의 과잉이 소변으로 빠르게 배출되어 낮은 급성독성을 나타냅니다.[6] 2~3g 이상을 경구 섭취하면 메스꺼움, 복부 경련 및 설사를 유발할 수 있습니다. 이러한 효과는 흡수되지 않은 비타민 C가 장을 통과하는 삼투 효과에 기인합니다.[7]: 156 이론적으로 비타민C를 많이 섭취하면 철분 흡수가 과도하게 될 수 있습니다. 건강한 피험자의 보충에 대한 리뷰 요약은 이 문제를 보고하지 않았지만 유전성 혈색소증이 있는 개인이 부정적인 영향을 받을 수 있는 가능성을 테스트하지 않은 상태로 남겼습니다.[7]: 158
주류 의료계 사이에는 비타민C가 신장 결석 위험을 높인다는 오랜 믿음이 있습니다.[157] "아스코르브산 과다 섭취와 관련된 신장 결석 형성에 대한 보고는 신장 질환이 있는 개인에 국한됩니다."[7]: 156–157 리뷰에 따르면 "역학 연구의 데이터는 분명히 건강한 개인의 과도한 아스코르브산 섭취와 신장 결석 형성 사이의 연관성을 뒷받침하지 않는다"고 합니다.[158] 그러나 수년에 걸친 대규모 실험에서 비타민 C 보충제를 정기적으로 섭취한 남성의 신장 결석이 거의 두 배 증가했다고 보고했습니다.[159]
패혈증,[114] 중증 COVID-19[126][127] 및 암 치료를 위한 정맥 비타민 C의 이점에 대한 광범위한 연구가 있습니다.[160] 리뷰에는 하루에 24g의 높은 용량을 사용한 시험이 나열됩니다.[126] 가능한 부작용에 대한 우려는 고용량 비타민 C를 정맥 주사하면 비타민 C의 상생리학적 수준이 증가한 후 산화 분해되어 디하이드로아스코르브산으로 분해되어 옥살산 신장 결석 및 옥살산 신장병증의 위험이 증가한다는 것입니다. 신장이 과도한 비타민 C를 효율적으로 배출하기 때문에 신장 장애가 있는 사람의 경우 위험이 더 높을 수 있습니다. 둘째, 포도당-6-인산 탈수소효소 결핍 환자에서는 급성 용혈을 유발할 수 있으므로 고용량 비타민 C 치료를 피해야 합니다. 셋째, 비타민 C와 포도당이 유사한 분자 구조를 가지고 있어 혈당 측정기의 혈당 측정 정확도를 방해할 수 있으며, 이는 잘못된 고혈당 수치를 초래할 수 있습니다. 이러한 모든 우려에도 불구하고 패혈증, 패혈성 쇼크, COVID-19 및 기타 급성 질환으로 집중 치료 중인 환자에 대한 메타 분석에서는 단기 고용량 비타민 C 치료를 받는 환자에 대한 새로운 발병 신장 결석, 급성 신장 손상 또는 신장 대체 요법의 요구 사항이 증가하지 않았다고 보고했습니다. 이것은 정맥 비타민 C가 이러한 단기적인 적용 하에서 안전하다는 것을 시사합니다.[161][162][163]
역사
스커비는 히포크라테스에게 알려졌고, 그의 프롤레티토룸 2권과 그의 리베르 드 인테니스 애정행각에서 기술되었으며, 제임스 린드가 인용했습니다.[164] 괴혈병의 증상은 장로 플리니에 의해서도 설명되었습니다. (i) Pliny. "49". Naturalis historiae. Vol. 3.Pliny. "49". Naturalis historiae. Vol. 3.그리고 (ii)[165] 스트라보, Geographicorum, 16권, 1881년 국제 외과 백과사전에서 인용.
바다에서의 괴로움

1497년 바스코 다 가마 원정에서 감귤류의 치료 효과가 알려졌습니다.[166] 1500년대에 포르투갈 선원들은 심어진 채소밭과 야생에서 자란 과일 나무를 이용하기 위해 세인트 헬레나 섬에 들어갔습니다.[167] 당국은 때때로 긴 해상 항해 동안 괴혈병을 예방하기 위해 식물성 식품을 권장했습니다. 영국 동인도 회사의 첫 외과의사인 존 우달(John Woodall)은 1617년 그의 책 외과의사의 메이트(The Surgeon's Mate)에서 레몬 주스의 예방 및 치료법 사용을 권장했습니다.[168] 1734년, 네덜란드 작가 Johann Bachstrom는 "고통은 오로지 신선한 야채 음식과 채소에 대한 완전한 금욕 때문입니다"라고 단호한 의견을 제시했습니다.[169][170] Scurvy는 긴 해상 항해 동안 오랫동안 선원들의 주요 살해범이었습니다.[171] 조나단 램(Jonathan Lamb)에 따르면, "1499년 바스코 다 가마(Vasco da Gama)는 170명의 승무원 중 116명을 잃었고, 1520년 마젤란(Magellan)은 230명 중 208명을 잃었습니다.이 모든 것은 주로 괴로움에 관한 것입니다."[172]

이 질병의 원인에 대한 과학적 근거를 제시하기 위한 첫 번째 시도는 영국 해군의 한 배의 외과 의사인 제임스 린드에 의한 것이었습니다. 1747년 5월, 바다에 있는 동안, 린드는 몇몇 승무원들에게 일반적인 배급량 외에 오렌지 두 개와 레몬 한 개를 매일 제공했고, 다른 승무원들은 세계 최초로 통제된 실험 중 하나에서 사이다, 식초, 황산 또는 바닷물을 정상적인 배급량과 함께 계속했습니다.[173] 결과는 감귤류가 질병을 예방한다는 것을 보여주었습니다. 린드는 1753년에 그의 저서인 괴혈병에 관한 논문을 출판했습니다.[174]
신선한 과일은 배에 보관하는 데 비용이 많이 드는 반면, 주스로 끓이면 쉽게 보관할 수 있지만 비타민을 파괴합니다(특히 구리 주전자에 끓이면).[41] 영국 해군이 바다에서 레몬 주스를 표준 이슈로 채택하기 전인 1796년입니다. 1845년에는 서인도 제도의 선박들에게 대신 라임 주스가 제공되었고, 1860년에는 영국 해군 전역에서 라임 주스가 사용되어 미국에서 영국인들에게 "라임"이라는 별명을 사용하게 되었습니다.[173] 제임스 쿡 선장은 이전에 선원들을 고통에 빠뜨리지 않고 1772-75년 태평양 항해에 참여시킴으로써 "Sour kroout"을 배에 태우는 것의 장점을 보여주었습니다.[175] 그의 방법에 대한 보고서로 영국 왕립학회는 1776년 그에게 코플리 메달을 수여했습니다.[176]
18세기와 19세기에 괴혈병을 예방하는 것으로 알려진 음식에 항코르부틱이라는 이름이 사용되었습니다. 이 음식에는 레몬, 라임, 오렌지, 사우어크라우트, 양배추, 맥아, 휴대용 수프가 포함되었습니다.[177] 1928년, 캐나다의 북극 인류학자 빌할무르 스테판슨(Vilhjalmur Stefansson)은 이누이트 족이 주로 날고기로 된 식단으로 괴로운 것을 피한다는 것을 보여주었습니다. 캐나다 북부의 유콘 퍼스트 네이션스, 덴, 이누이트, 메티스의 전통적인 음식 식단에 대한 나중의 연구는 그들의 비타민 C의 일일 섭취량이 평균 52에서 62 mg/day 사이임을 보여주었습니다.[178]
디스커버리
1912년에 비타민 C가 발견되었고 1928년에 분리되어 1933년에 합성되어 최초로 합성된 비타민입니다.[179] 그 직후 타데우스 라이히슈타인은 현재 라이히슈타인 공정이라고 불리는 방법으로 비타민을 대량으로 합성하는 데 성공했습니다.[180] 이것은 비타민 C의 저렴한 대량 생산을 가능하게 했습니다. 1934년 호프만-라로슈는 라이히슈타인 공정 특허를 사들여 레독슨이라는 브랜드명으로 합성비타민C를 상표 등록하고 식이보충제로 시판하기 시작했습니다.[181][182]
1907년 노르웨이의 의사인 악셀 홀스트(Axel Holst)와 테오도르 프롤리히(Theodor Frølich)가 항피질 인자를 확인하는 데 도움이 되는 실험용 동물 모델을 발견했는데, 그는 선상 베리베리를 연구할 때 기니피그에게 곡물과 밀가루를 먹였고 베리베리 대신 괴혈병이 나타나자 깜짝 놀랐습니다. 그 당시에는 알려지지 않았지만, 쥐와 쥐는 자체적으로 비타민 C를 만들지 않았습니다.[183] 1912년 폴란드의 생화학자 카시미르 펑크는 비타민의 개념을 개발했습니다. 이 중 하나가 바로 반코르보틱 인자라고 생각했습니다. 1928년에 이것은 "수용성 C"로 불렸지만 화학적 구조는 결정되지 않았습니다.[184]

1928년부터 1932년까지 Albert Sent-Görgyi와 Joseph L. Svirbley의 헝가리 팀과 Charles Glen King의 미국 팀은 반코르보틱 요인을 확인했습니다. Szent-Györgyi는 동물의 부신에서 헥수론산을 분리하여 항코르보틱 인자로 의심했습니다.[186] 1931년 말, Szent-Györgyi는 Svirbelley에게 그의 부신 유래 헥수론산이 항코르부틱 인자일 수도 있다는 제안과 함께 마지막으로 그의 부신 유래 헥수론산을 주었습니다. 1932년 봄까지 킹의 연구소는 이를 증명했지만, 그 결과를 Szent-Györgyi에게 알리지 않고 발표했습니다. 이로 인해 우선순위에 대한 격렬한 논쟁이 벌어졌습니다.[186] 1933년 월터 노먼 하워스(Walter Norman Haworth)는 화학적으로 비타민을 l-헥수론산(l-hexuronic acid)으로 밝혀냈고, 1933년 합성을 통해 이를 입증했습니다.[187][188][189][190] Haworth와 Szent-Görgyi는 괴혈병에 대한 활성을 기리기 위해 L-헥수론산을 a-스코르브산, 그리고 화학적으로 l-아스코르브산으로 명명할 것을 제안했습니다.[190][179] 이 용어의 어원은 라틴어 "a-"에서 유래한 것으로, -scorbic은 고대 노르드어 스커부그르, 프랑스어 스커부트, 네덜란드어 스커부익, 저독일어 샤르보크와 같은 중세 라틴어 스코르부티쿠스(skorbuticus, 괴혈병과 관련됨)에서 유래했습니다.[191] 이 발견으로 인하여, Szent-Györgyi는 1937년 노벨 의학상을 수상하였고,[185] Haworth는 그 해 노벨 화학상을 공동 수상하였습니다.[192]
1957년 J. J. Burns는 일부 포유류가 간에서 비타민 C를 합성하는 4가지 효소의 마지막 사슬인 l-gulonolactone 산화효소를 생성하지 않기 때문에 괴혈병에 걸리기 쉽다는 것을 보여주었습니다.[193][194] 미국의 생화학자 어윈 스톤은 식품 보존성을 위해 비타민 C를 처음으로 이용했습니다. 그는 이후 인간이 l-gulonolactone 산화효소 코딩 유전자의 돌연변이 형태를 가지고 있다는 아이디어를 개발했습니다.[195] 스톤은 인간이 건강을 최적화하기 위해서는 하루 권장 섭취량보다 훨씬 많은 양의 비타민 C를 섭취해야 한다는 이론을 리누스 파울링에게 소개했습니다.[196]
2008년, 연구원들은 인간과 다른 영장류들에게서 적혈구가 산화된 l-디하이드로아스코르브산(DHA)을 다시 몸에 재사용하기 위해 아스코르브산으로 재활용함으로써 몸에 존재하는 비타민 C를 더 효율적으로 사용할 수 있는 메커니즘을 발전시켜 왔다는 것을 발견했습니다. 이 메커니즘은 자체 비타민 C를 합성하는 포유류에는 존재하지 않는 것으로 밝혀졌습니다.[197]
대용량 요법의 역사
비타민 C 메가도스는 비타민 C를 합성할 수 있는 포유류의 간에서 생산되는 양과 비슷하거나 더 많은 양의 비타민 C를 섭취하거나 주입하는 것을 설명하는 용어입니다. 실제 용어는 아니지만 이에 대한 주장은 1970년 리누스 파울링의 논문에서 설명되었습니다. 간단히 말해서, 그의 입장은 최적의 건강을 위해 인간이 비타민 C를 합성할 수 없는 것을 보상하기 위해 하루에 적어도 2,300mg을 섭취해야 한다는 것이었습니다. 이 권장 사항은 또한 인간과 거의 비슷한 동물인 고릴라의 소비 범위에 포함되었습니다.[84] 높은 섭취량에 대한 두 번째 주장은 일단 1,250 밀리그램을 초과하면 리터당 약 190~200 마이크로몰(µ mol/L)로 정체될 때까지 섭취량이 증가함에 따라 혈청 아스코르브산 농도가 증가한다는 것입니다. 언급한 바와 같이, 정부 권장 사항은 40~110 mg/day 범위이고 정상 혈장은 약 50 µ mol/L이므로, '정상'은 경구 섭취가 제안된 메가도스 범위에 있을 때 달성할 수 있는 것의 약 25%입니다.
Pauling은 1970년에 일반 감기의 예방과 치료로서 고용량 비타민 C의 개념을 대중화했습니다. 몇 년 후 그는 비타민 C가 심혈관 질환을 예방하고 처음에는 정맥으로 투여한 후 경구로 10g/day를 투여하면 말기 암을 치료할 수 있다고 제안했습니다.[199] 아스코르브산을 사용한 메가 도즈는 다른 챔피언들을 보유하고 있는데, 그들 중에는 화학자 어윈 스톤과[196] 논란의 여지가 있는 마티아스 라스와 패트릭 홀포드가 있는데, 이들은 모두 암과 HIV 감염을 치료하기 위해 근거 없는 치료 주장을 한 것으로 기소되었습니다.[200][201] 많은 양의 정맥 주사 아스코르브산이 말기 암을 치료하거나 화학 요법의 독성을 개선하는 데 사용될 수 있다는 생각은 폴링의 중요한 논문이 나온 지 약 40년이 지난 지금도 여전히 입증되지 않은 것으로 간주되며 여전히 양질의 연구가 필요합니다.[202][203][160]
메모들
참고문헌
- ^ "Ascorbic acid injection 500mg/5ml". (emc). July 15, 2015. Archived from the original on October 14, 2020. Retrieved October 12, 2020.
- ^ "Ascorbic acid 100mg tablets". (emc). October 29, 2018. Archived from the original on September 21, 2020. Retrieved October 12, 2020.
- ^ "Ascor- ascorbic acid injection". DailyMed. October 2, 2020. Archived from the original on October 29, 2020. Retrieved October 12, 2020.
- ^ a b c "Vitamin C: Fact sheet for health professionals". Office of Dietary Supplements, US National Institutes of Health. February 11, 2016. Archived from the original on July 30, 2017.
- ^ "Vitamin C". Chem Spider. Royal Society of Chemistry. Archived from the original on July 24, 2020. Retrieved July 25, 2020.
- ^ a b c d e "Vitamin C". Linus Pauling Institute. Micronutrient Information Center, Linus Pauling Institute, Oregon State University, Corvallis, OR. July 1, 2018. Archived from the original on July 12, 2019. Retrieved June 19, 2019.
- ^ a b c d e f g h i j k l m n o p Institute of Medicine (US) Panel on Dietary Antioxidants Related Compounds (2000). "Vitamin C". Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids. Washington, DC: The National Academies Press. pp. 95–185. doi:10.17226/9810. ISBN 978-0-309-06935-9. PMID 25077263. Archived from the original on September 2, 2017. Retrieved September 1, 2017.
- ^ a b c d e f g Marriott MP, Birt DF, Stallings VA, Yates AA, eds. (2020). "Vitamin C". Present Knowledge in Nutrition, Eleventh Edition. London, United Kingdom: Academic Press (Elsevier). pp. 155–70. ISBN 978-0-323-66162-1.
- ^ "Testing foods for vitamin C (ascorbic acid)" (PDF). British Nutrition Foundation. 2004. Archived (PDF) from the original on November 23, 2015.
- ^ "Measuring the vitamin C content of foods and fruit juices". Nuffield Foundation. November 24, 2011. Archived from the original on July 21, 2015.
- ^ a b Schleicher RL, Carroll MD, Ford ES, et al. (November 2009). "Serum vitamin C and the prevalence of vitamin C deficiency in the United States: 2003-2004 National Health and Nutrition Examination Survey (NHANES)". The American Journal of Clinical Nutrition. 90 (5): 1252–63. doi:10.3945/ajcn.2008.27016. PMID 19675106.
- ^ Narayanan S, Kumar SS, Manguvo A, et al. (June 2021). "Current estimates of serum vitamin C and vitamin C deficiency in the United States". Curr Dev Nutr. 7 (5): 1067. doi:10.1093/cdn/nzab053_060. PMC 8180804.
- ^ Rowe S, Carr AC (July 2020). "Global vitamin C status and prevalence of deficiency: A cause for concern?". Nutrients. 12 (7): 2008. doi:10.3390/nu12072008. PMC 7400810. PMID 32640674.
- ^ Emadi-Konjin P, Verjee Z, Levin AV, et al. (May 2005). "Measurement of intracellular vitamin C levels in human lymphocytes by reverse phase high performance liquid chromatography (HPLC)". Clinical Biochemistry. 38 (5): 450–6. doi:10.1016/j.clinbiochem.2005.01.018. PMID 15820776.
- ^ a b "Dietary guidelines for Indians" (PDF). National Institute of Nutrition, India. 2011. Archived from the original (PDF) on December 22, 2018. Retrieved February 10, 2019.
- ^ World Health Organization (2005). "Chapter 7: Vitamin C". Vitamin and mineral requirements in human nutrition (2nd ed.). Geneva: World Health Organization. hdl:10665/42716. ISBN 978-92-4-154612-6.
- ^ "Commission Directive 2008/100/EC of 28 October 2008 amending Council Directive 90/496/EEC on nutrition labeling for foodstuffs as regards recommended daily allowances, energy conversion factors and definitions". The Commission of the European Communities. October 29, 2008. Archived from the original on October 2, 2016.
- ^ "Vitamin C". Natural Health Product Monograph. Health Canada. Archived from the original on April 3, 2013.
- ^ a b "Overview of dietary reference intakes for Japanese" (PDF). Ministry of Health, Labor and Welfare (Japan). 2015. Archived (PDF) from the original on October 21, 2022. Retrieved August 19, 2021.
- ^ a b "Overview on dietary reference values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies" (PDF). 2017. Archived (PDF) from the original on August 28, 2017.
- ^ Luo J, Shen L, Zheng D (2014). "Association between vitamin C intake and lung cancer: a dose-response meta-analysis". Scientific Reports. 4: 6161. Bibcode:2014NatSR...4E6161L. doi:10.1038/srep06161. PMC 5381428. PMID 25145261.
- ^ "TABLE 1: Nutrient intakes from food and beverages" (PDF). National Health and Nutrition Examination Survey: What We Eat in America, DHHS-USDA Dietary Survey Integration. Centers for Disease Control and Prevention, U.S. Department of Health & Human Services. Archived from the original (PDF) on February 24, 2017.
- ^ "TABLE 37: Nutrient intakes from dietary supplements" (PDF). National Health and Nutrition Examination Survey: What We Eat in America, DHHS-USDA Dietary Survey Integration. Centers for Disease Control and Prevention, U.S. Department of Health & Human Services. Archived from the original (PDF) on October 6, 2017.
- ^ "Tolerable upper intake levels for vitamins and minerals" (PDF). European Food Safety Authority. 2006. Archived (PDF) from the original on March 16, 2016.
- ^ "Federal Register May 27, 2016 food labeling: Revision of the nutrition and supplement facts labels. FR page 33982" (PDF). Archived (PDF) from the original on August 8, 2016.
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Archived from the original on April 7, 2020. Retrieved May 16, 2020.
- ^ 규정 (EU) 제1169/2011호 유럽 의회 및 이사회 보관, 2017년 7월 26일 유럽 연합의 Wayback Machine Official Journal of the European. 304/61 페이지 (2009).
- ^ a b Duarte A, Caixeirinho D, Miguel G, et al. (2010). "Vitamin C content of citrus from conventional versus organic farming systems". Acta Horticulturae. 868 (868): 389–94. doi:10.17660/ActaHortic.2010.868.52. hdl:10400.1/1158. Archived from the original on October 1, 2018. Retrieved May 5, 2018.
- ^ "NDL/FNIC food composition database home page". USDA Nutrient Data Laboratory, the Food and Nutrition Information Center and Information Systems Division of the National Agricultural Library. Archived from the original on January 15, 2023. Retrieved November 30, 2014.
- ^ a b "Natural food-fruit vitamin C content". The Natural Food Hub. Archived from the original on March 7, 2007. Retrieved March 7, 2007.
- ^ a b c "USDA national nutrient database for standard reference legacy: vitamin C" (PDF). U.S. Department of Agriculture, Agricultural Research Service. 2018. Archived (PDF) from the original on November 18, 2021. Retrieved September 27, 2020.
- ^ Brand JC, Rae C, McDonnell J, et al. (1987). "The nutritional composition of Australian aboriginal bushfoods. I". Food Technology in Australia. 35 (6): 293–6.
- ^ Justi KC, Visentainer JV, Evelázio de Souza N, et al. (December 2000). "Nutritional composition and vitamin C stability in stored camu-camu (Myrciaria dubia) pulp". Archivos Latinoamericanos de Nutricion. 50 (4): 405–8. PMID 11464674.
- ^ Vendramini AL, Trugo LC (2000). "Chemical composition of acerola fruit (Malpighia punicifolia L.) at three stages of maturity". Food Chemistry. 71 (2): 195–8. doi:10.1016/S0308-8146(00)00152-7.
- ^ Begum RM (2008). A textbook of foods, nutrition & dietetics. Sterling Publishers Pvt. Ltd. p. 72. ISBN 978-81-207-3714-3.
- ^ Sinha N, Sidhu J, Barta J, et al. (2012). Handbook of fruits and fruit processing. John Wiley & Sons. ISBN 978-1-118-35263-2.
- ^ Gutzeit D, Baleanu G, Winterhalter P, et al. (2008). "Vitamin C content in sea buckthorn berries (Hippophaë rhamnoides L. ssp . rhamnoides) and related products: A kinetic study on storage stability and the determination of processing effects". J Food Sci. 73 (9): C615–C20. doi:10.1111/j.1750-3841.2008.00957.x. PMID 19021790.
- ^ Clark S (January 8, 2007). "Comparing milk: human, cow, goat & commercial infant formula". Washington State University. Archived from the original on January 29, 2007. Retrieved February 28, 2007.
- ^ Roig MG, Rivera ZS, Kennedy JF (May 1995). "A model study on rate of degradation of L-ascorbic acid during processing using home-produced juice concentrates". International Journal of Food Sciences and Nutrition. 46 (2): 107–15. doi:10.3109/09637489509012538. PMID 7621082.
- ^ Allen MA, Burgess SG (1950). "The losses of ascorbic acid during the large-scale cooking of green vegetables by different methods". The British Journal of Nutrition. 4 (2–3): 95–100. doi:10.1079/BJN19500024. PMID 14801407.
- ^ a b "Safety (MSDS) data for ascorbic acid". Oxford University. October 9, 2005. Archived from the original on February 9, 2007. Retrieved February 21, 2007.
- ^ a b c "Introduction". Vitamin C fortification of food aid commodities: final report. National Academies Press (US). 1997. Archived from the original on January 21, 2024. Retrieved January 3, 2024.
- ^ a b c d "Ascorbic acid (Monograph)". The American Society of Health-System Pharmacists. Archived from the original on December 30, 2016. Retrieved December 8, 2016.
- ^ Davis JL, Paris HL, Beals JW, et al. (2016). "Liposomal-encapsulated ascorbic acid: influence on vitamin C bioavailability and capacity to protect against ischemia-reperfusion injury". Nutrition and Metabolic Insights. 9: 25–30. doi:10.4137/NMI.S39764. PMC 4915787. PMID 27375360.
- ^ "Why fortify?". Food Fortification Initiative. December 2023. Archived from the original on March 8, 2023. Retrieved January 3, 2024.
- ^ a b "Map: Count of nutrients in fortification standards". Global Fortification Data Exchange. Archived from the original on April 11, 2019. Retrieved January 3, 2024.
- ^ "USAID's Bureau for Humanitarian Assistance website". November 21, 2023.
- ^ Washburn C, Jensen C (2017). "Pretreatments to prevent darkening of fruits prior to canning or dehydrating". Utah State University. Archived from the original on December 15, 2020. Retrieved January 26, 2020.
- ^ "Ingredients". The Federation of Bakers. Archived from the original on February 26, 2021. Retrieved April 3, 2021.
- ^ "Frequently asked questions why food additives". Food Additives and Ingredients Association UK & Ireland- Making life taste better. Archived from the original on June 1, 2019. Retrieved October 27, 2010.
- ^ a b c d e 영국 식품 표준 기관:
- ^ a b c 미국 식품의약국:"Listing of food additives status part I". Food and Drug Administration. Archived from the original on January 17, 2012. Retrieved October 27, 2011.
- ^ a b c d 캐나다 보건국
- ^ a b c d e 호주 뉴질랜드 식품 표준 코드"Standard 1.2.4 – labeling of ingredients". September 8, 2011. Archived from the original on September 2, 2013. Retrieved October 27, 2011.
- ^ "Listing of food additives status part II". US Food and Drug Administration. Archived from the original on November 8, 2011. Retrieved October 27, 2011.
- ^ Böttger F, Vallés-Martí A, Cahn L, et al. (October 2021). "High-dose intravenous vitamin C, a promising multi-targeting agent in the treatment of cancer". J Exp Clin Cancer Res. 40 (1): 343. doi:10.1186/s13046-021-02134-y. PMC 8557029. PMID 34717701.
- ^ Park S, Ahn S, Shin Y, et al. (2018). "Vitamin C in cancer: a metabolomics perspective". Front Physiol. 9: 762. doi:10.3389/fphys.2018.00762. PMC 6018397. PMID 29971019.
- ^ Sideri O, Tsaousis KT, Li HJ, et al. (2019). "The potential role of nutrition on lens pathology: a systematic review and meta-analysis". Surv Ophthalmol. 64 (5): 668–78. doi:10.1016/j.survophthal.2019.03.003. PMID 30878580. S2CID 81981938.
- ^ Lykkesfeldt J, Tveden-Nyborg P (October 2019). "The pharmacokinetics of vitamin C". Nutrients. 11 (10): 2412. doi:10.3390/nu11102412. PMC 6835439. PMID 31601028.
- ^ a b Savini I, Rossi A, Pierro C, et al. (April 2008). "SVCT1 and SVCT2: key proteins for vitamin C uptake". Amino Acids. 34 (3): 347–55. doi:10.1007/s00726-007-0555-7. PMID 17541511. S2CID 312905.
- ^ Rumsey SC, Kwon O, Xu GW, et al. (July 1997). "Glucose transporter isoforms GLUT1 and GLUT3 transport dehydroascorbic acid". The Journal of Biological Chemistry. 272 (30): 18982–9. doi:10.1074/jbc.272.30.18982. PMID 9228080.
- ^ a b c Linster CL, Van Schaftingen E (January 2007). "Vitamin C. Biosynthesis, recycling and degradation in mammals". The FEBS Journal. 274 (1): 1–22. doi:10.1111/j.1742-4658.2006.05607.x. PMID 17222174. S2CID 21345196.
- ^ May JM, Qu ZC, Neel DR, et al. (May 2003). "Recycling of vitamin C from its oxidized forms by human endothelial cells". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1640 (2–3): 153–61. doi:10.1016/S0167-4889(03)00043-0. PMID 12729925.
- ^ a b Padayatty SJ, Levine M (September 2016). "Vitamin C: the known and the unknown and Goldilocks". Oral Diseases. 22 (6): 463–93. doi:10.1111/odi.12446. PMC 4959991. PMID 26808119.
- ^ Branduardi P, Fossati T, Sauer M, et al. (October 2007). "Biosynthesis of vitamin C by yeast leads to increased stress resistance". PLOS ONE. 2 (10): e1092. Bibcode:2007PLoSO...2.1092B. doi:10.1371/journal.pone.0001092. PMC 2034532. PMID 17971855.
- ^ Wheeler GL, Jones MA, Smirnoff N (May 1998). "The biosynthetic pathway of vitamin C in higher plants". Nature. 393 (6683): 365–9. Bibcode:1998Natur.393..365W. doi:10.1038/30728. PMID 9620799. S2CID 4421568.
- ^ a b c Stone I (1972). "The natural history of ascorbic acid in the evolution of the mammals and primates and is significance for present-day man evolution of mammals and primates" (PDF). Journal of Orthomolecular Psychiatry. 1 (2): 82–9. Archived (PDF) from the original on October 2, 2023. Retrieved December 31, 2023.
- ^ Bánhegyi G, Mándl J (2001). "The hepatic glycogenoreticular system". Pathology & Oncology Research. 7 (2): 107–10. CiteSeerX 10.1.1.602.5659. doi:10.1007/BF03032575. PMID 11458272. S2CID 20139913.
- ^ a b Valpuesta V, Botella MA (2004). "Biosynthesis of L-ascorbic acid in plants: new pathways for an old antioxidant" (PDF). Trends in Plant Science. 9 (12): 573–7. doi:10.1016/j.tplants.2004.10.002. PMID 15564123. Archived (PDF) from the original on December 25, 2020. Retrieved October 8, 2018.
- ^ Nishikimi M, Yagi K (December 1991). "Molecular basis for the deficiency in humans of gulonolactone oxidase, a key enzyme for ascorbic acid biosynthesis". The Amer J Clin Nutr. 54 (6 Suppl): 1203S–8S. doi:10.1093/ajcn/54.6.1203s. PMID 1962571.
- ^ Nishikimi M, Kawai T, Yagi K (October 1992). "Guinea pigs possess a highly mutated gene for L-gulono-gamma-lactone oxidase, the key enzyme for L-ascorbic acid biosynthesis missing in this species". The Journal of Biological Chemistry. 267 (30): 21967–72. doi:10.1016/S0021-9258(19)36707-9. PMID 1400507.
- ^ Ohta Y, Nishikimi M (October 1999). "Random nucleotide substitutions in primate nonfunctional gene for L-gulono-gamma-lactone oxidase, the missing enzyme in L-ascorbic acid biosynthesis". Biochimica et Biophysica Acta (BBA) - General Subjects. 1472 (1–2): 408–11. doi:10.1016/S0304-4165(99)00123-3. PMID 10572964.
- ^ Wang S, Berge GE, Sund RB (August 2001). "Plasma ascorbic acid concentrations in healthy dogs". Res. Vet. Sci. 71 (1): 33–5. doi:10.1053/rvsc.2001.0481. PMID 11666145.
- ^ Ranjan R, Ranjan A, Dhaliwal GS, et al. (2012). "l-Ascorbic acid (vitamin C) supplementation to optimize health and reproduction in cattle". Vet Q. 32 (3–4): 145–50. doi:10.1080/01652176.2012.734640. PMID 23078207. S2CID 1674389.
- ^ a b c Dewick PM (2009). Medicinal natural products: a biosynthetic approach (3rd ed.). John Wiley and Sons. p. 493. ISBN 978-0-470-74167-2.
- ^ Miller RE, Fowler ME (2014). Fowler's zoo and wild animal medicine, volume 8. Elsevier Health Sciences. p. 389. ISBN 978-1-4557-7399-2. Archived from the original on December 7, 2016. Retrieved June 2, 2016.
- ^ Jenness R, Birney E, Ayaz K (1980). "Variation of l-gulonolactone oxidase activity in placental mammals". Comparative Biochemistry and Physiology B. 67 (2): 195–204. doi:10.1016/0305-0491(80)90131-5.
- ^ Cui J, Pan YH, Zhang Y, et al. (February 2011). "Progressive pseudogenization: vitamin C synthesis and its loss in bats". Molecular Biology and Evolution. 28 (2): 1025–31. doi:10.1093/molbev/msq286. PMID 21037206.
- ^ Cui J, Yuan X, Wang L, et al. (November 2011). "Recent loss of vitamin C biosynthesis ability in bats". PLOS ONE. 6 (11): e27114. Bibcode:2011PLoSO...627114C. doi:10.1371/journal.pone.0027114. PMC 3206078. PMID 22069493.
- ^ Martinez del Rio C (July 1997). "Can passerines synthesize vitamin C?". The Auk. 114 (3): 513–6. doi:10.2307/4089257. JSTOR 4089257.
- ^ a b c Drouin G, Godin JR, Pagé B (August 2011). "The genetics of vitamin C loss in vertebrates". Current Genomics. 12 (5): 371–8. doi:10.2174/138920211796429736. PMC 3145266. PMID 22294879.
- ^ Berra TM (2008). Freshwater fish distribution. University of Chicago Press. p. 55. ISBN 978-0-226-04443-9.
- ^ Milton K (June 1999). "Nutritional characteristics of wild primate foods: do the diets of our closest living relatives have lessons for us?" (PDF). Nutrition. 15 (6): 488–98. CiteSeerX 10.1.1.564.1533. doi:10.1016/S0899-9007(99)00078-7. PMID 10378206. Archived (PDF) from the original on August 10, 2017.
- ^ a b Pauling L (December 1970). "Evolution and the need for ascorbic acid". Proceedings of the National Academy of Sciences of the United States of America. 67 (4): 1643–8. Bibcode:1970PNAS...67.1643P. doi:10.1073/pnas.67.4.1643. PMC 283405. PMID 5275366.
- ^ Parrott T (October 2022). "Nutritional diseases of nonhuman primates". Merck Veterinary Manual. Archived from the original on December 24, 2023. Retrieved December 24, 2023.
- ^ Lachapelle MY, Drouin G (February 2011). "Inactivation dates of the human and guinea pig vitamin C genes". Genetica. 139 (2): 199–207. doi:10.1007/s10709-010-9537-x. PMID 21140195. S2CID 7747147.
- ^ Yang H (June 2013). "Conserved or lost: molecular evolution of the key gene GULO in vertebrate vitamin C biosynthesis". Biochemical Genetics. 51 (5–6): 413–25. doi:10.1007/s10528-013-9574-0. PMID 23404229. S2CID 14393449.
- ^ Zhang ZD, Frankish A, Hunt T, et al. (2010). "Identification and analysis of unitary pseudogenes: historic and contemporary gene losses in humans and other primates". Genome Biology. 11 (3): R26. doi:10.1186/gb-2010-11-3-r26. PMC 2864566. PMID 20210993.
- ^ Koshizaka T, Nishikimi M, Ozawa T, et al. (February 1988). "Isolation and sequence analysis of a complementary DNA encoding rat liver L-gulono-gamma-lactone oxidase, a key enzyme for L-ascorbic acid biosynthesis". The Journal of Biological Chemistry. 263 (4): 1619–21. doi:10.1016/S0021-9258(19)77923-X. PMID 3338984.
- ^ a b Pollock JI, Mullin RJ (1987). "Vitamin C biosynthesis in prosimians: evidence for the anthropoid affinity of Tarsius". American Journal of Physical Anthropology. 73 (1): 65–70. doi:10.1002/ajpa.1330730106. PMID 3113259.
- ^ Poux C, Douzery EJ (2004). "Primate phylogeny, evolutionary rate variations, and divergence times: a contribution from the nuclear gene IRBP". American Journal of Physical Anthropology. 124 (1): 01–16. doi:10.1002/ajpa.10322. PMID 15085543.
- ^ Goodman M, Porter CA, Czelusniak J, et al. (June 1998). "Toward a phylogenetic classification of Primates based on DNA evidence complemented by fossil evidence". Molecular Phylogenetics and Evolution. 9 (3): 585–98. doi:10.1006/mpev.1998.0495. PMID 9668008. S2CID 23525774.
- ^ Porter CA, Page SL, Czelusniak J, et al. (April 1997). "Phylogeny and evolution of selected primates as determined by sequences of the ε-globin locus and 5′ flanking regions". Int J Primatology. 18 (2): 261–95. doi:10.1023/A:1026328804319. hdl:2027.42/44561. S2CID 1851788.
- ^ Proctor P (1970). "Similar functions of uric acid and ascorbate in man?". Nature. 228 (5274): 868. Bibcode:1970Natur.228..868P. doi:10.1038/228868a0. PMID 5477017. S2CID 4146946.
- ^ Leferink NG, van den Berg WA, van Berkel WJ (February 2008). "l-Galactono-gamma-lactone dehydrogenase from Arabidopsis thaliana, a flavoprotein involved in vitamin C biosynthesis". The FEBS Journal. 275 (4): 713–26. doi:10.1111/j.1742-4658.2007.06233.x. PMID 18190525. S2CID 25096297.
- ^ Mieda T, Yabuta Y, Rapolu M, et al. (September 2004). "Feedback inhibition of spinach L-galactose dehydrogenase by L-ascorbate". Plant & Cell Physiology. 45 (9): 1271–9. doi:10.1093/pcp/pch152. PMID 15509850.
- ^ Grillet L, Ouerdane L, Flis P, et al. (January 2014). "Ascorbate efflux as a new strategy for iron reduction and transport in plants". The Journal of Biological Chemistry. 289 (5): 2515–25. doi:10.1074/jbc.M113.514828. PMC 3908387. PMID 24347170.
- ^ a b c Gallie DR (2013). "L-ascorbic acid: a multifunctional molecule supporting plant growth and development". Scientifica. 2013: 1–24. doi:10.1155/2013/795964. PMC 3820358. PMID 24278786.
- ^ a b c Mellidou I, Kanellis AK (2017). "Genetic control of ascorbic acid biosynthesis and recycling in horticultural crops". Frontiers in Chemistry. 5: 50. Bibcode:2017FrCh....5...50M. doi:10.3389/fchem.2017.00050. PMC 5504230. PMID 28744455.
- ^ Bulley S, Laing W (October 1, 2016). "The regulation of ascorbate biosynthesis". Current Opinion in Plant Biology. SI: 33: Cell signalling and gene regulation 2016. 33: 15–22. doi:10.1016/j.pbi.2016.04.010. ISSN 1369-5266. PMID 27179323.
- ^ Eggersdorfer M, Laudert D, Létinois U, et al. (December 2012). "One hundred years of vitamins-a success story of the natural sciences". Angewandte Chemie. 51 (52): 12960–12990. doi:10.1002/anie.201205886. PMID 23208776.
- ^ "The production of vitamin C" (PDF). Competition Commission. 2001. Archived from the original (PDF) on January 19, 2012. Retrieved February 20, 2007.
- ^ Zhou M, Bi Y, Ding M, et al. (2021). "One-step biosynthesis of vitamin C in Saccharomyces cerevisiae". Front Microbiol. 12: 643472. doi:10.3389/fmicb.2021.643472. PMC 7947327. PMID 33717042.
- ^ Tian YS, Deng YD, Zhang WH, et al. (August 2022). "Metabolic engineering of Escherichia coli for direct production of vitamin C from D-glucose". Biotechnol Biofuels Bioprod. 15 (1): 86. doi:10.1186/s13068-022-02184-0. PMC 9396866. PMID 35996146.
- ^ "Vantage market research: global vitamin C market size & share to surpass $1.8 Bn by 2028". Globe Newswire (Press release). November 8, 2022. Archived from the original on December 21, 2023. Retrieved December 21, 2023.
- ^ "Vitamin C price trend and forecast". ChemAnalyst. September 2023. Archived from the original on December 21, 2023. Retrieved December 21, 2023.
- ^ Bjelakovic G, Nikolova D, Gluud LL, et al. (March 2012). "Antioxidant supplements for prevention of mortality in healthy participants and patients with various diseases". The Cochrane Database of Systematic Reviews. 2012 (3): CD007176. doi:10.1002/14651858.CD007176.pub2. hdl:10138/136201. PMC 8407395. PMID 22419320.
- ^ World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. hdl:10665/44053. ISBN 978-92-4-154765-9.
- ^ "Ascorbic acid - drug usage statistics". ClinCalc. Archived from the original on January 18, 2024. Retrieved January 14, 2024.
- ^ Magiorkinis E, Beloukas A, Diamantis A (April 2011). "Scurvy: past, present and future". The European Journal of Internal Medicine. 22 (2): 147–52. doi:10.1016/j.ejim.2010.10.006. PMID 21402244.
- ^ Hodges RE, Baker EM, Hood J, et al. (May 1969). "Experimental scurvy in man". The American Journal of Clinical Nutrition. 22 (5): 535–48. doi:10.1093/ajcn/22.5.535. PMID 4977512.
- ^ Pemberton J (June 2006). "Medical experiments carried out in Sheffield on conscientious objectors to military service during the 1939-45 war". International Journal of Epidemiology. 35 (3): 556–8. doi:10.1093/ije/dyl020. PMID 16510534.
- ^ Belsky JB, Wira CR, Jacob V, et al. (December 2018). "A review of micronutrients in sepsis: the role of thiamine, L-carnitine, vitamin C, selenium and vitamin D". Nutrition Research Reviews. 31 (2): 281–90. doi:10.1017/S0954422418000124. PMID 29984680. S2CID 51599526.
- ^ a b Liang B, Su J, Shao H, et al. (March 2023). "The outcome of IV vitamin C therapy in patients with sepsis or septic shock: a meta-analysis of randomized controlled trials". Crit Care. 27 (1): 109. doi:10.1186/s13054-023-04392-y. PMC 10012592. PMID 36915173.
- ^ Berger MM, Oudemans-van Straaten HM (March 2015). "Vitamin C supplementation in the critically ill patient". Curr Opin Clin Nutr Metab Care. 18 (2): 193–201. doi:10.1097/MCO.0000000000000148. PMID 25635594. S2CID 37895257.
- ^ Xu C, Yi T, Tan S, et al. (April 2023). "Association of oral or intravenous vitamin C supplementation with mortality: A systematic review and meta-analysis". Nutrients. 15 (8): 1848. doi:10.3390/nu15081848. PMC 10146309. PMID 37111066.
- ^ Liang H, Mu Q, Sun W, et al. (2023). "Effect of intravenous vitamin C on adult septic patients: a systematic review and meta-analysis". Front Nutr. 10: 1211194. doi:10.3389/fnut.2023.1211194. PMC 10437115. PMID 37599680.
- ^ a b Hemilä H, Chalker E (January 2013). "Vitamin C for preventing and treating the common cold". The Cochrane Database of Systematic Reviews. 2013 (1): CD000980. doi:10.1002/14651858.CD000980.pub4. PMC 1160577. PMID 23440782.
- ^ Hemilä H, Chalker E (December 2023). "Vitamin C reduces the severity of common colds: a meta-analysis". BMC Public Health. 23 (1): 2468. doi:10.1186/s12889-023-17229-8. PMC 10712193. PMID 38082300.
- ^ Wintergerst ES, Maggini S, Hornig DH (2006). "Immune-enhancing role of vitamin C and zinc and effect on clinical conditions" (PDF). Annals of Nutrition & Metabolism. 50 (2): 85–94. doi:10.1159/000090495. PMID 16373990. S2CID 21756498. Archived (PDF) from the original on July 22, 2018. Retrieved August 25, 2019.
- ^ EFSA Panel on Dietetic Products, Nutrition and Allergies (2009). "Scientific Opinion on the substantiation of health claims related to vitamin C and protection of DNA, proteins and lipids from oxidative damage (ID 129, 138, 143, 148), antioxidant function of lutein (ID 146), maintenance of vision (ID 141, 142), collagen formation (ID 130, 131, 136, 137, 149), function of the nervous system (ID 133), function of the immune system (ID 134), function of the immune system during and after extreme physical exercise (ID 144), non-haem iron absorption (ID 132, 147), energy-yielding metabolism (ID 135), and relief in case of irritation in the upper respiratory tract (ID 1714, 1715) pursuant to Article 13(1) of Regulation (EC) No 1924/2006". EFSA Journal. 7 (9): 1226. doi:10.2903/j.efsa.2009.1226.
- ^ EFSA Panel on Dietetic Products, Nutrition and Allergies (2015). "Vitamin C and contribution to the normal function of the immune system: evaluation of a health claim pursuant to Article 14 of Regulation (EC) No 1924/2006". EFSA Journal. 13 (11): 4298. doi:10.2903/j.efsa.2015.4298. hdl:11380/1296052.
- ^ Bramstedt KA (October 2020). "Unicorn poo and blessed waters: COVID-19 quackery and FDA Warning Letters". Ther Innov Regul Sci. 55 (1): 239–44. doi:10.1007/s43441-020-00224-1. PMC 7528445. PMID 33001378.
- ^ "Vitamin C". COVID-19 Treatment Guidelines. April 21, 2021. Archived from the original on November 20, 2021. Retrieved January 2, 2022.
- ^ "COVID-19 treatment guidelines". U.S. National Institutes of Health. December 26, 2022. Archived from the original on November 20, 2021. Retrieved December 18, 2023.
- ^ a b c d Kow CS, Hasan SS, Ramachandram DS (December 2023). "The effect of vitamin C on the risk of mortality in patients with COVID-19: a systematic review and meta-analysis of randomized controlled trials". Inflammopharmacology. 31 (6): 3357–62. doi:10.1007/s10787-023-01200-5. PMC 10111321. PMID 37071316.
- ^ a b c Huang WY, Hong J, Ahn SI, et al. (December 2022). "Association of vitamin C treatment with clinical outcomes for COVID-19 patients: A systematic review and meta-analysis". Healthcare. 10 (12): 2456. doi:10.3390/healthcare10122456. PMC 9777834. PMID 36553979.
- ^ a b c Olczak-Pruc M, Swieczkowski D, Ladny JR, et al. (October 2022). "Vitamin C supplementation for the treatment of COVID-19: A systematic review and meta-analysis". Nutrients. 14 (19): 4217. doi:10.3390/nu14194217. PMC 9570769. PMID 36235869.
- ^ Cortés-Jofré M, Rueda JR, Asenjo-Lobos C, et al. (March 2020). "Drugs for preventing lung cancer in healthy people". The Cochrane Database of Systematic Reviews. 2020 (3): CD002141. doi:10.1002/14651858.CD002141.pub3. PMC 7059884. PMID 32130738.
- ^ Stratton J, Godwin M (June 2011). "The effect of supplemental vitamins and minerals on the development of prostate cancer: a systematic review and meta-analysis". Family Practice. 28 (3): 243–52. doi:10.1093/fampra/cmq115. PMID 21273283.
- ^ Heine-Bröring RC, Winkels RM, Renkema JM, et al. (May 2015). "Dietary supplement use and colorectal cancer risk: a systematic review and meta-analyses of prospective cohort studies". Int J Cancer. 136 (10): 2388–401. doi:10.1002/ijc.29277. PMID 25335850. S2CID 44706004.
- ^ Fulan H, Changxing J, Baina WY, et al. (October 2011). "Retinol, vitamins A, C, and E and breast cancer risk: a meta-analysis and meta-regression". Cancer Causes & Control. 22 (10): 1383–96. doi:10.1007/s10552-011-9811-y. PMID 21761132. S2CID 24867472.
- ^ Lee Y (November 2023). "Role of vitamin C in targeting cancer stem cells and cellular plasticity". Cancers (Basel). 15 (23): 5657. doi:10.3390/cancers15235657. PMC 10705783. PMID 38067361.
- ^ Satheesh NJ, Samuel SM, Büsselberg D (January 2020). "Combination therapy with vitamin C could eradicate cancer stem cells". Biomolecules. 10 (1): 79. doi:10.3390/biom10010079. PMC 7022456. PMID 31947879.
- ^ Al-Khudairy L, Flowers N, Wheelhouse R, et al. (March 2017). "Vitamin C supplementation for the primary prevention of cardiovascular disease". The Cochrane Database of Systematic Reviews. 2017 (3): CD011114. doi:10.1002/14651858.CD011114.pub2. PMC 6464316. PMID 28301692.
- ^ Chen GC, Lu DB, Pang Z, et al. (November 2013). "Vitamin C intake, circulating vitamin C and risk of stroke: a meta-analysis of prospective studies". J Amer Heart Assoc. 2 (6): e000329. doi:10.1161/JAHA.113.000329. PMC 3886767. PMID 24284213.
- ^ Ashor AW, Lara J, Mathers JC, et al. (July 2014). "Effect of vitamin C on endothelial function in health and disease: a systematic review and meta-analysis of randomized controlled trials". Atherosclerosis. 235 (1): 9–20. doi:10.1016/j.atherosclerosis.2014.04.004. PMID 24792921.
- ^ Ran L, Zhao W, Tan X, et al. (April 2020). "Association between serum vitamin C and the blood pressure: A systematic review and meta-analysis of observational studies". Cardiovasc Ther. 2020: 4940673. doi:10.1155/2020/4940673. PMC 7211237. PMID 32426036.
- ^ a b Guan Y, Dai P, Wang H (February 2020). "Effects of vitamin C supplementation on essential hypertension: A systematic review and meta-analysis". Medicine (Baltimore). 99 (8): e19274. doi:10.1097/MD.0000000000019274. PMC 7034722. PMID 32080138.
- ^ Lbban E, Kwon K, Ashor A, et al. (December 2023). "Vitamin C supplementation showed greater effects on systolic blood pressure in hypertensive and diabetic patients: an updated systematic review and meta-analysis of randomized clinical trials". Int J Food Sci Nutr. 74 (8): 814–25. doi:10.1080/09637486.2023.2264549. PMID 37791386. S2CID 263621742. Archived from the original on January 21, 2024. Retrieved December 23, 2023.
- ^ Mason SA, Keske MA, Wadley GD (February 2021). "Effects of vitamin C supplementation on glycemic control and cardiovascular risk factors in people With type 2 diabetes: A GRADE-assessed systematic review and meta-analysis of randomized controlled trials". Diabetes Care. 44 (2): 618–30. doi:10.2337/dc20-1893. hdl:10536/DRO/DU:30147432. PMID 33472962. Archived from the original on January 21, 2024. Retrieved December 21, 2023.
- ^ Nosratabadi S, Ashtary-Larky D, Hosseini F, et al. (August 2023). "The effects of vitamin C supplementation on glycemic control in patients with type 2 diabetes: A systematic review and meta-analysis". Diabetes and Metabolic Syndrome. 17 (8): 102824. doi:10.1016/j.dsx.2023.102824. PMID 37523928. S2CID 259581695.
- ^ DeLoughery TG (March 2017). "Iron deficiency anemia". Med Clin North Am (Review). 101 (2): 319–32. doi:10.1016/j.mcna.2016.09.004. PMID 28189173.
- ^ Nathan N, Patel P (November 10, 2021). "Why is topical vitamin C important for skin health?". Harvard Health Publishing, Harvard Medical School. Archived from the original on October 14, 2022. Retrieved October 14, 2022.
- ^ Pullar JM, Carr AC, Vissers MC (August 2017). "The roles of vitamin C in skin health". Nutrients. 9 (8): 866. doi:10.3390/nu9080866. PMC 5579659. PMID 28805671.
- ^ Al-Niaimi F, Chiang NY (July 2017). "Topical vitamin C and the skin: Mechanisms of action and clinical applications". J Clin Aesthet Dermatol. 10 (7): 14–17. PMC 5605218. PMID 29104718.
- ^ Sanabria B, Berger LE, Mohd H, et al. (September 2023). "Clinical efficacy of topical vitamin C on the appearance of wrinkles: A systematic literature review". J Drugs Dermatol. 22 (9): 898–904. doi:10.36849/JDD.7332 (inactive January 31, 2024). PMID 37683066.
{{cite journal}}: CS1 메인트: DOI 2024년 1월 기준 비활성화 (링크) - ^ Correia G, Magina S (July 2023). "Efficacy of topical vitamin C in melasma and photoaging: A systematic review". J Cosmet Dermatol. 22 (7): 1938–45. doi:10.1111/jocd.15748. PMID 37128827. S2CID 258439047.
- ^ Lopes da Silva S, Vellas B, Elemans S, et al. (2014). "Plasma nutrient status of patients with Alzheimer's disease: Systematic review and meta-analysis". Alzheimer's & Dementia. 10 (4): 485–502. doi:10.1016/j.jalz.2013.05.1771. PMID 24144963.
- ^ Li FJ, Shen L, Ji HF (2012). "Dietary intakes of vitamin E, vitamin C, and β-carotene and risk of Alzheimer's disease: a meta-analysis". Journal of Alzheimer's Disease. 31 (2): 253–8. doi:10.3233/JAD-2012-120349. PMID 22543848.
- ^ Harrison FE (2012). "A critical review of vitamin C for the prevention of age-related cognitive decline and Alzheimer's disease". Journal of Alzheimer's Disease. 29 (4): 711–26. doi:10.3233/JAD-2012-111853. PMC 3727637. PMID 22366772.
- ^ Sideri O, Tsaousis KT, Li HJ, et al. (2019). "The potential role of nutrition on lens pathology: a systematic review and meta-analysis". Surv Ophthalmol. 64 (5): 668–78. doi:10.1016/j.survophthal.2019.03.003. PMID 30878580. S2CID 81981938.
- ^ Jiang H, Yin Y, Wu CR, et al. (January 2019). "Dietary vitamin and carotenoid intake and risk of age-related cataract". Am J Clin Nutr. 109 (1): 43–54. doi:10.1093/ajcn/nqy270. PMID 30624584.
- ^ Evans JR, Lawrenson JG (July 2017). "Antioxidant vitamin and mineral supplements for preventing age-related macular degeneration". Cochrane Database Syst Rev. 2017 (7): CD000253. doi:10.1002/14651858.CD000253.pub4. PMC 6483250. PMID 28756617.
- ^ Mi N, Zhang M, Ying Z, et al. (January 2024). "Vitamin intake and periodontal disease: a meta-analysis of observational studies". BMC Oral Health. 24 (1): 117. doi:10.1186/s12903-024-03850-5. PMC 10799494. PMID 38245765.
- ^ Tada A, Miura H (July 2019). "The relationship between vitamin C and periodontal diseases: A systematic review". Int J Environ Res Public Health. 16 (14): 2472. doi:10.3390/ijerph16142472. PMC 6678404. PMID 31336735.
- ^ Goodwin JS, Tangum MR (November 1998). "Battling quackery: attitudes about micronutrient supplements in American academic medicine". Archives of Internal Medicine. 158 (20): 2187–91. doi:10.1001/archinte.158.20.2187. PMID 9818798.
- ^ Naidu KA (August 2003). "Vitamin C in human health and disease is still a mystery? An overview" (PDF). Nutrition Journal. 2 (7): 7. doi:10.1186/1475-2891-2-7. PMC 201008. PMID 14498993. Archived (PDF) from the original on September 18, 2012.
- ^ Thomas LD, Elinder CG, Tiselius HG, et al. (March 2013). "Ascorbic acid supplements and kidney stone incidence among men: a prospective study". JAMA Internal Medicine. 173 (5): 386–8. doi:10.1001/jamainternmed.2013.2296. PMID 23381591.
- ^ a b Jacobs C, Hutton B, Ng T, et al. (February 2015). "Is there a role for oral or intravenous ascorbate (vitamin C) in treating patients with cancer? A systematic review". The Oncologist. 20 (2): 210–23. doi:10.1634/theoncologist.2014-0381. PMC 4319640. PMID 25601965.
- ^ Shrestha DB, Budhathoki P, Sedhai YR, et al. (October 2021). "Vitamin C in critically ill patients: An updated systematic review and meta-analysis". Nutrients. 13 (10): 3564. doi:10.3390/nu13103564. PMC 8539952. PMID 34684565.
- ^ Holford P, Carr AC, Zawari M, et al. (November 2021). "Vitamin C intervention for critical COVID-19: A pragmatic review of the current level of evidence". Life. 11 (11): 1166. Bibcode:2021Life...11.1166H. doi:10.3390/life11111166. PMC 8624950. PMID 34833042.
- ^ Abobaker A, Alzwi A, Alraied AH (December 2020). "Overview of the possible role of vitamin C in management of COVID-19". Pharmacol Rep. 72 (6): 1517–28. doi:10.1007/s43440-020-00176-1. PMC 7592143. PMID 33113146.
- ^ Lind J (1772). A Treatise on the Scurvy (3rd ed.). London, England: G. Pearch and W. Woodfall. p. 285. Archived from the original on January 1, 2016.
- ^ Ashhurst J, ed. (1881). The International Encyclopedia of Surgery. Vol. 1. New York, New York: William Wood and Co. p. 278. Archived from the original on May 5, 2016.
- ^ Rajakumar K (October 2001). "Infantile scurvy: a historical perspective". Pediatrics. 108 (4): E76. CiteSeerX 10.1.1.566.5857. doi:10.1542/peds.108.4.e76. PMID 11581484. Archived from the original on September 4, 2015.
As they sailed farther up the east coast of Africa, they met local traders, who traded them fresh oranges. Within six days of eating the oranges, da Gama's crew recovered fully
- ^ Livermore H (2004). "Santa Helena, a forgotten Portuguese discovery" (PDF). Estudos Em Homenagem a Luis Antonio de Oliveira Ramos [Studies in Homage to Luis Antonio de Oliveira Ramos.]: 623–631. Archived from the original (PDF) on May 29, 2011.
On returning, Lopes' ship had left him on St Helena, where with admirable sagacity and industry he planted vegetables and nurseries with which passing ships were marvelously sustained. [...] There were 'wild groves' of oranges, lemons and other fruits that ripened all the year round, large pomegranates and figs.
- ^ Woodall J (1617). The Surgion's Mate. London, England: Edward Griffin. p. 89. Archived from the original on April 11, 2016.
Succus Limonum, or juice of Lemons ... [is] the most precious help that ever was discovered against the Scurvy[;] to be drunk at all times; ...
- ^ Armstrong A (1858). "Observation on naval hygiene and scurvy, more particularly as the later appeared during the Polar voyage". British and Foreign Medico-chirurgical Review: Or, Quarterly Journal of Practical Medicine and Surgery. 22: 295–305.
- ^ Bachstrom JF (1734). Observationes circa scorbutum [Observations on scurvy] (in Latin). Leiden (Lugdunum Batavorum), Netherlands: Conrad Wishof. p. 16. Archived from the original on January 1, 2016.
... sed ex nostra causa optime explicatur, que est absentia, carentia & abstinentia a vegetabilibus recentibus, ... ( ... but [this misfortune] is explained very well by our [supposed] cause, which is the absence of, lack of, and abstinence from fresh vegetables, ...
- ^ Lamb J (February 17, 2011). "Captain Cook and the scourge of scurvy". British History in depth. BBC. Archived from the original on February 21, 2011.
- ^ Lamb J (2001). Preserving the self in the south seas, 1680–1840. University of Chicago Press. p. 117. ISBN 978-0-226-46849-5. Archived from the original on April 30, 2016.
- ^ a b c Baron JH (June 2009). "Sailors' scurvy before and after James Lind--a reassessment". Nutrition Reviews. 67 (6): 315–32. doi:10.1111/j.1753-4887.2009.00205.x. PMID 19519673. S2CID 20435128.
- ^ Lind J (1753). A treatise of the scurvy. London: A. Millar. 1757년 판에서 린드는 자신의 실험에 대해 다음과 같이 논합니다.
- ^ Beaglehole JH, Cook JD, Edwards PR (1999). The journals of Captain Cook. Harmondsworth [Eng.]: Penguin. ISBN 978-0-14-043647-1.
- ^ "Copley Medal, past winners". The Royal Society. Archived from the original on September 6, 2015. Retrieved January 1, 2024.
- ^ Reeve J, Stevens DA (2006). "Cook's Voyages 1768–1780". Navy and the nation: the influence of the navy on modern Australia. Allen & Unwin Academic. p. 74. ISBN 978-1-74114-200-6.
- ^ Kuhnlein HV, Receveur O, Soueida R, et al. (June 2004). "Arctic indigenous peoples experience the nutrition transition with changing dietary patterns and obesity". The Journal of Nutrition. 134 (6): 1447–53. doi:10.1093/jn/134.6.1447. PMID 15173410.
- ^ a b Squires VR (2011). The role of food, agriculture, forestry and fisheries in human nutrition - Volume IV. EOLSS Publications. p. 121. ISBN 978-1-84826-195-2. Archived from the original on January 11, 2023. Retrieved September 17, 2017.
- ^ Stacey M, Manners DJ (1978). "Edmund Langley Hirst". Advances in carbohydrate chemistry and biochemistry. Vol. 35. pp. 1–29. doi:10.1016/S0065-2318(08)60217-6. ISBN 978-0-12-007235-4. PMID 356548.
- ^ "Redoxon trademark information by Hoffman-la Roche, Inc. (1934)". Archived from the original on November 16, 2018. Retrieved December 25, 2017.
- ^ Wang W, Xu H (2016). "Industrial fermentation of Vitamin C". In Vandamme EJ, Revuelta JI (eds.). Industrial biotechnology of vitamins, biopigments, and antioxidants. Wiley-VCH Verlag GmbH & Co. KGaA. p. 161. ISBN 978-3-527-33734-7.
- ^ Norum KR, Grav HJ (June 2002). "[Axel Holst and Theodor Frolich--pioneers in the combat of scurvy]". Tidsskrift for den Norske Laegeforening (in Norwegian). 122 (17): 1686–7. PMID 12555613.
- ^ Rosenfeld L (April 1997). "Vitamine--vitamin. The early years of discovery". Clinical Chemistry. 43 (4): 680–5. doi:10.1093/clinchem/43.4.680. PMID 9105273.
- ^ a b Zetterström R (May 2009). "Nobel Prize 1937 to Albert von Szent-Györgyi: identification of vitamin C as the anti-scorbutic factor". Acta Paediatrica. 98 (5): 915–19. doi:10.1111/j.1651-2227.2009.01239.x. PMID 19239412. S2CID 11077461.
- ^ a b Svirbely JL, Szent-Györgyi A (1932). "The chemical nature of vitamin C". The Biochemical Journal. 26 (3): 865–70. Bibcode:1932Sci....75..357K. doi:10.1126/science.75.1944.357-a. PMC 1260981. PMID 16744896.
- ^ Juhász-Nagy S (March 2002). "[Albert Szent-Györgyi--biography of a free genius]". Orvosi Hetilap (in Hungarian). 143 (12): 611–4. PMID 11963399.
- ^ Kenéz J (December 1973). "[Eventful life of a scientist. 80th birthday of Nobel prize winner Albert Szent-Györgyi]". Munchener Medizinische Wochenschrift (in German). 115 (51): 2324–6. PMID 4589872.
- ^ Szállási A (December 1974). "[2 interesting early articles by Albert Szent-Györgyi]". Orvosi Hetilap (in Hungarian). 115 (52): 3118–9. PMID 4612454.
- ^ a b "The Albert Szent-Gyorgyi Papers: Szeged, 1931-1947: Vitamin C, Muscles, and WWII". Profiles in Science. United States National Library of Medicine. Archived from the original on May 5, 2009.
- ^ "Scurvy". Online Entymology Dictionary. Archived from the original on December 15, 2020. Retrieved November 19, 2017.
- ^ Hirst EL (April 1950). "Sir Norman Haworth". Nature. 165 (4198): 587. Bibcode:1950Natur.165..587H. doi:10.1038/165587a0. PMID 15416703.
- ^ Burns JJ, Evans C (December 1956). "The synthesis of L-ascorbic acid in the rat from D-glucuronolactone and L-gulonolactone" (PDF). The Journal of Biological Chemistry. 223 (2): 897–905. doi:10.1016/S0021-9258(18)65088-4. PMID 13385237. Archived from the original on December 3, 2022. Retrieved December 3, 2022.
- ^ Burns JJ, Moltz A, Peyser P (December 1956). "Missing step in guinea pigs required for the biosynthesis of L-ascorbic acid". Science. 124 (3232): 1148–9. Bibcode:1956Sci...124.1148B. doi:10.1126/science.124.3232.1148-a. PMID 13380431.
- ^ Henson DE, Block G, Levine M (April 1991). "Ascorbic acid: biologic functions and relation to cancer". Journal of the National Cancer Institute. 83 (8): 547–50. doi:10.1093/jnci/83.8.547. PMID 1672383. Archived from the original on December 25, 2020. Retrieved March 18, 2020.
- ^ a b Saul A. "Orthomolecular Medicine Hall of fame - Irwin Stone, Ph.D." Orthomolecular Organization. Archived from the original on August 9, 2011. Retrieved December 25, 2023.
- ^ Montel-Hagen A, Kinet S, Manel N, et al. (March 2008). "Erythrocyte Glut1 triggers dehydroascorbic acid uptake in mammals unable to synthesize vitamin C". Cell. 132 (6): 1039–48. doi:10.1016/j.cell.2008.01.042. PMID 18358815. S2CID 18128118.
- ^ Mandl J, Szarka A, Bánhegyi G (August 2009). "Vitamin C: update on physiology and pharmacology". British Journal of Pharmacology. 157 (7): 1097–110. doi:10.1111/j.1476-5381.2009.00282.x. PMC 2743829. PMID 19508394.
- ^ Cameron E, Pauling L (October 1976). "Supplemental ascorbate in the supportive treatment of cancer: Prolongation of survival times in terminal human cancer". Proceedings of the National Academy of Sciences of the United States of America. 73 (10): 3685–9. Bibcode:1976PNAS...73.3685C. doi:10.1073/pnas.73.10.3685. PMC 431183. PMID 1068480.
- ^ Boseley S (September 12, 2008). "Fall of the vitamin doctor: Matthias Rath drops libel action". The Guardian. Archived from the original on December 1, 2016. Retrieved January 5, 2024.
- ^ Colquhoun D (August 15, 2007). "The age of endarkenment Science guardian.co.uk". Guardian. Archived from the original on March 6, 2023. Retrieved January 5, 2024.
- ^ Barret S (September 14, 2014). "The dark side of Linus Pauling's legacy". www.quackwatch.org. Archived from the original on September 4, 2018. Retrieved December 18, 2018.
- ^ Wilson MK, Baguley BC, Wall C, et al. (March 2014). "Review of high-dose intravenous vitamin C as an anticancer agent". Asia-Pacific Journal of Clinical Oncology. 10 (1): 22–37. doi:10.1111/ajco.12173. PMID 24571058. S2CID 206983069.