리보플라빈
Riboflavin | |
 화학구조 | |
| 임상자료 | |
|---|---|
| 상호 | 많은[1] |
| 기타이름 | 락토크롬, 락토플라빈, 비타민G[2] |
| AHFS/Drugs.com | 모노그래프 |
| 라이센스 데이터 | |
| 경로 행정부. | 입으로, 근육내로, 정맥내로 |
| ATC코드 | |
| 법적지위 | |
| 법적지위 |
|
| 약동학적 자료 | |
| 제거 반감기 | 66분~84분 |
| 배설 | 소변 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드럭뱅크 | |
| 켐스파이더 | |
| 유니아이 | |
| 케그 | |
| ChEBI | |
| 쳄블 | |
| E번 | E101, E101(iii) (색상) |
| CompTox 대시보드 (EPA) | |
| ECHA 인포카드 | 100.001.370 |
| 화학 및 물리 데이터 | |
| 공식 | C17H20N4O6 |
| 어금니 질량 | 376.369g·mol−1 |
| 3D 모델(JSMO) | |
| |
| |
비타민 B라고도2 알려진 리보플라빈은 음식에서 발견되는 비타민으로 건강보조식품으로 판매됩니다.[3]이것은 플라빈 모노뉴클레오티드와 플라빈 아데닌 다이뉴클레오티드의 두 가지 주요 조효소의 형성에 필수적입니다.이 조효소들은 정상적인 성장과 발달뿐만 아니라 에너지 대사, 세포 호흡, 항체 생성에 관여합니다.조효소는 나이아신, 비타민 B6, 엽산의 대사에도 필요합니다.리보플라빈은 각막박리를 치료하기 위해 처방되며, 경구로 복용하면 성인의 편두통 발생을 줄일 수 있습니다.
리보플라빈 결핍은 드물고 대개 다른 비타민과 영양소의 결핍을 동반합니다.경구 보충제나 주사제로 예방하거나 치료할 수 있습니다.수용성 비타민으로서, 영양 요건을 초과하여 섭취된 리보플라빈은 저장되지 않습니다; 그것은 흡수되지 않거나 소변으로 흡수되고 빠르게 배설되어 소변이 밝은 노란색 색조를 갖게 합니다.리보플라빈의 천연 공급원은 고기, 생선과 가금류, 달걀, 유제품, 녹색 채소, 버섯, 아몬드 등입니다.어떤 나라들은 곡물에 그것을 첨가할 것을 합니다.[3]
리보플라빈은 1920년에 발견되었고 1933년에 분리되었으며 1935년에 처음 합성되었습니다.정제된 고체 형태로 수용성 황색-주황색 결정성 분말입니다.비타민으로서의 기능 외에도 식용 색소로 사용됩니다.생합성은 박테리아, 곰팡이, 식물에서 일어나지만 동물에서는 일어나지 않습니다.리보플라빈의 산업적 합성은 처음에 화학 공정을 사용하여 달성되었지만, 현재의 상업적 제조는 균류 및 유전자 변형 박테리아 균주를 사용한 발효 방법에 의존합니다.
정의.
비타민 B라고도2 알려진 리보플라빈은 수용성 비타민으로 B 비타민 중 하나입니다.[3][4][5]비타민 B로 알려진 엽산과 비타민 B와는6 달리, 리보플라빈은 단지 하나의 화학적 화합물입니다.이것은 조효소 플라빈 모노뉴클레오타이드(FMN, 리보플라빈-5'-인산으로도 알려져 있음)와 플라빈 아데닌 다이뉴클레오타이드(FAD)의 합성에서 출발하는 화합물입니다.FAD는 모든 종의 게놈(플라보단백질)[6][7]에서 플라빈 의존성 단백질 암호화 유전자 수의 75%에 결합하는 것으로 보고된 더 풍부한 형태의 플라빈이며 인간 암호화 플라보단백질의 84%에 대한 공동 효소 역할을 합니다.[6]
리보플라빈은 정제된 고체 형태의 노란색-주황색 결정성 분말로 약간의 냄새와 쓴 맛이 있습니다.물과 염화나트륨 수용액과 같은 극성 용매에는 용해되고 알코올에는 약간 용해됩니다.클로로포름, 벤젠 또는 아세톤과 같은 무극성 또는 약극성 유기 용매에는 용해되지 않습니다.[8]용액에서 또는 분말로 건조 보관하는 동안, 리보플라빈은 빛에 노출되지 않으면 열이 안정적입니다.분해하기 위해 가열하면 산화질소가 포함된 유독 가스를 방출합니다.[8]
기능들
리보플라빈은 FMN과 FAD라는 두 가지 주요 조효소의 형성에 필수적입니다.[3][9]이 조효소들은 에너지 대사, 세포 호흡, 항체 생성, 성장과 발달에 관여합니다.[9]리보플라빈은 탄수화물, 단백질, 지방의 대사에 필수적입니다.[3]FAD는 트립토판을 나이아신(비타민 B3)[10]으로 전환시키는 데 기여하고 비타민6 B를 조효소 피리독살 5'-인산으로 전환하려면 FMN이 필요합니다.[10] 리보플라빈은 호모시스테인의 정상적인 순환 수준을 유지하는 데 관여합니다. 리보플라빈 결핍 시 호모시스테인 수치가 증가하여 심혈관 질환의 위험을 높입니다.[10]
산화환원반응
산화 환원 반응은 전자의 이동을 수반하는 과정입니다.플라빈 조효소는 플라빈이 산화물 사이에서 전환되는 능력을 이용하여 1-2 전자 산화 환원 반응을 일으키는 인간(그리고 원시, 박테리아 및 곰팡이 유전체에 의해 암호화된 것을 포함하여 모든 유기체에 걸쳐 수백 개 이상의 플라빈 효소)의 기능을 지원합니다.반 reduced 및 완전히 축소된 형태.FAD는 또한 내인성 항산화제인 글루타티온의 필수적인 효소 정보인 글루타티온 환원효소의 활성에도 필요합니다.[10]
미세영양소대사
리보플라빈, FMN, FAD는 나이아신, 비타민 B6, 엽산의 대사에 관여합니다.[4]트립토판으로부터 나이아신을 함유한 조효소인 NAD와 NADP의 합성은 FAD 의존성 효소인 키뉴레닌 3-모노옥시게나제를 포함합니다.리보플라빈의 식이 결핍은 NAD와 NADP의 생성을 감소시켜 나이아신 결핍을 촉진시킬 수 있습니다.[4]비타민 B를6 그것의 조효소인 피리독살 5'-인산 합성효소로 전환하는 것은 FMN을 필요로 하는 피리독신 5'-인산 산화효소를 포함합니다. 엽산 대사에 관여하는 효소인 5,10-메틸렌테트라하이드로폴산 환원효소는 호모시스테인으로부터 아미노산인 메티오닌을 형성하기 위해 FAD를 필요로 합니다.[4][4]
리보플라빈 결핍은 헤모글로빈과 적혈구 생성에 필수적인 식이광물인 철분의 대사를 방해하는 것으로 보입니다.리보플라빈과 철분이 모두 부족한 사람들의 리보플라빈 결핍을 완화시키는 것은 철분 결핍성 빈혈 치료를 위한 철분 보충의 효과를 향상시킵니다.[11]
합성
생합성
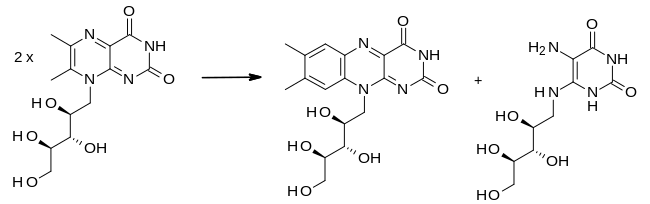
생합성은 박테리아, 곰팡이, 식물에서 일어나지만 동물에서는 일어나지 않습니다.[5]리보플라빈에 대한 생합성 전구체는 리불로스 5-인산과 구아노신 3-인산입니다.전자는 L-3,4-디하이드록시-2-부타논-4-인산으로 전환되는 반면, 후자는 5-아미노-6-(D-리비티아미노)우라실로 이어지는 일련의 반응에서 전환됩니다.그리고 이 두 화합물은 반응 EC 2.5.1.78에서 효소 루마진 합성효소에 의해 촉매되는 경로의 두 번째 단계를 위한 기질입니다.[12][13][14]
생합성의 마지막 단계에서, 2개의 6,7-디메틸-8-리비틸루마진은 돌연변이 반응에서 리보플라빈 합성효소에 의해 결합됩니다.이것은 리보플라빈의 한 분자와 5-아미노-6-(D-리비티아미노) 우라실의 한 분자를 생성합니다.후자는 순서대로 이전 반응으로 재활용됩니다.[12][13]
리보플라빈의 보조 인자 FMN 및 FAD로의 전환은 효소 리보플라빈 키나제와 FAD 합성효소가 순차적으로 작용함으로써 수행됩니다.[13][15]
산업합성

리보플라빈의 산업 규모 생산은 Ashbya gossypii, Candida famata 및 Candida flaveri와 같은 필라멘트 균류를 포함한 다양한 미생물을 사용합니다.B. 서브틸리스는 리보플라빈의 생산을 증가시키고 항생제(암피실린)[17] 내성 마커를 도입하기 위해 유전적으로 변형되어 사료 및 식품 강화용 리보플라빈을 생산하기 위해 상업적 규모로 사용되고 있습니다.2012년까지 연간 4,000톤 이상이 이러한 발효 공정을 통해 생산되었습니다.[18]
고농도의 탄화수소 또는 방향족 화합물이 존재하는 경우, 일부 박테리아는 보호 메커니즘으로서 리보플라빈을 과잉 생산합니다.그러한 유기체 중 하나는 마이크로코커스 루테우스(Micrococcus luteus, American Type Culture Collection number ATCC 49442)인데, 피리딘에서 자라는 동안 리보플라빈이 생성되어 노란색을 띠게 되지만 숙신산과 같은 다른 기질에서 자랄 때는 그렇지 않습니다.[16]
실험실 합성
리보플라빈의 첫 번째 총 합성은 리차드 쿤의 그룹에 의해 수행되었습니다.[18][19]D-리보스를 사용하여 환원성 아미노화하여 생성된 치환 아닐린을 마지막 단계에서 알록산으로 축합하였습니다.
사용하다
각막박리 치료
각막각막은 각막이 점점 얇아지는 가장 흔한 형태의 각막외반증입니다.각막 콜라겐 가교를 통해 치료되는 질환으로 각막 경직도가 높아집니다.교차 결합은 국소 리보플라빈 용액을 각막에 도포하여 이루어지며, 이 용액은 자외선 A 빛에 노출됩니다.[20][21]
편두통 예방
2012년 미국 신경학 협회의 가이드라인에서 고용량 리보플라빈(400 mg)은 "아마도 효과적이며 편두통 예방을 위해 고려되어야 한다"고 밝혔으며,[22] 이는 또한 영국 국립 편두통 센터가 제공한 권고 사항입니다.[23]2017년 리뷰에 따르면 하루에 400 mg씩 최소 3개월 동안 매일 리보플라빈을 복용하는 것이 성인들의 편두통 빈도를 줄일 수 있다고 보고했습니다.[24]소아·청소년 편두통 예방 또는 치료를 위한 고용량 리보플라빈에 대한 연구는 아직 결론이 나지 않아 보충제를 권장하지 않습니다.[1][3][25]
식용색소
리보플라빈은 식용 색소(노란색-주황색 결정성 분말)로 사용되며,[8] 유럽에서는 식품 첨가제로 사용하기 위해 E 번호인 E101로 지정되어 있습니다.[26]
식사 권장 사항
미국 의학 아카데미는 1998년 리보플라빈에 대한 EAR(Estimate Average Requirements)와 RDA(Recommended Dietary Allowances)를 업데이트했습니다.14세 이상 여성과 남성의 리보플라빈 EAR은[update] 각각 0.9mg/일과 1.1mg/일이고, RDA는 각각 1.1mg/일입니다.RDA는 평균 이상의 요구 조건을 가진 사람들에게 적절한 섭취 수준을 제공하기 위해 EAR보다 높습니다.임신 중의 RDA는 1.4 mg/day이고 수유부의 RDA는 1.6 mg/day입니다.12개월까지의 유아의 경우 적정 섭취량(AI)은 0.3–0.4 mg/day이고, 1–13세 어린이의 경우 RDA가 0.5–0.9 mg/day로 증가합니다.안전성의 경우, IOM은 증거가 충분할 때 비타민과 미네랄에 대해 허용 가능한 상위 섭취 수준(ULs)을 설정합니다.리보플라빈의 경우 고용량으로 인한 부작용에 대한 인체 데이터가 없기 때문에 UL이 없습니다.EARs, RDAs, AIs 및 ULs를 종합하여 DRIs(식용 기준 섭취량)라고 합니다.[4][27]
유럽 식품 안전청(EFSA)은 RDA 대신 인구 기준 섭취량(PRI), EAR 대신 평균 요구량(Average Requirement)으로 정보의 집합을 식이 기준 값(Dietry Reference Values)이라고 합니다.AI와 UL은 미국과 동일하게 정의됩니다.15세 이상 여성과 남성의 경우 PRI는 1.6mg/day로 설정됩니다.임신 중의 PRI는 1.9 mg/day이고 수유부의 PRI는 2.0 mg/day입니다.1-14세 어린이의 경우 PRI가 0.6에서 1.4 mg/일로 증가합니다.이 PRI들은 미국의 RDA들보다 더 높습니다.[28][29]EFSA는 또한 최대 안전 섭취량을 고려했고 미국 국립 의학 아카데미와 마찬가지로 UL을 설정하기에 충분한 정보가 없다고 결정했습니다.[30]
| 권장 식이요법 허용량 미국 | |
| 연령대(년) | 리보플라빈 RDA(mg/d)[4] |
|---|---|
| 0-6개월 | 0.3* |
| 6-12개월 | 0.4* |
| 1–3 | 0.5 |
| 4–8 | 0.6 |
| 9–13 | 0.9 |
| 여성 14~18세 | 1.0 |
| 남성 14–18 | 1.3 |
| 여성 19+ | 1.1 |
| 남성 19+ | 1.3 |
| 임산부 | 1.4 |
| 수유중인 암컷 | 1.6 |
| * 신생아에 대한 적절한 섭취량, 아직 RDA/RDI가 확립되지[4] 않음 | |
| 유럽연합을 차지하는 인구 기준 | |
| 연령대(년) | 리보플라빈(mg/d)[29]에 대한 PRI |
| 7-11개월 | 0.4 |
| 1–3 | 0.6 |
| 4–6 | 0.7 |
| 7–10 | 1.0 |
| 11–14 | 1.4 |
| 15– | 1.6 |
| 임산부 | 1.9 |
| 수유중인 암컷 | 2.0 |
안전.
사람의 경우, 과다 섭취에 의해 생성되는 리보플라빈 독성에 대한 증거가 없으며 투여량이 증가함에 따라 흡수 효율이 떨어집니다.과도한 리보플라빈은 신장을 통해 소변으로 배출되어 플라비뇨증으로 알려진 밝은 노란색을 만듭니다.[5][27][31]편두통의 빈도와 중증도를 치료하기 위한 리보플라빈의 효과에 대한 임상 시험 동안 피험자들은 3-12개월 동안 하루에 최대 400 mg의 리보플라빈을 경구로 투여받았습니다.복통과 설사는 보고된 부작용 중 하나였습니다.[24]
라벨링
미국 식품 및 식이 보충제 표시 목적의 경우 1인분의 양은 일일 가치(%DV)의 백분율로 표시됩니다.리보플라빈 표시 목적상 일일치의 100%는 1.7 mg 이었으나, 2016년 5월 27일부로 1.3 mg으로 개정되어 RDA와 합의하였습니다.[32][33] Reference Daily Incuption에서 구 및 신 성인 일일치 표가 제공합니다.
원천
미국 농무부 농업연구국은 수백 가지 식품에 포함된 리보플라빈 성분을 검색할 수 있는 식품 구성 데이터베이스를 유지하고 있습니다.[34]
|
|
|
밀을 도정하면 리보플라빈이 85% 손실되기 때문에 [citation needed]흰 밀가루는 일부 국가에서 농축됩니다.리보플라빈은 유아식, 아침 시리얼, 파스타, 비타민이 풍부한 식사 대용 제품에도 첨가됩니다.[3]리보플라빈은 물에 대한 용해도가 낮기 때문에 액체 제품에 포함시키는 것이 어렵습니다. 따라서, 보다 용해성이 높은 리보플라빈의 형태인 리보플라빈-5'-인산(FMN, 착색제로 사용될 때 E101이라고도 불림)[26]에 대한 요구사항.빵과 바로 먹을 수 있는 아침 시리얼의 풍부함은 비타민의 식이 공급에 크게 기여합니다.프리 리보플라빈은 단백질이 결합된 FMN 및 FAD와 함께 동물성 식품에 자연적으로 존재합니다.젖소의 우유는 주로 자유 리보플라빈을 함유하고 있지만 FMN과 FAD 둘 다 낮은 농도로 존재합니다.[35]
요새화
어떤 나라들은 곡물 식품의 강화를 요구하거나 권장합니다.[36]2021년 기준으로 56개국(북남미, 동남아프리카)은 밀가루 또는 옥수수(옥수수) 밀가루에 리보플라빈 또는 리보플라빈-5'-인산 나트륨을 첨가한 식품 강화를 요구하고 있습니다.규정된 양은 1.3mg/kg에서 5.75mg/kg 사이입니다.[37]추가적으로 16개국이 자발적인 요새화 프로그램을 가지고 있습니다.예를 들어, 인도 정부는 "마이다" (흰색) 밀가루와 "아타" (통밀) 밀가루에 대해 4.0 mg/kg을 권장합니다.[38]
흡수, 대사, 배설
식단에서 리보플라빈의 90% 이상은 단백질이 결합된 FMN과 FAD 형태입니다.[3]위의 위산에 노출되면 조효소가 방출되고, 조효소는 이어서 근위 소장에서 효소적으로 가수분해되어 유리 리보플라빈을 방출합니다.[39]
흡수는 급속 능동 수송 시스템을 통해 발생하며, 일부 추가 수동 확산은 고농도에서 발생합니다.[39]담즙염은 섭취를 촉진시켜 식사와 함께 비타민을 섭취하면 흡수력이 좋아집니다.[4][5]성인을 대상으로 한 소규모 임상시험에서 1회 투여로 흡수할 수 있는 리보플라빈의 최대량은 27mg이라고 보고했습니다.[39]새로 흡수된 리보플라빈의 대부분은 첫 번째 패스에서 간에 의해 차지되는데, 이는 혈장에서 리보플라빈의 식후 출현이 흡수를 과소평가할 수 있음을 나타냅니다.[5]RFVT1은 소장과 태반에 존재하며, RFVT2는 뇌와 침샘에서 높게 발현되며, RFVT3는 소장, 고환, 전립선에서 가장 높게 발현되는 세 가지 리보플라빈 수송 단백질이 확인되었습니다.[5][40]이러한 수송 단백질을 암호화하는 유전자에 돌연변이가 있는 유아는 경구로 리보플라빈을 투여하여 치료할 수 있습니다.[40]
리보플라빈은 FMN으로 가역적으로 전환된 후 FAD로 전환됩니다.리보플라빈에서 FMN으로 가는 것은 아연을 필요로 하는 리보플라빈 키나아제의 기능입니다; 그 반대는 포스파타아제에 의해 이루어집니다.FMN에서 FAD까지는 마그네슘을 필요로 하는 FAD 합성효소의 기능이며, 그 반대는 피로인산화효소에 의해 이루어집니다.FAD는 자신의 형성을 하향 조절하는 억제성 최종 산물인 것으로 보입니다.[5]
과다한 리보플라빈이 소장에 흡수되면 혈액에서 빠르게 제거돼 소변으로 배출됩니다.[5]소변 색깔은 수화 상태 바이오마커로 사용되며, 정상적인 조건에서는 소변 비중 및 소변 삼투압과 상관관계가 있습니다.[41]그러나 리보플라빈을 다량으로 보충하면 소변이 정상보다 더 노랗게 보입니다.[31]정상적인 식이 섭취를 할 경우, 요 생산량의 약 3분의 2는 리보플라빈이고, 나머지는 세포 내의 산화로부터 하이드록시메틸리보플라빈으로 부분적으로 대사되고, 다른 대사 물질로 대사됩니다.섭취량이 흡수 능력을 초과하면, 리보플라빈은 대장으로 전달되고, 대장에서 세균에 의해 대변에서 검출될 수 있는 다양한 대사 물질로 이화됩니다.[5]흡수되지 않은 리보플라빈이 대장 마이크로바이옴에 영향을 줄 수 있다는 추측이 있습니다.[42]
결핍증
유행
리보플라빈 결핍은 밀가루나 옥수수 식사 강화 프로그램이 있는 미국과 다른 나라에서 흔하지 않습니다.[37]미국 인구를 대상으로 한 2년에 한 번씩 실시하는 조사에서 20세 이상의 경우 여성의 22%, 남성의 19%가 일반적으로 비타민 미네랄 다중 보충제인 리보플라빈이 포함된 보충제를 섭취하고 있다고 보고했습니다.비보충제 사용자의 경우 성인 여성의 식이 섭취량은 평균 1.74 mg/일, 남성은 2.44 mg/일이었습니다.이 양은 리보플라빈의 RDA인 1.1mg/day와 1.3mg/day를 각각 초과합니다.[43]모든 연령대에서 평균적으로 음식 섭취가 RDA를 초과했습니다.[44]2001-02년 미국의 한 조사에 따르면 인구의 3% 미만이 리보플라빈의 평균 요구량 추정치보다 적은 양을 소비했다고 합니다.[45]
징후 및 증상
리보플라빈 결핍(리보플라빈증이라고도 함)은 구내염을 일으키는데, 그 증상으로는 입술이 트고 갈라지는 증상, 입꼬리의 염증(각성 구내염), 인후통, 붉은 혀의 고통, 탈모 등이 있습니다.[3]눈이 가렵고, 물기가 많고, 충혈되고, 빛에 민감해질 수 있습니다.[3]리보플라빈 결핍은 빈혈과 관련이 있습니다.[46]리보플라빈이 장기간 결핍되면 간과 신경계의 퇴화를 초래할 수 있습니다.[3][4]리보플라빈 결핍은 임산부에서 전폐증의 위험을 증가시킬 수 있습니다.[3][10]임신 중 리보플라빈의 결핍은 심장과 사지 기형을 포함한 태아의 선천적 결함을 초래할 수 있습니다.[47][48]
위험요소
낮은 리보플라빈 수치를 가질 위험이 있는 사람들은 알코올 중독자, 채식주의 운동선수, 채식주의자를 포함합니다.[3]만약 엄마가 고기와 유제품을 피한다면, 임신중이거나 수유중인 여성과 그들의 유아들 또한 위험에 처할 수 있습니다.[3][10]거식증과 유당불내증은 리보플라빈 결핍의 위험을 증가시킵니다.[10]운동선수나 노동자와 같이 육체적으로 힘든 삶을 사는 사람들은 더 많은 리보플라빈 섭취를 요구할 수 있습니다.[10]갑상샘기능저하증, 부신기능저하증, 리보플라빈 수송체 결핍증 환자에서 리보플라빈이 FAD와 FMN으로 전환되는 것은 장애가 됩니다.[10]
원인들
리보플라빈 결핍은 일반적으로 다른 영양소 결핍, 특히 다른 수용성 비타민과 함께 발견됩니다.[3]리보플라빈의 결핍은 1차적일 수 있고(즉, 정기적인 식단에서 비타민 공급원이 부족하여 발생할 수 있음) 또는 2차적일 수 있으며, 이는 장에서의 흡수에 영향을 미치는 조건의 결과일 수 있습니다.이차적인 결핍은 일반적으로 신체가 비타민을 사용할 수 없거나 비타민의 배설 비율이 증가함으로써 발생합니다.[10]결핍의 위험을 높이는 식단 패턴으로는 채식주의와 저유식 채식주의가 있습니다.[5]암, 심장병, 당뇨병과 같은 질병은 리보플라빈 결핍을 유발하거나 악화시킬 수 있습니다.[4]
리보플라빈의 흡수, 운반, 대사 또는 플라보 단백질에 의한 사용을 손상시키는 드문 유전적 결함이 있습니다.[40][49]이것들 중 하나는 이전에 브라운-비알레토-반 라레 증후군으로 알려진 리보플라빈 수송 결핍입니다.[40][49]트랜스포터 단백질 RDVT2와 RDVT3를 각각 코딩하는 유전자 SLC52A2와 SLC52A3의 변형이 결함입니다.[40][49]유아와 어린 아이는 근육 약화, 난청을 포함한 뇌신경 결손, 감각 무긴장증을 포함한 감각 증상, 섭식 장애, 감각 운동 축삭 신경병증 및 뇌신경 병리로 인한 호흡 장애를 가지고 있습니다.[49]치료를 받지 않을 때, 리보플라빈 수송기가 부족한 유아들은 숨쉬기가 힘들었고 생애 첫 10년 동안 죽을 위험이 있습니다.많은 양의 리보플라빈을 경구 보충하는 치료는 생명을 구하는 것입니다.[40][49]
대사의 다른 선천적 오류로는 글루타르산혈증 2형의 부분집합으로도 알려진 리보플라빈 반응성 다중 아실-CoA 탈수소효소 결핍, 성인의 경우 고혈압 위험과 관련이 있는 메틸에테트라하이드로폴산 환원효소의 C677T 변종 등이 있습니다.[5]
진단평가
리보플라빈 상태 평가는 결핍이 의심될 때마다 비특이적인 증상을 보이는 경우를 확인하는 데 필수적입니다.정상적인 리보플라빈 섭취가 있는 건강한 성인의 총 리보플라빈 배설량은 하루에 약 120마이크로그램인 반면, 하루에 40마이크로그램 미만의 배설량은 결핍을 나타냅니다.[3][50]리보플라빈 배설률은 사람이 나이가 들수록 감소하지만, 만성적인 스트레스와 일부 처방약의 사용 기간에는 증가합니다.[3]
인간에게 사용되는 지표는 적혈구 글루타티온 환원효소(EGR), 적혈구 플라빈 농도 및 소변 배설입니다.[4][5]적혈구 글루타티온 환원효소 활성 계수(EGRAC)는 조직 포화도와 장기 리보플라빈 상태를 측정할 수 있습니다.[50][3]결과는 배양 배지에 FAD를 첨가하거나 첨가하지 않은 효소 활성에 의해 결정되는 활성 계수 비율로 표시됩니다.EGRAC가 1.0 ~ 1.2이면 충분한 양의 리보플라빈이 존재함을 나타내며, 1.2 ~ 1.4는 부족한 것으로 간주됩니다.[3][5]덜 민감한 "적혈구 플라빈 방법"의 경우 400 nmol/L 이상의 값은 적합한 것으로 간주되고 270 nmol/L 미만의 값은 부족한 것으로 간주됩니다.[4][50]소변 배설은 크레아티닌 1g당 리보플라빈 nmol로 표현됩니다.Low는 50~72 nmol/g의 범위로 정의됩니다.결핍은 50 nmol/g 미만입니다.요로 배설 부하 테스트는 식이 요구 사항을 결정하는 데 사용되었습니다.성인 남성의 경우 경구 투여량이 0.5 mg에서 1.1 mg으로 증가함에 따라 소변 리보플라빈이 약간 선형적으로 증가하여 이후 24시간 소변 수집 시 100 마이크로그램에 도달했습니다.[4]1.1 mg의 부하 용량을 초과하면 소변 배설량이 급격히 증가하여 2.5 mg의 용량으로 24시간 소변 수집 시 800 마이크로그램의 소변 출력이 발생했습니다.[4]
역사
"리보플라빈"이라는 이름은 "리보스"(리비톨이 환원된 형태를 이루는 설탕)와 산화된 분자에 노란색을 부여하는 고리 부분인 "플라빈"(플라빈)에서 유래되었습니다.[5]산화된 형태와 함께 신진대사에서 일어나는 환원된 형태는 주황색-노란색의 바늘이나 결정체로 나타납니다.[8]비타민이 필수 영양소라는 개념보다 앞서 가장 먼저 보고된 것은 알렉산더 윈터 블라이스였습니다.1879년 블라이스는 젖소 우유의 수용성 성분을 분리해 냈고, 이 성분을 "락토크롬"이라고 이름 지었으며, 빛에 노출되면 황록색을 띠게 됩니다.[2]
1900년대 초, 몇몇 연구소들은 쥐의 성장을 유지하는데 필수적인 음식의 구성요소들을 조사하고 있었습니다.이들 성분은 처음에는 지용성 "비타민" A와 수용성 "비타민" B로 분류되었습니다. ("e"는 1920년에 떨어졌습니다.)[51]비타민 B는 열에 잘 견디는 물질인1 B와 열에 잘 견디는 물질인 B의2 두 가지 성분을 가지고 있다고 또한 생각되었습니다.[2]비타민 B는2 펠라그라 예방에 필요한 인자로 잠정적으로 밝혀졌지만, 그것은 나중에 니아신(비타민 B3) 결핍 때문인 것으로 확인되었습니다.혼란은 리보플라빈(B2) 결핍이 펠라그라에서 볼 수 있는 것과 유사한 구내염 증상을 유발하지만 광범위한 말초 피부 병변이 없기 때문입니다.이러한 이유로, 인간의 리보플라빈 결핍을 확인한 역사 초기에, 그 상태는 때때로 "펠라그라 사인 펠라그라" (펠라그라가 없는 펠라그라)라고 불렸습니다.[52]
1935년, 폴 교기는 화학자 리차드 쿤과 의사 T와 공동으로 연구했습니다.Wagner-Jaureg는 B가 없는2 식단을 유지하는 쥐들이 살을 찌울 수 없다고 보고했습니다.[53]효모로부터 B를2 분리하면 쥐에게 먹였을 때 정상적인 성장을 회복하는 밝은 황록색 형광 제품의 존재를 알 수 있었습니다.복원된 성장은 형광의 강도에 정비례했습니다.이 관찰은 연구자들이 1933년에 급속 화학 생물 분석법을 개발하고 난백에서 그 인자를 분리할 수 있게 했고, 그것을 오보플라빈이라고 불렀습니다.[2]그리고 나서 같은 그룹이 유청으로부터 유사한 제제를 분리하고 락토플라빈이라고 불렀습니다.1934년, 쿤의 그룹은 이 플라빈들의 화학적 구조가 동일하다는 것을 확인했고, "리보플라빈"을 이름으로 정했고, 또한 비타민을 합성할 수 있었습니다.[2]
1937년경, 리보플라빈은 "비타민 G"라고도 불렸습니다.[54]1938년, Richard Kun은 B와2 B를6 포함한 비타민에 대한 연구로 노벨 화학상을 수상했습니다.[55]1939년 윌리엄 H. 세브렐(William H. Sebrell)과 로이 E. 버틀러(Roy E. Butler)가 진행한 임상시험을 통해 리보플라빈이 인간의 건강에 필수적임을 확인했습니다.리보플라빈이 적은 식단을 먹은 여성들은 구내염과 다른 결핍의 징후들이 생겼고, 이것들은 합성 리보플라빈으로 치료했을 때 역전되었습니다.보충제가 중단되었을 때 증상이 다시 나타났습니다.[2]
참고문헌
- ^ a b "Riboflavin". Drugs.com. 22 July 2021. Retrieved 8 October 2021.
- ^ a b c d e f Northrop-Clewes CA, Thurnham DI (2012). "The discovery and characterization of riboflavin". Annals of Nutrition & Metabolism. 61 (3): 224–30. doi:10.1159/000343111. PMID 23183293. S2CID 7331172.
- ^ a b c d e f g h i j k l m n o p q r s t u "Riboflavin: Fact Sheet for Health Professionals". Office of Dietary Supplements, US National Institutes of Health. 11 May 2022. Retrieved 20 August 2023.
- ^ a b c d e f g h i j k l m n o Institute of Medicine (1998). "Riboflavin". Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, DC: The National Academies Press. pp. 87–122. ISBN 978-0-309-06554-2. Archived from the original on 17 July 2015. Retrieved 29 August 2017.
- ^ a b c d e f g h i j k l m n o Merrill AH, McCormick DB (2020). "Riboflavin". In BP Marriott, DF Birt, VA Stallings, AA Yates (eds.). Present Knowledge in Nutrition, Eleventh Edition. London, United Kingdom: Academic Press (Elsevier). pp. 189–208. ISBN 978-0-323-66162-1.
- ^ a b Lienhart WD, Gudipati V, Macheroux P (July 2013). "The human flavoproteome". Archives of Biochemistry and Biophysics. 535 (2): 150–62. doi:10.1016/j.abb.2013.02.015. PMC 3684772. PMID 23500531.
- ^ Macheroux P, Kappes B, Ealick SE (August 2011). "Flavogenomics--a genomic and structural view of flavin-dependent proteins". The FEBS Journal. 278 (15): 2625–34. doi:10.1111/j.1742-4658.2011.08202.x. PMID 21635694. S2CID 22220250.
- ^ a b c d "Riboflavin". PubChem, US National Library of Medicine. 9 October 2021. Retrieved 15 October 2021.
- ^ a b Mewies M, McIntire WS, Scrutton NS (1998). "Covalent attachment of flavin adenine dinucleotide (FAD) and flavin mononucleotide (FMN) to enzymes: The current state of affairs". Protein Science. 7 (1): 7–20. doi:10.1002/pro.5560070102. PMC 2143808. PMID 9514256.
- ^ a b c d e f g h i j "Riboflavin". Micronutrient Information Center, Linus Pauling Institute, Oregon State University. 2013. Retrieved 8 October 2021.
- ^ Fishman SM, Christian P, West KP (June 2000). "The role of vitamins in the prevention and control of anaemia". Public Health Nutr. 3 (2): 125–50. doi:10.1017/s1368980000000173. PMID 10948381.
- ^ a b Fischer M, Bacher A (2008). "Biosynthesis of vitamin B2: Structure and mechanism of riboflavin synthase". Archives of Biochemistry and Biophysics. 474 (2): 252–265. doi:10.1016/j.abb.2008.02.008. PMID 18298940.
- ^ a b c Caspi R (17 March 2009). "Pathway: flavin biosynthesis III (fungi)". MetaCyc Metabolic Pathway Database. Retrieved 21 November 2021.
- ^ Wei Y, Kumar P, Wahome N, Mantis NJ, Middaugh CR (2018). "Biomedical Applications of Lumazine Synthase". Journal of Pharmaceutical Sciences. 107 (9): 2283–96. doi:10.1016/j.xphs.2018.05.002. PMID 29763607. S2CID 21729139.
- ^ Devlin TM (2011). Textbook of Biochemistry: with Clinical Correlations (7th ed.). Hoboken, NJ: John Wiley & Sons. ISBN 978-0-470-28173-4.
- ^ a b Sims GK, O'loughlin EJ (October 1992). "Riboflavin Production during Growth of Micrococcus luteus on Pyridine". Applied and Environmental Microbiology. 58 (10): 3423–5. Bibcode:1992ApEnM..58.3423S. doi:10.1128/AEM.58.10.3423-3425.1992. PMC 183117. PMID 16348793.
- ^ Stahmann KP, Revuelta JL, Seulberger H (May 2000). "Three biotechnical processes using Ashbya gossypii, Candida famata, or Bacillus subtilis compete with chemical riboflavin production". Applied Microbiology and Biotechnology. 53 (5): 509–16. doi:10.1007/s002530051649. PMID 10855708. S2CID 2471994.
- ^ a b Eggersdorfer M, Laudert D, Létinois U, McClymont T, Medlock J, Netscher T, Bonrath W (December 2012). "One hundred years of vitamins-a success story of the natural sciences". Angewandte Chemie. 51 (52): 12960–12990. doi:10.1002/anie.201205886. PMID 23208776.
- ^ Kuhn R, Reinemund K, Weygand F, Ströbele R (1935). "Über die Synthese des Lactoflavins (Vitamin B 2 )". Berichte der Deutschen Chemischen Gesellschaft (A and B Series) (in German). 68 (9): 1765–1774. doi:10.1002/cber.19350680922.
- ^ Mastropasqua L (2015). "Collagen cross-linking: when and how? A review of the state of the art of the technique and new perspectives". Eye and Vision. 2: 19. doi:10.1186/s40662-015-0030-6. PMC 4675057. PMID 26665102.
- ^ Sorkin N, Varssano D (June 2014). "Corneal collagen crosslinking: a systematic review". Ophthalmologica. 232 (1): 10–27. doi:10.1159/000357979. PMID 24751584. S2CID 32696531.
- ^ Holland S, Silberstein SD, Freitag F, Dodick DW, Argoff C, Ashman E (April 2012). "Evidence-based guideline update: NSAIDs and other complementary treatments for episodic migraine prevention in adults: report of the Quality Standards Subcommittee of the American Academy of Neurology and the American Headache Society". Neurology. 78 (17): 1346–53. doi:10.1212/wnl.0b013e3182535d0c. PMC 3335449. PMID 22529203.
- ^ ""Natural" remedies for migraine – should I try them?". UK National Migraine Centre. 2021. Retrieved 8 October 2021.
- ^ a b Thompson DF, Saluja HS (August 2017). "Prophylaxis of migraine headaches with riboflavin: A systematic review". Journal of Clinical Pharmacy and Therapeutics. 42 (4): 394–403. doi:10.1111/jcpt.12548. PMID 28485121. S2CID 29848028.
- ^ Sherwood M, Goldman RD (March 2014). "Effectiveness of riboflavin in pediatric migraine prevention". Canadian Family Physician. 60 (3): 244–6. PMC 3952759. PMID 24627379.
- ^ a b "Approved additives and E numbers". food.gov.uk. UK Food Standards Agency. 10 August 2023. Retrieved 20 August 2023.
- ^ a b Gropper SS, Smith JL, Groff JL (2009). "Ch. 9: Riboflavin". Advanced Nutrition and Human Metabolism (5th ed.). Wadsworth: CENGAG Learning. pp. 329–33. ISBN 9780495116578.
- ^ Turck D, Bresson JL, Burlingame B, Dean T, Fairweather-Tait S, Heinonen M, et al. (August 2017). "Dietary Reference Values for riboflavin". EFSA J. 15 (8): e04919. doi:10.2903/j.efsa.2017.4919. PMC 7010026. PMID 32625611.
- ^ a b "Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies" (PDF). 2017. Archived (PDF) from the original on 28 August 2017.
- ^ "Tolerable Upper Intake Levels For Vitamins And Minerals" (PDF). European Food Safety Authority. 2006. Archived (PDF) from the original on 16 March 2016.
- ^ a b "Riboflavin (Oral Route)". Mayo Clinic. February 2021. Retrieved 28 October 2021.
- ^ "Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982" (PDF). Archived (PDF) from the original on 8 August 2016.
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Archived from the original on 7 April 2020. Retrieved 16 May 2020.
- ^ a b c d "USDA Food Composition Databases; Food Search; SR Legacy Foods". United States Department of Agriculture, Agricultural Research Service. Release 28. 7 May 2019. Retrieved 28 November 2021.
- ^ Kanno C, Kanehara N, Shirafuji K, Tanji R, Imai T (February 1991). "Binding form of vitamin B2 in bovine milk: its concentration, distribution and binding linkage". Journal of Nutritional Science and Vitaminology. 37 (1): 15–27. doi:10.3177/jnsv.37.15. PMID 1880629.
- ^ "What nutrients are added to flour and rice in fortification?". Food Fortification Initiative. 2021. Retrieved 8 October 2021.
- ^ a b "Map: Count of Nutrients In Fortification Standards". Global Fortification Data Exchange. Retrieved 11 October 2021.
- ^ "Direction under Section 16(5) of Foods Safety and Standards Act, 2006 regarding Operationalisation of Food Safety & Standards (Fortification of Foods) Regulations, 2017 relating to standards for fortification of food" (PDF). Food Safety & Standards Authority of India (FSSAI). 19 May 2017. Retrieved 30 November 2021.
- ^ a b c Zempleni J, Galloway JR, McCormick DB (January 1996). "Pharmacokinetics of orally and intravenously administered riboflavin in healthy humans". American Journal of Clinical Nutrition. 63 (1): 54–66. doi:10.1093/ajcn/63.1.54. PMID 8604671.
- ^ a b c d e f Jaeger B, Bosch AM (July 2016). "Clinical presentation and outcome of riboflavin transporter deficiency: mini review after five years of experience". Journal of Inherited Metabolic Disease. 39 (4): 559–64. doi:10.1007/s10545-016-9924-2. PMC 4920840. PMID 26973221.
- ^ Ellis LA, Yates BA, McKenzie AL, Muñoz CX, Casa DJ, Armstrong LE (August 2016). "Effects of Three Oral Nutritional Supplements on Human Hydration Indices". Int J Sport Nutr Exerc Metab. 26 (4): 356–62. doi:10.1123/ijsnem.2015-0244. PMID 26731792.
- ^ Steinert RE, Sadaghian Sadabad M, Harmsen HJ, Weber P (December 2016). "The prebiotic concept and human health: a changing landscape with riboflavin as a novel prebiotic candidate?". Eur J Clin Nutr. 70 (12): 1348–1353. doi:10.1038/ejcn.2016.119. PMID 27380884. S2CID 29319823.
- ^ "Total Nutrient Intakes: Percent Reporting and Mean Amounts of Selected Vitamins and Minerals from Food and Beverages and Dietary Supplements, by Gender and Age, What We Eat in America, NHANES 2017-2018" (PDF). U.S. Department of Agriculture, Agricultural Research Service. 2020. Retrieved 24 October 2021.
- ^ "Nutrient Intakes from Food and Beverages: Mean Amounts Consumed per Individual, by Gender and Age, What We Eat in America, NHANES 2017-2018" (PDF). U.S. Department of Agriculture, Agricultural Research Service. 2020. Retrieved 24 October 2021.
- ^ Moshfegh A, Goldman J, Cleveland L (September 2005). "What We Eat in America 2001-2002: Usual Nutrient Intakes from Food Compared to Dietary Reference Intakes" (PDF). U.S. Department of Agriculture, Agricultural Research Service. Retrieved 24 October 2021.
- ^ Thakur K, Tomar SK, Singh AK, Mandal S, Arora S (November 2017). "Riboflavin and health: A review of recent human research". Crit Rev Food Sci Nutr. 57 (17): 3650–3660. doi:10.1080/10408398.2016.1145104. PMID 27029320. S2CID 205692748.
- ^ Smedts HP, Rakhshandehroo M, Verkleij-Hagoort AC, de Vries JH, Ottenkamp J, Steegers EA, Steegers-Theunissen RP (October 2008). "Maternal intake of fat, riboflavin and nicotinamide and the risk of having offspring with congenital heart defects". European Journal of Nutrition. 47 (7): 357–65. doi:10.1007/s00394-008-0735-6. PMID 18779918. S2CID 25548935.
- ^ Robitaille J, Carmichael SL, Shaw GM, Olney RS (September 2009). "Maternal nutrient intake and risks for transverse and longitudinal limb deficiencies: data from the National Birth Defects Prevention Study, 1997-2003". Birth Defects Research. Part A, Clinical and Molecular Teratology. 85 (9): 773–9. doi:10.1002/bdra.20587. PMID 19350655.
- ^ a b c d e Cali E, Dominik N, Manole A, Houlden H (8 April 2021). "Riboflavin transporter deficiency". GeneReviews (Adam MP, Ardinger HH, Pagon RA, et Al., Editors). University of Washington, Seattle. PMID 26072523.
- ^ a b c Hoey L, McNulty H, Strain JJ (June 2009). "Studies of biomarker responses to intervention with riboflavin: a systematic review". The American Journal of Clinical Nutrition. 89 (6): 1960S–1980S. doi:10.3945/ajcn.2009.27230b. PMID 19403631.
- ^ Rosenfeld L (1997). "Vitamine—vitamin. The early years of discovery". Clinical Chemistry. 43 (4): 680–685. doi:10.1093/clinchem/43.4.680. PMID 9105273.
- ^ Sebrell WH, Butler RE (1939). "Riboflavin Deficiency in Man (Ariboflavinosis)". Public Health Reports. 54 (48): 2121–31. doi:10.2307/4583104. JSTOR 4583104.
- ^ György P (March 1935). "Investigations on the vitamin B(2) complex: The differentiation of lactoflavin and the "rat antipellagra" factor". The Biochemical Journal. 29 (3): 741–759. doi:10.1042/bj0290741. PMC 1266542. PMID 16745720.
- ^ Levine H, Remington RE (May 1937). "The Vitamin G Content of Some Foods". J Nutr. 13 (5): 525–42. doi:10.1093/jn/13.5.525.
- ^ "The Nobel Prize in Chemistry 1938". Nobelprize.org. Retrieved 5 July 2018.