HER2
HER2수용체 tyrosine-protein kinase erbB-2는 보통 세포의 막에 존재하는 단백질로 ERBB2 유전자에 의해 암호화됩니다.ERBB는 원래 조류 게놈에서 분리된 유전자인 적혈구 생성 종양 유전자 B로부터 약칭됩니다.인간 단백질은 일반적으로 HER2(인간 표피 성장 인자 수용체 2) 또는 CD340(분화 클러스터 340)이라고도 합니다.[5][6][7]
HER2는 인체 표피 성장인자 수용체(HER/EGFR/ERBB) 계열의 일원입니다.그러나 ERBB 계열의 다른 구성원들과는 달리, HER2는 리간드에 직접적으로 결합하지 않습니다.HER2 활성화는 암과 같은 HER2 농도가 높을 때 다른 ERBB 멤버와의 이종이중화 또는 동종이중화에 의해 발생합니다.[8]이 종양 유전자의 증폭 또는 과발현은 특정 공격형 유방암의 발생과 진행에 중요한 역할을 하는 것으로 나타났습니다.최근 몇 년 동안 단백질은 유방암 환자의 약 30%에게 중요한 바이오마커이자 치료의 대상이 되었습니다.[9]
이름.
HER2는 인간 표피 성장 인자 수용체, 즉 HER1과 유사한 구조를 가지고 있기 때문에 그렇게 이름 붙여졌습니다.뇌는 신경 종양의 한 종류인 설치류 교모세포종 세포주에서 유래되었기 때문에 그렇게 이름 붙여졌습니다.ErbB-2는 나중에 EGFR을 코딩하는 것으로 발견된 종양 유전자인 ErbB(조류 적혈구 생성 종양 유전자 B)와 유사하여 이름 지어졌습니다.유전자의 분자 복제는 HER2, Neu, 그리고 ErbB-2가 모두 같은 오르톨로그에 의해 암호화된다는 것을 보여주었습니다.[10]
유전자
인간 염색체 17번 (17q12)의 긴 팔에 있는, 알려진 원생균인 ERBB2.
기능.
ErbB 계열은 4개의 개별 혈장 막 결합 수용체 티로신 키나제로 구성되어 있습니다.그 중 하나는 erbB-2이고, 다른 멤버는 erbB-1, erbB-3 (뉴레굴린-결합; 키나아제 도메인이 결여됨), 및 erbB-4입니다.4개 모두 세포외 리간드 결합 도메인, 막횡단 도메인, 및 리간드 의존적 및 리간드 비의존적 활성을 나타낼 수 있는 세포내 도메인을 포함합니다.특히 HER2에 대한 리간드는 아직 확인되지 않았습니다.[11][12]HER2는 다른 세 수용체 중 어느 하나와 이종이중화될 수 있으며, 다른 ErbB 수용체의 선호되는 이중화 파트너로 간주됩니다.[13]
이량체화는 수용체의 세포질 영역 내에서 티로신 잔기의 자가인산화를 초래하고 다양한 신호 경로를 개시합니다.
신호전달
HER2에 의해 활성화되는 신호 경로는 다음과 같습니다.[14]
- 미토겐 활성화 단백질 키나아제(MAPK)
- 포스포이노시티드 3-키나아제 (PI3K/Akt)
- 포스포리파아제 C c
- 단백질 키나아제 C (PKC)
- 신호 변환기 및 전사활성화기(STAT)
요약하면, ErbB 수용체 계열을 통한 신호 전달은 세포 증식을 촉진하고 세포 자멸을 반대하므로, 조절되지 않는 세포 성장이 일어나지 않도록 엄격하게 조절되어야 합니다.
임상적 의의
암
ERBB2 유전자의 과발현으로도 알려진 증폭은 유방암의 약 15-30%에서 발생합니다.[9][15]HER2 양성 유방암은 다른 유방암과 관련이 있을 것으로 생각되는 다른 유전적으로 구별되는 다른 유방암과 비교하여 질병 재발 증가 및 불량한 예후와 관련이 있는 것으로 잘 알려져 있으나,유방암에서 HER2를 표적으로 하는 약물제는 HER2 양성 유방암과 관련된 역사적으로 문제가 되었던 어려움의 좋지 않은 예후를 유의하고 긍정적으로 변화시켰습니다.[16]과발현은 또한 난소,[17] 위, 폐의[18] 선암 및 자궁 장액성 자궁내막암과 같은 공격적인 형태의 자궁암에서도 발생하는 것으로 알려져 있습니다.[19][20] 예를 들어, HER2는 위암[21][22] 환자의 약 7-34%와 침관암의 30%에서 과발현됩니다.[23]
HER2는 공국적이고 대부분의 경우 유방, 고환 생식 세포, 위, 식도 종양과 관련된 원생균 유전자인 GRB7과 증폭됩니다.
HER2 단백질은 종양 발생에 역할을 할 수 있는 세포막에 클러스터를 형성하는 것으로 나타났습니다.[24][25]
증거는 또한 EGFR 표적 암 약물인 세툭시맙에 대한 내성에서 HER2 신호전달을 포함하고 있습니다.[26]
HER2의 높은 발현은 식도 선암에서 더 나은 생존과 관련이 있습니다.[27]
HER2 복사 번호의 높은 증폭은 위 심장 선암 환자의 생존 시간에 긍정적으로 기여합니다.[28]
돌연변이
또한, 수용체 과발현이 없는 경우에 리간드 독립적인 이 수용체의 발화를 유발하는 다양한 구조적 변화가 확인되었습니다.HER2는 다양한 종양에서 발견되며 이러한 종양 중 일부는 HER2의 막 횡단 영역을 지정하는 시퀀스에서 점 돌연변이를 운반합니다.막간 영역에서 글루탐산 또는 글루탐산에 대한 발린의 대체는 리간드가 없을 때 이 단백질의 구성 이량체화를 초래할 수 있습니다.[29]
HER2 돌연변이는 비소세포폐암(NSCLC)에서 발견되었으며 치료를 직접 할 수 있습니다.[30]
마약 표적으로
HER2는 단일클론항체 트라스투주맙(Herceptin으로 시판됨)의 표적입니다.트라스투주맙은 HER2가 과발현된 암에서만 효과가 있습니다.항암치료를 받고 있는 모든 HER2 양성 유방암 환자들에게 트라스투주맙 치료기간은 1년이 권장됩니다.[31]12개월간의 트라스투주맙 치료가 최적입니다.무작위 실험에서는 12개월을 초과하는 추가적인 이점이 없는 반면, 6개월은 12개월보다 낮은 것으로 나타났습니다.트라스투주맙은 매주 또는 3주마다 정맥주사를 투여합니다.[32]
HER2에 대한 트라스투주맙 결합의 중요한 하류 효과는 세포 증식을 중단시키는 단백질인 p27의 증가입니다.[33]HER2 및 HER3 수용체의 이량체화를 억제하는 또 다른 단일클론항체인 페르투주맙은 2012년 6월 FDA에 의해 트라스투주맙과 병용 사용을 승인받았습니다.
2015년 11월 현재, HER2+ 전이성 유방암, 예를 들어, margetuximab에 대한 신규한 표적화제의 임상시험이 진행 중이고 최근에 완료된 다수의 임상시험이 있습니다.[34]
또한, NeuVax(Galena Biopharma)는 펩타이드 기반의 면역치료제로, '킬러' T세포가 HER2를 발현하는 암세포를 표적 및 파괴하도록 유도합니다.임상 3상에 진입했습니다.
ER-/HER2+ 유방암에 비해 ER+(Estrogen receptor positive)/HER2+를 가진 환자는 PI3K/AKT 분자 경로를 억제하는 약물로부터 실제로 더 많은 이득을 얻을 수 있다는 것이 밝혀졌습니다.[35]
HER2의 과발현은 다른 유전자의 증폭에 의해서도 억제될 수 있습니다.어떤 유전자가 이런 바람직한 효과를 가질 수 있는지를 찾기 위한 연구가 현재 진행되고 있습니다.
HER2의 발현은 에스트로겐 수용체를 통한 신호전달에 의해 조절됩니다.일반적으로 에스트로겐 수용체를 통해 작용하는 에스트라디올과 타목시펜은 HER2의 발현을 하향 조절합니다.그러나, AIB-3의 coactivator 비율이 corepressor PAX2의 비율을 초과하는 경우, 타목시펜의 존재하에서 HER2의 발현이 상향조절되어 타목시펜 저항성 유방암이 발생하게 됩니다.[36][37]
승인된 항-HER2 치료제 중에는 또한 티로신 키나아제 억제제(lapatinib, neratinib 및 tucatinib) 및 항체-약물 접합체(ado-trastuzumab emtansine 및 trastuzumab deruxecan)가 있습니다.[38]

진단
유방암 환자의 유방생검에서 HER2 검사를 시행하여 예후를 평가하고 트라스투주맙 치료의 적합성을 판단합니다.트라스투주맙은 가격이 비싸고 심장 독성과 관련이 있기 때문에 HER2 양성 개체로 제한되는 것이 중요합니다.[39]HER2 양성 종양의 경우, 트라스투주맙의 이점이 위험을 분명히 능가합니다.
검사는 일반적으로 세침 흡인술, 핵심 바늘 생검, 진공 보조 유방 생검 또는 외과적 절제술로 얻은 유방 생검 샘플에 대해 수행됩니다.
면역조직화학(IHC)은 일반적으로 샘플에 존재하는 HER2 단백질의 양을 측정하는 데 사용되며, IHC에서 모호한 샘플에 형광 인 시츄 혼성화(FISH)가 사용됩니다.그러나 몇몇 장소에서는 처음에는 FISH가 사용되고, 다음에는 애매모호한 경우에 IHC가 사용됩니다.[40]
면역조직화학
면역조직화학에 의해, 샘플은 세포막 염색 패턴에 기초한 점수를 받습니다.
| 스코어[41][42] | 패턴[43] | 상태[41][42] |
|---|---|---|
| 0 | 둘 중 하나:[43]
| HER2 음성 (존재하지 않음) |
| 1+ | 희미하거나 거의 감지되지 않는 불완전한 막 얼룩으로 침습성 종양 세포의 10% 이내입니다.[43] | |
| 2+ | 종양 세포의 >10%에서 관찰되는 약하거나 중간 정도의 완전한 막 얼룩.[43] | 경계선/등초점 |
| 3+ | 종양 세포의 10% 이상에서 완전하고 강도가 높은 원주형 막 염색.[43] | HER2 양성 |
각 점수를 보여주는 현미경 사진:[44]
-
0
-
1+
-
2+
-
3+
형광 in situ hybridization
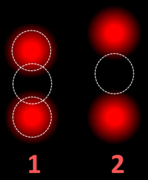
FISH는 면역조직화학보다 더 신뢰할 수 있고 존재하는 유전자의 복제의 수를 측정하는데 사용될 수 있습니다.[45]이것은 보통 염색체의 양을 세기 위해 염색체 열거 탐침 17 (CEP17)을 사용합니다.따라서, HER2/CEP17 비율은 염색체 수와 비교하여 HER2의 증폭을 반영합니다.20개의 세포의 신호는 보통 세어집니다.
-
이 셀은 HER2(빨간색)의 신호 2개와 CEP17(녹색)의 신호 3개를 표시합니다.
-
신호 직경보다 서로 가까운 두 개의 신호는 하나로 계산됩니다.
-
이 신호들 중 하나는 너무 희미하고, 아마도 파편일 것입니다.
-
한 가지 유형의 신호만 있는 셀은 카운트에서 제외됩니다.
-
중복되는 셀도 카운트에서 제외됩니다.
-
노란색 신호는 빨간색과 녹색(중복)으로 계산됩니다.
-
-
FIX(Situ Hybridization)[46]의 형광에 대한 HER2 평가 알고리즘
| HER2/CEP17 비율 | |||
|---|---|---|---|
| ≥2.0 | <2.0 | ||
| 셀당 평균 HER2 복사 수 | ≥4.0 | HER2 양성 | 추가적인 작업이 필요 |
| <4.0 | 추가적인 작업이 필요 | HER2 음성 | |
초기 HER2 결과가 원발성 유방암의 바늘 생검에 음성인 경우, 이후 유방 절제술에 대해 새로운 HER2 검사를 수행할 수 있습니다.[46]
세럼
HER2의 세포외 도메인은 종양 세포의 표면으로부터 떨어져 나와 순환으로 들어갈 수 있습니다.효소-결합 면역흡수제 검사(ELISA)에 의한 혈청 HER2의 측정은 조직 검사보다 HER2 상태를 결정하는 훨씬 덜 침습적인 방법을 제공하여 결과적으로 광범위하게 조사되었습니다.지금까지의 결과는 혈청 HER2 농도의 변화가 트라스투주맙 치료에 대한 반응을 예측하는 데 유용할 수 있음을 시사했습니다.[47]그러나 트라스투주맙 치료의 적격성을 판단하는 능력은 덜 명확합니다.[48]
상호작용
HER2/neu는 다음과 상호 작용하는 것으로 나타났습니다.
참고 항목
참고문헌
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000141736 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG00000062312 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "ERBB2 erb-b2 receptor tyrosine kinase 2 [Homo sapiens (human)] - Gene - NCBI". www.ncbi.nlm.nih.gov. Retrieved 2016-06-14.
- ^ "ERBB2". Genetics Home Reference. Retrieved 2016-06-19.
- ^ Barh D, Gunduz M (2015-01-22). Noninvasive Molecular Markers in Gynecologic Cancers. CRC Press. p. 427. ISBN 9781466569393.
- ^ Hsu JL, Hung MC (2016). "The role of HER2, EGFR, and other receptor tyrosine kinases in breast cancer". Cancer and Metastasis Reviews. 35 (4): 575–588. doi:10.1007/s10555-016-9649-6. PMC 5215954. PMID 27913999.
- ^ a b Mitri Z, Constantine T, O'Regan R (2012). "The HER2 Receptor in Breast Cancer: Pathophysiology, Clinical Use, and New Advances in Therapy". Chemotherapy Research and Practice. 2012: 743193. doi:10.1155/2012/743193. PMC 3539433. PMID 23320171.
- ^ Coussens L, Yang-Feng TL, Liao YC, Chen E, Gray A, McGrath J, et al. (December 1985). "Tyrosine kinase receptor with extensive homology to EGF receptor shares chromosomal location with neu oncogene". Science. 230 (4730): 1132–1139. Bibcode:1985Sci...230.1132C. doi:10.1126/science.2999974. PMID 2999974.
- ^ Keshamouni VG, Mattingly RR, Reddy KB (June 2002). "Mechanism of 17-beta-estradiol-induced Erk1/2 activation in breast cancer cells. A role for HER2 AND PKC-delta". The Journal of Biological Chemistry. 277 (25): 22558–22565. doi:10.1074/jbc.M202351200. PMID 11960991.
- ^ Rusnak DW, Affleck K, Cockerill SG, Stubberfield C, Harris R, Page M, et al. (October 2001). "The characterization of novel, dual ErbB-2/EGFR, tyrosine kinase inhibitors: potential therapy for cancer". Cancer Research. 61 (19): 7196–7203. PMID 11585755.
- ^ Olayioye MA (2001). "Update on HER-2 as a target for cancer therapy: intracellular signaling pathways of ErbB2/HER-2 and family members". Breast Cancer Research. 3 (6): 385–389. doi:10.1186/bcr327. PMC 138705. PMID 11737890.
- ^ Roy V, Perez EA (November 2009). "Beyond trastuzumab: small molecule tyrosine kinase inhibitors in HER-2-positive breast cancer". The Oncologist. 14 (11): 1061–1069. doi:10.1634/theoncologist.2009-0142. PMID 19887469. S2CID 207242039.
- ^ Burstein HJ (October 2005). "The distinctive nature of HER2-positive breast cancers". The New England Journal of Medicine. 353 (16): 1652–1654. doi:10.1056/NEJMp058197. PMID 16236735. S2CID 26675265.
- ^ Tan M, Yu D (2007). "Molecular Mechanisms of ErbB2-Mediated Breast Cancer Chemoresistance". Breast Cancer Chemosensitivity. Advances in Experimental Medicine and Biology. Vol. 608. pp. 119–29. doi:10.1007/978-0-387-74039-3_9. ISBN 978-0-387-74037-9. PMID 17993237.
- ^ Kumar V, Abbas A, Aster J (2013). Robbins basic pathology. Philadelphia: Elsevier/Saunders. p. 697. ISBN 9781437717815.
- ^ Kumar V, Abbas A, Aster J (2013). Robbins basic pathology. Philadelphia: Elsevier/Saunders. p. 179. ISBN 9781437717815.
- ^ Santin AD, Bellone S, Roman JJ, McKenney JK, Pecorelli S (August 2008). "Trastuzumab treatment in patients with advanced or recurrent endometrial carcinoma overexpressing HER2/neu". International Journal of Gynaecology and Obstetrics. 102 (2): 128–131. doi:10.1016/j.ijgo.2008.04.008. PMID 18555254. S2CID 25674060.
- ^ Buza N, Roque DM, Santin AD (March 2014). "HER2/neu in Endometrial Cancer: A Promising Therapeutic Target With Diagnostic Challenges". Archives of Pathology & Laboratory Medicine. 138 (3): 343–350. doi:10.5858/arpa.2012-0416-RA. PMID 24576030.
- ^ Rüschoff J, Hanna W, Bilous M, Hofmann M, Osamura RY, Penault-Llorca F, et al. (May 2012). "HER2 testing in gastric cancer: a practical approach". Modern Pathology. 25 (5): 637–650. doi:10.1038/modpathol.2011.198. PMID 22222640.
- ^ Meza-Junco J, Au HJ, Sawyer MB (March 2011). "Critical appraisal of trastuzumab in treatment of advanced stomach cancer". Cancer Management and Research. 3 (3): 57–64. doi:10.2147/CMAR.S12698. PMC 3085240. PMID 21556317.
- ^ Chiosea SI, Williams L, Griffith CC, Thompson LD, Weinreb I, Bauman JE, et al. (June 2015). "Molecular characterization of apocrine salivary duct carcinoma". The American Journal of Surgical Pathology. 39 (6): 744–752. doi:10.1097/PAS.0000000000000410. PMID 25723113. S2CID 34106002.
- ^ Nagy P, Jenei A, Kirsch AK, Szöllosi J, Damjanovich S, Jovin TM (June 1999). "Activation-dependent clustering of the erbB2 receptor tyrosine kinase detected by scanning near-field optical microscopy". Journal of Cell Science. 112 ( Pt 11) (11): 1733–1741. doi:10.1242/jcs.112.11.1733. hdl:2437/166028. PMID 10318765.
- ^ Kaufmann R, Müller P, Hildenbrand G, Hausmann M, Cremer C (April 2011). "Analysis of Her2/neu membrane protein clusters in different types of breast cancer cells using localization microscopy". Journal of Microscopy. 242 (1): 46–54. doi:10.1111/j.1365-2818.2010.03436.x. PMID 21118230. S2CID 2119158.
- ^ Yonesaka K, Zejnullahu K, Okamoto I, Satoh T, Cappuzzo F, Souglakos J, et al. (September 2011). "Activation of ERBB2 signaling causes resistance to the EGFR-directed therapeutic antibody cetuximab". Science Translational Medicine. 3 (99): 99ra86. doi:10.1126/scitranslmed.3002442. PMC 3268675. PMID 21900593.
- ^ Plum PS, Gebauer F, Krämer M, Alakus H, Berlth F, Chon SH, et al. (January 2019). "HER2/neu (ERBB2) expression and gene amplification correlates with better survival in esophageal adenocarcinoma". BMC Cancer. 19 (1): 38. doi:10.1186/s12885-018-5242-4. PMC 6325716. PMID 30621632.
- ^ Zhao XK, Xing P, Song X, Zhao M, Zhao L, Dang Y, et al. (November 2021). "Focal amplifications are associated with chromothripsis events and diverse prognoses in gastric cardia adenocarcinoma". Nature Communications. 12 (1): 6489. Bibcode:2021NatCo..12.6489Z. doi:10.1038/s41467-021-26745-3. PMC 8586158. PMID 34764264.
- ^ Brandt-Rauf PW, Rackovsky S, Pincus MR (November 1990). "Correlation of the structure of the transmembrane domain of the neu oncogene-encoded p185 protein with its function". Proceedings of the National Academy of Sciences of the United States of America. 87 (21): 8660–8664. Bibcode:1990PNAS...87.8660B. doi:10.1073/pnas.87.21.8660. PMC 55017. PMID 1978329.
- ^ Mazières J, Peters S, Lepage B, Cortot AB, Barlesi F, Beau-Faller M, et al. (June 2013). "Lung cancer that harbors an HER2 mutation: epidemiologic characteristics and therapeutic perspectives". Journal of Clinical Oncology. 31 (16): 1997–2003. doi:10.1200/JCO.2012.45.6095. PMID 23610105. S2CID 37663670.
- ^ Mates M, Fletcher GG, Freedman OC, Eisen A, Gandhi S, Trudeau ME, Dent SF (March 2015). "Systemic targeted therapy for her2-positive early female breast cancer: a systematic review of the evidence for the 2014 Cancer Care Ontario systemic therapy guideline". Current Oncology. 22 (Suppl 1): S114–S122. doi:10.3747/co.22.2322. PMC 4381787. PMID 25848335.
- ^ Hayes DF, Lippman ME (2018). "Chapter 75: Breast Cancer". In Kasper DL, Fauci AS, Hauser SL, Longo DL, Jameson JL, Loscalzo J (eds.). Harrison's Principles of Internal Medicine (20th ed.). McGraw-Hill Education. ISBN 978-1-259-64403-0.
- ^ Le XF, Pruefer F, Bast RC (January 2005). "HER2-targeting antibodies modulate the cyclin-dependent kinase inhibitor p27Kip1 via multiple signaling pathways". Cell Cycle. 4 (1): 87–95. doi:10.4161/cc.4.1.1360. PMID 15611642.
- ^ Jiang H, Rugo HS (November 2015). "Human epidermal growth factor receptor 2 positive (HER2+) metastatic breast cancer: how the latest results are improving therapeutic options". Therapeutic Advances in Medical Oncology. 7 (6): 321–339. doi:10.1177/1758834015599389. PMC 4622301. PMID 26557900.
- ^ lay-url = https://www.sciencedaily.com/releases/2010/05/100506112557.htm / lay-source = 사이언스데일리
- ^ "Study sheds new light on tamoxifen resistance". Cordis News. Cordis. 2008-11-13. Archived from the original on 2009-02-20. Retrieved 2008-11-14.
- ^ Hurtado A, Holmes KA, Geistlinger TR, Hutcheson IR, Nicholson RI, Brown M, et al. (December 2008). "Regulation of ERBB2 by oestrogen receptor-PAX2 determines response to tamoxifen". Nature. 456 (7222): 663–666. Bibcode:2008Natur.456..663H. doi:10.1038/nature07483. PMC 2920208. PMID 19005469.
- ^ Vranić S, Bešlija S, Gatalica Z (February 2021). "Targeting HER2 expression in cancer: New drugs and new indications". Bosnian Journal of Basic Medical Sciences. 21 (1): 1–4. doi:10.17305/bjbms.2020.4908. PMC 7861626. PMID 32530388.
- ^ Telli ML, Hunt SA, Carlson RW, Guardino AE (August 2007). "Trastuzumab-related cardiotoxicity: calling into question the concept of reversibility". Journal of Clinical Oncology. 25 (23): 3525–3533. doi:10.1200/JCO.2007.11.0106. PMID 17687157.
- ^ Petroni S, Caldarola L, Scamarcio R, Giotta F, Latorre A, Mangia A; et al. (2016). "FISH testing of HER2 immunohistochemistry 1+ invasive breast cancer with unfavorable characteristics". Oncol Lett. 12 (5): 3115–3122. doi:10.3892/ol.2016.5125. PMC 5103906. PMID 27899970.
{{cite journal}}: CS1 유지 : 여러 이름 : 저자 목록 (링크) - ^ a b "IHC Tests (ImmunoHistoChemistry)". Breastcancer.org. Retrieved 2019-10-04. 2015년 10월 23일 최종 수정
- ^ a b Iqbal N, Iqbal N (2014). "Human Epidermal Growth Factor Receptor 2 (HER2) in Cancers: Overexpression and Therapeutic Implications". Molecular Biology International. 2014: 852748. doi:10.1155/2014/852748. PMC 4170925. PMID 25276427.
- ^ a b c d e 2018 ASCO/CAP 지침:
- "Figure 1. Algorithm for evaluation of human epidermal growth factor receptor 2 (HER2) protein expression by immunohistochemistry (IHC) assay of the invasive component of a breast cancer specimen" (PDF). College of American Pathologists: Homepage. Retrieved 2022-09-12.
- :Ahn S, Woo JW, Lee K, Park SY (2020). "HER2 status in breast cancer: changes in guidelines and complicating factors for interpretation". J Pathol Transl Med. 54 (1): 34–44. doi:10.4132/jptm.2019.11.03. PMC 6986968. PMID 31693827.{{cite journal}}CS1 maint : 여러 이름 : 저자 목록 (링크) - ^ Nitta H, Kelly BD, Padilla M, Wick N, Brunhoeber P, Bai I, et al. (May 2012). "A gene-protein assay for human epidermal growth factor receptor 2 (HER2): brightfield tricolor visualization of HER2 protein, the HER2 gene, and chromosome 17 centromere (CEN17) in formalin-fixed, paraffin-embedded breast cancer tissue sections". Diagnostic Pathology. 7: 60. doi:10.1186/1746-1596-7-60. PMC 3487810. PMID 22647525.
- "Creative Commons Attribution License(http://creativecommons.org/licenses/by/2.0) ) 조항에 따라 배포된 Open Access 기사입니다." - ^ Giuliano AE, Hurvitz SA (2019). "Breast Disorder". In Papadakis MA, McPhee SJ, Rabow MW (eds.). Current Medical Diagnosis & Treatment. New York, NY: McGraw-Hill.
- ^ a b c Mikael Hägström, MD의 다이어그램 및 표. 각색: : CS1 메인트: 복수의 이름: 저자 목록 (link)
- ^ Ali SM, Carney WP, Esteva FJ, Fornier M, Harris L, Köstler WJ, et al. (September 2008). "Serum HER-2/neu and relative resistance to trastuzumab-based therapy in patients with metastatic breast cancer". Cancer. 113 (6): 1294–1301. doi:10.1002/cncr.23689. PMID 18661530. S2CID 7307111.
- ^ Lennon S, Barton C, Banken L, Gianni L, Marty M, Baselga J, Leyland-Jones B (April 2009). "Utility of serum HER2 extracellular domain assessment in clinical decision making: pooled analysis of four trials of trastuzumab in metastatic breast cancer". Journal of Clinical Oncology. 27 (10): 1685–1693. doi:10.1200/JCO.2008.16.8351. PMID 19255335.
- ^ Schroeder JA, Adriance MC, McConnell EJ, Thompson MC, Pockaj B, Gendler SJ (June 2002). "ErbB-beta-catenin complexes are associated with human infiltrating ductal breast and murine mammary tumor virus (MMTV)-Wnt-1 and MMTV-c-Neu transgenic carcinomas". The Journal of Biological Chemistry. 277 (25): 22692–22698. doi:10.1074/jbc.M201975200. PMID 11950845.
- ^ Bonvini P, An WG, Rosolen A, Nguyen P, Trepel J, Garcia de Herreros A, et al. (February 2001). "Geldanamycin abrogates ErbB2 association with proteasome-resistant beta-catenin in melanoma cells, increases beta-catenin-E-cadherin association, and decreases beta-catenin-sensitive transcription". Cancer Research. 61 (4): 1671–1677. PMID 11245482.
- ^ Kanai Y, Ochiai A, Shibata T, Oyama T, Ushijima S, Akimoto S, Hirohashi S (March 1995). "c-erbB-2 gene product directly associates with beta-catenin and plakoglobin". Biochemical and Biophysical Research Communications. 208 (3): 1067–1072. doi:10.1006/bbrc.1995.1443. PMID 7702605.
- ^ Huang YZ, Won S, Ali DW, Wang Q, Tanowitz M, Du QS, et al. (May 2000). "Regulation of neuregulin signaling by PSD-95 interacting with ErbB4 at CNS synapses". Neuron. 26 (2): 443–455. doi:10.1016/s0896-6273(00)81176-9. PMID 10839362. S2CID 1429113.
- ^ a b Jaulin-Bastard F, Saito H, Le Bivic A, Ollendorff V, Marchetto S, Birnbaum D, Borg JP (May 2001). "The ERBB2/HER2 receptor differentially interacts with ERBIN and PICK1 PSD-95/DLG/ZO-1 domain proteins". The Journal of Biological Chemistry. 276 (18): 15256–15263. doi:10.1074/jbc.M010032200. PMID 11278603.
- ^ Bilder D, Birnbaum D, Borg JP, Bryant P, Huigbretse J, Jansen E, et al. (July 2000). "Collective nomenclature for LAP proteins". Nature Cell Biology. 2 (7): E114. doi:10.1038/35017119. PMID 10878817. S2CID 19749569.
- ^ Huang YZ, Zang M, Xiong WC, Luo Z, Mei L (January 2003). "Erbin suppresses the MAP kinase pathway". The Journal of Biological Chemistry. 278 (2): 1108–1114. doi:10.1074/jbc.M205413200. PMID 12379659.
- ^ a b Schulze WX, Deng L, Mann M (2005). "Phosphotyrosine interactome of the ErbB-receptor kinase family". Molecular Systems Biology. 1: 2005.0008. doi:10.1038/msb4100012. PMC 1681463. PMID 16729043.
- ^ Bourguignon LY, Zhu H, Zhou B, Diedrich F, Singleton PA, Hung MC (December 2001). "Hyaluronan promotes CD44v3-Vav2 interaction with Grb2-p185(HER2) and induces Rac1 and Ras signaling during ovarian tumor cell migration and growth". The Journal of Biological Chemistry. 276 (52): 48679–48692. doi:10.1074/jbc.M106759200. PMID 11606575.
- ^ a b Olayioye MA, Graus-Porta D, Beerli RR, Rohrer J, Gay B, Hynes NE (September 1998). "ErbB-1 and ErbB-2 acquire distinct signaling properties dependent upon their dimerization partner". Molecular and Cellular Biology. 18 (9): 5042–5051. doi:10.1128/mcb.18.9.5042. PMC 109089. PMID 9710588.
- ^ Xu W, Mimnaugh E, Rosser MF, Nicchitta C, Marcu M, Yarden Y, Neckers L (February 2001). "Sensitivity of mature Erbb2 to geldanamycin is conferred by its kinase domain and is mediated by the chaperone protein Hsp90". The Journal of Biological Chemistry. 276 (5): 3702–3708. doi:10.1074/jbc.M006864200. PMID 11071886.
- ^ Jeong JH, An JY, Kwon YT, Li LY, Lee YJ (October 2008). "Quercetin-induced ubiquitination and down-regulation of Her-2/neu". Journal of Cellular Biochemistry. 105 (2): 585–595. doi:10.1002/jcb.21859. PMC 2575035. PMID 18655187.
- ^ Grant SL, Hammacher A, Douglas AM, Goss GA, Mansfield RK, Heath JK, Begley CG (January 2002). "An unexpected biochemical and functional interaction between gp130 and the EGF receptor family in breast cancer cells". Oncogene. 21 (3): 460–474. doi:10.1038/sj.onc.1205100. PMID 11821958. S2CID 19754641.
- ^ Li Y, Yu WH, Ren J, Chen W, Huang L, Kharbanda S, et al. (August 2003). "Heregulin targets gamma-catenin to the nucleolus by a mechanism dependent on the DF3/MUC1 oncoprotein". Molecular Cancer Research. 1 (10): 765–775. PMID 12939402.
- ^ Schroeder JA, Thompson MC, Gardner MM, Gendler SJ (April 2001). "Transgenic MUC1 interacts with epidermal growth factor receptor and correlates with mitogen-activated protein kinase activation in the mouse mammary gland". The Journal of Biological Chemistry. 276 (16): 13057–13064. doi:10.1074/jbc.M011248200. PMID 11278868.
- ^ Gout I, Dhand R, Panayotou G, Fry MJ, Hiles I, Otsu M, Waterfield MD (December 1992). "Expression and characterization of the p85 subunit of the phosphatidylinositol 3-kinase complex and a related p85 beta protein by using the baculovirus expression system". The Biochemical Journal. 288 ( Pt 2) (2): 395–405. doi:10.1042/bj2880395. PMC 1132024. PMID 1334406.
- ^ Peles E, Levy RB, Or E, Ullrich A, Yarden Y (August 1991). "Oncogenic forms of the neu/HER2 tyrosine kinase are permanently coupled to phospholipase C gamma". The EMBO Journal. 10 (8): 2077–2086. doi:10.1002/j.1460-2075.1991.tb07739.x. PMC 452891. PMID 1676673.
- ^ Arteaga CL, Johnson MD, Todderud G, Coffey RJ, Carpenter G, Page DL (December 1991). "Elevated content of the tyrosine kinase substrate phospholipase C-gamma 1 in primary human breast carcinomas". Proceedings of the National Academy of Sciences of the United States of America. 88 (23): 10435–10439. Bibcode:1991PNAS...8810435A. doi:10.1073/pnas.88.23.10435. PMC 52943. PMID 1683701.
- ^ Wong L, Deb TB, Thompson SA, Wells A, Johnson GR (March 1999). "A differential requirement for the COOH-terminal region of the epidermal growth factor (EGF) receptor in amphiregulin and EGF mitogenic signaling". The Journal of Biological Chemistry. 274 (13): 8900–8909. doi:10.1074/jbc.274.13.8900. PMID 10085134.
추가열람
- Ross JS, Fletcher JA, Linette GP, Stec J, Clark E, Ayers M, et al. (2003). "The Her-2/neu gene and protein in breast cancer 2003: biomarker and target of therapy". The Oncologist. 8 (4): 307–325. doi:10.1634/theoncologist.8-4-307. PMID 12897328. S2CID 1055491.
- Zhou BP, Hung MC (October 2003). "Dysregulation of cellular signaling by HER2/neu in breast cancer". Seminars in Oncology. 30 (5 Suppl 16): 38–48. doi:10.1053/j.seminoncol.2003.08.006. PMID 14613025.
- Ménard S, Casalini P, Campiglio M, Pupa SM, Tagliabue E (December 2004). "Role of HER2/neu in tumor progression and therapy". Cellular and Molecular Life Sciences. 61 (23): 2965–2978. doi:10.1007/s00018-004-4277-7. PMID 15583858. S2CID 37611938.
- Becker JC, Muller-Tidow C, Serve H, Domschke W, Pohle T (June 2006). "Role of receptor tyrosine kinases in gastric cancer: new targets for a selective therapy". World Journal of Gastroenterology. 12 (21): 3297–3305. doi:10.3748/wjg.v12.i21.3297. PMC 4087885. PMID 16733844.
- Laudadio J, Quigley DI, Tubbs R, Wolff DJ (January 2007). "HER2 testing: a review of detection methodologies and their clinical performance". Expert Review of Molecular Diagnostics. 7 (1): 53–64. doi:10.1586/14737159.7.1.53. PMID 17187484. S2CID 9971746.
- Bianchi F, Tagliabue E, Ménard S, Campiglio M (March 2007). "Fhit expression protects against HER2-driven breast tumor development: unraveling the molecular interconnections". Cell Cycle. 6 (6): 643–646. doi:10.4161/cc.6.6.4033. PMID 17374991.
외부 링크
- AACR 암 개념 HER2에 대한 팩트시트
- 인생 네트워크를 위한 유방친구들 - HER2 양성 여성을 위한 남아프리카 유방암 지원 포럼
- Herceptin R : 유방암 환자의 내성 기전 이해를 위한 Herceptin 내성 데이터베이스Sci. Rep. 4:4483
- 미국 국립 의학 도서관의 리셉터,+erbB-2(MeSH)
- PDBe-KB는 인간 수용체 tyrosine-protein kinase erbB-2에 대해 PDB에서 이용 가능한 모든 구조 정보에 대한 개요를 제공합니다.
















![Algorithm for the evaluation of HER2 on fluorescence in situ hybridization (FISH).[46]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d2/HER2_FISH_algorithm.svg/579px-HER2_FISH_algorithm.svg.png)




