앤지오텐신변환효소
Angiotensin-converting enzyme| 앤지오텐신변환효소 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
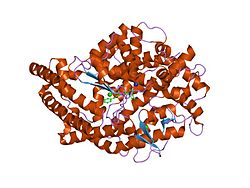
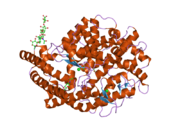
 앤지오텐신변환효소단량체, 드로소필라멜라노가스터 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 3.4.15.1 | ||||||||
| CAS 번호 | 9015-82-1 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 엔트리 | ||||||||
| ExPASy | NiceZyme 뷰 | ||||||||
| 케그 | KEGG 엔트리 | ||||||||
| 메타사이크 | 대사 경로 | ||||||||
| 프라이머리 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBum | ||||||||
| |||||||||
안지오텐신 변환 효소(EC 3.4.15.1) 또는 ACE는 레닌-안지오텐신 시스템(RAS)의 중심 성분으로, 체내 체액의 양을 조절하여 혈압을 조절합니다.그것은 안지오텐신I 호르몬을 활성 혈관 수축제 안지오텐신II로 변환한다.따라서 ACE는 혈관을 수축시켜 간접적으로 혈압을 높인다.ACE 억제제는 심혈관 [5]질환 치료를 위한 의약품으로 널리 사용되고 있다.
ACE의 덜 알려진 다른 기능은 브래디키닌,[6][8] 물질[7] P 및 아밀로이드 베타 단백질의 분해이다.
명명법
ACE 는, 다음의 이름으로도 알려져 있습니다.
- 디펩티딜카르복시펩티드가수분해효소I
- 펩티드가수분해효소P
- 디펩티드 가수분해효소
- 펩티딜디펩티드가수분해효소
- 앤지오텐신변환효소
- 키나아제II
- 앤지오텐신I변환효소
- 카르복시카텝신
- 디펩티딜카르복시펩티드가수분해효소
- '하이퍼텐신변환효소'펩티딜디펩티드가수분해효소I
- 펩티딜디펩티드 가수분해효소
- 펩티딜디펩티드 가수분해효소
- 내피세포펩티딜디펩티드가수분해효소
- 펩티딜디펩티드가수분해효소-4
- PDH
- 펩티딜디펩티드히드로라아제
- DCP
- CD143
기능.
ACE는 C 말단에서 디펩타이드를 제거함으로써 펩타이드를 가수분해한다.마찬가지로 디펩타이드 His-Leu를 [9]제거함으로써 비활성 데카펩타이드 안지오텐신 I을 옥타펩타이드 안지오텐신 II로 변환한다.
ACE는 레닌-안지오텐신 시스템(RAS)의 중심 성분으로, 체내 체액의 양을 조절하여 혈압을 조절한다.

앤지오텐신II는 기질 농도 의존적인 방식으로 [10]강력한 혈관 수축제이다.앤지오텐신 II는 1형 앤지오텐신 II 수용체(AT1)와 결합하며, 이는 혈관 수축과 그에 따른 혈압 상승을 초래하는 많은 작용을 일으킨다.

ACE는 또한 강력한 혈관확장제인 브라디키닌과 다른 혈관 활성 [12]펩타이드를 분해하는 키닌 칼리크레인 시스템의 일부이다.
키나아제 II는 앤지오텐신 변환 효소와 동일하다.따라서 혈관수축제(ANG II)를 생성하는 동일한 효소(ACE)도 혈관확장제(Bradykinin)[11]를 폐기한다.
메커니즘
ACE는 아연 금속단백질가수분해효소이다.[13]아연 중심은 펩타이드 가수분해를 촉매한다.아연의 중요한 역할을 반영하여 ACE는 금속담금제에 [14]의해 억제될 수 있다.
E384 잔류물은 기계적으로 중요합니다.일반적인 염기로서 아연 결합수를 탈양성자화하여 친핵성 Zn-OH 중심을 생성한다.생성된 암모늄기는 C-N [16]결합을 분해하는 일반 산 역할을 한다.
염화물 이온의 기능은 매우 복잡하고 매우 논란이 되고 있다.염화에 의한 음이온 활성화는 [17]ACE의 특징입니다.염화물에 의한 가수분해 활성화는 기질에 크게 의존한다는 것이 실험적으로 확인되었다.예를 들어, 예를 들어 가수분해율을 증가시킵니다.Hip-His-Leu는 Hip-Ala-Pro와 [16]같은 다른 기질의 가수분해를 억제합니다.생리적 조건 하에서 효소는 안지오텐신 I에 대한 최대 활성의 약 60%에 도달하는 반면 브라디키닌에 대한 최대 활성에 도달한다.따라서 ACE의 음이온 활성화 기능은 높은 [17]기질특이성을 제공하는 것으로 가정한다.다른 이론들은 염화물이 단순히 [16]효소의 전체적인 구조를 안정시킬 수 있다고 말한다.
유전학
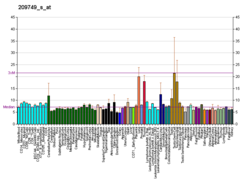
ACE 유전자인 ACE는 두 개의 동질효소를 암호화한다.체세포 동질효소는 혈관내피세포, 상피신장세포, 고환레이디그세포를 포함한 많은 조직, 주로 폐에서 발현되는 반면, 배아는 정자에서만 발현된다.뇌 조직에는 국소 RAS에 참여하고 Aβ42를 Aβ40으로 변환하는 베타 아밀로이드 형태의 ACE 효소가 있다.후자는 주로 ACE 효소의 N 도메인 부분의 함수이다.따라서 혈액-뇌 장벽을 넘고 우선적으로 선택된 N-말단 활성을 가진 ACE 억제제는 Aβ42의 축적과 [citation needed]치매 진행을 유발할 수 있다.
질병 관련성
ACE 억제제는 고혈압, 심부전, 당뇨병 신증, 제2형 당뇨병과 같은 질환의 치료에 의약품으로 널리 사용된다.
ACE 억제제는 [18]경쟁적으로 ACE를 억제한다.그 결과 안지오텐신II의 형성이 저하되고 브라디키닌의 신진대사가 저하되어 동맥과 정맥의 체계적인 확장과 동맥 혈압의 저하가 초래됩니다.또한 앤지오텐신II 형성을 억제함으로써 부신피질로부터의 앤지오텐신II 매개 알도스테론 분비를 감소시켜 수분 및 나트륨 재흡수의 감소 및 세포외 [19]부피의 감소를 초래한다.
알츠하이머병에 대한 ACE의 효과는 여전히 논란이 많다.알츠하이머 환자들은 보통 뇌에서 더 높은 ACE 수치를 보인다.일부 연구는 혈액 뇌 장벽(BBB)을 통과할 수 있는 ACE 억제제가 뇌에서 네프리신과 같은 주요 아밀로이드-베타 분해 효소의 활동을 증가시켜 알츠하이머병의 [20]느린 진행을 야기할 수 있다고 제안한다.보다 최근의 연구에 따르면 ACE 억제제는 아폴리포단백질 E4 대립 유전자(ApoE4)가 없을 때 알츠하이머병의 위험을 줄일 수 있지만,[21] ApoE4-carrier에는 영향을 미치지 않는다.또 다른 최근의 가설은 ACE 수치가 높을수록 알츠하이머를 예방할 수 있다는 것이다.ACE는 뇌혈관의 베타아밀로이드를 분해하여 질병의 [22]진행을 막는 데 도움을 줄 수 있다고 가정한다.
ACE1 D-alle 빈도와 COVID-19의 유병률 및 사망률 사이의 음의 상관관계가 [23]확립되었다.
병리학
- ACE의 높은 수치는 또한 살코이드증에서 발견되며, 이 질병을 진단하고 모니터링하는데 사용된다.ACE의 높은 수치는 나병, 갑상선 기능 항진증, 급성 간염, 일차 담도 간경화, 당뇨병, 다발성 골수종, 골관절염, 아밀로이드증, 고셔병, 진폐증, 히스토플라스마증, 그리고 세균성 결핵에서도 발견된다.그것은 또한 광범위한 플라크 건선을 가진 일부 환자들에게서 나타난다.
- 신장병, 폐색성 폐질환, 갑상선 기능 저하증은 혈청 수치가 낮아집니다.
경기력에 미치는 영향
앤지오텐신 변환 효소 유전자는 2018년 [24]현재 160개 이상의 다형성을 가지고 있다.
연구에 따르면 앤지오텐신 변환 효소의 유전자형이 다르면 운동 [25][26]성과에 다양한 영향을 미칠 수 있다.
rs1799752 I/D 다형은 유전자의 [24]인트론 16에서 287 염기쌍 알라닌 배열의 삽입(I) 또는 결손(D)으로 구성된다.DD 유전자형은 ACE 단백질의 높은 혈장 수준, 중간 수준의 DI 유전자형, 낮은 [24]수준의 II와 관련이 있습니다.신체 운동 중, D-알레 운반체에 대한 ACE의 높은 수치로 인해, 안지오텐신 II를 생성하는 더 높은 용량으로 인해, 혈압은 I-알레 운반체에 비해 더 빨리 상승할 것이다.그 결과 최대 심박수가 낮아지고 최대 산소흡수량(VO)이2max 낮아집니다.따라서 D-alle carrier는 심혈관 질환의 위험이 10% 증가한다.또한 D-alle은 I-alle에 [27]비해 훈련에 대한 응답으로 좌심실 성장이 크게 증가하는 것과 관련이 있다.반면, I-알레르 운반체는 일반적으로 낮은 ACE 수준과 높은 최대 산소 섭취로 인해 최대 심박수가 증가하여 향상된 [27]지구력을 보인다.I 대립 유전자는 정예 거리 달리기 선수, 노 젓는 선수 및 사이클 선수에서 빈도가 증가하여 발견됩니다.단거리 수영 선수는 [28][29]내구력보다 체력에 더 의존하기 때문에 D-알레의 빈도가 더 높다.
역사
그 효소는 레오나드 T에 의해 보고되었다.1956년 [30]스키그스 주니어인간 고환의 결정 구조는 2002년에 R에 의해 해결되었다.K. 라비 아차랴의 [15]연구실에 있는 나테시.그것은 주로 폐의 모세혈관에 위치하지만 내피세포와 [31]신장상피세포에서도 발견될 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c GRCh38: 앙상블 릴리즈 89: ENSG00000159640 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리즈 89: ENSMUSG000020681 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Kaplan's Essentials of Cardiac Anesthesia. Elsevier. 2018. doi:10.1016/c2012-0-06151-0. ISBN 978-0-323-49798-5.
Mechanisms of Action:ACE inhibitors act by inhibiting one of several proteases responsible for cleaving the decapeptide Ang I to form the octapeptide Ang II. Because ACE is also the enzyme that degrades bradykinin, ACE inhibitors increase circulating and tissue levels of bradykinin (Fig. 8.4).
- ^ Fillardi PP (2015). ACEi and ARBS in Hypertension and Heart Failure. Vol. 5. Switzerland: Springer International Publishing. pp. 10–13. ISBN 978-3-319-09787-9.
- ^ Dicpinigaitis PV (January 2006). "Angiotensin-converting enzyme inhibitor-induced cough: ACCP evidence-based clinical practice guidelines". Chest. 129 (1 Suppl): 169S–173S. doi:10.1378/chest.129.1_suppl.169S. PMID 16428706.
- ^ Hemming ML, Selkoe DJ (November 2005). "Amyloid beta-protein is degraded by cellular angiotensin-converting enzyme (ACE) and elevated by an ACE inhibitor". The Journal of Biological Chemistry. 280 (45): 37644–50. doi:10.1074/jbc.M508460200. PMC 2409196. PMID 16154999.
- ^ Coates D (Jun 2003). "The angiotensin converting enzyme (ACE)". The International Journal of Biochemistry & Cell Biology. Renin–Angiotensin Systems: State of the Art. 35 (6): 769–73. doi:10.1016/S1357-2725(02)00309-6. PMID 12676162.
- ^ Zhang R, Xu X, Chen T, Li L, Rao P (May 2000). "An assay for angiotensin-converting enzyme using capillary zone electrophoresis". Analytical Biochemistry. 280 (2): 286–90. doi:10.1006/abio.2000.4535. PMID 10790312.
- ^ a b Boulpaep EL, Boron WF (2005). "Integration of Salt and Water Balance". Medical Physiology: a Cellular and Molecular Approach. Philadelphia, Pa.: Elsevier Saunders. pp. 866–867. ISBN 978-1-4160-2328-9.
- ^ Imig JD (Mar 2004). "ACE Inhibition and Bradykinin-Mediated Renal Vascular Responses: EDHF Involvement". Hypertension. 43 (3): 533–5. doi:10.1161/01.HYP.0000118054.86193.ce. PMID 14757781.
- ^ Wang W, McKinnie SM, Farhan M, Paul M, McDonald T, McLean B, Llorens-Cortes C, Hazra S, Murray AG, Vederas JC, Oudit GY (May 2016). "Angiotensin Converting Enzyme 2 Metabolizes and Partially Inactivates Pyrapelin-13 and Apelin-17: Physiological Effects in the Cardiovascular System". Hypertension. 68 (2): 365–77. doi:10.1161/HYPERTENSIONAHA.115.06892. PMID 27217402. S2CID 829514.
- ^ Bünning P, Riordan JF (Jul 1985). "The functional role of zinc in angiotensin converting enzyme: implications for the enzyme mechanism". Journal of Inorganic Biochemistry. 24 (3): 183–98. doi:10.1016/0162-0134(85)85002-9. PMID 2995578.
- ^ a b Natesh R, Schwager SL, Sturrock ED, Acharya KR (2003). "Crystal structure of the human angiotensin-converting enzyme-lisinopril complex". Nature. 421 (6922): 551–4. Bibcode:2003Natur.421..551N. doi:10.1038/nature01370. PMID 12540854. S2CID 4137382.
- ^ a b c Zhang C, Wu S, Xu D (Jun 2013). "Catalytic mechanism of angiotensin-converting enzyme and effects of the chloride ion". The Journal of Physical Chemistry B. 117 (22): 6635–45. doi:10.1021/jp400974n. PMID 23672666.
- ^ a b Bünning P (1983). "The catalytic mechanism of angiotensin converting enzyme". Clinical and Experimental Hypertension, Part A. 5 (7–8): 1263–75. doi:10.3109/10641968309048856. PMID 6315268.
- ^ "Angiotensin converting enzyme (ace) inhibitors" (PDF). British Hypertension Society. Archived from the original (PDF) on 2017-11-18.
- ^ Klabunde RE. "ACE-inhibitors". Cardiovascular Pharmacology Concepts. cvpharmacology.com. Retrieved 2009-03-26.
- ^ Brooks L (2004). "The Importance of Treating the Blood Pressure: ACE Inhibitors May Slow Alzheimer's Disease". Medscape. Medscape Cardiology.
- ^ Qiu WQ, Mwamburi M, Besser LM, Zhu H, Li H, Wallack M, Phillips L, Qiao L, Budson AE, Stern R, Kowall N (2013-01-01). "Angiotensin converting enzyme inhibitors and the reduced risk of Alzheimer's disease in the absence of apolipoprotein E4 allele". Journal of Alzheimer's Disease. 37 (2): 421–8. doi:10.3233/JAD-130716. PMC 3972060. PMID 23948883.
- ^ "ACE Enzyme May Enhance Immune Responses And Prevent Alzheimer's". Science 2.0. 27 August 2014. Retrieved 2016-03-01.
- ^ Joris R. Delanghe, Marijn M. Speeckaert, Marc L. De Buyzere (2020). "The host's angiotensin-converting enzyme polymorphism may explain epidemiological findings in COVID-19 infections". Clinica Chimica Acta; International Journal of Clinical Chemistry. 505: 192–193. doi:10.1016/j.cca.2020.03.031. PMC 7102561. PMID 32220422.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ a b c Cintra, Mariangela Torreglosa Ruiz; Balarin, Marly Aparecida Spadotto; Tanaka, Sarah Cristina Sato Vaz; Silva, Vanessa Iorrana Mota da; Marqui, Alessandra Bernadete Trovó de; Resende, Elisabete Aparecida Mantovani Rodrigues de; Lima, Marco Fábio Prata; Gomes, Mariana Kefálas Oliveira (November 2018). "Polycystic ovarian syndrome: rs1799752 polymorphism of ACE gene". Revista da Associação Médica Brasileira. 64 (11): 1017–1022. doi:10.1590/1806-9282.64.11.1017. PMID 30570054.
- ^ Flück, Martin; Kramer, Manuel; Fitze, Daniel P.; Kasper, Stephanie; Franchi, Martino V.; Valdivieso, Paola (8 May 2019). "Cellular Aspects of Muscle Specialization Demonstrate Genotype – Phenotype Interaction Effects in Athletes". Frontiers in Physiology. 10: 526. doi:10.3389/fphys.2019.00526. PMC 6518954. PMID 31139091.
- ^ Wang P, Fedoruk MN, Rupert JL (2008). "Keeping pace with ACE: are ACE inhibitors and angiotensin II type 1 receptor antagonists potential doping agents?". Sports Medicine. 38 (12): 1065–79. doi:10.2165/00007256-200838120-00008. PMID 19026021. S2CID 7614657.
- ^ a b Montgomery HE, Clarkson P, Dollery CM, Prasad K, Losi MA, Hemingway H, Statters D, Jubb M, Girvain M, Varnava A, World M, Deanfield J, Talmud P, McEwan JR, McKenna WJ, Humphries S (Aug 1997). "Association of angiotensin-converting enzyme gene I/D polymorphism with change in left ventricular mass in response to physical training". Circulation. 96 (3): 741–7. doi:10.1161/01.CIR.96.3.741. PMID 9264477.
- ^ Sanders J, Montgomery H, Woods D (2001). "Kardiale Anpassung an Körperliches Training" [The cardiac response to physical training] (PDF). Deutsche Zeitschrift für Sportmednizin (in German). Jahrgang 52 (3): 86–92.
- ^ Costa AM, Silva AJ, Garrido ND, Louro H, de Oliveira RJ, Breitenfeld L (Aug 2009). "Association between ACE D allele and elite short distance swimming". European Journal of Applied Physiology. 106 (6): 785–90. doi:10.1007/s00421-009-1080-z. hdl:10400.15/3565. PMID 19458960. S2CID 21167767.
- ^ Skeggs LT, Kahn JR, Shumway NP (Mar 1956). "The preparation and function of the hypertensin-converting enzyme". The Journal of Experimental Medicine. 103 (3): 295–9. doi:10.1084/jem.103.3.295. PMC 2136590. PMID 13295487.
- ^ Kierszenbaum, Abraham L. (2007). Histology and cell biology: an introduction to pathology. Mosby Elsevier. ISBN 978-0-323-04527-8.
추가 정보
- Niu T, Chen X, Xu X (2002). "Angiotensin converting enzyme gene insertion/deletion polymorphism and cardiovascular disease: therapeutic implications". Drugs. 62 (7): 977–93. doi:10.2165/00003495-200262070-00001. PMID 11985486. S2CID 46986772.
- Roĭtberg GE, Tikhonravov AV, Dorosh ZV (2004). "[Role of angiotensin-converting enzyme gene polymorphism in the development of metabolic syndrome]". Terapevticheskiĭ Arkhiv. 75 (12): 72–7. PMID 14959477.
- Vynohradova SV (2005). "[The role of angiotensin-converting enzyme gene I/D polymorphism in development of metabolic disorders in patients with cardiovascular pathology]". T︠S︡itologii︠a︡ I Genetika. 39 (1): 63–70. PMID 16018179.
- König S, Luger TA, Scholzen TE (Oct 2006). "Monitoring neuropeptide-specific proteases: processing of the proopiomelanocortin peptides adrenocorticotropin and alpha-melanocyte-stimulating hormone in the skin". Experimental Dermatology. 15 (10): 751–61. doi:10.1111/j.1600-0625.2006.00472.x. PMID 16984256. S2CID 32034934.
- Sabbagh AS, Otrock ZK, Mahfoud ZR, Zaatari GS, Mahfouz RA, et al. (Mar 2007). "Angiotensin-converting enzyme gene polymorphism and allele frequencies in the Lebanese population: prevalence and review of the literature". Molecular Biology Reports. 34 (1): 47–52. doi:10.1007/s11033-006-9013-y. PMID 17103020. S2CID 9939390.
- Castellon R, Hamdi HK (2007). "Demystifying the ACE polymorphism: from genetics to biology". Current Pharmaceutical Design. 13 (12): 1191–8. doi:10.2174/138161207780618902. PMID 17504229.
- Lazartigues E, Feng Y, Lavoie JL (2007). "The two fACEs of the tissue renin–angiotensin systems: implication in cardiovascular diseases". Current Pharmaceutical Design. 13 (12): 1231–45. doi:10.2174/138161207780618911. PMID 17504232.