푸린
Purine | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 9H-푸린 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.004.020 |
| 케그 | |
| 메쉬 | 푸린 |
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C5H4N4 | |
| 몰 질량 | 120.115g/140g−1 |
| 녹는점 | 214 °C (417 °F, 487 K) |
| 500 g/L (RT) | |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
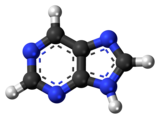
퓨린은 두 개의 고리(피리미딘과 이미다졸)가 함께 융합된 복소환 방향족 유기 화합물이다.수용성입니다.푸린은 또한 치환된 푸린과 그들의 호변이성체를 포함하는 더 넓은 종류의 분자인 푸린에 그것의 이름을 붙입니다.그것들은 [1]자연에서 가장 널리 발생하는 질소 함유 복소환이다.
식사원
푸린체는 고기와 고기 제품, 특히 간과 신장 같은 내부 장기에서 고농도로 발견됩니다.일반적으로 식물성 식단은 푸린체가 [2]적다.고순도 식물과 해조류는 약간의 콩과 스피루리나를 포함합니다.고순도 소스의 예로는 스위트브레드, 멸치, 정어리, 간, 쇠고기 신장, 뇌, 고기 추출물(예: 옥소, 보브릴), 청어, 고등어, 가리비, 식용육, 효모(맥주, 효모 추출물, 영양 효모) 및 그레이비 [3]등이 있다.
붉은 고기, 쇠고기, 돼지고기, 가금류, 어패류, 아스파라거스, 콜리플라워, 시금치, 버섯, 완두콩, 렌즈콩, 말린 완두콩, 오트밀, 밀기울, 밀배아 및 [4]산사에도 적당량의 푸린이 함유되어 있다.
생화학
퓨린과 피리미딘은 두 그룹의 뉴클레오티드 염기를 포함한 두 그룹의 질소 염기를 구성합니다.푸린 염기는 구아닌(G) 및 아데닌(A)이며, 이들은 디옥시리보핵산(디옥시구아노신 및 디옥시아데노신)과 디옥시리보핵산(디옥시구아노신 및 디옥시아노신)과 리보핵산(구아노신, 아데노신)을 형성한다.인산과의 이러한 뉴클레오시드는 각각 DNA와 RNA의 구성 요소인 대응하는 뉴클레오티드(디옥시구아닐산, 디옥시아데닐산 및 구아닐산, 아데닐산)를 형성합니다.퓨린 염기는 또한 구아노신 일인산(GMP)과 아데노신 일인산(AMP) 화합물 내의 많은 대사 및 신호 전달 과정에서 필수적인 역할을 한다.
이러한 필수 세포 과정을 수행하기 위해서는 푸린과 피리미딘이 세포에 의해, 그리고 비슷한 양으로 필요하다.푸린과 피리미딘은 모두 자가 억제 및 활성화된다.푸린체가 생성되면 푸린체 형성에 필요한 효소를 억제합니다.이러한 자기억제는 또한 피리미딘 형성에 필요한 효소를 활성화하기 때문에 일어난다.피리미딘은 유사한 방법으로 자기 억제와 푸린 활성화를 동시에 한다.이 때문에 세포에는 항상 [5]거의 같은 양의 두 물질이 있습니다.
특성.
푸린은 매우 약한 산(pKa 8.93)이며 훨씬 더 약한 염기(pKa 2.39)[6]이다.순수한 물에 녹는 경우 pH는 이 두 pKa 값의 절반입니다.
푸린은 방향족이며, 각각 4개의 질소 원자 중 다른 하나에 결합된 수소를 가진 4개의 호변이성체를 가지고 있다.이들은 1-H, 3-H, 7-H 및 9-H로 식별됩니다(번호부 링 이미지 참조).일반적인 결정 형태는 7-H 호변이성체를 선호하는 반면 극성 용제에서는 9-H와 7-H 호변이성체가 우세하다.[7]고리의 치환기와 다른 분자와의 상호작용은 이러한 호변이성체의 [8]평형을 바꿀 수 있다.
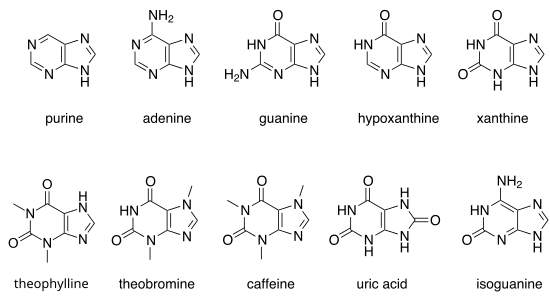
주목할 만한 푸린체
자연적으로 발생하는 푸린체가 많다.이들은 핵염기 아데닌(2)과 구아닌(3)을 포함한다.DNA에서 이러한 염기는 각각 상보적인 피리미딘, 티민 및 시토신과 수소 결합을 형성한다.이를 보완적 염기쌍이라고 합니다.RNA에서 아데닌의 보체는 티민 대신 우라실이다.
다른 주목할 만한 퓨린으로는 하이포산틴, 크산틴, 테오필린, 테오브로민, 카페인, 요산 및 이소구아닌이 있다.
기능들

DNA와 RNA에서 퓨린의 중요한 역할 외에도, 퓨린은 ATP, GTP, 고리형 AMP, NADH, 그리고 조효소 A와 같은 많은 다른 중요한 생체 분자에서도 중요한 성분이다.푸린 (1) 자체는 자연에서 발견되지 않았지만 유기 합성에 의해 생성될 수 있다.
그들은 또한 퓨린 작동성 수용체에 작용하면서 신경전달물질로서 직접적으로 기능할 수 있다.아데노신은 아데노신 수용체를 활성화시킨다.
역사
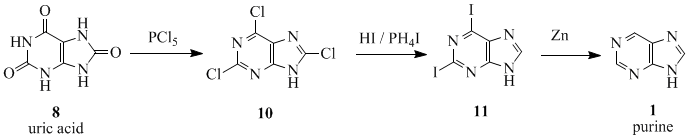
푸린이라는 단어는 [10][11]1884년 독일의 화학자 [9]에밀 피셔에 의해 만들어졌다.그는 [11]1898년에 처음으로 그것을 합성했다.반응 시퀀스의 시작 물질은 요산 (8)으로,[12] 1776년 칼 빌헬름 셸에 의해 신장 결석으로부터 분리되었습니다.요산(8)을 PCl과5 반응시켜 2,6,8-트리클로로푸린(10)을 얻은 후 HI 및 PHI로4 변환하여 2,6-디요오드푸린(11)을 얻었다.이 제품은 아연 분진을 사용하여 푸린(1)으로 환원되었습니다.
대사
많은 생물들은 푸린체를 합성하고 분해하는 대사 경로를 가지고 있다.
변형된 퓨린 뉴클레오티드의 축적은 다양한 세포 과정, 특히 DNA와 RNA를 포함하는 과정에 결함이 있다.생존하기 위해, 유기체는 활성 NTP 및 dNTP 풀에서 제거되는 이러한 푸린 유도체를 가수 분해하는 많은 디옥시푸린 포스포히드로라아제를 가지고 있다.퓨린 염기의 탈아미네이션은 ITP, dITP, XTP [13]및 dXTP와 같은 뉴클레오티드의 축적을 초래할 수 있다.
퓨린의 생성과 분해를 조절하는 효소의 결함은 세포의 DNA 서열을 심각하게 바꿀 수 있는데, 이것은 퓨린 대사 효소의 특정 유전자 변형을 가지고 있는 사람들이 왜 어떤 종류의 암에 걸릴 위험이 더 높은지를 설명해 줄 수 있다.
생명의 세 영역에서 푸린 생합성
진핵생물, 박테리아, 고세균 등 생명체의 3개 영역 모두 퓨린의 de novo 생합성을 수행할 수 있다.이 능력은 생명을 위한 푸딩의 중요성을 반영한다.생화학적 합성의 경로는 진핵생물과 박테리아 종에서 매우 유사하지만, 고대 [14]종들 사이에서 더 가변적이다.푸린 생합성에 필요한 거의 완전하거나 완전한 유전자 세트가 연구 [14]대상 65종의 고고학 종 중 58종에 존재하는 것으로 확인되었다.하지만, 유전자를 코드하는 푸린체가 완전히, 또는 거의 완전히 결여된 7종의 고고학 종들도 확인되었다.푸린체를 합성할 수 없는 고생물은 성장을 위해 외인성 푸린체를 획득할 수 있으며, 따라서 성장을 위해 외인성 푸린체를 필요로 하는 진핵생물의 푸린 돌연변이, 예를 들어 아스코마이세테균 Neurospora crassa와 [15]유사하다.[14]
통풍과의 관계
육류와 해산물의 높은 소비량은 통풍의 위험 증가와 관련이 있는 반면, 유제품의 높은 소비량은 위험 감소와 관련이 있다.푸린체가 풍부한 채소나 단백질을 적당히 섭취하는 것은 [16]통풍의 위험 증가와 관련이 없다.고요산혈증의 위험성과 유사한 결과가 발견되었다.
실험실 합성
푸린 대사에서의 푸린체 체내 합성 외에 푸린체를 인공적으로 생성할 수도 있다.
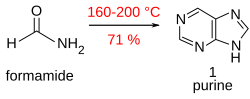
푸린(1)은 170°C에서 [17]28시간 동안 개방된 용기에서 포름아미드를 가열하면 양호한 수율로 얻을 수 있다.
이 놀라운 반응과 그와 같은 다른 반응들은 생명의 [18]기원의 맥락에서 논의되어 왔다.
1968년 8월 20일 특허를 취득한 현재 인정되고 있는 아데닌의 산업 규모 생산 방법은 포름아미드 방법의 변형된 형태이다.이 방법은 포름아미드를 밀폐 플라스크 내에서 섭씨 120도 조건에서 5시간 동안 가열하여 아데닌을 생성한다.산촉매로서 옥시염산인(포스포릴염화물) 또는 오염화인(phantachloride)을 사용하고 햇빛이나 자외선 조건을 이용하여 반응량을 크게 증가시킨다.5시간이 경과하고 포름아미드-인산염-아데닌 용액이 식으면 포름아미드 및 현재 형성된 아데닌을 포함한 플라스크에 물을 넣는다.그런 다음 물-포름아미드-아데닌 용액을 활성탄의 여과 기둥에 붓습니다.물과 포름아미드 분자는 작은 분자로, 숯을 통과하여 폐플라스크로 들어갑니다; 하지만, 큰 아데닌 분자는 아데닌과 숯의 탄소 사이에서 상호작용하는 반데르발 힘 때문에 숯에 부착되거나 "흡착"됩니다.숯은 표면적이 넓기 때문에 특정 크기(물이나 포름아미드보다 더 큰 크기)를 통과하는 대부분의 분자를 포획할 수 있습니다.활성탄-아데닌 구조상에 물(아쿠아 암모니아)에 용해된 암모니아 가스를 주입하여 아데닌을 암모니아 수용액으로 방출한다.물, 암모니아 및 아데닌을 포함한 용액은 공기 건조 상태로 방치되며, 이전에 용액을 염기성으로 만들고 아데닌을 용해시킬 수 있는 암모니아 가스의 손실로 인해 아데닌이 용해성을 잃음으로써 아데닌이 결정화되어 [19]저장 가능한 순수 백색 분말로 결정화된다.
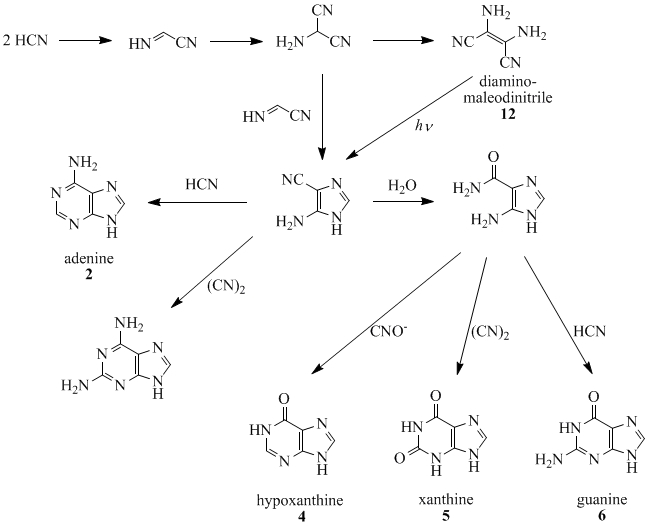
Oro, Orgel, 그리고 동료들은 4분자의 HCN이 4중합되어 디아미노말레오디니트릴(12)을 형성하고, 이것은 거의 모든 자연적으로 발생하는 푸린으로 [20][21][22][23][24]전환될 수 있다는 것을 보여주었다.예를 들어, 5개의 HCN 분자는 발열 반응에서 응축되어 아데닌을 만드는데, 특히 암모니아가 있을 때 그렇습니다.
Traube Purine 합성(1900)은 아민 치환 피리미딘과 [25]포름산 사이의 고전적 반응(Wilhelm Traube의 이름을 딴 것)이다.
퓨린리보뉴클레오시드의 생물전합성
생명체가 어떻게 생겨났는지를 이해하기 위해서는 그럴듯한 사전 생물 조건 하에서 생명체의 핵심 구성 요소를 형성할 수 있는 화학적 경로에 대한 지식이 필요하다.Nam 등은 RNA 형성을 [26]유도하는 핵심 단계인 수성 마이크로드립에서 리보뉴클레오시드를 제공하기 위해 퓨린과 피리미딘 핵산염기들이 리보스와 직접 응축되는 것을 입증했다.또, 베커 외 [27]연구진에 의해서, 푸린 리보뉴클레오시드를 합성하기 위한, 그럴듯한 프리바이오틱 공정을 제시했다.
「 」를 참조해 주세요.
레퍼런스
- ^ Rosemeyer H (March 2004). "The chemodiversity of purine as a constituent of natural products". Chemistry & Biodiversity. 1 (3): 361–401. doi:10.1002/cbdv.200490033. PMID 17191854. S2CID 12416667.
- ^ "Gout: List of Foods High and Low in Purine Content". Dietaryfiberfood.com. 2016-04-08. Archived from the original on 2011-11-12. Retrieved 2016-07-16.
- ^ Kaneko K, Aoyagi Y, Fukuuchi T, Inazawa K, Yamaoka N (2014). "Total purine and purine base content of common foodstuffs for facilitating nutritional therapy for gout and hyperuricemia". Biological & Pharmaceutical Bulletin. 37 (5): 709–721. doi:10.1248/bpb.b13-00967. PMID 24553148.
- ^ "Gout Diet: What Foods To Avoid". Healthcastle.com. Archived from the original on 2017-08-14. Retrieved 2016-07-16.
- ^ Guyton AC (2006). Textbook of Medical Physiology. Philadelphia, PA: Elsevier. p. 37. ISBN 978-0-7216-0240-0.
- ^ Seela F, et al. (2014). Schaumann E (ed.). Houben-Weyl Methods of Organic Chemistry. Vol. E 9b/2 (4th Supplement: Hetarenes III (Six-Membered Rings and Larger Hetero-Rings with Maximum Unsaturation) - Part 2b ed.). p. 310. ISBN 9783131815040. Archived from the original on 2022-02-17. Retrieved 2020-05-15.
- ^ Raczyńska ED, Gal JF, Maria PC, Kamińska B, Igielska M, Kurpiewski J, Juras W (April 2020). "Purine tautomeric preferences and bond-length alternation in relation with protonation-deprotonation and alkali metal cationization". Journal of Molecular Modeling. 26 (5): 93. doi:10.1007/s00894-020-4343-6. PMC 7256107. PMID 32248379.
- ^ Stasyuk OA, Szatyłowicz H, Krygowski TM (April 2012). "Effect of the H-bonding on aromaticity of purine tautomers". The Journal of Organic Chemistry. 77 (8): 4035–4045. doi:10.1021/jo300406r. PMID 22448684.
- ^ McGuigan H (1921). An Introduction To Chemical Pharmacology. P. Blakiston's Sons & Co. p. 283. Archived from the original on April 16, 2020. Retrieved July 18, 2012.
- ^ Fischer E (1884). "Ueber die Harnsäure. I." [On uric acid. I.]. Berichte der Deutschen Chemischen Gesellschaft. 17: 328–338. doi:10.1002/cber.18840170196. Archived from the original on 2021-01-18. Retrieved 2016-04-20.

페이지 329Wayback Machine에서 2022-02-17 아카이브: "Um eine repicelle Nomenklatur der so entheen zahlreichen zu ermöglicen, betrachte ich 디젤벤 als Abkömmlinge derchen was serminge derstoffindung CH3"CNH와543 nenne die letztere Methylpurin." (많은 기존 물질에 대한 합리적인 명명법을 가능하게 하기 위해, 나는 그것들을 아직 알려지지 않은 수소 화합물3 CH의 유도체로 간주했다.CNH543 및 후자를 "메틸푸린"이라고 부른다. - ^ a b Fischer E (1898). "Ueber das Purin und seine Methylderivate" [On purine and its methyl derivatives]. Berichte der Deutschen Chemischen Gesellschaft. 31 (3): 2550–2574. doi:10.1002/cber.18980310304. Archived from the original on 2020-10-18. Retrieved 2016-04-20.

페이지의 주부터 승객을 머신에:"…hielt 지느러미·에스 für zweckmäßig,allediese Produkte ebenso Harnsäure als Derivate 해부sauerstofffreien Verbindung C5H4N4 zu betrachten,undwählte fürdiese 소굴 Namen Purin, 의무 불이행자 aus denWörtern purum 운트 uricumkombiniert 전쟁 죽음 위에."(…I 방편으로서 p. 이 모든 것을 고려하는 것을 2020-10-18 2550Archived로드ucts는 요산과 마찬가지로 무산소 화합물544 CHN의 유도체로서 이들을 위해 "푸린"이라는 이름을 선택했는데, 이는 [라틴어] purum과 uricum에서 비롯되었다.) - ^ Scheele CW (1776). "Examen chemicum calculi urinari" [A chemical examination of kidney stones]. Opuscula. 2: 73.
- ^ Davies O, Mendes P, Smallbone K, Malys N (April 2012). "Characterisation of multiple substrate-specific (d)ITP/(d)XTPase and modelling of deaminated purine nucleotide metabolism". BMB Reports. 45 (4): 259–264. doi:10.5483/BMBRep.2012.45.4.259. PMID 22531138.
- ^ a b c 브라운 AM, Hoopes SL, 화이트 RH, 사리스키 CA.고고학에서의 푸린 생합성: 주제에 대한 변주.Biol Direct. 2011년 12월 14일; 6:63.doi: 10.1186/1745-6150-6-63.PMID 22168471;PMCID:PMC3261824
- ^ Neurospora crassa J. Gen. Microbiol의 푸린 돌연변이에 의해 축적된 Bernstein, H. 이미다졸 화합물. 5:41-46 (1961)
- ^ Choi HK, Atkinson K, Karlson EW, Willett W, Curhan G (March 2004). "Purine-rich foods, dairy and protein intake, and the risk of gout in men". The New England Journal of Medicine. 350 (11): 1093–1103. doi:10.1056/NEJMoa035700. PMID 15014182.
- ^ Yamada H, Okamoto T (1972). "A One-step Synthesis of Purine Ring from Formamide". Chemical & Pharmaceutical Bulletin. 20 (3): 623. doi:10.1248/cpb.20.623. Archived from the original on 2016-05-16.
- ^ Saladino R, Crestini C, Ciciriello F, Costanzo G, Di Mauro E (December 2006). "About a formamide-based origin of informational polymers: syntheses of nucleobases and favourable thermodynamic niches for early polymers". Origins of Life and Evolution of the Biosphere. 36 (5–6): 523–531. Bibcode:2006OLEB...36..523S. doi:10.1007/s11084-006-9053-2. PMID 17136429. S2CID 36278915.
- ^ [1], "아데닌을 준비하는 프로세스", 1966-11-10 웨이백 머신에서 2021-05-26 보관
- ^ Sanchez RA, Ferris JP, Orgel LE (December 1967). "Studies in prebiotic synthesis. II. Synthesis of purine precursors and amino acids from aqueous hydrogen cyanide". Journal of Molecular Biology. 30 (2): 223–253. doi:10.1016/S0022-2836(67)80037-8. PMID 4297187.
- ^ Ferris JP, Orgel LE (March 1966). "An Unusual Photochemical Rearrangement in the Synthesis of Adenine from Hydrogen Cyanide". Journal of the American Chemical Society. 88 (5): 1074. doi:10.1021/ja00957a050.
- ^ Ferris JP, Kuder JE, Catalano AW (November 1969). "Photochemical reactions and the chemical evolution of purines and nicotinamide derivatives". Science. 166 (3906): 765–766. Bibcode:1969Sci...166..765F. doi:10.1126/science.166.3906.765. PMID 4241847. S2CID 695243.
- ^ Oro J, Kamat SS (April 1961). "Amino-acid synthesis from hydrogen cyanide under possible primitive earth conditions". Nature. 190 (4774): 442–443. Bibcode:1961Natur.190..442O. doi:10.1038/190442a0. PMID 13731262. S2CID 4219284.
- ^ Bauer W (1985). Houben-Weyl Methods of Organic Chemistry Vol. E 5, 4th Edition Supplement. Thieme Georg Verlag. p. 1547. ISBN 9783131811547.
- ^ Hassner A, Stumer C (2002). Organic Syntheses Based on Name Reactions (2nd ed.). Elsevier. ISBN 0-08-043259-X.
- ^ Nam I, Nam HG, Zare RN.수성 마이크로액적 중 푸린과 피리미딘 리보뉴클레오시드의 비생물학적 합성.Proc Natl Acad Sci U S. 2018년 1월 2일;115 (1):36-40.doi:10.1073/pnas.1718559115.Epub 2017년 12월 18일.PMID 29255025, PMCID: PMC5776833
- ^ Becker S, Thoma I, Deutsch A, Gerhke T, Mayer P, Zipse H, Carell T.고수율, 엄격히 위치선택적인 프리바이오틱 퓨린 뉴클레오시드 형성 경로.과학. 2016년 5월 13일;352(6287):833-6. doi:10.1126/science.aad2808.PMID 27174989.