옥살로아세트산
Oxaloacetic acid | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 옥소부탄디오산 | |
| 기타 이름 옥살로아세트산 옥살아세트산 2-옥소수신산 케토숙신산 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.005.755 |
| EC 번호 |
|
PubChem CID | |
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| C4H4O5 | |
| 몰 질량 | 132.07 g/140 |
| 밀도 | 1.6 g/cm3 |
| 녹는점 | 161 °C (322 °F, 434 K) |
| 열화학 | |
표준 엔탈피/ 형성 (δHf⦵298) | -943.21 kJ/mol |
표준 엔탈피/ 연소 (δHc⦵298) | - 1205.58 kJ/mol |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
옥살아세트산(옥살아세트산 또는 OAA라고도 함)은2 화학식이 HOCC(O22)CHCOH인 결정성 유기 화합물이다. 옥살아세트산은 결합염기 옥살아세트산 형태로 동물에서 일어나는 많은 과정의 대사 중간체이다.글루코네시스, 요소 회로, 글리옥실산 회로, 아미노산 합성, 지방산 합성 및 구연산 [1]회로에 관여합니다.
특성.
옥살로아세트산은 연속적인 탈양성자를 거쳐 이이온을 얻는다.
- HOCC2(O)CHCOH22 occ−2 OCC(O)CHCOH22 + H+, pKa = 2.22
- −OCC2(O)CHCOH22 occ−2 OCC(O)CHCO22− + H+, pKa = 3.89
높은 pH에서 에놀화 가능한 양성자는 이온화된다.
- −OCC2(O)CHCO22− occ−2 OCC(O−)CHCO2− + H+, pKa = 13.03
옥살로아세트산의 에놀 형태는 특히 안정적이기 때문에 두 tameter의 녹는점이 서로 다르다(시스 등소형의 경우 152°C, 트랜스 등소형의 경우 184°C).이 반응은 옥살아세트산 호변이효소에 의해 촉매된다. 트랜스-에놀-옥살아세트산은 주석산이 후마라아제 [2]기질일 때도 나타난다.

생합성
옥살로아세테이트는 자연에서 여러 가지 방법으로 형성된다.주요 경로는 구연산 회로에서 말산탈수소효소에 의해 촉매되는 L-말산 산화에 의한 것이다.또한 말산은 숙신산탈수소효소에 의해 느린 반응으로 산화되며, 초기 생성물은 [3]에놀옥살아세트산이다.
또한 ATP의 가수분해에 의해 유도되는 피루브산과 탄산의 응축에서 발생한다.
- CHC3(O)CO2− + HCO3− + ATP → OCCHC−22(O)CO2− + ADP + Pi
식물의 중엽에서 발생하는 이 과정은 포스포에놀피루브산을 통해 진행되며, 포스포에놀피루브산카르복실화효소에 의해 촉매된다.
옥살아세트산은 아스파라긴산의 트랜스 또는 탈아미네이션에서도 발생할 수 있다.
생화학적 기능
옥살아세트산은 아세틸-CoA와 반응하여 구연산 합성효소에 의해 촉매되는 구연산 회로의 중간체이다.또한 포도당 생성, 요소 회로, 글리옥실산 회로, 아미노산 합성 및 지방산 합성에 관여합니다.옥살아세테이트는 또한 복합체 II의 강력한 억제제이다.
글루코네제
글루코네제네시스(Gluconeogenesis)는[1] 일련의 효소 촉매 반응으로 구성된 대사 경로로, 비탄수화물 기질로부터 포도당을 생성한다.이 과정의 시작은 피루브산염 분자가 발견되는 미토콘드리아 매트릭스에서 일어난다.피루브산 분자는 피루브산 카르복실화효소에 의해 카르복실화되며, 각 ATP 및 물 분자에 의해 활성화된다.이 반응은 옥살아세트산염의 형성을 일으킨다.NADH는 옥살아세트산을 말산으로 환원시킨다.이 변환은 미토콘드리아 밖으로 분자를 운반하기 위해 필요하다.일단 세포에 들어가면, 말산은 NAD+를 사용하여 다시 옥살아세트산염으로 산화된다.그리고 나서 옥살아세트산은 나머지 반응이 일어나는 세포에 남습니다.옥살아세트산은 나중에 포스포에놀피루브산카르복시키나제에 의해 탈탄산화 및 인산화되며 구아노신3인산(GTP)을 인산염원으로 사용하여 2-포스포에놀피루브산이 된다.포도당은 한층 더 하류 처리 후에 얻을 수 있다.
요소 순환
요소 회로는 분해된 아미노산으로부터 하나의 암모늄 분자, 아스파르트산으로부터 다른 암모늄 분자,[1] 그리고 중탄산염 분자 하나를 사용하여 요소를 형성하게 하는 대사 경로입니다.이 경로는 간세포에서 흔히 발생한다.요소 회로와 관련된 반응은 NADH를 생성하며 NADH는 두 가지 다른 방법으로 생성될 수 있다.이들 중 하나는 옥살아세트산염을 사용한다.세포질에는 푸마르산염 분자가 있다.푸마르산염은 푸마라아제 효소의 작용에 의해 말산으로 변할 수 있다.말산은 말산탈수소효소에 의해 작용하여 옥살아세트산이 되어 NADH 분자를 생성한다. 그 후, 트랜스아미나아제들이 다른 케토산을 선호하기 때문에 옥살아세트산은 아스파르트산염으로 재활용된다.이 재활용은 세포로 들어가는 질소의 흐름을 유지합니다.
글리옥실산회로
글리옥실산 회로는 구연산 [4]회로의 변형이다.이것은 이소시트르산분해효소 및 말산합성효소를 이용하여 식물과 박테리아에서 발생하는 동화 경로이다.회로의 일부 중간 단계는 구연산 회로와 약간 다르다. 그럼에도 불구하고 옥살아세트산은 [1]두 과정 모두에서 동일한 기능을 가진다.즉, 이 회로에서 옥살아세트산은 1차 반응물 및 최종 생성물로서도 작용한다.사실 옥살아세트산염은 글리옥실산염 순환의 루프가 아세틸-CoA의 두 분자를 포함하고 있기 때문에 글리옥실산염 순환의 순산물이다.
지방산 합성
이전 단계에서 아세틸-CoA는 미토콘드리아에서 지방산 합성효소가 상주하는 세포질로 전달된다.아세틸-CoA는 구연산염으로 운반되며, 구연산염은 아세틸-CoA와 옥살로아세테이트로부터 미토콘드리아 매트릭스에서 이전에 형성되었다.이 반응은 보통 구연산 순환을 시작하지만, 에너지가 필요하지 않을 때 세포질로 운반되고, 세포질은 세포질 아세틸 -CoA와 옥살아세트산염으로 분해된다.
주기의 다른 부분은 지방산 [5]합성을 위해 NADPH를 필요로 한다.이 환원력의 일부는 내부 미토콘드리아층이 옥살아세테이트를 투과할 수 없는 한 세포질 옥살아세테이트가 미토콘드리아로 되돌아갈 때 발생한다.먼저 옥살아세트산염은 NADH를 사용하여 말산염으로 환원된다.그런 다음 말산은 피루브산으로 탈탄산된다.이제 이 피루브산은 쉽게 미토콘드리아로 들어가 피루브산 카르복실화효소에 의해 다시 옥살아세트산으로 카르복실화된다.이와 같이 미토콘드리아에서 세포질로 아세틸-CoA가 전달되면 NADH 분자가 생성된다.자발적인 전반적인 반응은 다음과 같이 요약할 수 있다.
- HCO3– + ATP + 아세틸-CoA → ADP + Pi + 말로닐-CoA
아미노산합성
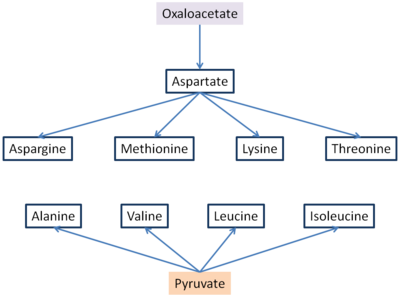
옥살아세트산 및 [6]피루브산으로부터 6개의 필수 아미노산과 3개의 비필수 아미노산을 합성한다.아스파르트산염 및 알라닌은 각각 옥살아세트산염 및 피루브산염에서 글루탐산염으로부터의 트랜스아미네이션에 의해 형성된다.아스파라긴은 아스파르트산염의 아미드화에 의해 합성되며 글루타민은 NH4를 기증한다.이것들은 비필수 아미노산이고, 그들의 간단한 생합성 경로는 모든 유기체에서 발생한다.메티오닌, 트레오닌, 리신, 이소류신, 발린, 류신은 인간과 대부분의 척추동물에서 필수적인 아미노산이다.박테리아에서 그들의 생합성 경로는 복잡하고 상호 연결되어 있다.
옥살산염생합성
옥살아세트산은 가수분해로 [7]옥살산염을 생성한다.
- 옥살아세트산염2+HOγ옥살산염+아세테이트
이 과정은 옥살로아세타아제 효소에 의해 촉매된다.이 효소는 식물에서는 볼 수 있지만 동물의 [8]세계에서는 알려져 있지 않다.
인터랙티브 패스 맵
| 아래의 유전자, 단백질 및 대사물을 클릭하여 각각의 기사와 연결하세요.[§ 1] 당분해 및 글루코네제네시스 편집
| 아래의 유전자, 단백질 및 대사물을 클릭하여 각각의 기사와 연결하세요. [§ 1] |
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d Nelson, David L.; Cox, Michael M. (2005). Principles of Biochemistry (4th ed.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ van Vugt-Lussenburg, BMA; van der Weel, L; Hagen, WR; Hagedoorn, P-L (February 26, 2021), "Biochemical Similarities and Differences between the Catalytic [4Fe-4S] Cluster Containing Fumarases FumA and FumB from Escherichia coli", PLOS ONE (published February 6, 2013), 8 (2): e55549, doi:10.1371/journal.pone.0055549, PMC 3565967, PMID 23405168
- ^ M.V. Panchenko; A.D. Vinogradov (1991). "Direct demonstration of enol-oxaloacetate as an immediate product of malate oxidation by the mammalian succinate dehydrogenase". FEBS Letters. 286 (1–2): 76–78. doi:10.1016/0014-5793(91)80944-X. PMID 1864383.
- ^ "Welcome to The Chemistry Place". www.pearsonhighered.com. Retrieved 5 April 2018.
- ^ "fatty acids synthesis". www.rpi.edu.
- ^ https://web.archive.org/web/20131021203457/http://faculty.ksu.edu.sa/69436/Documents/lecture-15-aa_from_oxaloacetate_and_pyruvate.pptx. Archived from the original on 2013-10-21. Retrieved 2013-10-21.
{{cite web}}:누락 또는 비어 있음title=(도움말) - ^ Gadd, Geoffrey M. "구연산과 옥살산의 풍아 생산: 금속의 분화, 생리학 및 생물 지구 화학적 과정의 중요성" 미생물 생리학에서의 진보(1999), 41, 47-92.
- ^ 쉬, 화웨이. "옥살산염 축적 및 규제는 벼잎의 글리콜산 산화효소와는 무관합니다." 실험 식물학 저널 제57권, 제9페이지 1899-1908, 2006년