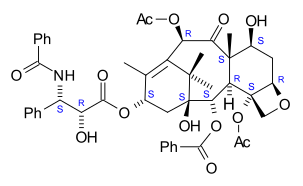
파클리탁셀
Paclitaxel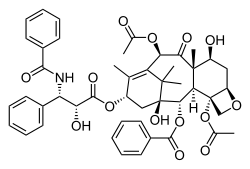 | |
 | |
| 임상 데이터 | |
|---|---|
| 상호 | Taxol, 기타 |
| AHFS/Drugs.com | 모노그래프 |
| Medline Plus | a607070 |
| 라이선스 데이터 |
|
| 임신 카테고리 |
|
| 루트 행정부. | 정맥주사(IV) |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 | |
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 6.5% (입에 [2]의한) |
| 단백질 결합 | 89 ~ 98 % |
| 대사 | 간(CYP2C8 및 CYP3A4) |
| 반감기 제거 | 5.8시간 |
| 배설물 | 분변과 소변 |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| PDB배위자 | |
| CompTox 대시보드 (EPA ) | |
| ECHA 정보 카드 | 100.127.725 |
| 화학 및 물리 데이터 | |
| 공식 | C47H51NO14 |
| 몰 질량 | 853.918 g/120−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
Paclitaxel(PTX)은 여러 종류의 [3]암을 치료하기 위해 사용되는 화학요법 약물이다.이것은 난소암, 식도암, 유방암, 폐암, 카포시 육종, 자궁경부암,[3] 췌장암을 포함한다.정맥주사로 [3]투여한다.알부민 결합 [3]배합도 있습니다.
일반적인 부작용으로는 탈모, 골수 억제, 저림, 알레르기 반응, 근육통,[3] 설사 등이 있다.다른 심각한 부작용으로는 심장 질환, 감염 위험 증가, 폐 염증이 [3]있다.임신 중에 복용하면 선천성 [4][3]기형의 원인이 될 수 있다는 우려가 있습니다.Paclitaxel은 약의 [5]택산 계열에 속합니다.그것은 세포 [3]분열 중에 미소관의 정상적인 기능에 간섭하여 작용한다.
Paclitaxel은 1971년 태평양 주목에서 처음 분리되었고 1993년 [6][7]의료용으로 승인되었다.그것은 세계보건기구의 필수 [8]의약품 목록에 있다.그것은 전구체로부터 만들어졌고, 최근에는 세포 [7]배양에 의해 만들어졌다.
의료용
Paclitaxel은 영국에서 카포시 [9]육종뿐만 아니라 난소, 유방, 폐, 방광, 전립선, 흑색종, 식도 및 다른 유형의 고형 종양 암에 대해 승인되었습니다.
2001년 6월 미국 국립보건관리연구소(NICE)의 지침에서는 치료용으로는 부적합한 환자의 비소세포 폐암과 난소암의 1차 및 2차 치료에 사용할 것을 권고하고 있다.2001년 9월, NICE는 파클리탁셀을 무연환 화학요법 실패 후 진행된 유방암 치료에 사용할 수 있어야 하지만, 최초 사용은 임상시험으로 제한되어야 한다고 권고했다.2006년 9월, NICE는 파클리탁셀을 초기 림프절 [10]양성 유방암의 보조 치료에 사용하지 말 것을 권고했다.2018년에는 미국에서 유방암, 췌장암,[11][12] 난소암, 카포시 육종 및 비소세포 폐암 치료에 대한 승인을 받았다.
유사 화합물
알부민 결합 파클리탁셀(상표명 아브락산, nab-paclitaxel이라고도 함)은 파클리탁셀이 알부민 나노 입자와 결합하는 대체 제제이다.파클리탁셀의 임상 독성의 대부분은 용매 크레모포 EL과 관련이 있으며,[13] 용매 크레모포 EL은 전달을 위해 용해됩니다.
Abraxis BioScience는 Abraxane을 개발했는데, 이 Abraxane은 파클리탁셀이 종종 독성이 있는 용매 전달 방법의 대체 전달제로 알부민과 결합되어 있다.이는 2005년 1월 FDA에 의해 전이성 질환에 대한 결합 화학요법 실패 또는 보조 화학요법 [14]6개월 이내 재발 후 유방암 치료를 위해 승인되었다.이후 국소적으로 진행되거나 전이되는 비소세포 폐암과 췌장의 전이성 선암에 대해서도 [15]승인되었다.
파클리탁셀 생산에 대한 합성적 접근은 Docetaxel의 개발로 이어졌다.Docetaxel은 paclitaxel과 유사한 임상 용도를 가지고 있으며, Taxotere라는 브랜드명으로 판매되고 있습니다.
파클리탁셀, 10-데아세틸바카틴 III, 바카틴 III, 파클리탁셀 C 및 7-에피파클리탁셀을 포함한 택산은 [16]헤이즐의 잎과 껍질에서 발견되었다.많은 식품 산업에서 대량 생산되고 있으며 폐기된 물질로 간주되는 조개껍데기에서 이러한 화합물이 발견됨에 따라 파클리탁셀의 향후 가용성에 관심이 모아지고 있습니다.
재협착
파클리탁셀은 관상동맥 및 말초 스텐트의 재협착(재협착)을 방지하기 위한 항증식제로서 사용되며, 국소적으로 동맥의 벽에 전달되는 파클리탁셀 코팅은 스텐트 내의 [17]네오티마(scar tissue)의 성장을 제한한다.관상동맥 배치를 위한 파클리탁셀 약제 배출 스텐트는 미국에서 보스턴 사이언티픽의 상표명 Taxus로 판매된다.대퇴골동맥 배치를 위한 파클리탁셀 약제 배출 스텐트도 이용할 수 있다.
부작용
일반적인 부작용으로는 메스꺼움과 구토, 식욕부진, 맛의 변화, 가늘어지거나 부서지기 쉬운 털, 팔이나 다리 관절의 통증, 손톱 색깔의 변화, 손이나 [18]발가락의 따끔거림 등이 있다.이상타박상, 출혈, 통증, 발적, 붓기, 손발증후군, 2일 이상 정상적인 배변습관 변화, 발열, 오한, 기침, 인후통, 삼키기 어려움, 어지럼증, 호흡곤란, 심한 피로감, 피부발진, 안면홍조, 난자에 의한 여성불임 등의 심각한 부작용리안 손상, 가슴 통증도 발생할 [18]수 있습니다.신경장애도 생길 [3]수 있다.
덱사메타손은 [19]일부 부작용을 완화하기 위해 파클리탁셀 주입 전에 투여된다.
이러한 부작용의 상당수는 사용되는 파출소와 관련되어 있으며, 폴리옥시에틸화 피마자유인 크레모포 EL과 시클로스포린, 테니포시드에 대한 알레르기와 폴리옥시에틸화 피스타유를 포함한 다른 약물에 대한 알레르기는 파클리탁셀에 [20]대한 부작용 위험을 증가시킬 수 있다.
작용 메커니즘
파클리탁셀은 튜브린을 표적으로 하는 여러 세포골격제 중 하나이다.파클리탁셀 처리 세포는 유사분열 방추 조립, 염색체 분리, 세포 분열에 결함이 있다.코르히틴과 같은 미세관 조립을 억제하는 다른 튜브린 표적 약물과 달리 파클리탁셀은 미세관 폴리머를 안정화시켜 분해로부터 보호합니다.따라서 염색체는 중기의 스핀들 구성을 달성할 수 없다.이는 유사분열 진행과 유사분열 체크포인트의 장기 활성화를 차단하며 세포분열 [21][22]없이 세포주기의 G0상으로의 회귀 또는 아포토시스를 유발한다.
paclitaxel의 스핀들 기능을 억제하는 능력은 일반적으로 미세관 역학 [23]억제에 기인하지만, 다른 연구에서는 유사분열을 차단하는 데 필요한 농도보다 낮은 농도에서 역학 억제가 일어난다는 것을 보여주었다.높은 치료 농도에서 파클리탁셀은 유사분열 [24]중에 정상적으로 활성화되는 과정인 중심체로부터의 미세관 분리를 억제하는 것으로 보인다.파클리탁셀은 미세관의 [25]베타 튜브린 서브유닛에 결합한다.
화학
paclitaxel의 명명법은 4환식 17원자 골격 위에 구조되어 있다.총 11개의 스테레오 센터가 있습니다.활성 입체 이성질체는 (-)-파클리탁셀(여기 표시)이다.
생산.
나무껍질 가공
1967년부터 1993년까지 생산된 거의 모든 파클리탁셀은 태평양 주목의 나무껍질인 택수스 브레비폴리아에서 추출되었으며,[26] 그 과정에서 나무가 죽었다.사용된 공정은 먼로 월과 만수크 와니의 원래 격리 방법의 후예입니다. 1987년까지 미국 국립 암 연구소(NCI)는 콜로라도 볼더에 있는 하우저 화학 연구소와 계약하여 단계 II 및 III [citation needed]실험에 필요한 규모로 나무껍질을 처리하도록 했습니다.태평양 주목의 야생 개체수와 파클리탁셀의 최종 수요 규모는 불확실했지만, 천연물의 대체적이고 지속 가능한 원천이 필요하다는 것은 분명했다.처음에 소싱 범위를 넓히려는 시도에서는 나무에서 바늘을 사용하거나 재배된 [citation needed]것을 포함한 다른 관련 택서스 종의 재료를 사용했지만, 이러한 시도는 상대적으로 낮고 종종 변동성이 큰 수확량 때문에 어려움을 겪었다.1990년대 초, 태평양 북서부 숲의 생태에 대한 민감도가 높아짐에 따라, 파클리탁셀은 이러한 [27]소스로부터 임상적으로 유용한 규모로 성공적으로 추출되었습니다.
반합성
동시에, 미국과 프랑스의 합성 화학자들은 [citation needed]1970년대 후반부터 파클리탁셀에 관심을 가지고 있었다.앞서 언급한 바와 같이, 1992년까지 파클리탁셀의 총합성을 달성하기 위한 광범위한 노력이 진행되었으며, 이는 실용적인 상업적 생산보다는 새로운 화학적 이해를 창출하고자 하는 욕구에 자극되었다.이와는 대조적으로, CNRS(Centre National de la recherche scientifique)의 피에르 포티에 프랑스 그룹은 전체 공정 수율 문제를 다루었고, 이는 CNRS 캠퍼스에서 성장한 Taxus baccatin이라는 유럽의 주목으로부터 비교적 많은 양의 10-deacetylbacatin 화합물을 분리하는 것이 가능하다는 것을 보여주었다.대량으로 [citation needed]입수할 수 있습니다.그 구조상 10-데아세틸바카틴은 파클리탁셀을 생성하기 위한 짧은 반신합성의 실행 가능한 시작 물질로 간주되었다.1988년, 포이티에와 공동 연구진은 유럽 주목의 바늘에서 [28]파클리탁셀까지 반합성 경로를 발표했다.
그러나 NCI의 견해는 이 루트조차 [citation needed]실용적이지 않다는 것이었다.로버트 A의 그룹. Holton은 또한 실용적인 반합성 생산 경로를 추구했다; Holton의 그룹은 1989년 말에 Potier [citation needed]공정의 두 배의 수율로 파클리탁셀로 가는 반합성 경로를 개발했다.홀튼이 일했던 플로리다 주립대학은 브리스톨 마이어스 스퀴브(BMS)와 반합성 및 미래 [citation needed]특허를 허가하는 계약을 체결했다.1992년 Holton은 80%의 수율로 개선된 공정을 특허 받았으며, BMS는 이 공정을 자체 도입하여 유럽 [citation needed]주목의 침엽에서 분리된 10-deacetylbacatin으로부터 아일랜드에서 파클리탁셀을 제조하기 시작했습니다.1993년 초, BMS는 1995년 말까지 태평양 주목나무 껍질에 대한 의존을 중단하겠다고 발표했고,[citation needed] 그 사용에 대한 생태학적 논란은 사실상 종결되었습니다.이 발표는 1989년 공동연구개발협정(CRADA) 적용에서 NCI에 대해 이루어진 대체 공급경로를 개발하겠다는 약속도 이행했다.
2013년 현재, BMS는 유럽 주목의 바늘을 이용한 반합성 방법을 사용하여 파클리탁셀을 [29]생산하고 있습니다.2012년까지 [30]BMS와 협력한 또 다른 기업 Phyton Biotech, Inc.는 식물 세포 발효([31]PCF) 기술을 사용하고 있습니다.발효 탱크에서 특정 Taxus 세포주를 배양함으로써, 그들은 더 이상 실제 주목나무 [32]농장에서 재료를 지속적으로 조달할 필요가 없다.이어서 약 40%의 파클리탁셀을 함유하는 고농축 분말에 농축할 수 있는 수지에 의해 현탁액에서 직접 파클리탁셀을 포획한다.그런 다음 이 화합물은 한 번의 크로마토그래피 단계에 이어 결정화 [33]과정을 거쳐 정제된다.반합성법에 비해 PCF는 유해한 화학물질이 많이 필요하지 않으며 상당한 [34]양의 에너지를 절약합니다.
1993년, [35]주목나무에 사는 새로 기술된 내생균에서 자연산물로 파클리탁셀이 발견되었다.그것은 이후로 다른 식내서성 균류의 Nodulisporium sylviforme,[표창 필요한]알 터 나리아 택시, 크라도 스포 리움 속 cladosporioides MD2, Metarhizium anisopliae, 아스 페르질 candidus MD3, 털곰팡이 rouxianus, Chaetomella raphigera, Phyllosticta tabernaemontanae, Phomopsis, Pestalotiopsis pauciseta, Phyllosticta citricarp 포함한 많은 문화에서 보고되었다., 포도 카르 푸스류. , Fusarium solani, Pestalotiopsis terminaliae, Pestalotiopsis breviseta, Botryodiplodia theobromae, Gliocladium sp., Alternaria alternata var. monosporus, Cladosporaides, Cladospora spolioides, Nigospora spora spora sp.그러나, 다른 연구들이 독립적으로 생산될 가능성이 [36][37]낮다는 것을 발견하면서, 내생식물에 의한 생산에는 모순된 증거가 있었다.
생합성
택솔은 4환식 디터펜으로 디터펜의 생합성은 IPP 분자의 첨가에 의해 길어진 FPP 분자로 시작하여 제라닐게라닐이인산(GPP)[38]을 형성한다.Taxol의 생합성에는 [39]19단계가 있다.이 19단계는 여러 단계로 고려될 수 있으며, 첫 번째 단계는 일련의 산소화를 거치는 택산 골격의 형성이다.산소화에 이어 두 개의 아세틸화와 벤조일화가 중간에서 발생합니다.택산 코어의 산소화는 C5와 C10, C2와 C9, C13에 이어 C7, 그리고 나중에 경로에서 C1 수산화에서 발생하는 것으로 여겨진다.경로의 후반부에서 C9에서의 산화는 케톤 관능기와 옥세탄을 형성하여 중간 바카틴 III를 형성한다.경로의 마지막 단계는 바카틴 [40]III에 부착된 C13 측쇄의 형성을 포함한다.Taxol의 생합성은 그림에서 더 자세히 설명되며, 1~7단계는 모두 Taxadiene Synthase 효소(그림의 TS)에서 발생한다.Taxol의 생합성은 SN1 메커니즘을 통해 E, E, E-GPP가 피로인산을 잃는 것으로 시작된다(그림의 1단계).이중 결합은 친전자성 첨가를 통해 양이온을 공격하여 3차 양이온을 생성하고 첫 번째 링 폐쇄를 만듭니다(2단계).또 다른 친전자성 공격이 일어나 제1의 6원환을 생성하고 또 다른 제3의 양이온을 생성함으로써 구조를 더욱 환화시킨다(스텝 3).분자내 양성자 이동이 일어나 버티실릴 양이온을 공격하고(스텝 4), 이중 결합을 형성하여 3차 양이온을 생성한다.스텝 5에서 친전자성 사이클라이제이션이 일어나 분자 내 양성자 전달이 타세닐 양이온을 공격한다(스텝 6).이것은 Taxadien으로 알려진 융합 고리 구조의 중간체를 형성합니다.그런 다음 Taxadiene는 NADPH를 통해 일련의 10가지 산화를 거치며 중간 Taxadiene-5α-acetoxy-10β-ol을 형성한다(그림의 후반부에서 여러 단계).일련의 히드록실화 및 에스테르피시화가 발생하여 중간 10-탈아세틸-바카틴 III를 형성하고, 중간 10-탈아세틸-바카틴 III는 에스테르화 및 측쇄 히드록실화를 [38]거친다.이것은 마침내 제품 택솔을 산출한다.
종합합성
1992년까지 전 세계 최소 30개 학술 연구팀이 이 천연물의 총합성을 위해 노력했으며, 단순한 천연물과 기타 쉽게 구할 수 있는 시작 [41]물질로부터 합성을 진행하였다.이러한 종합 합성 노력은 주로 파클리탁셀의 실질적인 상업적 생산에 대한 기대보다는 새로운 화학적 이해를 창출하고자 하는 욕구에 의해 동기 부여되었다.훨씬 덜 복잡한 시작 물질에서 전체 합성을 완료한 첫 번째 실험실은 로버트 A의 연구 그룹이었다. 홀튼은 K.C.의 첫 번째 기사를 출판할 수 있었다. 니콜라우는 1994년 2월 7일에 첫 기사를 인쇄했다.비록 홀턴 제출한 달 말까지 Nicolaou 전에 출판물 각 이 거대한 양, 다년간efforts—11–18 작가들 각각의 1994년 2월 publications—has의에 나타나고 이로 인하여 발생되는 가까운 우연의 일치 그 경주의 끝이"넥타이"[43]또는"사진 판정"[41]주의로 불린 것을 이끌(2112월 1993년 대 1월 24일 1994년)[42].eac지만H그룹은 그들의 합성 전략과 전술이 [43]우월하다고 주장해 왔다.
2006년 현재, 5개의 추가 연구 그룹이 파클리탁셀의 총 합성에 성공했다고 보고했다.1997년에는 Wender 등, 1998년에는 Kwajima 등, 1998년에는 Mukaiyama 등, 1996년에는 Danishefsky 등, 2006년에는 Takahashi 등.[needs update]그 날 현재 모든 전략은 ABCD 고리 시스템을 포함하는 10-deacetylbaccatin-type core를 준비하는 것을 목표로 하고 있으며, 그 후 일반적으로 13-hydroxyl group에 "[41]꼬리"를 추가하는 것이 일반적이었다.
"1990년대 초반 [파클리탁셀]과 [태평양 주목]을 둘러싼 정치적 풍토"는...토탈 합성과 공급 문제 사이의 [a] 연관성을 강화하는 데 도움이 되었다." 그리고 토탈 합성 활동은 테스트를 위한 아날로그 생성을 통해 파클리탁셀의 구조-활성 관계를 탐구하는 데 필요했지만, 토탈 합성 노력은 유의한 수량을 제공하기 위한 "심각한 상업적 경로"로 간주되지 않았다.es 의학적 테스트 또는 치료적 사용을 [44]위한 천연 제품.
역사
파클리탁셀의 발견은 1962년 NCI가 지원하는 스크리닝 [7]프로그램의 결과로 시작되었다.몇 년 후 태평양 주목의 나무껍질인 택수스 브레비폴리아에서 분리되었고, 그래서 "택솔"[7]이라는 이름이 붙여졌다.
이 발견은 먼로 E에 의해 이루어졌다. 월과 만석 C. 1971년 [45]노스캐롤라이나주 트라이앵글 파크에 있는 리서치 트라이앵글 연구소의 Wani.이 과학자들은 주목나무 껍질에서 천연물을 분리해 구조를 결정하고 "택솔"이라는 이름을 붙여 첫 번째 생물학적 실험을 [citation needed]준비했다.이 화합물은 BMS에 의해 상업적으로 개발되었으며, BMS는 "paclitaxel"[citation needed]이라는 총칭으로 지정되었습니다.
식물 선별 프로그램
1955년, 미국의 NCI는 외부 기관과 [46]회사가 제출한 화합물의 항암 활동을 위한 공공 선별 센터 역할을 하는 암 화학 치료 국립 서비스 센터(CCNSC)를 설립했습니다.선별된 대부분의 화합물은 합성 기원이었지만 1958년부터 그곳에서 근무한 화학자 조나단 하트웰은 천연물 유도 화합물에 대한 경험이 있어 식물 선별 [47]작업을 시작했다.1960년 7월 NCI는 미국 농무부(USDA) 식물학자에게 연간 [48]약 1,000종의 식물 표본을 수집하도록 의뢰했다.1962년 8월 21일, 식물학자 중 한 명인 Arthur S. Barclay는 200종 이상의 다른 종으로부터 물질을 수집하기 위한 4개월간의 여행의 일환으로 워싱턴 팩우드 마을 북쪽 숲에 있는 태평양 주목 나무에서 나무껍질을 수집했다.그 후 다수의 전문 CCNSC 하청업체에서 이 물질을 처리했으며,[49] 1964년 5월 22일 세포 분석에서 나무의 샘플 중 하나가 세포 독성이 있는 것으로 밝혀졌다.
따라서 1964년 말 또는 1965년 초에 먼로 E가 운영하는 분리 분리 연구소가 설립되었습니다.노스캐롤라이나주, 리서치 트라이앵글 파크의 월은 1966년 9월에 새로운 택서스 샘플에 대한 연구를 시작했고, 1967년 4월 마이애미 [50]비치에서 열린 미국 화학 협회 회의에서 그 발견을 발표했다.그들은 1967년 [49]6월에 순수 복합 택솔이라는 이름을 붙였다.월과 그의 동료인 와니는 1971년에 [51]화학 구조를 포함한 결과를 발표했다.
NCI는 더 많은 Taxus 나무껍질을 채취하고 증가하는 Taxol의 양을 분리하기 위한 작업을 계속했다.1969년까지 약 1,200kg(2,600lb)의 나무껍질에서 28kg(62lb)의 원유 추출물이 분리되었지만, 최종적으로는 10g(0.35oz)의 순수한 [52]물질만 산출되었지만, 몇 년 동안 NCI는 이 화합물을 사용하지 않았다.1975년, 그것은 다른 체외 시스템에서 활성화된 것으로 나타났다. 2년 후, 새로운 부서장이 데이터를 검토하고 마침내 발견 [53]과정의 다음 단계로 이동할 것을 권고했다.이를 위해 정제된 타졸의 양을 최대 600g(21온스)까지 늘려야 했으며 1977년에는 7,000파운드(3,200kg)의 나무껍질을 추가로 요청했다.
1978년, 두 명의 NCI 연구자는 백혈병 [54]생쥐에게 타키솔이 약간 효과가 있다는 보고서를 발표했다.1978년 11월, 타키솔은 이종 이식 연구에 [55]효과가 있는 것으로 나타났다.한편, Taxol은 1979년 초에 Susan B에 의해 출판되면서 세포 생물학뿐만 아니라 암 사회에서도 잘 알려지기 시작했다. Albert Einstein 의과대학의 분자 약리학자인 Horwitz는 택솔이 미세관의 안정화와 관련된 이전에는 알려지지 않은 작용 메커니즘을 가지고 있다는 것을 보여주었다.제제 문제와 함께, 연구자들의 관심 증가는 1980년까지 NCI가 20,000파운드(9,100 kg)의 나무껍질을 [56]수집해야 한다는 것을 의미했다.동물 독성학 연구는 1982년 6월까지 완료되었고, 11월에 NCI는 인간 [56]임상시험을 시작하는 데 필요한 IND를 신청했다.
초기 임상시험, 공급 및 BMS로의 이행
1984년 4월에 임상 1상이 시작되었고, [57]1년 후에 임상 2상을 시작하기로 결정이 내려졌다.이 더 큰 실험들은 더 많은 나무껍질이 필요했고 12,000파운드의 추가 수집이 의뢰되었고, 이것은 1986년 말까지 일부 2단계 실험을 시작할 수 있게 했다.하지만 그때쯤에는 택솔에 대한 수요가 상당할 수 있고 최소한 60,000파운드 이상의 나무껍질이 필요할 수도 있다는 것이 인식되었다.이 전례 없이 많은 양이 지역 정치인들과 산림민들이 이 프로그램에 [58]불안을 표시하면서 주목 인구에 미치는 영향에 대한 생태학적 우려를 처음으로 집중시켰다.
1988년 5월 2기 임상시험의 첫 번째 공개보고서는 흑색종과 난치성 [59]난소암에 대한 유망한 효과를 보여주었다.이 시점에서 NCI의 천연물 지부의 Gordon Cragg는 미국의 모든 난소암과 흑색종 환자를 치료하기에 충분한 타키솔을 합성하려면 연간 36만 그루의 나무를 파괴해야 한다고 계산했다.처음으로 [58]공급 문제에 대한 진지한 검토가 이루어졌다.NCI는 실용적이고 특히 필요한 자금 규모 때문에 제약회사와의 제휴를 모색하기로 결정하였고, 1989년 8월 현재의 재고와 공급, 데이터에 대한 독점적 접근을 제공하는 공동 연구 개발 협정(CRADA)을 발표했다.r은 추가 원료 수집, 타키솔 분리 및 임상시험 자금 지원을 위해 자금을 제공할 의향이 있는 회사에 대해 수집되었습니다.택솔에 관한 상당한 학술서적의 저자인 굿맨과 웨일스의 말을 빌리자면, "NCI는 협력이 아니라 택솔의 양도(및 그 문제)[58]를 생각하고 있었다."
이 제안이 널리 알려졌지만, 1989년 12월 파트너로 선정된 미국 기업 브리스톨 마이어스 스퀴브(BMS)를 포함해 4개 회사만이 CRADA에 응답했다.BMS의 선택은 나중에 논란이 되었고 1991년과 1992년에 의회 청문회의 주제가 되었습니다.NCI가 상업적 파트너를 찾는 것 외에는 선택의 여지가 없었던 것은 분명하지만, 거래 조건에 대한 논란도 있었고, 결국 2003년 NIH가 [60]금전적 가치를 보장하지 못했다는 결론을 내린 회계 사무소의 보고서로 이어졌다.USDA 및 내무부와의 관련 CRADA에서 Bristol-Myers Squibb는 Taxus brevifolia의 모든 연방 공급에 대한 독점적인 첫 번째 거절을 받았다.이 독점 계약으로 인해 BMS가 "암 독점"[61]을 제공한다는 비판이 일고 있습니다.CRADA가 시행된 지 18개월 후, BMS는 신약 신청서(NDA)를 제출했고, 1992년 말 FDA의 승인을 받았습니다.[58] 이 화합물에 대한 특허는 없었지만 왁스맨 해치법의 조항은 브리스톨 마이어스 스퀴브에게 5년간의 독점 판매권을 부여했다.
1990년에 BMS는 Taxol(R)이라는 상표명을 Taxol(R)로 출원했습니다.이것은 1992년에 논쟁적으로 승인되었다.동시에 파클리탁셀은 화합물의 총칭(INN)인 타키솔을 대체했다.네이처 잡지를 포함한 비평가들은 taxol이라는 이름이 20년 이상 동안 그리고 600개가 넘는 과학 기사에서 사용되었다고 주장하며, 그 상표가 수여되지 말았어야 했고 BMS가 그것에 [62]대한 권리를 포기해야 한다고 주장했습니다.BMS는 이름을 변경하면 종양학자들이 혼란스러워하고 환자의 건강을 해칠 수 있다고 주장했습니다.BMS는 법정에서 [63]그 이름에 대한 권리를 계속 옹호해 왔습니다.BMS는 Goodman과 Walsh에 의해 잘못된 표현을 했다는 비판도 받고 있습니다.Goodman과 Walsh는 회사 보고서에서 "1971년이 되어서야...테스트...처음에 'paclitaxel'[64]로 설명되었던 파클리탁셀의 분리를 가능하게 했습니다.이 인용문은 엄밀히 말하면 정확하다: 이의는 이것이 복합 택솔이라는 이름을 붙인 것은 고립을 하는 과학자이며 20년 이상 동안 다른 어떤 방법으로도 언급되지 않았다는 오해를 불러일으킬 수 있는 설명을 게을리 한 것 같다.연간 매출은 2000년에 정점에 달해 16억달러에 달했습니다.현재 파클리탁셀은 범용 형태로 판매되고 있습니다.
사회와 문화
2006년 현재[update] 유방암 초기 환자 1인당 NHS 비용은 4주기를 치료한다고 가정할 때 약 4,000파운드(약)였다.6,[65]000달러).
조사.
카페인은 대장암세포에서 [66]파클리탁셀에 의해 유발되는 아포토시스를 억제하는 것으로 추측되고 있다.
파클리탁셀은 직접적인 임상적 사용 외에도 미세관 안정제로서 생물학 및 생물의학 연구에 광범위하게 사용된다.일반적으로 운동성 측정과 같은 미세관을 포함하는 시험관내 측정에서는 세포 내에서 발견되는 다양한 핵인자 및 기타 안정화 요소가 없을 때 미세관 무결성을 유지하기 위해 파클리탁셀에 의존합니다.예를 들어, 미세관 운동 단백질의 거동을 변화시키는 것을 목적으로 하는 약물의 시험관내 시험이나 돌연변이 운동 단백질의 연구에 사용된다.또한 Paclitaxel은 인슐린 섬유화를 억제하기 위해 시험관내 사용되었으며, 10:1 몰비(insulin:paclitaxel)에서 인슐린 섬유화를 70% 가까이 방해하였다.Iso-thermal tititiating calorometry(ITC) 소견은 파클리탁셀이 수소 결합과 판데르발 힘을 [67]통해 인슐린과 상호작용하는 자발적 경향을 나타냈다.또한 파클리탁셀의 억제역할은 파클리탁셀이 '오프패스웨이' 올리고머 중간체 형성을 유도하고 [68]이후 콜로이드 안정성을 높여 리조임 섬유화를 억제하는 것으로 관찰되었기 때문에 단백질 용액의 콜로이드 안정성에 미치는 영향에 기인한다.파클리탁셀은 생체 내 연구에도 사용된다; 그것은 초파리와 같은 유기체를 테스트하기 위해 공급되거나 세포 내 미세관 분해를 억제하거나 세포 내 미세관의 수를 증가시키기 위해 개별 세포에 주입될 수 있다.파클리탁셀은 체내[69] 탈수 생쥐에서 재수정을 유도하고 메틸에스테르 [70]측쇄를 통해 체외에서 hPAD2를 억제한다.앤지오텍 제약회사는 1999년[71] 다발성 경화증 치료제로 2상 임상시험을 시작했지만 2002년에는 통계적으로 [72]유의미한 결과가 나오지 않았다고 보고했다.
2016년 시험관내 다약물 내성 마우스 종양 세포는 엑소좀에 봉입된 파클리탁셀로 처리되었다.일반 용량보다 98% 적은 용량에서도 동일한 효과가 있었다.또한 염료가 표시된 엑소좀은 종양세포를 표시할 수 있어 [73][74]진단에 도움을 줄 수 있다.
기타 이미지
파클리탁셀의 공간충전 모델
레퍼런스
- ^ a b "Paclitaxel Use During Pregnancy". Drugs.com. 24 January 2019. Retrieved 19 May 2020.
- ^ Peltier S, Oger JM, Lagarce F, Couet W, Benoît JP (June 2006). "Enhanced oral paclitaxel bioavailability after administration of paclitaxel-loaded lipid nanocapsules". Pharmaceutical Research. 23 (6): 1243–50. doi:10.1007/s11095-006-0022-2. PMID 16715372. S2CID 231917.
- ^ a b c d e f g h i "Paclitaxel". The American Society of Health-System Pharmacists. Archived from the original on September 14, 2017. Retrieved January 2, 2015.
- ^ Berveiller P, Mir O (2012). "Taxanes during pregnancy: probably safe, but still to be optimized". Oncology. 83 (4): 239–40. doi:10.1159/000341820. PMID 22907122.
- ^ Chang AE, Ganz PA, Hayes DF, Kinsella T, Pass HI, Schiller JH, Stone RM, Strecher V (2007). Oncology: An Evidence-Based Approach. Springer Science & Business Media. p. 34. ISBN 9780387310565. Archived from the original on 2016-12-21.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 512. ISBN 9783527607495. Archived from the original on 2016-12-21.
- ^ a b c d "Taxol® (NSC 125973)". National Cancer Institute. Archived from the original on 5 September 2015. Retrieved 14 February 2016. 웨이백 머신
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Saville MW, Lietzau J, Pluda JM, Feuerstein I, Odom J, Wilson WH, et al. (July 1995). "Treatment of HIV-associated Kaposi's sarcoma with paclitaxel". Lancet (Submitted manuscript). 346 (8966): 26–8. doi:10.1016/S0140-6736(95)92654-2. PMID 7603142. S2CID 44624033. Archived from the original on 2019-06-26. Retrieved 2018-10-28.
- ^ "British National Formulary".
- ^ "Paclitaxel, Protein-Bound Suspension". Paclitaxel, Protein-Bound Suspension. Cancer.Org. January 6, 2015. Retrieved January 24, 2015.[영구 데드링크]
- ^ 제품 정보:TAXOL(R) IV 주사, 파클리탁셀 IV 주사.Bristol-Myers Squibb Company, 프린스턴, NJ, 2013.2018년 10월 4일 https://www.accessdata.fda.gov/drugsatfda_docs/label/2015/020262s051lbl.pdf에서 액세스.
- ^ Gelderblom H, Verweij J, Nooter K, Sparreboom A (September 2001). "Cremophor EL: the drawbacks and advantages of vehicle selection for drug formulation". European Journal of Cancer. 37 (13): 1590–8. doi:10.1016/S0959-8049(01)00171-X. PMID 11527683.
- ^ "2005-05-26 웨이백 머신에 Abraxane 약물 정보 보관"미국 식품의약국2005년 1월 7일2007년 3월 9일에 취득.
- ^ 제품정보 : ABRACHANE(R) 정맥주입 서스펜션, 파클리탁셀 단백질 결합입자 정맥주입 서스펜션.Celgene Corporation (FDA 기준), 서밋, 뉴저지, 2018.2018년 10월 4일 https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/021660s045lbl.pdf에서 액세스.
- ^ Ottaggio L, Bestoso F, Armirotti A, Balbi A, Damonte G, Mazzei M, et al. (January 2008). "Taxanes from Shells and Leaves of Corylus avellana". Journal of Natural Products. 71 (1): 58–60. doi:10.1021/np0704046. PMID 18163585.
- ^ Heldman AW, Cheng L, Jenkins GM, Heller PF, Kim DW, Ware M, et al. (May 2001). "Paclitaxel stent coating inhibits neointimal hyperplasia at 4 weeks in a porcine model of coronary restenosis". Circulation. 103 (18): 2289–95. doi:10.1161/01.CIR.103.18.2289. PMID 11342479.
- ^ a b Abou-Donia, Mohamed (5 February 2015). Mammalian Toxicology. John Wiley & Sons. p. 626. ISBN 978-1-118-68285-2.
- ^ Hoskins, William J. (2005). Principles and Practice of Gynecologic Oncology. Lippincott Williams & Wilkins. p. 531. ISBN 978-0-7817-4689-2.
- ^ "Medline Plus Entry for Paclitaxel Injection Archived at the Wayback Machine 2010-02-12." MEDLINE. 2008년 9월 1일 최종 리뷰.10-2-21에 접속.
- ^ Bharadwaj R, Yu H (March 2004). "The spindle checkpoint, aneuploidy, and cancer". Oncogene. 23 (11): 2016–27. doi:10.1038/sj.onc.1207374. PMID 15021889.
- ^ Brito DA, Yang Z, Rieder CL (August 2008). "Microtubules do not promote mitotic slippage when the spindle assembly checkpoint cannot be satisfied". The Journal of Cell Biology. 182 (4): 623–9. doi:10.1083/jcb.200805072. PMC 2518701. PMID 18710927.
- ^ Jordan MA, Wilson L (April 2004). "Microtubules as a target for anticancer drugs". Nature Reviews. Cancer. 4 (4): 253–65. doi:10.1038/nrc1317. PMID 15057285. S2CID 10228718.
- ^ Ganguly A, Yang H, Cabral F (November 2010). "Paclitaxel-dependent cell lines reveal a novel drug activity". Molecular Cancer Therapeutics. 9 (11): 2914–23. doi:10.1158/1535-7163.MCT-10-0552. PMC 2978777. PMID 20978163.
- ^ Löwe J, Li H, Downing KH, Nogales E (November 2001). "Refined structure of alpha beta-tubulin at 3.5 A resolution". Journal of Molecular Biology. 313 (5): 1045–57. doi:10.1006/jmbi.2001.5077. PMID 11700061.
- ^ Gersmann H, Aldred J (10 November 2011). "Medicinal tree used in chemotherapy drug faces extinction". The Guardian. Archived from the original on 16 February 2017. Retrieved 2017-02-15.
- ^ 굿맨 & 월시 2001, 페이지 172-5
- ^ 굿맨 & 월시 2001, 페이지 100-1
- ^ "Paclitaxel Injection, USP" (PDF). Injectable Pharmaceuticals. Archived from the original (PDF) on 2016-09-18. Retrieved 2016-04-22.
- ^ "History". Archived from the original on 24 May 2016. Retrieved 22 April 2016.
- ^ "Phyton BioTech Paclitaxel". Archived from the original on 7 August 2016. Retrieved 22 April 2016.
- ^ Imseng N, Schillberg S, Schürch C, Schmid D, Schütte K, Gorr G, Eibl D, Eibl R (2014). Meyer H, Schmidhalter D (eds.). Suspension Culture of Plant Cells under Heterotrophic Conditions. Industrial Scale Suspension Culture of Living Cells. Wiley-Blackwell. pp. 224–257. ISBN 978-3-527-33547-3.
- ^ 길버트 고와 롤랜드 프랭크.식물 세포 발효(PCF®) 기술을 통한 복합 API의 상용 의약품 생산.10월 13일 CPHI 2015 프레젠테이션
- ^ "2004 Greener Synthetic Pathways Award: Bristol-Myers Squibb Company: Development of a Green Synthesis for TAXOL Manufacture via Plant Cell Fermentation and Extraction". Archived from the original on 2006-10-02.
- ^ Stierle A, Strobel G, Stierle D (April 1993). "Taxol and taxane production by Taxomyces andreanae, an endophytic fungus of Pacific yew". Science. 260 (5105): 214–6. Bibcode:1993Sci...260..214S. doi:10.1126/science.8097061. PMID 8097061.
- ^ Staniek A, Woerdenbag HJ, Kayser O (December 2009). "Taxomyces andreanae: a presumed paclitaxel producer demystified?". Planta Medica. 75 (15): 1561–6. doi:10.1055/s-0029-1186181. PMID 19809969.
- ^ Heinig U, Scholz S, Jennewein S (2013). "Getting to the bottom of taxol biosynthesis by fungi" (PDF). Fungal Diversity. 60: 161–170. doi:10.1007/s13225-013-0228-7. S2CID 18642421.
- ^ a b Dewick, Paul M. (2009-02-06). Medicinal Natural Products. Chichester, UK: John Wiley & Sons, Ltd. doi:10.1002/9780470742761. ISBN 978-0-470-74276-1. Archived from the original on May 4, 2016.
- ^ Howat, Susan; Park, Bora; Oh, Il Suk; Jin, Young-Woo; Lee, Eun-Kyong; Loake, Gary J. (2014-05-25). "Paclitaxel: biosynthesis, production and future prospects". New Biotechnology. 31 (3): 242–245. doi:10.1016/j.nbt.2014.02.010. ISSN 1871-6784. PMID 24614567.
- ^ Croteau, Rodney; Ketchum, Raymond E. B.; Long, Robert M.; Kaspera, Rüdiger; Wildung, Mark R. (February 2006). "Taxol Biosynthesis and Molecular Genetics". Phytochemistry Reviews. 5 (1): 75–97. doi:10.1007/s11101-005-3748-2. ISSN 1568-7767. PMC 2901146. PMID 20622989.
- ^ a b c Hall N (2003). "Creating complexity: The beauty and logic of synthesis". Chem. Commun. (6): 661–664. doi:10.1039/b212248k. PMID 12703766.
- ^ N. Hall을 봐, 멍청아.Holton 및 Nicolaou taxol total 합성 기사에 나오는 미국 화학 협회 간행물 Chemical and Engineering News(C&EN) 1994년 2월 21일자 32쪽 및 1차 인용문을 참조하십시오.
- ^ a b Flam F (February 1994). "Race to synthesize taxol ends in a tie". Science. 263 (5149): 911. Bibcode:1994Sci...263..911F. doi:10.1126/science.7906053. PMID 7906053.
- ^ 굿맨 & 월시 2001, 179-182페이지.
- ^ Wall ME, Wani MC (February 1995). "Camptothecin and taxol: discovery to clinic--thirteenth Bruce F. Cain Memorial Award Lecture". Cancer Research. 55 (4): 753–60. PMID 7850785. Archived from the original on November 24, 2016.
- ^ 굿맨 & 월시 2001, 17페이지
- ^ 굿맨 & 월시 2001, 페이지 22
- ^ 굿맨 & 월시 2001, 페이지 25, 28
- ^ a b 굿맨 & 월시 2001, 페이지 51
- ^ Wall ME, Wani MC (February 1995). "Camptothecin and taxol: discovery to clinic--thirteenth Bruce F. Cain Memorial Award Lecture". Cancer Research. 55 (4): 753–60. PMID 7850785.
- ^ Wani MC, Taylor HL, Wall ME, Coggon P, McPhail AT (May 1971). "Plant antitumor agents. VI. The isolation and structure of taxol, a novel antileukemic and antitumor agent from Taxus brevifolia". Journal of the American Chemical Society. 93 (9): 2325–7. doi:10.1021/ja00738a045. PMID 5553076.
- ^ 굿맨 & 월시 2001, 페이지 81
- ^ 굿맨 & 월시 2001, 페이지 79, 81
- ^ Fuchs DA, Johnson RK (August 1978). "Cytologic evidence that taxol, an antineoplastic agent from Taxus brevifolia, acts as a mitotic spindle poison". Cancer Treatment Reports. 62 (8): 1219–22. PMID 688258.
- ^ 굿맨 & 월시 2001, 95페이지
- ^ a b Goodman & Walsh 2001, 97페이지
- ^ 굿맨 & 월시 2001, 페이지 115
- ^ a b c d Goodman & Walsh 2001, 페이지 120
- ^ Rowinsky EK, Donehower RC, Rosenshein NB, Ettinger DS, McGuire WP (1988). "Phase II study of taxol in advanced epithelial malignancies". Proceedings of the Association of Clinical Oncology. 7: 136.
- ^ "Technology Transfer: NIH-Private Sector Partnership in the Development of Taxol" (PDF). Archived from the original (PDF) on 2007-07-26. Retrieved 2016-07-17.
- ^ Nader R, Love J (February 1993). "Looting the medicine chest: how Bristol-Myers Squibb made off with the public's cancer research". The Progressive. Archived from the original on 2004-09-24.
- ^ "Names for hi-jacking". Nature. 373 (6513): 370. February 1995. Bibcode:1995Natur.373..370.. doi:10.1038/373370a0. PMID 7830775. S2CID 31510966.
- ^ 굿맨 & 월시 2001, 페이지 170
- ^ Bristol-Myers Squibb, TAXOL(paclitaxel), 1997년 3월 Goodman & Walsh 2001에서 인용한 바와 같이, 2페이지.
- ^ "NICE Guidance TA108". Archived from the original on 2007-06-30.
- ^ Mhaidat NM, Alzoubi KH, Al-Azzam SI, Alsaad AA (January 2014). "Caffeine inhibits paclitaxel‑induced apoptosis in colorectal cancer cells through the upregulation of Mcl‑1 levels". Molecular Medicine Reports. 9 (1): 243–8. doi:10.3892/mmr.2013.1763. PMID 24173825. Archived from the original on 2015-06-22.
- ^ Kachooei E, Moosavi-Movahedi AA, Khodagholi F, Mozaffarian F, Sadeghi P, Hadi-Alijanvand H, et al. (June 2014). "Inhibition study on insulin fibrillation and cytotoxicity by paclitaxel". Journal of Biochemistry. 155 (6): 361–73. doi:10.1093/jb/mvu012. PMID 24535601.
- ^ Kachooei E, Mozaffarian F, Khodagholi F, Sadeghi P, Karami L, Ghasemi A, et al. (May 2018). "Paclitaxel inhibited lysozyme fibrillation by increasing colloidal stability through formation of "off-pathway" oligomers". International Journal of Biological Macromolecules. 111: 870–879. doi:10.1016/j.ijbiomac.2018.01.072. PMID 29352977.
- ^ Moscarello MA, Mak B, Nguyen TA, Wood DD, Mastronardi F, Ludwin SK (April 2002). "Paclitaxel (Taxol) attenuates clinical disease in a spontaneously demyelinating transgenic mouse and induces remyelination". Multiple Sclerosis. 8 (2): 130–8. doi:10.1191/1352458502ms776oa. PMID 11990870. S2CID 45994154.
- ^ Musse AA, Polverini E, Raijmakers R, Harauz G (October 2008). "Kinetics of human peptidylarginine deiminase 2 (hPAD2)--reduction of Ca2+ dependence by phospholipids and assessment of proposed inhibition by paclitaxel side chains". Biochemistry and Cell Biology. 86 (5): 437–47. doi:10.1139/o08-124. PMID 18923545.
- ^ MS Society of Canada Phase II 캐나다에서 진행 중인 Secondary Progressive MS용 Miceell Paclitaxel 임상시험 2012-03-15 Wayback Machine에서 아카이브 완료
- ^ 캐나다 MS Society of Canada Angiotech Halts(MS Society of Canada Angiotech Halts) 연구: 웨이백 머신에서 2012-03-15년 아카이브된 통계적 유의성 없음
- ^ Lavars, Nick (2016-01-14). "Cloaking chemo drugs in cellular bubbles destroys cancer with one fiftieth of a regular dose". www.gizmag.com. Archived from the original on 2016-02-24. Retrieved 2016-02-14.
- ^ Kim MS, Haney MJ, Zhao Y, Mahajan V, Deygen I, Klyachko NL, et al. (April 2016). "Development of exosome-encapsulated paclitaxel to overcome MDR in cancer cells". Nanomedicine. 12 (3): 655–664. doi:10.1016/j.nano.2015.10.012. PMC 4809755. PMID 26586551.
추가 정보
- Goodman J, Walsh V (5 March 2001). The Story of Taxol: Nature and Politics in the Pursuit of an Anti-Cancer Drug. Cambridge University Press. ISBN 978-0-521-56123-5.
외부 링크
- "Paclitaxel". Drug Information Portal. U.S. National Library of Medicine.
- "Paclitaxel". National Cancer Institute. 5 October 2006.
- "Paclitaxel". NCI Drug Dictionary. 2 February 2011.
- 이달의 분자: Neil Edwards, Bristol 대학, TAXOL.
- 플로리다 주립대학교의 '택솔 이야기'입니다.
- Berenson, Alex (October 1, 2006). "Hope, at $4,200 a Dose". The New York Times. Retrieved 2007-03-31.