클라람부실
Chlorambucil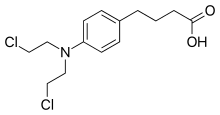 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | 로이케란 등 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a682899 |
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 |
|
| 약동학 데이터 | |
| 생체이용가능성 | ? |
| 신진대사 | 간 |
| 제거 반감기 | 1.5시간 |
| 배설 | 해당 없음 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.005.603 |
| 화학 및 물리적 데이터 | |
| 공식 | C14H19CL2NO2 |
| 어금질량 | 304.21 g·190−1 |
| 3D 모델(JSmol) | |
| |
| |
| (iii) | |
로이커란이라는 상표명으로 판매되는 클로로암부실은 만성 림프성 백혈병(CLL), 호지킨 림프종, 비호지킨 림프종을 치료하는 데 사용되는 화학요법 약물이다.[1] CLL에게 그것은 선호되는 치료법이다.[2] 그것은 입으로 주는 것이다.[2]
일반적인 부작용으로는 골수 억제가 있다.[2] 다른 심각한 부작용으로는 추가 암, 불임, 알레르기 반응의 장기적 위험 증가가 있다.[2] 임신 중에 사용하면 종종 아기에게 해를 끼친다.[2] 클로로암부칠은 알킬링제 약품군에 속한다.[2] DNA와 RNA의 형성을 차단해 효과가 있다.[2]
클로로암부실은 1957년 미국에서 의료용으로 승인되었다.[2] 그것은 세계보건기구의 필수 의약품 목록에 올라 있는데, 건강 시스템에 필요한 가장 안전하고 효과적인 의약품이다.[3] 그것은 원래 질소 겨자로 만들어졌다.[2]
의학적 용법
클로로암부칠의 현재 용도는 주로 만성 림프구 백혈병인데, 클로로암부칠은 젊은 환자들에게 있어 주로 루다라빈으로 대체되어 왔으나, 대부분의 환자들이 잘 견디고 있기 때문이다.[4] 비호지킨 림프종, 월든스트룀 매크로글로불린혈증, 다낭성 베라, 영양성 신소종, 난소암 등의 일부 유형을 치료하는 데 사용할 수 있다. 더욱이 신프로토스 증후군 등 각종 자가면역 및 염증 질환에 대한 면역억제제로도 쓰이고 있다.
부작용
골수 억제(혈증, 중성미자, 혈소판감소증)는 클로로암부칠의 가장 흔히 발생하는 부작용이다. 약품에서 손을 떼면, 이 부작용은 일반적으로 되돌릴 수 있다. 많은 알킬링제처럼 클로로암부실은 다른 형태의 암의 발생과 연관되어 있다.
덜 흔하게 발생하는 부작용은 다음과 같다.
약리학
작용기전
클로로암부실은 DNA 복제를 방해하고 세포 안의 DNA를 손상시켜 항암 효과를 낸다. DNA 손상은 세포질 p53 축적을 통한 세포 주기 구속과 세포 사멸을 유도하고 이후 세포사멸 촉진제인 Bcl-2 관련 X 단백질의 활성화를 유도한다.[5][6][7]
클로로암부실은 세포 주기의 모든 단계에서 DNA를 교차 연결하고 이중헬리 DNA를 가진 세 가지 다른 공밸런트 유도 생성 방법을 통해 DNA 손상을 유발한다.[8][9][10]
- 알킬 집단을 DNA 베이스에 부착함으로써 알킬화 염기를 대체하려는 그들의 시도에서 수리 효소에 의해 DNA가 파편화되어 영향을 받은 DNA로부터 DNA 합성과 RNA 전사를 방지하게 된다.
- 합성이나 전사를 위해 DNA가 분리되는 것을 막는 교차 링크 형성을 통한 DNA 손상.
- 돌연변이로 이어지는 뉴클레오티드의 오공 유도.
클로로암부실이 종양세포를 죽이는 정확한 메커니즘은 아직 완전히 이해되지 않았다.
생물학적 가용성에 대한 제한사항
최근 연구에서 암 조직에서 과다하게 발현되는 효소인 글루타티온 전달효소 Pi(GST P1-1)에 의해 클로로암부실이 해독되는 것으로 나타났다.[11]
이것은 클로로암부실이 전기영양체로서 글루타티온과의 결합에 의해 덜 반응하게 되어 그 약물이 세포에 덜 독성이 되게 하기 때문에 중요하다.
위와 같이 클로로암부칠은 hGSTA 1-1에 의해 촉매로 작용하여 클로로암부칠의 모노글루타티오닐 유도체가 형성된다.
화학
클로로암부실은 흰색에서 옅은 베이지색 결정체 또는 약간의 냄새가 나는 과립 분말이다. 분해하기 위해 가열하면 염화수소와 질소산화물의 매우 독성이 강한 가스를 방출한다.[12]
역사
질소 무스타드는 제1차 세계 대전 중 황 겨자 가스에 노출된 군인들이 백혈구 수치가 감소하는 것을 관찰한 후, 황 겨자 가스의 유도화로부터 생겨났다.[13] 황 머스터드 가스는 인간에게 쓰일 수 없을 만큼 독성이 강했기 때문에 길먼은 그 작용제의 전기성을 줄임으로써 전자가 풍부한 집단에 대해 화학적으로 매우 반응하게 함으로써 독성이 적은 약물을 얻을 수 있을 것이라는 가설을 세웠다. 이를 위해 그는 황을 질소와 교환하여 전기생성이 덜한 유추를 만들어 질소 무수장으로 이끌었다.[14]
인간에게 허용 가능한 치료 지표로, 질소 무수드는 1946년에 이 병원에 처음 도입되었다.[15] 오늘날에도 여전히 진료실에서 사용되고 있는 메클로레타민 염산염(머스틴 염산염)과 같은 알리파틱 무수드가 먼저 개발되었다.
1950년대에는 클로로암부칠과 같은 방향족 무스킷이 알리파틱 질소 무스처드보다 독성이 덜한 알킬링제로 도입되어 전기생성이 덜하고 DNA와 더 천천히 반응하는 것으로 판명되었다. 또한 이러한 에이전트를 구두로 관리할 수 있어 상당한 이점이 있다.
클로로암부실은 에버렛 외 연구진에 의해 처음으로 합성되었다.[5]
참조
- ^ "Chlorambucil". National Cancer Institute. 17 September 2014. Archived from the original on 21 December 2016. Retrieved 19 December 2016.
- ^ a b c d e f g h i "Chlorambucil". The American Society of Health-System Pharmacists. Archived from the original on 21 December 2016. Retrieved 8 December 2016.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Rai KR, Peterson BL, Appelbaum FR, Kolitz J, Elias L, Shepherd L, Hines J, Threatte GA, Larson RA, Cheson BD, Schiffer CA (2000). "Fludarabine compared with chlorambucil as primary therapy for chronic lymphocytic leukemia". N Engl J Med. 343 (24): 1750–7. doi:10.1056/NEJM200012143432402. PMID 11114313.
- ^ a b "Leukeran (Chlorambucil) Drug Information: Description, User Reviews, Drug Side Effects, Interactions – Prescribing Information at RxList". RxList. Archived from the original on 2015-12-22. Retrieved 2015-12-21.
- ^ "chlorambucil – CancerConnect News". CancerConnect News. Archived from the original on 2015-12-22. Retrieved 2015-12-21.
- ^ "Leukeran" (PDF). Archived (PDF) from the original on 2015-12-22.
- ^ "Chlorambucil". Archived from the original on 2017-01-03.
{{cite journal}}: Cite 저널은 필요로 한다.journal=(도움말) - ^ Di Antonio, Marco; McLuckie, Keith I. E.; Balasubramanian, Shankar (2014). "Chlorambucil". Journal of the American Chemical Society. 136 (16): 5860–5863. doi:10.1021/ja5014344. PMC 4132976. PMID 24697838.
- ^ "chlorambucil C14H19Cl2NO2 – PubChem". pubchem.ncbi.nlm.nih.gov. Archived from the original on 2015-12-22. Retrieved 2015-12-21.
- ^ Parker, Lorien J.; Ciccone, Sarah; Italiano, Louis C.; Primavera, Alessandra; Oakley, Aaron J.; Morton, Craig J.; Hancock, Nancy C.; Bello, Mario Lo; Parker, Michael W. (2008-06-27). "The anti-cancer drug chlorambucil as a substrate for the human polymorphic enzyme glutathione transferase P1-1: kinetic properties and crystallographic characterisation of allelic variants" (PDF). Journal of Molecular Biology. 380 (1): 131–144. doi:10.1016/j.jmb.2008.04.066. hdl:2108/101037. ISSN 1089-8638. PMID 18511072.
- ^ "chlorambucil C14H19Cl2NO2 – PubChem". pubchem.ncbi.nlm.nih.gov. Archived from the original on 2015-12-22. Retrieved 2015-12-21.
- ^ "Archived copy". Archived from the original on 2014-06-23. Retrieved 2016-11-24.
{{cite web}}: CS1 maint: 타이틀로 보관된 사본(링크) - ^ Gilman, A.G.; Rall, T.W.; Nies, A.S.; Taylor, P. (1990). Goodman and Gilman's The Pharmacological Basis of Therapeutics. New York: Pergamon.
- ^ Anslow, W. P. (1948). "The intravenous, subcutaneous and cutaneous toxicity of bis(-chloroethyl) sulfide (mustard gas) and of various derivatives". J. Pharmacol. Exp. Ther.
외부 링크
- 로이케란(제조업체 홈페이지)
- "Chlorambucil". Drug Information Portal. U.S. National Library of Medicine.