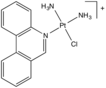
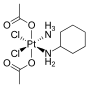
백금기반의 항소성 물질
Platinum-based antineoplastic백금성 항소성 약물(비공식적으로 플라틴이라고 함)은 암을 치료하는 데 사용되는 화학요법제다. 그들은 백금의 조정 콤플렉스다. 이 약들은 항암치료를 받고 있는 사람들의 거의 절반이 암 치료를 위해 사용된다. 이런 형태의 화학요법에서는 일반적으로 사용되는 약에는 시스플라틴, 옥살리플라틴, 카보플라틴 등이 있지만, 여러 가지가 제안되거나 개발 중에 있다.[1] 자궁경부암 초기 여성의 화학요법에 백금성 화학요법제를 추가하면 생존력이 향상되고 재발 위험이 감소하는 것으로 보인다.[2]
전체적으로 이 약들은 신경독성을 포함하는 40개 이상의 특정 부작용의 조합을 유발할 수 있는데, 이는 다신증 등 말초신경병증에 의해 발현된다.[3]
작용기전
주로 시스플라틴에 대해 연구되었지만, 아마도 다른 구성원에 대해서도 연구되었을 것이다. 백금성 항소성 물질은 모노어덕트, 인터스트랜드 교차링크, 주내 교차링크 또는 DNA 단백질 교차링크로서 DNA의 교차연결을 유발한다. 대부분 구아닌의 인접한 N-7 위치에서 작용하여 1, 2 inrasrand crosslink를 형성한다.[4][5] 결과적으로 교차 연결은 DNA 수리 및/또는 DNA 합성을 억제한다.
백금성 항소성 물질은 알킬군은 없지만 알킬화 항소성 물질과 유사한 효과로 인해 "알킬화 유사 물질"로 설명되기도 한다.[6]
예
백금 기반 항암제를 개선하기 위한 전략에는 보통 중성관측 리간드의 변화, 음이온 성질의 변화(할리드 대 다양한 카르복실산염) 또는 금속의 산화 상태 변화(Pt(II) 대 Pt(IV)가 포함된다. 종양 부위에 유입되는 리포플라틴의 경우 백금을 보다 효율적으로 전달해 독성의 가능성을 줄이는 나노기술이 개발됐다.[7]
시스플라틴은 가장 먼저 개발되었다.[8] 시스플라틴은 고환암에 특히 효과적이다; 치료율은 10%에서 85%[9]로 개선되었다. 마찬가지로, 보조 화학요법에 시스플라틴을 첨가한 결과, 무질병 생존율이 약 85%까지 현저하게 증가하였다. [10] 이 시스플라틴의 응용은 1980년대 초 소아 종양학자인 로저 패커에 의해 개발되었다. [11]
- 승인된 백금 기반 항암제
- 백금 기반 항암제 시험 중
시련에 남아 있는 피코플라틴
참조
- ^ a b Johnstone, TC; Park, GY; Lippard, SJ (2014). "Understanding and improving platinum anticancer drugs--phenanthriplatin". Anticancer Res. 34 (1): 471–6. PMC 3937549. PMID 24403503.
- ^ Falcetta, FS; Medeiros, LR; Edelweiss, MI; Pohlmann, PR; Stein, AT; Rosa, DD (22 November 2016). "Adjuvant platinum-based chemotherapy for early stage cervical cancer". The Cochrane Database of Systematic Reviews. 11: CD005342. doi:10.1002/14651858.CD005342.pub4. PMC 4164460. PMID 27873308.
- ^ Oun R, Moussa YE, Wheate NJ (2018). "The side effects of platinum-based chemotherapy drugs: a review for chemists". Dalton Transactions. 47 (19): 6645–6653. doi:10.1039/c8dt00838h. PMID 29632935.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Poklar N, Pilch DS, Lippard SJ, Redding EA, Dunham SU, Breslauer KJ (July 1996). "Influence of cisplatin intrastrand crosslinking on the conformation, thermal stability, and energetics of a 20-mer DNA duplex". Proc. Natl. Acad. Sci. U.S.A. 93 (15): 7606–11. Bibcode:1996PNAS...93.7606P. doi:10.1073/pnas.93.15.7606. PMC 38793. PMID 8755522.
- ^ Rudd GN, Hartley JA, Souhami RL (1995). "Persistence of cisplatin-induced DNA interstrand crosslinking in peripheral blood mononuclear cells from elderly and young individuals". Cancer Chemother. Pharmacol. 35 (4): 323–6. doi:10.1007/BF00689452. PMID 7828275. S2CID 24036376.
- ^ Cruet-Hennequart S, Glynn MT, Murillo LS, Coyne S, Carty MP (April 2008). "Enhanced DNA-PK-mediated RPA2 hyperphosphorylation in DNA polymerase eta-deficient human cells treated with cisplatin and oxaliplatin". DNA Repair. 7 (4): 582–96. doi:10.1016/j.dnarep.2007.12.012. PMID 18289945.
- ^ Johnstone, Timothy C.; Suntharalingam, Kogularamanan; Lippard, Stephen J. (2016). "The Next Generation of Platinum Drugs: Targeted Pt(II) Agents, Nanoparticle Delivery, and Pt(IV) Prodrugs". Chemical Reviews. 116 (5): 3436–3486. doi:10.1021/acs.chemrev.5b00597. ISSN 0009-2665. PMC 4792284. PMID 26865551.
- ^ Kelland, L. (2007). "The resurgence of platinum-based cancer chemotherapy". Nature Reviews Cancer. 7 (8): 573–584. doi:10.1038/nrc2167. PMID 17625587. S2CID 205468214.
- ^ Einhorn LH. (1 November 1990). "Treatment of testicular cancer: a new and improved model". J. Clin. Oncol. 8 (11): 1777–81. doi:10.1200/JCO.1990.8.11.1777. PMID 1700077.
- ^ Packer, R. (1994). "Outcome for children with medulloblastoma treated with radiation and cisplatin, CCNU, and vincristine chemotherapy". Journal of Neurosurgery. 81 (5): 690–698. doi:10.3171/jns.1994.81.5.0690. PMID 7931615.
- ^ Packer, R. (1994). "Outcome for children with medulloblastoma treated with radiation and cisplatin, CCNU, and vincristine chemotherapy". Journal of Neurosurgery. 81 (5): 690–698. doi:10.3171/jns.1994.81.5.0690. PMID 7931615.