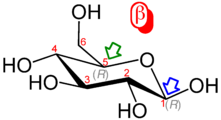
포도당
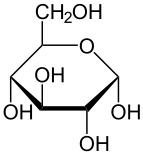
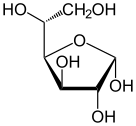
Glucose d-포도당의 골격식 | |
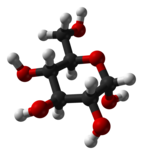
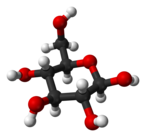
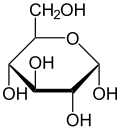 α-d-글루코피라노스의 하워스 프로젝션 | |
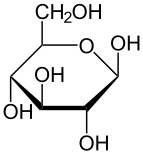
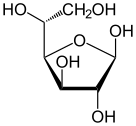
 fischer 사영 d-포도당 | |
| 이름 | |
|---|---|
| 발음 | /ˈɡluːkoʊz/, /ɡluːkoʊs/ |
| IUPAC 이름 허용되는 사소한 이름:[1]
| |
| 기본 설정 IUPAC 이름 PIN은 천연 제품에 대해 식별되지 않습니다. | |
체계적 IUPAC 이름
| |
| 기타이름 혈당 덱스트로스 옥수수당 d-글루코스 포도당 | |
| 식별자 | |
3D 모델(Jsmol) | |
| 3D Met | |
| 약어 | Glc |
| 1281604 | |
| ChEBI | |
| CHEMBL | |
| 켐스파이더 | |
| EC 번호 |
|
| 83256 | |
| KEGG | |
| MeSH | 포도당 |
펍켐 CID | |
| RTECS 번호 |
|
| 유니아이 |
|
| |
| |
| 특성. | |
| C6H12O6 | |
| 어금니 질량 | 180.156g/mol |
| 외모 | 흰가루 |
| 밀도 | 1.54g/cm3 |
| 융점 | α-d-Glucose: 146 °C (295 °F; 419 K) β-d-Glucose: 150 °C (302 °F; 423 K) |
| 909 g/L (25 °C (77 °F)) | |
| −101.5×10−6 cm3/mol | |
| 8.6827 | |
| 열화학 | |
열용량 (C) | 218.6 J/(K·mol)[2] |
성대 어금니 엔트로피 (S⦵298) | 209.2 J/(K·mol)[2] |
의 스텐달피 형성 (δ) | −1271 kJ/mol[3] |
연소열, 높은 값(HHV) | 2,805 kJ/mol (670 kcal/mol) |
| 약리학 | |
| B05CX01 (WHO) V04CA02 (WHO), V06DC01 (WHO) | |
| 유해성 | |
| NFPA704(파이어다이아몬드) | |
| SDS(Safety Data Sheet) | ICSC 08655 |
달리 명시된 경우를 제외하고는 표준 상태(25°C [77°F], 100kPa)에 있는 재료에 대한 데이터가 제공됩니다. | |
포도당은 분자식을 가진 당입니다. CHO6126. 포도당은 전체적으로 탄수화물의 하위 범주인 [4]단당류가 가장 풍부합니다. 포도당은 주로 식물과 대부분의 조류가 물과 이산화탄소로부터 광합성을 하는 동안 햇빛의 에너지를 이용하여 만들어지는데, 여기서 포도당은 세계에서 가장 풍부한 탄수화물인 세포벽의 셀룰로오스를 만드는 데 사용됩니다.[5]
에너지 대사에서 포도당은 모든 유기체에서 가장 중요한 에너지원입니다. 대사를 위한 포도당은 고분자로 저장되며, 식물에는 주로 전분과 아밀로펙틴으로, 동물에는 글리코겐으로 저장됩니다. 포도당은 혈당으로 동물의 혈액을 순환합니다. 자연적으로 생성되는 형태의 포도당은 d-글루코오스인 반면, 그 입체이성질체 l-글루코오스는 합성적으로 비교적 적은 양으로 생성되고 생물학적으로 덜 활성화됩니다.[6] 포도당은 6개의 탄소 원자와 알데히드 그룹을 포함하는 단당류이므로 알도헥소스입니다. 포도당 분자는 고리(고리) 형태뿐만 아니라 개방 사슬(비고리) 형태로 존재할 수 있습니다. 포도당은 자연적으로 발생하며 과일과 식물의 다른 부분에서 자유 상태로 발견됩니다. 동물에서 포도당은 글리코겐 분해로 알려진 과정에서 글리코겐의 분해로부터 방출됩니다.
포도당은 정맥내 설탕 용액으로서 세계보건기구의 필수 의약품 목록에 올라 있습니다.[7] 또한 염화나트륨과 함께 목록에 올라 있습니다.[7]
포도당이라는 이름은 고대 그리스 γλεῦκος (글레 û코스, "와인, 머스트")에서 유래했으며, γλυκύς (글릭 ý, "달다")에서 유래했습니다. 접미사 "-ose"는 설탕을 나타내는 화학 분류기입니다.
역사
포도당은 1747년 독일 화학자 안드레아스 마르그라프에 의해 건포도에서 처음 분리되었습니다.[10][11] 포도당은 1792년 독일의 또 다른 화학자 요한 토비아스 로위츠에 의해 포도에서 발견되었고, 사탕수수 설탕과는 다른 것으로 구별되었습니다. 포도당은 1838년 장 밥티스트 뒤마가 만든 용어로 화학 문헌에 널리 퍼졌습니다. Friedrich August Kekulé는 글루코스 수용액에서 선편광된 빛의 평면이 오른쪽으로 향하기 때문에 덱스트로오스라는 용어를 제안했습니다. 대조적으로, l-과당(일반적으로 d-과당이라고 함)과 l-포도당(l-포도당)은 선편광된 빛을 왼쪽으로 돌립니다. 선편광의 평면의 회전에 따른 초기 표기법(d 및 l-nomenature)은 나중에 카보닐기에서 가장 멀리 떨어진 비대칭 중심의 절대적인 구성을 지칭하는 d- 및 l-notation에 유리하게 폐기되었으며, d- 또는 l-glyceraldehyde의 구성과 일치합니다.[12][13]
포도당은 많은 유기체의 기본적인 필수 물질이기 때문에, 그 화학적 구성과 구조에 대한 올바른 이해는 유기 화학의 전반적인 발전에 크게 기여했습니다. 이러한 이해는 주로 1902년 노벨 화학상을 받은 독일 화학자 에밀 피셔의 연구 결과에서 비롯되었습니다.[14] 포도당의 합성은 유기 물질의 구조를 확립했고 결과적으로 Jacobus Henricus van't Hoff의 화학 동역학 이론과 탄소를 함유한 분자에서 화학 결합의 배열에 대한 최초의 확정적인 검증을 형성했습니다.[15] 1891년과 1894년 사이에 Fischer는 알려진 모든 당의 입체화학적 배열을 확립하고 가능한 이성질체를 정확하게 예측하여 Van't Hoff의 비대칭 탄소 원자 이론을 적용했습니다. 이름은 처음에 천연 물질을 가리켰습니다. 그들의 거울상이성질체는 절대 입체화학(예: Fischer 명명법, d/l 명명법)을 고려하여 체계적 명명법의 도입과 함께 동일한 이름이 붙여졌습니다.
포도당의 대사를 밝혀낸 공로로 오토 마이어호프는 1922년 노벨 생리학·의학상을 수상했습니다.[16] 한스 폰 오일러-첼핀은 1929년 "설탕의 발효와 이 과정에서의 효소의 비중에 대한 연구"로 아서 하든과 함께 노벨 화학상을 수상했습니다.[17][18] 1947년, 베르나르도 하우스세이 (글루코스와 유도된 탄수화물의 대사에서 뇌하수체의 역할을 발견한 공로로)와 칼과 거티 코리 (글루코스로부터 글리코겐의 전환을 발견한 공로로)가 노벨 생리학·의학상을 수상했습니다.[19][20][21] 1970년 루이스 르루아르는 탄수화물의 생합성에서 포도당 유래 당 뉴클레오타이드를 발견한 공로로 노벨 화학상을 수상했습니다.[22]
화학적, 물리적 성질
포도당은 물과 아세트산에는 잘 녹지만 메탄올과 에탄올에는 잘 녹지 않는 흰색 또는 무색의 고체를 형성합니다. 이들은 146°C(295°F)와 150°C(302°F)(β)에서 녹고, 188°C(370°F)에서 시작하여 다양한 휘발성 생성물이 방출되면서 분해되어 최종적으로 탄소의 잔류물을 남깁니다.[23] 포도당은 물에서 25°C(77°F)에서 12.16의 pK 값을 갖습니다.[24]
단당류의 하위 범주인 육탄당으로 분류되며 탄소 수가 6개입니다. d-포도당은 16개의 알도헥소스 입체 이성질체 중 하나입니다. d-이성질체, d-포도당, 일명 덱스트로오스는 자연계에서 널리 발생하지만 l-이성질체, l-포도당은 그렇지 않습니다. 포도당은 우유 당(락토스), 사탕수수 당(수크로스), 맥아당, 셀룰로오스, 글리코겐 등의 탄수화물을 가수분해하여 얻을 수 있습니다. 덱스트로스는 일반적으로 미국과 일본의 옥수수 전분, 유럽의 감자와 밀 전분, 열대 지역의 타피오카 전분에서 상업적으로 제조됩니다.[25] 제조 공정은 제트에서 조절된 pH에서 가압 증기를 통해 가수분해한 후 추가적인 효소 해중합을 사용합니다.[26] 결합되지 않은 포도당은 꿀의 주요 성분 중 하나입니다.
구조 및 명명법

포도당은 일반적으로 닫힌 피란 고리(α-glucopyranose monhydrate, 때로는 덱스트로스 수화물에 의해 덜 정확하게 알려져 있음)를 갖는 단수화물로서 고체 형태로 존재합니다. 반면 수용액에서는 작은 정도로 개방 사슬이며 주로 α- 또는 β-피라노스로 존재하며, 이들은 상호 전환됩니다. 수용액으로부터, α-글루코피라노스, β-글루코피라노스 및 α-글루코피라노스 일수화물의 세 가지 알려진 형태가 결정화될 수 있습니다.[27] 포도당은 이당류인 유당과 수크로스(캔 또는 비트당), 라피노스와 같은 올리고당과 전분, 아밀로펙틴, 글리코겐 및 셀룰로오스와 같은 다당류의 구성 요소입니다. 포도당의 유리 전이 온도는 31°C(88°F)이고 고든-테일러 상수(두 물질 혼합물의 서로 다른 질량 분율에 대한 유리 전이 온도 예측을 위해 실험적으로 결정된 상수)[28]는 4.5입니다.[29]
| d-포도당의 형태와 사영 비교 | ||
|---|---|---|
| 나타투영 | 하워스 사영 | |
 |  α-d-glucofuranose α-d-glucofuranose | 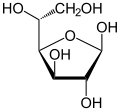 β-d-glucofuranose β-d-glucofuranose |
 α-d-gluc피라노스 α-d-gluc피라노스 |  β-d-gluc피라노스 β-d-gluc피라노스 | |
| (1) 톨렌스/피셔 (2) 하워스 투영 (3) 의자 형태 (4) 밀 투영의 α-d-Glucopyranose | ||
 | ||
오픈체인 형태

글루코스의 개방 사슬 형태는 평형 상태의 수용액에서 글루코스 분자의 0.02% 미만을 차지합니다.[30] 나머지는 두 개의 순환 헤미아세탈 형태 중 하나입니다. 개방 사슬 형태에서 포도당 분자는 6개의 탄소 원자로 구성된 개방형(순환형과 반대로) 비분지 골격을 가지며, 여기서 C-1은 알데히드기 H(C=O)-의 일부입니다. 따라서 포도당도 알도스, 즉 알도헥소스로 분류됩니다. 알데히드기는 포도당을 환원당으로 만들어 펠링 테스트에서 양성 반응을 보입니다.
순환형
용액에서 글루코스의 개방 사슬 형태("D-" 또는 "L-")는 각각 하나의 산소 원자에 의해 닫힌 탄소 고리를 포함하는 몇 개의 고리형 이성질체와 평형 상태로 존재합니다. 그러나 수용액에서는 포도당 분자의 99% 이상이 피라노스 형태로 존재합니다. 오픈체인 형태는 약 0.25%로 제한되며 퓨라노스 형태는 무시할 수 있을 정도로 존재합니다. "포도당"과 "D-포도당"이라는 용어는 일반적으로 이러한 순환 형태에도 사용됩니다. 고리는 알데히드기(C-1에서)와 C-4 또는 C-5 하이드록실기 사이의 분자 내 친핵성 부가 반응에 의해 개방 사슬 형태에서 발생하여 헤미아세탈 결합인 -C(OH)H-O-를 형성합니다.
C-1과 C-5 사이의 반응은 유도체화된 피란 골격을 포함하는 단당류 당인 피라노스라고 불리는 6개의 헤테로사이클릭 시스템을 생성합니다. C-1과 C-4 사이의 (훨씬 드문) 반응은 고리형 에테르 푸란의 이름을 따서 명명된 5원의 푸라노스 고리를 생성합니다. 어느 경우든, 고리의 각 탄소는 수소와 하이드록실이 하나씩 부착되어 있는데, 하이드록실이 열린 분자의 나머지로 대체되는 마지막 탄소(C-4 또는 C-5)를 제외하고는 -(CHOH2)입니다.HOH)-H 또는 -(각각 CHOH)-H).
고리가 닫히는 반응은 "α-"와 "β-"로 표시되는 두 가지 생성물을 제공할 수 있습니다. 글루코피라노스 분자가 하워스 투영에 그려질 때, "α-"라는 명칭은 C-1에 붙어있는 하이드록시기와 C-5에 있는 -CHOH2 그룹이 고리의 평면의 반대쪽에 있다는 것을 의미하는 반면, "β-"는 평면의 같은 쪽에 있다는 것을 의미합니다. 따라서 개방 사슬 이성질체 D-글루코피라노스는 α-D-글루코피라노스, β-D-글루코피라노스, α-D-글루코피라노스, β-D-글루코피라노스의 4가지 별개의 고리 이성질체를 생성합니다. 이 5가지 구조는 평형 및 상호 전환 상태로 존재하며, 상호 전환은 산 촉매 작용과 함께 훨씬 더 빠릅니다.

다른 개방 사슬 이성질체 L-포도당은 유사하게 4개의 서로 다른 순환 형태의 L-포도당을 생성하며, 각각은 해당 D-포도당의 거울 이미지입니다.
글루코피라노스 고리(α 또는 β)는 시클로헥산의 "의자" 및 "보트" 형태와 유사한 몇 가지 비평면 형태를 가정할 수 있습니다. 유사하게, 글루코푸라노스 고리는 사이클로펜탄의 "외피" 형태와 유사한 여러 모양을 가정할 수 있습니다.
고체 상태에서는 글루코피라노스 형태만 관찰됩니다.
1,2-O-이소프로필리덴-D-글루코푸라노스와 같은 글루코푸라노스의 일부 유도체는 안정적이며 결정성 고체로서 순수하게 얻을 수 있습니다.[31][32] 예를 들어, α-D-글루코스와 파라-톨릴보론산 HC-3(CH64)-B(OH)2의 반응은 정상적인 피라노스 고리를 개혁하여 4배 에스테르 α-D-글루코푸라노스-1,2:3,5-비스(p-톨릴보론산)를 생성합니다.[33]
상호회전

뮤타로테이션은 고리 형성 반응의 일시적인 반전으로 구성되어 개방 사슬 형태가 되며, 이어서 고리의 개질이 이루어집니다. 고리 폐쇄 단계는 개방 단계에 의해 생성된 것과 다른 -OH 기를 사용할 수도 있고(따라서 피라노스와 푸라노스 형태 사이의 전환), 또는 C-1 상에서 생성된 새로운 헤미아세탈 그룹은 원래의 것과 동일하거나 반대의 핸들링을 가질 수도 있습니다(따라서 α와 β 형태 사이의 전환). 따라서 개방 사슬 형태는 용액에서 거의 감지할 수 없지만 평형의 필수 구성 요소입니다.
열린 사슬 형태는 열역학적으로 불안정하고, 자발적으로 고리 형태로 이성질화됩니다. (고리 폐쇄 반응은 이론적으로 4개 또는 3개의 원자 고리를 만들 수 있지만, 이것들은 매우 긴장되어 실제로는 관찰되지 않습니다.) 상온의 용액에서 4개의 고리형 이성질체는 시간 척도에 따라 상호 변환되며, 이 과정을 뮤타로테이션이라고 합니다.[34] 임의의 비율에서 시작하여 혼합물은 α:β 36:64의 안정적인 비율로 수렴합니다. 아노머 효과의 영향이 없다면 그 비율은 α:β 11:89가 될 것입니다.[35] 뮤타로테이션은 0°C(32°F)에 가까운 온도에서 상당히 느립니다.
광학적 활동
물이든 고체 형태이든 d-(+)-포도당은 dextrotational이며, 이는 광원 쪽을 바라보면서 편광된 빛의 방향을 시계방향으로 회전한다는 것을 의미합니다. 그 효과는 분자의 키랄성 때문이며, 실제로 거울상 이성질체인 l-(-)-포도당은 같은 양만큼 좌회전(편광을 반시계 방향으로 회전)합니다. 효과의 강도는 5개의 자동차 회사마다 다릅니다.
d-접두사는 화합물의 광학적 특성을 직접적으로 언급하지 않습니다. 이것은 C-5 카이랄 중심이 d-글리세르알데히드(dextrotational)와 같은 취급성을 가지고 있음을 나타냅니다. d-글루코스가 덱스트로로타티보틱이라는 사실은 C-5뿐만 아니라 4개의 카이랄 중심의 결합된 효과이며, 실제로 다른 d-알도헥소스 중 일부는 레보로타티보틱입니다.
순수한 α-d-글루코스는 +112.2° mL/(dm·g)의 특정 회전각을 가지며, 순수한 β-d-글루코스는 +17.5° mL/(dm·g)이기 때문에 두 아노머 사이의 전환을 편광계에서 관찰할 수 있습니다.[36] 상호 회전에 의해 일정 시간 후 평형에 도달했을 때 회전각은 +52.7° mL/(dm·g)입니다.[36] 산이나 염기를 첨가함으로써 이 변환은 훨씬 가속화됩니다. 평형은 개방 사슬 알데히드 형태를 통해 이루어집니다.
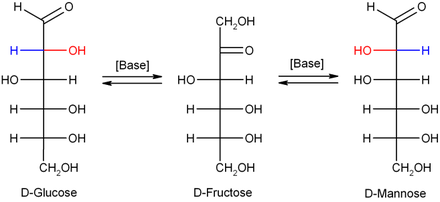
이성질화
묽은 수산화나트륨 또는 다른 묽은 염기에서는 단당류인 만노스, 포도당 및 과당이 상호 전환되어(로브리 드 브루인-알베르다-반 에켄슈타인 변환을 통해) 이러한 이성질체 사이의 균형이 형성됩니다. 이 반응은 에네디올을 통해 진행됩니다.
생화학적 성질
| 일반적인 단당류의 대사 및 포도당의 일부 생화학적 반응 |
|---|
 |
포도당은 가장 풍부한 단당류입니다. 포도당은 또한 대부분의 살아있는 유기체에서 가장 널리 사용되는 알도헥소스입니다. 이에 대한 한 가지 가능한 설명은 포도당이 단백질의 아민 그룹과 비특이적으로 반응하는 경향이 다른 알도헥소스보다 낮다는 것입니다.[37] 당화 반응은 당화혈색소와 [37]같은 많은 단백질의 기능을 손상시키거나 파괴합니다. 포도당의 낮은 당화 속도는 다른 알도헥소스에 비해 더 안정적인 순환 형태를 가지고 있기 때문에 반응성 오픈체인 형태보다 더 적은 시간을 소비합니다.[37] 글루코스가 모든 알도헥소스 중에서 가장 안정적인 고리 형태를 갖는 이유는 글루코스의 하이드록시기(d-글루코스의 아노머 탄소 상의 하이드록시기를 제외하고)가 적도 위치에 있기 때문입니다. 아마도 글루코스는 다른 단당류에 비해 단백질과의 당화가 적기 때문에 가장 풍부한 천연 단당류일 것입니다.[37][38] 또 다른 가설은 글루코스가 β-d-글루코스 형태의 적도 위치에 5개의 히드록시 치환기를 모두 가지고 있는 유일한 d-알도헥소스인 글루코스가 화학 반응,[39]: 194, 199 예를 들어 에스테르화[40]: 363 또는 아세탈 형성에 더 쉽게 접근할 수 있다는 것입니다.[41] 이러한 이유로 d-glucose는 천연 다당류(글리칸)에서도 매우 선호되는 구성 블록입니다. 포도당으로만 구성된 다당류를 글루칸이라고 합니다.
포도당은 햇빛, 물, 이산화탄소를 이용한 광합성을 통해 식물이 생산하며 모든 생물이 에너지와 탄소원으로 사용할 수 있습니다. 그러나 대부분의 포도당은 유리된 형태가 아니라 그 고분자, 즉 에너지 비축 물질인 유당, 수크로스, 전분 등과 식물이나 균류, 절지동물에서 각각 세포벽의 구성 성분인 셀룰로오스, 키틴 등의 형태로 발생합니다. 이 고분자는 동물, 곰팡이, 박테리아가 섭취하면 효소를 이용해 포도당으로 분해됩니다. 모든 동물들은 필요에 따라 특정 전구체로부터 포도당을 스스로 생산할 수도 있습니다. 신경세포, 신수질, 적혈구의 세포는 에너지 생산을 위해 포도당에 의존합니다.[42] 성인 인간의 경우, 약 18 g(0.63 oz)의 포도당이 있으며,[43] 그 중 약 4 g(0.14 oz)의 포도당이 혈액에 존재합니다.[44] 성인의 간에서 약 180~220g (6.3~7.8온스)의 포도당이 24시간 동안 생산됩니다.[43]
당뇨병의 장기 합병증(예: 실명, 신부전, 말초신경병증) 중 많은 부분이 아마도 단백질이나 지질의 당화 때문일 것입니다.[45] 대조적으로, 단백질에 당을 효소적으로 조절하는 첨가는 글리코실화라고 불리며 많은 단백질의 기능에 필수적입니다.[46]
흡수
섭취된 포도당은 처음에는 인간의 혀에서 단맛을 내기 위해 수용체에 결합합니다. T1R2와 T1R3 단백질의 이 복합체는 포도당 함유 식품 공급원을 식별하는 것을 가능하게 합니다. 포도당은 주로 음식에서 나옵니다. 음식의 전환에 의해 하루에 약 300g (11온스)가 생성되지만,[47] 몸의 세포에 있는 다른 대사산물로부터도 합성됩니다. 인간의 경우, 포도당이 함유된 다당류의 분해는 이미 부분적으로 소장의 브러시 경계에 있는 말타제, 락타제, 수크라제뿐만 아니라 타액에 함유된 아밀라제에 의해 저작 중에 발생합니다. 포도당은 많은 탄수화물의 구성 요소이며 특정 효소를 사용하여 탄수화물에서 분리할 수 있습니다. 글리코시다아제의 하위 그룹인 글루코시다아제는 먼저 장쇄 글루코스 함유 다당류의 가수분해를 촉매하여 말단 글루코스를 제거합니다. 차례로, 이당류는 대부분 특정 글리코시다아제에 의해 포도당으로 분해됩니다. 분해 효소의 이름은 종종 특정한 다당류와 이당류에서 유래하는데, 특히 다당류 사슬의 분해에는 아밀라아제(전분의 성분인 아밀로스의 이름을 따서 명명됨), 셀룰라아제(셀룰로오스의 이름을 따서 명명됨), 키티나아제(키틴의 이름을 따서 명명됨) 등이 있습니다. 또한 이당류의 분해에는 말타제, 락타제, 수크라제, 트레할라제 등이 있습니다. 인간의 경우, 글리코시다아제를 코딩하는 약 70개의 유전자가 알려져 있습니다. 글리코겐, 스핑고지질, 점액다당류 및 폴리(ADP-리보스)의 소화 및 분해 기능을 가지고 있습니다. 인간은 셀룰라아제, 키티나아제, 트레할라아제를 생산하지 않지만 장내 미생물군의 박테리아는 생산합니다.
세포의 세포막과 세포 구획의 막으로 들어가거나 나가기 위해서는 포도당이 주요 촉진자 슈퍼패밀리의 특별한 수송 단백질을 필요로 합니다. 소장([48]더 정확하게는 공장에서)에서 포도당은 나트륨/포도당 공동수송체 1(SGLT1)을 통한 나트륨 이온-포도당 심포트(sodium ion-glucose symport)라고 불리는 2차 능동 수송 메커니즘을 통해 포도당 수송체의[49] 도움으로 장 상피로 흡수됩니다.[50] 포도당 수송체 GLUT2를 통해 장 상피 세포의 기저외측에서 추가적인 전달이 일어나고 [50]간 세포, 신장 세포, 랑게르한스 섬의 세포, 뉴런, 성상세포 및 타니세포로 흡수됩니다.[51] 포도당은 간문맥을 통해 간으로 들어가 세포 글리코겐으로 저장됩니다.[52] 간세포에서는 6번 위치에서 글루코키나아제에 의해 인산화되어 글루코키나아제 6-인산이 형성되는데, 글루코키나아제는 세포를 떠나지 못합니다. 포도당 6-포스파타제는 포도당 6-인산을 다시 간에서만 포도당으로 전환시킬 수 있기 때문에 우리 몸은 충분한 혈당 농도를 유지할 수 있습니다. 다른 세포에서는 14개의 GLUT 단백질 중 하나를 통한 수동적인 수송에 의해 흡수가 일어납니다.[50] 다른 세포 유형에서는 헥소키나아제를 통해 인산화가 일어나 포도당이 더 이상 세포 밖으로 확산되지 않습니다.
포도당 수송체 GLUT1은 대부분의 세포 유형에서 생성되며 신경 세포와 췌장 β-세포에서 특히 중요합니다.[50] GLUT3는 신경세포에서 고도로 발현됩니다.[50] 혈류로부터 포도당은 (골격근과[53] 심장근의) 근육 세포와 지방 세포로부터 GLUT4에 의해 흡수됩니다.[54] GLUT14는 고환에서만 발현됩니다.[55] 과량의 포도당은 분해되어 지방산으로 전환되고, 이 지방산은 트리글리세리드로 저장됩니다. 신장에서 소변의 포도당은 정점 세포막에서 SGLT1과 SGLT2를 통해 흡수되고 기저외측 세포막에서 GLUT2를 통해 전달됩니다.[56] 신장 포도당 재흡수의 약 90%는 SGLT2를 통해 이루어지고 약 3%는 SGLT1을 통해 이루어집니다.[57]
생합성
식물과 일부 원핵생물에서 포도당은 광합성의 산물입니다.[58] 또한 글루코스는 글리코겐(동물과 버섯) 또는 전분(식물)과 같은 고분자 형태의 글루코스가 분해되어 형성됩니다. 글리코겐의 절단을 글리코겐 분해라고 하고, 전분의 절단을 전분 분해라고 합니다.[59]
2~4개의 탄소 원자(C)를 포함하는 분자에서 시작하여 6개의 탄소 원자를 포함하는 포도당 분자에서 끝나는 대사 경로를 포도당신생합성이라고 하며 모든 생물체에서 발생합니다. 더 작은 출발 물질은 다른 대사 경로의 결과입니다. 궁극적으로 거의 모든 생체 분자는 광합성 과정에서 식물과 미생물의 이산화탄소 동화에서 비롯됩니다.[40]: 359 α-d-포도당 형성의 자유 에너지는 몰당 917.2 킬로줄입니다.[40]: 59 인간의 경우 포도당신생합성은 간과 신장에서 [60]발생하지만 다른 세포 유형에서도 발생합니다. 간에는 약 150g의 글리코겐이, 골격근에는 약 250g의 글리코겐이 저장됩니다.[61] 그러나 글리코겐이 분해될 때 근육세포에서 방출되는 포도당은 헥소키나아제에 의해 포도당이 인산화되고, 인산기를 제거하기 위해 포도당-6-포스파타아제가 발현되지 않기 때문에 순환계로 전달되지 못합니다. 포도당과 달리 포도당-6-인산의 수송 단백질은 없습니다. 포도당신생합성은 유기체가 에너지를 소비하는 동안 젖산이나 특정 아미노산을 포함한 다른 대사 산물로부터 포도당을 축적할 수 있도록 합니다. 신장 세뇨관 세포는 또한 포도당을 생성할 수 있습니다.
포도당은 또한 주변 환경에서 살아있는 유기체 외부에서 발견될 수 있습니다. 대기 중 포도당 농도는 항공기로 시료를 채취하여 검출되며, 위치에 따라 차이가 있는 것으로 알려져 있습니다. 예를 들어, 중국 내륙의 대기 중 포도당 농도는 0.8~20.1pg/L인 반면, 중국 동부 해안의 포도당 농도는 10.3~142pg/L입니다.[62]
포도당 분해
인간에서 포도당은 해당과정과[63] 오탄당 인산 경로에 의해 대사됩니다.[64] 해당과정은 작은 변화를 가지고 [39]: 551 [65]모든 생물체가 사용하며 모든 생물체는 단당류의 분해로 에너지를 생성합니다.[65] 대사의 추가 과정에서, 그것은 산화적 탈탄산, 시트르산 회로(동음이의 Krebs cycle) 및 호흡 사슬을 통해 물과 이산화탄소로 완전히 분해될 수 있습니다. 이를 위해 사용할 수 있는 산소가 충분하지 않으면 동물의 포도당 분해는 젖산 발효를 통해 젖산에 혐기성으로 발생하고 훨씬 적은 에너지를 방출합니다. 근육질 젖산은 포유동물에서 혈류를 통해 간으로 들어가고, 여기서 포도당신생합성이 일어납니다(코리사이클). 높은 포도당 공급으로 크렙스 회로의 대사산물인 아세틸-CoA는 지방산 합성에도 사용될 수 있습니다.[66] 포도당은 또한 간과 골격근에서 주로 발견되는 신체의 글리코겐 저장을 보충하는 데 사용됩니다. 이러한 과정은 호르몬적으로 조절됩니다.
다른 생물체에서는 다른 형태의 발효가 일어날 수 있습니다. 박테리아 대장균은 포도당을 유일한 탄소원으로 포함하는 영양 배지에서 자랄 수 있습니다.[40]: 59 일부 박테리아 및 변형된 형태의 고세균에서는 엔트너-두도로프 경로를 통해 포도당이 분해됩니다.[67]
세포에서 포도당을 에너지원으로 사용하는 것은 호기성 호흡, 혐기성 호흡 또는 발효에 의한 것입니다. 해당과정의 첫 번째 단계는 헥소키나아제에 의해 포도당이 인산화되어 포도당 6-인산을 형성하는 것입니다. 포도당이 즉시 인산화되는 주된 이유는 전하를 띤 인산기가 포도당 6-인산이 세포막을 쉽게 통과하지 못하게 하기 때문에 포도당이 세포 밖으로 확산되는 것을 막기 위해서입니다.[68] 또한 고에너지 인산기의 첨가는 해당과정의 나중 단계에서 후속 분해를 위해 포도당을 활성화합니다. 생리학적 조건에서 이 초기 반응은 되돌릴 수 없습니다.
혐기성 호흡에서 1개의 포도당 분자는 2개의 ATP 분자의 순 이득을 생성합니다(기질 수준의 인산화를 통해 해당과정에서 4개의 ATP 분자가 생성되지만 2개는 해당과정에서 사용되는 효소에 의해 필요합니다).[69] 호기성 호흡에서 포도당 분자는 유기체에 따라 최대 30 또는 32 ATP 분자의 순 생산이 발생한다는 점에서 훨씬 더 수익적입니다.[70]
아래의 유전자, 단백질, 대사산물을 클릭하면 각각의 기사로 연결됩니다.[§ 1]
- ^ 대화형 경로 맵은 WikiPathways에서 편집할 수 있습니다. "GlycolysisGluconeogenesis_WP534".
종양 세포는 종종 비교적 빠르게 성장하고 해당과정에 의해 평균 이상의 포도당을 소비하며, [71]이는 산소가 있는 상태에서도 포유동물에서 발효의 최종 산물인 젖산을 형성합니다. 이것을 워버그 효과라고 합니다. 종양에서 포도당의 흡수를 증가시키기 위해 다양한 SGLT와 GLUT가 과도하게 생성됩니다.[72][73]
효모에서 에탄올은 산소가 존재하는 경우에도 높은 포도당 농도에서 발효됩니다(보통 발효보다는 호흡으로 이어짐). 이것을 크랩트리 효과라고 합니다.
포도당은 또한 비생물적인 방법을 통해 분해되어 이산화탄소를 형성할 수 있습니다. 이는 22°C 및 pH 2.5에서 산화 및 가수분해를 통해 실험적으로 발생하는 것으로 입증되었습니다.[74]
에너지원
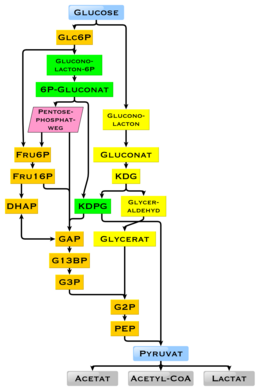
포도당은 생물학에서 어디에나 있는 연료입니다. 박테리아에서 인간에 이르기까지 호기성 호흡, 혐기성 호흡(박테리아에서) 또는 발효를 통해 유기체에서 에너지원으로 사용됩니다. 포도당은 호기성 호흡을 통해 인체의 주요 에너지원으로, 1g당 약 3.75킬로칼로리(16킬로줄)의 음식 에너지를 제공합니다.[75] 탄수화물(예: 전분)의 분해는 단당류와 이당류를 생성하며, 대부분은 포도당입니다. 해당과정을 거쳐 나중에 시트르산 회로와 산화적 인산화의 반응에서 포도당은 산화되어 결국 이산화탄소와 물을 형성하고, 대부분 ATP의 형태로 에너지를 생산합니다. 인슐린 반응 및 기타 메커니즘은 혈액 내 포도당 농도를 조절합니다. 포도당의 생리학적 열량은 출처에 따라 그램[76] 당 16.2 킬로줄 또는 15.7 kJ/g (3.74 kcal/g)입니다.[77] 식물 생물량에서 탄수화물의 높은 가용성은 진화 과정에서 특히 미생물에서 에너지와 탄소 저장을 위해 포도당을 활용하는 다양한 방법으로 이어졌습니다. 최종 제품을 더 이상 에너지 생산에 사용할 수 없는 차이가 존재합니다. 개별 유전자와 유전자 산물인 효소의 존재는 어떤 반응이 가능한지를 결정합니다. 해당과정의 대사 경로는 거의 모든 생물이 사용합니다. 해당과정의 사용에서 본질적인 차이점은 NADPH가 간접적으로 생성되어야 하는 동화작용의 환원제로서 회복된다는 것입니다.[78]
포도당과 산소는 뇌에 거의 모든 에너지를 공급하기 [79]때문에 그것의 가용성은 심리적 과정에 영향을 미칩니다. 포도당이 부족하면 정신적 노력(예: 자기 통제, 노력적 의사 결정)이 필요한 심리적 과정이 손상됩니다.[80][81][82][83] 주요 에너지원으로 포도당과 산소에 의존하는 뇌에서 포도당 농도는 보통 4~6mM([43]5mM은 90mg/dL)이지만 금식 시에는 2~3mM으로 감소합니다.[84] 혼란은 1mM 이하에서 발생하고 혼수는 낮은 수준에서 발생합니다.[84]
혈액 속의 포도당은 혈당이라고 불립니다. 혈당 수치는 시상하부의 포도당 결합 신경 세포에 의해 조절됩니다.[85] 또한 뇌의 포도당은 핵에 있는 보상체계의 포도당 수용체에 결합합니다.[85] 혀의 달콤한 수용체에 포도당이 결합하면 포도당을 통해 또는 다른 당을 통해 에너지 대사의 다양한 호르몬의 방출을 유도하여 세포 흡수를 증가시키고 혈당 수치를 낮춥니다.[86] 인공 감미료는 혈당 수치를 낮추지 않습니다.[86]
짧은 시간의 금식 상태에서, 예를 들어, 밤새 금식한 후의 건강한 사람의 혈당 함량은 약 70 내지 100 mg/dL (4 내지 5.5 mM)입니다. 혈장에서 측정값은 약 10~15% 더 높습니다. 또한 모세혈관층을 통과하는 과정에서 포도당이 조직으로 흡수되기 때문에 동맥혈 내 수치가 정맥혈 내 농도보다 높습니다. 혈당 측정에 자주 사용되는 모세혈관 혈액에서도 정맥혈보다 수치가 높은 경우가 있습니다. 혈액의 포도당 함량은 인슐린, 인크레틴, 글루카곤 호르몬에 의해 조절됩니다.[85][87] 인슐린은 포도당 수치를 낮추고 글루카곤은 증가시킵니다.[43] 또한 아드레날린, 티록신, 글루코코르티코이드, 소마토트로핀, 아드레노코르티코트로핀 호르몬은 포도당 수치를 증가시킵니다.[43] 포도당 자동 조절이라고 하는 호르몬 독립적인 조절도 있습니다.[88] 음식 섭취 후 혈당 농도가 높아집니다. 정맥 전혈에서 180 mg/dL 이상의 값은 병리학적이며 고혈당증, 40 mg/dL 미만의 값은 저혈당증이라고 합니다.[89] 필요할 때 포도당은 간과 신장 글리코겐에서 유래한 포도당-6-인산으로부터 포도당-6-포스파타제에 의해 혈류로 방출되어 혈당 농도의 항상성을 조절합니다.[60][42] 반추동물에서 혈당 농도는 더 낮습니다(소의 경우 60 mg/dL, 양의 경우 40 mg/dL). 왜냐하면 탄수화물은 장내 미생물에 의해 단사슬 지방산으로 더 많이 전환되기 때문입니다.[90]
일부 포도당은 성상세포에 의해 젖산으로 전환되어 뇌세포에 의해 에너지원으로 사용되고, 일부 포도당은 장세포와 적혈구에 의해 사용되며, 나머지는 간, 지방조직, 근육세포에 도달하여 글리코겐(인슐린의 영향으로)으로 흡수되어 저장됩니다. 간세포 글리코겐은 인슐린이 부족하거나 없을 때 포도당으로 전환되어 혈액으로 되돌아갈 수 있고, 근육세포 글리코겐은 효소가 부족하기 때문에 혈액으로 되돌아가지 않습니다. 지방 세포에서 포도당은 일부 지방 유형을 합성하고 다른 목적을 갖는 반응을 촉진하는 데 사용됩니다. 글리코겐은 포도당 자체보다 훨씬 더 "공간 효율적"이고 반응성이 낮기 때문에 신체의 "포도당 에너지 저장" 메커니즘입니다.
포도당은 인체 건강에 중요하기 때문에 일반적인 의료 혈액 검사인 포도당 검사의 분석 물질입니다.[91] 혈액 샘플을 채취하기 전에 먹거나 금식하는 것은 혈액 내 포도당 분석에 영향을 미칩니다. 높은 금식 혈당 수치는 당뇨병이나 당뇨병의 징후일 수 있습니다.[92]
혈당 지수는 섭취한 탄수화물로부터 혈당 수치로의 흡수 및 전환 속도를 나타내는 지표로, 포도당과 비교하여 섭취 후 혈당 수치의 곡선 아래 면적으로 측정됩니다(혈당은 100으로 정의됨).[93] 지방 함량이 높은 음식은 탄수화물의 흡수를 늦추고 아이스크림과 같은 혈당 지수를 낮추기 [93][94]때문에 혈당 지수의 임상적 중요성은 논란의 여지가 있습니다.[94] 대체 지표는 탄수화물 섭취가 혈중 인슐린 수치에 미치는 영향으로 [95]측정되는 인슐린 지수입니다. 혈당 부하는 혈당 지수와 섭취한 음식의 양을 기준으로 섭취 후 혈당 수치에 첨가되는 포도당의 양을 나타내는 지표입니다.
전조
유기체는 포도당을 몇 가지 중요한 물질의 합성을 위한 전구체로 사용합니다. 일반적인 글루코오스 중합체(다당류)는 전분, 셀룰로오스, 글리코겐("동물 전분")입니다. 이러한 고분자(전분 또는 글리코겐) 중 일부는 에너지 저장소 역할을 하고, 다른 일부(셀룰로오스 및 글루코스 유도체로부터 생성된 키틴)는 구조적 역할을 합니다. 포도당의 올리고당은 다른 당과 결합하여 중요한 에너지 저장고 역할을 합니다. 여기에는 포도당-갈락토오스 이당류인 우유의 우세한 당인 유당과 포도당과 과당으로 구성된 또 다른 이당류인 수크로스가 포함됩니다. 포도당은 또한 글리코실화라고 불리는 과정에서 특정 단백질과 지질에 첨가됩니다. 이것은 종종 그들의 기능에 중요합니다. 포도당을 다른 분자에 결합시키는 효소는 보통 인산화된 포도당을 사용하여 포도당-인산 결합의 파괴와 결합하여 새로운 결합의 형성을 촉진합니다.
포도당은 단량체로 직접 사용하는 것 외에도 다양한 생체 분자를 합성하기 위해 분해될 수 있습니다. 포도당이 에너지의 주요 저장고이자 유기 탄소의 공급원 역할을 하기 때문에 이것은 중요합니다. 포도당은 분해되어 지질로 전환될 수 있습니다. 또한 비타민 C(아스코르브산)와 같은 다른 중요한 분자의 합성을 위한 전구체이기도 합니다. 살아있는 유기체에서 포도당은 다양한 대사 경로의 출발 물질인 여러 다른 화학 화합물로 전환됩니다. 그 중 과당(폴리올 경로를 통해),[50] 만노스(2번 위치의 포도당 에피머), 갈락토스(4번 위치의 에피머), 푸코오스, 다양한 우론산 및 아미노당과 같은 다른 모든 단당류는[96] 포도당에서 생성됩니다.[52] 포도당은 해당과정의 일부인 포도당-6-인산으로의 인산화 외에도 글루코노-1,5-락톤으로 분해되는 동안 산화될 수 있습니다. 포도당은 일부 박테리아에서 트레할로스 또는 덱스트란 생합성의 구성 요소로 사용되고 동물에서는 글리코겐의 구성 요소로 사용됩니다. 포도당은 또한 박테리아 자일로스 이성질화효소에서 과당으로 전환될 수 있습니다. 또한 포도당 대사산물은 모든 비필수 아미노산, 만니톨과 소르비톨과 같은 당알코올, 지방산, 콜레스테롤, 핵산을 생성합니다.[96] 마지막으로, 글루코스는 당단백질, 당지질, 펩티도글리칸, 글리코사이드 및 기타 물질(글리코실트랜스퍼라제에 의해 촉매됨)로의 단백질의 글리코실화에서 빌딩 블록으로 사용되며, 글리코시다제에 의해 이들로부터 절단될 수 있습니다.
병리학
당뇨병
당뇨병은 체내의 인슐린이 부족하거나 체내의 세포가 인슐린에 적절하게 반응하지 못하기 때문에 신체가 혈액의 포도당 수치를 조절할 수 없는 대사 장애입니다. 이러한 각 상황은 췌장의 소진과 인슐린 저항성을 통해 지속적으로 높은 혈당 수치로 인해 발생할 수 있습니다. 췌장은 인슐린과 글루카곤 호르몬의 분비를 담당하는 기관입니다.[97] 인슐린은 포도당 수치를 조절하는 호르몬으로 몸의 세포가 포도당을 흡수하고 사용할 수 있게 해줍니다. 포도당이 없으면 세포 안으로 들어갈 수 없기 때문에 몸의 기능을 위한 연료로 사용될 수 없습니다.[98] 췌장이 지속적으로 높은 혈당 수치에 노출되면 췌장의 인슐린 생성 세포가 손상되어 체내 인슐린이 부족해질 수 있습니다. 인슐린 저항성은 지속적으로 높아진 혈당 수치에 반응하여 췌장이 점점 더 많은 인슐린을 생산하려고 할 때 발생합니다. 결국 나머지 신체는 췌장이 생산하고 있는 인슐린에 저항성을 갖게 되고, 따라서 동일한 혈당 강하 효과를 얻기 위해 더 많은 인슐린이 필요하게 되고, 췌장은 저항성과 경쟁하기 위해 더 많은 인슐린을 생산해야 합니다. 이 부정적인 나선은 췌장 탈진과 당뇨병의 질병 진행에 기여합니다.
혈당 강하 요법에 대한 신체의 반응을 모니터링하기 위해 포도당 수치를 측정할 수 있습니다. 혈당 모니터링은 8시간 금식 후 혈중 포도당 수치를 측정하는 금식 포도당 검사와 같이 여러 가지 방법으로 수행할 수 있습니다. 또 다른 검사는 2시간 포도당 내성 검사(GTT)입니다 – 이 검사를 위해 공복 포도당 검사를 받은 후 75그램의 포도당 음료를 마시고 재검사를 받습니다. 이 테스트는 사람의 신체가 포도당을 처리하는 능력을 측정합니다. 인슐린이 세포에 의해 흡수되어 혈류로 빠져나가는 것을 허용하기 때문에 시간이 지남에 따라 혈당 수치가 감소해야 합니다.
저혈당관리

당뇨병이나 저혈당을 유발하는 다른 질환을 가진 사람들은 종종 다양한 형태로 소량의 당을 운반합니다. 일반적으로 사용되는 설탕 중 하나는 포도당이며, 종종 포도당 정제(한 가지 이상의 다른 성분을 결합제로 사용하여 정제 모양으로 압착하는 포도당), 하드 캔디 또는 설탕 패킷의 형태로 제공됩니다.
원천

대부분의 식이 탄수화물은 (다당류 전분 및 글리코겐과 같이) 포도당을 포함하거나 다른 단당류와 함께 (헤테로-다당류 수크로스 및 유당과 같이) 포도당을 포함합니다.[99] 결합되지 않은 포도당은 꿀의 주요 성분 중 하나입니다. 포도당은 매우 풍부하며 로마의 침엽수 Wollemia nobilis의 수컷 원뿔체,[100] 중국의 Ilex as prella 식물의 뿌리,[101] 캘리포니아의 쌀에서 추출된 지푸라기 등 전 세계의 다양한 천연 공급원에서 분리되었습니다.[102]
| 음식. 물건 | 탄수화물, 포함하여 [a]합계 식이섬유 | 총 당류 | 공짜 과당 | 공짜 포도당 | 수크로스 | 비율 과당/과당 포도당 | 자당 의 비율 총당(%) |
|---|---|---|---|---|---|---|---|
| 과일들 | |||||||
| 사과 | 13.8 | 10.4 | 5.9 | 2.4 | 2.1 | 2.0 | 19.9 |
| 살구 | 11.1 | 9.2 | 0.9 | 2.4 | 5.9 | 0.7 | 63.5 |
| 바나나 | 22.8 | 12.2 | 4.9 | 5.0 | 2.4 | 1.0 | 20.0 |
| 무화과, 건조 | 63.9 | 47.9 | 22.9 | 24.8 | 0.9 | 0.93 | 0.15 |
| 포도 | 18.1 | 15.5 | 8.1 | 7.2 | 0.2 | 1.1 | 1 |
| 배꼽오렌지 | 12.5 | 8.5 | 2.25 | 2.0 | 4.3 | 1.1 | 50.4 |
| 복숭아 | 9.5 | 8.4 | 1.5 | 2.0 | 4.8 | 0.9 | 56.7 |
| 먹는 배 | 15.5 | 9.8 | 6.2 | 2.8 | 0.8 | 2.1 | 8.0 |
| 파인애플. | 13.1 | 9.9 | 2.1 | 1.7 | 6.0 | 1.1 | 60.8 |
| 자두 | 11.4 | 9.9 | 3.1 | 5.1 | 1.6 | 0.66 | 16.2 |
| 야채들 | |||||||
| 비트, 레드 | 9.6 | 6.8 | 0.1 | 0.1 | 6.5 | 1.0 | 96.2 |
| 당근 | 9.6 | 4.7 | 0.6 | 0.6 | 3.6 | 1.0 | 77 |
| 고추, 단것 | 6.0 | 4.2 | 2.3 | 1.9 | 0.0 | 1.2 | 0.0 |
| 양파, 달콤한 | 7.6 | 5.0 | 2.0 | 2.3 | 0.7 | 0.9 | 14.3 |
| 고구마 | 20.1 | 4.2 | 0.7 | 1.0 | 2.5 | 0.9 | 60.3 |
| 얌 | 27.9 | 0.5 | 트레이스 | 트레이스 | 트레이스 | — | 트레이스 |
| 사탕수수 | 13–18 | 0.2–1.0 | 0.2–1.0 | 11–16 | 1.0 | 높은 | |
| 사탕무 | 17–18 | 0.1–0.5 | 0.1–0.5 | 16–17 | 1.0 | 높은 | |
| 곡류. | |||||||
| 옥수수, 달콤한 | 19.0 | 6.2 | 1.9 | 3.4 | 0.9 | 0.61 | 15.0 |
- ^ 탄수화물 값은 USDA 데이터베이스에서 계산되며 항상 당, 전분 및 "식이 섬유질"의 합계와 일치하지는 않습니다.
상업생산
글루코스는 글루코스 아밀라아제를 이용한 효소적 가수분해나 산을 이용하여 전분으로부터 산업적으로 생산됩니다. 효소 가수분해는 산 촉매 가수분해 반응을 크게 대체했습니다.[104] 그 결과 연간 전 세계 생산량이 2천만 톤(2011년 기준)인 글루코스 시럽(90% 이상의 글루코스를 건조 물질에 효소적으로 함유)[104]이 생성됩니다.[105] 이것이 이전의 일반적인 이름인 "전분당"의 이유입니다. 아밀라아제는 Bacillus licheniformis[106] 또는 Bacillus subtilis(균주 MN-385)에서 가장 많이 유래하며,[106] 이는 원래 사용된 효소보다 열안정성이 높습니다.[106][107] 1982년부터 아스페르길루스 니제르의 풀루라나아제가 글루코스 시럽 생산에 사용되어 아밀로펙틴을 전분(아밀로스)으로 전환시켜 글루코스의 수율을 높였습니다.[108] 반응은 pH = 4.6–5.2 및 55–60 °C의 온도에서 수행됩니다. 옥수수 시럽은 건조 물질에 20%에서 95% 사이의 포도당을 함유하고 있습니다.[109][110] 일본 형태의 글루코스 시럽인 미즈아메는 고구마나 쌀 전분으로 만들어집니다.[111] 말토덱스트린은 약 20%의 포도당을 함유하고 있습니다.
많은 작물이 전분의 공급원으로 사용될 수 있습니다. 옥수수,[104] 쌀,[104] 밀,[104] 카사바,[104] 감자,[104] 보리,[104] 고구마,[112] 옥수수 껍질, 그리고 사고는 모두 세계의 다양한 지역에서 사용됩니다. 미국에서는 옥수수 전분(옥수수에서 나오는)이 거의 독점적으로 사용됩니다. 일부 상업적인 포도당은 포도당과 과당의 약 1:1 혼합물인 역당의 성분으로 발생합니다. 원칙적으로 셀룰로오스는 포도당으로 가수분해될 수 있지만 이 공정은 아직 상업적으로 실용적이지 않습니다.[27]
과당으로의 전환
미국에서는 과당이 100g당 374kcal의 생리학적 발열량으로 더 높은 감미력을 가지고 있기 때문에 거의 독점적으로 옥수수(더 정확하게는 옥수수 시럽)가 포도당과 과당의 혼합물인 이소글루코스 생산을 위한 포도당 공급원으로 사용됩니다. 이소글루코스의 연간 생산량은 800만 톤(2011년 기준)입니다.[105] 옥수수 시럽으로 만들었을 때 최종 제품은 고과당 옥수수 시럽(HFCS)입니다.
상업용

포도당은 주로 과당과 포도당 함유 식품의 생산에 사용됩니다. 식품에서는 감미료인 습윤제로 사용하여 부피를 늘리고 부드러운 입안감을 만들어 줍니다.[104] 포도 주스(와인용) 또는 맥아(맥주용)와 같은 다양한 포도당 공급원은 알코올 음료를 생산하는 동안 에탄올로의 발효에 사용됩니다. 미국의 대부분의 청량 음료는 HFCS-55(건조 질량의 과당 함량 55%)를 사용하는 반면, 미국의 다른 HFCS 가당 식품은 대부분 HFCS-42(건조 질량의 과당 함량 42%)를 사용합니다.[114] 반면 멕시코에서는 탄산음료가 사탕수수당에 의해 단맛을 내는데, 이는 단맛의 힘이 더 강합니다.[115] 또한 포도당 시럽은 특히 사탕, 토피, 퐁당과 같은 제과류 생산에 사용됩니다.[116] 물이 없는 조건에서 가열될 때 포도당의 전형적인 화학 반응은 캐러멜화와 아미노산이 있는 상태에서 마이야르 반응입니다.
또한 다양한 유기산은 글루코스로부터 생명공학적으로 생산될 수 있으며, 예를 들어 Clostridium thermoaceticum을 사용하여 발효시켜 아세트산을 생산하고, Penicillium notatum을 사용하여 아라보아스코르브산을 생산하고, Rizopus dellemar를 사용하여 푸마르산을 생산하고, 글루콘산 생산을 위한 아스페르길루스 니제르, 이소시트르산 생산을 위한 칸디다 브룸프티, 이타콘산 생산을 위한 아스페르길루스 테레우스, 2-케토글루콘산 생산을 위한 슈도모나스 플루오레센스, 5-케토글루콘산 생산을 위한 글루코노박터 서브옥시단스, 코직산 생산을 위한 누룩곰팡이, 젖산 생산을 위한 락토바실러스 델브루에키, 말산 생산을 위한 락토바실러스 브레비스, 프로피온산 생산을 위한 프로피오니박터 셔마니, 피루브산 생산을 위한 녹농균(Pseudomonas aeruginosa) 및 타르타르산 생산을 위한 글루코노박터 서브옥시단([117][additional citation(s) needed]Gluconobacter suboxidans). 일반적인 전사인자 TFIIH의 XPB 소단위체의 억제를 통해 포유동물의 전사를 억제하는 트립톨라이드와 같은 강력한 생체활성 천연물은 글루코스 수송체 발현이 증가된 저산소 암세포를 표적으로 하는 글루코스 접합체로 최근 보고되고 있습니다.[118] 최근 포도당은 다양한 암과 감염을 막기 위해 저혈당과 고유산균을 유도하기 위한 젖산과 인슐린을 함유한 "키트"의 핵심 성분으로 상업적으로 사용되고 있습니다.[119]
분석.
더 큰 분자에서 특정 위치에서 글루코스 분자가 검출되어야 할 경우, 핵자기공명 분광법, X선 결정학 분석 또는 렉틴 면역염색은 글루코스 또는 만노스만 결합하는 콘카나발린 A 리포터 효소 접합체로 수행됩니다.
고전적인 정성적 검출 반응
이러한 반응은 역사적 의미만 있습니다.
펠링 테스트
펠링 검사는 알도스 검출을 위한 고전적인 방법입니다.[120] 상호회전으로 인해 포도당은 항상 오픈체인 알데히드로 소량 존재합니다. 상기 알데히드기는 상기 Fehling 시약(Fehling (I) 용액 및 Fehling (II) 용액을 첨가함으로써 카르복실산으로 산화되고, 상기 Cu2+ 타르트레이트 착물은+ Cu로 환원되어 벽돌 적색 침전물(CuO2)을 형성하는 것을 특징으로 하는 방법.
톨렌스 테스트
Tollens 테스트에서 샘플 용액에 암모니아성 AgNO를3 첨가한 후 포도당은 Ag를+ 원소 은으로 환원시킵니다.[121]
바푸드 테스트
Barfoed의 테스트에서는 용해된 구리 아세테이트, 아세트산나트륨 및 아세트산 용액을 테스트할 설탕 용액에 첨가한 후 수조에서 몇 분 동안 가열합니다.[122] 포도당과 다른 단당류는 빠르게 붉은 색과 적갈색의 산화 구리를 생성합니다2.
나이랜더 검정
환원당으로서, Nylander의 테스트에서 포도당이 반응합니다.[123]
기타시험
글루코스와 함께 묽은 수산화칼륨 용액을 100℃로 가열하면 강한 붉은 갈색과 카라멜 같은 냄새가 납니다.[124] 농축 황산은 상온에서 흑화 없이 건조한 포도당을 녹여 당황산을 형성합니다.[124][verification needed] 효모 용액에서 알코올 발효는 CO2 1분자에 대한 포도당 2.0454분자의 비율로 이산화탄소를 생성합니다.[124] 글루코스는 염화스탠과 함께 검은 덩어리를 형성합니다.[124] 암모니아성 은 용액에서 포도당(유당 및 덱스트린)은 은의 침착을 유도합니다. 암모니아성 아세트산납 용액에서는 글루코스가 존재하는 상태에서 백색 납 글리코사이드가 생성되는데, 글루코스는 조리 시 용해도가 떨어지고 갈색으로 변합니다.[124] 암모니아성 구리 용액에서, 황색 구리 산화물 수화물은 실온에서 글루코스와 함께 형성되는 반면, 적색 구리 산화물은 끓는 동안 형성되는 것입니다(단, 암모니아성 구리 아세테이트 용액을 제외하고는 덱스트린과 동일함).[124] Hager's 시약을 사용하면 끓이는 동안 포도당이 산화수은을 형성합니다.[124] 알칼리성 비스무트 용액은 글루코스로 원소 흑갈색 비스무트를 침전시키는 데 사용됩니다.[124] 몰리브덴산암모늄 용액에 끓인 포도당은 용액을 파란색으로 바꿉니다. 인디고 카민과 탄산나트륨이 첨가된 용액은 포도당과 함께 끓이면 물이 빠집니다.[124]
기기계량
굴절계 및 편광계
다른 탄수화물의 비율이 낮은 포도당 농축 용액에서는 편광계로 농도를 측정할 수 있습니다. 설탕 혼합물의 경우, 예를 들어 와인 생산 과정에서 Oechsle 측정과 같이 굴절계로 농도를 측정할 수 있습니다.
용액 내 광측정 효소법
포도당 산화효소(GOx)는 산소를 소비하는 동안 포도당을 글루콘산과 과산화수소로 전환시킵니다. 또 다른 효소인 퍼옥시다아제는 페놀과 4-아미노안티피린의 발색 반응(Trinder reaction)[125]을 보라색 염료로 촉매합니다.
측광 테스트 스트립 방법
테스트 스트립 방법은 글루코스를 글루콘산으로 효소적으로 전환하여 과산화수소를 형성하는 방법. 시약은 폴리머 매트릭스, 이른바 테스트 스트립에 고정되며, 이는 다소 강렬한 색상을 가정합니다. LED 기반 휴대용 광도계를 사용하여 510nm에서 반사 측정할 수 있습니다. 이를 통해 비과학자의 일상적인 혈당 측정이 가능합니다. 페놀과 4-아미노안티피린의 반응 외에도 더 높은 파장(550 nm, 750 nm)에서 측광을 허용하는 새로운 발색 반응이 개발되었습니다.[126]
전류 측정 포도당 센서
포도당의 전기 분석도 위에서 언급한 효소 반응을 기반으로 합니다. 생성된 과산화수소는 600mV의 전위에서 양극 산화에 의해 암페어메트릭으로 정량화될 수 있습니다.[127] GOx는 전극 표면이나 전극 가까이에 배치된 막에 고정됩니다. 백금이나 금과 같은 귀금속은 붕소로 도핑된 탄소나노튜브 전극뿐만 아니라 전극에도 사용됩니다.[128] Cu-CuO 나노와이어는 효소가 없는 전류 측정 전극으로도 사용되어 검출 한계가 50μmol/L에 도달합니다.[129] 특히 유망한 방법은 산화 과정에서 흐르는 전자가 분자선을 통해 효소에서 전극으로 직접 전달되는 소위 "효소 배선"입니다.[130]
기타 감각적 방법
포도당을 측정하는 다른 다양한 화학 센서가 있습니다.[131][132] 생명과학에서 포도당 분석의 중요성을 감안할 때, 보론산의 사용을 기반으로 한 당류에 대한 수많은 광학 프로브도 개발되었으며,[133] 이는 다른 (광학적) 방법이 조건부로 사용되지 않거나 또는 조건부로만 사용할 수 있는 세포내 감각 응용에 특히 유용합니다. 당의 1,2-디올 그룹에 매우 특이적으로 결합하는 유기 보론산 유도체 외에도 선택적 포도당 결합 단백질(예: 콘카나발린 A)을 수용체로 사용하는 기능적 메커니즘에 의해 분류되는 다른 프로브 개념도 있습니다. 또한, 형광-광학 센서를 사용하여 산소를 소비하는 등 대사 생성물의 농도를 통해 간접적으로 포도당 농도를 검출하는 방법이 개발되었습니다.[134] 마지막으로 (형광표지) 효소의 고유흡광도 또는 형광을 리포터로 사용하는 효소 기반 개념이 있습니다.[131]
구리요오드법
포도당은 구리 요오드 측정법으로 정량화할 수 있습니다.[135]
크로마토그래피법
특히, 꿀 등의 포도당을 포함하는 복합 혼합물의 분석을 위해, 고성능 액체 크로마토그래피, 가스[135] 크로마토그래피 등의 크로마토그래피 방법이 질량 분석법과 병용되는 경우가 많습니다.[136][137] 동위원소 비율을 고려하여 이러한 방법으로 첨가당에 의한 꿀의 불순물을 안정적으로 검출하는 것도 가능합니다.[138] 실릴화 시약을 이용한 유도체화가 일반적으로 사용됩니다.[139] 또한 이당류와 삼당류의 비율을 정량화할 수 있습니다.
생체내 분석
유기체의 세포에서 포도당 흡수는 2-디옥시-D-글루코스 또는 플루오로데옥시글루코스로 측정됩니다.[84] 18(F)플루오로데옥시글루코스는 종양학 및 신경학의 양전자 방출 단층촬영에서 추적자로 사용되며,[140] 여기서 가장 일반적으로 사용되는 진단제입니다.[141]
참고문헌
- ^ 탄수화물의 명명법 (Recommendation 1996) 2-Carb-2. iupac.qmul.ac.uk
- ^ a b Boerio-Goates, Juliana (1991), "Heat-capacity measurements and thermodynamic functions of crystalline α-D-glucose at temperatures from 10K to 340K", J. Chem. Thermodyn., 23 (5): 403–09, doi:10.1016/S0021-9614(05)80128-4
- ^ Ponomarev, V. V.; Migarskaya, L. B. (1960), "Heats of combustion of some amino-acids", Russ. J. Phys. Chem. (Engl. Transl.), 34: 1182–83
- ^ Domb, Abraham J.; Kost, Joseph; Wiseman, David (1998-02-04). Handbook of Biodegradable Polymers. CRC Press. p. 275. ISBN 978-1-4200-4936-7.
- ^ Kamide, Kenji (2005). Cellulose products and Cellulose Derivatives: Molecular Characterization and its Applications (1st ed.). Amsterdam: Elsevier. p. 1. ISBN 9780080454443. Retrieved 13 May 2021.
- ^ "L-glucose". Biology Articles, Tutorials & Dictionary Online. 2019-10-07. Retrieved 2022-05-06.
- ^ a b World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ "Online Etymology Dictionary". Etymonline.com. Archived from the original on 2016-11-26. Retrieved 2016-11-25.
- ^ 테나르, 게이뤼삭, 비오, 뒤마 (1838) "Rapport sur un mémoire de M. Péligiot, intitulé: Rechurches surla nature et les prétés chimiques des suces". Wayback Machine에 보관된 2015-12-06 (Peligiot씨의 회고록에 대한 보고서, 제목: 당류의 성질 및 화학적 성질에 대한 조사), Competes rendus, 7: 106-113. 109페이지부터. 웨이백 머신에서 보관된 2015-12-06: "Ilrésult des comparations faites par M. Péligot, quele sucre de laison, celui d'amidon, celui de diabètes et celuiel de miel on parfaitement lamme composition et lémes prétés, et al. 구성적 언슬군단 퀸 프로포즈 d'affeler Glucose (1) γλευχος, mo û트, vin doux." 펠리고 씨가 비교한 바에 따르면 포도에서 추출한 설탕과 전분에서 추출한 설탕, 당뇨병에서 추출한 설탕과 꿀에서 추출한 설탕은 정확히 같은 성분과 동일한 특성을 가지고 있으며, 우리가 글루코스(1) γλευχος이라고 부르는 단 하나의 물질을 구성하고 있습니다... (1) 달콤한 와인입니다.
- ^ a b Encyclopedia of Food and Health. Academic Press. 2015. p. 239. ISBN 9780123849533. Archived from the original on 2018-02-23.
- ^ Marggraf (1747) "키미크 경험은 진정성 없는 수크레 드 다이버스 식물, 퀴퀴센트 단노스 콘테레" 2016-06-24 Wayback Machine 보관 [우리 땅에서 자라는 다양한 식물에서 진짜 설탕을 추출하려는 의도로 만들어진 화학 실험] Histoire de l'académie royale des sciences et belles-lettres de Berlin, 79–90쪽. 90페이지부터: 웨이백 머신에 보관된 2014-10-27 "Lesraisins secs, et humectés d'une petite quanté d'eau, de manie qu'ils mollissent, peuvent alors et re pilés, & le suc'onen expressime, et depuré & épaisi, fournira une espece de Sucre" (Raisins, 소량의 물로 촉촉하게 적셔져 부드러운 방식으로, 그런 다음 압착할 수 있고, [정제하고 걸쭉해진 후] 짜낸 주스는 일종의 설탕을 제공합니다.
- ^ 존 F. 로비: 탄수화물 화학의 필수 요소. Springer Science & Business Media, 2012, ISBN 978-1-461-21622-3 페이지 7.
- ^ Rosanoff, M. A. (1906). "On Fischer's Classification of Stereo-Isomers.1". Journal of the American Chemical Society. 28: 114–121. doi:10.1021/ja01967a014.
- ^ Emil Fischer, Nobel Foundation, archived from the original on 2009-09-03, retrieved 2009-09-02
- ^ Fraser-Reid, Bert, "van't Hoff's Glucose", Chem. Eng. News, 77 (39): 8
- ^ "Otto Meyerhof - Facts - NobelPrize.org " Wayback Machine에서 아카이브됨 2018-07-15 NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Hans von Euler-Chelpin - Facts - NobelPrize.org " Wayback Machine에서 아카이브된 2018-09-03. NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Arthur Harden - Facts - NobelPrize.org " Wayback Machine에서 아카이브됨 2018-09-03 NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Bernardo Houssay - Facts - NobelPrize.org " 2018-07-15, Wayback Machine에서 아카이브됨. NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Carl Cori - Facts - NobelPrize.org " Wayback Machine에서 아카이브된 2018-07-15. NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Gerty Cori - Facts - NobelPrize.org " Wayback Machine에서 아카이브된 2018-07-15. NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ "Luis Leloir - Facts - NobelPrize.org " Wayback Machine에서 아카이브된 2018-07-15. NobelPrize.org . 2018년 9월 5일에 검색되었습니다.
- ^ 강원유와 장즈준(2020): "칼륨염보다 육탄당의 촉매적 빠른 열분해를 통한 초산의 선택적 생산", 촉매, 권 10, 502-515쪽. doi:10.3390/catal100502
- ^ Bosch, L.I.; Fyles, T.M.; James, T.D. (2004). "Binary and ternary phenylboronic acid complexes with saccharides and Lewis bases". Tetrahedron. 60 (49): 11175–11190. doi:10.1016/j.tet.2004.08.046. ISSN 0040-4020.
- ^ Yebra-Biurrun, M.C. (2005), "Sweeteners", Encyclopedia of Analytical Science, Elsevier, pp. 562–572, doi:10.1016/b0-12-369397-7/00610-5, ISBN 978-0-12-369397-6
- ^ "glucose." 컬럼비아 백과사전, 6번째.. 2015. Encyclopedia.com . 2015.11.17 http://www.encyclopedia.com Wayback Machine에서 아카이브 2009-04-26.
- ^ a b Schenck, Fred W. (2006). "Glucose and Glucose-Containing Syrups". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a12_457.pub2. ISBN 978-3527306732.
- ^ 패트릭 F. 여우: 고급 낙농 화학 3권: 유당, 물, 소금 및 비타민, 스프링거, 1992. 제3권 ISBN 9780412630200 페이지 316
- ^ 벤저민 카바예로, 폴 핑글라스, 피델 텔드라: 식품 보건 백과사전. 아카데믹 프레스 (2016). ISBN 9780123849533, Volume 1, p. 76.
- ^ "16.4: Cyclic Structures of Monosaccharides". Chemistry LibreTexts. 2014-07-18. Retrieved 2023-04-17.
- ^ Takagi, S.; Jeffrey, G. A. (1979). "1,2-O-isopropylidene-D-glucofuranose". Acta Crystallographica Section B. B35 (6): 1522–1525. Bibcode:1979AcCrB..35.1522T. doi:10.1107/S0567740879006968.
- ^ Bielecki, Mia; Eggert, Hanne; Christian Norrild, Jens (1999). "A fluorescent glucose sensor binding covalently to all five hydroxy groups of α-D-glucofuranose. A reinvestigation". Journal of the Chemical Society, Perkin Transactions. 2 (3): 449–456. doi:10.1039/A808896I.
- ^ Chandran, Sreekanth K.; Nangia, Ashwini (2006). "Modulated crystal structure (Z′ = 2) of α-d-glucofuranose-1,2:3,5-bis(p-tolyl)boronate". CrystEngComm. 8 (8): 581–585. doi:10.1039/B608029D.
- ^ McMurry, John E. (1988), Organic Chemistry (2nd ed.), Brooks/Cole, p. 866, ISBN 0534079687.
- ^ Juaristi, Eusebio; Cuevas, Gabriel (1995), The Anomeric Effect, CRC Press, pp. 9–10, ISBN 978-0-8493-8941-2
- ^ a b 만프레드 헤세, 허버트 마이어, 베른드 지, 스테판 비엔츠, 로랑 비글러, 토마스 폭스: 오르가니셴 케미의 스펙트로스코피셰 메도텐. 제8판 개정판. Georg Thiem, 2011, ISBN 978-3-13-160038-7, 페이지 34 (독일어).
- ^ a b c d Bunn, H. F.; Higgins, P. J. (1981). "Reaction of monosaccharides with proteins: possible evolutionary significance". Science. 213 (4504): 222–24. Bibcode:1981Sci...213..222B. doi:10.1126/science.12192669. PMID 12192669.
- ^ 제레미 엠. Berg: Stryer Biochie. Springer-Verlag, 2017, ISBN 978-3-662-54620-8, 페이지 531. (독일어)
- ^ a b Garrett, Reginald H. (2013). Biochemistry (5th ed.). Belmont, CA: Brooks/Cole, Cengage Learning. ISBN 978-1-133-10629-6.
- ^ a b c d Voet, Donald; Voet, Judith G. (2011). Biochemistry (4th ed.). Hoboken, NJ: John Wiley & Sons. ISBN 978-0470-57095-1.
- ^ 앨버트 L. 레닝거, 생화학, 6쇄, Worth Publishers Inc. 1972, ISBN 0-87901-009-6 페이지 228.
- ^ a b 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, 페이지 195. (독일어)
- ^ a b c d e U. 사티아나라야나: 생화학. Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7 페이지 674.
- ^ Wasserman, D. H. (2009). "Four grams of glucose". American Journal of Physiology. Endocrinology and Metabolism. 296 (1): E11–21. doi:10.1152/ajpendo.90563.2008. PMC 2636990. PMID 18840763.
- ^ "High Blood Glucose and Diabetes Complications: The buildup of molecules known as AGEs may be the key link", Diabetes Forecast, American Diabetes Association, 2010, ISSN 0095-8301, archived from the original on 2013-10-14, retrieved 2010-05-20
- ^ Varki, A.; Cummings, R. D.; Esko, J. D.; Freeze, H. H.; Stanley, P.; Bertozzi, C. R.; Hart, G. W.; Etzler, M. E. (2009). Varki, Ajit (ed.). Essentials of Glycobiology (2nd ed.). Cold Spring Harbor Laboratories Press. ISBN 978-0-87969-770-9. PMID 20301239. Archived from the original on 2016-12-06.
- ^ 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 404.
- ^ 해롤드 A. 하퍼: 메디진스키 생화학. Springer-Verlag, 2013, ISBN 978-3-662-22150-1, 페이지 641. (독일어)
- ^ Navale, A. M.; Paranjape, A. N. (2016). "Glucose transporters: Physiological and pathological roles". Biophysical Reviews. 8 (1): 5–9. doi:10.1007/s12551-015-0186-2. PMC 5425736. PMID 28510148.
- ^ a b c d e f 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, 페이지 199, 200. (독일어)
- ^ Thorens, B. (2015). "GLUT2, glucose sensing and glucose homeostasis". Diabetologia. 58 (2): 221–32. doi:10.1007/s00125-014-3451-1. PMID 25421524.
- ^ a b 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, 페이지 214. (독일어)
- ^ Huang, S.; Czech, M. P. (2007). "The GLUT4 glucose transporter". Cell Metabolism. 5 (4): 237–52. doi:10.1016/j.cmet.2007.03.006. PMID 17403369.
- ^ Govers, R. (2014). Cellular regulation of glucose uptake by glucose transporter GLUT4. Vol. 66. pp. 173–240. doi:10.1016/B978-0-12-801401-1.00006-2. ISBN 9780128014011. PMID 25344989.
{{cite book}}:journal=무시됨(도움말) - ^ Wu, Xiaohua; Freeze, Hudson H. (December 2002). "GLUT14, a Duplicon of GLUT3, is Specifically Expressed in Testis as Alternative Splice Forms". Genomics. 80 (6): 553–7. doi:10.1006/geno.2002.7010. PMID 12504846.
- ^ Ghezzi, C.; Loo DDF; Wright, E. M. (2018). "Physiology of renal glucose handling via SGLT1, SGLT2, and GLUT2". Diabetologia. 61 (10): 2087–2097. doi:10.1007/s00125-018-4656-5. PMC 6133168. PMID 30132032.
- ^ Poulsen, S. B.; Fenton, R. A.; Rieg, T. (2015). "Sodium-glucose cotransport". Current Opinion in Nephrology and Hypertension. 24 (5): 463–9. doi:10.1097/MNH.0000000000000152. PMC 5364028. PMID 26125647.
- ^ "Chemistry for Biologists: Photosynthesis". www.rsc.org. Archived from the original on 2016-08-04. Retrieved 2018-02-05.
- ^ Smith, Alison M.; Zeeman, Samuel C.; Smith, Steven M. (2005). "Starch Degradation". Annu. Rev. Plant Biol. 56: 73–98. doi:10.1146/annurev.arplant.56.032604.144257. PMID 15862090.
- ^ a b 레젝 세이블프스키: 포도당 항상성과 인슐린 저항성. Bentham Science Publishers, 2011, ISBN 978-1-608-05189-2, 페이지 46.
- ^ 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, 페이지 389.
- ^ Wang, Gehui; Kawamura, Kimitaka; Hatakeyama, Shiro; Takami, Akinori; Li, Hong; Wang, Wei (2007-04-04). "Aircraft Measurement of Organic Aerosols over China". Environmental Science & Technology. 41 (9): 3115–3120. Bibcode:2007EnST...41.3115W. doi:10.1021/es062601h. ISSN 0013-936X. PMID 17539513.
- ^ Adeva-Andany, M. M.; Pérez-Felpete, N.; Fernández-Fernández, C.; Donapetry-García, C.; Pazos-García, C. (2016). "Liver glucose metabolism in humans". Bioscience Reports. 36 (6): e00416. doi:10.1042/BSR20160385. PMC 5293555. PMID 27707936.
- ^ H. 로버트 호튼, 로렌스 A. Moran, K. Gray Scrimgeour, Marc D. Perry, J. David Rawn: Biochie. Pearson Studium; 4. aktualisierte Auflage 2008; ISBN 978-3-8273-7312-0; p. 490-496. (독일어)
- ^ a b 브라이언 케이. 홀: 스트릭버거의 진화. Jones & Bartlett Publishers, 2013, ISBN 978-1-449-61484-3, 페이지 164.
- ^ Jones, J. G. (2016). "Hepatic glucose and lipid metabolism". Diabetologia. 59 (6): 1098–103. doi:10.1007/s00125-016-3940-5. PMID 27048250.
- ^ Entner, N.; Doudoroff, M. (1952). "Glucose and gluconic acid oxidation of Pseudomonas saccharophila". J Biol Chem. 196 (2): 853–862. doi:10.1016/S0021-9258(19)52415-2. PMID 12981024.
- ^ Bonadonna, Riccardo C; Bonora, Enzo; Del Prato, Stefano; Saccomani, Maria; Cobelli, Claudio; Natali, Andrea; Frascerra, Silvia; Pecori, Neda; Ferrannini, Eleuterio; Bier, Dennis; DeFronzo, Ralph A; Gulli, Giovanni (July 1996). "Roles of glucose transport and glucose phosphorylation in muscle insulin resistance of NIDDM" (PDF). Diabetes. 45 (7): 915–25. doi:10.2337/diab.45.7.915. PMID 8666143. S2CID 219249555. Archived (PDF) from the original on 2017-03-06. Retrieved March 5, 2017.
- ^ Medical Biochemistry at a Glance @Google books, Blackwell Publishing, 2006, p. 52, ISBN 978-1-4051-1322-9, archived from the original on 2018-02-23
- ^ Medical Biochemistry at a Glance @Google books, Blackwell Publishing, 2006, p. 50, ISBN 978-1-4051-1322-9, archived from the original on 2018-02-23
- ^ Annibaldi, A.; Widmann, C. (2010). "Glucose metabolism in cancer cells". Current Opinion in Clinical Nutrition and Metabolic Care. 13 (4): 466–70. doi:10.1097/MCO.0b013e32833a5577. PMID 20473153. S2CID 205782021.
- ^ Szablewski, L. (2013). "Expression of glucose transporters in cancers". Biochimica et Biophysica Acta (BBA) - Reviews on Cancer. 1835 (2): 164–9. doi:10.1016/j.bbcan.2012.12.004. PMID 23266512.
- ^ Adekola, K.; Rosen, S. T.; Shanmugam, M. (2012). "Glucose transporters in cancer metabolism". Current Opinion in Oncology. 24 (6): 650–4. doi:10.1097/CCO.0b013e328356da72. PMC 6392426. PMID 22913968.
- ^ Schümann, U.; Gründler, P. (1998). "Electrochemical degradation of organic substances at PbO2 anodes: Monitoring by continuous CO2 measurements". Water Research. 32 (9): 2835–2842. doi:10.1016/s0043-1354(98)00046-3. ISSN 0043-1354.
- ^ "Chapter 3: Calculation of the Energy Content of Foods – Energy Conversion Factors", Food energy – methods of analysis and conversion factors, FAO Food and Nutrition Paper 77, Rome: Food and Agriculture Organization, 2003, ISBN 978-92-5-105014-9, archived from the original on 2010-05-24
- ^ Georg Schwedt: Zuckersü ße Chemie. John Wiley & Sons, 2012, ISBN 978-3-527-66001-8, 페이지 100 (독일어).
- ^ 슈미트, 랭: 생리학 드 멘첸, 30세. 오플라주. Springer Verlag, 2007, p. 907 (독일어).
- ^ Dandekar, T.; Schuster, S.; Snel, B.; Huynen, M.; Bork, P. (1999). "Pathway alignment: Application to the comparative analysis of glycolytic enzymes". The Biochemical Journal. 343 (1): 115–124. doi:10.1042/bj3430115. PMC 1220531. PMID 10493919.
- ^ Dash, Pramod. "Blood Brain Barrier and Cerebral Metabolism (Section 4, Chapter 11)". Neuroscience Online: An Electronic Textbook for the Neurosciences. Department of Neurobiology and Anatomy – The University of Texas Medical School at Houston. Archived from the original on 2016-11-17.
- ^ Fairclough, Stephen H.; Houston, Kim (2004), "A metabolic measure of mental effort", Biol. Psychol., 66 (2): 177–190, doi:10.1016/j.biopsycho.2003.10.001, PMID 15041139, S2CID 44500072
- ^ Gailliot, Matthew T.; Baumeister, Roy F.; DeWall, C. Nathan; Plant, E. Ashby; Brewer, Lauren E.; Schmeichel, Brandon J.; Tice, Dianne M.; Maner, Jon K. (2007), "Self-Control Relies on Glucose as a Limited Energy Source: Willpower is More than a Metaphor" (PDF), J. Pers. Soc. Psychol., 92 (2): 325–336, CiteSeerX 10.1.1.337.3766, doi:10.1037/0022-3514.92.2.325, PMID 17279852, S2CID 7496171, archived (PDF) from the original on 2017-08-18
- ^ Gailliot, Matthew T.; Baumeister, Roy F. (2007), "The Physiology of Willpower: Linking Blood Glucose to Self-Control", Personal. Soc. Psychol. Rev., 11 (4): 303–327, CiteSeerX 10.1.1.475.9484, doi:10.1177/1088868307303030, PMID 18453466, S2CID 14380313
- ^ Masicampo, E. J.; Baumeister, Roy F. (2008), "Toward a Physiology of Dual-Process Reasoning and Judgment: Lemonade, Willpower, and Expensive Rule-Based Analysis", Psychol. Sci., 19 (3): 255–60, doi:10.1111/j.1467-9280.2008.02077.x, PMID 18315798, S2CID 38596025
- ^ a b c 도나드 드와이어: 뇌의 포도당 대사. 학술출판부, 2002, ISBN 978-0123-66852-3, 페이지 XIII.
- ^ a b c Koekkoek, L. L.; Mul, J. D.; La Fleur, S. E. (2017). "Glucose-Sensing in the Reward System". Frontiers in Neuroscience. 11: 716. doi:10.3389/fnins.2017.00716. PMC 5742113. PMID 29311793.
- ^ a b Tucker, R. M.; Tan, S. Y. (2017). "Do non-nutritive sweeteners influence acute glucose homeostasis in humans? A systematic review". Physiology & Behavior. 182: 17–26. doi:10.1016/j.physbeh.2017.09.016. PMID 28939430. S2CID 38764657.
- ^ La Fleur, S. E.; Fliers, E.; Kalsbeek, A. (2014). "Neuroscience of glucose homeostasis". Diabetes and the Nervous System. Handbook of Clinical Neurology. Vol. 126. pp. 341–351. doi:10.1016/B978-0-444-53480-4.00026-6. ISBN 9780444534804. PMID 25410233..
- ^ Bisschop, P. H.; Fliers, E.; Kalsbeek, A. (2015). "Autonomic regulation of hepatic glucose production". Comprehensive Physiology. 5 (1): 147–165. doi:10.1002/cphy.c140009. PMID 25589267.
- ^ W. A. Scherbaum, B. M. Lobnig, In: Hans-Peter Wolff, Thomas R. 웨이라우치: Internistische Therapie 2006, 2007. 16판 Elsevier, 2006, ISBN 3-437-23182-0, p. 927, 985 (in German).
- ^ 해롤드 A. 하퍼: 메디진스키 생화학. Springer-Verlag, 2013, ISBN 978-3-662-22150-1, p. 294.
- ^ Clarke, S. F.; Foster, J. R. (2012). "A history of blood glucose meters and their role in self-monitoring of diabetes mellitus". British Journal of Biomedical Science. 69 (2): 83–93. CiteSeerX 10.1.1.468.2196. doi:10.1080/09674845.2012.12002443. PMID 22872934. S2CID 34263228.
- ^ "Diagnosing Diabetes and Learning About Prediabetes". American Diabetes Association. Archived from the original on 2017-07-28. Retrieved 2018-02-20.
- ^ a b 리처드 A. 하비, 데니스 R. 페리어: 생화학. 제5판, Lipincott Williams & Wilkins, 2011, ISBN 978-1-608-3114-6, 페이지 366
- ^ a b 우 사티아나라야나: 생화학. Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7, 페이지 508.
- ^ Holt, S. H.; Miller, J. C.; Petocz, P. (1997). "An insulin index of foods: The insulin demand generated by 1000-kJ portions of common foods". The American Journal of Clinical Nutrition. 66 (5): 1264–1276. doi:10.1093/ajcn/66.5.1264. PMID 9356547.
- ^ a b 피터 C. Heinrich: Löffler/Petrides Biochemie und Pathiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, 페이지 27. (독일어)
- ^ Röder PV, Wu B, Liu Y, Han W (2016). "Pancreatic Regulation of Glucose Homeostasis". Exp. Mol. Med. 48 (3, March): e219–. doi:10.1038/emm.2016.6. PMC 4892884. PMID 26964835.
- ^ Estela, Carlos (2011) "혈당 수치", 수학 모델링 학부 저널: 1+2: 3권: 12조 2항
- ^ "Carbohydrates and Blood Sugar". The Nutrition Source. 2013-08-05. Archived from the original on 2017-01-30. Retrieved 2017-01-30 – via Harvard T.H. Chan School of Public Health.
- ^ Venditti, Alessandro; Frezza, Claudio; Vincenti, Flaminia; Brodella, Antonia; Sciubba, Fabio; Montesano, Camilla; Franceschin, Marco; Sergi, Manuel; Foddai, Sebastiano; Di Cocco, Maria Enrica; Curini, Roberta (2019). "A syn-ent-labdadiene derivative with a rare spiro-β-lactone function from the male cones of Wollemia nobilis". Phytochemistry. 158: 91–95. Bibcode:2019PChem.158...91V. doi:10.1016/j.phytochem.2018.11.012. ISSN 0031-9422. PMID 30481664. S2CID 53757166.
- ^ Lei, Yu; Shi, She-Po; Song, Yue-Lin; Bi, Dan; Tu, Peng-Fei (2014). "Triterpene Saponins from the Roots of Ilex asprella". Chemistry & Biodiversity. 11 (5): 767–775. doi:10.1002/cbdv.201300155. ISSN 1612-1872. PMID 24827686. S2CID 40353516.
- ^ Balan, Venkatesh; Bals, Bryan; Chundawat, Shishir P. S.; Marshall, Derek; Dale, Bruce E. (2009), "Lignocellulosic Biomass Pretreatment Using AFEX", Biofuels, Methods in Molecular Biology, vol. 581, Totowa, NJ: Humana Press, pp. 61–77, Bibcode:2009biof.book...61B, doi:10.1007/978-1-60761-214-8_5, ISBN 978-1-60761-213-1, PMID 19768616, retrieved 2021-11-11
- ^ "FoodData Central". fdc.nal.usda.gov.
- ^ a b c d e f g h i P. J. 펠로우: 식품 가공 기술. 우드헤드 출판사, 2016, ISBN 978-0-081-00523-1, 페이지 197.
- ^ a b 토마스 베커, 디트마 브라이하우프, 호르스트 베르너 도엘, 아르민 피에테르, 귄터 슐레겔, 사카유 시미즈, 야마다 히데아키: 생명공학, 인: 울만의 산업 화학 백과사전, 7판, Wiley-VCH, 2011. ISBN 978-3-527-32943-4. 6권 48쪽.
- ^ a b c 일본 아밀라아제 연구회: 아밀라아제 및 관련 효소 핸드북 Elsevier, 2014, ISBN 978-1-483-29939-6, p. 195.
- ^ Madsen, G. B.; Norman, B. E.; Slott, S. (1973). "A New, Heat Stable Bacterial Amylase and its Use in High Temperature Liquefaction". Starch – Stärke. 25 (9): 304–308. doi:10.1002/star.19730250906.
- ^ Norman, B. E. (1982). "A Novel Debranching Enzyme for Application in the Glucose Syrup Industry". Starch – Stärke. 34 (10): 340–346. doi:10.1002/star.19820341005.
- ^ James N. BeMiller, Roy L. Whistler (2009). Starch: Chemistry and Technology. Food Science and Technology (3rd ed.). New York: Academic Press. ISBN 978-0080926551.
- ^ BeMiller, James N.; Whistler, Roy L., eds. (2009). Starch: Chemistry and Technology. Food Science and Technology (3rd ed.). New York: Academic Press. ISBN 978-0080926551. Retrieved 25 November 2016.
- ^ 앨런 데이비슨: Oxford Companion to Food (1999). "Mizuame", p. 510 ISBN 0-19-211579-0.
- ^ 앨런 데이비슨: Oxford 식품의 동반자. OUP Oxford, 2014, ISBN 978-0-191-04072-6, p. 527.
- ^ "Sugar". Learning, Food Resources. food.oregonstate.edu. Oregon State University, Corvallis, OR. 2012-05-23. Archived from the original on 2011-07-18. Retrieved 2018-06-28.
- ^ "High Fructose Corn Syrup: Questions and Answers". US Food and Drug Administration. 2014-11-05. Archived from the original on 2018-01-25. Retrieved 2017-12-18.
- ^ 케빈 팡: 멕시칸 콜라가 미국에서 히트를 쳤습니다. 인: 시애틀 타임즈, 2004년 10월 29일.
- ^ 스티브 T. 베켓: 베켓의 산업용 초콜릿 제조 및 사용. John Wiley & Sons, 2017, ISBN 978-1-118-78014-5, 페이지 82.
- ^ 제임스 A. 켄트: 리겔의 공업화학 편람. Springer Science & Business Media, 2013, ISBN 978-1-475-76431-4, 페이지 938.
- ^ Datan E, Minn I, Peng X, He QL, Ahn H, Yu B, Pomper MG, Liu JO (2020). "A Glucose-Triptolide Conjugate Selectively Targets Cancer Cells under Hypoxia". iScience. 23 (9): 101536. Bibcode:2020iSci...23j1536D. doi:10.1016/j.isci.2020.101536. PMC 7509213. PMID 33083765.
- ^ Goodwin, Matthew L.; Gladden, L. Bruce; Nijsten, Maarten W. N. (2020-09-03). "Lactate-Protected Hypoglycemia (LPH)". Frontiers in Neuroscience. 14: 920. doi:10.3389/fnins.2020.00920. ISSN 1662-453X. PMC 7497796. PMID 33013305.
- ^ H. 펠링: 정량적인 Bestimung des Zuckersim Harn. 인: 아르키프퓌르 생리학 헤일쿤데 (1848), 7권, 64–73쪽 (독일어).
- ^ B. 톨렌스: 위버 암몬-알칼리셰 실베를뢰숭알스 레겐소프 알데하이드. Berichte der Deutschen Chemischen Gesellschaft (1882), 15권, 1635–1639쪽 (독일어).
- ^ Barfoed, C. (1873). "Ueber die Nachweisung des Traubenzuckers neben Dextrin und verwandten Körpern". Zeitschrift für Analytische Chemie (in German). 12: 27–32. doi:10.1007/BF01462957. S2CID 95749674.
- ^ 에밀 니랜더: 위버 알칼리스케 비스무틀뢰성 알스 레겐소프 트라우벤주커 임 하른, 자이츠크리프퓌르 생리학 화학. 8권, 1884년 3호, 175-185쪽 초록. 2015-09-23을 웨이백 기계(독일어)에 보관했습니다.
- ^ a b c d e f g h i Georg Schwedt: Zuckersü ße Chemie. John Wiley & Sons, 2012, ISBN 978-3-527-66001-8, 페이지 102(독일어).
- ^ Trinder, P. (1969). "Determination of Glucose in Blood Using Glucose Oxidase with an Alternative Oxygen Acceptor". Annals of Clinical Biochemistry. 6: 24–27. doi:10.1177/000456326900600108. S2CID 58131350.
- ^ Mizoguchi, Makoto; Ishiyama, Munetaka; Shiga, Masanobu (1998). "Water-soluble chromogenic reagent for colorimetric detection of hydrogen peroxide—an alternative to 4-aminoantipyrine working at a long wavelength". Analytical Communications. 35 (2): 71–74. doi:10.1039/A709038B.
- ^ Wang, J. (2008). "Electrochemical glucose biosensors". Chemical Reviews. 108 (2): 814–825. doi:10.1021/cr068123a. PMID 18154363..
- ^ Chen, X.; Chen, J.; Deng, C.; Xiao, C.; Yang, Y.; Nie, Z.; Yao, S. (2008). "Amperometric glucose biosensor based on boron-doped carbon nanotubes modified electrode". Talanta. 76 (4): 763–767. doi:10.1016/j.talanta.2008.04.023. PMID 18656655.
- ^ Wang, Guangfeng; Wei, Yan; Zhang, Wei; Zhang, Xiaojun; Fang, Bin; Wang, Lun (2010). "Enzyme-free amperometric sensing of glucose using Cu-CuO nanowire composites". Microchimica Acta. 168 (1–2): 87–92. doi:10.1007/s00604-009-0260-1. S2CID 98567636.
- ^ Ohara, T. J.; Rajagopalan, R.; Heller, A. (1994). ""Wired" enzyme electrodes for amperometric determination of glucose or lactate in the presence of interfering substances". Analytical Chemistry. 66 (15): 2451–2457. doi:10.1021/ac00087a008. PMID 8092486.
- ^ a b Borisov, S. M.; Wolfbeis, O. S. (2008). "Optical biosensors". Chemical Reviews. 108 (2): 423–461. doi:10.1021/cr068105t. PMID 18229952.
- ^ Ferri, S.; Kojima, K.; Sode, K. (2011). "Review of glucose oxidases and glucose dehydrogenases: A bird's eye view of glucose sensing enzymes". Journal of Diabetes Science and Technology. 5 (5): 1068–76. doi:10.1177/193229681100500507. PMC 3208862. PMID 22027299.
- ^ Mader, Heike S.; Wolfbeis, Otto S. (2008). "Boronic acid based probes for microdetermination of saccharides and glycosylated biomolecules". Microchimica Acta. 162 (1–2): 1–34. doi:10.1007/s00604-008-0947-8. S2CID 96768832.
- ^ Wolfbeis, Otto S.; Oehme, Ines; Papkovskaya, Natalya; Klimant, Ingo (2000). "Sol–gel based glucose biosensors employing optical oxygen transducers, and a method for compensating for variable oxygen background". Biosensors and Bioelectronics. 15 (1–2): 69–76. doi:10.1016/S0956-5663(99)00073-1. PMID 10826645.
- ^ a b Galant, A. L.; Kaufman, R. C.; Wilson, J. D. (2015). "Glucose: Detection and analysis". Food Chemistry. 188: 149–160. doi:10.1016/j.foodchem.2015.04.071. PMID 26041177.
- ^ Sanz, M. L.; Sanz, J.; Martínez-Castro, I. (2004). "Gas chromatographic-mass spectrometric method for the qualitative and quantitative determination of disaccharides and trisaccharides in honey". Journal of Chromatography A. 1059 (1–2): 143–148. doi:10.1016/j.chroma.2004.09.095. PMID 15628134.
- ^ Max Planck Institute of Molecular Plant Physiology in Golm Database (2007-07-19). "Glucose mass spectrum". Golm Metabolome Database. Archived from the original on 2018-09-09. Retrieved 2018-06-04.
- ^ Cabañero, A. I.; Recio, J. L.; Rupérez, M. (2006). "Liquid chromatography coupled to isotope ratio mass spectrometry: a new perspective on honey adulteration detection". J Agric Food Chem. 54 (26): 9719–9727. doi:10.1021/jf062067x. PMID 17177492.
- ^ Becker, M.; Liebner, F.; Rosenau, T.; Potthast, A. (2013). "Ethoximation-silylation approach for mono- and disaccharide analysis and characterization of their identification parameters by GC/MS". Talanta. 115: 642–51. doi:10.1016/j.talanta.2013.05.052. PMID 24054643.
- ^ Gesellschaft Deutscher Chemiker: wayback=20100331071121 Anlagenzum Positions papier der Fachgruppe Nuclearchemie Archived 2010-03-31 at the Wayback Machine, 2000년 2월.
- ^ Maschauer, S.; Prante, O. (2014). "Sweetening pharmaceutical radiochemistry by (18)f-fluoroglycosylation: A short review". BioMed Research International. 2014: 1–16. doi:10.1155/2014/214748. PMC 4058687. PMID 24991541.