주석산
Tartaric acid | |
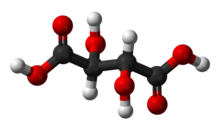 L-(+)-타르타르산의 볼 앤 스틱 모델 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 2,3-디히드록시부탄데오산 | |
| 기타 이름 주석산 2,3-디히드록시수진산 트레아산 라세미산 우빈산 파라타르산 윈스톤 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| ECHA 정보 카드 | 100.121.903 |
| E번호 | E334(항산화제 등) |
| 케그 | |
| 메쉬 | 주석산+치석 |
PubChem CID |
|
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| CHO466(기본식) HOCCH2(OH)CH(OH)COH2(구조식) | |
| 몰 질량 | 150.087 g/g |
| 외모 | 화이트 파우더 |
| 밀도 | 1.737 g/cm3 (R, R, S, S-) 1.79 g/cm3 (레이스메이트) 1.886 g/cm3 (메소) |
| 녹는점 | 169, 172 °C (R, R, S, S-) 206 °C (레이스메이트) 165-6°C(메소) |
| |
| 산도(pKa) | L(+) 25°C: pKa1 = 2.89, pKa2 = 4.40 메소 25 °C: pKa1= 3.22, pKa2= 4.85 |
| 켤레 기저 | 비트레이트 |
자화율(δ) | - 67.5 · 10−6 cm3 / 세로 |
| 위험 요소 | |
| GHS [3]라벨링: | |
 | |
| 위험. | |
| H318 | |
| P280, P305+P351+P338+P310 | |
| 관련 화합물 | |
기타 캐티온 | 주석산나트륨 주석산나트륨 주석산칼륨 주석산2칼륨 |
관련 카르본산 | 낙산 숙신산 디메르캅토숙신산 사과산 말레인산 푸마르산 |
관련 화합물 | 2,3-부탄디올 시콜산 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
타르타르산은 많은 과일, 특히 포도에서 자연적으로 발생하는 백색 결정성 유기산이지만 바나나, [4]타마린드, 감귤류에서도 발생합니다.흔히 타르타르의 크림으로 알려진 소금인 비트레이트 칼륨은 발효 과정에서 자연적으로 발달합니다.이것은 보통 중탄산나트륨과 혼합되어 식품 제조 시 발효제로 사용되는 베이킹 파우더로 판매된다.산 자체는 항산화제 E334로 식품에 첨가되어 독특한 신맛을 낸다.자연적으로 발생하는 타르타르산은 유기 화학 합성에 유용한 원료이다.타르타르산은 α-히드록시-카르본산이며, 산특성이 이분해 및 알다르산이며, 숙신산의 디히드록실 유도체이다.
역사
타르타르산은 수세기 동안 와인 제조업자들에게 알려져 왔다.그러나 추출을 위한 화학 과정은 1769년 스웨덴의 화학자 칼 빌헬름 쉴레에 [5]의해 개발되었다.
타르타르산은 화학적 키랄리티의 발견에 중요한 역할을 했다.주석산의 이러한 특성은 1832년 [6][7]편광의 회전 능력을 관찰한 Jean Batiste Biot에 의해 처음 관찰되었다.루이 파스퇴르는 1847년 그가 키랄로 발견한 타르트산나트륨 암모늄 결정의 모양을 조사함으로써 이 연구를 계속했다.다른 모양의 결정을 수동으로 분류함으로써 파스퇴르는 최초로 순수한 레보타르산 샘플을 [8][9][10][11][12]생산했습니다.
입체화학
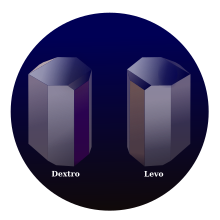
자연발생하는 산의 형태는 덱스트로 주석산 또는 L-(+)-타르타르산(구식명 d-타르타르산)이다.천연으로 사용할 수 있기 때문에 에난티오머나 메소 이성질체보다 저렴합니다.덱스트로와 레보 접두사는 옛 용어입니다.[13]현대 교과서에서는 자연 형태를 (2R,3R)-타르타르산(L-(+)-타르타르산)으로, 그 에난티오머를 (2S,3S)-타르타르산(D-(-)-타르타르산)으로 표기하고 있다.메소 디아스테레오머는 (2R,3S)-타르타르산 또는 (2S,3R)-타르타르산이라고 한다.
- 덱스트로와 레보는 단사정형 구상체[14] 결정과 직교정형 결정을 형성한다.
- 라세믹 타르타르산은 단사정계[15] 및 삼사정계 결정(공간기 P1)을 형성).[16][17]
- 무수 메소 주석산은 트리클린산과 오르토롬산의 2가지 무수 다형을 형성한다.
- 단수화 메소 주석산은 수용액으로부터의 결정화가 일어나는 [18]온도에 따라 단사정형 및 삼사정형 다형으로 결정화된다.
펠링 용액 중 주석산은 구리에 결합한다.II) 불용성 수산화염의 형성을 방지하는 이온.
| DL-타르타르산(라세미산)(비율이 1:1인 경우) | 메소타르산 | |
|---|---|---|
| 덱스트로타르산 (L-(+)-타르타르산) | 레보타르산 (D-(-)-타르타르산) | |
 |  |  |
| 통칭 | 주석산 | 레보타르산 | 덱스트로타르산 | 메소타르산 | 라세미산 |
|---|---|---|---|---|---|
| 동의어 | (2S,3S)-타르타르산 (S,S)-타르타르산 (-)-알코올산 l-아미노산(산) 레보타르산 D-타르타르산 디트레아산 ('이성체')[19] | (2R,3R)-타르타르산 (R,R)-타르타르산 (+)-아연산 d-아크롬산(산) L-타르타르산 L-트레아산 ('천연 이성질체')[20] | (2R,3S)-타르타르산 메소아미노카르산 에리스라산 | rac-(2R,3S)-타르타르산 (2RS,3SR)-타르타르산 (±)-아연산 DL-타르타르산 dl-아크롬산(산) 파라타르산 우빈산 | |
| PubChem | PubChem의 CID 875 | PubChem의 CID 439655 | PubChem의 CID 444305 | PubChem의 CID 78956 | PubChem의 CID 5851 |
| EINECS 번호 | |||||
| CAS 번호 | 526-83-0 | 147-71-7 | 87-69-4 | 147-73-9 | 133-37-9 |
생산.
L-(+)-타르타르산
타르타르산의 L-(+)-타르타르산 이성질체는 산업적으로 가장 많이 생산된다.그것은 발효의 고체 부산물인 리로부터 얻어진다.이전의 부산물은 대부분 칼륨 비트레이트(KHCHO)로446 구성되어 있다.이 칼륨 소금은 수산화칼슘 "석회 우유"(Ca(OH)"2[21]로 처리하면 주석산칼슘(CaCHO446)으로 전환됩니다.
실제로 염화칼슘을 첨가하면 주석산칼슘의 높은 수율을 얻을 수 있다.그런 다음 주석산칼슘은 수성 황산으로 소금을 처리하여 주석산으로 변환됩니다.
라세미 주석산
말레인산으로부터 다단계 반응으로 라세믹 타르타르산을 제조할 수 있다.제1공정에서는 텅스텐산칼륨을 [21]촉매로 과산화수소에 의해 말레인산을 에폭시화한다.
- HOCHCOH2222 + HO22 → OCH22(COH2)
다음 단계에서는 에폭시드를 가수분해한다.
- OCH22(COH2)2 + HO2 → (HOCH)(2COH2)2
메소타르타르산
덱스트로-타르타르산을 165°C의 물에서 약 2일간 가열하면 라세미산과 메소-타르타르산의 혼합물이 형성되며,[22] 수산화은을 사용하여 디브로모수신산으로도 제조할 수 있다.
- HOCHBrCHBrCOH22 + 2 AgOH → HOCH2(OH)CH(OH)COH2 + 2 AgBr
메소-타르타르산은 결정화에 의해 잔류 라세미산으로부터 분리될 수 있으며, 라세메이트는 용해성이 낮다.
반응성
L-(+)-타르타르산은 여러 가지 반응에 관여할 수 있다.L-(+)-타르타르산을 과산화수소로 처리하면 아래와 같이 디히드록시말레인산이 생성된다.
- HOCH2(OH)CH(OH)COH2 + HO222 → HOCC(OH)C(OH2)COH2 + 2 HO
디히드록시말레인산은 질산에 [23]의해 타르트론산으로 산화될 수 있다.
파생상품
주석산의 중요한 유도체로는 소금, 주석 크림(비타르트산칼륨), 로셸 소금(주석산칼륨, 가벼운 설사제) 및 주석 구토(주석산칼륨)[24][25][26]가 있다.비대칭 합성의 공동 촉매로서 디이소프로필 주석산염을 이용한다.
주석산은 근육 독소로 말산의 생성을 억제하여 작용하며, 고용량일 경우 마비 [27]및 사망을 일으킨다.중앙치사량(LD)은50 사람의 경우 약 7.5g/kg, 토끼의 경우 5.3g/kg,[28] 생쥐의 경우 약 4.4g/kg이다.이 수치를 고려할 때, 70kg(150파운드)의 사람을 죽이는 데 500g(18온스) 이상이 소요되므로, 많은 식품, 특히 신맛이 나는 단 음식에 안전하게 포함될 수 있습니다.식품첨가물로서 E번호 E334의 항산화제로서 타르타르산을 사용하고, 타르타르산염은 항산화제 또는 유화제로서 기능하는 다른 첨가제이다.
물에 주석 크림을 넣으면 주석산염 용액이 구리층을 녹일 수 있기 때문에 구리 동전을 매우 잘 청소하는 현탁액이 발생한다.II) 동전의 표면에 존재하는 산화물.결과적으로 발생하는 구리(II)-타르트산염 복합체는 물에 쉽게 용해됩니다.
와인의 주석산
타르타르산은 와인 음료수에게 "와인 다이아몬드"의 공급원으로 가장 즉시 인식될 수 있다. 와인 다이아몬드는 때때로 코르크 마개 또는 병 바닥에 자연적으로 형성되는 작은 역산칼륨 결정이다.이러한 "타르트레이트"는 때때로 깨진 유리로 오인되더라도 무해하며, 차가운 안정화를 통해 많은 와인에 예방됩니다(와인의 프로필을 바꿀 수 있기 때문에 항상 선호되는 것은 아닙니다).숙성된 배럴의 내부에 남아 있는 주석산염은 한때 역산칼륨의 주요 산업 공급원이었다.
주석산은 화학적으로 중요한 역할을 하며, "필수" 발효의 pH를 많은 바람직하지 않은 부패균이 살 수 없는 수준으로 낮추고 발효 후 방부제 역할을 한다.구연산과 사과산도 작용하지만 입안에서 타르타르산은 와인의 신맛의 일부를 제공합니다.
감귤류의 주석산
연구 결과에 따르면 감귤류에서는 유기농에서 생산된 과일이 기존 [29]농업에서 생산된 과일보다 높은 수준의 주석산을 함유하고 있다.
적용들
타르타르산과 그 유도체는 제약 분야에서 매우 많이 사용된다.예를 들어, 구연산과 함께 발포성 소금 생산에 사용되어 경구약물의 [23]맛을 개선해 왔다.타르타르 구토산으로 알려진 산의 칼륨 안티모닐 유도체는 기침 시럽에 기대제로 소량 포함되어 있습니다.
타르타르산은 또한 산업용으로 여러 가지 응용이 있다.그 산은 칼슘과 마그네슘과 같은 금속 이온을 킬레이트시키는 것으로 관찰되었다.따라서 농가에서는 토양 비료에서 미량 영양소를 착화시키는 킬레이트제와 이들 금속의 알루미늄,[21] 구리, 철, 합금으로 이루어진 금속 표면을 청소하는 킬레이트제로 사용되어 왔다.
송곳니의 독성
타르타르산은 인간과 실험 동물들에 의해 잘 견뎌지는 반면, 2021년 4월 JAVMA의 편집자에게 보낸 편지는 [30]포도에 있는 타르타르산이 개의 포도 및 건포도 독성의 원인이 될 수 있다는 가설을 세웠다.
레퍼런스
- ^ 주석산 – 화합물 요약, PubChem.
- ^ Dawson, R.M.C. et al., Data for Phiothical Research, Oxford, Clarendon Press, 1959.
- ^ GHS: 산업안전보건연구소의 GESTIS 물질 데이터베이스 기록
- ^ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). "Organic acids concentration in citrus juice from conventional versus organic farming". Acta Horticulturae (933): 601–606. doi:10.17660/actahortic.2012.933.78. hdl:10400.1/2790. ISSN 0567-7572.
- ^ 레치우스, 안데르스 자한(1770) "Försök med vinsten och des syra"(타타르와 그 산성 크림으로 실험), Kungliga Vetenskapsakademiens Handlingar(왕립과학아카데미회의 진행), 31: 207–213.209페이지부터: "§. 6. Desa försök omtalte jag för Hr. 칼 빌헬름 셸레(en snabb och lörgirug Pharmacié Studiosus)…( 6. 6. 칼 빌헬름 셸레(약리학을 빠르고 공부한 학생)를 대신해 이러한 실험을 언급합니다…)
- ^ Biot(1835) "Mémoire sur la polarization circularaire et sur sus applications la la chimie organique", Mémoire de l'l'Academie des sciences de l'Institut, 두 번째 시리즈, 13:39–175.타르타르산(아시드 타르타리케 크리스탈리세)이 평면 편광을 회전시키는 것은 페이지 168에 이은 표 G에 나와 있다. (참고:이 기사는 1832년 11월 5일 프랑스 왕립과학원에 읽혔다.)
- ^ Biot(1838) "Pour discerner les mélanges et les combinasons chimiques definies you non definies, qui agissent sur la lumiér polarisé; suivies d'applications aux combinas de l'c l'e acide tartarique l'e, l'e et l'e et l'e l'eau, l'e et l'le et l'l'l'l'l'l'l'주석산과 물, 알코올(예: 에탄올), 목재(예: 메탄올)의 조합에 대한 적용과 함께 Mémoires de l'l'Academie des sciences de l'Institut, 두 번째 시리즈, 15:93–279.
- ^ L. 파스퇴르(1848) "Mémoire sur la relation qui pe qui peut exister entre cristalline et la cosse de la 편광 로타토아르"(결정 형태와 화학적 조성 사이에 존재할 수 있는 관계 및 회전 편광의 원인에 대한 기억), 데스파르미 과학(Métesus de larmie desParmie)26 : 535 ~538 。
- ^ L. 파스퇴르(1848) "결정 형태와 화학적 조성, 회전 편파 사이에 존재할 수 있는 관계에 대하여", Annales de Chimie et de Physical, 3rd, 24–45."
- ^ 파스퇴르, 루이(1850) "라세미산을 구성하는 두 산의 특정 특성에 대한 조사", Anales de Chimie et Ficture, 3rd 시리즈, 28(3) : 56–99"그림 II를 참조하십시오(Pasteur의 연구 결과를 검증하기 위해 임명된 위원회의 보고서, 99–117페이지 참조). [프랑스어]
- ^ George B. Kauffman and Robin D. Myers (1998). "Pasteur's resolution of racemic acid: A sesquicentennial retrospect and a new translation" (PDF). The Chemical Educator. 3 (6): 1–4. doi:10.1007/s00897980257a. S2CID 95862598. Archived from the original (PDF) on 2006-01-17.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ Flack, H.D. (2009). "Louis Pasteur's discovery of molecular chirality and spontaneous resolution in 1848, together with a complete review of his crystallographic and chemical work" (PDF). Acta Crystallographica A. 65 (5): 371–389. Bibcode:2009AcCrA..65..371F. doi:10.1107/S0108767309024088. PMID 19687573. Archived from the original (PDF) on 2012-09-06.
- ^ "Lecture 28: Stereochemical Nomenclature; Racemization and Resolution CosmoLearning Chemistry". CosmoLearning.
- ^ W, T, Astbury (Feb 1923). "The Crystalline Structure and Properties of Tartaric Acid". Proc. Royal Soc. A. 102 (718): 506–528. Bibcode:1923RSPSA.102..506A. doi:10.1098/rspa.1923.0010.
{{cite journal}}: CS1 유지: 여러 이름: P. Groth의 Chemische Krystallographie에 기초한 저자 목록(링크) - ^ CRC 화학 및 물리 핸드북, 제49판
- ^ Samantha Callear and Michael Hursthouse (2008). "D-Tartaric acid". Crystallography Open Database.
- ^ Paul Luner; et al. (Jul 2002). "(+-)-Tartaric acid". Acta Crystallographica Section C. 58 (6): o333–o335. doi:10.1107/S0108270102006650. PMID 12050433., "(±)-Tartaric acid". Crystallography Open Database. 2002.
- ^ G. A. Bootsma and J. C. Schoone (1967). "Crystal Structures of Meso Tartaric Acid". Acta Crystallogr. 22 (4): 522–532. doi:10.1107/S0365110X67001070.
- ^ "d-Tartaric acid". PubChem.
- ^ "L-(+)-Tartaric acid". PubChem. Archived from the original on May 16, 2015.
- ^ a b c 울만 공업화학 백과사전의 J.M. 카사이안 '타르타르산'; VCH: 와인하임, 2002, 35, 671-678.doi: 10.1002/14356007.26_163.
- ^ 아우구스투스 프라이스 웨스트입니다실험적인 유기 화학.월드 북 컴퍼니:뉴욕, 1920, 232-237
- ^ a b Blair, G. T.; DeFraties, J. J. (2000). "Hydroxy Dicarboxylic Acids". Kirk Othmer Encyclopedia of Chemical Technology. pp. 1–19. doi:10.1002/0471238961.0825041802120109.a01. ISBN 0471238961.
- ^ Zalkin, Allan; Templeton, David H.; Ueki, Tatzuo (1973). "Crystal structure of l-tris(1,10-phenathroline)iron(II) bis(antimony(III) d-tartrate) octahydrate". Inorganic Chemistry. 12 (7): 1641–1646. doi:10.1021/ic50125a033.
- ^ Haq, I; Khan, C (1982). "Hazards of a traditional eye-cosmetic--SURMA". The Journal of the Pakistan Medical Association. 32 (1): 7–8. PMID 6804665.
- ^ McCallum, RI (1977). "President's address. Observations upon antimony". Proceedings of the Royal Society of Medicine. 70 (11): 756–63. doi:10.1177/003591577707001103. PMC 1543508. PMID 341167.
- ^ Alfred Swaine Taylor, Edward Hartshorne (1861). Medical jurisprudence. Blanchard and Lea. p. 61.
- ^ Joseph A. Maga, Anthony T. Tu (1995). Food additive toxicology. CRC Press. pp. 137–138. ISBN 0-8247-9245-9.
- ^ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). "Organic Acids Concentration in Citrus Juice from Conventional Versus Organic Farming". Acta Horticulturae (933): 601–606. doi:10.17660/actahortic.2012.933.78. hdl:10400.1/2790. ISSN 0567-7572.
- ^ McReynolds, Tony (April 1, 2021). "What causes grape toxicity in dogs? Playdough might have led to a breakthrough". American Animal Hospital Association.







